Teoria funkcjona lu g
|
|
|
- Błażej Zalewski
- 6 lat temu
- Przeglądów:
Transkrypt
1 Notatki do wyk ladu XI Teoria funkcjona lu g estości Density Functional Theory - DFT Czy znajomość funkcji falowej jest niezb edna? Ψ(1,, 3,..., N) dla uk ladu N-elektronowego zależy od 4N zmiennych (dla uproszczenia oznaczono wspó lrzedne przestrzenne ( r M ) i wspó lrzedn a spinowa (σ M ) dla M-tego elektronu jako M) Ψ(1,, 3,..., N) - g estość prawdopodobieństwa znalezienia elektronów w punktach określonych przez wartości wspó lrz ednych 1,, 3,..., N Prawdopodobieństwo zdarzenia pewnego wynosi 1: σ 1,σ...,σ N... Ψ(1,, 3,..., N) d r 1 d r... d r N = 1 G estość elektronowa ρ( r): ρ( r) = N... Ψ(σ1, r,, 3,..., N) d r... d r N σ 1,σ...,σ N G estość elektronowa ρ( r) zależy tylko od 3 zmiennych (x, y, z) i jest mierzalna. Do skonstruowania hamiltonianu dla czasteczki potrzebne: po lożenia jader ( R j ) i ladunki jader (Z j ). liczba elektronów (N), Dla stanu podstawowego: ρ( r)d r = N po lożenia jader wyznaczaja ostrza gestości elektronowej (wystepuj a dla r R j ) ρ( r) r Rj = Z j ρ( R j ), czyli g estość elektronowa ρ( r) zawiera wszystkie informacje potrzebne do skonstruowania hamiltonianu dla czasteczki (do rozwiazania równania Schrödingera).
2 W teorii funkcji falowej energie uk ladu i funkcje falowa otrzymujemy znajdujac minimum funkcjona lu, który (przy za lożeniu, że funkcja falowa jest znormalizowana) ma postać: E[Ψ] = Ψ ĤΨdτ W teorii DFT energie uk ladu E i gestość elektronowa ρ( r) można otrzymać, znajdujac minimum funkcjona lu Hohenberga-Kohna (Nobel dla Kohna w 1989) E[ρ] = F [ρ] + v je ( r)ρ( r)d r gdzie v je ( r) jest potencja lem przyciagania jader, a F [ρ] jest uniwersalnym ale nieznanym funkcjona lem - takim samym dla wszystkich moleku l. W 190 r. pierwsze przybliżone wyrażenie dla energii jako funkcjona lu g estości elektronowej (Thomas-Fermi) - dla energii kinetycznej wzór, wynikajacy z modelu jednorodnego, nieoddzia lujacego gazu elektronowego, w opisie odpychania elektronów pominieto wymian e i korelacj e. Na podstawie takiego modelu (także po dodaniu poprawki Diraca na wymiane) nie można przewidzieć istnienia wiazania chemicznego! Brak procedur, pozwalajacych na systematyczne ulepszanie znajdowanej gestości elektronowej, do czasu pojawienia si e koncepcji Kohna-Shama. Jako punkt wyjścia przyj eto fikcyjny uk lad nieoddzia lujacych elektronów, które maja dla stanu podstawowego taka sama gestość elektronowa jak dla interesujacego nas uk ladu rzeczywistego (gdzie elektrony, oczywiście, oddzia luja ze soba). W teorii Kohna-Shama zak lada sie, że ρ( r) jest suma gestości orbitalnych ρ( r) = N ψ i ( r) i=1 gdzie N jest liczba elektronów, a ψ i oznacza orbital.
3 Funkcjona l F [ρ] zak lada si e wtedy w postaci F [ρ] = 1 N i=1 ψ i ( r) ψ i ( r)d r + 1 ρ( r1 )ρ( r ) d r 1 d r + E xc [ρ], r 1 gdzie E xc [ρ] jest nieznanym funkcjona lem wymienno-korelacyjnym, bed acym suma funkcjona lu wymiennego E x [ρ] i funkcjona lu korelacyjnego E c [ρ]: E xc [ρ] = E x [ρ] + E c [ρ] Minimalizacja funkcjona lu E[ρ] = F [ρ] + v je ( r)ρ( r)d r ze wzgl edu na zmiany spinorbitali ψ i ( r) daje równania Kohna-Shama: ĥ KS [ρ]ψ i = ε i ψ i gdzie ĥks[ρ] jest operatorem Kohna-Shama (podobnym do operatora Focka) ĥ KS [ρ] = 1 + v( r) + Ĵ[ρ]( r) + v xc[ρ]( r) Ĵ[ρ]( r) jest tu operatorem kulombowskim, takim samym jak w teorii Hartree-Focka, a v xc [ρ]( r) jest nieznanym potencja lem wymienno-korelacyjnym, bed acym suma potencja lu wymiennego v x [ρ]( r) i potencja lu korelacyjnego v c [ρ]( r): v xc [ρ]( r) = v x [ρ]( r) + v c [ρ]( r) Wszystkie operatory sa lokalne. 3
4 Przypomienie: postać ˆF - operatora Focka (dla metody RHF) ˆF (i) = 1 i α Z α r αi + ˆV ee (i) (1) gdzie 1 i jest operatorem energii kinetycznej i-tego elektronu, Z α r αi to operator oddzia lywania tego elektronu z jadrami, α a ˆV ee (i) - potencja l pochodzacy od oddzia lywania i-tego elektronu z innymi elektronami (oznaczenia użyto zamiast ). N/ ˆV ee (i) = (Ĵq(i) ˆK q (i)) () q Ogólna definicja operatorów Ĵq(i) i ˆKq (i): Ĵ q (i)ψ p (i) = ψq(j) 1 ψ q (j)d r j ψ p (i) (3) r ij operator kulombowski - lokalny ˆK q (i)ψ p (i) = ψ q(j) 1 r ij ψ p (j)d r j ψ q (i) (4) operator wymienny - nielokalny W metodach DFT cz esto stosuje si e funkcjona ly hybrydowe, dla których v xc [ρ]( r) = c v x [ρ]( r) + (1 c) ˆK[ρ]( r) + v c [ρ]( r) gdzie ˆK[ρ]( r) jest operatorem wymiennym w teorii Hartree-Focka. Zaproponowano wiele postaci funkcjona lów i ciagle trwaja prace nad nowymi. Typy funkcjona lów Typ funkcjona lu wielkości od których zależy E xc LDA ρ GGA ρ, ρ mgga ρ, ρ, ρ, ψ a LDA - Local Density Approximation. GGA - Generalized Gradient Approximation. mgga Meta Generalized Gradient Approximation ψ a - orbitale obsadzone 4
5 Funkcjona ly sa zwykle oznaczane symbolami zawierajacymi litery (pierwsze litery nazwisk twórców) i cyfry. Przyk ladowe nazwy: Funkcjona ly, zawierajace operatory lokalne: SVWN - typu LDA PBE - typu GGA Funkcjona ly hybrydowe: PBE0, B3LYP, B3PW91 Metoda Hartree-Focka metoda wariacyjna (energia jest zawsze wyższa od dok ladnej) nie zawiera żadnych parametrów nie można otrzymać dok ladnego wyniku, tylko najlepszy wynik osiagalny w ramach w przybliżenia jednoelektronowego Metody oparte na DFT zasada wariacyjna obowiazuje tylko dla dok ladnego funkcjona lu (nieznanego) - nie stosuje si e wartość energii zależy od postaci zastosowanego funkcjona lu otrzymanie dok ladnego wyniku by loby możliwe, jeśli znany by lby dok ladny funkcjona l wymienno-korelacyjny Podobieństwo sposobu rozwiazywania równań Focka i równań Kohna-Shama - metoda iteracyjna 5
6 Metoda Hartree-Focka a opis dysocjacji czasteczki Czasteczka wodoru. Dla bardzo dużej odleg lości mi edzy atomami energia jest równa sumie energii izolowanych atomów dysocjacja czasteczki na atomy metoda Hartree-Focka - z ly opis dysocjacji czasteczki Metoda Hartree-Focka - funkcja falowa dla czasteczki (n -liczba elektronów): φ 1 (1) φ 1 ()... φ 1 (n) Φ(1,,..., n) = 1 φ (1) φ ()... φ (n) n!.... φ (1) φ n ()... φ n (n) spinorbital φ i - iloczyn orbitalu molekularnego i funkcji spinowej (5) Metoda RHF - funkcja falowa dla H Φ(1, ) = 1 ψ 1 (1)α(1) ψ 1 (1)β(1) ψ 1 ()α() ψ 1 ()β() (6) ψ 1 to orbital molekularny 6
7 Najprostsze przybliżenie: orbital molekularny ψ 1 jako kombinacja liniowa dwóch orbitali atomowych ψ 1 = 1s a + 1s b (7) 1s a orbital 1s atomu wodoru scentrowany na atomie wodoru a 1s b orbital 1s atomu wodoru scentrowany na atomie wodoru b Φ(1, ) = 1 (1s a (1) + 1s b (1))α(1) (1s a () + 1s b ())α() (1s a (1) + 1s b (1))β(1) (1s a () + 1s b ())β() Φ(1, ) = 1 (1s a (1)1s a ()α(1)β() + 1s b (1)1s a ()α(1)β() (9) +1s a (1)1s b ()α(1)β() + 1s b (1)1s b ()α(1)β() (10) 1s a (1)1s a ()β(1)α() 1s b (1)1s a ()β(1)α() (11) 1s a (1)1s b ()β(1)α() 1s b (1)1s b ()β(1)α()) (1) Φ(1, ) = 1 (1s a (1)1s a ()α(1)β() + 1s b (1)1s a () α(1)β() (13) }{{}{}}{ + 1s a (1)1s b () α(1)β() + 1s b (1)1s b ()α(1)β() (14) 1s a (1)1s a ()β(1)α() 1s b (1)1s a () β(1)α() (15) }{{}{}}{ 1s a (1)1s b () β(1)α() 1s b (1)1s b ()β(1)α()) (16) (8) Φ(1, ) = 1 (1s a (1)1s a () (α(1)β() β(1)α()) (17) +1s a (1)1s b () (α(1)β() β(1)α()) (18) +1s b (1)1s a () (α(1)β() β(1)α()) (19) +1s b (1)1s b () (α(1)β() β(1)α())) (0) 7
8 Φ(1, ) = 1 (1) (1s a (1)1s b () + 1s b (1)1s a () + 1s a (1)1s a () + 1s b (1)1s b ()) () (α(1)β() β(1)α()) (3) Cz eść spinowa funkcji falowej - singlet (S = 0) Cz eść przestrzenna funkcji falowej: Ψ MO = 1s a (1)1s b () + 1s b (1)1s a () + 1s a (1)1s a () + 1s b (1)1s b () (4) Stosujac funkcje postaci Ψ MO, nawet dla dużych odleg lości miedzy jadrami otrzymuje sie duże prawdopodobieństwo znalezienia obu elektronów przy jednym z jader. Zatem wed lug metody RHF czasteczka H nie dysocjuje na atomy. Metoda ta przewiduje produkty dysocjacji, które nie sa ani atomami ani jonami! 8
9 Prace Heitlera i Londona(197 )- wyjaśnienie trwa lości czasteczki wodoru przy zastosowaniu praw mechaniki kwantowej. Prace Hartree, Focka, Slatera Hund, Slater, Hückel - teoria orbitali molekularnych Operator Hamiltona dla czasteczki wodoru (jednostki atomowe) Ĥ = r a1 1 r b 1 r a 1 r b1 + 1 r R ab (5) gdzie: Ĥ a (1) = r a1 ; Ĥ b () = 1 1 r b ; Ĥ ab (1, ) = 1 r a 1 r b1 + 1 r R ab Ĥ = Ĥa(1) + Ĥb() + Ĥab(1, ) (6) Istota podejścia Heitlera i Londona Dla dużej odleg lości miedzy jadrami: Ĥ = Ĥa(1) + Ĥb() (7) Zatem: Ψ HL (1, ) = χ a (1) χ b () (8) gdzie: Ĥ a (1)χ a (1) = E a χ a (1) Ĥ b ()χ b () = E b χ b () χ a i χ b rozwiazania równania Schrödingera dla atomu wodoru. Dla stanu podstawowego - orbitale 1s. Ψ HL (1, ) = 1s a (1) 1s b () (9) 9
10 Funkcja falowa (iloczyn przestrzennej i spinowej) musi być antysymetryczna wzgledem permutacji elektronów! Stan singletowy: Cześć spinowa funkcji falowej antysymetryczna wzgledem permutacji elektronów σ(1, ) = α(1)β() β(1)α() (30) Cz eść przestrzenna funkcji falowej symetryczna wzgl edem permutacji elektronów Ψ HL (1, ) = 1s a (1) 1s b () + 1s b (1) 1s a () (31) Po znormalizowaniu: Ψ HL (1, ) = ( S) 1 (1s a (1) 1s b () + 1s b (1) 1s a ()) (3) Funkcja Heiltera-Londona ma w laściwa symetrie i jest dok ladnym rozwiazaniem równania Schrödingera dla czasteczki H, gdy R ab Opis stanu podstawowego czasteczki H - zastosowanie funkcji Heiltera-Londona jako funkcji próbnej w metodzie wariacyjnej. E = (Ψ HL )ĤΨHL dτ (33) Energia wiazania: D e = E( ) E(R e ) (34) Wynik metody Heitlera-Londona: D e =3,14 ev. Wartość doświadczalna: D e =4,75 ev Pierwsza poprawna wartość energii wiazania czasteczki wyznaczona teoretycznie. 10
11 Z zasady wariacyjnej: Wynik dok ladny: E( )= E H E HL (R e ) > E exact (R e ) (E exact wartość dok ladna) Energia wiazania uzyskana dowolna metoda wariacyjna: D e D exact e Poprawa wyniku metody Heitlera-Londona. Zastosowanie zamiast orbitali 1s atomu wodoru funkcji χ = N e ζr/a 0, gdzie ζ jest parametrem wariacyjnym. Dla każdej odleg lości miedzy jadrami znajdowana wartość ζ dajaca możliwie najniższa energie. Wynik: D e = 3,78 ev Uwzglednienie możliwości znalezienia sie obu elektronów przy tym samym jadrze (istnieje trwa ly jon H!) Dodanie funkcji: 1s a (1)1s a () i 1s b (1)1s b () Metoda wiazań walencyjnych gdzie c jest parametrem wariacyjnym Ψ V B = (1s a (1)1s b () + 1s b (1)1s a ())+ (35) c (1s a (1)1s a () + 1s b (1)1s b ()) (36) ( dla każdej wartości R ab znajdowana jest wartość c dajaca możliwie najniższa energie, R ab, to c 0) (wynik D e =4,0 ev) Interpretacja: struktura kowalencyjna H H: Ψ kow = 1s a (1)1s b () + 1s b (1)1s a () struktury jonowe H H + i H + H : Ψ jon I = 1s a (1)1s a () i Ψ jon II = 1s b (1)1s b () Ψ V B = Ψ kow + c (Ψ jon I + Ψ jon II ) (37) 11
12 Metoda VB: D e =4,0 ev; poprawny opis dysocjacji H metoda MO: z ly opis dysocjacji wiazania Prosta metoda LCAO MO: D e =,68 ev; najlepszy wynik SCF: D e = 3,64 ev. Dlaczego metoda MO a nie VB jest powszechnie używana? Po obliczeniu iloczynu cz eści przestrzennej funkcji VB (równ.(35) i (36)) i funkcji spinowej dla stanu singletowego (równ.(30)) widać, że funkcja falowa metody VB ma postać: c 1 1 1s a (1)α(1) 1s b (1))β(1) 1s a (1)α(1) 1s a (1))β(1) Φ V B (1, ) = (38) 1s a ()α() 1s b ()β() + 1 1s b (1)α(1) 1s b ()α() 1s a (1)β(1) (1s a ()β() + (39) 1s a ()α() 1s a ()β() + 1 1s b (1)α(1) 1s b ()α() (40) 1s b (1)β(1) (1s b ()β() kombinacji liniowej wyznaczników zbudowanych z orbitali atomowych. Metoda VB: elektrony przypisane orbitalom atomowym poszczególnych atomów elektrony tworza pary, odpowiadajace wiazaniom kowalencyjnym (struktury Lewisa), badź strukturom jonowym 1
13 do poprawnego przewidywania struktury geometrycznej czasteczek niezbedne poj ecie hybrydyzacji orbitali atomowych (Linus Pauling 1930) do wyjaśnienia czterowartościowości w egla niezb edna koncepcja promocji elektronu z orbitalu s na p dla niektórych czasteczek niezbedne dodatkowe pojecie: struktury rezonansowe (Pauling 198) (szeroko stosowane przez chemików) Problemy metody VB: wyjaśnienie w laściwości czasteczek aromatycznych np. benzenu wymaga uwzglednienia rezonansu struktur Kekulé, Dewara a nawet jonowych liczba koniecznych do uwzgl ednienia struktur szybko rośnie i znalezienie ich nie jest proste np. antracenu: 49 struktury kowalencyjne dla benzenu:5, dla naftalenu: 4, dla ogromne trudności z wyjaśnieniem magnetycznych w laściwości czasteczek np. paramagnetyzmu tlenu trudności z wyjaśnieniem trwa lości jonów molekularnych i czasteczek z nieparzysta liczba elektronów Metoda MO - orbitale molekularne zdelokalizowane na ca l a czasteczk e, potem przyporzadkowanie elektronów wyjaśnienie w laściwości czasteczek aromatycznych, magnetycznych w laściwości czasteczek i trwa lości jonów molekularnych np. H + nie wymaga żadnych dodatkowych poj eć z ly opis dysocjacji - nie nadaje sie do opisu procesów wymagajacych zrywania i tworzenia wiazań, czyli reakcji chemicznych! 13
14 Metod e MO można poprawiać w sposób koncepcyjnie prosty i systematyczny Energie E + orbitalu wiaż acego σ 1s i E orbitalu antywiażacego σ1s dla dużych odleg lości staja sie sobie równe - uk lad otwartopow lokowy! Dla uk ladów otwartopow lokowych - metoda UHF. Przypomnienie: funkcja w postaci jednego wyznacznika nie nadaje si e do opisu stanów otwartopow lokowych o niskim spinie! Lepszy opis stanu czasteczki H dla dużych odleg lości da funkcja: Φ(1, ) = 1 (1s a (1) + 1s b (1))α(1) (1s a () + 1s b ())α() (1s a (1) + 1s b (1))β(1) (1s a () + 1s b ())β() 1 (1s c 1 a (1) 1s b (1))α(1) (1s a () 1s b ())α() (1s a (1) 1s b (1))β(1) (1s a () 1s b ())β() gdzie c 1 -parametr wariacyjny + (41) (4) Po rozwinieciu wyznaczników nieznormalizowana cześć przestrzenna tej funkcji ma postać: Ψ(1, ) = (1s a (1) + 1s b (1))(1s a (1) + 1s b (1))+ (43) c 1 (1s a (1) 1s b (1))(1s a (1) 1s b (1)) (44) Po rozwinieciu wyrażeń w nawiasach i podzieleniu przez (1 c 1 ): identyczna z Ψ V B, jeśli 1+c 1 1 c 1 oznaczyć c. Ψ(1, ) = (1s a (1)1s b () + 1s b (1)1s a ())+ (45) 1 + c 1 1 c 1 (1s a (1)1s a () + 1s b (1)1s b ()) (46) Uwzgl ednienie wi ecej niż jednego wyznacznika w rozwini eciu funkcji falowej -najprostszy sposób uwzgl ednienia korelacji elektronowej 14
Teoria funkcjona lu g
 Notatki do wyk ladu XII (z 1.01.015) Uwaga! Strony 1-14 sa w wiekszości powtórzeniem stron z Notatek do wyk ladu XI z 15.1.014 Teoria funkcjona lu g estości Density Functional Theory - DFT Czy znajomość
Notatki do wyk ladu XII (z 1.01.015) Uwaga! Strony 1-14 sa w wiekszości powtórzeniem stron z Notatek do wyk ladu XI z 15.1.014 Teoria funkcjona lu g estości Density Functional Theory - DFT Czy znajomość
Teoria funkcjona lu g Density Functional Theory (DFT)
 Teoria funkcjona lu g estości Density Functional Theory (DFT) Cz eść slajdów tego wyk ladu pochodzi z wyk ladu wyg loszonego przez dra Lukasza Rajchela w Interdyscyplinarnym Centrum Modelowania Matematycznego
Teoria funkcjona lu g estości Density Functional Theory (DFT) Cz eść slajdów tego wyk ladu pochodzi z wyk ladu wyg loszonego przez dra Lukasza Rajchela w Interdyscyplinarnym Centrum Modelowania Matematycznego
Metoda Hartree-Focka (Hartree ego-focka)
 Notatki do wyk ladu V Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika Slatera,
Notatki do wyk ladu V Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika Slatera,
Notatki do wyk ladu IV (z 27.10.2014)
 Dla orbitalnego momentu p edu (L): Notatki do wyk ladu IV (z 7.10.014) ˆL ψ nlm = l(l + 1) ψ nlm (1) ˆL z ψ nlm = m ψ nlm () l + 1 możliwych wartości rzutu L z na wyróżniony kierunek w przestrzeni (l -liczba
Dla orbitalnego momentu p edu (L): Notatki do wyk ladu IV (z 7.10.014) ˆL ψ nlm = l(l + 1) ψ nlm (1) ˆL z ψ nlm = m ψ nlm () l + 1 możliwych wartości rzutu L z na wyróżniony kierunek w przestrzeni (l -liczba
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
JEDNOSTKI ATOMOWE =1, m e =1, e=1, ; 1 E 2 h = 4, J. Energia atomu wodoru lub jonu wodoropodobnego w jednostkach atomowych:
 do wyk ladu z 1.10.13 Atom wodoru i jon wodoropodobny Ze - ladunek jadra, e - ladunek elektronu, µ - masa zredukowana µ = mem j m e+m j ( µ m e ) M j - masa jadra, m e - masa elektronu, ε 0 - przenikalność
do wyk ladu z 1.10.13 Atom wodoru i jon wodoropodobny Ze - ladunek jadra, e - ladunek elektronu, µ - masa zredukowana µ = mem j m e+m j ( µ m e ) M j - masa jadra, m e - masa elektronu, ε 0 - przenikalność
Oddzia lywania miedzycz. jony molekularne lub atomy. edzy A i B:
 Notatki do wyk ladu XIII Oddzia lywania miedzycz asteczkowe A i B zamknietopow lokowe czasteczki, jony molekularne lub atomy. Energia oddzia lywania E oddz mi edzy A i B: E oddz = E AB (E A + E B ) ()
Notatki do wyk ladu XIII Oddzia lywania miedzycz asteczkowe A i B zamknietopow lokowe czasteczki, jony molekularne lub atomy. Energia oddzia lywania E oddz mi edzy A i B: E oddz = E AB (E A + E B ) ()
Notatki do wyk ladu IV (z ) Metoda Hartree-Focka (Hartree ego-focka)
 Notatki do wyk ladu IV (z 1.11.01) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa opisujac a stan uk ladu n-elektronowego ma postać wyznacznika
Notatki do wyk ladu IV (z 1.11.01) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa opisujac a stan uk ladu n-elektronowego ma postać wyznacznika
Notatki do wyk ladu V (z ) Metoda Hartree-Focka (Hartree ego-focka)
 Notatki do wyk ladu V (z 03.11.014) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika
Notatki do wyk ladu V (z 03.11.014) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika
TEORIA FUNKCJONA LÓW. (Density Functional Theory - DFT) Monika Musia l
 TEORIA FUNKCJONA LÓW GȨSTOŚCI (Density Functional Theory - DFT) Monika Musia l PRZEDMIOT BADAŃ Uk lad N elektronów + K j ader atomowych Przybliżenie Borna-Oppenheimera Zamiast funkcji falowej Ψ(r 1,σ 1,r
TEORIA FUNKCJONA LÓW GȨSTOŚCI (Density Functional Theory - DFT) Monika Musia l PRZEDMIOT BADAŃ Uk lad N elektronów + K j ader atomowych Przybliżenie Borna-Oppenheimera Zamiast funkcji falowej Ψ(r 1,σ 1,r
Teoria funkcjonału gęstości
 Teoria funkcjonału gęstości Łukasz Rajchel Interdyscyplinarne Centrum Modelowania Matematycznego i Komputerowego Uniwersytet Warszawski lrajchel1981@gmail.com Wykład dostępny w sieci: http://tiger.chem.uw.edu.pl/staff/lrajchel/
Teoria funkcjonału gęstości Łukasz Rajchel Interdyscyplinarne Centrum Modelowania Matematycznego i Komputerowego Uniwersytet Warszawski lrajchel1981@gmail.com Wykład dostępny w sieci: http://tiger.chem.uw.edu.pl/staff/lrajchel/
Symbol termu: edu (sumy ca lkowitego orbitalnego momentu edu i ca lkowitego spinu) Przyk lad: 2 P 3. kwantowa
 Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
Metody obliczeniowe chemii kwantowej oparte na funkcji falowej. Dla uk ladu N elektronów i K j ader atomowych hamiltonian przyjmuje postać:
 Metody obliczeniowe chemii kwantowej oparte na funkcji falowej Równanie Schrödingera: ĤΨ = EΨ Dla uk ladu N elektronów i K j ader atomowych hamiltonian przyjmuje postać: Ĥ = h 2 K α=1 1 2M α 2 α h2 2m
Metody obliczeniowe chemii kwantowej oparte na funkcji falowej Równanie Schrödingera: ĤΨ = EΨ Dla uk ladu N elektronów i K j ader atomowych hamiltonian przyjmuje postać: Ĥ = h 2 K α=1 1 2M α 2 α h2 2m
Metody obliczeniowe chemii teoretycznej
 Metody obliczeniowe chemii teoretycznej mechanika kwantowa mechanika klasyczna ւ ց WFT DFT MM FFM metody bazuj ace na metody bazuj ace na Mechanika Molekularna funkcji falowej gȩstości elektronowej Wave
Metody obliczeniowe chemii teoretycznej mechanika kwantowa mechanika klasyczna ւ ց WFT DFT MM FFM metody bazuj ace na metody bazuj ace na Mechanika Molekularna funkcji falowej gȩstości elektronowej Wave
Rozdział 22 METODA FUNKCJONAŁÓW GĘSTOŚCI Wstęp. Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 22 METODA FUNKCJONAŁÓW GĘSTOŚCI 22.1 Wstęp Definiujemy dla gazu elektronowego operatory anihilacji ψ σ (r) i kreacji ψ σ(r) pola fermionowego ψ σ
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 22 METODA FUNKCJONAŁÓW GĘSTOŚCI 22.1 Wstęp Definiujemy dla gazu elektronowego operatory anihilacji ψ σ (r) i kreacji ψ σ(r) pola fermionowego ψ σ
Hierarchia baz gaussowskich (5)
 Hierarchia baz gaussowskich (5) Bazy split-valence czyli VDZ, VTZ, etc. (np. bazy Pople a 6-31G, 6-311G, etc) Bazy split-valence spolaryzowane VDZP, VTZP, etc. Bazy bazy Dunninga (konsystentne korelacyjnie)
Hierarchia baz gaussowskich (5) Bazy split-valence czyli VDZ, VTZ, etc. (np. bazy Pople a 6-31G, 6-311G, etc) Bazy split-valence spolaryzowane VDZP, VTZP, etc. Bazy bazy Dunninga (konsystentne korelacyjnie)
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
i elektronów w czasteczkach (laboratoryjnym) operator Hamiltona dla czasteczki dwuatomowej (jadra 2M b a i b; m -masa elektronu e 2 r ij
 Notatki do wyk ladu IX Rozdzielenie ruchu jader i elektronów w czasteczkach W dowolnym uk ladzie wspó lrzednych (laboratoryjnym) operator Hamiltona dla czasteczki dwuatomowej (jadra a i b)ma postać: Ĥ
Notatki do wyk ladu IX Rozdzielenie ruchu jader i elektronów w czasteczkach W dowolnym uk ladzie wspó lrzednych (laboratoryjnym) operator Hamiltona dla czasteczki dwuatomowej (jadra a i b)ma postać: Ĥ
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia. Monika Musia l
 STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
Rozdział 23 KWANTOWA DYNAMIKA MOLEKULARNA Wstęp. Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 3 KWANTOWA DYNAMIKA MOLEKULARNA 3.1 Wstęp Metoda ta umożliwia opis układu złożonego z wielu jonów i elektronów w stanie podstawowym. Hamiltonian układu
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 3 KWANTOWA DYNAMIKA MOLEKULARNA 3.1 Wstęp Metoda ta umożliwia opis układu złożonego z wielu jonów i elektronów w stanie podstawowym. Hamiltonian układu
Podstawowe metody i przybliżenia: metoda wariacyjna, rachunek zaburzeń
 Wyk lad 6 Podstawowe metody i przybliżenia: metoda wariacyjna, rachunek zaburzeń Uk lady modelowe czastka swobodna czastka na barierze potencja lu czastka w pudle oscylator harmoniczny oscylator Morse
Wyk lad 6 Podstawowe metody i przybliżenia: metoda wariacyjna, rachunek zaburzeń Uk lady modelowe czastka swobodna czastka na barierze potencja lu czastka w pudle oscylator harmoniczny oscylator Morse
Chemia kwantowa makroczasteczek dla III roku biofizyki; kurs WBt-ZZ28
 Chemia kwantowa makroczasteczek konspekt wyk ladu dla III roku biofizyki; kurs WBt-ZZ28 Mariusz Radoń (ostatnia aktualizacja: 5 czerwca 2017) Z uwagi na roboczy charakter niniejszych notatek moga sie w
Chemia kwantowa makroczasteczek konspekt wyk ladu dla III roku biofizyki; kurs WBt-ZZ28 Mariusz Radoń (ostatnia aktualizacja: 5 czerwca 2017) Z uwagi na roboczy charakter niniejszych notatek moga sie w
po lożenie cz astki i od czasu (t). Dla cz astki, która może poruszać siȩ tylko w jednym wymiarze (tu x)
 Stan czastki określa funkcja falowa Ψ zależna od wspó lrzȩdnych określaj acych po lożenie cz astki i od czasu (t). Dla cz astki, która może poruszać siȩ tylko w jednym wymiarze (tu x) Wartości funkcji
Stan czastki określa funkcja falowa Ψ zależna od wspó lrzȩdnych określaj acych po lożenie cz astki i od czasu (t). Dla cz astki, która może poruszać siȩ tylko w jednym wymiarze (tu x) Wartości funkcji
Korelacja elektronowa. e z rachunku prawdopodobieństwa i statystyki. Zmienne losowe x i y sa. ρ(x, y) = ρ 1 (x) ρ 2 (y)
 Notatki do wyk ladu XII Korelacja elektronowa Nazwa korelacja elektronowa wywodzi si e z rachunku prawdopodobieństwa i statystyki. Zmienne losowe x i y sa niezależne jeśli ρ(x, y) = ρ 1 (x) ρ 2 (y) Oznacza
Notatki do wyk ladu XII Korelacja elektronowa Nazwa korelacja elektronowa wywodzi si e z rachunku prawdopodobieństwa i statystyki. Zmienne losowe x i y sa niezależne jeśli ρ(x, y) = ρ 1 (x) ρ 2 (y) Oznacza
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Monika Musia l
 WYK LAD STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Monika Musia l http : //zcht.mf c.us.edu.pl/ mm WYK LAD - wyznaczanie orbitali atomowych i molekularnych Uk lad zamkniȩtopow
WYK LAD STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Monika Musia l http : //zcht.mf c.us.edu.pl/ mm WYK LAD - wyznaczanie orbitali atomowych i molekularnych Uk lad zamkniȩtopow
Inżynieria Biomedyczna. Wykład XII
 Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe)
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 13 UKŁADY KILKU CZĄSTEK W MECHANICE KWANTOWEJ 13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe) Zajmiemy się kwantowym opisem atomu He
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 13 UKŁADY KILKU CZĄSTEK W MECHANICE KWANTOWEJ 13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe) Zajmiemy się kwantowym opisem atomu He
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
po lożenie cz astki i od czasu (t). Dla cz astki, która może poruszać siȩ tylko w jednym wymiarze (tu x)
 Stan czastki określa funkcja falowa Ψ zależna od wspó lrzȩdnych określaj acych po lożenie cz astki i od czasu (t). Dla cz astki, która może poruszać siȩ tylko w jednym wymiarze (tu x) Wartości funkcji
Stan czastki określa funkcja falowa Ψ zależna od wspó lrzȩdnych określaj acych po lożenie cz astki i od czasu (t). Dla cz astki, która może poruszać siȩ tylko w jednym wymiarze (tu x) Wartości funkcji
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Układy wieloelektronowe
 Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Metoda Hückla. edzy elektronami π. Ĥ ef (i) (1) i=1. kinetyczna tego elektronu oraz energie
 Notatki do wyk ladu X (z 08.12.2014) Metoda Hückla Uproszczona wersja metody orbitali molekularnych (MO) w przybliżeniu liniowej kombinacji orbitali atomowych (LCAO) stosowana do opisu struktury elektronowej
Notatki do wyk ladu X (z 08.12.2014) Metoda Hückla Uproszczona wersja metody orbitali molekularnych (MO) w przybliżeniu liniowej kombinacji orbitali atomowych (LCAO) stosowana do opisu struktury elektronowej
Uk lady modelowe II - oscylator
 Wyk lad 4 Uk lady modelowe II - oscylator Model Prawo Hooke a F = m d 2 x = kx = dv dt2 dx Potencja l Równanie ruchu V = 1 2 kx2 d 2 x dt 2 + k m x = 0 Obraz klasyczny Rozwiazania k x = A sin t = A sin
Wyk lad 4 Uk lady modelowe II - oscylator Model Prawo Hooke a F = m d 2 x = kx = dv dt2 dx Potencja l Równanie ruchu V = 1 2 kx2 d 2 x dt 2 + k m x = 0 Obraz klasyczny Rozwiazania k x = A sin t = A sin
1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Pytania egzaminacyjne: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny- interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest liczba wybijanych elektronów
1 Pytania egzaminacyjne: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny- interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest liczba wybijanych elektronów
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Metoda oddzia lywania konfiguracji (CI)
 Metoda oddzia lywania konfiguracji (CI) Spinorbitale: obsadzone φ a i wirtualne φ r : ɛ a ɛ HOMO, ɛ r ɛ LUMO ê r a wykonuje podstawienie φ a φ r, np. ê 7 2 φ 1 φ 2 φ 3... φ N = φ 1 φ 7 φ 3... φ N Operator
Metoda oddzia lywania konfiguracji (CI) Spinorbitale: obsadzone φ a i wirtualne φ r : ɛ a ɛ HOMO, ɛ r ɛ LUMO ê r a wykonuje podstawienie φ a φ r, np. ê 7 2 φ 1 φ 2 φ 3... φ N = φ 1 φ 7 φ 3... φ N Operator
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Rotacje i drgania czasteczek
 Rotacje i drgania czasteczek wieloatomowych Gdy znamy powierzchnie energii potencjalnej V( R 1, R 2,..., R N ) to możemy obliczyć poziomy energetyczne czasteczki. Poziomy te sa w ogólności efektem: rotacji
Rotacje i drgania czasteczek wieloatomowych Gdy znamy powierzchnie energii potencjalnej V( R 1, R 2,..., R N ) to możemy obliczyć poziomy energetyczne czasteczki. Poziomy te sa w ogólności efektem: rotacji
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uklady modelowe III - rotator, atom wodoru
 Wyk lad 5 Uklady modelowe III - rotator, atom wodoru Model Separacja ruchu środka masy R = m 1r 1 + m 2 r 2 m 1 + m 2 Ĥ = Ĥ tr (R) + Ĥ rot (r) Ĥ tr 2 (R) = 2(m 1 + m 2 ) R [ Ψ E tr (R; t) = exp i (k R
Wyk lad 5 Uklady modelowe III - rotator, atom wodoru Model Separacja ruchu środka masy R = m 1r 1 + m 2 r 2 m 1 + m 2 Ĥ = Ĥ tr (R) + Ĥ rot (r) Ĥ tr 2 (R) = 2(m 1 + m 2 ) R [ Ψ E tr (R; t) = exp i (k R
Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały
 WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
CHEMIA KWANTOWA MONIKA MUSIA L METODA HÜCKLA. Ćwiczenia. http://zcht.mfc.us.edu.pl/ mm
 CHEMIA KWANTOWA MONIKA MUSIA L METODA HÜCKLA Ćwiczenia Zwi azki organiczne zawieraj ace uk lady π-elektronowe Sprzȩżony uk lad wi azań podwójnych: -C=C-C=C-C=C-C=C- Skumulowany uk lad wi azań podwójnych:
CHEMIA KWANTOWA MONIKA MUSIA L METODA HÜCKLA Ćwiczenia Zwi azki organiczne zawieraj ace uk lady π-elektronowe Sprzȩżony uk lad wi azań podwójnych: -C=C-C=C-C=C-C=C- Skumulowany uk lad wi azań podwójnych:
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Uwzględnienie energii korelacji w metodach ab initio - przykłady
 Uwzględnienie energii korelacji w metodach ab initio - przykłady Funkcje falowe (i funkcje bazy) jawnie skorelowane - zależa jawnie od odległości międzyelektronowych r ij = r i r j Funkcje falowe w postaci
Uwzględnienie energii korelacji w metodach ab initio - przykłady Funkcje falowe (i funkcje bazy) jawnie skorelowane - zależa jawnie od odległości międzyelektronowych r ij = r i r j Funkcje falowe w postaci
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
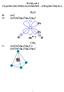 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Korelacja elektronowa
 Korelacja elektronowa oraz metody jej uwzgl edniania oparte na funkcji falowej Mariusz Radoń 04.04.2017 11.04.2017 Wymiana i korelacja kulombowska W metodzie HF Elektrony o jednakowych spinach nie moga
Korelacja elektronowa oraz metody jej uwzgl edniania oparte na funkcji falowej Mariusz Radoń 04.04.2017 11.04.2017 Wymiana i korelacja kulombowska W metodzie HF Elektrony o jednakowych spinach nie moga
Postulaty mechaniki kwantowej
 Wyk lad 2 Postulaty mechaniki kwantowej 1 wymiar Postulat Stan czastki określa funkcja falowa Ψ = Ψ(x, t) zależna od po lożenia czastki x oraz czasu t. Interpretacje fizyczna ma jedynie kwadrat modu lu
Wyk lad 2 Postulaty mechaniki kwantowej 1 wymiar Postulat Stan czastki określa funkcja falowa Ψ = Ψ(x, t) zależna od po lożenia czastki x oraz czasu t. Interpretacje fizyczna ma jedynie kwadrat modu lu
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Stany atomu wieloelektronowego o określonej energii. być przypisywane elektrony w tym stanie atomu.
 Notatki do wyk ladu VI Stany atomu wieloelektronowego o określonej energii. Konfiguracja elektronowa atomu - zbiór spinorbitali, wykorzystywanych do konstrukcji funkcji falowej dla danego stanu atomu;
Notatki do wyk ladu VI Stany atomu wieloelektronowego o określonej energii. Konfiguracja elektronowa atomu - zbiór spinorbitali, wykorzystywanych do konstrukcji funkcji falowej dla danego stanu atomu;
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Czastka swobodna Bariera potencja lu Pud lo jednowymiarowe FEMO Pud la wielowymiarowe. Wyk lad 3. Uk lady modelowe I
 Wyk lad 3 Uk lady modelowe I Hamiltonian, równania Schrödingera hamiltonian Ĥ(x) = ˆT (x) = 2 d 2 2m dx 2 równanie Schrödingera zależne od czasu stany stacjonarne 2 2 Ψ(x, t) Ψ(x, t) 2m x 2 = i t dψ E
Wyk lad 3 Uk lady modelowe I Hamiltonian, równania Schrödingera hamiltonian Ĥ(x) = ˆT (x) = 2 d 2 2m dx 2 równanie Schrödingera zależne od czasu stany stacjonarne 2 2 Ψ(x, t) Ψ(x, t) 2m x 2 = i t dψ E
Monika Musia l. METODA MIESZANIA KONFIGURACJI Configuration Interaction (CI) (ujȩcie wyznacznikowe)
 Monika Musia l METODA MIESZANIA KONFIGURACJI Configuration Interaction (CI) (ujȩcie wyznacznikowe) ĤΨ i = E i Ψ i W metodzie mieszania konfiguracji wariacyjna funkcja falowa, jest liniow a kombinacj a
Monika Musia l METODA MIESZANIA KONFIGURACJI Configuration Interaction (CI) (ujȩcie wyznacznikowe) ĤΨ i = E i Ψ i W metodzie mieszania konfiguracji wariacyjna funkcja falowa, jest liniow a kombinacj a
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
W lasności elektryczne moleku l
 W lasności elektryczne moleku l Hamiltonian dla czasteczki w jednorodnym polu elektrycznym E ma postać: Ĥ(E) = Ĥ + E ˆµ x gdzie zak ladamy, że pole jest zorientowane wzd luż osi x a ˆµ x jest operatorem
W lasności elektryczne moleku l Hamiltonian dla czasteczki w jednorodnym polu elektrycznym E ma postać: Ĥ(E) = Ĥ + E ˆµ x gdzie zak ladamy, że pole jest zorientowane wzd luż osi x a ˆµ x jest operatorem
TEORIA ORBITALI MOLEKULARNYCH (MO) dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
CHEMIA KWANTOWA MONIKA MUSIA L. Ćwiczenia. mm
 CHEMIA KWANTOWA MONIKA MUSIA L Ćwiczenia METODY PRZYBLIŻONE ROZWIA ZYWANIA RÓWNANIA SCHRÖDINGERA METODA WARIACYJNA metoda wariacyjna ĤΨ n = E n Ψ n Ψ n ortonormalne Szukamy rozwi azań dla stanu podstawowego,
CHEMIA KWANTOWA MONIKA MUSIA L Ćwiczenia METODY PRZYBLIŻONE ROZWIA ZYWANIA RÓWNANIA SCHRÖDINGERA METODA WARIACYJNA metoda wariacyjna ĤΨ n = E n Ψ n Ψ n ortonormalne Szukamy rozwi azań dla stanu podstawowego,
Metody obliczeniowe ab initio w fizyce struktur atomowych. Wykład 1: Wstęp
 Metody obliczeniowe ab initio w fizyce struktur atomowych. Wykład 1: Wstęp dr inż. Paweł Scharoch, dr Jerzy Peisert Instytut Fizyki Politechniki Wrocławskiej, 03.02.2005r. Streszczenie: wyjaśnienie pojęcia
Metody obliczeniowe ab initio w fizyce struktur atomowych. Wykład 1: Wstęp dr inż. Paweł Scharoch, dr Jerzy Peisert Instytut Fizyki Politechniki Wrocławskiej, 03.02.2005r. Streszczenie: wyjaśnienie pojęcia
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
2. Opis zajęć dydaktycznych i pracy studenta
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi poziom Sylabus modułu: Moduł przedmiotów specjalizacyjnych A (0310-CH-S2-004) Nazwa wariantu modułu (opcjonalnie): Metody
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi poziom Sylabus modułu: Moduł przedmiotów specjalizacyjnych A (0310-CH-S2-004) Nazwa wariantu modułu (opcjonalnie): Metody
Korelacja elektronowa w metodzie elongacji
 March 28, 2006 1 2 3 4 5 6 Waskie gard la metody jednowyznacznikowe wyznaczanie ca lek dwuelektronowych potrzebnych do budowy macierzy Focka: formalnie O(N 4 ), asymptotycznie O(N 2 ) diagonalizacja macierzy
March 28, 2006 1 2 3 4 5 6 Waskie gard la metody jednowyznacznikowe wyznaczanie ca lek dwuelektronowych potrzebnych do budowy macierzy Focka: formalnie O(N 4 ), asymptotycznie O(N 2 ) diagonalizacja macierzy
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Zastosowanie metody LDA do obliczeń stanów elektronowych wybranych układów nanoskopowych
 Uniwersytet Jagielloński Wydział Fizyki, Astronomii i Informatyki Stosowanej Instytut Fizyki im. Mariana Smoluchowskiego Zakład Teorii Materii Skondensowanej i Nanofizyki Magdalena Birowska Karolina Milowska
Uniwersytet Jagielloński Wydział Fizyki, Astronomii i Informatyki Stosowanej Instytut Fizyki im. Mariana Smoluchowskiego Zakład Teorii Materii Skondensowanej i Nanofizyki Magdalena Birowska Karolina Milowska
Testowanie hipotez statystycznych
 Testowanie hipotez statystycznych Wyk lad 8 Natalia Nehrebecka Stanis law Cichocki 29 listopada 2015 Plan zajeć 1 Rozk lad estymatora b Rozk lad sumy kwadratów reszt 2 Hipotezy proste - test t Badanie
Testowanie hipotez statystycznych Wyk lad 8 Natalia Nehrebecka Stanis law Cichocki 29 listopada 2015 Plan zajeć 1 Rozk lad estymatora b Rozk lad sumy kwadratów reszt 2 Hipotezy proste - test t Badanie
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Wyk lad 7 Baza i wymiar przestrzeni liniowej
 Wyk lad 7 Baza i wymiar przestrzeni liniowej 1 Baza przestrzeni liniowej Niech V bedzie przestrzenia liniowa. Powiemy, że podzbiór X V jest maksymalnym zbiorem liniowo niezależnym, jeśli X jest zbiorem
Wyk lad 7 Baza i wymiar przestrzeni liniowej 1 Baza przestrzeni liniowej Niech V bedzie przestrzenia liniowa. Powiemy, że podzbiór X V jest maksymalnym zbiorem liniowo niezależnym, jeśli X jest zbiorem
Podstawy chemii. dr hab. Wacław Makowski. Wykład 1: Wprowadzenie
 Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
RJC. Wiązania Chemiczne & Slides 1 to 39
 Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
WYMAGANIA NA POSZCZEGÓLNE STOPNIE SZKOLNE Z CHEMII klasa I
 WYMAGANIA NA POSZCZEGÓLNE STOPNIE SZKOLNE Z CHEMII klasa I Aby uzyskać ocenę wyższą niż dana ocena, uczeń musi opanować wiadomości i umiejętności dotyczące danej oceny oraz ocen od niej niższych. Dział:
WYMAGANIA NA POSZCZEGÓLNE STOPNIE SZKOLNE Z CHEMII klasa I Aby uzyskać ocenę wyższą niż dana ocena, uczeń musi opanować wiadomości i umiejętności dotyczące danej oceny oraz ocen od niej niższych. Dział:
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki
 OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
Testowanie hipotez statystycznych
 round Testowanie hipotez statystycznych Wyk lad 9 Natalia Nehrebecka Stanis law Cichocki 13 grudnia 2014 Plan zajeć 1 Rozk lad estymatora b Rozk lad sumy kwadratów reszt 2 Hipotezy proste - test t Badanie
round Testowanie hipotez statystycznych Wyk lad 9 Natalia Nehrebecka Stanis law Cichocki 13 grudnia 2014 Plan zajeć 1 Rozk lad estymatora b Rozk lad sumy kwadratów reszt 2 Hipotezy proste - test t Badanie
Chemia kwantowa. Pytania egzaminacyjne. 2010/2011: 1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
WYK LAD 5: GEOMETRIA ANALITYCZNA W R 3, PROSTA I P LASZCZYZNA W PRZESTRZENI R 3
 WYK LAD 5: GEOMETRIA ANALITYCZNA W R 3, PROSTA I P LASZCZYZNA W PRZESTRZENI R 3 Definicja 1 Przestrzenia R 3 nazywamy zbiór uporzadkowanych trójek (x, y, z), czyli R 3 = {(x, y, z) : x, y, z R} Przestrzeń
WYK LAD 5: GEOMETRIA ANALITYCZNA W R 3, PROSTA I P LASZCZYZNA W PRZESTRZENI R 3 Definicja 1 Przestrzenia R 3 nazywamy zbiór uporzadkowanych trójek (x, y, z), czyli R 3 = {(x, y, z) : x, y, z R} Przestrzeń
Kierunek i poziom studiów: Chemia. Drugi. Sylabus modułu: Chemia kwantowa i modelowanie molekularne (0310-CH-S2-B-062)
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia. Drugi. Sylabus modułu: Chemia kwantowa i modelowanie molekularne (0310-CH-S2-B-062) 1. Informacje ogólne koordynator modułu dr
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia. Drugi. Sylabus modułu: Chemia kwantowa i modelowanie molekularne (0310-CH-S2-B-062) 1. Informacje ogólne koordynator modułu dr
w jednowymiarowym pudle potencja lu
 Do wyk ladu II czastka w pudle potencja lu oscylator harmoniczny rotator sztywny Ścis le rozwiazania równania Schrödingera: atom wodoru i jon wodoropodobny) Czastka w jednowymiarowym pudle potencja lu
Do wyk ladu II czastka w pudle potencja lu oscylator harmoniczny rotator sztywny Ścis le rozwiazania równania Schrödingera: atom wodoru i jon wodoropodobny) Czastka w jednowymiarowym pudle potencja lu
Grupa Moniki Musiał. Uniwersytet Śląski Instytut Chemii Zakład Chemii Teoretycznej
 Wieloreferencyjna metoda sprzężonych klasterów w dwuwalencyjnych sektorach przestrzeni Focka oraz metoda równań ruchu w zastosowaniu do opisu stanów wzbudzonych Grupa Moniki Musiał Uniwersytet Śląski Instytut
Wieloreferencyjna metoda sprzężonych klasterów w dwuwalencyjnych sektorach przestrzeni Focka oraz metoda równań ruchu w zastosowaniu do opisu stanów wzbudzonych Grupa Moniki Musiał Uniwersytet Śląski Instytut
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 2 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 2 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
METODY POSTHARTREE-FOCKOWSKIE MONIKA MUSIA L
 METODY POSTHARTREE-FOCKOWSKIE MONIKA MUSIA L Jednym z ważniejszych zadań chemii kwantowej jest opracowywanie nowych metod obliczeniowych umożliwiaj acych bardzo dok ladne wyznaczanie e- nergii korelacji
METODY POSTHARTREE-FOCKOWSKIE MONIKA MUSIA L Jednym z ważniejszych zadań chemii kwantowej jest opracowywanie nowych metod obliczeniowych umożliwiaj acych bardzo dok ladne wyznaczanie e- nergii korelacji
Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych
 Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych Wstęp Krzywa energii potencjalnej 1 to wykres zależności energii potencjalnej cząsteczek od długości wiązania (czyli od wzajemnej
Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych Wstęp Krzywa energii potencjalnej 1 to wykres zależności energii potencjalnej cząsteczek od długości wiązania (czyli od wzajemnej
Rzędy wiązań chemicznych
 Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Wyznaczanie w lasności molekularnych w stanach wzbudzonych oraz w uk ladach skoniugowanych.
 Uniwersytet Śl aski Wydzia l Matematyki Fizyki i Chemii Piotr Zerzucha Wyznaczanie w lasności molekularnych w stanach wzbudzonych oraz w uk ladach skoniugowanych. Praca doktorska wykonana w Zak ladzie
Uniwersytet Śl aski Wydzia l Matematyki Fizyki i Chemii Piotr Zerzucha Wyznaczanie w lasności molekularnych w stanach wzbudzonych oraz w uk ladach skoniugowanych. Praca doktorska wykonana w Zak ladzie
Statystyka w analizie i planowaniu eksperymentu
 29 marca 2011 Przestrzeń statystyczna - podstawowe zadania statystyki Zdarzeniom losowym określonym na pewnej przestrzeni zdarzeń elementarnych Ω można zazwyczaj na wiele różnych sposobów przypisać jakieś
29 marca 2011 Przestrzeń statystyczna - podstawowe zadania statystyki Zdarzeniom losowym określonym na pewnej przestrzeni zdarzeń elementarnych Ω można zazwyczaj na wiele różnych sposobów przypisać jakieś
