1. Przesłanki doświadczalne mechaniki kwantowej.
|
|
|
- Aneta Sobczak
- 7 lat temu
- Przeglądów:
Transkrypt
1 1 Pytania egzaminacyjne: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny- interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest liczba wybijanych elektronów i ich pęd z natężeniem i częstością padającego promieniowania. 4.Fotonuwalniaelektronoenergii2eVzmetalu,dlaktóregopracawyjścia wynosi 2 ev. Jaka jest największa możliwa długość fali tego fotonu? 5. Wskazać prawa zachowania, których spełnienie pozwala poprawnie zinterpretować zjawisko Comptona. 6.Czyfotonposiadapęd-wyjaśnićwoparciuozjawiskoComptona 7. Hipoteza de Broglie a. Fala de Broglie a. Relacje de Broglie a. 8.ObliczdługośćfalideBroglie adlaelektronu(m e = kg)oenergii 10eV. 9.ObliczdługośćfalideBroglie adlaprotonu(m p = kg)oenergii 10eV. 10.ObliczprzeciętnądługośćfalideBroglie adlaatomuhelu(m=7300m e )w temperaturze pokojowej. 11. Zasada nieoznaczoności: podstawowe relacje i interpretacja. 12. Założenia teorii Bohra budowy atomu wodoru. 13. Teoria Bohra: energia, prędkość i pęd elektronu w atomie wodoru; promienie orbit elektronowych w jonach wodoropodobnych. 14. Widmo elektronowe atomu wodoru. 15. Serie widmowe atomu wodoru w nadfiolecie. 16. Serie widmowe atomu wodoru w zakresie widzialnym 17. Serie widmowe atomu wodoru w podczerwieni. 18. Określić wymiar SI[kg,m,s] następujących wielkości x: x 1 = n2 h 2 mke 2;x 2= Zke2 n h ;x 3= mz2 k 2 e 4 n 2 h 2 gdzie:n głównaliczbakwantowa;z liczbaatomowa; h stałaplancka kreślona; m masa elektronu; k stała Coulomba; e ładunek elektronu
2 2 19. Postulaty mechaniki kwantowej: ogólna charakterystyka. 20. Pierwszy postulat mechaniki kwantowej. 21. Drugi postulat mechaniki kwantowej. 22. Trzeci postulat mechaniki kwantowej. 23. Czwarty postulat mechaniki kwantowej. 24. Piąty postulat mechaniki kwantowej. 25. Normalizacja funkcji falowej, przykład. 26. Interpretacja funkcji falowej: prawdopodobieństwo i gęstość prawdopodobieństwa. 27. Reguły Jordana konstrukcji operatorów kwantowomechanicznych: przykład. 28. Własności operatorów kwantowomechanicznych: liniowość i hermitowskość. 29.Wykazaćhermitowskośćoperatorai d dx 30.Wykazaćhermitowskośćoperatora d2 dx Podać przykład równania własnego dowolnego operatora; udowodnić, że występująca w równaniu funkcja jest funkcją własną operatora. 32. Wykazać, że wartości własne operatora hermitowskiego są rzeczywiste. 33. Wykazać, że funkcje własne operatora hermitowskiego odpowiadające różnym wartościom własnym są ortogonalne. 34.Obliczyćkomutator[ˆp x,ˆx]. 35. Wykazać, że komutujące operatory posiadają wspólny zbiór funkcji własnych. 36. Wykazać przemienność operatorów posiadających wspólny zbiór funkcji własnych. 37. Równanie Schrödingera zależne od czasu. Zależność od czasu funkcji falowej w stanach stacjonarnych. 38. Równanie Schrödingera dla stanów stacjonarnych. 39.Funkcjastanu,Ψ k,jestfunkcjąwłasnąoperatoraˆf(zwartościąwłasnąf k ). Co można powiedzieć o wyniku pomiaru zmiennej F? 40.OkreślićwartośćoczekiwanąoperatoraˆFwstanieΨ n jeżelifunkcjaψ n jest jego funkcją własną. 41. Funkcja Ψ może być rozwinięta na układ zupełny funkcji własnych operatora ˆF,φ i.wyrazićwartośćspodziewanąoperatorapoprzezjegowartościwłasne. 42.Zbadaćczyfunkcjae ar jestfunkcjąwłasnąoperatorad/dx. 43.ZnormalizowaćfunkcjeΨ=e ar wcałejprzestrzeni.
3 3 44. Cząstka swobodna: operator energii, równanie Schrödingera, pęd cząstki. 45. Cząstka swobodna: funkcja falowa, normalizacja, wartości własne operatora energii. 46. Cząstka w pudle potencjału: hamiltonian, równanie Schrödingera, pęd cząstki. 47. Cząstka w pudle potencjału: funkcja falowa, normalizacja, wartości wąsne energii. 48. Kwantowanie energii kinetycznej atomów i cząsteczek w zbiorniku; poziomy energetyczne translacji. 49. Równanie ruchu dla oscylatora harmonicznego wg fizyki klasycznej. 50. Fukcje opisujące położenie, prędkość cząstki w ruchu harmonicznym w ujęciu klasycznym. 51. Energia całkowita, kinetyczna i potencjalna oscylatora harmonicznego w ujęciu klasycznym. 52. Przeliczyć na elektronowolty oraz dżule na mol energię drgań o częstości 1000cm 1 (h= Js,e= Podaćfunkcjęwłasnąhamiltonianudlav=0(zdokładnościądostałejnormalizacyjnej); udowodnić, że spełnia równanie Schrödingera dla oscylatory harmonicznego. 54.WykazaćżefunkcjaΨ=ξe ξ2 2 spełniarównanie: dlav=1( λ α 1=2v) 2 Ψ ξ 2 ξ2 Ψ+ λ α Ψ=0 55.ZnależćtrzywielomianyHermite a:h 1,H 2,H 3 (H v (x)=( 1) v e x2 d v dx v e x2 56. Hamiltonian i równanie Schrödingera dla oscylatora harmonicznego. 57. Wartości własne hamiltonianu dla oscylatora harmonicznego. 58. Funkcje własne hamiltonianu dla oscylatora harmonicznego. 59. Porównanie ruchu harmonicznego wg fizyki klasycznej i kwantowej. 60. Oscylacje cząsteczki dwuatomowej, poziomy energetyczne, reguły wyboru. 61. Moment pędu w fizyce klasycznej. 62. Operator momentu pędu: współrzędne kartezjańskie i sferyczne. 63. Wykazać, że operator kwadratu momentu pędu jest przemienny z operatorem dowolnej składowej momentu pędu. 64.Obliczyćkomutatoroperatorówskładowychmomentupędunp.[ˆM x,ˆm y ] 65. Równanie własne operatora składowej zetowej momentu pędu.
4 4 66. Równanie własne operatora kwadratu momentu pędu. 67. Wartośći własne operatorów kwadratu i składowej zetowej momentu pędu 68. Funkcje własne operatora składowej zetowej momentu pędu. 69. Funkcje własne i wartości własne kwadratu składowej zetowej momentu pędu. 70. Funkcje własne operatora kwadratu momentu pędu. 71. Liczby kwantowe w zagadnieniu momentu pędu. 72. Rotator sztywny: hamiltonian, równanie Schrödingera, wartości własne, degeneracja. 73. Energia poziomów rotacyjnych; stała rotacyjna, przejścia rotacyjne. 74. Widmo rotacyjne cząsteczek, poziomy energetyczne, reguły wyboru. 75. Zaproponować wyznaczenie długości wiązania w cząsteczce dwuatomowej w oparciu o jej widmo rotacyjne. 76. Formy energii molekularnej: oscylacyjna, rotacyjna, translacyjna. Porównanie odległości między poziomami energetycznymi w poszczególnych formach. 77. Hamiltonian i równanie Schrödingera dla atomu wodoru; związek hamiltonianu z operatorem kwadratu momentu pędu. 78. Ogólny schemat rozwiązywania równania Schrödingera dla atomu wodoru. 79. Kwantowanie wartości własnych hamiltonianu w atomie wodoru; degeneracja, korelacja z teorią Bohra. 80. Funkcje własne hamiltonianu dla atomu wodoru. Ogólna charakterystyka. 81. Część radialna funkcji falowej w jonach wodoropodobnych. 82. Część kątowa funkcji falowej w atomie wodoru. 83. Liczby kwantowe w atomie wodoru i jonach wodoropodobnych. 84. Orbitale atomowe; postać rzeczywista. 85. Warstwice orbitalu, warstwice gęstości prawdopodobieństwa. 86. Kontury orbitalu i kontury gęstości prawdopodobieństwa. 87. Radialna gęstość prawdopodobieństwa. 88. Promienie orbit bohrowskich a maksima radialnej gęstości prawdopodobieństwa w atomie wodoru. 89. Powierzchnie węzłowe w części radialnej i w części kątowej orbitali w atomie wodoru. 90. Orbitale s: kształt konturu, część radialna, część kątowa. 91. Orbitale p: kształt konturu, część radialna, część kątowa.
5 5 92. Orbitale d: kształt konturu, część radialna, część kątowa. 93. Spin i spinowa liczba kwantowa; liczby kwantowe opisujące stan elektronu watomie. 94.Układrównańwłasnychdlaoperatorówspinowych:ŝ 2 iŝ z. 95. Zasada wariacyjna. 96. Metoda wariacyjna. 97. Metoda Ritza 98. Skonstruować wyznacznik sekularny i zapisać równania sekularna gdy N (=wymiar bazy) wynosi 3. Wskazać calki nakładania i elementy macierzy operatora energii. 99. Macierzowa postać równań sekularnych; zdefiniować występujące w nich macierze Zapisać operator Hamiltona dla atomu N-elektronowego Omówić zakaz Pauliego Realizacja zakazu Pauliego dla wyznacznikowej funkcji falowej Zapisać N-elektrową funkcję falową w przybliżeniu orbitalnym Omówić przybliżenie jednoelektronowe. 105.Zróżniczkowaćpoc p następującewyrażenie(ǫ=jestfunkcjąparametrów c p ) N N N N ǫ c r c qs rq = c r c qh rq q=1r=1 q=1r= Podać po dwa przykłady pierwiastków o niezapełnionej podpowłoce f należących do różnych okresów w tablicy Mendelejewa Podać wyrażenie określające maksymalną liczbę elektronów na podpowłoce o liczbie kwantowej l Podać dwa przykłady pierwiastków zamkniętopowłokowych, z których każdy należy do innego stanu skupienia Podać przykład czterech pierwiastków, których konfiguracje elektronowe stanowią odstępstwo od reguł zabudowy elektronowej(przynajmniej jeden z niezapełnioną podpowłoką f). 110.Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjinp Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjind Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjinf Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjinp 2.
6 6 114.Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjind Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjins 1 p Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjins 1 d Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracjins 1 f Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracji2s 1 3s Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracji2p 1 3p Wyznaczyćtermyatomoweiwskazaćpodstawowydlakonfiguracji3d 1 4d Podać przykład czterech pierwiastków, należących do różnych grup w układzie okresowym, których term podstawowy jest singletem Podać przykład czterech pierwiastków należących do różnych grup w układzie okresowym, których term podstawowy jest dubletem Podać przykład czterech pierwiastków należących do różnych grup w układzie okresowym, których term podstawowy jest trypletem Podać przykład czterech pierwiastków należących do różnych grup w układzie okresowym, których term podstawowy jest kwartetem Podać przykład dwóch pierwiastków należących do różnych grup w układzie okresowym, których term podstawowy jest kwintetem Podać przykład dwóch pierwiastków należących do różnych grup w układzie okresowym, których term podstawowy jest sekstetem. 127.Wskazaćtermpodstawowydlakonfiguracjip Wskazaćtermpodstawowydlakonfiguracjid Wskazaćtermpodstawowydlakonfiguracjid Wskazaćtermpodstawowydlakonfiguracjid Wskazaćtermpodstawowydlakonfiguracjid Wskazaćtermpodstawowydlakonfiguracjif Wskazaćtermpodstawowydlakonfiguracjif Wskazaćtermpodstawowydlakonfiguracjif Wskazaćtermpodstawowydlakonfiguracjif Wskazaćtermpodstawowydlakonfiguracjif Wskazaćtermpodstawowydlakonfiguracjif Reguły Hunda dla termów atomowych Wyjaśnić istotę błędu wprowadzonego przez przybliżenie orbitalne Degeneracja poziomów energetycznych w atomach wieloelektronowych.
7 Zasady dodawania wektorów momentów pędu Część kątowa orbitali w atomie wieloelektronowym Przybliżone metody wyznaczania części radialnych orbitali w atomie wieloelektronowym Reguły Slatera Przybliżenie Borna-Oppenheimera Skonstruować hamiltonian w ramach przybliżenia Borna-Oppenheimera dla cząsteczkiskładającejsięzdwóchatomówoliczbachatomowychz 1 iz Skonstruować hamiltonian w ramach przybliżenia Borna-Oppenheimera dla dwuatomowej cząsteczki homojądrowej Skonstruować pełny hamiltonian dla cząsteczki benzenu. 149.SkonstruowaćpełnyhamiltoniandlajonuSO Skonstruować pełny hamiltonian dla cząsteczki czterofluorku uranu Skonstruować pełny hamiltonian dla dimeru kwasu mrówkowego Skonstruować hamiltonian w ramach przybliżenia Borna-Oppenheimera dla kompleksu złożonego z trzech cząsteczek wody. 153.CząsteczkaH + 2 icząsteczkah ZnormalizowaćorbitalmolekularnyΨ=N(χ a +χ b )przyzałożeniu,żefunkcjeχ a,bsąunormowane. 155.ZnormalizowaćorbitalmolekularnyΨ=N(χ a χ b )przyzałożeniu,żefunkcjeχ a,bsąunormowane Wyznaczyć energię orbitalu wiążącego w cząsteczce wodoru 157. Klasyfikacja orbitali molekularnych 158. Scharakteryzować orbital molekularny typu σ Scharakteryzować orbital molekularny typu π Scharakteryzować orbital molekularny typu δ Orbitale wiążące i antywiążące metoda LCAOMO Cząsteczki dwuatomowe homojądrowe Poziomy energetyczne w cząsteczkach dwuatomowych homojądrowych Rząd wiązania w homojądrowych cząsteczkach dwuatomowych Trwałość cząsteczek dwuatomowych Konfiguracje elektronowe dwuatomowych cząsteczek homojądrowych.
8 Struktura elektronowa cząsteczki CO. 169.EnergieidługościwiązańwszereguN 2,N + 2,N Własności paramagnetyczne cząsteczek dwuatomowych homojądrowych Omówić pojęcie hybrydyzacji orbitali atomowych Wykazać niezmienniczość wyznacznikowej funkcji falowej przy transformacji ortogonalnej orbitali Gęstość elektronowa wobec transformacji unitarnej(ortogonalnej) orbitali Hybrydyzacja sp.przykłady cząsteczek zawierających atomy o takiej hybrydyzacji. 175.Hybrydyzacjasp 2.przykładycząsteczekzawierającychatomyotakiejhybrydyzacji. 176.Hybrydyzacjasp 3.przykładycząsteczekzawierającychatomyotakiejhybrydyzacji. 177.Hybrydyzacjasp 3 d.przykładycząsteczekzawierającychatomyotakiejhybrydyzacji. 178.Hybrydyzacjasp 3 d 2.przykładycząsteczekzawierającychatomyotakiejhybrydyzacji Hybrydyzacja sd.przykłady cząsteczek zawierających atomy o takiej hybrydyzacji. 180.ScharakteryzowaćgeometrięcząsteczekCH 4 ibacl 2 ;posłużyćsiępojęciem hybrydyzacji. 181.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekC 2 H 4 iscl 2 ; 182.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekC 2 H 2 iicl 2 ; 183.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekPCl 5 izncl 2 ; 184.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekSF 6 ih 2 O; 185.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekBCl 3 inh 3 ; 186.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekNO 3 ih 3O + ; 187.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekSO 2 4 ibricl ; 188.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekNH + 4 ihgcl 2;
9 9 189.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekPCl 6 iso 2; 190.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekIF 5 ino 2 ; 191.ScharakteryzowaćstrukturęelektronowąigeometrięcząsteczekBrF 5 iso 3 ; 192. Układy π-elektronowe Węglowdory o układach π-elektronowych skumulowanych, skoniugowanych i izolowanych Metoda Hückla Konstrukcja macierzy energii(macierzy operatora Hamiltona) w metodzie Hückla Równania sekularne w metodzie Hückla Parametryzacja całki kulombowskiej w metodzie Hückla Parametryzacja całki rezonansowej w metodzie Hückla Energie orbitalne w metodzie Hückla Węglowodory naprzemienne i nienaprzemienne Zapisać i rozwiązać układ równań sekularnych w metodzie Hückla dla rodnika allilowego Orbitale Hückla dla etenu(energia, symetria, współczynniki LCAO) Orbitale Hückla dla allilu(energia, symetria, charakterystyka) Orbitale Hückla dla butadienu(rozkład energii, symetria, plaszczyzny węzłowe) Orbitale Hückla dla heksatrienu(rozkład energii, symetria, plaszczyzny węzłowe) Orbitale Hückla dla cyklopropenylu(rozkład energii, symetria, plaszczyzny węzłowe) Orbitale Hückla dla cyklobutadienu(rozkład energii, symetria, plaszczyzny węzłowe) Orbitale Hückla dla cyklopentadienylu(rozkład energii, symetria, plaszczyzny węzłowe) Orbitale Hückla dla benzenu(energia, symetria, plaszczyzny węzłowe) Struktura π-elektronowa węglowodorów aromatycznych Udział heteroatomów w układzie π-elektronowym węglowodorów aromatycznych.
10 212. Aromatyczność i reguła Hückla. 213.Strukturaπ-elektronowaihybrydyzacjaatomówwcząsteczcepiroluC 4 H 4 NH. 214.Strukturaπ-elektronowaihybrydyzacjaatomówwcząsteczcepirydynyC 5 H 5 N. 215.Strukturaπ-elektronowaihybrydyzacjaatomówwcząsteczcefuranuC 4 H 4 O. 216.Strukturaπ-elektronowaihybrydyzacjaatomówwcząsteczcetiofenuC 4 H 4 S. 217.Strukturaπ-elektronowaihybrydyzacjaatomówwcząsteczceanilinyC 6 H 5 NH Struktura π-elektronowa i hybrydyzacja atomów w cząsteczce nitrobenzenu C 6 H 5 NO Strukturaπ-elektronowaihybrydyzacjaatomówwcząsteczcestyrenuC 6 H 5 CH= CH Struktura π-elektronowa i hybrydyzacja atomów w cząsteczce aldehydu benzoesowegoc 6 H 5 CHO Struktura π-elektronowa i hybrydyzacja atomów w cząsteczce imidazolu C 3 N 2 H Strukturaπ-elektronowaihybrydyzacjaatomówwcząsteczcefenoluC 6 H 5 OH Energia delokalizacji w metodzie Hückla Rząd wiązania w metodzie Hückla Populacja π-elektronowa atomu( gęstość π-elektronowa ) w metodzie Hückla. 226.Wyznaczyćenergiędelokalizacjidlacząsteczkibutadienu(e 1 =1.62,e 2 = 0.62) Obliczyć π-elektronowy rząd wiązania dla cząsteczki etenu Obliczyć π-elektronowy rząd wiązania dla wiązania 1-2 w cząsteczce butadienu: φ 1 = 0.37π (π 2 +π 3 )+0.37π 4 φ 2 = 0.60π (π 2 π 3 ) 0.60π Obliczyć π-elektronowy rząd wiązania dla wiązania 2-3 w cząsteczce butadienu: φ 1 = 0.37π (π 2 +π 3 )+0.37π 4 φ 2 = 0.60π (π 2 π 3 ) 0.60π Obliczyć π-elektronową populację dowolnego atomu( gęstość π-elektronową ) w cząsteczce butadienu: φ 1 = 0.37π (π 2 +π 3 )+0.37π 4 φ 2 = 0.60π (π 2 π 3 ) 0.60π 4 10
Chemia kwantowa. Pytania egzaminacyjne. 2010/2011: 1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Mechanika kwantowa. Erwin Schrödinger ( ) Werner Heisenberg
 Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
Stara i nowa teoria kwantowa
 Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Spis treści. Przedmowa redaktora do wydania czwartego 11
 Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały
 WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
Fizyka 3.3 WYKŁAD II
 Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Atom wodoru i jony wodoropodobne
 Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Zad Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji.
 Zad. 1.1. Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji. Zad. 1.1.a. Funkcja: ϕ = sin2x Zad. 1.1.b. Funkcja: ϕ = e x 2 2 Operator: f = d2 dx
Zad. 1.1. Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji. Zad. 1.1.a. Funkcja: ϕ = sin2x Zad. 1.1.b. Funkcja: ϕ = e x 2 2 Operator: f = d2 dx
Wykład 16: Atomy wieloelektronowe
 Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Atom wodoru w mechanice kwantowej. Równanie Schrödingera
 Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 9 Podstawy teorii kwantów fale materii, dualizm falowo-korpuskularny, funkcja falowa, równanie Schrödingera, stacjonarne równanie
 Wykład 9 Podstawy teorii kwantów fale materii, dualizm falowo-korpuskularny, funkcja falowa, równanie Schrödingera, stacjonarne równanie Schrödingera, zasada nieoznaczoności Heisenberga, ruch cząstki swobodnej,
Wykład 9 Podstawy teorii kwantów fale materii, dualizm falowo-korpuskularny, funkcja falowa, równanie Schrödingera, stacjonarne równanie Schrödingera, zasada nieoznaczoności Heisenberga, ruch cząstki swobodnej,
Chemia ogólna - część I: Atomy i cząsteczki
 dr ab. Wacław Makowski Cemia ogólna - część I: Atomy i cząsteczki 1. Kwantowanie. Atom wodoru 3. Atomy wieloelektronowe 4. Termy atomowe 5. Cząsteczki dwuatomowe 6. Hybrydyzacja 7. Orbitale zdelokalizowane
dr ab. Wacław Makowski Cemia ogólna - część I: Atomy i cząsteczki 1. Kwantowanie. Atom wodoru 3. Atomy wieloelektronowe 4. Termy atomowe 5. Cząsteczki dwuatomowe 6. Hybrydyzacja 7. Orbitale zdelokalizowane
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Podstawy chemii. dr hab. Wacław Makowski. Wykład 1: Wprowadzenie
 Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Układy wieloelektronowe
 Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
FALE MATERII. De Broglie, na podstawie analogii optycznych, w roku 1924 wysunął hipotezę, że
 FAL MATRII De Broglie, na podstawie analogii optycznych, w roku 194 wysunął hipotezę, że cząstki materialne także charakteryzują się dualizmem korpuskularno-falowym. Hipoteza de Broglie a Cząstce materialnej
FAL MATRII De Broglie, na podstawie analogii optycznych, w roku 194 wysunął hipotezę, że cząstki materialne także charakteryzują się dualizmem korpuskularno-falowym. Hipoteza de Broglie a Cząstce materialnej
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
Symbol termu: edu (sumy ca lkowitego orbitalnego momentu edu i ca lkowitego spinu) Przyk lad: 2 P 3. kwantowa
 Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
Fizyka 2. Janusz Andrzejewski
 Fizyka 2 wykład 14 Janusz Andrzejewski Atom wodoru Wczesne modele atomu -W czasach Newtona atom uważany była za małą twardą kulkę co dość dobrze sprawdzało się w rozważaniach dotyczących kinetycznej teorii
Fizyka 2 wykład 14 Janusz Andrzejewski Atom wodoru Wczesne modele atomu -W czasach Newtona atom uważany była za małą twardą kulkę co dość dobrze sprawdzało się w rozważaniach dotyczących kinetycznej teorii
JEDNOSTKI ATOMOWE =1, m e =1, e=1, ; 1 E 2 h = 4, J. Energia atomu wodoru lub jonu wodoropodobnego w jednostkach atomowych:
 do wyk ladu z 1.10.13 Atom wodoru i jon wodoropodobny Ze - ladunek jadra, e - ladunek elektronu, µ - masa zredukowana µ = mem j m e+m j ( µ m e ) M j - masa jadra, m e - masa elektronu, ε 0 - przenikalność
do wyk ladu z 1.10.13 Atom wodoru i jon wodoropodobny Ze - ladunek jadra, e - ladunek elektronu, µ - masa zredukowana µ = mem j m e+m j ( µ m e ) M j - masa jadra, m e - masa elektronu, ε 0 - przenikalność
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków).
 Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Chemia Ogólna wykład 1
 Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Fizyka 3. Konsultacje: p. 329, Mechatronika
 Fizyka 3 Konsultacje: p. 39, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 1 sprawdzian 30 pkt 15.1 18 3.0 18.1 1 3.5 1.1 4 4.0 4.1 7 4.5 7.1 30 5.0 http:\\adam.mech.pw.edu.pl\~marzan Program: - elementy
Fizyka 3 Konsultacje: p. 39, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 1 sprawdzian 30 pkt 15.1 18 3.0 18.1 1 3.5 1.1 4 4.0 4.1 7 4.5 7.1 30 5.0 http:\\adam.mech.pw.edu.pl\~marzan Program: - elementy
IX. MECHANIKA (FIZYKA) KWANTOWA
 IX. MECHANIKA (FIZYKA) KWANTOWA IX.1. OPERACJE OBSERWACJI. a) klasycznie nie ważna kolejność, w jakiej wykonujemy pomiary. AB = BA A pomiar wielkości A B pomiar wielkości B b) kwantowo wartość obserwacji
IX. MECHANIKA (FIZYKA) KWANTOWA IX.1. OPERACJE OBSERWACJI. a) klasycznie nie ważna kolejność, w jakiej wykonujemy pomiary. AB = BA A pomiar wielkości A B pomiar wielkości B b) kwantowo wartość obserwacji
Chemia teoretyczna I Semestr V (1 )
 1/ 6 Chemia Chemia teoretyczna I Semestr V (1 ) Osoba odpowiedzialna za przedmiot: dr hab. inż. Aleksander Herman. 2/ 6 Wykład Program Podstawy mechaniki kwantowej Ważne problemy modelowe Charakterystyka
1/ 6 Chemia Chemia teoretyczna I Semestr V (1 ) Osoba odpowiedzialna za przedmiot: dr hab. inż. Aleksander Herman. 2/ 6 Wykład Program Podstawy mechaniki kwantowej Ważne problemy modelowe Charakterystyka
gęstością prawdopodobieństwa
 Funkcja falowa Zgodnie z hipotezą de Broglie'a, cząstki takie jak elektron czy proton, mają własności falowe. Własności falowe cząstki (lub innego obiektu) w mechanice kwantowej opisuje tzw. funkcja falowa(,t)
Funkcja falowa Zgodnie z hipotezą de Broglie'a, cząstki takie jak elektron czy proton, mają własności falowe. Własności falowe cząstki (lub innego obiektu) w mechanice kwantowej opisuje tzw. funkcja falowa(,t)
RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU
 X. RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU Równanie Schrődingera niezależne od czasu to równanie postaci: ħ 2 2m d 2 x dx 2 V xx = E x (X.1) Warunki regularności na x i a) skończone b) ciągłe c) jednoznaczne
X. RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU Równanie Schrődingera niezależne od czasu to równanie postaci: ħ 2 2m d 2 x dx 2 V xx = E x (X.1) Warunki regularności na x i a) skończone b) ciągłe c) jednoznaczne
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
h 2 h p Mechanika falowa podstawy pˆ 2
 Mechanika falowa podstawy Hipoteza de Broglie a Zarówno promieniowanie jak i cząstki materialne posiadają naturę dwoistą korpuskularno-falową. Z każdą mikrocząstką można związać pewien proces falowy pierwotnie
Mechanika falowa podstawy Hipoteza de Broglie a Zarówno promieniowanie jak i cząstki materialne posiadają naturę dwoistą korpuskularno-falową. Z każdą mikrocząstką można związać pewien proces falowy pierwotnie
Atom wodoru. Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu:
 ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
Rok akademicki: 2012/2013 Kod: JFM s Punkty ECTS: 6. Poziom studiów: Studia I stopnia Forma i tryb studiów: Stacjonarne
 Nazwa modułu: Wstęp do fizyki atomowej i kwantowej Rok akademicki: 2012/2013 Kod: JFM-1-302-s Punkty ECTS: 6 Wydział: Fizyki i Informatyki Stosowanej Kierunek: Fizyka Medyczna Specjalność: Poziom studiów:
Nazwa modułu: Wstęp do fizyki atomowej i kwantowej Rok akademicki: 2012/2013 Kod: JFM-1-302-s Punkty ECTS: 6 Wydział: Fizyki i Informatyki Stosowanej Kierunek: Fizyka Medyczna Specjalność: Poziom studiów:
Konfiguracja elektronowa atomu
 Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
Zadania z mechaniki kwantowej
 Zadania z mechaniki kwantowej Gabriel Wlazłowski 13 maja 2016 Rachunek zaburzeń bez czasu 1. Metodą rachunku zaburzeń obliczyć pierwszą i drugą poprawkę dla poziomów energetycznych oscylatora harmonicznego
Zadania z mechaniki kwantowej Gabriel Wlazłowski 13 maja 2016 Rachunek zaburzeń bez czasu 1. Metodą rachunku zaburzeń obliczyć pierwszą i drugą poprawkę dla poziomów energetycznych oscylatora harmonicznego
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego
 Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
Wykład I.2 1 Kłopoty z mechaniką klasyczną. 2 Postulaty mechaniki kwantowej 1. Stan układu funkcja falowa ψ(x), ψ(x) 2 interpretacja
 Wykład I.2 1 Kłopoty z mechaniką klasyczną 2 Postulaty mechaniki kwantowej 1. Stan układu funkcja falowa ψ(x), ψ(x) 2 interpretacja probabilistyczna 2. Wielkości fizyczne operatory hermitowskie (obserwable)
Wykład I.2 1 Kłopoty z mechaniką klasyczną 2 Postulaty mechaniki kwantowej 1. Stan układu funkcja falowa ψ(x), ψ(x) 2 interpretacja probabilistyczna 2. Wielkości fizyczne operatory hermitowskie (obserwable)
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu
 Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
Inżynieria Biomedyczna. Wykład XII
 Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Początek XX wieku. Dualizm korpuskularno - falowy
 Początek XX wieku Światło: fala czy cząstka? Kwantowanie energii promieniowania termicznego postulat Plancka efekt fotoelektryczny efekt Comptona Fale materii de Broglie a Dualizm korpuskularno - falowy
Początek XX wieku Światło: fala czy cząstka? Kwantowanie energii promieniowania termicznego postulat Plancka efekt fotoelektryczny efekt Comptona Fale materii de Broglie a Dualizm korpuskularno - falowy
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
0900 FS2 2 FAC. Fizyka atomu i cząsteczki FT 8. WYDZIAŁ FIZYKI UwB KOD USOS: Karta przedmiotu. Przedmiot moduł ECTS. kierunek studiów: FIZYKA 2 st.
 WYDZIAŁ FIZYKI UwB KOD USOS: 0900 FS2 2 FAC Karta przedmiotu Przedmiot moduł ECTS Fizyka atomu i cząsteczki FT 8 kierunek studiów: FIZYKA 2 st. specjalność: FIZYKA TEORETYCZNA Formy zajęć wykład konwersatorium
WYDZIAŁ FIZYKI UwB KOD USOS: 0900 FS2 2 FAC Karta przedmiotu Przedmiot moduł ECTS Fizyka atomu i cząsteczki FT 8 kierunek studiów: FIZYKA 2 st. specjalność: FIZYKA TEORETYCZNA Formy zajęć wykład konwersatorium
13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe)
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 13 UKŁADY KILKU CZĄSTEK W MECHANICE KWANTOWEJ 13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe) Zajmiemy się kwantowym opisem atomu He
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 13 UKŁADY KILKU CZĄSTEK W MECHANICE KWANTOWEJ 13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe) Zajmiemy się kwantowym opisem atomu He
Dotyczy to zarówno istniejących już związków, jak i związków, których jeszcze dotąd nie otrzymano.
 Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki
 OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
PODSTAWY MECHANIKI KWANTOWEJ
 PODSTAWY MECHANIKI KWANTOWEJ Za dzień narodzenia mechaniki kwantowej jest uważany 14 grudnia roku 1900. Tego dnia, na posiedzeniu Niemieckiego Towarzystwa Fizycznego w Instytucie Fizyki Uniwersytetu Berlińskiego
PODSTAWY MECHANIKI KWANTOWEJ Za dzień narodzenia mechaniki kwantowej jest uważany 14 grudnia roku 1900. Tego dnia, na posiedzeniu Niemieckiego Towarzystwa Fizycznego w Instytucie Fizyki Uniwersytetu Berlińskiego
POSTULATY MECHANIKI KWANTOWEJ cd i formalizm matematyczny
 POSTULATY MECHANIKI KWANTOWEJ cd i formalizm matematyczny Funkcja Falowa Postulat 1 Dla każdego układu istnieje funkcja falowa (funkcja współrzędnych i czasu), która jest ciągła, całkowalna w kwadracie,
POSTULATY MECHANIKI KWANTOWEJ cd i formalizm matematyczny Funkcja Falowa Postulat 1 Dla każdego układu istnieje funkcja falowa (funkcja współrzędnych i czasu), która jest ciągła, całkowalna w kwadracie,
Ciało doskonale czarne absorbuje całkowicie padające promieniowanie. Parametry promieniowania ciała doskonale czarnego zależą tylko jego temperatury.
 1 Ciało doskonale czarne absorbuje całkowicie padające promieniowanie. Parametry promieniowania ciała doskonale czarnego zależą tylko jego temperatury. natężenie natężenie teoria klasyczna wynik eksperymentu
1 Ciało doskonale czarne absorbuje całkowicie padające promieniowanie. Parametry promieniowania ciała doskonale czarnego zależą tylko jego temperatury. natężenie natężenie teoria klasyczna wynik eksperymentu
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Efekt Comptona. Efektem Comptona nazywamy zmianę długości fali elektromagnetycznej w wyniku rozpraszania jej na swobodnych elektronach
 Efekt Comptona. Efektem Comptona nazywamy zmianę długości fali elektromagnetycznej w wyniku rozpraszania jej na swobodnych elektronach Efekt Comptona. p f Θ foton elektron p f p e 0 p e Zderzenia fotonów
Efekt Comptona. Efektem Comptona nazywamy zmianę długości fali elektromagnetycznej w wyniku rozpraszania jej na swobodnych elektronach Efekt Comptona. p f Θ foton elektron p f p e 0 p e Zderzenia fotonów
Postulaty interpretacyjne mechaniki kwantowej Wykład 6
 Postulaty interpretacyjne mechaniki kwantowej Wykład 6 Karol Kołodziej Instytut Fizyki Uniwersytet Śląski, Katowice http://kk.us.edu.pl 19 września 2014 Karol Kołodziej Postulaty interpretacyjne mechaniki
Postulaty interpretacyjne mechaniki kwantowej Wykład 6 Karol Kołodziej Instytut Fizyki Uniwersytet Śląski, Katowice http://kk.us.edu.pl 19 września 2014 Karol Kołodziej Postulaty interpretacyjne mechaniki
obrotów. Funkcje falowe cząstki ze spinem - spinory. Wykład II.3 29 Pierwsza konwencja Condona-Shortley a
 Wykład II.1 25 Obroty układu kwantowego Interpretacja aktywna i pasywna. Macierz obrotu w trzech wymiarach a operator obrotu w przestrzeni stanów. Reprezentacja obrotu w przestrzeni funkcji falowych. Transformacje
Wykład II.1 25 Obroty układu kwantowego Interpretacja aktywna i pasywna. Macierz obrotu w trzech wymiarach a operator obrotu w przestrzeni stanów. Reprezentacja obrotu w przestrzeni funkcji falowych. Transformacje
Liczby kwantowe elektronu w atomie wodoru
 Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
p.n.e. Demokryt z Abdery. Wszystko jest zbudowane z niewidzialnych cząstek - atomów (atomos ->niepodzielny)
 O atomie 460-370 p.n.e. Demokryt z Abdery Wszystko jest zbudowane z niewidzialnych cząstek - atomów (atomos ->niepodzielny) 1808 John Dalton teoria atomistyczna 1. Pierwiastki składają się z małych, niepodzielnych
O atomie 460-370 p.n.e. Demokryt z Abdery Wszystko jest zbudowane z niewidzialnych cząstek - atomów (atomos ->niepodzielny) 1808 John Dalton teoria atomistyczna 1. Pierwiastki składają się z małych, niepodzielnych
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE.
 1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
Księgarnia PWN: Krzysztof Pigoń, Zdzisław Ruziewicz Chemia fizyczna. T. 2
 Księgarnia PWN: Krzysztof Pigoń, Zdzisław Ruziewicz Chemia fizyczna. T. 2 Przedmowa XIII 8. PODSTAWY MECHANIKI KWANTOWEJ I STRUKTURA ELEKTRONOWA ATOMÓW 1 8.1. Podstawy doświadczalne teorii kwantów 1 8.1.1.
Księgarnia PWN: Krzysztof Pigoń, Zdzisław Ruziewicz Chemia fizyczna. T. 2 Przedmowa XIII 8. PODSTAWY MECHANIKI KWANTOWEJ I STRUKTURA ELEKTRONOWA ATOMÓW 1 8.1. Podstawy doświadczalne teorii kwantów 1 8.1.1.
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Metody obliczeniowe chemii kwantowej oparte na funkcji falowej. Dla uk ladu N elektronów i K j ader atomowych hamiltonian przyjmuje postać:
 Metody obliczeniowe chemii kwantowej oparte na funkcji falowej Równanie Schrödingera: ĤΨ = EΨ Dla uk ladu N elektronów i K j ader atomowych hamiltonian przyjmuje postać: Ĥ = h 2 K α=1 1 2M α 2 α h2 2m
Metody obliczeniowe chemii kwantowej oparte na funkcji falowej Równanie Schrödingera: ĤΨ = EΨ Dla uk ladu N elektronów i K j ader atomowych hamiltonian przyjmuje postać: Ĥ = h 2 K α=1 1 2M α 2 α h2 2m
CHEMIA KWANTOWA MONIKA MUSIA L METODA HÜCKLA. Ćwiczenia. http://zcht.mfc.us.edu.pl/ mm
 CHEMIA KWANTOWA MONIKA MUSIA L METODA HÜCKLA Ćwiczenia Zwi azki organiczne zawieraj ace uk lady π-elektronowe Sprzȩżony uk lad wi azań podwójnych: -C=C-C=C-C=C-C=C- Skumulowany uk lad wi azań podwójnych:
CHEMIA KWANTOWA MONIKA MUSIA L METODA HÜCKLA Ćwiczenia Zwi azki organiczne zawieraj ace uk lady π-elektronowe Sprzȩżony uk lad wi azań podwójnych: -C=C-C=C-C=C-C=C- Skumulowany uk lad wi azań podwójnych:
Jak matematycznie opisać własności falowe materii? Czym są fale materii?
 Funkcja falowa Jak matematycznie opisać własności falowe materii? Czym są fale materii? Własności falowe materii (cząstek, układów cząstek) opisuje matematycznie pewna funkcja falowa ( x, Funkcja falowa
Funkcja falowa Jak matematycznie opisać własności falowe materii? Czym są fale materii? Własności falowe materii (cząstek, układów cząstek) opisuje matematycznie pewna funkcja falowa ( x, Funkcja falowa
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Równanie falowe Schrödingera ( ) ( ) Prostokątna studnia potencjału o skończonej głębokości. i 2 =-1 jednostka urojona. Ψ t. V x.
 Równanie falowe Schrödingera h Ψ( x, t) + V( x, t) Ψ( x, t) W jednym wymiarze ( ) ( ) gdy V x, t = V x x Ψ = ih t Gdy V(x,t)=V =const cząstka swobodna, na którą nie działa siła Fala biegnąca Ψ s ( x, t)
Równanie falowe Schrödingera h Ψ( x, t) + V( x, t) Ψ( x, t) W jednym wymiarze ( ) ( ) gdy V x, t = V x x Ψ = ih t Gdy V(x,t)=V =const cząstka swobodna, na którą nie działa siła Fala biegnąca Ψ s ( x, t)
Wykład Atom o wielu elektronach Laser Rezonans magnetyczny
 Wykład 21. 12.2016 Atom o wielu elektronach Laser Rezonans magnetyczny Jeszcze o atomach Przypomnienie: liczby kwantowe elektronu w atomie wodoru, zakaz Pauliego, powłoki, podpowłoki, orbitale, Atomy wieloelektronowe
Wykład 21. 12.2016 Atom o wielu elektronach Laser Rezonans magnetyczny Jeszcze o atomach Przypomnienie: liczby kwantowe elektronu w atomie wodoru, zakaz Pauliego, powłoki, podpowłoki, orbitale, Atomy wieloelektronowe
Wczesne modele atomu
 Wczesne modele atomu Wczesne modele atomu Demokryt (400 p.n.e.) Grecki filozof Demokryt rozpoczął poszukiwania opisu materii około 2400 lat temu. Postawił pytanie: Czy materia może być podzielona na mniejsze
Wczesne modele atomu Wczesne modele atomu Demokryt (400 p.n.e.) Grecki filozof Demokryt rozpoczął poszukiwania opisu materii około 2400 lat temu. Postawił pytanie: Czy materia może być podzielona na mniejsze
Modele atomu wodoru. Modele atomu wodoru Thomson'a Rutherford'a Bohr'a
 Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
Mechanika kwantowa Schrödingera
 Fizyka 2 Wykład 2 1 Mechanika kwantowa Schrödingera Hipoteza de Broglie a wydawała się nie zgadzać z dynamiką Newtona. Mechanika kwantowa Schrödingera zawiera mechanikę kwantową jako przypadek graniczny
Fizyka 2 Wykład 2 1 Mechanika kwantowa Schrödingera Hipoteza de Broglie a wydawała się nie zgadzać z dynamiką Newtona. Mechanika kwantowa Schrödingera zawiera mechanikę kwantową jako przypadek graniczny
Rozdział 23 KWANTOWA DYNAMIKA MOLEKULARNA Wstęp. Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 3 KWANTOWA DYNAMIKA MOLEKULARNA 3.1 Wstęp Metoda ta umożliwia opis układu złożonego z wielu jonów i elektronów w stanie podstawowym. Hamiltonian układu
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 3 KWANTOWA DYNAMIKA MOLEKULARNA 3.1 Wstęp Metoda ta umożliwia opis układu złożonego z wielu jonów i elektronów w stanie podstawowym. Hamiltonian układu
gdzie λ - długość fali, h - stała Plancka, p - pęd cząstki.
 3.7. Model współczesny Louis Victor Pierre Raymond de Broglie (189-1987) (Rysunek 3-35) w swojej pracy doktorskiej z 194 roku, wysunął przypuszczenie, że skoro fale elektromagnetyczne mogą przejawiać naturę
3.7. Model współczesny Louis Victor Pierre Raymond de Broglie (189-1987) (Rysunek 3-35) w swojej pracy doktorskiej z 194 roku, wysunął przypuszczenie, że skoro fale elektromagnetyczne mogą przejawiać naturę
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
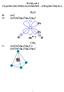 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
VII. CZĄSTKI I FALE VII.1. POSTULAT DE BROGLIE'A (1924) De Broglie wysunął postulat fal materii tzn. małym cząstkom przypisał fale.
 VII. CZĄSTKI I FALE VII.1. POSTULAT DE BROGLIE'A (1924) De Broglie wysunął postulat fal materii tzn. małym cząstkom przypisał fale. Światło wykazuje zjawisko dyfrakcyjne. Rys.VII.1.Światło padające na
VII. CZĄSTKI I FALE VII.1. POSTULAT DE BROGLIE'A (1924) De Broglie wysunął postulat fal materii tzn. małym cząstkom przypisał fale. Światło wykazuje zjawisko dyfrakcyjne. Rys.VII.1.Światło padające na
INŻYNIERIA BIOMEDYCZNA. Wykład IX
 INŻYNIERIA BIOMEDYCZNA Wykład IX 1 PLAN Fizyka około 1900 roku Promieniowanie elektromagnetyczne Natura materii Równanie Schrödingera Struktura elektronowa atomu Oryginalne dokumenty nie pozostawiają wątpliwości,
INŻYNIERIA BIOMEDYCZNA Wykład IX 1 PLAN Fizyka około 1900 roku Promieniowanie elektromagnetyczne Natura materii Równanie Schrödingera Struktura elektronowa atomu Oryginalne dokumenty nie pozostawiają wątpliwości,
INŻYNIERIA BIOMEDYCZNA. Wykład IX
 INŻYNIERIA BIOMEDYCZNA Wykład IX 01.12.2018 1 PLAN Fizyka około 1900 roku Promieniowanie elektromagnetyczne Natura materii Równanie Schrödingera Struktura elektronowa atomu Oryginalne dokumenty nie pozostawiają
INŻYNIERIA BIOMEDYCZNA Wykład IX 01.12.2018 1 PLAN Fizyka około 1900 roku Promieniowanie elektromagnetyczne Natura materii Równanie Schrödingera Struktura elektronowa atomu Oryginalne dokumenty nie pozostawiają
INŻYNIERIA BIOMEDYCZNA. Wykład IX
 INŻYNIERIA BIOMEDYCZNA Wykład IX 1 PLAN Fizyka około 1900 roku Promieniowanie elektromagnetyczne Natura materii Równanie Schrödingera Struktura elektronowa atomu Oryginalne dokumenty nie pozostawiają wątpliwości,
INŻYNIERIA BIOMEDYCZNA Wykład IX 1 PLAN Fizyka około 1900 roku Promieniowanie elektromagnetyczne Natura materii Równanie Schrödingera Struktura elektronowa atomu Oryginalne dokumenty nie pozostawiają wątpliwości,
