13. Termodynamika - równania Gibbsa, Gibbsa-Duhema i wstęp do diagramów fazowych.
|
|
|
- Przybysław Wacław Leszczyński
- 6 lat temu
- Przeglądów:
Transkrypt
1 13. Termodynamka - równana Gbbsa, Gbbsa-Duhema wstęp do dagramów fazowyh Potenjały termodynamzne: Energa wewnętrzna U reprezentuje ałkowtą energę układu, będąą sumą energ knetyznyh potenjalnyh zarówno w skal mkro- jak makroskopowej. Z defnj jest ona funkją entrop, śnena, oraz lzby mol w układze: U U S V N1 N n (,,... ) (13.1) Jak pokażemy sobe w dalszej zęś, różnzka energ wewnętrznej ma postać: du TdS pdv dn du 0 S, V, N onst (13.2) Energa swobodna Helmholtza F, jest funkją wykorzystywaną w opse przeman zahodząyh w warunkah zotermzno-zohoryznyh, będąą różną energ wewnętrznej oraz lozynu temperatury entrop: Jej różnzka, po uwzględnenu różnzk (13.2), ma postać: F U TS (13.3) df SdT pdv dn df 0 T, V, N onst (13.4) Entalpa H, jest funkją stanu zawerająa w sobe wartość energ koneznej do utworzena układu, oraz lość energ koneznej aby utworzyć dla nego mejse przy danyh wartośah objętoś śnena. Po zróżnzkowanu otrzymujemy: H U pv (13.5) dh TdS Vdp dn dh 0 S, p, N onst (13.6) Entalpa swobodna Gbbsa G jest z punktu wdzena naszyh zajęć najbardzej nteresująym potenjałem. Stosujemy go, gdy nteresuje nas wyznazene pray neobjętośowej, zyl np. pray układu zwązanej ze zmaną lzby mol substratów produktów. Potenjału tego używamy w warunkah zotermzno-zobaryznyh, które przy opsywanu zjawsk transportu w ele stałym są najzęśej rozważane. Entalpę swobodną Gbbsa wyrażamy wzorem: W tym przypadku różnzka ma postać: G H TS (13.7)
2 dg SdT Vdp dn dg 0 T, p, N onst (13.8) Rozważmy teraz zmanę stanu w układze w trake przemany ze stanu I do II. Zmana entalp Gbbsa wynese: G G H H ( T S T S ) U U ( p V p V ) ( T S T S ) (13.9) II I II I II II I I II I II II I I II II I I Jeśl rozważymy teraz warunk zobaryzno-zotermzne, oraz fakt że w układze zamknętym zmana energ wewnętrznej równa jest sume pray epła ( U w q ), to możemy zapsać: G G q w p( V V ) T ( S S ) q w pv T S (13.10) II I II I II I Całkowta praa wykonana przez lub nad układem może zostać podzelona na dwa złony: praę objętośową neobjętośową w': po podstawenu do (13.10) otrzymamy: w w' p V (13.11) G q w' T S (13.12) Zmanę entrop możemy rozdzelć na tą zahodząą w wynku przemany odwraalnej (d e S) neodwraalnej (d S). Gdy to uwzględnmy, to dostanemy wyrażene: dg Td s dw' (13.13) jeśl zatem mamy do zynena tylko z praą objętośową podzas przemany neodwraalnej, która to przemana jest dodatkowo samorzutna (a zatem entropa rośne), to warunkem jest: G 0 (13.14) Na kone tej zęś podajmy pewne zależnoś wynkająe z posta potenjałów termodynamznyh: Zgodne z równanem (13.2): du du du T, p, ds dv dn V, N S, N S, V (13.15) zgodne z (13.4): df df df S, p, dt dv dn V, N T, N T, V (13.16) zgodne z (13.6):
3 dh dh dh T, V, ds dp dn p, N SN, S, p (13.17) zgodne z (13.8): dg dg dg T, V, dt dp dn p, N TN, p, T (13.18) Równane kanonzne - równana Gbbsa Gbbsa-Duhema: Za równane kanonzne termodynamk uznajemy równane (13.1): U U S N1 N n (,,... ) (13.19) różnzkują to równane otrzymujemy tzw. różnzkową postać równana Gbbsa: U U U du ds dv dn S V N Zgodne z zależnośam przedstawonym w (13.15): (13.20) du TdS pdv dn (13.21) Trzeba pamętać, że powyższe równane ne nakłada żadnyh ogranzeń na system, zyl nasze zmenne mogą być zależne od zasu. Po sałkowanu formy różnzkowej otrzymujemy ozywśe ałkową postać równana Gbbsa: Różnzkują postać ałkową dostajemy: U TS pv N (13.22) du Tds SdT pdv Vdp dn N d Odejmjmy teraz od równana (13.23) równane (13.21): (13.23) (13.24) 0 du du Tds SdT pdv Vdp dn Nd TdS pdv dn zyl: 0 SdT Vdp Nd (13.25) Powyższe równane to ogólna postać równana Gbbsa-Duhema. Zakładają teraz że nasz proes przebega w warunkah zotermznyh zohoryznyh (takh jake przeważne rozważamy w proesah dyfuzyjnyh), zyl gdy dt oraz dp =0, możemy zapsać:
4 Nd 0 (13.26) skąd już łatwo można przejść poprzez dzelene stronam do posta używanej przez nas na zajęah: Reguła faz Gbbsa Układ jednoskładnkowy, p-fazowy n 0 (13.27) Rozważmy na pozątek jednoskładnkowy układ welofazowy. Przez fazę będzemy rozumeć obszar układu który jest hemzne fzyzne jednorodny, oraz wyraźne oddzelony od reszty układu otozena. Różne fazy, o le tylko spełnone są odpowedne warunk, mogą współstneć ze sobą w układze. Przykładem może być układ woda-lód w temperaturze 0 C przy śnenu 1 atm. Aby układ był w równowadze termodynamznej, (tzw. równowadze fazowej w tym przypadku), konezny jest brak sły napędowej w układze, która podobne jak do tej pory może zostać wyrażona poprzez gradent potenjału hemznego. Będze to mało mejse, gdy potenjały hemzne we wszystkh fazah będą jednakowe: (1) (2) (2) (3) ( p1) ( p) ; ;...; (13.28) Gdyby warunek ten ne był spełnony, ząstk z faz o wyższym potenjale przehodzłyby do tyh o nższym. W każdej z faz w warunkah równowag termodynamznej, mus być spełnone równane Gbbsa- Duhema (13.25): (1) (1) SdT Vdp N d... ( p) ( p) SdT Vdp N d 0 0 (13.29) Wdzmy, że stan równowag opsuje nam zatem zestaw 2p-1 równań: p-1 równań typu (13.28) p równań typu (13.29). Równoześne wdzmy, że układ opsany jest poprzez p+2 parametrów: (1) ( ),..., p, pt,. Możemy teraz wyznazyć lzbę stopn swobody, zyl lzbę nezależnyh parametrów ntensywnyh przy danej lzbe faz: f p 2 (2 p 1) 3 p (13.30) Wdzmy zatem, że gdy mamy układ jednofazowy (p=1), lzba stopn swobody wynos 2, a zatem zarówno temperatura jak śnene może ulegać zmane. W przypadku układu dwufazowego (p=2), zmane może ulegać tylko jedno z nh. Dla układu trójfazowego (p=3), jednoskładnkowego, lzba stopn swobody wynos zero, a zatem mamy do zynena z tzw. punktem potrójnym, występująym przy danej wartoś śnena temperatury.
5 Układ C-składnkowy, p-fazowy W przypadku układów C-składnkowyh p-fazowyh, mówmy już razej o równowadze hemznej. Odstępstwo od nej może oznazać wystąpene reakj hemznyh, którym mogą towarzyszyć przemany fazowe. Równowaga przedstawona w (13.28) mus w tym przypadku ule rozszerzenu na wszystke składnk: ; ;...; (1) (2) (2) (3) ( p1) ( p) ; ;...;... (1) (2) (2) (3) ( p1) ( p) C C C C C C (13.31) Zestaw relaj Gbbsa-Duhema równeż ulegne zmane: SdT Vdp N d 0... (1) (1) SdT Vdp N d 0 ( p) ( p) (13.32) Wdzmy zatem, że łązna lość równań opsująyh stan równowag wynos w tym przypadku C (p- 1)+p dla odpowedno równań (13.31) (13.32), natomast lzba parametrów ntensywnyh wynos C p+2. W tej sytuaj, lzba stopn swobody może zostać wyrażona jako: f C p 2 C p 1 p C p 2 (13.33) Jeśl rozważamy fazy skondensowane (eze ała stałe), to musmy pamętać, ż śnene praktyzne ne będze wpływało na warunk równowag (możemy przyjąć p=0), w zwązku z zym możemy lzbę nezależnyh parametrów zmnejszyć o jeden. Otrzymujemy wtedy regułę faz Gbbsa dla faz skondensowanyh: f C p 1 (13.34) Podobne jak mało to mejse dla układu jednoskładnkowego, dla układu C-składnkowego równeż możemy dokonać pewnego podzału w zależnoś od lzby stopn swobody: równowaga zerozmenna (punkty zerozmenne) - dla f=0. W tej sytuaj zmana dowolnego parametru powoduje znknęe jednej z faz. równowaga jednozmenna (lne równowag jednozmennej) - zmana któregokolwek z parametrów wymusza jednoznazne określoną zmanę nnego parametru, jeśl lzba faz ma ne ule zmane. obszary równowag dwu- welozmennej - odpowedne parametry mogą ulegać zmane w określonyh zakresah stnena takh obszarów.
6 13.4. Równowaga faz w układah dwuskładnkowyh Ops stanu w takh układah wymaga zdefnowana trzeh parametrów: temperatury, śnena stężena jednego ze składnków, przy zym dla faz skondensowanyh, na któryh będzemy sę teraz konentrować, śnene traktujemy jako wartość stałą. Zgodne z równanem (13.34) dla dwuskładnkowego układu przy założenu występowana tylko faz skondensowanyh, maksymalna lzba faz będąyh w równowadze zerozmennej wynos 3, przy zym najzęśej są to dwe fazy stałe jedna ekła. Grafzna reprezentaja równowag w układze dwuskładnkowym przedstawana jest na dagrame skład-temperatura. Pozątek kone os składu odpowadają zystym składnkom. W tego typu układah mogą być stablne fazy: zystyh składnków zwązków stehometryznyh mędzy składnkam roztworów mędzy składnkam zwązkam hemznym Rozważmy teraz przykładowy układ dwuskładnkowy, w którym mamy dwe substanje tworząe roztwory stałe w ogranzonym zakrese składów: Rys Układ dwuskładnkowy z ogranzoną meszalnośą. W układze tym możemy rozróżnć klka obszarów: pole stablnoś fazy ekłej L pola jednofazowe stablnyh roztworów stałyh α, β dwufazowe pola równowag fazy ekłej stałej L+α, L+β dwufazowe pole meszanny roztworów stałyh α+β Na podstawe dagramu możemy określć składy oraz udzały poszzególnyh faz. W tym elu będzemy stosować znaną z hem fzyznej regułę dźwgn. Rozważmy dwe sytuaje przedstawone na ponższym dagrame:
7 Rys Zastosowane reguły dźwgn Załóżmy na pozątek, że jesteśmy w temperaturze T b nteresuje nas skład fazowy, wedzą że średn skład hemzny wynos b (odpowada rzutow punktu b na oś składu). W elu określane składu fazowego hemznego, musmy poprowadzć z punktu b tzw. konodę, zyl odnek zotermy łąząy składy faz pozostająyh w równowadze. Zgodne z tym o wdać na dagrame, w równowadze w tej sytuaj pozostaje faza α o składze a oraz faza L o składze. Jest ozywste, że w tej sytuaj mus być spełnona równość: gdze F - udzał danej fazy F F (13.35) L b a L Poneważ możemy zapsać: L F F F F (13.36) L b a L o po dalszym przekształenu prowadz do zależnoś: L F F b a FL b F L b L b a (13.37) a w konsekwenj do wyrażena: L b F FL b a (13.38) Ostatezne otrzymujemy: L L F (1 F ) F L b b b a a (13.39) Analogzne wyprowadzene można przeprowadzć dla F L. W przypadku temperatury T e, dla średnego składu hemznego e wdzmy, że tworzyć sę będą dwe fazy: faza α o składze d oraz faza β o składze f. Ih udzały to odpowedno:
8 oraz F f f d F e e d f d (13.40) (13.41) Zastosowana dagramów fazowyh ne ogranzają sę tylko do przewdywana składu hemznego fazowego w danej temperaturze. Opróz tego umożlwają nam równeż wyznazene krzywej hłodzena stopu o danym składze, o pozwala do pewnego stopna na przewdzene końowej struktury stopu w temperaturze pokojowej. Wróćmy do naszego dagramu rozważmy proes hłodzena stopów od stanu ekłego do temperatury pokojowej. Rys Krzywe hłodzena stopów. Weźmy na pozątek stop I. Gdy zazynamy go hłodzć, w punke 1 trafamy na lnę lkwdusu. Od tego momentu ze stopu zazyna ją krystalzować kryształy α o składze zmenająym sę wzdłuż ln soldusu końząej sę w punke 2. W momene gdy dohodzmy do punktu 2, zanka nam faza ekła aż do punktu 3 krystalzuje sę nam tylko faza α. W punke 3 whodzmy w obszar 2-fazowy - opróz fazy α zazyna sę nam wtórna krystalzaja fazy β, której dokładny skład oraz udzał możemy już wyznazyć z reguły dźwgn. Podobną analzę możemy przeprowadzć dla stopu II. W jego przypadku od punktu 4 zazyna sę krystalzaja fazy α która trwa aż do momentu, gdy dojdzemy do punktu 5. W punke 5 zazyna sę nam wydzelene kryształów eutektyk, zyl meszanny α+β o określonyh proporjah. Udzał eutektyk wynos przy tej temperaturze (5-a)/(e-a), podzas gdy udzał fazy α wynos (e-5)/(e-a). Skład fazowy eutektyk wyznazamy jako F α =(b-e)/(b-a) oraz F β =(e-a)/(b-a). Od punktu 5 w dół, mamy do zynena z krystalzają fazy α połązonej z krystalzają eutektyk. Zatrzymajmy sę tutaj na moment w elu wyjaśnena pewnyh kwest zwązanyh z krystalzają wtórną. W przypadku układów z ogranzoną rozpuszzalnośą, opróz ln soldusu lkwdusu, pojawa sę nam dodatkowa lna, tzw. solvus (zaznazony na zelono na Rys. 13.4). Lna to określa nam lmt rozpuszzalnoś jednego składnka w drugm dla danyh temperatur. Wróćmy teraz do naszego stopu I. Wdzmy, że w punke nr. 3 podzas hłodzena będzemy przenać lnę solvusa. Oznaza to, że nasze kryształy α ponżej tej ln traą stablność - jest w nh za dużo β w tyh
9 temperaturah. Na skutek tego, kryształy β zazną sę nam wydzelać z perwotnyh kryształów α, dają tzw. wtórne kryształy β" (wtórne, bo wydzelają sę z nnego kryształu a ne z krystalzują ezy). Analogzna sytuaja będze zahodzła na drugm końu naszego układu pod solvusem zwązanym z fazą β, z tym że wydzelaną fazą będze α". Kwesta krystalzaj wtórnej jest dość złożona, jak popatrzymy na nasz dagram fazowy to łatwo możemy zauważyć, że zjawsko to pownnśmy także rozważać w obszarah typu α+(α+β) e oraz β+(α+β) e, gdze wydzelająe sę kryształy perwotne odpowedno α β równeż będą sę rozpadać ze spadkem temperatury...jednak ne będzemy aż tak bardzo sę nad tym zastanawać. Generalne obowązująy ops dagramu fazowego o ogranzonej rozpuszzalnoś przedstawony jest ponżej: Rys Dagram fazowy opsany z punktu wdzena mkrostruktury. Fazy perwotne będzemy rozpsywać w obszarah pod solvusem, w obszarah pod lną eutektyk mamy do zynena z meszanną zystyh faz eutektyk (proszę pamętać - eutektyka ne jest fazą). W przedstawonym układze melśmy do zynena z przemaną eutektyzną - faza ekła krystalzowała z wydzelenem sę dwóh faz stałyh. Ozywśe ne jest to jedyna możlwość. W ponższej tabel przedstawony możlwe typy równowag zerozmennyh:
10 Tab Typy równowag zerozmennyh [1]. Istneje szereg różnyh typów dagramów dwuskładnkowyh np. dagramy dwuskładnkowe z pełną rozpuszzalnośą, ze zwązkam hemznym, dagramy eutektyzne, perytektyzne td. Nektórym z nh zajmemy sę na zajęah. Bblografa [1] K. Tkaz-Śmeh, Termodynamka dla Ceramków, Akadema Górnzo-Hutnza 2013, s.280
Wyznaczenie współczynnika podziału kwasu octowego pomiędzy fazą organiczną a wodną
 Ćwzene 13 Wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną a wodną Cel ćwzena Celem ćwzena jest wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną (butanolem) a wodną w oparu
Ćwzene 13 Wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną a wodną Cel ćwzena Celem ćwzena jest wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną (butanolem) a wodną w oparu
TERMODYNAMIKA TECHNICZNA I CHEMICZNA
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene de G n na odstawe tego, że otenjał termodynamzny
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene de G n na odstawe tego, że otenjał termodynamzny
FUGATYWNOŚCI I AKTYWNOŚCI
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część VI TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene G n de,t, n j G na odstawe tego, że otenjał
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część VI TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene G n de,t, n j G na odstawe tego, że otenjał
Podstawy termodynamiki
 Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
Parametry stanu w przemianie izobarycznej zmieniają się według zależności
 Przyad szzegóne rzemany otroowej /6 5.4. Przemana zobaryzna Przemana rzy stałym śnen, zy zobaryzna jest rzemaną otroową o wyładn m = 0, gdyż m = 0 == onst. Przemana ta zahodz, gdy ogrzewa sę gaz zamnęty
Przyad szzegóne rzemany otroowej /6 5.4. Przemana zobaryzna Przemana rzy stałym śnen, zy zobaryzna jest rzemaną otroową o wyładn m = 0, gdyż m = 0 == onst. Przemana ta zahodz, gdy ogrzewa sę gaz zamnęty
Kwantowa natura promieniowania elektromagnetycznego
 Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
Wykład Turbina parowa kondensacyjna
 Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
I. Elementy analizy matematycznej
 WSTAWKA MATEMATYCZNA I. Elementy analzy matematycznej Pochodna funkcj f(x) Pochodna funkcj podaje nam prędkość zman funkcj: df f (x + x) f (x) f '(x) = = lm x 0 (1) dx x Pochodna funkcj podaje nam zarazem
WSTAWKA MATEMATYCZNA I. Elementy analzy matematycznej Pochodna funkcj f(x) Pochodna funkcj podaje nam prędkość zman funkcj: df f (x + x) f (x) f '(x) = = lm x 0 (1) dx x Pochodna funkcj podaje nam zarazem
Sieć kątowa metoda spostrzeżeń pośredniczących. Układ równań obserwacyjnych
 Seć kątowa etoda spostrzeżeń pośrednząyh Układ równań obserwayjnyh rzyrosty współrzędnyh X = X X X X = X X Y = Y Y X Y = Y Y Długość odnka X ' ' ' ' x y Współzynnk kerunkowe x y * B * x y x y gdze - odpowedn
Seć kątowa etoda spostrzeżeń pośrednząyh Układ równań obserwayjnyh rzyrosty współrzędnyh X = X X X X = X X Y = Y Y X Y = Y Y Długość odnka X ' ' ' ' x y Współzynnk kerunkowe x y * B * x y x y gdze - odpowedn
α i = n i /n β i = V i /V α i = β i γ i = m i /m
 Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
WYKŁAD 8. Równowagi w układach jedno- i dwuskładnikowych
 WYKŁD 8. Równowag w układah jedno- dwuskładnkowyh Równowaga faz równane Claususa-Claeyrona Rozatrzmy ykl Carnota na ozomyh odnkah zoterm CD, odowadająyh równowadze ez-ara ewnej substanj. T kr Na odnku
WYKŁD 8. Równowag w układah jedno- dwuskładnkowyh Równowaga faz równane Claususa-Claeyrona Rozatrzmy ykl Carnota na ozomyh odnkah zoterm CD, odowadająyh równowadze ez-ara ewnej substanj. T kr Na odnku
RUCH OBROTOWY Można opisać ruch obrotowy ze stałym przyspieszeniem ε poprzez analogię do ruchu postępowego jednostajnie zmiennego.
 RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
V. TERMODYNAMIKA KLASYCZNA
 46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
Wykład Mikroskopowa interpretacja ciepła i pracy Entropia
 Wykład 7 5.13 Mkroskopowa nterpretacja cepła pracy. 5.14 Entropa 5.15 Funkcja rozdzału 6 II zasada termodynamk 6.1 Sformułowane Claususa oraz Kelvna-Plancka II zasady termodynamk 6.2 Procesy odwracalne
Wykład 7 5.13 Mkroskopowa nterpretacja cepła pracy. 5.14 Entropa 5.15 Funkcja rozdzału 6 II zasada termodynamk 6.1 Sformułowane Claususa oraz Kelvna-Plancka II zasady termodynamk 6.2 Procesy odwracalne
TERMODYNAMIKA II.A PROJEKT [WŁASNOŚCI PŁYNÓW ZŁOŻOWYCH - PODSTAWY] SPIS TREŚ CI. andrzej.magdziarz@agh.edu.pl. http://home.agh.edu.
![TERMODYNAMIKA II.A PROJEKT [WŁASNOŚCI PŁYNÓW ZŁOŻOWYCH - PODSTAWY] SPIS TREŚ CI. andrzej.magdziarz@agh.edu.pl. http://home.agh.edu. TERMODYNAMIKA II.A PROJEKT [WŁASNOŚCI PŁYNÓW ZŁOŻOWYCH - PODSTAWY] SPIS TREŚ CI. andrzej.magdziarz@agh.edu.pl. http://home.agh.edu.](/thumbs/27/11937916.jpg) TERMODYNAMIKA II.A PROJEKT [WŁASNOŚI PŁYNÓW ZŁOŻOWYH - PODSTAWY] andrzej.magdzarz@agh.edu.l htt://home.agh.edu.l/magdz erson 0.10 (005/09/0) SPIS TREŚ I 1. DWUFAZOWY UKŁAD GAZ-IEZ... 1.1. ILOŚĆ SUBSTANJI,
TERMODYNAMIKA II.A PROJEKT [WŁASNOŚI PŁYNÓW ZŁOŻOWYH - PODSTAWY] andrzej.magdzarz@agh.edu.l htt://home.agh.edu.l/magdz erson 0.10 (005/09/0) SPIS TREŚ I 1. DWUFAZOWY UKŁAD GAZ-IEZ... 1.1. ILOŚĆ SUBSTANJI,
WYSYCHANIE ZABYTKOWYCH MURÓW Z CEGŁY *
 ROCZNIKI INŻYNIERII BUDOWLANEJ ZESZYT 7/007 Komsja Inżyner Budowlanej Oddzał Polskej Akadem Nauk w Katowah WYSYCHANIE ZABYTKOWYCH MURÓW Z CEGŁY * Andrzej KUCHARCZYK Poltehnka Opolska, Opole. Wprowadzene
ROCZNIKI INŻYNIERII BUDOWLANEJ ZESZYT 7/007 Komsja Inżyner Budowlanej Oddzał Polskej Akadem Nauk w Katowah WYSYCHANIE ZABYTKOWYCH MURÓW Z CEGŁY * Andrzej KUCHARCZYK Poltehnka Opolska, Opole. Wprowadzene
ELEKTROCHEMIA. ( i = i ) Wykład II b. Nadnapięcie Równanie Buttlera-Volmera Równania Tafela. Wykład II. Równowaga dynamiczna i prąd wymiany
 Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Stanisław Cichocki Natalia Nehrebecka. Zajęcia 4
 Stansław Cchock Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0-1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających Interpretacja
Stansław Cchock Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0-1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających Interpretacja
Współczynniki aktywności w roztworach elektrolitów. W.a. w roztworach elektrolitów (2) W.a. w roztworach elektrolitów (3) 1 r. Przypomnienie!
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Wykład 8. Silnik Stirlinga (R. Stirling, 1816)
 Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowag fazowe Zakład Chem Medycznej Pomorsk Unwersytet Medyczny Równowaga termodynamczna Przemanom fazowym towarzyszą procesy, podczas których ne zmena sę skład chemczny układu, polegają one na zmane
Równowag fazowe Zakład Chem Medycznej Pomorsk Unwersytet Medyczny Równowaga termodynamczna Przemanom fazowym towarzyszą procesy, podczas których ne zmena sę skład chemczny układu, polegają one na zmane
Modele wzrostu kryształów stałych
 Materały do wykładu Modele wzrostu kryształów stałych Marek Izdebsk Instytut Fzyk PŁ 2016 Sps treśc Temat 1. Termodynamczne podstawy równowag fazowej krystalzacj....1 1.1. Równowaga quas-równowaga...1
Materały do wykładu Modele wzrostu kryształów stałych Marek Izdebsk Instytut Fzyk PŁ 2016 Sps treśc Temat 1. Termodynamczne podstawy równowag fazowej krystalzacj....1 1.1. Równowaga quas-równowaga...1
Natalia Nehrebecka. Zajęcia 4
 St ł Cchock Stansław C h k Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0 1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających
St ł Cchock Stansław C h k Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0 1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
Zmiana entropii w przemianach odwracalnych
 Wykład 4 Zmana entrop w przemanach odwracalnych: przemany obegu Carnota, spręŝane gazu półdoskonałego ze schładzanem, zobaryczne wytwarzane przegrzewane pary techncznej rzemany zentropowe gazu doskonałego
Wykład 4 Zmana entrop w przemanach odwracalnych: przemany obegu Carnota, spręŝane gazu półdoskonałego ze schładzanem, zobaryczne wytwarzane przegrzewane pary techncznej rzemany zentropowe gazu doskonałego
XXX OLIMPIADA FIZYCZNA ETAP III Zadanie doświadczalne
 XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
Stanisław Cichocki. Natalia Nehrebecka. Wykład 6
 Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Zastosowane modelu potęgowego Przekształcene Boxa-Coxa 2. Zmenne cągłe za zmenne dyskretne 3. Interpretacja parametrów przy zmennych dyskretnych 1. Zastosowane
Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Zastosowane modelu potęgowego Przekształcene Boxa-Coxa 2. Zmenne cągłe za zmenne dyskretne 3. Interpretacja parametrów przy zmennych dyskretnych 1. Zastosowane
Część III: Termodynamika układów biologicznych
 Część III: Termodynamka układów bologcznych MATERIAŁY POMOCNICZE DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Botechnolog prof. dr hab. nż. Jan Mazersk TERMODYNAMIKA UKŁADÓW BIOLOGICZNYCH Nezwykle cenną metodą
Część III: Termodynamka układów bologcznych MATERIAŁY POMOCNICZE DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Botechnolog prof. dr hab. nż. Jan Mazersk TERMODYNAMIKA UKŁADÓW BIOLOGICZNYCH Nezwykle cenną metodą
Zestaw zadań 4: Przestrzenie wektorowe i podprzestrzenie. Liniowa niezależność. Sumy i sumy proste podprzestrzeni.
 Zestaw zadań : Przestrzene wektorowe podprzestrzene. Lnowa nezależność. Sumy sumy proste podprzestrzen. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar :
Zestaw zadań : Przestrzene wektorowe podprzestrzene. Lnowa nezależność. Sumy sumy proste podprzestrzen. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar :
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Stanisław Cichocki. Natalia Nehrebecka. Wykład 7
 Stansław Cchock Natala Nehrebecka Wykład 7 1 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy zmennych dyskretnych 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy
Stansław Cchock Natala Nehrebecka Wykład 7 1 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy zmennych dyskretnych 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy
Przykład 5.1. Kratownica dwukrotnie statycznie niewyznaczalna
 rzykład.. Kratownca dwukrotne statyczne newyznaczana oecene: korzystaąc z metody sł wyznaczyć sły w prętach ponższe kratowncy. const Rozwązane zadana rozpoczynamy od obczena stopna statyczne newyznaczanośc
rzykład.. Kratownca dwukrotne statyczne newyznaczana oecene: korzystaąc z metody sł wyznaczyć sły w prętach ponższe kratowncy. const Rozwązane zadana rozpoczynamy od obczena stopna statyczne newyznaczanośc
Fizyka, technologia oraz modelowanie wzrostu kryształów
 Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Wykład Mikro- i makrostany oraz prawdopodobie
 Wykład 6 5.5 Mkro- makrostany oraz prawdopodobeństwo termodynamczne cd. 5.6 Modele fzyczne 5.7 Aproksymacja Strlna 5.8 Statystyka Boseo-Enstena 5.10 Statystyka Fermeo-Draca 5.10 Statystyka Maxwell a-boltzmann
Wykład 6 5.5 Mkro- makrostany oraz prawdopodobeństwo termodynamczne cd. 5.6 Modele fzyczne 5.7 Aproksymacja Strlna 5.8 Statystyka Boseo-Enstena 5.10 Statystyka Fermeo-Draca 5.10 Statystyka Maxwell a-boltzmann
TERMODYNAMIKA TECHNICZNA I CHEMICZNA
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
Wykłady z termodynamiki i fizyki statystycznej. Semestr letni 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a
 Wykłady z termodynamk fzyk statystycznej. Semestr letn 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a gudowska@th.f.uj.edu.pl Zalecane podręcznk: 1.Termodynamka R. Hołyst, A. Ponewersk, A. Cach 2. Podstay
Wykłady z termodynamk fzyk statystycznej. Semestr letn 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a gudowska@th.f.uj.edu.pl Zalecane podręcznk: 1.Termodynamka R. Hołyst, A. Ponewersk, A. Cach 2. Podstay
[, ] [, ] [, ] ~ [23, 2;163,3] 19,023 2,7
![[, ] [, ] [, ] ~ [23, 2;163,3] 19,023 2,7 [, ] [, ] [, ] ~ [23, 2;163,3] 19,023 2,7](/thumbs/66/55630048.jpg) 6. Przez 0 losowo wybrayh d merzoo zas dojazdu do pray paa A uzyskują próbkę x,..., x 0. Wyk przedstawały sę astępująo: jest to próbka losowa z rozkładu 0 0 x 300, 944. x Zakładamy, że N ( µ, z ezaym parametram
6. Przez 0 losowo wybrayh d merzoo zas dojazdu do pray paa A uzyskują próbkę x,..., x 0. Wyk przedstawały sę astępująo: jest to próbka losowa z rozkładu 0 0 x 300, 944. x Zakładamy, że N ( µ, z ezaym parametram
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadanie teoretyczne
 XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
KINEMATYKA MANIPULATORÓW
 KIEMK MIULOÓW WOWDEIE. Manpulator obot można podzelć na zęść terująą mehanzną. Część mehanzna nazywana jet manpulatorem. punktu wdzena Mehank ta zęść jet najbardzej ntereująa. Manpulator zaadnzo można
KIEMK MIULOÓW WOWDEIE. Manpulator obot można podzelć na zęść terująą mehanzną. Część mehanzna nazywana jet manpulatorem. punktu wdzena Mehank ta zęść jet najbardzej ntereująa. Manpulator zaadnzo można
3. ŁUK ELEKTRYCZNY PRĄDU STAŁEGO I PRZEMIENNEGO
 3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 1. Układy równań liniowych
 Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny
 Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Modele wieloczynnikowe. Modele wieloczynnikowe. Modele wieloczynnikowe ogólne. α β β β ε. Analiza i Zarządzanie Portfelem cz. 4.
 Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
Diagnostyka układów kombinacyjnych
 Dagnostyka układów kombnacyjnych 1. Wprowadzene Dagnostyka obejmuje: stwerdzene stanu układu, systemu lub ogólne sec logcznej. Jest to tzw. kontrola stanu wykrywająca czy dzałane sec ne jest zakłócane
Dagnostyka układów kombnacyjnych 1. Wprowadzene Dagnostyka obejmuje: stwerdzene stanu układu, systemu lub ogólne sec logcznej. Jest to tzw. kontrola stanu wykrywająca czy dzałane sec ne jest zakłócane
SPEKTROSKOPIA MOLEKULARNA
 SPEKTROSKOPIA MOLEKULARNA Ćwzene 1 Badane wązana wodorowego za pomoą spektroskop absorpyjnej w podzerwen. A. BADANIE AUTOASOCJACJI ALKOHOLU OKTYLOWEGO ODCZYNNIKI Substanja badana: oktanol (d=0.83 g/m 3
SPEKTROSKOPIA MOLEKULARNA Ćwzene 1 Badane wązana wodorowego za pomoą spektroskop absorpyjnej w podzerwen. A. BADANIE AUTOASOCJACJI ALKOHOLU OKTYLOWEGO ODCZYNNIKI Substanja badana: oktanol (d=0.83 g/m 3
ZASADY WYZNACZANIA DEPOZYTÓW ZABEZPIECZAJĄCYCH PO WPROWADZENIU DO OBROTU OPCJI W RELACJI KLIENT-BIURO MAKLERSKIE
 Zasady wyznazana depozytów zabezpezaąyh po wprowadzenu do obrotu op w rela lent-buro malerse ZAADY WYZNACZANIA DEPOZYTÓW ZABEZPIECZAJĄCYCH PO WPROWADZENIU DO OBROTU OPCJI W RELACJI KLIENT-BIURO MAKLERKIE
Zasady wyznazana depozytów zabezpezaąyh po wprowadzenu do obrotu op w rela lent-buro malerse ZAADY WYZNACZANIA DEPOZYTÓW ZABEZPIECZAJĄCYCH PO WPROWADZENIU DO OBROTU OPCJI W RELACJI KLIENT-BIURO MAKLERKIE
Chemia fizyczna. Notatki z wykładów dr hab. Szczepana Zapotocznego
 Anna Krzykawska Chema fzyzna Notatk z wykładów dr hab. Szzepana Zapotoznego Zwększene lzby absolwentów nnowayjnyh kerunków studów: Zaawansowane materały nanotehnologa oraz Studa matematyzno-przyrodnze
Anna Krzykawska Chema fzyzna Notatk z wykładów dr hab. Szzepana Zapotoznego Zwększene lzby absolwentów nnowayjnyh kerunków studów: Zaawansowane materały nanotehnologa oraz Studa matematyzno-przyrodnze
Kształtowanie się firm informatycznych jako nowych elementów struktury przestrzennej przemysłu
 PRACE KOMISJI GEOGRAFII PRZEMY SŁU Nr 7 WARSZAWA KRAKÓW 2004 Akadema Pedagogczna, Kraków Kształtowane sę frm nformatycznych jako nowych elementów struktury przestrzennej przemysłu Postępujący proces rozwoju
PRACE KOMISJI GEOGRAFII PRZEMY SŁU Nr 7 WARSZAWA KRAKÓW 2004 Akadema Pedagogczna, Kraków Kształtowane sę frm nformatycznych jako nowych elementów struktury przestrzennej przemysłu Postępujący proces rozwoju
MATERIAŁOZNAWSTWO Wydział Mechaniczny, Mechatronika, sem. I. dr inż. Hanna Smoleńska
 MATERIAŁOZNAWSTWO Wydział Mechaniczny, Mechatronika, sem. I dr inż. Hanna Smoleńska UKŁADY RÓWNOWAGI FAZOWEJ Równowaga termodynamiczna pojęcie stosowane w termodynamice. Oznacza stan, w którym makroskopowe
MATERIAŁOZNAWSTWO Wydział Mechaniczny, Mechatronika, sem. I dr inż. Hanna Smoleńska UKŁADY RÓWNOWAGI FAZOWEJ Równowaga termodynamiczna pojęcie stosowane w termodynamice. Oznacza stan, w którym makroskopowe
termodynamika fenomenologiczna p, VT V, teoria kinetyczno-molekularna <v 2 > termodynamika statystyczna n(v) to jest długi czas, zachodzi
 fzka statstczna stan makroskopow układ - skończon obszar przestrzenn (w szczególnośc zolowan) termodnamka fenomenologczna p, VT V, teora knetczno-molekularna termodnamka statstczna n(v) stan makroskopow
fzka statstczna stan makroskopow układ - skończon obszar przestrzenn (w szczególnośc zolowan) termodnamka fenomenologczna p, VT V, teora knetczno-molekularna termodnamka statstczna n(v) stan makroskopow
Natalia Nehrebecka. Zajęcia 3
 St ł Cchock Stansław C h k Natala Nehrebecka Zajęca 3 1. Dobroć dopasowana równana regresj. Współczynnk determnacj R Dk Dekompozycja warancj zmennej zależnej ż Współczynnk determnacj R. Zmenne cągłe a
St ł Cchock Stansław C h k Natala Nehrebecka Zajęca 3 1. Dobroć dopasowana równana regresj. Współczynnk determnacj R Dk Dekompozycja warancj zmennej zależnej ż Współczynnk determnacj R. Zmenne cągłe a
Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE
 Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
KURS STATYSTYKA. Lekcja 6 Regresja i linie regresji ZADANIE DOMOWE. www.etrapez.pl Strona 1
 KURS STATYSTYKA Lekcja 6 Regresja lne regresj ZADANIE DOMOWE www.etrapez.pl Strona 1 Część 1: TEST Zaznacz poprawną odpowedź (tylko jedna jest prawdzwa). Pytane 1 Funkcja regresj I rodzaju cechy Y zależnej
KURS STATYSTYKA Lekcja 6 Regresja lne regresj ZADANIE DOMOWE www.etrapez.pl Strona 1 Część 1: TEST Zaznacz poprawną odpowedź (tylko jedna jest prawdzwa). Pytane 1 Funkcja regresj I rodzaju cechy Y zależnej
2. STOPIEŃ KINEMATYCZNEJ NIEWYZNACZALNOŚCI
 Część. STOPIEŃ KINEMATYCZNEJ NIEWYZNACZALNOŚCI.. STOPIEŃ KINEMATYCZNEJ NIEWYZNACZALNOŚCI W metodze sł w celu przyjęca układu podstawowego należało odrzucć węzy nadlczbowe. O lczbe odrzuconych węzów decydował
Część. STOPIEŃ KINEMATYCZNEJ NIEWYZNACZALNOŚCI.. STOPIEŃ KINEMATYCZNEJ NIEWYZNACZALNOŚCI W metodze sł w celu przyjęca układu podstawowego należało odrzucć węzy nadlczbowe. O lczbe odrzuconych węzów decydował
5. Pochodna funkcji. lim. x c x c. (x c) = lim. g(c + h) g(c) = lim
 5. Pocodna funkcj Defncja 5.1 Nec f: (a, b) R nec c (a, b). Jeśl stneje granca lm x c x c to nazywamy ją pocodną funkcj f w punkce c oznaczamy symbolem f (c) Twerdzene 5.1 Jeśl funkcja f: (a, b) R ma pocodną
5. Pocodna funkcj Defncja 5.1 Nec f: (a, b) R nec c (a, b). Jeśl stneje granca lm x c x c to nazywamy ją pocodną funkcj f w punkce c oznaczamy symbolem f (c) Twerdzene 5.1 Jeśl funkcja f: (a, b) R ma pocodną
Model ASAD. ceny i płace mogą ulegać zmianom (w odróżnieniu od poprzednio omawianych modeli)
 Model odstawowe założena modelu: ceny płace mogą ulegać zmanom (w odróżnenu od poprzedno omawanych model) punktem odnesena analzy jest obserwacja pozomu produkcj cen (a ne stopy procentowej jak w modelu
Model odstawowe założena modelu: ceny płace mogą ulegać zmanom (w odróżnenu od poprzedno omawanych model) punktem odnesena analzy jest obserwacja pozomu produkcj cen (a ne stopy procentowej jak w modelu
MECHANIKA 2 MOMENT BEZWŁADNOŚCI. Wykład Nr 10. Prowadzący: dr Krzysztof Polko
 MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
= σ σ. 5. CML Capital Market Line, Rynkowa Linia Kapitału
 5 CML Catal Market Lne, ynkowa Lna Katału Zbór ortolo o nalny odchylenu standardowy zbór eektywny ozważy ortolo złożone ze wszystkch aktywów stnejących na rynku Załóży, że jest ch N A * P H P Q P 3 * B
5 CML Catal Market Lne, ynkowa Lna Katału Zbór ortolo o nalny odchylenu standardowy zbór eektywny ozważy ortolo złożone ze wszystkch aktywów stnejących na rynku Załóży, że jest ch N A * P H P Q P 3 * B
powierzchnia rozdziału - dwie fazy ciekłe - jedna faza gazowa - dwa składniki
 Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
BADANIA OPERACYJNE. Podejmowanie decyzji w warunkach niepewności. dr Adam Sojda
 BADANIA OPERACYJNE Podejmowane decyzj w warunkach nepewnośc dr Adam Sojda Teora podejmowana decyzj gry z naturą Wynk dzałana zależy ne tylko od tego, jaką podejmujemy decyzję, ale równeż od tego, jak wystąp
BADANIA OPERACYJNE Podejmowane decyzj w warunkach nepewnośc dr Adam Sojda Teora podejmowana decyzj gry z naturą Wynk dzałana zależy ne tylko od tego, jaką podejmujemy decyzję, ale równeż od tego, jak wystąp
Wykład 3. Entropia i potencjały termodynamiczne
 Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Stanisław Cichocki. Natalia Nehrebecka. Wykład 6
 Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Interpretacja parametrów przy zmennych objaśnających cągłych Semelastyczność 2. Zastosowane modelu potęgowego Model potęgowy 3. Zmenne cągłe za zmenne dyskretne
Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Interpretacja parametrów przy zmennych objaśnających cągłych Semelastyczność 2. Zastosowane modelu potęgowego Model potęgowy 3. Zmenne cągłe za zmenne dyskretne
7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH
 WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
Rozwiązywanie zadań optymalizacji w środowisku programu MATLAB
 Rozwązywane zadań optymalzacj w środowsku programu MATLAB Zagadnene optymalzacj polega na znajdowanu najlepszego, względem ustalonego kryterum, rozwązana należącego do zboru rozwązań dopuszczalnych. Standardowe
Rozwązywane zadań optymalzacj w środowsku programu MATLAB Zagadnene optymalzacj polega na znajdowanu najlepszego, względem ustalonego kryterum, rozwązana należącego do zboru rozwązań dopuszczalnych. Standardowe
ZASADA ZACHOWANIA MOMENTU PĘDU: PODSTAWY DYNAMIKI BRYŁY SZTYWNEJ
 ZASADA ZACHOWANIA MOMENTU PĘDU: PODSTAWY DYNAMIKI BYŁY SZTYWNEJ 1. Welkośc w uchu obotowym. Moment pędu moment sły 3. Zasada zachowana momentu pędu 4. uch obotowy były sztywnej względem ustalonej os -II
ZASADA ZACHOWANIA MOMENTU PĘDU: PODSTAWY DYNAMIKI BYŁY SZTYWNEJ 1. Welkośc w uchu obotowym. Moment pędu moment sły 3. Zasada zachowana momentu pędu 4. uch obotowy były sztywnej względem ustalonej os -II
Analiza danych. Analiza danych wielowymiarowych. Regresja liniowa. Dyskryminacja liniowa. PARA ZMIENNYCH LOSOWYCH
 Analza danych Analza danych welowymarowych. Regresja lnowa. Dyskrymnacja lnowa. Jakub Wróblewsk jakubw@pjwstk.edu.pl http://zajeca.jakubw.pl/ PARA ZMIENNYCH LOSOWYCH Parę zmennych losowych X, Y możemy
Analza danych Analza danych welowymarowych. Regresja lnowa. Dyskrymnacja lnowa. Jakub Wróblewsk jakubw@pjwstk.edu.pl http://zajeca.jakubw.pl/ PARA ZMIENNYCH LOSOWYCH Parę zmennych losowych X, Y możemy
Zaawansowane metody numeryczne
 Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Inżynieria materiałowa: wykorzystywanie praw termodynamiki a czasem... walka z termodynamiką
 Inżynieria materiałowa: wykorzystywanie praw termodynamiki a czasem... walka z termodynamiką Kilka definicji Faza Stan materii jednorodny wewnętrznie, nie tylko pod względem składu chemicznego, ale również
Inżynieria materiałowa: wykorzystywanie praw termodynamiki a czasem... walka z termodynamiką Kilka definicji Faza Stan materii jednorodny wewnętrznie, nie tylko pod względem składu chemicznego, ale również
Termodynamiczne modelowanie procesów spalania, wybuchu i detonacji nieidealnych układów wysokoenergetycznych
 BIULETYN WAT VOL. LIX, NR 3, 2010 Termodynamczne modelowane procesów spalana, wybuchu detonacj nedealnych układów wysokoenergetycznych SEBASTIAN GRYS, WALDEMAR A. TRZCIŃSKI Wojskowa Akadema Technczna,
BIULETYN WAT VOL. LIX, NR 3, 2010 Termodynamczne modelowane procesów spalana, wybuchu detonacj nedealnych układów wysokoenergetycznych SEBASTIAN GRYS, WALDEMAR A. TRZCIŃSKI Wojskowa Akadema Technczna,
Definicja szybkości reakcji
 Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
KRZYWA BÉZIERA TWORZENIE I WIZUALIZACJA KRZYWYCH PARAMETRYCZNYCH NA PRZYKŁADZIE KRZYWEJ BÉZIERA
 KRZYWA BÉZIERA TWORZENIE I WIZUALIZACJA KRZYWYCH PARAMETRYCZNYCH NA PRZYKŁADZIE KRZYWEJ BÉZIERA Krzysztof Serżęga Wyższa Szkoła Informatyk Zarządzana w Rzeszowe Streszczene Artykuł porusza temat zwązany
KRZYWA BÉZIERA TWORZENIE I WIZUALIZACJA KRZYWYCH PARAMETRYCZNYCH NA PRZYKŁADZIE KRZYWEJ BÉZIERA Krzysztof Serżęga Wyższa Szkoła Informatyk Zarządzana w Rzeszowe Streszczene Artykuł porusza temat zwązany
Termodynamiczny opis przejść fazowych pierwszego rodzaju
 Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ],
![STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ], STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ],](/thumbs/27/11347185.jpg) STATECZNOŚĆ SKARP W przypadku obektu wykonanego z gruntów nespostych zaprojektowane bezpecznego nachylena skarp sprowadza sę do przekształcena wzoru na współczynnk statecznośc do postac: tgφ tgα = n gdze:
STATECZNOŚĆ SKARP W przypadku obektu wykonanego z gruntów nespostych zaprojektowane bezpecznego nachylena skarp sprowadza sę do przekształcena wzoru na współczynnk statecznośc do postac: tgφ tgα = n gdze:
Pokazać, że wyżej zdefiniowana struktura algebraiczna jest przestrzenią wektorową nad ciałem
 Zestaw zadań : Przestrzene wektorowe. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar : C C C, (z, v) z v := z v jest przestrzeną lnową nad całem lczb zespolonych
Zestaw zadań : Przestrzene wektorowe. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar : C C C, (z, v) z v := z v jest przestrzeną lnową nad całem lczb zespolonych
Diagonalizacja macierzy kwadratowej
 Dagonalzacja macerzy kwadratowej Dana jest macerz A nân. Jej wartośc własne wektory własne spełnają równane Ax x dla,..., n Każde z równań własnych osobno można zapsać w postac: a a an x x a a an x x an
Dagonalzacja macerzy kwadratowej Dana jest macerz A nân. Jej wartośc własne wektory własne spełnają równane Ax x dla,..., n Każde z równań własnych osobno można zapsać w postac: a a an x x a a an x x an
OGÓLNE PODSTAWY SPEKTROSKOPII
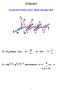 WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
Rachunek prawdopodobieństwa i statystyka W 11: Analizy zależnościpomiędzy zmiennymi losowymi Model regresji wielokrotnej
 Rachunek prawdopodobeństwa statstka W 11: Analz zależnoścpomędz zmennm losowm Model regresj welokrotnej Dr Anna ADRIAN Paw B5, pok 407 adan@agh.edu.pl Model regresj lnowej Model regresj lnowej prostej
Rachunek prawdopodobeństwa statstka W 11: Analz zależnoścpomędz zmennm losowm Model regresj welokrotnej Dr Anna ADRIAN Paw B5, pok 407 adan@agh.edu.pl Model regresj lnowej Model regresj lnowej prostej
Natalia Nehrebecka Stanisław Cichocki. Wykład 10
 Natala Nehrebecka Stansław Cchock Wykład 10 1 1. Testy dagnostyczne 2. Testowane prawdłowośc formy funkcyjnej modelu 3. Testowane normalnośc składnków losowych 4. Testowane stablnośc parametrów 5. Testowane
Natala Nehrebecka Stansław Cchock Wykład 10 1 1. Testy dagnostyczne 2. Testowane prawdłowośc formy funkcyjnej modelu 3. Testowane normalnośc składnków losowych 4. Testowane stablnośc parametrów 5. Testowane
Zasady termodynamiki
 Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Płyny nienewtonowskie i zjawisko tiksotropii
 Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron
 Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
INDUKCJA ELEKTROMAGNETYCZNA. - Prąd powstający w wyniku indukcji elektro-magnetycznej.
 INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
Elementy termodynamiki i wprowadzenie do zespołów statystycznych. Katarzyna Sznajd-Weron
 Elementy termodynamiki i wprowadzenie do zespołów statystycznych Katarzyna Sznajd-Weron Wielkości makroskopowe - termodynamika Termodynamika - metoda fenomenologiczna Fenomenologia w fizyce: widzimy jak
Elementy termodynamiki i wprowadzenie do zespołów statystycznych Katarzyna Sznajd-Weron Wielkości makroskopowe - termodynamika Termodynamika - metoda fenomenologiczna Fenomenologia w fizyce: widzimy jak
Refraktometria. sin β sin β
 efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Wykład 13. Rozkład kanoniczny Boltzmanna Rozkład Maxwella-Boltzmanna III Zasada Termodynamiki. Rozkład Boltzmanna!!!
 Wykład 13 Rozkład kanonczny Boltzmanna Rozkład Maxwella-Boltzmanna III Zasada Termodynamk W. Domnk Wydzał Fzyk UW Termodynamka 2018/2019 1/30 Rozkład Boltzmanna!!! termostat T E n układ P n exp E n Z warunku
Wykład 13 Rozkład kanonczny Boltzmanna Rozkład Maxwella-Boltzmanna III Zasada Termodynamk W. Domnk Wydzał Fzyk UW Termodynamka 2018/2019 1/30 Rozkład Boltzmanna!!! termostat T E n układ P n exp E n Z warunku
EKONOMETRIA I Spotkanie 1, dn. 05.10.2010
 EKONOMETRIA I Spotkane, dn. 5..2 Dr Katarzyna Beń Program ramowy: http://www.sgh.waw.pl/nstytuty/e/oferta_dydaktyczna/ekonometra_stacjonarne_nest acjonarne/ Zadana, dane do zadań, ważne nformacje: http://www.e-sgh.pl/ben/ekonometra
EKONOMETRIA I Spotkane, dn. 5..2 Dr Katarzyna Beń Program ramowy: http://www.sgh.waw.pl/nstytuty/e/oferta_dydaktyczna/ekonometra_stacjonarne_nest acjonarne/ Zadana, dane do zadań, ważne nformacje: http://www.e-sgh.pl/ben/ekonometra
Wykład 10 Teoria kinetyczna i termodynamika
 Wykład 0 Teora knetyczna termodynamka Prawa gazów doskonałych Z dośwadczeń wynka, że przy dostateczne małych gęstoścach, wszystke gazy, nezależne od składu chemcznego wykazują podobne zachowana: w stałej
Wykład 0 Teora knetyczna termodynamka Prawa gazów doskonałych Z dośwadczeń wynka, że przy dostateczne małych gęstoścach, wszystke gazy, nezależne od składu chemcznego wykazują podobne zachowana: w stałej
I PRACOWNIA FIZYCZNA, UMK TORUŃ WYZNACZANIE MOMENTU BEZWŁADNOŚCI BRYŁY SZTYWNEJ ZA POMOCĄ WAHADŁA TORSYJNEGO
 PACOWNA FZYCZNA, UMK TOUŃ nstrukja do ćwzena nr 9 * WYZNACZANE MOMENTU BEZWŁANOŚC BYŁY SZTYWNEJ ZA POMOCĄ WAHAŁA TOSYJNEGO. Cel ćwzena Wyznazene momentu bezwładnoś za pomoą wahadła torsyjnego (metoda dynamzna).
PACOWNA FZYCZNA, UMK TOUŃ nstrukja do ćwzena nr 9 * WYZNACZANE MOMENTU BEZWŁANOŚC BYŁY SZTYWNEJ ZA POMOCĄ WAHAŁA TOSYJNEGO. Cel ćwzena Wyznazene momentu bezwładnoś za pomoą wahadła torsyjnego (metoda dynamzna).
(M2) Dynamika 1. ŚRODEK MASY. T. Środek ciężkości i środek masy
 (MD) MECHANIKA - Dynamka T. Środek cężkośc środek masy (M) Dynamka T: Środek cężkośc środek masy robert.szczotka(at)gmal.com Fzyka astronoma, Lceum 01/014 1 (MD) MECHANIKA - Dynamka T. Środek cężkośc środek
(MD) MECHANIKA - Dynamka T. Środek cężkośc środek masy (M) Dynamka T: Środek cężkośc środek masy robert.szczotka(at)gmal.com Fzyka astronoma, Lceum 01/014 1 (MD) MECHANIKA - Dynamka T. Środek cężkośc środek
Termodynamika Techniczna dla MWT, Rozdział 14. AJ Wojtowicz IF UMK. 5.2. Generacja entropii; transfer ciepła przy skończonej róŝnicy temperatur
 ermodynamka echnczna dla MW, Rozdzał 4. AJ Wojtowcz IF UMK Rozdzał 4. Zmana entrop w przemanach odwracalnych.. rzemany obegu Carnota.. SpręŜane gazu półdoskonałego ze schładzanem.3. Izobaryczne wytwarzane
ermodynamka echnczna dla MW, Rozdzał 4. AJ Wojtowcz IF UMK Rozdzał 4. Zmana entrop w przemanach odwracalnych.. rzemany obegu Carnota.. SpręŜane gazu półdoskonałego ze schładzanem.3. Izobaryczne wytwarzane
Opracowanie metody predykcji czasu życia baterii na obiekcie i oceny jej aktualnego stanu na podstawie analizy bieżących parametrów jej eksploatacji.
 Zakład Systemów Zaslana (Z-5) Opracowane nr 323/Z5 z pracy statutowej pt. Opracowane metody predykcj czasu życa bater na obekce oceny jej aktualnego stanu na podstawe analzy beżących parametrów jej eksploatacj.
Zakład Systemów Zaslana (Z-5) Opracowane nr 323/Z5 z pracy statutowej pt. Opracowane metody predykcj czasu życa bater na obekce oceny jej aktualnego stanu na podstawe analzy beżących parametrów jej eksploatacj.
Regulamin promocji 14 wiosna
 promocja_14_wosna strona 1/5 Regulamn promocj 14 wosna 1. Organzatorem promocj 14 wosna, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa od 01 lutego 2014 do 30
promocja_14_wosna strona 1/5 Regulamn promocj 14 wosna 1. Organzatorem promocj 14 wosna, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa od 01 lutego 2014 do 30
Obraz statyczny układu
 Termodynamika Obraz statyczny układu energia kinetyczna E k = mv 2 / 2 energia wewnetrzna energia powierzchniowa inne energie U inne parametry: T, m, P, V, S... Ep= mgh energia potencjalna STAN I PRZEMIANA
Termodynamika Obraz statyczny układu energia kinetyczna E k = mv 2 / 2 energia wewnetrzna energia powierzchniowa inne energie U inne parametry: T, m, P, V, S... Ep= mgh energia potencjalna STAN I PRZEMIANA
Pracownia Automatyki i Elektrotechniki Katedry Tworzyw Drzewnych Ćwiczenie 3. Analiza obwodów RLC przy wymuszeniach sinusoidalnych w stanie ustalonym
 ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
Model ISLM. Inwestycje - w modelu ISLM przyjmujemy, że inwestycje przyjmują postać funkcji liniowej:
 dr Bartłomej Rokck Ćwczena z Makroekonom I Model ISLM Podstawowe założena modelu: penądz odgrywa ważną rolę przy determnowanu pozomu dochodu zatrudnena nwestycje ne mają charakteru autonomcznego, a ch
dr Bartłomej Rokck Ćwczena z Makroekonom I Model ISLM Podstawowe założena modelu: penądz odgrywa ważną rolę przy determnowanu pozomu dochodu zatrudnena nwestycje ne mają charakteru autonomcznego, a ch
Model IS-LM-BP. Model IS-LM-BP jest wersją modelu ISLM w gospodarce otwartej. Pokazuje on zatem jak
 Ćwczena z Makroekonom II Model IS-LM- Model IS-LM- jest wersją modelu ISLM w gospodarce otwartej. Pokazuje on zatem jak gospodarka taka zachowuje sę w krótkm okrese, w efekce dzałań podejmowanych w ramach
Ćwczena z Makroekonom II Model IS-LM- Model IS-LM- jest wersją modelu ISLM w gospodarce otwartej. Pokazuje on zatem jak gospodarka taka zachowuje sę w krótkm okrese, w efekce dzałań podejmowanych w ramach
Fizyka 1- Mechanika. Wykład 7 16.XI Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów
 zyka - Mechanka Wykład 7 6.XI.07 Zygunt Szeflńsk Środowskowe Laboratoru Cężkch Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Zasada zachowana pędu Układ zolowany Każde cało oże w dowolny sposób oddzaływać
zyka - Mechanka Wykład 7 6.XI.07 Zygunt Szeflńsk Środowskowe Laboratoru Cężkch Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Zasada zachowana pędu Układ zolowany Każde cało oże w dowolny sposób oddzaływać
Statystyka Opisowa 2014 część 2. Katarzyna Lubnauer
 Statystyka Opsowa 2014 część 2 Katarzyna Lubnauer Lteratura: 1. Statystyka w Zarządzanu Admr D. Aczel 2. Statystyka Opsowa od Podstaw Ewa Waslewska 3. Statystyka, Lucjan Kowalsk. 4. Statystyka opsowa,
Statystyka Opsowa 2014 część 2 Katarzyna Lubnauer Lteratura: 1. Statystyka w Zarządzanu Admr D. Aczel 2. Statystyka Opsowa od Podstaw Ewa Waslewska 3. Statystyka, Lucjan Kowalsk. 4. Statystyka opsowa,
