POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
|
|
|
- Krystyna Wróbel
- 6 lat temu
- Przeglądów:
Transkrypt
1 WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt pośredn : + K k' D () (K - stała równowag perwszej reakcj, k' - stała szybkośc drugego etapu) Przy tego typu reakcjach następczych, perwszy etap przebega zwykle szybko, zaś drug etap wolno. Etapem określającym szybkość reakcj jest węc etap drug: v = = k' [] (3) Wyrażene na stałą równowag perwszego etapu posada postać: K = a a a = f f f [] [] [] (4) gdze a jest aktywnoścą: Równana te prowadzą do następującego wyrażena na stałą szybkośc rozpatrywanej reakcj: v k K f f = = ' [ ] [] f (5) Wartość współczynnków aktywnośc, f, oszacować można na podstawe równana Debye'a - Hückel'a: logf = ' z I (6) gdze I jest słą jonową roztworu: 1 I = c z (7) zaś z jest ładunkem -tego jonu. Spełnona mus być równeż zależność: str. 1
2 z = z + z (8) Występujące w równanu (1.4) (1.5) współczynnk aktywnośc opsać można węc wyrażenem: log f f f [ ( ) ] = ' J z + z z + z = ' J z z (9) Równane (5) napsać można węc w postac: v = = k [] (10) gdze: k = = k' K f f f [] (11) Równana (10) (11) słuszne są wtedy, gdy stężene substratu jest dużo wyższe od stężena substratu, a węc stężene jest stałe w czase trwana reakcj. Z równana (1.1) wynka ponao, ż: v = = d [] d[] oraz = k[] (1) co prowadz do zależnośc: log k k' K[] lub naczej = ' z z I (13) logk = X + Y I (14) gdze: X= log k' K [] oraz Y = ' z z (15) Równane (14)) wskazuje ż szybkość reakcj następczej jonowej zależna jest od sły jonowej roztworu (stężena obcego elektroltu). Przykładem reakcj rozważanego typu jest reakcja jonów OH - (reagent ) z foletem krystalcznym (reagent ): str.
3 H 3 H 3 N l - N + H 3 H 3 H 3 N H 3 Rysunek 1. Jedna ze struktur rezonansowych foletu krystalcznego Przebeg reakcj wygodne można śledzć metodą kolorymetryczną, gdyż folet krystalczny posada slne wdmo absorpcyjne, zaś produkt reakcj jest bezbarwny. Równane (1) po scałkowanu przybera postać: ln c c0 = kt gdze c - stężena foletu w czase t, c 0 - stężene początkowe foletu (dla t = 0), t - czas od rozpoczęca reakcj (w sekundach). (16) Równane (1.16) przekształcć można do postac: l n = kt gdyż c 0 (17) gdze oznacza absorbancję roztworu w chwl t, zaś o w chwl początkowej (należy odróżnć symbol absorbancj od symbolu substratu ). EL ĆWIZENI elem ćwczena jest znalezene zależnośc stałej szybkośc reakcj foletu krystalcznego z jonam wodorotlenowym od sły jonowej roztworu. PRTUR SPEOL: z przystawką na 4 kuwety Kuwety szklane - 4 szt., d =1 cm. str. 3
4 SZKŁO Zlewk 100 ml - szt. Kolbk marowe 50 ml - 4szt. Ppety welomarowe 5 ml 10 ml. Tryskawka z wodą destylowaną. ODZYNNIKI Roztwór KNO 3 (lub nnej sol, np.kl) 1 mol dm -3. Roztwór KOH (lub NaOH) 0.1 mol dm -3. Roztwór foletu krystalcznego 10-4 mol dm -3. WYKONNIE ĆWIZENI 1. Zmerzyć wdmo foletu krystalcznego o stężenu 10-5 mol dm -3. Wdmo wykonać w zakrese od nm co 10 nm. Wyznaczyć długość fal dla maksymalnej absorpcj.. Zmerzyć zmanę absorbancj w czase, roztworów zawerających folet krystalczny, NaOH oraz obcą sól o stężenach wyszczególnonych w tabel ponżej Roztwór nr Stężene /mol dm -3 Folet krystalczny NaOH KNO 3 (lub Kl) zas rozpoczęca reakcj przyjąć za równy momentow dodana do roztworów jonów OH -. bsorbancję merzyć co 5 mnut od chwl rozpoczęca reakcj. Pomary zakończyć po 30 mnutach od chwl rozpoczęca reakcj. OPROWNIE WYNIKÓW 1. Wykreślć zależnośc absorbancj od czasu.. Wyznaczyć stałą szybkośc reakcj dla poszczególnych roztworów. 3. Wykreślć zależność ( ) logk f I =. 4. Na podstawe wykresu wyznaczyć wartość lczbową stałej Debye'a-Hückel'a. Porównać z wartoścą lteraturową. str. 4
5 Wzór tabel schematu opracowana.. Wydzał. Kerunek Studa nestacjonarne Nr grupy: Nr zespołu:. Imę Nazwsko studenta.. Nr ćwczena:... Data wykonywana ćwczena:. Nazwsko Prowadzącego: 1. Temat ćwczena:. el ćwczena: 3. Pomary: 4. Oblczena: 5. Wykresy: 6. Wnosk: str. 5
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda-kwas octowychloroform metodą potencjometryczną ćwczene nr 9 Opracowała dr hab. Małgorzata Jóźwak Zakres
Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda-kwas octowychloroform metodą potencjometryczną ćwczene nr 9 Opracowała dr hab. Małgorzata Jóźwak Zakres
SZYBKOŚĆ REAKCJI JONOWYCH W ZALEŻNOŚCI OD SIŁY JONOWEJ ROZTWORU
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW SZYBKOŚĆ REAKCI ONOWYCH W ZALEŻNOŚCI OD SIŁY ONOWE ROZTWORU Opiekun: Krzysztof Kozieł Miejsce ćwiczenia: Czerwona Chemia,
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW SZYBKOŚĆ REAKCI ONOWYCH W ZALEŻNOŚCI OD SIŁY ONOWE ROZTWORU Opiekun: Krzysztof Kozieł Miejsce ćwiczenia: Czerwona Chemia,
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
1 Kinetyka reakcji chemicznych
 Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Współczynniki aktywności w roztworach elektrolitów. W.a. w roztworach elektrolitów (2) W.a. w roztworach elektrolitów (3) 1 r. Przypomnienie!
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
ELEKTROCHEMIA. ( i = i ) Wykład II b. Nadnapięcie Równanie Buttlera-Volmera Równania Tafela. Wykład II. Równowaga dynamiczna i prąd wymiany
 Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
RÓWNOWAGI REAKCJI KOMPLEKSOWANIA
 POLITECHNIK POZNŃSK ZKŁD CHEMII FIZYCZNEJ ĆWICZENI PRCOWNI CHEMII FIZYCZNEJ RÓWNOWGI REKCJI KOMPLEKSOWNI WSTĘP Ważną grupę reakcji chemicznych wykorzystywanych w chemii fizycznej i analitycznej stanowią
POLITECHNIK POZNŃSK ZKŁD CHEMII FIZYCZNEJ ĆWICZENI PRCOWNI CHEMII FIZYCZNEJ RÓWNOWGI REKCJI KOMPLEKSOWNI WSTĘP Ważną grupę reakcji chemicznych wykorzystywanych w chemii fizycznej i analitycznej stanowią
Wyznaczanie współczynnika sztywności zastępczej układu sprężyn
 Wyznaczane zastępczej sprężyn Ćwczene nr 10 Wprowadzene W przypadku klku sprężyn ze sobą połączonych, można mu przypsać tzw. współczynnk zastępczej k z. W skrajnych przypadkach sprężyny mogą być ze sobą
Wyznaczane zastępczej sprężyn Ćwczene nr 10 Wprowadzene W przypadku klku sprężyn ze sobą połączonych, można mu przypsać tzw. współczynnk zastępczej k z. W skrajnych przypadkach sprężyny mogą być ze sobą
Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych
 CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
EFEKT SOLNY BRÖNSTEDA
 EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
Pracownia Automatyki i Elektrotechniki Katedry Tworzyw Drzewnych Ćwiczenie 3. Analiza obwodów RLC przy wymuszeniach sinusoidalnych w stanie ustalonym
 ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Sprawozdanie powinno zawierać:
 Sprawozdane pownno zawerać: 1. wypełnoną stronę tytułową (gotowa do ćw. nr 0 na strone drugej, do pozostałych ćwczeń zameszczona na strone 3), 2. krótk ops celu dośwadczena, 3. krótk ops metody pomaru,
Sprawozdane pownno zawerać: 1. wypełnoną stronę tytułową (gotowa do ćw. nr 0 na strone drugej, do pozostałych ćwczeń zameszczona na strone 3), 2. krótk ops celu dośwadczena, 3. krótk ops metody pomaru,
MATEMATYKA POZIOM ROZSZERZONY Kryteria oceniania odpowiedzi. Arkusz A II. Strona 1 z 5
 MATEMATYKA POZIOM ROZSZERZONY Krytera ocenana odpowedz Arkusz A II Strona 1 z 5 Odpowedz Pytane 1 2 3 4 5 6 7 8 9 Odpowedź D C C A B 153 135 232 333 Zad. 10. (0-3) Dana jest funkcja postac. Korzystając
MATEMATYKA POZIOM ROZSZERZONY Krytera ocenana odpowedz Arkusz A II Strona 1 z 5 Odpowedz Pytane 1 2 3 4 5 6 7 8 9 Odpowedź D C C A B 153 135 232 333 Zad. 10. (0-3) Dana jest funkcja postac. Korzystając
WYZNACZENIE CHARAKTERYSTYK DYNAMICZNYCH PRZETWORNIKÓW POMIAROWYCH
 Zakład Metrolog Systemów Pomarowych P o l t e c h n k a P o z n ańska ul. Jana Pawła II 6-965 POZNAŃ (budynek Centrum Mechatronk, Bomechank Nanonżyner) www.zmsp.mt.put.poznan.pl tel. +8 6 665 35 7 fa +8
Zakład Metrolog Systemów Pomarowych P o l t e c h n k a P o z n ańska ul. Jana Pawła II 6-965 POZNAŃ (budynek Centrum Mechatronk, Bomechank Nanonżyner) www.zmsp.mt.put.poznan.pl tel. +8 6 665 35 7 fa +8
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
AUTOMATYKA I STEROWANIE W CHŁODNICTWIE, KLIMATYZACJI I OGRZEWNICTWIE L3 STEROWANIE INWERTEROWYM URZĄDZENIEM CHŁODNICZYM W TRYBIE PD ORAZ PID
 ĆWICZENIE LABORAORYJNE AUOMAYKA I SEROWANIE W CHŁODNICWIE, KLIMAYZACJI I OGRZEWNICWIE L3 SEROWANIE INWEREROWYM URZĄDZENIEM CHŁODNICZYM W RYBIE PD ORAZ PID Wersja: 03-09-30 -- 3.. Cel ćwczena Celem ćwczena
ĆWICZENIE LABORAORYJNE AUOMAYKA I SEROWANIE W CHŁODNICWIE, KLIMAYZACJI I OGRZEWNICWIE L3 SEROWANIE INWEREROWYM URZĄDZENIEM CHŁODNICZYM W RYBIE PD ORAZ PID Wersja: 03-09-30 -- 3.. Cel ćwczena Celem ćwczena
XXX OLIMPIADA FIZYCZNA ETAP III Zadanie doświadczalne
 XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
Kwantowa natura promieniowania elektromagnetycznego
 Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
A4.05 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
(Ćwiczenie nr 4) Wpływ siły jonowej roztworu na stałą szybkości reakcji.
 (Ćwiczenie nr 4) Wpływ siły jonowej roztworu na stałą szybości reacji Wstęp Rozpatrzmy reację zachodzącą w roztworze pomiędzy jonami i w wyniu tórej powstaje produt D: D stała szybości reacji () Gdy reacja
(Ćwiczenie nr 4) Wpływ siły jonowej roztworu na stałą szybości reacji Wstęp Rozpatrzmy reację zachodzącą w roztworze pomiędzy jonami i w wyniu tórej powstaje produt D: D stała szybości reacji () Gdy reacja
LABORATORIUM PODSTAW ELEKTROTECHNIKI Badanie obwodów prądu sinusoidalnie zmiennego
 Ćwczene 1 Wydzał Geonżyner, Górnctwa Geolog ABORATORUM PODSTAW EEKTROTECHNK Badane obwodów prądu snusodalne zmennego Opracował: Grzegorz Wśnewsk Zagadnena do przygotowana Ops elementów RC zaslanych prądem
Ćwczene 1 Wydzał Geonżyner, Górnctwa Geolog ABORATORUM PODSTAW EEKTROTECHNK Badane obwodów prądu snusodalne zmennego Opracował: Grzegorz Wśnewsk Zagadnena do przygotowana Ops elementów RC zaslanych prądem
Wyznaczenie współczynnika podziału kwasu octowego pomiędzy fazą organiczną a wodną
 Ćwzene 13 Wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną a wodną Cel ćwzena Celem ćwzena jest wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną (butanolem) a wodną w oparu
Ćwzene 13 Wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną a wodną Cel ćwzena Celem ćwzena jest wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną (butanolem) a wodną w oparu
Przykładowy zestaw zadań z chemii Odpowiedzi i schemat punktowania poziom podstawowy
 ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM PODSTAWOWY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Poprawne rozwiązania zadań, uwzględniające
ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM PODSTAWOWY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Poprawne rozwiązania zadań, uwzględniające
Badanie współzależności dwóch cech ilościowych X i Y. Analiza korelacji prostej
 Badane współzależnośc dwóch cech loścowych X Y. Analza korelacj prostej Kody znaków: żółte wyróżnene nowe pojęce czerwony uwaga kursywa komentarz 1 Zagadnena 1. Zwązek determnstyczny (funkcyjny) a korelacyjny.
Badane współzależnośc dwóch cech loścowych X Y. Analza korelacj prostej Kody znaków: żółte wyróżnene nowe pojęce czerwony uwaga kursywa komentarz 1 Zagadnena 1. Zwązek determnstyczny (funkcyjny) a korelacyjny.
WOJSKOWA AKADEMIA TECHNICZNA ĆWICZENIA LABORATORYJNE Z FIZYKI. SPRAWOZDANIE Z PRACY LABORATORYJNEJ nr 0. Badanie rozkładu rzutu śnieżkami do celu
 WOJSKOWA AKADEMIA TECHNICZNA ĆWICZENIA LABORATORJNE Z FIZKI trzec termn wpsu zalczena do USOSu upływa...prowadząc(a/y)... grupa... podgrupa... zespół... semestr... roku akademckego... student(ka)... SPRAWOZDANIE
WOJSKOWA AKADEMIA TECHNICZNA ĆWICZENIA LABORATORJNE Z FIZKI trzec termn wpsu zalczena do USOSu upływa...prowadząc(a/y)... grupa... podgrupa... zespół... semestr... roku akademckego... student(ka)... SPRAWOZDANIE
CHP001004C - Fizykochemia materiałów
 dr nż. Marlena Gąsor-Głogowska 1 CHP001004C - Fzykochema materałów Lteratura: 1. Oblczena chemczne. Skrypt do ćwczeń rachunkowych z chem. M. Łukasewcz, O. Mchalsk, J. Szymońska. Wydawnctwo Unwersytetu
dr nż. Marlena Gąsor-Głogowska 1 CHP001004C - Fzykochema materałów Lteratura: 1. Oblczena chemczne. Skrypt do ćwczeń rachunkowych z chem. M. Łukasewcz, O. Mchalsk, J. Szymońska. Wydawnctwo Unwersytetu
WYZNACZANIE WSPÓŁCZYNNIKA LEPKOŚCI CIECZY METODĄ STOKESA
 WYZNACZANIE WSPÓŁCZYNNIKA LEPKOŚCI CIECZY METODĄ STOKESA. Ops teoretyczny do ćwczena zameszczony jest na strone www.wtc.wat.edu.pl w dzale DYDAKTYKA FIZYKA ĆWICZENIA LABORATORYJNE.. Ops układu pomarowego
WYZNACZANIE WSPÓŁCZYNNIKA LEPKOŚCI CIECZY METODĄ STOKESA. Ops teoretyczny do ćwczena zameszczony jest na strone www.wtc.wat.edu.pl w dzale DYDAKTYKA FIZYKA ĆWICZENIA LABORATORYJNE.. Ops układu pomarowego
CHP001004C - Fizykochemia materiałów
 dr nż. Marlena Gąsor-Głogowska 1 CHP001004C - Fzykochema materałów Lteratura: 1. Oblczena chemczne. Skrypt do ćwczeń rachunkowych z chem. Łukasewcz M., Mchalsk O., Szymońska J. Wydawnctwo Unwersytetu Rolnczego
dr nż. Marlena Gąsor-Głogowska 1 CHP001004C - Fzykochema materałów Lteratura: 1. Oblczena chemczne. Skrypt do ćwczeń rachunkowych z chem. Łukasewcz M., Mchalsk O., Szymońska J. Wydawnctwo Unwersytetu Rolnczego
Spektroskopia molekularna. Ćwiczenie nr 1. Widma absorpcyjne błękitu tymolowego
 Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
WOJSKOWA AKADEMIA TECHNICZNA ĆWICZENIA LABORATORYJNE Z FIZYKI. SPRAWOZDANIE Z PRACY LABORATORYJNEJ nr 0. Badanie rozkładu rzutu śnieżkami do celu
 WOJSKOWA AKADEMIA TECHNICZNA ĆWICZENIA LABORATORJNE Z FIZKI trzec termn wpsu zalczena do USOSu upływa...prowadząca(y)... grupa... podgrupa... zespół... semestr roku akademckego... student(ka)... SPRAWOZDANIE
WOJSKOWA AKADEMIA TECHNICZNA ĆWICZENIA LABORATORJNE Z FIZKI trzec termn wpsu zalczena do USOSu upływa...prowadząca(y)... grupa... podgrupa... zespół... semestr roku akademckego... student(ka)... SPRAWOZDANIE
7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH
 WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
Rozwiązywanie zadań optymalizacji w środowisku programu MATLAB
 Rozwązywane zadań optymalzacj w środowsku programu MATLAB Zagadnene optymalzacj polega na znajdowanu najlepszego, względem ustalonego kryterum, rozwązana należącego do zboru rozwązań dopuszczalnych. Standardowe
Rozwązywane zadań optymalzacj w środowsku programu MATLAB Zagadnene optymalzacj polega na znajdowanu najlepszego, względem ustalonego kryterum, rozwązana należącego do zboru rozwązań dopuszczalnych. Standardowe
Wodorotlenki. n to liczba grup wodorotlenowych w cząsteczce wodorotlenku (równa wartościowości M)
 Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
d[a] = dt gdzie: [A] - stężenie aspiryny [OH - ] - stężenie jonów hydroksylowych - ] K[A][OH
![d[a] = dt gdzie: [A] - stężenie aspiryny [OH - ] - stężenie jonów hydroksylowych - ] K[A][OH d[a] = dt gdzie: [A] - stężenie aspiryny [OH - ] - stężenie jonów hydroksylowych - ] K[A][OH](/thumbs/48/24702101.jpg) 1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
MODEL ODPOWIEDZI I SCHEMAT OCENIANIA ARKUSZA II
 MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadanie teoretyczne
 XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
13. TERMODYNAMIKA WYZNACZANIE ENTALPII REAKCJI ZOBOJĘTNIANIA MOCNEJ ZASADY MOCNYMI KWASAMI I ENTALPII PROCESU ROZPUSZCZANIA SOLI
 Wykonanie ćwiczenia 13. TERMODYNAMIKA WYZNACZANIE ENTALPII REAKCJI ZOBOJĘTNIANIA MOCNEJ ZASADY MOCNYMI KWASAMI I ENTALPII PROCESU ROZPUSZCZANIA SOLI Zadania do wykonania: 1. Wykonać pomiar temperatury
Wykonanie ćwiczenia 13. TERMODYNAMIKA WYZNACZANIE ENTALPII REAKCJI ZOBOJĘTNIANIA MOCNEJ ZASADY MOCNYMI KWASAMI I ENTALPII PROCESU ROZPUSZCZANIA SOLI Zadania do wykonania: 1. Wykonać pomiar temperatury
Pomiar mocy i energii
 Zakład Napędów Weloźródłowych Instytut Maszyn Roboczych CęŜkch PW Laboratorum Elektrotechnk Elektronk Ćwczene P3 - protokół Pomar mocy energ Data wykonana ćwczena... Zespół wykonujący ćwczene: Nazwsko
Zakład Napędów Weloźródłowych Instytut Maszyn Roboczych CęŜkch PW Laboratorum Elektrotechnk Elektronk Ćwczene P3 - protokół Pomar mocy energ Data wykonana ćwczena... Zespół wykonujący ćwczene: Nazwsko
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali
 Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Inżynieria Środowiska
 ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny.
 1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
VI Podkarpacki Konkurs Chemiczny 2013/2014
 VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
Ćw. 26. Wyznaczanie siły elektromotorycznej ogniwa na podstawie prawa Ohma dla obwodu zamkniętego
 6 KATEDRA FZYK STOSOWANEJ PRACOWNA FZYK Ćw. 6. Wyznaczane sły eektromotorycznej ognwa na podstawe prawa Ohma da obwodu zamknętego Wprowadzene Prądem nazywamy uporządkowany ruch ładunku eektrycznego. Najczęścej
6 KATEDRA FZYK STOSOWANEJ PRACOWNA FZYK Ćw. 6. Wyznaczane sły eektromotorycznej ognwa na podstawe prawa Ohma da obwodu zamknętego Wprowadzene Prądem nazywamy uporządkowany ruch ładunku eektrycznego. Najczęścej
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY. Zakład Budowy i Eksploatacji Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA
 PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wyznaczanie stałej szybkości i rzędu reakcji metodą graficzną. opiekun mgr K.
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie stałej szybkości i rzędu reakcji metodą graficzną opiekun mgr K. Łudzik ćwiczenie nr 27 Zakres zagadnień obowiązujących do ćwiczenia 1. Zastosowanie
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie stałej szybkości i rzędu reakcji metodą graficzną opiekun mgr K. Łudzik ćwiczenie nr 27 Zakres zagadnień obowiązujących do ćwiczenia 1. Zastosowanie
1 Hydroliza soli. Hydroliza soli 1
 Hydroliza soli 1 1 Hydroliza soli Niektóre sole, rozpuszczone w wodzie, reagują z cząsteczkami rozpuszczalnika. Reakcja ta nosi miano hydrolizy. Reakcję hydrolizy soli o wzorze BA, można schematycznie
Hydroliza soli 1 1 Hydroliza soli Niektóre sole, rozpuszczone w wodzie, reagują z cząsteczkami rozpuszczalnika. Reakcja ta nosi miano hydrolizy. Reakcję hydrolizy soli o wzorze BA, można schematycznie
Obliczenia chemiczne. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
KINETYKA INWERSJI SACHAROZY
 Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 2(88)/2012
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW (88)/01 Hubert Sar, Potr Fundowcz 1 WYZNACZANIE ASOWEGO OENTU BEZWŁADNOŚCI WZGLĘDE OSI PIONOWEJ DLA SAOCHODU TYPU VAN NA PODSTAWIE WZORU EPIRYCZNEGO 1. Wstęp asowy moment
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW (88)/01 Hubert Sar, Potr Fundowcz 1 WYZNACZANIE ASOWEGO OENTU BEZWŁADNOŚCI WZGLĘDE OSI PIONOWEJ DLA SAOCHODU TYPU VAN NA PODSTAWIE WZORU EPIRYCZNEGO 1. Wstęp asowy moment
Przykład 3.1. Wyznaczenie zmiany odległości między punktami ramy trójprzegubowej
 Przykład Wyznaczene zmany odegłośc mędzy unktam ramy trójrzegubowej Poecene: Korzystając ze wzoru axwea-ohra wyznaczyć zmanę odegłośc mędzy unktam w onższym układze Przyjąć da wszystkch rętów EI = const
Przykład Wyznaczene zmany odegłośc mędzy unktam ramy trójrzegubowej Poecene: Korzystając ze wzoru axwea-ohra wyznaczyć zmanę odegłośc mędzy unktam w onższym układze Przyjąć da wszystkch rętów EI = const
α i = n i /n β i = V i /V α i = β i γ i = m i /m
 Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
3. ŁUK ELEKTRYCZNY PRĄDU STAŁEGO I PRZEMIENNEGO
 3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. a RT.
 Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
LABORATORIUM Z KATALIZY HOMOGENICZNEJ I HETEROGENICZNEJ WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
Refraktometria. sin β sin β
 efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
Przykład 5.1. Kratownica dwukrotnie statycznie niewyznaczalna
 rzykład.. Kratownca dwukrotne statyczne newyznaczana oecene: korzystaąc z metody sł wyznaczyć sły w prętach ponższe kratowncy. const Rozwązane zadana rozpoczynamy od obczena stopna statyczne newyznaczanośc
rzykład.. Kratownca dwukrotne statyczne newyznaczana oecene: korzystaąc z metody sł wyznaczyć sły w prętach ponższe kratowncy. const Rozwązane zadana rozpoczynamy od obczena stopna statyczne newyznaczanośc
Termochemia Prawo Hessa Równania termochemiczne Obliczanie efektów cieplnych Prawo Kirchoffa
 ermchema.3.. Praw essa.3.. Równana termchemczne.3.3. Oblczane efektów ceplnych.3.4. Praw Krchffa ermchema praw essa ERMOCEMIA CIEPŁO REAKCJI - PRAWO ESSA W warunkach zchrycznych termchema zajmuje sę pmarem
ermchema.3.. Praw essa.3.. Równana termchemczne.3.3. Oblczane efektów ceplnych.3.4. Praw Krchffa ermchema praw essa ERMOCEMIA CIEPŁO REAKCJI - PRAWO ESSA W warunkach zchrycznych termchema zajmuje sę pmarem
Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE
 Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
5. Rezonans napięć i prądów
 ezonans napęć prądów W-9 el ćwczena: 5 ezonans napęć prądów Dr hab nŝ Dorota Nowak-Woźny Wyznaczene krzywej rezonansowej dla szeregowego równoległego obwodu Zagadnena: Fzyczne podstawy zjawska rezonansu
ezonans napęć prądów W-9 el ćwczena: 5 ezonans napęć prądów Dr hab nŝ Dorota Nowak-Woźny Wyznaczene krzywej rezonansowej dla szeregowego równoległego obwodu Zagadnena: Fzyczne podstawy zjawska rezonansu
Portfele zawierające walor pozbawiony ryzyka. Elementy teorii rynku kapitałowego
 Portel nwestycyjny ćwczena Na podst. Wtold Jurek: Konstrukcja analza rozdzał 5 dr chał Konopczyńsk Portele zawerające walor pozbawony ryzyka. lementy teor rynku kaptałowego 1. Pożyczane penędzy amy dwa
Portel nwestycyjny ćwczena Na podst. Wtold Jurek: Konstrukcja analza rozdzał 5 dr chał Konopczyńsk Portele zawerające walor pozbawony ryzyka. lementy teor rynku kaptałowego 1. Pożyczane penędzy amy dwa
Wyznaczanie długości fali światła metodą pierścieni Newtona
 013 Katedra Fzyk SGGW Ćwczene 368 Nazwsko... Data... Nr na lśce... Imę... Wydzał... Dzeń tyg.... Ćwczene 368: Godzna.... Wyznaczane długośc fal śwatła metodą perścen Newtona Cechowane podzałk okularu pomarowego
013 Katedra Fzyk SGGW Ćwczene 368 Nazwsko... Data... Nr na lśce... Imę... Wydzał... Dzeń tyg.... Ćwczene 368: Godzna.... Wyznaczane długośc fal śwatła metodą perścen Newtona Cechowane podzałk okularu pomarowego
INDUKCJA ELEKTROMAGNETYCZNA. - Prąd powstający w wyniku indukcji elektro-magnetycznej.
 INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
Zastosowanie symulatora ChemCad do modelowania złożonych układów reakcyjnych procesów petrochemicznych
 NAFTA-GAZ styczeń 2011 ROK LXVII Anna Rembesa-Śmszek Instytut Nafty Gazu, Kraków Andrzej Wyczesany Poltechnka Krakowska, Kraków Zastosowane symulatora ChemCad do modelowana złożonych układów reakcyjnych
NAFTA-GAZ styczeń 2011 ROK LXVII Anna Rembesa-Śmszek Instytut Nafty Gazu, Kraków Andrzej Wyczesany Poltechnka Krakowska, Kraków Zastosowane symulatora ChemCad do modelowana złożonych układów reakcyjnych
WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI
 Ćwiczenie nr 4 WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej szybkości reakcji zmydlania estru etylowego w dwóch różnych temperaturach,
Ćwiczenie nr 4 WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej szybkości reakcji zmydlania estru etylowego w dwóch różnych temperaturach,
Tensorowe. Wielkości fizyczne. Wielkości i Jednostki UŜywane w Elektryce Wielkość Fizyczna to właściwość fizyczna zjawisk lub obiektów,
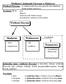 Welkośc Jednosk UŜywane w Elekryce Welkość Fzyczna o właścwość fzyczna zjawsk lub obeków, Przykłady: W. f.: kórą moŝna zmerzyć. czas, długość, naęŝene pola elekrycznego, przenkalność elekryczna kryszałów.
Welkośc Jednosk UŜywane w Elekryce Welkość Fzyczna o właścwość fzyczna zjawsk lub obeków, Przykłady: W. f.: kórą moŝna zmerzyć. czas, długość, naęŝene pola elekrycznego, przenkalność elekryczna kryszałów.
Stanisław Cichocki Natalia Nehrebecka. Zajęcia 4
 Stansław Cchock Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0-1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających Interpretacja
Stansław Cchock Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0-1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających Interpretacja
Ile wynosi suma miar kątów wewnętrznych w pięciokącie?
 1 Ile wynos suma mar kątów wewnętrznych w pęcokące? 1 Narysuj pęcokąt foremny 2 Połącz środek okręgu opsanego na tym pęcokące ze wszystkm werzchołkam pęcokąta 3 Oblcz kąty każdego z otrzymanych trójkątów
1 Ile wynos suma mar kątów wewnętrznych w pęcokące? 1 Narysuj pęcokąt foremny 2 Połącz środek okręgu opsanego na tym pęcokące ze wszystkm werzchołkam pęcokąta 3 Oblcz kąty każdego z otrzymanych trójkątów
a) 1 mol b) 0,5 mola c) 1,7 mola d) potrzebna jest znajomość objętości zbiornika, aby można było przeprowadzić obliczenia
 1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
OGÓLNE PODSTAWY SPEKTROSKOPII
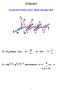 WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
Laboratorium ochrony danych
 Laboratorum ochrony danych Ćwczene nr Temat ćwczena: Cała skończone rozszerzone Cel dydaktyczny: Opanowane programowej metody konstruowana cał skończonych rozszerzonych GF(pm), poznane ch własnośc oraz
Laboratorum ochrony danych Ćwczene nr Temat ćwczena: Cała skończone rozszerzone Cel dydaktyczny: Opanowane programowej metody konstruowana cał skończonych rozszerzonych GF(pm), poznane ch własnośc oraz
Przykład 4.1. Belka dwukrotnie statycznie niewyznaczalna o stałej sztywności zginania
 Przykład.. Beka dwukrotne statyczne newyznaczana o stałej sztywnośc zgnana Poecene: korzystając z metody sł sporządzć wykresy sł przekrojowych da ponŝszej bek. Wyznaczyć ugęce oraz wzgędną zmanę kąta w
Przykład.. Beka dwukrotne statyczne newyznaczana o stałej sztywnośc zgnana Poecene: korzystając z metody sł sporządzć wykresy sł przekrojowych da ponŝszej bek. Wyznaczyć ugęce oraz wzgędną zmanę kąta w
Równowagi jonowe - ph roztworu
 Równowagi jonowe - ph roztworu Kwasy, zasady i sole nazywa się elektrolitami, ponieważ przewodzą prąd elektryczny, zarówno w wodnych roztworach, jak i w stanie stopionym (sole). Nie wszystkie wodne roztwory
Równowagi jonowe - ph roztworu Kwasy, zasady i sole nazywa się elektrolitami, ponieważ przewodzą prąd elektryczny, zarówno w wodnych roztworach, jak i w stanie stopionym (sole). Nie wszystkie wodne roztwory
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Laboratorium 5. Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna
 Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
LICEALIŚCI LICZĄ PRZYKŁADOWE ZADANIA Z ROZWIĄZANIAMI
 Zadanie 1: Słaby kwas HA o stężeniu 0,1 mol/litr jest zdysocjowany w 1,3 %. Oblicz stałą dysocjacji tego kwasu. Jeżeli jest to słaby kwas, można użyć wzoru uproszczonego: K = α C = (0,013) 0,1 = 1,74 10-5
Zadanie 1: Słaby kwas HA o stężeniu 0,1 mol/litr jest zdysocjowany w 1,3 %. Oblicz stałą dysocjacji tego kwasu. Jeżeli jest to słaby kwas, można użyć wzoru uproszczonego: K = α C = (0,013) 0,1 = 1,74 10-5
Programowanie Równoległe i Rozproszone
 Programowane Równoległe Rozproszone Wykład Programowane Równoległe Rozproszone Lucjan Stapp Wydzał Matematyk Nauk Informacyjnych Poltechnka Warszawska (l.stapp@mn.pw.edu.pl) /38 PRR Wykład Chcemy rozwązać
Programowane Równoległe Rozproszone Wykład Programowane Równoległe Rozproszone Lucjan Stapp Wydzał Matematyk Nauk Informacyjnych Poltechnka Warszawska (l.stapp@mn.pw.edu.pl) /38 PRR Wykład Chcemy rozwązać
dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K
![dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K](/thumbs/55/36391740.jpg) RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
Wykład 4. Anna Ptaszek. 27 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 4. Anna Ptaszek 1 / 31
 Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 27 października 2015 1 / 31 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 27 października 2015 1 / 31 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wpływ stężenia kwasu na szybkość hydrolizy estru
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wpływ stężenia kwasu na szybkość hydrolizy estru ćwiczenie nr 25 opracowała dr B. Nowicka, aktualizacja D. Waliszewski Zakres zagadnień obowiązujących do
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wpływ stężenia kwasu na szybkość hydrolizy estru ćwiczenie nr 25 opracowała dr B. Nowicka, aktualizacja D. Waliszewski Zakres zagadnień obowiązujących do
Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 1. Układy równań liniowych
 Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym
 1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
OCENIANIE ARKUSZA POZIOM ROZSZERZONY
 OCENIANIE ARKUSZA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne z poleceniem (nie na temat)
OCENIANIE ARKUSZA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne z poleceniem (nie na temat)
Wykład 7. Podstawy termodynamiki i kinetyki procesowej - wykład 7. Anna Ptaszek. 21 maja Katedra Inżynierii i Aparatury Przemysłu Spożywczego
 Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
3. Badanie kinetyki enzymów
 3. Badanie kinetyki enzymów Przy stałym stężeniu enzymu, a przy zmieniającym się początkowym stężeniu substratu, zmiany szybkości reakcji katalizy, wyrażonej jako liczba moli substratu przetworzonego w
3. Badanie kinetyki enzymów Przy stałym stężeniu enzymu, a przy zmieniającym się początkowym stężeniu substratu, zmiany szybkości reakcji katalizy, wyrażonej jako liczba moli substratu przetworzonego w
 Zadane 1: Wyznacz średne ruchome 3-okresowe z następujących danych obrazujących zużyce energ elektrycznej [kwh] w pewnym zakładze w mesącach styczeń - lpec 1998 r.: 400; 410; 430; 40; 400; 380; 370. Zadane
Zadane 1: Wyznacz średne ruchome 3-okresowe z następujących danych obrazujących zużyce energ elektrycznej [kwh] w pewnym zakładze w mesącach styczeń - lpec 1998 r.: 400; 410; 430; 40; 400; 380; 370. Zadane
OCENIANIE ARKUSZA POZIOM ROZSZERZONY
 Próbny egzamin maturalny z chemii OCENIANIE ARKUSZA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne
Próbny egzamin maturalny z chemii OCENIANIE ARKUSZA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne
roztwory elektrolitów KWASY i ZASADY
 roztwory elektrolitów KWASY i ZASADY nieelektrolit słaby elektrolit mocny elektrolit Przewodnictwo właściwe elektrolitów < 10-2 Ω -1 m -1 dla metali 10 6-10 8 Ω -1 m -1 Pomiar przewodnictwa elektrycznego
roztwory elektrolitów KWASY i ZASADY nieelektrolit słaby elektrolit mocny elektrolit Przewodnictwo właściwe elektrolitów < 10-2 Ω -1 m -1 dla metali 10 6-10 8 Ω -1 m -1 Pomiar przewodnictwa elektrycznego
Laboratorium Podstaw Biofizyki
 CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
Elektrochemia - prawa elektrolizy Faraday a. Zadania
 Elektrochemia - prawa elektrolizy Faraday a Zadania I prawo Faraday a Masa substancji wydzielonej na elektrodach podczas elektrolizy jest proporcjonalna do natężenia prądu i czasu trwania elektrolizy q
Elektrochemia - prawa elektrolizy Faraday a Zadania I prawo Faraday a Masa substancji wydzielonej na elektrodach podczas elektrolizy jest proporcjonalna do natężenia prądu i czasu trwania elektrolizy q
STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ],
![STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ], STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ],](/thumbs/27/11347185.jpg) STATECZNOŚĆ SKARP W przypadku obektu wykonanego z gruntów nespostych zaprojektowane bezpecznego nachylena skarp sprowadza sę do przekształcena wzoru na współczynnk statecznośc do postac: tgφ tgα = n gdze:
STATECZNOŚĆ SKARP W przypadku obektu wykonanego z gruntów nespostych zaprojektowane bezpecznego nachylena skarp sprowadza sę do przekształcena wzoru na współczynnk statecznośc do postac: tgφ tgα = n gdze:
WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO
 10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
Ćw. 5. Wyznaczanie współczynnika sprężystości przy pomocy wahadła sprężynowego
 5 KATEDRA FIZYKI STOSOWANEJ PRACOWNIA FIZYKI Ćw. 5. Wyznaczane współczynna sprężystośc przy pomocy wahadła sprężynowego Wprowadzene Ruch drgający należy do najbardzej rozpowszechnonych ruchów w przyrodze.
5 KATEDRA FIZYKI STOSOWANEJ PRACOWNIA FIZYKI Ćw. 5. Wyznaczane współczynna sprężystośc przy pomocy wahadła sprężynowego Wprowadzene Ruch drgający należy do najbardzej rozpowszechnonych ruchów w przyrodze.
RUCH OBROTOWY Można opisać ruch obrotowy ze stałym przyspieszeniem ε poprzez analogię do ruchu postępowego jednostajnie zmiennego.
 RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
VII Podkarpacki Konkurs Chemiczny 2014/2015
 II Podkarpacki Konkurs Chemiczny 2014/2015 ETAP I 12.11.2014 r. Godz. 10.00-12.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Który z podanych zestawów zawiera wyłącznie
II Podkarpacki Konkurs Chemiczny 2014/2015 ETAP I 12.11.2014 r. Godz. 10.00-12.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Który z podanych zestawów zawiera wyłącznie
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów. 07 marca 2019 r. zawody III stopnia (wojewódzkie) Schemat punktowania zadań
 Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 07 marca 2019 r. zawody III stopnia (wojewódzkie) Schemat punktowania zadań Maksymalna liczba punktów 40. 90% 36 pkt. Uwaga! 1. Wszystkie
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 07 marca 2019 r. zawody III stopnia (wojewódzkie) Schemat punktowania zadań Maksymalna liczba punktów 40. 90% 36 pkt. Uwaga! 1. Wszystkie
