Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
|
|
|
- Alojzy Kaźmierczak
- 6 lat temu
- Przeglądów:
Transkrypt
1 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo w podczerwieni (IR) powstaje tylko wtedy gdy podczas drgań występuje zmiana momentu dipolowego cząsteczki! Przykłady kiedy nie występuje widmo IR: dla cząsteczek symetrycznych N 2, 2, H 2, dla gazów szlachetnych. 1 2 Stałe siłowe wiązań 3 4 1
2 Stałe siłowe wiązań Wiązanie chemiczne utrzymujące atomy w postaci cząsteczki charakteryzuje stała siłowa ƒ. Prawo Hooka Siłę sprowadzającą układ do stanu równowagi opisuje równanie F = ƒx Zależność częstości drgań ν od stałej siłowej ƒ i mas atomów (m 1, m 2 ): Wiązanie Zakresy absorpcji drgań rozciągających Stała siłowa ƒ (N/m) Rejon obliczenia absorpcji liczba falowa (cm -1 ) doświadczenie C H 5, C 5, H 7, C = 12, µ masa zredukowana 5 częstotliwość ν = c/ λ; liczba falowa ( częstość ) ν = 1/ λ 6 Drgania: rozciągające (walencyjne) - ν np.: ν C-H ; ν C-C ; ν C= drgania rozciągające symetryczne Przykłady: Animacje - Wikipedia drgania rozciągające asymetryczne Elementy techniki pracy w spektrofotometrii w podczerwieni Wielkość badanej próbki kilka ml (mg) W skali mikro ilości poniżej 0,01µl (0,01 µg) Zapis widm kuwety solne: z chlorku sodu, bromku potasu, jodku lub bromku cezu przepuszczalność chlorku sodu w zakresie cm -1 bromku potasu w zakresie cm -1 ; kuwety z okienkami polietylenowymi, teflonowymi, z żywic, itp. deformacyjne - δ np. : δ C-H ; δ C-C ; δ C- drgania deformacyjne wahadłowe drgania deformacyjne wachlarzowe drgania deformacyjne nożycowe drgania deformacyjne skręcające Widma cieczy zapis się jako film cieczy; Widma ciał stałych jako zawiesinę w oleju (najczęściej w nujolu) w postaci pastylki w KBr Gazy kuwety gazowe
3 KREŚLANIE STRUKTURY Drgania rozciągające (ν): Wiązania pojedyncze: H cm 1 alkohole i fenole ok ok cm -1 kwasy karboksylowe N H cm 1 aminy, amidy C H cm 1 poniżej 3000 cm 1 alkany powyżej 3100 cm 1 alkeny i ww. aromatyczne ok cm 1 alkiny Zakres pasm drgań rozciągających wiązań między atomami o większych masach: C C, C N, C cm Drgania rozciągające (ν): Wiązania podwójne: cm -1 C=C cm 1 ; C= cm 1 N= cm 1 WĘGLWDRY SZKIELET WĘGLWDRWY Węglowodory alifatyczne Wiązania potrójne: cm 1 (C C ; C N) Drgania deformacyjne (δ): H, N H, C H cm -1 Pasma drgań rozciągających (ν) C H : cm -1 asym.; cm -1 sym. Pasma drgań deformacyjnych (δ) C H : cm -1 asym.; cm -1 sym. Zakres cm -1 charakterystyczny dla każdej cząsteczki tzw. odcisk palca trudny do interpretacji,
4 13 14 Chloropropan H 3 C CH 2 CH 2 Cl WĘGLWDRY SZKIELET WĘGLWDRWY Węglowodory nienasycone Pasma drgań rozciągających (ν) =C H: cm -1 Pasma drgań deformacyjnych (δ) =C H: cm cm -1 ν C-Cl Pasma drgań rozciągających (ν) C=C: cm -1 Pasma drgań rozciągających (ν) C H: cm -1 Pasma drgań deformacyjnych (δ) C H: cm -1 Pasma drgań rozciągających (ν) C C: cm -1 pasma drgań rozciągających wiązań C-Cl : cm -1 C-Br : cm
5 17 18 WĘGLWDRY SZKIELET WĘGLWDRWY ν C-H δ C-H 1-heptyn CH C - (CH 2 ) 4 - Węglowodory aromatyczne Pasma drgań rozciągających =C H: cm -1 Pasma drgań rozciągających C=C: cm -1 znaczenie diagnostyczne mają dwa pasma ok.1580 i 1500 cm -1 Pasma drgań deformacyjnych =C H poza płaszczyzną pierścienia: cm -1 charakterystyczny obraz widma zależy od podstawienia ν C C 2-heptyn - C C - (CH 2 ) 3 - Zakres nadtonów i drgań kombinacyjnych: cm -1 (mono-, orto-, meta-, para-) obraz widma zależy od liczby podstawników i miejsca podstawienia
6 Wiązania węgiel wodór i węgiel węgiel nadtony ν C H ν C H ν C C ν C=C ν C=C δ C-H δ C-H δ =C H δ =C H Przykład: rozróżnienie pasm drgań rozciągających C H przy wiązaniu pojedynczym i wiązaniach wielokrotnych; Pojedyncze C H Podwójne = C H Potrójne C H Podstawienie pierścienia aromatycznego cykloheksan C-H aromat alifat nadtony określenie podstawienia w pierścieniu aromatycznym n-butylobenzen nadtony i pasma drgań kombinacyjnych CH 2 CH 2 CH
7 Podstawienie pierścienia aromatycznego Etery ugrupowanie C C mono- dwa silne pasma cm cm-1 νc CH3 CH2 CH2 orto- jedno silne pasmo CH cm-1 zakres drgań deformacyjnych =C-H zginające poza płaszczyznę pierścienia eter dipropylowy CH2 CH3 metadwa pasma: silne i średnie cm cm-1 parajedno silne pasmo cm-1 25 Etery ugrupowanie C C fenetol etoksybenzen 26 Alkohole, grupa H CH2-CH
8 Alkohole, grupa H Fenole δ CH alif alkohol sec-butylowy roztwór w CCl Grupa hydroksylowa 3-(p-hydroksyfenylo)-1-propanol film cieczy H CH 2 CH 2 -CH 2 H
9 Grupa hydroksylowa wiązania międzycząsteczkowe wiązania wewnątrzcząsteczkowe Keton, grupa karbonylowa C = roztwory: 0,1 mol/dm 3 1 mol/dm 3 0,1 mol/dm 3 1 mol/dm 3 v =C-H v =C-H pasmo drgań wiązania izolowanego -H v =C-H ν C = Drgania rozciągające cm Keton - acetofenon
10 Aldehyd, grupa C H Acetaldehyd - C - H H CH 2 = C - H ν C = - drgania rozciągające: cm -1 ν C-H - drgania rozciągające: cm Grupa karboksylowa Grupa karboksylowa kwas propionowy kwas migdałowy H H kwas p-toluilowy H 3 C H 39 Roztwór w CCl
11 Film cieczy Wzór sumaryczny: C 8 H 8 2 ester octan metylu cm cm cm-1 Film cieczy IR: szerokie pasmo cm -1 drgania rozciągające wiązania -H karboksylowego silne pasmo 1750 cm -1 drania rozciągające wiązania C=; Pasma 1600 cm -1 i 1500 cm -1 świadczą o występowaniu pierścienia aromatycznego odpowiadają drganiom wiązań C=C w pierścieniu aromatycznym; Pasma 1450 cm -1 i 1390 cm -1 świadczą o występowaniu grupy alkilowej. - C - - Roztwór w CCl 4 H Chlorek kwasowy: pasmo absorpcyjne ν(c=) w zakresie cm -1 chlorek propionylu -CH 2 - C - Cl chlorek oktanoilu R - C - Cl R = C 9 H
12 Bezwodnik kwasowy: dwa pasma absorpcyjne drgań wiązań C= w zakresie cm -1 Bezwodnik kwasu benzoesowego - C - - C - bezwodnik propionowy -CH 2 - C - - C - CH Benzamid Acetamid ν C=Carom ν C = δ C-H alif ν N-H as νn-h sym δ N-H Film cieczy - C - NH
13 Nitryl Związki nitrowe N δ C-H N 2 v N2 v C N cm -1 H 3 C H 3 C CH - C N rozc. as cm -1 rozc. sym cm -1 Izonitryle R-N C: v -N C ~ cm -1 Cl Sole diazoniowe Ar-N N + : v -N N ~ cm C N 2 50 Aminy aminy pierwszorzędowe H N H m-anizydyna H N H ν C N ν N H cm -1 δ N H ν N H dwa pasma amina I rz. ok cm -1 ν C N cm -1 ν N H cm -1 dwa pasma amina I rz. δ N H ok cm -1 pasmo asocjacyjne ν C cm
14 Aminy aminy drugorzędowe Amina trzeciorzędowa ν N H jedno pasmo amina II rz. trietyloamina N H 3 C CH 2 CH 2 CH Wpływ rozpuszczalnika na widmo n- butanolu 55 14
Widma w podczerwieni (IR)
 Spektroskopowe metody identyfikacji związków organicznych Widma w podczerwieni (IR) dr 2 Widmo w podczerwieni Liczba drgań zależy od liczby atomów w cząsteczce: cząsteczka nieliniowa o n atomach ma 3n-6
Spektroskopowe metody identyfikacji związków organicznych Widma w podczerwieni (IR) dr 2 Widmo w podczerwieni Liczba drgań zależy od liczby atomów w cząsteczce: cząsteczka nieliniowa o n atomach ma 3n-6
Jak analizować widmo IR?
 Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Kilka wskazówek ułatwiających analizę widm w podczerwieni
 Kilka wskazówek ułatwiających analizę widm w podczerwieni Opracowanie wg dostępnej literatury spektroskopowej: Dr Alina T. Dubis e-mail: alina@uwb.edu.pl Instytut Chemii Uniwersytet w Białymstoku Al. J.
Kilka wskazówek ułatwiających analizę widm w podczerwieni Opracowanie wg dostępnej literatury spektroskopowej: Dr Alina T. Dubis e-mail: alina@uwb.edu.pl Instytut Chemii Uniwersytet w Białymstoku Al. J.
Podczerwień bliska: cm -1 (0,7-2,5 µm) Podczerwień właściwa: cm -1 (2,5-14,3 µm) Podczerwień daleka: cm -1 (14,3-50 µm)
 SPEKTROSKOPIA W PODCZERWIENI Podczerwień bliska: 14300-4000 cm -1 (0,7-2,5 µm) Podczerwień właściwa: 4000-700 cm -1 (2,5-14,3 µm) Podczerwień daleka: 700-200 cm -1 (14,3-50 µm) WIELKOŚCI CHARAKTERYZUJĄCE
SPEKTROSKOPIA W PODCZERWIENI Podczerwień bliska: 14300-4000 cm -1 (0,7-2,5 µm) Podczerwień właściwa: 4000-700 cm -1 (2,5-14,3 µm) Podczerwień daleka: 700-200 cm -1 (14,3-50 µm) WIELKOŚCI CHARAKTERYZUJĄCE
SPEKTROSKOPIA W PODCZERWIENI
 SPEKTROSKOPIA W PODCZERWIENI Obszar widma elektromagnetycznego ( od ok. 14000 do 200cm-1 ) między obszarem widzialnym a mikrofalowym nazywamy podczerwienią (IR). W określeniu struktury związków organicznych
SPEKTROSKOPIA W PODCZERWIENI Obszar widma elektromagnetycznego ( od ok. 14000 do 200cm-1 ) między obszarem widzialnym a mikrofalowym nazywamy podczerwienią (IR). W określeniu struktury związków organicznych
Spektroskopia molekularna. Spektroskopia w podczerwieni
 Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
SPEKTROSKOPIA W PODCZERWIENI
 SPEKTROSKOPIA W PODCZERWIENI Rys. 1 Zakres widma elektromagnetycznego. Obszar widma elektromagnetycznego o liczbie falowej (odwrotność długości fali) od ok. 14000 do 200cm-1 między obszarem widzialnym
SPEKTROSKOPIA W PODCZERWIENI Rys. 1 Zakres widma elektromagnetycznego. Obszar widma elektromagnetycznego o liczbie falowej (odwrotność długości fali) od ok. 14000 do 200cm-1 między obszarem widzialnym
spektroskopia IR i Ramana
 spektroskopia IR i Ramana oscylacje (wibracje) 3N-6 lub 3N-5 drgań normalnych nie wszystkie drgania obserwuje się w IR - nieaktywne w IR gdy nie zmienia się moment dipolowy - pasma niektórych drgań mają
spektroskopia IR i Ramana oscylacje (wibracje) 3N-6 lub 3N-5 drgań normalnych nie wszystkie drgania obserwuje się w IR - nieaktywne w IR gdy nie zmienia się moment dipolowy - pasma niektórych drgań mają
Spektroskopia. Spotkanie pierwsze. Prowadzący: Dr Barbara Gil
 Spektroskopia Spotkanie pierwsze Prowadzący: Dr Barbara Gil Temat rozwaŝań Spektroskopia nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na
Spektroskopia Spotkanie pierwsze Prowadzący: Dr Barbara Gil Temat rozwaŝań Spektroskopia nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na
KARTA PRACY DO ZADANIA 1. Pomiar widma aminokwasu na spektrometrze FTIR, model 6700.
 KARTA PRACY D ZADANIA 1 Pomiar widma aminokwasu na spektrometrze FTIR, model 6700. Wykonaj zadanie zgodnie z instrukcją nr 1 i wypełnij tabelę (w odpowiednich komórkach wstaw "X"). ZAKRES SPEKTRALNY ZMIERZNEG
KARTA PRACY D ZADANIA 1 Pomiar widma aminokwasu na spektrometrze FTIR, model 6700. Wykonaj zadanie zgodnie z instrukcją nr 1 i wypełnij tabelę (w odpowiednich komórkach wstaw "X"). ZAKRES SPEKTRALNY ZMIERZNEG
PODSTAWY METODY SPEKTROSKOPI W PODCZERWIENI ABSORPCJA, EMISJA
 PODSTAWY METODY SPEKTROSKOPI W PODCZERWIENI ABSORPCJA, EMISJA Materia może oddziaływać z promieniowaniem poprzez absorpcję i emisję. Procesy te polegają na pochłonięciu lub wyemitowaniu fotonu przez cząstkę
PODSTAWY METODY SPEKTROSKOPI W PODCZERWIENI ABSORPCJA, EMISJA Materia może oddziaływać z promieniowaniem poprzez absorpcję i emisję. Procesy te polegają na pochłonięciu lub wyemitowaniu fotonu przez cząstkę
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Akademia Górniczo-Hutnicza Wydział Inżynierii Materiałowej i Ceramiki Katedra Chemii Krzemianów i Związków Wielkocząsteczkowych
 Akademia Górniczo-Hutnicza Wydział nżynierii Materiałowej i Ceramiki Katedra Chemii Krzemianów i Związków Wielkocząsteczkowych nstrukcja do ćwiczeń laboratoryjnych Kierunek studiów: Technologia chemiczna
Akademia Górniczo-Hutnicza Wydział nżynierii Materiałowej i Ceramiki Katedra Chemii Krzemianów i Związków Wielkocząsteczkowych nstrukcja do ćwiczeń laboratoryjnych Kierunek studiów: Technologia chemiczna
FIZYKOCHEMICZNE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH. Witold Danikiewicz
 FIZYKOCEMICZNE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYC Witold Danikiewicz Instytut Chemii Organicznej PAN ul. Kasprzaka 44/52, 01-224 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli
FIZYKOCEMICZNE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYC Witold Danikiewicz Instytut Chemii Organicznej PAN ul. Kasprzaka 44/52, 01-224 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli
PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR
 PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR WSTĘP Metody spektroskopowe Spektroskopia bada i teoretycznie wyjaśnia oddziaływania pomiędzy materią będącą zbiorowiskiem
PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR WSTĘP Metody spektroskopowe Spektroskopia bada i teoretycznie wyjaśnia oddziaływania pomiędzy materią będącą zbiorowiskiem
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zastosowanie spektroskopii w podczerwieni w jakościowej i ilościowej analizie organicznej
 Zastosowanie spektroskopii w podczerwieni w jakościowej i ilościowej analizie organicznej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie
Zastosowanie spektroskopii w podczerwieni w jakościowej i ilościowej analizie organicznej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie
CHEMIA ORGANICZNA. dr hab. Włodzimierz Gałęzowski Wydział Chemii UAM (61)
 EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
IR I 11. IDENTYFIKACJA GRUP FUNKCYJNYCH W WIDMACH IR
 IR I 11. IDENTYFIKACJA GRUP FUNKCYJNYCH W WIDMACH IR Celem ćwiczenia jest zapoznanie się z techniką wykonywania widm związków w postaci pastylek wykonanych z bromku potasu oraz interpretacja otrzymanych
IR I 11. IDENTYFIKACJA GRUP FUNKCYJNYCH W WIDMACH IR Celem ćwiczenia jest zapoznanie się z techniką wykonywania widm związków w postaci pastylek wykonanych z bromku potasu oraz interpretacja otrzymanych
ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH
 ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR
 Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w położeniu co najmniej jeden atom wodoru mogą ulegać enolizacji przez przesunięcie protonu
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w położeniu co najmniej jeden atom wodoru mogą ulegać enolizacji przez przesunięcie protonu
POŁOŻENIA SYGNAŁÓW PROTONÓW POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA
 POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR
 Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR Szczególnym i bardzo charakterystycznym rodzajem oddziaływań międzycząsteczkowych jest wiązanie wodorowe. Powstaje ono między molekułami,
Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR Szczególnym i bardzo charakterystycznym rodzajem oddziaływań międzycząsteczkowych jest wiązanie wodorowe. Powstaje ono między molekułami,
Zastosowanie spektroskopii w podczerwieni w analizie jakościowej i ilościowej. dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB
 Zastosowanie spektroskopii w podczerwieni w analizie jakościowej i ilościowej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie Promieniowanie
Zastosowanie spektroskopii w podczerwieni w analizie jakościowej i ilościowej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie Promieniowanie
Analiza instrumentalna Wykład nr 3
 Analiza instrumentalna Wykład nr 3 KT2_2 brak zajęć lab. w dniu 18.10.2012 SPEKTROSKOPIA IR SPKTROSKOPIA RAMANA WIDMO OSCYLACYJNE Zręby atomowe w molekule wykonują oscylacje wokół położenia równowagi.
Analiza instrumentalna Wykład nr 3 KT2_2 brak zajęć lab. w dniu 18.10.2012 SPEKTROSKOPIA IR SPKTROSKOPIA RAMANA WIDMO OSCYLACYJNE Zręby atomowe w molekule wykonują oscylacje wokół położenia równowagi.
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Spektroskopowe metody identyfikacji związków organicznych
 Spektroskopowe metody identyfikacji związków organicznych Wstęp Spektroskopia jest metodą analityczną zajmującą się analizą widm powstających w wyniku oddziaływania promieniowania elektromagnetycznego
Spektroskopowe metody identyfikacji związków organicznych Wstęp Spektroskopia jest metodą analityczną zajmującą się analizą widm powstających w wyniku oddziaływania promieniowania elektromagnetycznego
Spektroskopia w podczerwieni
 Spektroskopia w podczerwieni Metody badań strukturalnych ciała stałego dr inż. Magdalena Król Co to jest spektroskopia? Spektroskopia jest to nauka zajmująca się oddziaływaniem fali elektromagnetycznej
Spektroskopia w podczerwieni Metody badań strukturalnych ciała stałego dr inż. Magdalena Król Co to jest spektroskopia? Spektroskopia jest to nauka zajmująca się oddziaływaniem fali elektromagnetycznej
Spektrometria w bliskiej podczerwieni - zastosowanie w cukrownictwie. Radosław Gruska Politechnika Łódzka Wydział Biotechnologii i Nauk o Żywności
 Spektrometria w bliskiej podczerwieni - zastosowanie w cukrownictwie Radosław Gruska Politechnika Łódzka Wydział Biotechnologii i Nauk o Żywności Spektroskopia, a spektrometria Spektroskopia nauka o powstawaniu
Spektrometria w bliskiej podczerwieni - zastosowanie w cukrownictwie Radosław Gruska Politechnika Łódzka Wydział Biotechnologii i Nauk o Żywności Spektroskopia, a spektrometria Spektroskopia nauka o powstawaniu
Identyfikacja płomieniowa tworzyw sztucznych Iloczyny rozpuszczalności trudno rozpuszczalnych związków w wodzie w temperaturze pokojowej
 Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
WĘGLOWODORY, ALKOHOLE, FENOLE. I. Wprowadzenie teoretyczne
 WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
Organiczne związki azotu
 Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Analiza Organiczna. Jan Kowalski grupa B dwójka 7(A) Własności fizykochemiczne badanego związku. Zmierzona temperatura topnienia (1)
 Przykład sprawozdania z analizy w nawiasach (czerwonym kolorem) podano numery odnośników zawierających uwagi dotyczące kolejnych podpunktów sprawozdania Jan Kowalski grupa B dwójka 7(A) analiza Wynik przeprowadzonej
Przykład sprawozdania z analizy w nawiasach (czerwonym kolorem) podano numery odnośników zawierających uwagi dotyczące kolejnych podpunktów sprawozdania Jan Kowalski grupa B dwójka 7(A) analiza Wynik przeprowadzonej
WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE.
 1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
17. DODATKI Tabela 1. Symbole okre laj ce wielokrotno ci i podwielokrotno ci ułamków dziesi tnych Symbol Okre lenie Wielokrotno Tabela 2.
 17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
SPEKTROSKOPIA W PODCZERWIENI
 ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH Witold Danikiewicz Intytut Cheii Organicznej PAN ul. Kaprzaka 44/52, 01-224 Warzawa Litopad 2013 tyczeń 2014 SPEKTROSKOPIA W PODCZERWIENI IR 2
ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH Witold Danikiewicz Intytut Cheii Organicznej PAN ul. Kaprzaka 44/52, 01-224 Warzawa Litopad 2013 tyczeń 2014 SPEKTROSKOPIA W PODCZERWIENI IR 2
SPEKTROSKOPIA W PODCZERWIENI
 ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH Witold Danikiewicz Intytut Cheii Organicznej PAN ul. Kaprzaka 44/52, 01-224 Warzawa Seetr ziowy 2017/2018 SPEKTROSKOPIA W PODCZERWIENI IR 2 Spektrokopia
ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH Witold Danikiewicz Intytut Cheii Organicznej PAN ul. Kaprzaka 44/52, 01-224 Warzawa Seetr ziowy 2017/2018 SPEKTROSKOPIA W PODCZERWIENI IR 2 Spektrokopia
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab.
 WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
Zastosowania spektroskopii Ramana
 dr inż. Beata Brożek-Płuska Politechnika Łódzka, Wydział Chemiczny, Międzyresortowy Instytut Techniki Radiacyjnej, Laboratorium Laserowej Spektroskopii Molekularnej WYKŁAD 8 Zastosowanie spektroskopii
dr inż. Beata Brożek-Płuska Politechnika Łódzka, Wydział Chemiczny, Międzyresortowy Instytut Techniki Radiacyjnej, Laboratorium Laserowej Spektroskopii Molekularnej WYKŁAD 8 Zastosowanie spektroskopii
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodami spektroskopii IR i NMR
 Ćwiczenie 3 Pomiar równowagi keto-enolowej metodami spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w pozycji α co najmniej jeden atom H wykazują tautomerię polegającą na wymianie tego
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodami spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w pozycji α co najmniej jeden atom H wykazują tautomerię polegającą na wymianie tego
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów.
 Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów. Wprowadzenie teoretyczne Cel ćwiczeń: Poznanie metod otrzymywania oraz badania właściwości węglowodorów alifatycznych
Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów. Wprowadzenie teoretyczne Cel ćwiczeń: Poznanie metod otrzymywania oraz badania właściwości węglowodorów alifatycznych
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Spektroskopia w podczerwieni
 Spektroskopia w podczerwieni Podstawy teoretyczne spektroskopii w podczerwieni Podstawowe pojęcia związane ze spektroskopią oscylacyjną Interpretacja widm Budowa spektrometru FTIR Podstawowe techniki pomiarowe
Spektroskopia w podczerwieni Podstawy teoretyczne spektroskopii w podczerwieni Podstawowe pojęcia związane ze spektroskopią oscylacyjną Interpretacja widm Budowa spektrometru FTIR Podstawowe techniki pomiarowe
Spektroskopowe metody identyfikacji związków organicznych / Robert. Spis treści
 Spektroskopowe metody identyfikacji związków organicznych / Robert M. Silverstein, Francis X. Webster, David J. Kiemle. wyd. 2, dodr. 4. - Warszawa, 2012 Spis treści ROZDZIAŁ 1 SPEKTROMETRIA MAS 1 1.1
Spektroskopowe metody identyfikacji związków organicznych / Robert M. Silverstein, Francis X. Webster, David J. Kiemle. wyd. 2, dodr. 4. - Warszawa, 2012 Spis treści ROZDZIAŁ 1 SPEKTROMETRIA MAS 1 1.1
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
IDENTYFIKACJA JAKOŚCIOWA NIEZNANEGO ZWIĄZKU ORGANICZNEGO
 IDENTYFIKACJA JAKOŚCIOWA NIEZNANEGO ZWIĄZKU ORGANICZNEGO Schemat raportu końcowego w ramach ćwiczeń laboratoryjnych z przedmiotu Badanie struktury związków organicznych 1. Symbol kodujący identyfikowaną
IDENTYFIKACJA JAKOŚCIOWA NIEZNANEGO ZWIĄZKU ORGANICZNEGO Schemat raportu końcowego w ramach ćwiczeń laboratoryjnych z przedmiotu Badanie struktury związków organicznych 1. Symbol kodujący identyfikowaną
IDENTYFIKACJA ZWIĄZKÓW ORGANICZNYCH METODAMI SPEKTROSKOPOWYMI SPEKTROSKOPIA W PODCZERWIENI (IR)
 IDENTYFIKACJA ZWIĄZKÓW ORGANICZNYC METODAMI SPEKTROSKOPOWYMI SPEKTROSKOPIA W PODCZERWIENI (IR) Metodą o bardzo dużym znaczeniu w organicznej analizie strukturalnej jest spektroskopia w podczerwieni (spektroskopia
IDENTYFIKACJA ZWIĄZKÓW ORGANICZNYC METODAMI SPEKTROSKOPOWYMI SPEKTROSKOPIA W PODCZERWIENI (IR) Metodą o bardzo dużym znaczeniu w organicznej analizie strukturalnej jest spektroskopia w podczerwieni (spektroskopia
Metody spektroskopowe w identyfikacji związków organicznych. Barbara Guzowska-Świder Zakład Informatyki Chemicznej, PRz
 Metody spektroskopowe w identyfikacji związków organicznych Barbara Guzowska-Świder Zakład Informatyki Chemicznej, PRz Metody spektralne wykorzystują zjawiska związane z oddziaływaniem materii z promieniowaniem
Metody spektroskopowe w identyfikacji związków organicznych Barbara Guzowska-Świder Zakład Informatyki Chemicznej, PRz Metody spektralne wykorzystują zjawiska związane z oddziaływaniem materii z promieniowaniem
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
SPEKTROSKOPIA W PODCZERWIENI
 ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH Witold Danikiewicz Intytut Cheii Organicznej PAN ul. Kaprzaka 44/52, 01-224 Warzawa Litopad 2013 tyczeń 2014 SPEKTROSKOPIA W PODCZERWIENI IR 2
ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH Witold Danikiewicz Intytut Cheii Organicznej PAN ul. Kaprzaka 44/52, 01-224 Warzawa Litopad 2013 tyczeń 2014 SPEKTROSKOPIA W PODCZERWIENI IR 2
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
Zastosowanie spektroskopii UV/VIS do określania struktury związków organicznych
 Zwiększenie liczby wysoko wykwalifikowanych absolwentów kierunków ścisłych Uniwersytetu Jagiellońskiego POKL.04.01.02-00-097/09-00 Zastosowanie spektroskopii UV/VIS do określania struktury związków organicznych
Zwiększenie liczby wysoko wykwalifikowanych absolwentów kierunków ścisłych Uniwersytetu Jagiellońskiego POKL.04.01.02-00-097/09-00 Zastosowanie spektroskopii UV/VIS do określania struktury związków organicznych
I KSZTAŁCENIA PRAKTYCZNEGO. Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
EGZAMIN WSTĘPNY NA STUDIUM DOKTORANCKIE W CBMIM PAN W ŁODZI. Zestaw pytań z chemii organicznej
 EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ
 FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). C. alkiny D. areny
 Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
PRÓBNY EGZAMIN MATURALNY Z CHEMII
 Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 90 minut Informacje 1.
Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 90 minut Informacje 1.
m 1, m 2 - masy atomów tworzących wiązanie. Im
 Dr inż. Grażyna Żukowska Wykorzystanie metod spektroskopii oscylacyjnej do analizy materiałów organicznych i nieorganicznych 1. Informacje podstawowe Spektroskopia Ramana i spektroskopia w podczerwieni
Dr inż. Grażyna Żukowska Wykorzystanie metod spektroskopii oscylacyjnej do analizy materiałów organicznych i nieorganicznych 1. Informacje podstawowe Spektroskopia Ramana i spektroskopia w podczerwieni
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Podział związków organicznych
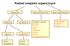 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE
 SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE Promieniowanie o długości fali 2-50 μm nazywamy promieniowaniem podczerwonym. Absorpcja lub emisja promieniowania z tego zakresu jest
SPEKTROSKOPIA IR I SPEKTROSKOPIA RAMANA JAKO METODY KOMPLEMENTARNE Promieniowanie o długości fali 2-50 μm nazywamy promieniowaniem podczerwonym. Absorpcja lub emisja promieniowania z tego zakresu jest
CHEMIA ORGANICZNA CHEMIA ORGANICZNA CHEMIA ZWIĄZKÓW PIERWIASTKA WĘGLA TLENEK WĘGLA (IV) KWAS WĘGLOWY + SOLE KWASU WĘGLOWEGO
 CHEMIA ORGANICZNA CHEMIA ORGANICZNA CHEMIA ZWIĄZKÓW PIERWIASTKA WĘGLA WYJĄTKI: TENEK WĘGLA(II) TLENEK WĘGLA (IV) KWAS WĘGLOWY + SOLE KWASU WĘGLOWEGO KLASYFIKACJA ZWIĄZKÓW ORGANICZNYCH KLASYFIKACJA ZWIĄZKÓW
CHEMIA ORGANICZNA CHEMIA ORGANICZNA CHEMIA ZWIĄZKÓW PIERWIASTKA WĘGLA WYJĄTKI: TENEK WĘGLA(II) TLENEK WĘGLA (IV) KWAS WĘGLOWY + SOLE KWASU WĘGLOWEGO KLASYFIKACJA ZWIĄZKÓW ORGANICZNYCH KLASYFIKACJA ZWIĄZKÓW
Reflekcyjno-absorpcyjna spektroskopia w podczerwieni RAIRS (IRRAS) Reflection-Absorption InfraRed Spectroscopy
 Reflekcyjno-absorpcyjna spektroskopia w podczerwieni RAIRS (IRRAS) Reflection-Absorption InfraRed Spectroscopy Odbicie promienia od powierzchni metalu E n 1 Równania Fresnela E θ 1 θ 1 r E = E odb, 0,
Reflekcyjno-absorpcyjna spektroskopia w podczerwieni RAIRS (IRRAS) Reflection-Absorption InfraRed Spectroscopy Odbicie promienia od powierzchni metalu E n 1 Równania Fresnela E θ 1 θ 1 r E = E odb, 0,
Część I ZADANIA PROBLEMOWE (26 punktów)
 Zadanie 1 (0 6 punktów) Część I ZADANIA PROBLEMOWE (26 punktów) W podanym niżej tekście w miejsce kropek wpisz: - kwas solny - kwas mlekowy - kwas octowy - zjełczałe masło - woda sodowa - pokrzywa - zsiadłe
Zadanie 1 (0 6 punktów) Część I ZADANIA PROBLEMOWE (26 punktów) W podanym niżej tekście w miejsce kropek wpisz: - kwas solny - kwas mlekowy - kwas octowy - zjełczałe masło - woda sodowa - pokrzywa - zsiadłe
Optyczna spektroskopia oscylacyjna. w badaniach powierzchni
 Optyczna spektroskopia oscylacyjna w badaniach powierzchni Zalety oscylacyjnej spektroskopii optycznej uŝycie fotonów jako cząsteczek wzbudzających i rejestrowanych nie wymaga uŝycia próŝni (moŝliwość
Optyczna spektroskopia oscylacyjna w badaniach powierzchni Zalety oscylacyjnej spektroskopii optycznej uŝycie fotonów jako cząsteczek wzbudzających i rejestrowanych nie wymaga uŝycia próŝni (moŝliwość
Skala ocen: ndst 0 20, dst , dst , db , db , bdb Informacja:
 Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Spektroskopia molekularna. Ćwiczenie nr 1. Widma absorpcyjne błękitu tymolowego
 Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Alkohole i fenole. Opracowanie: Bartłomiej SIEPSIAK klasa 3d Opiekun: p. Teresa Gębicka
 Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Br Br. Br Br OH 2 OH NH NH 2 2. Zakład Chemii Organicznej: kopiowanie zabronione
 Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
Sprawozdanie z badania potwierdzających tożsamość substancji Oliwa Ozonowana
 KATEDRA CHEMII ORGANICZNEJ i STOSOWANEJ Wydział Chemii Uniwersytetu Łódzkiego 91-403 Łódź, ul. Tamka 12 Tel. +42 635 57 69, Fax +42 665 51 62 e-mail: romanski@uni.lodz.pl Sprawozdanie z badania potwierdzających
KATEDRA CHEMII ORGANICZNEJ i STOSOWANEJ Wydział Chemii Uniwersytetu Łódzkiego 91-403 Łódź, ul. Tamka 12 Tel. +42 635 57 69, Fax +42 665 51 62 e-mail: romanski@uni.lodz.pl Sprawozdanie z badania potwierdzających
I II I II III II. I. Wartościowość pierwiastków chemicznych. oznacza się cyfrą rzymską. tlenek żelaza (III) C IV O II 2
 I. Wartościowość pierwiastków chemicznych oznacza się cyfrą rzymską tlenek żelaza (III) C IV II 2 oznacza liczbę wiązań za pomocą, których atomy łączą się ze sobą H wodór jest I wartościowy od atomu wodoru
I. Wartościowość pierwiastków chemicznych oznacza się cyfrą rzymską tlenek żelaza (III) C IV II 2 oznacza liczbę wiązań za pomocą, których atomy łączą się ze sobą H wodór jest I wartościowy od atomu wodoru
Slajd 1. Slajd 2. Aminy. trietyloamina. amoniak. chlorofil
 Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
ANALIZA WYNIKÓW MATURY 2017 Z CHEMII
 ANALIZA WYNIKÓW MATURY 2017 Z CHEMII Wrocław, 30 listopada 2017 r. Jolanta Baldy Okręgowa Komisja Egzaminacyjna we Wrocławiu Matura 2017 z chemii w liczbach Średni wynik procentowy Okręg 38% Kraj 41% Okręg
ANALIZA WYNIKÓW MATURY 2017 Z CHEMII Wrocław, 30 listopada 2017 r. Jolanta Baldy Okręgowa Komisja Egzaminacyjna we Wrocławiu Matura 2017 z chemii w liczbach Średni wynik procentowy Okręg 38% Kraj 41% Okręg
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami.
![Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami.](/thumbs/100/143872318.jpg) Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. I. Gęstość propanu w warunkach normalnych wynosi II. Jeżeli stężenie procentowe nasyconego roztworu pewnej
Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. I. Gęstość propanu w warunkach normalnych wynosi II. Jeżeli stężenie procentowe nasyconego roztworu pewnej
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości.
 Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości. Cel główny: przypomnienie i utrwalenie wiadomości dotyczących węglowodorów i pochodnych
Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości. Cel główny: przypomnienie i utrwalenie wiadomości dotyczących węglowodorów i pochodnych
Roztwory elekreolitów
 Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW DOTYCHCZASOWYCH GIMNAZJÓW 2017/2018. Eliminacje szkolne
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW DOTYCHCZASOWYCH GIMNAZJÓW 2017/2018 Eliminacje szkolne Podczas rozwiązywania zadań
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII DLA UCZNIÓW DOTYCHCZASOWYCH GIMNAZJÓW 2017/2018 Eliminacje szkolne Podczas rozwiązywania zadań
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Spis treści 1. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2001 2 2. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2002 7
 Spis treści 1. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2001 2 2. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2002 7 3. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2003 13 4. MIELEC - DANE ZA ROK 2001 19 5. MIELEC
Spis treści 1. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2001 2 2. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2002 7 3. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2003 13 4. MIELEC - DANE ZA ROK 2001 19 5. MIELEC
