Kilka wskazówek ułatwiających analizę widm w podczerwieni
|
|
|
- Dagmara Jankowska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Kilka wskazówek ułatwiających analizę widm w podczerwieni Opracowanie wg dostępnej literatury spektroskopowej: Dr Alina T. Dubis alina@uwb.edu.pl Instytut Chemii Uniwersytet w Białymstoku Al. J. Piłsudskiego 11/ Białystok Białystok, 2008
2 Jak analizować widmo IR? Analizując widma w podczerwieni można stwierdzić, że nawet dla dość prostych związków zawierających jedną grupę funkcyjną, widma składają się z wielu pasm absorpcyjnych, z których nie wszystkie można zinterpretować. Bardzo istotne jest to, aby w obszarze częstości cm -1 odnaleźć charakterystyczne pasma grup funkcyjnych (Tabela 1): cm -1 N H rozciągające 1 i 2-rzędowe aminy cm -1 O H rozciągające alkohole, szerokie i silne pasmo cm -1 C H rozciągające alkeny cm -1 C H rozciągające alkany cm -1 C=O rozciągające ketony, aldehydy, estry cm -1 C=C rozciągające alkeny Rozpoczynamy analizę od zakresu cm -1. Patrzymy na zakres drgań rozciągających C H około 3000 cm -1 : Czy pasma znajdują się na prawo od 3000 cm -1? Czy są jakieś pasma na lewo od 3000 cm -1? W próbce występują: Grupy alkilowe (obecne w większości związków organicznych) Wiązania wielokrotne lub aromatyczne w cząsteczce Analizujemy obszar cm -1 (należy sprawdzić dokładne położenie pasma karbonylowego w celu określenia charakteru związku karbonylowego) oraz czy są pasma takie jak: Czy również jest pasmo O H? Czy również jest pasmo C O? Czy również jest pasmo aldehydowe C H? Czy również jest pasmo N H? Nie ma żadnych z wyżej wymienionych? Próbka może zawierać grupę funkcyjną: karboksylową estrową aldehydowa amidową ketonową Poszukujemy szerokiego pasma O H w obszarze cm -1. Jeżeli takie pasmo występuje to: 2
3 Interpretacja Czy pasmo O H jest obecne? alkohol lub fenol Poszukujemy jednego lub dwóch ostrych pasm N H w obszarze cm -1. Jeżeli takie pasma są obecne to: Czy są dwa pasma? Czy jest tylko jedno pasmo? Interpretacja: Pierwszorzędowa amina Drugorzędowa amina Sprawdzamy inne elementy strukturalne: Czy są drgania C O? Czy obecne jest pasmo drgań rozciągających C=C? Czy są obecne pasma drgań rozciągających aromatycznych? Czy występuje pasmo C C? Czy są obecne pasma grupy -NO 2? Interpretacja: eter (lub ester o ile występuje również pasmo karbonylowe ) alken związek aromatyczny alkin związek nitro Jeżeli nieobecne są główne grupy funkcyjne (pasma inne niż rozciągające C H) w obszarze cm -1, to związek jest prawdopodobnie prostym węglowodorem. Również sprawdzamy obszar cm -1. Aromaty, chlorki alkilowe, kwasy karboksylowe, aminy i amidy dają średnią lub silną absorpcje (drgania zginające) w tym obszarze Nie należy interpretować każdego pasma w widmie IR. Należy się skoncentrować na interpretacji głównych pasm i nauczyć się je rozpoznawać. 3
4 Alkany Widma prostych alkanów charakteryzuje absorpcja drgań rozciągających i zginających grup C H (drgania C C rozciągające są zbyt słabe, aby mogły być zarejestrowane). W widmach prostych alkanów, które maja bardzo mało pasm, każde pasmo w widmie można zinterpretować. C H rozciągające od cm -1 C H zginające lub nożycowe od cm -1 C H kołyszące CH 2 od cm -1 C H kołyszące widoczne jedynie w długołańcuchowych alkanach od cm -1 Widmo oktanu pokazane poniżej zawiera pasma w obszarze cm -1 pochodzące od drgań rozciągających C-H, drgania nożycowe C-H (1470 cm -1 ), kołyszące CH 2 (1383 cm -1 ) i kołyszące długiego łańcucha CH 2 (728 cm -1 ). Skoro większość związków organicznych zawiera takie element strukturalne, to drgania C-H zazwyczaj są obecne w widmach IR. Obszar cm -1 jest nazywany regionem daktyloskopowym. Pasma w tym obszarze podchodzą od złożonych drgań szkieletowych dających w rezultacie skomplikowany obraz. Zazwyczaj obszar ten jest dość złożony i trudny w interpretacji, jednakże każdy związek organiczny ma swój unikalny wzór absorpcji odcisk palca, który może być stosowanych do identyfikacji związków poprzez porównanie z obszarem daktyloskopowym wzorca. 4
5 Alkeny Alkeny są związkami posiadającymi wiązanie podwójne C=C. Drganie rozciągające C=C zazwyczaj daje średnio intensywne pasmo w obszarze cm -1. Drgania rozciągające wiązań C=C H występują przy wyższej częstości niż podobne drgania C C H w alkanach. Warto zapamiętać, że: tylko alkeny i związki aromatyczne dają pasma absorpcyjne C-H rozciągające nieco powyżej 3000 cm -1. Związki nieposiadające wiązań wielokrotnych C=C dają pasma absorpcyjne tylko poniżej 3000 cm -1. Najsilniejsze pasma występujące w widmach alkenów pochodzą od drgań zginających węgiel wodór grupy =C H. Pasma te występują w obszarze cm -1 (uwaga: pasma te zachodzą na obszar daktyloskopowy). Podsumowanie: C=C rozciągające cm -1 =C H rozciągające cm -1 =C H zginające cm -1 W widmie oktenu można zaobserwować pasmo położone powyżej 3000 cm -1 pochodzące od drgań rozciągających =C H i kilka pasm położonych poniżej 3000 cm -1 pochodzących od drgań rozciągających C H (alkanu). Pasmo drgań rozciągających C=C położone jest ok cm -1. Pasmo drgań deformacyjnych nożycowych C H (1465 cm -1 ) i kołyszących CH 2 (1378) są również obecne. Pasma te są typowe dla łańcucha nasyconego i występują w większości związków organicznych. Pasma położone przy 917 cm -1 i 1044 cm -1 pochodzą od drgań zginających poza płaszczyznę grupy =C-H. 5
6 Poniżej pokazano nałożone widmo 1-oktenu z widmem oktanu. Należy zwrócić uwagę jak są do siebie podobne, za wyjątkiem pasm pochodzących od drgań C=C i C=C H rozciągających/deformacyjnych. 6
7 7
8 Alkiny Alkiny to związki zawierające w swojej strukturze wiązanie potrójne wegiel-węgiel ( C C ). Pasmo drgań rozciągających C C pojawia się jako słabe pasmo pomiędzy cm -1. Jest ono bardzo ważnym diagnostycznym narzędziem, ponieważ bardzo niewiele związków organicznych daje absorpcję IR w tym obszarze. Terminalne alkiny (ale nie wewnętrzne) mają silne, wąskie pasmo drgań rozciągających C H w zakresie cm -1. (Zazwyczaj to pasmo jest nierozróżnialne od pasm pochodzących od innych grup funkcyjnych obecnych w cząsteczce absorbujących w tym samym zakresie jak np. drganie rozciągające O-H ). Ponadto terminalne alkiny charakteryzują się pasmem drgania zginającego C H w obszarze cm -1. Streszczenie: C C rozciągające cm -1 C C H: C H rozciągające cm -1 C C H: C H zginające cm -1 W widmie 1-heksynu końcowa grupa alkinowa wykazuje pasmo drgań rozciągających C H przy wiązaniu potrójnym (3324), pasmo drgań rozciągających wiązania potrójnego węgielwęgiel (2126), oraz drganie zginające C H wiązania C-H sąsiadującego z wiązaniem potrójnym (636 cm-1). Pozostałe pasma pochodzą od części nasyconej cząsteczki - drgań C H rozciągających, deformacyjnych w płaszczyźnie i poza płaszczyzną. 8
9 9
10 Halogenki alkilowe Halogenki alkilowe są związkami, w których występuje wiązanie C X, gdzie X jest atomem chloru, bromu, jodu bądź fluoru. Drgania C X pojawiają się w obszarze częstości cm -1, czasami poza typowym zakresem średniej podczerwieni. Drganie rozciągające C Cl pojawia się sie w widmie w obszarze cm -1, podczas gdy drganie rozciągające C Br występuje przy nieco niższej częstości cm -1. W halogenkach, w których atom X występuje przy końcowym atomie węgla, drgania C H kołyszące grupy CH 2 X obserwuje się od cm -1. Dodatkową komplikacją widma jest obfitość pasm absorpcyjnych w obszarze cm -1, szczególnie w krótszych halogenkach alkilowych. Zauważyć należy, że pasma te leżą w obszarze daktyloskopowym. Podsumowując, następujące pasma są charakterystyczne dla halogenków alkilowych: C H kołyszące (-CH 2 X) od cm -1 C X rozciągające (głównie) od cm -1 o C Cl rozciągające cm -1 o C Br rozciągające cm -1 Poniżej zamieszczono widma 1-bromopropanu i 1-chloro-2-metylpropanu. Pasma C Br i C Cl rozciągające występują w obszarze cm -1. Pokazano również drgania deformacyjne CH 2 X w obszarze cm
11 Widma 1-bromopropanu i 1-chloro-1-metylpropanu wyglądają podobnie, ale można zaobserwować różnice w obszarze daktyloskopowym. 11
12 Związki Aromatyczne Drgania rozciągające =C H w układach aromatycznych są obserwowane w obszarze częstości cm -1. Należy zapamiętać, że te częstości absorpcji są nieco większe niż częstości drgań C H w alkanach. Warto zapamiętać, że: tylko alkeny i związki aromatyczne dają pasmo absorpcyjne drgań rozciągających C H nieco powyżej 3000 cm -1. Związki, które nie posiadają wiązania C=C mają pasmo absorpcyjne drgań rozciągających C H poniżej 3000 cm -1. Aromatyczne węglowodory wykazują absorpcję w obszarze cm -1 i cm -1 spowodowaną drganiami rozciągającymi wegiel-węgiel w pierścieniu aromatycznym. Pasma w obszarze cm -1 pochodzące od drgań zginających w płaszczyźnie są dość słabe i dla większości związków aromatycznych nie są obserwowane. Oprócz pasm drgań rozciągających C H powyżej 3000 cm -1, istnieją dwa inne obszary w widmie IR charakterystyczne dla związków aromatycznych pozwalające odróżnić je od innych klas związków niearomatycznych cm -1 słabe pasma ( tzw. "nadtony ) cm -1 (out-of-plane "oop" pasma drgań poza płaszczyzną) Te pasma pozwalają nie tylko rozpoznać związki aromatyczny, ale również są bardzo użyteczne w określaniu liczby podstawników pierścienia aromatycznego. Kształt nadtonów w obszarze cm -1 odzwierciedla typ podstawienia pierścienia aromatycznego. Kształt oop pasm deformacyjnych poza płaszczyznę C H w obszarze cm -1 również charakteryzuje sposób podstawienia pierścienia aromatycznego. Warto zapamiętać, że związki aromatyczne w wielu przypadkach wykazują znacznie więcej pasm absorpcyjnych niż związki niezawierające pierścienia aromatycznego. Jeżeli będziesz musiał rozróżnić dwa widma wiedząc, że jedno z nich należy do związku aromatycznego, to z łatwością dokonasz identyfikacji ponieważ na pierwszy rzut oka duża ilość pasm sugeruje, że pochodzą one od związku aromatycznego. Podsumowanie: C H rozciągające cm -1 Nadtony, słabe pasma w obszarze cm -1 C C rozciągające (w pierścieniu) cm -1 C C rozciągające (w pierścieniu) cm -1 C H zginające poza płaszczyznę "oop" cm -1 Widmo toluen zawiera pasmo drgań rozciągających =C H aromatycznych (3099, 3068, 3032) i drań rozciągających C H alifatycznych (metylowa grupa) (2925 cm -1 ). Charakterystyczne nadtony widoczne są w obszarze cm -1. Również widoczne są drgania rozciągające 12
13 węgiel-węgiel pierścienia aromatycznego (1614, 1506, 1465), C H zginające w płaszczyźnie (1086, 1035), i poza płaszczyzną C H oop (738 cm -1 ). 13
14 Alkohole Alkohole wykazują charakterystyczną absorpcję związaną z drganiami rozciągającymi zarówno grupy O-H jak i C-O. Gdy widmo jest rejestrowane w formie cienkiego filmu wówczas drganie rozciągające O H alkoholu pojawia się w obszarze cm -1 jako bardzo intensywne i szerokie pasmo. Drgania rozciągające C O pojawiają się w obszarze cm -1. O H rozciągające zasocjowanej grupy cm -1 C O rozciągające cm -1 W widmie etanolu widoczne jest bardzo szerokie i silne pasmo drgań rozciągających grupy O H (3391) i wiązania C O (1102, 1055 cm -1 ). 14
15 Ketony Pasmo drgań rozciągających grupy C=O nasyconych alifatycznych ketonów pojawia się, ok 1715 cm -1. Sprzężenie grupy karbonylowej z wiązaniem podwójnym węgiel-węgiel lub pierścieniem aromatycznym, tak jak w alfa, beta-nienasyconych aldehydach i benzaldehydach, powoduje przesunięcie tego pasma do niższej częstości cm -1. Podsumowanie: C=O rozciągające o Alifatyczne ketony 1715 cm -1 o α, β-nienasycone ketony cm -1 Poniżej pokazane jest widmo 2-butanonu. Nasycone ketony dają pasmo drgań rozciągających grupy C=O przy 1715 cm -1. W widmie występują też pasma drgań rozciągających C H (ok cm -1 ) grup alkilowych. Nie ma konieczności interpretacji wszystkich pasm w obszarze daktyloskopowym poniżej 1500 cm -1 ). 15
16 Aldehydy Drgania rozciągające nasyconych, alifatycznych aldehydów pojawiają się w obszarze cm -1. Tak jak w ketonach, jeżeli atom węgla sąsiadujący z grupą karbonylową jest nienasycony, to częstość pasm absorpcyjnych przesuwa się w stronę niższych liczb falowych cm -1. Kolejnym pasmem absorpcyjnym o wartości diagnostycznej dla aldehydów jest pasmo pochodzące od drganie rozciągające O=C H. Drganie to zazwyczaj pojawia się jako jedno lub dwa pasma o średniej intensywności w obszarze cm -1. Pasmo położone ok cm -1 zazwyczaj bardzo trudno rozróżnić od innych drgań rozciągających C H (przypomnijmy sobie, że pasma drgań rozciągających alkanów C H pojawia sie w zakresie cm -1 ). Natomiast obecność średnio intensywnego pasma absorpcyjnego ok 2720 cm -1 jest bardzo użyteczna w rozpoznaniu charakteru aldehydowego związku. Jeżeli spodziewasz się, że analizowany związek jest aldehydem, zawsze poszukuj pasma ok 2720 cm -1. Pasmo to bardzo często pojawia się, jako boczny pik tuż po prawej stronie pasma drgań rozciągających C H alkanów. Podsumowanie: H C=O rozciągające cm -1 C=O rozciągające: o alifatyczne aldehydy cm -1 o alfa, beta-nienasycone aldehydy cm -1 Poniżej pokazano widma benzaldehydu i aldehydu butylowego. Zwróćmy uwagę, że drgania rozciągające O=C alfa, beta-nienasyconych związków np. benzaldehydu położone są przy niższych liczbach falowych niż w przypadku aldehydu nasyconego butanalu. Zauważmy charakterystyczne drgania rozciągające O=C H w obu aldehydach w obszarze cm -1, pasmo położone przy 2725 cm -1 w przypadku butanalu i przy 2745 cm -1 w przypadku benzaldehydu. 16
17 17
18 Kwasy karboksylowe Kwasy karboksylowe wykazują bardzo szerokie pasmo drgań rozciągających O H. Podobnie jak w alkoholach, pasmo drgań rozciągających O H w kwasach karboksylowych jest bardzo szerokie i pojawia się w zakresie cm -1, z maksimum przy 3000 cm -1. Jest to analogiczny obszar jak obszar drgań rozciągających C H grup alkilowych i aromatycznych. Tak wiec kwasy karboksylowe charakteryzują się nieco nieregularnym charakterem absorpcji w obszarze cm -1, z szerokim pasmem O H nałożonym na pasma drgań rozciągających C H. Powodem znacznego poszerzenia pasma drgań rozciągających grupy OH są silne wiązania wodorowe obecne w dimerach kwasów karboksylowych. Pasmo drgań rozciągających grupy C=O kwasów karboksylowych pojawia się pomiędzy cm -1. Dokładna pozycja tego pasma zależy od tego czy kwas jest nasycony czy nienasycony, zdimeryzowany czy zasocjowany w inny sposób. Pasmo C O pojawia się w obszarze cm -1, a pasmo deformacyjne grupy O H około cm -1 i cm -1. Jednakże pasma w obszarze cm -1 mogą nie dać się rozróżnić od pasm zginających C H, które występują również w tym samym obszarze częstości. Streszczenie: O H rozciągające cm -1 C=O rozciągające cm -1 C O rozciągające cm -1 O H zginające i cm -1 Poniżej pokazane jest widmo kwasu heksanowego. Zwróćmy uwagę, że pasmo drgań rozciągających O H nałożone jest na pasma drgań rozciągających C H. Pasma rozciągające C=O (1721 cm -1 ), rozciągające C O (1296 cm -1 ), zginające O H (1419, 948 cm -1 ), i rozciągające C O (1296 cm -1 ) są również obecne. 18
19 19
20 Estry Drgania rozciągające C=O estrów alifatycznych pojawiają się w zakresie cm -1 ; a w przypadku α, β-nienasyconych estrów pojawia się w zakresie cm -1. Drgania rozciągające C O pojawiają się jako dwa lub więcej pasm absorpcyjnych w obszarze cm -1. Podsumowanie: C=O rozciągające o alifatyczne cm -1 o α, β-nienasycone cm -1 C O rozciągające cm -1 Poniżej znajdują się widma octanu etylu i benzoesanu etylu. Pasmo drgań rozciągających C=O octanu etylu (1752 cm -1 ) leży przy wyższych liczbach falowych niż pasmo karbonylowe benzoesanu etylu (1726 cm -1 ). W zakresie cm -1 występują pasma drgań rozciągających C-O. 20
21 21
22 Aminy Drgania rozciągające N H amin pojawiają się w obszarze cm -1. Pasma te są słabsze i ostrzejsze niż w przypadku alkoholi, dla których obserwuje się absorpcję O-H w tym samym zakresie. Aminy pierwszorzędowe (RNH 2 ) dają dwa pasma asymetryczne i symetryczne rozciągające N H. Drugorzedowe aminy (R 2 NH) dają tylko jedno słabe pasmo N H w obszarze cm -1. Aminy trzeciorzędowe (R 3 N) nie dają pasm absorpcyjnych w tym obszarze, ponieważ nie posiadają wiązania N H. (Bardzo często w widmach ciekłych amin pierwszo i drugorzędowych pojawia się brzegowe pasmo po stronie niższych liczb falowych, pochodzące od nadtonu drgania zginającego N H patrz widmo aniliny). Pasmo drgań deformacyjnych N H amin pierwszorzędowych obserwowane jest w obszarze cm -1. Zazwyczaj aminy drugorzędowe nie dają pasm w tym obszarze a trzeciorzędowe aminy nigdy nie dają pasm w tym zakresie. (Pasmo to może być bardzo ostre i leżeć blisko pasma karbonylowego, co może być utrudnieniem w interpretacji widma). Kolejne pasma charakterystyczne dla amin pojawiają się w obszarze cm -1. Pasmo to pochodzi od deformacyjnych drgań grupy N H i charakteryzuje się tym, że jest intensywne i szerokie. Obserwowane jest tylko w aminach pierwszo i drugorzędowych. Pasma drgań rozciągających C N amin alifatycznych są średnio intensywne lub słabe i pojawiają się w obszarze cm -1. Aminy aromatyczne zazwyczaj dają bardzo intensywne pasmo w obszarze cm -1. Podsumowanie: N H rozciągające cm -1 o 1 aminy: dwa pasma i cm -1 o 2 aminy: jedno pasmo cm -1 o 3 aminy: brak pasm w tym obszarze N H zginające (tylko aminy pierwszorzędowe) cm -1 C N rozciągające (aminy aromatyczne) cm -1 C N rozciągające (aminy alifatyczne) cm -1 N H kołyszące (tylko aminy pierwszo i drugorzędowe) cm -1 22
23 Poniżej pokazane jest widmo aniliny. Ta pierwszorzędowa amina daje pasma drgań rozciągających N-H (3442, 3360 cm -1 ); widoczne jest również pasmo brzegowe pochodzące od natonu drgania zginającego N H. Pasmo drgań rozciągających C N pojawia się przy 1281 cm -1. Również pasmo zginające N H jest obecne przy 1619 cm
24 W widmie aminy drugorzędowej dietyloaminy widzimy tylko jedno pasmo drgań rozciągających N H (3288 cm -1 ). Dranie rozciągające C N występuje przy 1143 cm -1, a dla amin alifatycznych ( cm -1 ). Dietylamina daje również pasmo drgań kołyszących N H (733 cm -1 ). 24
25 Amina trzeciorzędowa trietylamina nie posiada wiązań N H i nie daje takich pasm absorpcyjnych zarówno rozciągających jak i kołyszących. Drgania rozciągające C N pojawiają się przy 1214 cm -1 (niearomatyczne). 25
26 Związki zawierające grupy nitrowe Drgania rozciągające N O w nitroalkanach występują ok 1550 cm -1 (asymetryczne) i 1365 cm -1 (symetryczne). Pasmo przy 1550 cm -1 odznacza się większą intensywnością. Jeżeli grupa nitrowa jest połączona z pierścieniem aromatycznym to drganie rozciągające N O jest przesunięte do niższych częstości: cm -1 i cm -1. Podsumowanie: N O asymetryczne rozciągające cm -1 N O symetryczne rozciągające cm -1 Poniżej znajdują się widma nitrometanu i m-nitrotoluenu. W nitrometanie pasmo rozciągające N O znajduje sie przy 1573 i 1383 cm -1, podczas gdy w nitrotoluenie jest przesunięte trochę na prawo i 1358 cm
27 27
Jak analizować widmo IR?
 Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia molekularna. Spektroskopia w podczerwieni
 Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
SPEKTROSKOPIA W PODCZERWIENI
 SPEKTROSKOPIA W PODCZERWIENI Obszar widma elektromagnetycznego ( od ok. 14000 do 200cm-1 ) między obszarem widzialnym a mikrofalowym nazywamy podczerwienią (IR). W określeniu struktury związków organicznych
SPEKTROSKOPIA W PODCZERWIENI Obszar widma elektromagnetycznego ( od ok. 14000 do 200cm-1 ) między obszarem widzialnym a mikrofalowym nazywamy podczerwienią (IR). W określeniu struktury związków organicznych
Spektroskopia. Spotkanie pierwsze. Prowadzący: Dr Barbara Gil
 Spektroskopia Spotkanie pierwsze Prowadzący: Dr Barbara Gil Temat rozwaŝań Spektroskopia nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na
Spektroskopia Spotkanie pierwsze Prowadzący: Dr Barbara Gil Temat rozwaŝań Spektroskopia nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na
SPEKTROSKOPIA W PODCZERWIENI
 SPEKTROSKOPIA W PODCZERWIENI Rys. 1 Zakres widma elektromagnetycznego. Obszar widma elektromagnetycznego o liczbie falowej (odwrotność długości fali) od ok. 14000 do 200cm-1 między obszarem widzialnym
SPEKTROSKOPIA W PODCZERWIENI Rys. 1 Zakres widma elektromagnetycznego. Obszar widma elektromagnetycznego o liczbie falowej (odwrotność długości fali) od ok. 14000 do 200cm-1 między obszarem widzialnym
Widma w podczerwieni (IR)
 Spektroskopowe metody identyfikacji związków organicznych Widma w podczerwieni (IR) dr 2 Widmo w podczerwieni Liczba drgań zależy od liczby atomów w cząsteczce: cząsteczka nieliniowa o n atomach ma 3n-6
Spektroskopowe metody identyfikacji związków organicznych Widma w podczerwieni (IR) dr 2 Widmo w podczerwieni Liczba drgań zależy od liczby atomów w cząsteczce: cząsteczka nieliniowa o n atomach ma 3n-6
KARTA PRACY DO ZADANIA 1. Pomiar widma aminokwasu na spektrometrze FTIR, model 6700.
 KARTA PRACY D ZADANIA 1 Pomiar widma aminokwasu na spektrometrze FTIR, model 6700. Wykonaj zadanie zgodnie z instrukcją nr 1 i wypełnij tabelę (w odpowiednich komórkach wstaw "X"). ZAKRES SPEKTRALNY ZMIERZNEG
KARTA PRACY D ZADANIA 1 Pomiar widma aminokwasu na spektrometrze FTIR, model 6700. Wykonaj zadanie zgodnie z instrukcją nr 1 i wypełnij tabelę (w odpowiednich komórkach wstaw "X"). ZAKRES SPEKTRALNY ZMIERZNEG
PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR
 PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR WSTĘP Metody spektroskopowe Spektroskopia bada i teoretycznie wyjaśnia oddziaływania pomiędzy materią będącą zbiorowiskiem
PRODUKTY CHEMICZNE Ćwiczenie nr 3 Oznaczanie zawartości oksygenatów w paliwach metodą FTIR WSTĘP Metody spektroskopowe Spektroskopia bada i teoretycznie wyjaśnia oddziaływania pomiędzy materią będącą zbiorowiskiem
Podczerwień bliska: cm -1 (0,7-2,5 µm) Podczerwień właściwa: cm -1 (2,5-14,3 µm) Podczerwień daleka: cm -1 (14,3-50 µm)
 SPEKTROSKOPIA W PODCZERWIENI Podczerwień bliska: 14300-4000 cm -1 (0,7-2,5 µm) Podczerwień właściwa: 4000-700 cm -1 (2,5-14,3 µm) Podczerwień daleka: 700-200 cm -1 (14,3-50 µm) WIELKOŚCI CHARAKTERYZUJĄCE
SPEKTROSKOPIA W PODCZERWIENI Podczerwień bliska: 14300-4000 cm -1 (0,7-2,5 µm) Podczerwień właściwa: 4000-700 cm -1 (2,5-14,3 µm) Podczerwień daleka: 700-200 cm -1 (14,3-50 µm) WIELKOŚCI CHARAKTERYZUJĄCE
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Zastosowanie spektroskopii w podczerwieni w jakościowej i ilościowej analizie organicznej
 Zastosowanie spektroskopii w podczerwieni w jakościowej i ilościowej analizie organicznej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie
Zastosowanie spektroskopii w podczerwieni w jakościowej i ilościowej analizie organicznej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie
IR I 11. IDENTYFIKACJA GRUP FUNKCYJNYCH W WIDMACH IR
 IR I 11. IDENTYFIKACJA GRUP FUNKCYJNYCH W WIDMACH IR Celem ćwiczenia jest zapoznanie się z techniką wykonywania widm związków w postaci pastylek wykonanych z bromku potasu oraz interpretacja otrzymanych
IR I 11. IDENTYFIKACJA GRUP FUNKCYJNYCH W WIDMACH IR Celem ćwiczenia jest zapoznanie się z techniką wykonywania widm związków w postaci pastylek wykonanych z bromku potasu oraz interpretacja otrzymanych
FIZYKOCHEMICZNE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH. Witold Danikiewicz
 FIZYKOCEMICZNE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYC Witold Danikiewicz Instytut Chemii Organicznej PAN ul. Kasprzaka 44/52, 01-224 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli
FIZYKOCEMICZNE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYC Witold Danikiewicz Instytut Chemii Organicznej PAN ul. Kasprzaka 44/52, 01-224 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli
spektroskopia IR i Ramana
 spektroskopia IR i Ramana oscylacje (wibracje) 3N-6 lub 3N-5 drgań normalnych nie wszystkie drgania obserwuje się w IR - nieaktywne w IR gdy nie zmienia się moment dipolowy - pasma niektórych drgań mają
spektroskopia IR i Ramana oscylacje (wibracje) 3N-6 lub 3N-5 drgań normalnych nie wszystkie drgania obserwuje się w IR - nieaktywne w IR gdy nie zmienia się moment dipolowy - pasma niektórych drgań mają
Zastosowanie spektroskopii w podczerwieni w analizie jakościowej i ilościowej. dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB
 Zastosowanie spektroskopii w podczerwieni w analizie jakościowej i ilościowej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie Promieniowanie
Zastosowanie spektroskopii w podczerwieni w analizie jakościowej i ilościowej dr Alina Dubis Zakład Chemii Produktów Naturalnych Instytut Chemii UwB Tematyka Spektroskopia - podział i zastosowanie Promieniowanie
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
PODSTAWY METODY SPEKTROSKOPI W PODCZERWIENI ABSORPCJA, EMISJA
 PODSTAWY METODY SPEKTROSKOPI W PODCZERWIENI ABSORPCJA, EMISJA Materia może oddziaływać z promieniowaniem poprzez absorpcję i emisję. Procesy te polegają na pochłonięciu lub wyemitowaniu fotonu przez cząstkę
PODSTAWY METODY SPEKTROSKOPI W PODCZERWIENI ABSORPCJA, EMISJA Materia może oddziaływać z promieniowaniem poprzez absorpcję i emisję. Procesy te polegają na pochłonięciu lub wyemitowaniu fotonu przez cząstkę
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR
 Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w położeniu co najmniej jeden atom wodoru mogą ulegać enolizacji przez przesunięcie protonu
Ćwiczenie 3 Pomiar równowagi keto-enolowej metodą spektroskopii IR i NMR 1. Wstęp Związki karbonylowe zawierające w położeniu co najmniej jeden atom wodoru mogą ulegać enolizacji przez przesunięcie protonu
Analiza Organiczna. Jan Kowalski grupa B dwójka 7(A) Własności fizykochemiczne badanego związku. Zmierzona temperatura topnienia (1)
 Przykład sprawozdania z analizy w nawiasach (czerwonym kolorem) podano numery odnośników zawierających uwagi dotyczące kolejnych podpunktów sprawozdania Jan Kowalski grupa B dwójka 7(A) analiza Wynik przeprowadzonej
Przykład sprawozdania z analizy w nawiasach (czerwonym kolorem) podano numery odnośników zawierających uwagi dotyczące kolejnych podpunktów sprawozdania Jan Kowalski grupa B dwójka 7(A) analiza Wynik przeprowadzonej
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
IDENTYFIKACJA ZWIĄZKÓW ORGANICZNYCH METODAMI SPEKTROSKOPOWYMI SPEKTROSKOPIA W PODCZERWIENI (IR)
 IDENTYFIKACJA ZWIĄZKÓW ORGANICZNYC METODAMI SPEKTROSKOPOWYMI SPEKTROSKOPIA W PODCZERWIENI (IR) Metodą o bardzo dużym znaczeniu w organicznej analizie strukturalnej jest spektroskopia w podczerwieni (spektroskopia
IDENTYFIKACJA ZWIĄZKÓW ORGANICZNYC METODAMI SPEKTROSKOPOWYMI SPEKTROSKOPIA W PODCZERWIENI (IR) Metodą o bardzo dużym znaczeniu w organicznej analizie strukturalnej jest spektroskopia w podczerwieni (spektroskopia
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem
 Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Spektroskopowe metody identyfikacji związków organicznych
 Spektroskopowe metody identyfikacji związków organicznych Wstęp Spektroskopia jest metodą analityczną zajmującą się analizą widm powstających w wyniku oddziaływania promieniowania elektromagnetycznego
Spektroskopowe metody identyfikacji związków organicznych Wstęp Spektroskopia jest metodą analityczną zajmującą się analizą widm powstających w wyniku oddziaływania promieniowania elektromagnetycznego
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne. Z CHEMII W KLASIE III gimnazjum
 WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE III gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE III gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
I. Węgiel i jego związki z wodorem
 NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH
 ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR
 Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR Szczególnym i bardzo charakterystycznym rodzajem oddziaływań międzycząsteczkowych jest wiązanie wodorowe. Powstaje ono między molekułami,
Ćwiczenie 2 Przejawy wiązań wodorowych w spektroskopii IR i NMR Szczególnym i bardzo charakterystycznym rodzajem oddziaływań międzycząsteczkowych jest wiązanie wodorowe. Powstaje ono między molekułami,
POŁOŻENIA SYGNAŁÓW PROTONÓW POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA
 POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Spektrometria w bliskiej podczerwieni - zastosowanie w cukrownictwie. Radosław Gruska Politechnika Łódzka Wydział Biotechnologii i Nauk o Żywności
 Spektrometria w bliskiej podczerwieni - zastosowanie w cukrownictwie Radosław Gruska Politechnika Łódzka Wydział Biotechnologii i Nauk o Żywności Spektroskopia, a spektrometria Spektroskopia nauka o powstawaniu
Spektrometria w bliskiej podczerwieni - zastosowanie w cukrownictwie Radosław Gruska Politechnika Łódzka Wydział Biotechnologii i Nauk o Żywności Spektroskopia, a spektrometria Spektroskopia nauka o powstawaniu
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA
 CHEMIA KLASA III 2016-09-01 LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA Treści nauczania Tom III podręcznika Ciekawi świata wyd. Operon I. WĘGLOWODORY 1. Chemia organiczna jako chemia związków
CHEMIA KLASA III 2016-09-01 LICEUM OGÓLNOKSZTAŁCĄCE ZAKRES ROZSZERZONY SZKOŁY BENEDYKTA Treści nauczania Tom III podręcznika Ciekawi świata wyd. Operon I. WĘGLOWODORY 1. Chemia organiczna jako chemia związków
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
Akademia Górniczo-Hutnicza Wydział Inżynierii Materiałowej i Ceramiki Katedra Chemii Krzemianów i Związków Wielkocząsteczkowych
 Akademia Górniczo-Hutnicza Wydział nżynierii Materiałowej i Ceramiki Katedra Chemii Krzemianów i Związków Wielkocząsteczkowych nstrukcja do ćwiczeń laboratoryjnych Kierunek studiów: Technologia chemiczna
Akademia Górniczo-Hutnicza Wydział nżynierii Materiałowej i Ceramiki Katedra Chemii Krzemianów i Związków Wielkocząsteczkowych nstrukcja do ćwiczeń laboratoryjnych Kierunek studiów: Technologia chemiczna
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej
 Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne:
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Br Br. Br Br OH 2 OH NH NH 2 2. Zakład Chemii Organicznej: kopiowanie zabronione
 Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Wymagania edukacyjne z chemii dla klasy 3b. Gimnazjum Publicznego im. Jana Pawła II w Żarnowcu. na rok szkolny 2015/2016
 Wymagania edukacyjne z chemii dla klasy 3b Gimnazjum Publicznego im. Jana Pawła II w Żarnowcu na rok szkolny 2015/2016 Nauczyciel: mgr Joanna Szasta Węgiel i jego związki z wodorem definiuje pojęcia: chemia
Wymagania edukacyjne z chemii dla klasy 3b Gimnazjum Publicznego im. Jana Pawła II w Żarnowcu na rok szkolny 2015/2016 Nauczyciel: mgr Joanna Szasta Węgiel i jego związki z wodorem definiuje pojęcia: chemia
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
Skala ocen: ndst 0 20, dst , dst , db , db , bdb Informacja:
 Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Zastosowania spektroskopii Ramana
 dr inż. Beata Brożek-Płuska Politechnika Łódzka, Wydział Chemiczny, Międzyresortowy Instytut Techniki Radiacyjnej, Laboratorium Laserowej Spektroskopii Molekularnej WYKŁAD 8 Zastosowanie spektroskopii
dr inż. Beata Brożek-Płuska Politechnika Łódzka, Wydział Chemiczny, Międzyresortowy Instytut Techniki Radiacyjnej, Laboratorium Laserowej Spektroskopii Molekularnej WYKŁAD 8 Zastosowanie spektroskopii
Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1.
 1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
Metody spektroskopowe w identyfikacji związków organicznych. Barbara Guzowska-Świder Zakład Informatyki Chemicznej, PRz
 Metody spektroskopowe w identyfikacji związków organicznych Barbara Guzowska-Świder Zakład Informatyki Chemicznej, PRz Metody spektralne wykorzystują zjawiska związane z oddziaływaniem materii z promieniowaniem
Metody spektroskopowe w identyfikacji związków organicznych Barbara Guzowska-Świder Zakład Informatyki Chemicznej, PRz Metody spektralne wykorzystują zjawiska związane z oddziaływaniem materii z promieniowaniem
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Analiza instrumentalna Wykład nr 3
 Analiza instrumentalna Wykład nr 3 KT2_2 brak zajęć lab. w dniu 18.10.2012 SPEKTROSKOPIA IR SPKTROSKOPIA RAMANA WIDMO OSCYLACYJNE Zręby atomowe w molekule wykonują oscylacje wokół położenia równowagi.
Analiza instrumentalna Wykład nr 3 KT2_2 brak zajęć lab. w dniu 18.10.2012 SPEKTROSKOPIA IR SPKTROSKOPIA RAMANA WIDMO OSCYLACYJNE Zręby atomowe w molekule wykonują oscylacje wokół położenia równowagi.
Spektroskopia masowa Materiały do ćwiczeń
 Uniwersytet Jagielloński, Collegium Medicum Katedra Chemii Organicznej Spektroskopia masowa Materiały do ćwiczeń Kraków 2011 2 Spis treści Wstęp 2 Budowa spektrometru masowego 2 Układ wprowadzenia próbki
Uniwersytet Jagielloński, Collegium Medicum Katedra Chemii Organicznej Spektroskopia masowa Materiały do ćwiczeń Kraków 2011 2 Spis treści Wstęp 2 Budowa spektrometru masowego 2 Układ wprowadzenia próbki
IDENTYFIKACJA JAKOŚCIOWA NIEZNANEGO ZWIĄZKU ORGANICZNEGO
 IDENTYFIKACJA JAKOŚCIOWA NIEZNANEGO ZWIĄZKU ORGANICZNEGO Schemat raportu końcowego w ramach ćwiczeń laboratoryjnych z przedmiotu Badanie struktury związków organicznych 1. Symbol kodujący identyfikowaną
IDENTYFIKACJA JAKOŚCIOWA NIEZNANEGO ZWIĄZKU ORGANICZNEGO Schemat raportu końcowego w ramach ćwiczeń laboratoryjnych z przedmiotu Badanie struktury związków organicznych 1. Symbol kodujący identyfikowaną
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ
 FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów.
 Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów. Wprowadzenie teoretyczne Cel ćwiczeń: Poznanie metod otrzymywania oraz badania właściwości węglowodorów alifatycznych
Ćwiczenie 3. Otrzymywanie i badanie właściwości chemicznych alkanów, alkenów, alkinów i arenów. Wprowadzenie teoretyczne Cel ćwiczeń: Poznanie metod otrzymywania oraz badania właściwości węglowodorów alifatycznych
WĘGLOWODORY, ALKOHOLE, FENOLE. I. Wprowadzenie teoretyczne
 WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Plan wynikowy z chemii poziom rozszerzony na rok szkolny 2015/2016 dla klasy III b
 Plan wynikowy z chemii poziom rozszerzony na rok szkolny 2015/2016 dla klasy III b Nauczyciel prowadzący: Dorota Foszczyńska Liczba tygodni nauki: 30 Liczba godzin w tygodniu: 4 Liczba godzin do wypracowania
Plan wynikowy z chemii poziom rozszerzony na rok szkolny 2015/2016 dla klasy III b Nauczyciel prowadzący: Dorota Foszczyńska Liczba tygodni nauki: 30 Liczba godzin w tygodniu: 4 Liczba godzin do wypracowania
Plan wynikowy do serii Chemia Nowej Ery - klasa 3
 Plan wynikowy do serii Chemia Nowej Ery - klasa 3 Na podstawie Programu nauczania chemii w gimnazjum autorstwa Teresy Kulawik i Marii Litwin oraz Wymagań programowych na poszczególne oceny przygotowanych
Plan wynikowy do serii Chemia Nowej Ery - klasa 3 Na podstawie Programu nauczania chemii w gimnazjum autorstwa Teresy Kulawik i Marii Litwin oraz Wymagań programowych na poszczególne oceny przygotowanych
WYMAGANIA EDUKACYJNE
 GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie III GIMNAZJUM Wymagania edukacyjne niezbędne do uzyskania
GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie III GIMNAZJUM Wymagania edukacyjne niezbędne do uzyskania
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Plan wynikowy i wymagania edukacyjne w klasie 3 gimnazjum. Węgiel i jego związki z wodorem. Wymagania edukacyjne. Tytuł rozdziału w podręczniku
 1 Plan wynikowy i wymagania edukacyjne w klasie 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z
1 Plan wynikowy i wymagania edukacyjne w klasie 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z
Wymagania edukacyjne chemia klasa 3 gimnazjum. Węgiel i jego związki z wodorem. Wymagania edukacyjne. Tytuł rozdziału w podręczniku
 1 Wymagania edukacyjne chemia klasa 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy
1 Wymagania edukacyjne chemia klasa 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy
Przedmiotowy system oceniania dla uczniów z obowiązkiem dostosowania wymagań z chemii kl. III
 Chemia klasa III - wymagania programowe opracowane na podstawie przewodnika dla nauczycieli opublikowanego przez wydawnictwo OPERON I. Węgiel I jego związki z wodorem Wymagania na ocenę dopuszczającą -
Chemia klasa III - wymagania programowe opracowane na podstawie przewodnika dla nauczycieli opublikowanego przez wydawnictwo OPERON I. Węgiel I jego związki z wodorem Wymagania na ocenę dopuszczającą -
Przedmiotowy system oceniania z chemii kl. III
 Chemia klasa III - wymagania programowe opracowane na podstawie przewodnika dla nauczycieli opublikowanego przez wydawnictwo OPERON I. Węgiel I jego związki z wodorem Wymagania na ocenę dopuszczającą -
Chemia klasa III - wymagania programowe opracowane na podstawie przewodnika dla nauczycieli opublikowanego przez wydawnictwo OPERON I. Węgiel I jego związki z wodorem Wymagania na ocenę dopuszczającą -
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna
 Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Podział związków organicznych
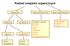 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
CHEMIA KLASA Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
1. Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
MIKROANALIZY WĘGLOWODORY. W1 Utlenianie węglowodorów nadmanganianem potasu w środowisku kwaśnym (w temp. pokojowej) RÓWNANIA REAKCJI: OBSERWACJE:
 MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Spektroskopowe metody identyfikacji związków organicznych / Robert. Spis treści
 Spektroskopowe metody identyfikacji związków organicznych / Robert M. Silverstein, Francis X. Webster, David J. Kiemle. wyd. 2, dodr. 4. - Warszawa, 2012 Spis treści ROZDZIAŁ 1 SPEKTROMETRIA MAS 1 1.1
Spektroskopowe metody identyfikacji związków organicznych / Robert M. Silverstein, Francis X. Webster, David J. Kiemle. wyd. 2, dodr. 4. - Warszawa, 2012 Spis treści ROZDZIAŁ 1 SPEKTROMETRIA MAS 1 1.1
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania programowe na poszczególne oceny z chemii w klasie III.
 Wymagania programowe na poszczególne oceny z chemii w klasie III. VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania programowe na poszczególne oceny z chemii w klasie III. VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/55/35935976.jpg) KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wymagania edukacyjne na poszczególne stopnie szkolne z chemii w klasie III.
 Wymagania edukacyjne na poszczególne stopnie szkolne z chemii w klasie III. Stopień dopuszczający: podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania edukacyjne na poszczególne stopnie szkolne z chemii w klasie III. Stopień dopuszczający: podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
Wymagania programowe na poszczególne oceny. Klasa 3 I semestr
 Wymagania programowe na poszczególne oceny. Klasa 3 I semestr VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania programowe na poszczególne oceny. Klasa 3 I semestr VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania programowe na poszczególne oceny CHEMIA klasa III
 Wymagania programowe na poszczególne oceny CHEMIA klasa III I. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania programowe na poszczególne oceny CHEMIA klasa III I. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
KLASA TRZECIA. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów. Wymagania edukacyjne. Tytuł rozdziału w podręczniku
 1 KLASA TRZECIA Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania Wymagania edukacyjne podstawowe (P) ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła 2.1. Szereg
1 KLASA TRZECIA Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania Wymagania edukacyjne podstawowe (P) ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła 2.1. Szereg
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony.
 WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
KARTA KURSU. Student posiada podstawową wiedzę z zakresu fizyki, matematyki i chemii nieorganicznej.
 Kierunek, stopień, tok studiów, rok akademicki, semestr Biologia, licencjat, studia stacjonarne, 2017/2018, II KARTA KURSU Nazwa Chemia organiczna I Nazwa w j. ang. Koordynator dr Waldemar Tejchman Zespół
Kierunek, stopień, tok studiów, rok akademicki, semestr Biologia, licencjat, studia stacjonarne, 2017/2018, II KARTA KURSU Nazwa Chemia organiczna I Nazwa w j. ang. Koordynator dr Waldemar Tejchman Zespół
Alkohole i fenole. Opracowanie: Bartłomiej SIEPSIAK klasa 3d Opiekun: p. Teresa Gębicka
 Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19. Chemia organiczna jako chemia związków węgla
 Jarosław Kuśnierz WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19 Chemia organiczna jako chemia związków węgla Ocena dopuszczająca [1] pojęcie chemii organicznej pierwiastki chemiczne wchodzące w skład
Jarosław Kuśnierz WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19 Chemia organiczna jako chemia związków węgla Ocena dopuszczająca [1] pojęcie chemii organicznej pierwiastki chemiczne wchodzące w skład
Wymagania programowe na poszczególne oceny
 Przedmiot: chemia Klasa: IIIa, IIIb Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną
Przedmiot: chemia Klasa: IIIa, IIIb Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
Ocenę niedostateczną otrzymuje uczeń, który: Ocenę dopuszczającą otrzymuje uczeń, który: Ocenę dostateczną otrzymuje uczeń, który:
 Kryteria oceniania z chemii dla klasy 3A i 3B Gimnazjum w Borui Kościelnej Rok szkolny: 2015/2016 Semestr: pierwszy Opracowała: mgr Krystyna Milkowska, mgr inż. Malwina Beyga Ocenę niedostateczną otrzymuje
Kryteria oceniania z chemii dla klasy 3A i 3B Gimnazjum w Borui Kościelnej Rok szkolny: 2015/2016 Semestr: pierwszy Opracowała: mgr Krystyna Milkowska, mgr inż. Malwina Beyga Ocenę niedostateczną otrzymuje
Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz:
 Wymagania z chemii na poszczególne oceny Klasa 3 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Potrafią wykryć obecność węgla i wodoru w związkach
Wymagania z chemii na poszczególne oceny Klasa 3 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Potrafią wykryć obecność węgla i wodoru w związkach
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony
 CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY
 WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wymagania edukacyjne z chemii dla klasy III
 Wymagania edukacyjne z chemii dla klasy III VII. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania edukacyjne z chemii dla klasy III VII. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Węgiel i jego związki z wodorem
 Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia
Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia
CHEMIA ORGANICZNA CHEMIA ORGANICZNA CHEMIA ZWIĄZKÓW PIERWIASTKA WĘGLA TLENEK WĘGLA (IV) KWAS WĘGLOWY + SOLE KWASU WĘGLOWEGO
 CHEMIA ORGANICZNA CHEMIA ORGANICZNA CHEMIA ZWIĄZKÓW PIERWIASTKA WĘGLA WYJĄTKI: TENEK WĘGLA(II) TLENEK WĘGLA (IV) KWAS WĘGLOWY + SOLE KWASU WĘGLOWEGO KLASYFIKACJA ZWIĄZKÓW ORGANICZNYCH KLASYFIKACJA ZWIĄZKÓW
CHEMIA ORGANICZNA CHEMIA ORGANICZNA CHEMIA ZWIĄZKÓW PIERWIASTKA WĘGLA WYJĄTKI: TENEK WĘGLA(II) TLENEK WĘGLA (IV) KWAS WĘGLOWY + SOLE KWASU WĘGLOWEGO KLASYFIKACJA ZWIĄZKÓW ORGANICZNYCH KLASYFIKACJA ZWIĄZKÓW
WĘGLOWODORY. Uczeń: Przykłady wymagań nadobowiązkowych Uczeń:
 WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum
 Lucyna Krupa Rok szkolny 2018/2019 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2018/2019 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
