TERMODYNAMIKA PROCESOWA I TECHNICZNA
|
|
|
- Franciszek Urbaniak
- 7 lat temu
- Przeglądów:
Transkrypt
1 TERMODYNAMIKA PROCESOWA I TECHNICZNA Wyład VII Roztory Defncje onencje Welośc meszana Roztory dealne Welośc cząstoe Rónana stanu dla roztoró Rónoaga fazoa Praa Raoulta Henry ego Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
2 ROZTWORY Defncje onencje Roztorem nazyamy meszannę co najmnej du zązó chemcznych torzących jednorodną fazę. Substancje torzące roztór nazyamy sładnam. Poszczególne sładn będzemy oznaczać lczbam naturalnym:, 2, 3,...,,...,. W ogólnym przypadu będzemy rozażać roztory sładnoe. Ilośc poszczególnych sładnó yrażone jednostach masy [g] lub lcznośc [mol] oreślają sład roztoru: m,m 2,m 3,...,m,...,m n,n 2, n 3,...,n,...,n Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 2
3 ROZTWORY Defncje onencje cd. Sład roztoru oreślają elośc estensyne. W pratyce ygodnej jest operoać eloścam ntensynym, tórym są zajemne stosun loścoe nazyane stężenam. Istneje ele różnych systemó stężeń. Najczęścej stosoane są: ułam moloe masoe oraz oncentracje objętoścoe popularne oreślane jao stężena moloe. Ponżej przedstaono odpoedne defncje: Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 3
4 ROZTWORY Defncje onencje cd.. Ułame moloy sładna n n n j n j Wymarem ułama moloego jest lomol / olomol rozt. Często jedna przyjmuje sę, że ułame moloy jest bezymaroy bądź mnoży sę jego artość przez oreśla tz. % mol. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 4
5 ROZTWORY Defncje onencje cd. 2. Ułame masoy sładna m m m j m j Wymarem ułama masoego jest logram / ologram rozt. Często jedna przyjmuje sę, że ułame masoy jest bezymaroy bądź mnoży sę jego artość przez oreśla tz. % mas. Tradycyjne przyjęło sę, że ułam moloy masoy sładnó roztorze gazoym oznacza sę lterą y. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 5
6 ROZTWORY Defncje onencje cd. 3. Koncentracja (stężene moloa sładna c n V 4. Koncentracja (stężene masoa sładna c c n V c m V c c m V Wszyste elośc oreślające ułam bądź oncentracje są eloścam ntensynym. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 6
7 ROZTWORY Defncje onencje cd. Welośc (zaróno estensyne ja ntensyne, tóre będą sę odnosły do -tego sładna będzemy oznaczać ndesem dolnym. Welośc bez dolnych ndesó będą dotyczyły całego roztoru. Jeżel dolnemu ndeso będze toarzyszył górny ndes będze to oznaczało elość charaterystyczną dla czystego sładna ( tej samej temperaturze pod tym samym cśnenem. Górny ndes M będze oznaczał tz. elość meszana (całego roztoru lub cząstoą sładna. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 7
8 ROZTWORY Defncje onencje cd. Rozpatrzmy symbolczne proces torzena roztoru. Będzemy załadać, że poszczególne sładn ne reagują ze sobą a temperatura cśnene są stałe tzn. p=const., T=const.W dalszym cągu będzemy rozażać doolną estensyną funcję stanu W. n n 2 n n n=σn = Roztór W = n W 2 = 2 n 2 W = n W = n W n W W=f(T,p,n,n 2,...n =. n ( n, n 2 Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej,... n W poyższej relacj możemy meć do czynena z rónoścą lub nerónoścą. Możlość ystąpena nerónośc jest podstaą do defncj tz. elośc meszana. 8
9 ROZTWORY Welośc meszana T=const., p=const. Rozpatrzmy doolną elość estensyną będącą funcją stanu W. Przed zmeszanem ażdy sładn charateryzoał sę artoścą: W = n. Po utorzenu roztoru cały roztór jest oreślony za pomocą: W=f(n,n 2,...n. Weloścą meszana roztoru W M nazyamy elość oreśloną zorem defncyjnym: W M def W W T const. pconst. Słone elość meszana W M jest to zrost lub spade artośc danej funcj stanu dla roztoru stosunu do prostej sumy charaterystycznej dla czystych sładnó przed zmeszanem ( tej samej temperaturze pod tym samym cśnenem. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 9
10 ROZTWORY Welośc meszana cd. Najczęścej stosoane elośc meszana to: objętość meszana, entalpa meszana entropa meszana. Objętość meszana jest na ogół ujemna, co oznacza że roztór zmnejsza soją objętość porónanu z sumą objętośc sładnó czystych. Dobrym przyładem taego roztoru jest uład etanol oda. Entalpa meszana zgodne z I zasadą termodynam jest róna tz. cepłu meszana: M H Q M Q M lość cepła tórą trzeba doproadzć do uładu aby czyste sładn utorzyły dany roztór (pod stałym cśnenem stałej temperaturze. Na ogół entalpa meszana róneż jest artoścą ujemną co oznacza, że podczas torzena roztoru ydzela sę pena lość cepła. W przeceńste do objętośc entalp, entropa meszana na ogół jest dodatna. Wyna to z II zasady termodynam fatu że torzene roztoru jest przemaną neodracalną. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
11 Roztory dealne Pojęce roztoró dealnych jest bardzo ażne gdyż proadza peen punt odnesena gdze różne łasnośc są szczególne proste. Pojęce to jest róneż podstaą do defncj tz. funcj nadmaroych, tóre są bardzo pomocne modeloanu np. rónoag fazoych. Roztorem dealnym nazyamy roztór spełnający da arun: V M,( RI H M,( RI Potrójne res oznaczają, że rónośc poyższe muszą oboązyać nezależne od sładu roztoru nezależne od temperatury cśnena. Słone defncja ta oznacza, że roztór dealny ne zmena an objętośc an entalp podczas postaana z czystych sładnó. Drug arune oznacza, że przy stałym cśnenu efet ceplny torzena roztoru dealnego jest róny. Perszy arune tzn. bra objętośc meszana jest czasam oreślany jao prao Amagata. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
12 Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej ROZTWORY Welośc cząstoe W nauce o roztorach bardzo ażne są tz. elośc cząstoe dotyczące poszczególnych sładnó. Ścsła defncja elośc cząstoej sładna jest następująca: n j p T n W,, Znajomość elośc cząstoych sładu roztoru pozala na oblczene danej elośc estensynej: n W
13 ROZTWORY Welośc cząstoe cd. Welośc cząstoe zależą od cśnena temperatury a taże od sładu danego roztoru. Są róneż ścśle zązane z eloścam łaścym czystych sładnó. Dla ustalonego cśnena temperatury można napsać: f (,, 2,...,,..., Funcja poyższa mus spełnać łasnośc granczne: lm lm ( ( Wartość oznacza tz. elość cząstoą roztorze nesończene rozceńczonym. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
14 ROZTWORY Wyznaczane elośc cząstoych cd. W przypadu roztoró rzeczystych często yznaczane elośc cząstoych za pomocą zoru defncyjnego jest trudne. Można natomast na ogół bez problemu yznaczać elośc łaśce roztoru jao funcje sładu. Oazuje sę, że na podstae znajomośc elośc łaścych roztoru można oblczyć szyste elośc cząstoe. Wychodząc ze zoru defncyjnego stosując zasady rachunu różnczoego można otrzymać: W n T, p, n j ( n n T, p, n j n n T, p, n j p, T,,,,,,,,, p T 2 p T p T p T j, j,2 j, j, j, j j j j j Otrzymany zór można zapsać zartej postac: Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
15 ROZTWORY Wyznaczane elośc cząstoych cd. r r, r r r p, T, j, r j Aby sorzystać z poyższego zoru należy dysponoać zależnoścą elośc łaścej od sładu roztoru yrażonego za pomocą ułamó moloych: f (, 2,...,,..., Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
16 Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej ROZTWORY Wyznaczane elośc cząstoych dla roztoró 2 - sładnoych '( ( ( ( 2 2, 2 2 d d d d T p '( ( 2, 2 d d d d T p Otrzymany zór znajduje często zastosoane przypadu roztoró 2 sładnoych (bnarnych, dla tórych =2, =,2 ' / ( d d f d d '( ( '( ( ( 2
17 ROZTWORY Wyznaczane elośc cząstoych dla roztoró 2 - sładnoych 2 ( ( ( '( '( Zastosoane poyższych zoró ymaga znajomośc funcj danej elośc łaścej zależnośc od sładu tym przypadu yrażonego za pomocą ułama moloego sładna. W przypadu gdy zależność ta jest podana postac grafcznej stneje możlość grafcznego yznaczena elośc cząstoych. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
18 ROZTWORY Wyznaczane elośc cząstoych dla roztoró 2 sładnoych cd. ( 2 D E α A C B 2 ( ( ( '( '( 2 ( = 2 = BC d tan ' BC AB' ( ' BC ( BC ( ' AB d DE d tan ' DE DA' ' DE ( 2 2 DE ' DA d -> 2 = = Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
19 ROZTWORY Wyznaczane elośc cząstoych dla roztoró 2 sładnoych cd. Metodą yreślną można róneż yznaczyć elośc cząstoe roztorach nesończene rozceńczonych ( = 2 = -> 2 = = Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
20 ROZTWORY Wyznaczane elośc cząstoych W przypadu gdy daną elość W można yznaczyć esperymentalne, stneje możlość oreślena elośc cząstoych bezpośredno za pomocą dośadczeń oraz zoru defncyjnego: W n T, p, n j lm n W n T const., pconst., n j const. gdze ΔW oznacza zmerzony esperymentalne przyrost artośc W po dodanu do roztoru sładna lośc Δn. Metodę tę można stosoać np. do yznaczana objętośc cząstoych. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
21 ROZTWORY Wyznaczane elośc cząstoych W szczególnych sytuacjach gdy dana elość meszana jest róna, elośc cząstoe są róne eloścom łaścym czystych sładnó ne zależą od sładu roztoru: M W W n n Sytuacja taa ma mejsce przypadu objętośc, entalp energ enętrznej roztoró dealnych. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
22 ROZTWORY Rónana stanu Zależnośc mędzy najażnejszym parametram uładu będącego roztorem opsuje rónane stanu roztoru, tórego ogólna postać jest następująca: F( p, T, V, n, n,..., n 2 Dla uładó zamnętych o ustalonym sładze ygodne jest stosoać postać, tórej ystępują objętość łaśca ułam moloe: F( p, T, v,,,..., 2 Jeżel chodz o onretne postace rónań stanu dla roztoró, to na ogół stosuje sę tae same rónana ja dla sładnó czystych. Podstaoym problemem są tutaj metody yznaczana parametró. Parametry te najczęścej yznacza sę na podstae parametró czystych sładnó za pomocą tz. reguł meszana. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
23 ROZTWORY Rónana stanu cd. Dla roztoru gazó dosonałych oczyśce oboązuje RSGD: pv ( n n... n... n RT 2 Rónane to można zapsać zartej postac: pv n RT nrt Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
24 ROZTWORY Rónana stanu cd. Dla roztoró spełnających prao Amagata można zasadze zastosoać doolne rónane stanu czystych sładnó, pod arunem, że rónane to będze rozązane zględem objętośc: V V gdze V f ( n, p, T Przyładem taego postępoana może być zastosoane rónana ralnego obcętego po drugm yraze: Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
25 Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej ROZTWORY Rónana stanu cd. ( T n B p n RT V gdze V V Wzór oreślający drug spółczynn ralu B(T dla roztoru jest łaśne przyładem prostej reguły meszana. Nestety to proste rozązane ma dosyć ogranczone zastosoane do obszaró tórych można stosoać obcęte rónana ralne z dodatoym założenem stosoalnośc praa Amagata. ( ( ( T n B p nrt T n B n p RT T n B p n RT V B(T p RT n V v T B T B gdze ( (
26 ROZTWORY Rónana stanu cd. Rónana 3 go stopna yodzące sę z rónana van der Waalsa można zapsać ogólnej postac: p( v, T RT a( T v b M ( v, b W rónanach typu van der Waalsa najczęścej ystępują de stałe: - stała a zależna od temperatury opsująca oddzałyana - stała b na ogół nezależna od temperatury opsująca objętość cząstecze. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
27 ROZTWORY Rónana stanu cd. W przypadu roztoró luczoym problemem jest oreślene tych parametró a(t b dla roztoru. W ogólnej sytuacj parametry te zależą od odpoednch parametró czystych substancj sładu roztoru: a( T b f ( b f ( a, b 2, a 2,..., b,..., a,,, 2, 2,...,,..., Konretne postace tych zależnośc nazyamy regułam meszana. Zależnośc te ponny spełnać arun granczne: lm lm a a b b Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
28 ROZTWORY Rónana stanu cd. Najczęścej przypadu rónań 3 go stopna stosoane są tz. adratoe reguły meszana nazyane też regułam van der Waalsa: a( T j j a j a j ( j a ( T a j ( T b b Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
29 RÓWNOWAGA FAZOWA Uag stępne Zagadnene rónoag fazoej ma fundamentalne znaczene opse elu procesó odbyających sę z udzałem du lub ęcej faz, tórych następuje ymana masy mędzy fazam. Przyłady tach procesó: Destylacja retyfacja Absorpcja desorpcja Adsorpcja Estracja Krystalzacja Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 29
30 RÓWNOWAGA FAZOWA Uag stępne Procesy te mogą zachodzć tylo tedy gdy dany uład będze odległy od stanu rónoag. Szybość przebegu tych procesó jest na ogół proporcjonalna do odległośc od stanu rónoag. Zatem, znajomość stanu rónoag jest podstaą do opsu tach procesó. Stany rónoag fazoej najczęścej rozpatruje sę uładach 2 fazoych: destylacja (cecz + para, absorpcja (cecz + gaz, adsorpcja (cało stałe + cecz lub gaz, estracja (cecz + cecz, rystalzacja (cecz + cało stałe. Zagadnene rónoag fazoej rozpatrzymy na przyładze uładu cecz - para. Węszość yproadzonych nosó można bez problemó uogólnć na nne ułady du lub ęcej fazoe. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 3
31 RÓWNOWAGA FAZOWA Uład cecz para (gaz Rozpatrzy uład zamnęty (bez ymany masy z otoczenem sładnoy sładający sę z du faz: cełej paroej. Fazę cełą będzemy oznaczać górnym ndesem L a paroą ndesem V. Para (Gaz n V,n 2V,,n V,,n V y,y 2,,y,,y p V,T V n V n L,2,..., const. Cecz n L,n 2L,,n L,,n L, 2,,,, p L,T L Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 3
32 Warun rónoag fazoej W uładze termodynamcznym dążącym do stanu rónoag tzn. gdy uład jest zoloany od otoczena, mędzy fazam torzącym uład zachodzą procesy ymany energ ceplnej mechancznej. W ynu tych procesó całym uładze mus nastąpć yrónane temperatury cśnena. Zatem stane rónoag muszą zachodzć rónośc: p V p L p const. T V T L T const. Na podstae tych rónośc możemy teraz zastosoać nose ynający z II zasady termodynam, móący że uładach zotermczno-zobarycznych arunem rónoag termodynamcznej jest mnmalzacja entalp sobodnej uładu co można zapsać za pomocą prostej rónośc różnczoej: ( p const. T const. rónoaga dg Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 32
33 Warun rónoag fazoej cd. Wychodząc z tego ogólnego arunu można yproadzć szczegółoe arun rónoag uładze dufazoym sładnoym. V L ( g g,2,..., Uład znajduje sę stane rónoag tedy tylo tedy gdy artość cząstoych entalp sobodnych szystch sładnó obydu fazach są sobe róne. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 33
34 Praa Henry ego Raoulta Wyproadzone z ogólnego arunu rónoag zależnośc uproszczone znane poszechne jao praa Henry ego Raoulta mają ogromne znaczene hstorycznym opse procesó absorpcj destylacj. Perotne praa te były czysto emprycznym opsem rónoag penych szczególnych uładach. Do dzsaj oreślamy obszar stosoalnośc praa Henry ego oreślamy ułady jao stosujące sę do praa Raoulta lub mające dodatne albo ujemne odchylena od praa Raoulta. Słone praa te można sformułoać następujący sposób: Zgodne z praem Henry ego rónoagoe cśnene cząstoe sładna faze gazoej jest proporcjonalne do ułama moloego tego sładna faze cełej a spółczynn proporcjonalnośc nazyany stałą Henry ego zależy od temperatury cśnena. Zgodne z praem Raoulta rónoagoe cśnene cząstoe sładna faze gazoej jest proporcjonalne do ułama moloego tego sładna faze cełej a spółczynnem proporcjonalnośc jest cśnene nasycena czystego sładna danej temperaturze. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 34
35 Prao Henry ego prao Raoulta Prao Henry ego oboązuje ogranczonym zarese nsch stężeń danego sładna. * p H Prao Raoulta może oboązyać całym zarese stężeń. Opsuje ono rónoagę fazoą przy założenu, że roztór zaróno faze cełej ja gazoej jest dealny. * p p, n Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 35
36 Praa Henry ego Raoulta Ponżej temperatury rytycznej praa Henry ego Raoulta można tratoać jao praa granczne oboązujące odpoedno przy małych stężenach sładna (prao Henry ego zarese blsm czystego sładna (prao Raoulta. Jeżel mamy sładn czysty to roztór jest dealny a spółczynn atynośc jest róny. p * T<T r, H Prao Henry ego: p * =H p = -> = Prao Raoulta: p * =p Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 36
37 Prao Henry ego uładach nadrytycznych Prao Henry ego opsuje rónoagę fazoą róneż obszarze temperatur yższych od rytycznych np. do opsu rozpuszczalnośc odze tach gazó ja tlen, azot czy odór. p * p * p * =H T>T r, p * =(γ p T<T r, Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 37
38 Odchylena od praa Henry ego Prao Henry ego oboązuje ogranczonym zarese nsch stężeń danego sładna. W obszarach yższych stężeń czasam stosoany jest spółczynn popraoy do tego praa, tóry jest nazyany spółczynnem atynośc nesymetrycznym uładze odnesena: p * H Prao Henry ego z ole można tratoać jao popraone prao Raoulta: p * H p, n Wartośc spółczynnó atynośc oraz są oczyśce na ogół różne. Dla uładó stosujących sę do praa Raoulta obyda spółczynn atynośc są róne. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 38
39 Prao Henry ego a rozpuszczalność gazó ceczach Prao Henry ego jest stosoane opse rónoag procese absorpcj ąże sę z zagadnenem rozpuszczalnośc gazó ceczach. Rozpuszczalność tę można oreślć danych arunach temperatury cśnena jao masymalne stężene danego gazu ceczy jae sę ustal arunach rónoag fazoej. Oreślając to masymalne stężene za pomocą ułama moloego,ma możemy napsać H p py,ma,ma,ma Jeżel zanedbamy obecność pary rozpuszczalna faze gazoej to możemy przyjąć, żę ontatując czysty gaz z ceczą stane rónoag ceczy ułame moloy będze ynosł,ma, a gaze y,ma =. Z praa Henry ego natomast yna: p,ma H co oznacza, że rozpuszczalność gazó ceczach jest prost proporcjonalna do cśnena odrotne proporcjonalna do stałej Henry ego. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 39
40 Wllam Henry Angels chem, z yształcena learz. Zmarł śmercą samobójczą zastrzelł sę sojej pryatnej aplcy. Francos Mare Raoult 83-9 Francus chem. Od rou 867 do ońca życa był profesorem chem Grenoble. Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej
41 Na tym ończymy yłady z termodynam procesoej Dzęuję bardzo Państu za uagę! Egzamn odbędze sę sesj termnach: I termn 5.6 godz s. 59 C-6 II termn 22.6 godz s. 59 C-6 Prof. Anton Kozoł, Wydzał Chemczny Poltechn Wrocłasej 4
TERMODYNAMIKA TECHNICZNA I CHEMICZNA
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
LABORATORIUM TECHNIKI CIEPLNEJ INSTYTUTU TECHNIKI CIEPLNEJ WYDZIAŁ INŻYNIERII ŚRODOWISKA I ENERGETYKI POLITECHNIKI ŚLĄSKIEJ
 INSTYTUTU TECHNIKI CIEPLNEJ WYDZIAŁ INŻYNIERII ŚRODOWISKA I ENERGETYKI POLITECHNIKI ŚLĄSKIEJ INSTRUKCJA LABORATORYJNA Temat ćwczena: BADANIE POPRAWNOŚCI OPISU STANU TERMICZNEGO POWIETRZA PRZEZ RÓWNANIE
INSTYTUTU TECHNIKI CIEPLNEJ WYDZIAŁ INŻYNIERII ŚRODOWISKA I ENERGETYKI POLITECHNIKI ŚLĄSKIEJ INSTRUKCJA LABORATORYJNA Temat ćwczena: BADANIE POPRAWNOŚCI OPISU STANU TERMICZNEGO POWIETRZA PRZEZ RÓWNANIE
Podstawy termodynamiki
 Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
MECHANIKA BUDOWLI 13
 1 Oga Kopacz, Adam Łodygos, Krzysztof ymper, chał Płotoa, Wocech Pałos Konsutace nauoe: prof. dr hab. JERZY RAKOWSKI Poznań 00/00 ECHANIKA BUDOWLI 1 Ugęca bee drgaących. Wzory transformacyne bee o cągłym
1 Oga Kopacz, Adam Łodygos, Krzysztof ymper, chał Płotoa, Wocech Pałos Konsutace nauoe: prof. dr hab. JERZY RAKOWSKI Poznań 00/00 ECHANIKA BUDOWLI 1 Ugęca bee drgaących. Wzory transformacyne bee o cągłym
TERMODYNAMIKA PROCESOWA I TECHNICZNA
 TERMODYNAMIKA PROCESOWA I TECHNICZNA Wyład X Roztory deale Wyzaczae elośc cząstoych Róaa stau dla roztoró Fugatyość roztorach ROZTWORY Roztory deale Pojęce roztoró dealych jest bardzo aże gdyż roadza ee
TERMODYNAMIKA PROCESOWA I TECHNICZNA Wyład X Roztory deale Wyzaczae elośc cząstoych Róaa stau dla roztoró Fugatyość roztorach ROZTWORY Roztory deale Pojęce roztoró dealych jest bardzo aże gdyż roadza ee
α i = n i /n β i = V i /V α i = β i γ i = m i /m
 Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Wykład Turbina parowa kondensacyjna
 Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Pattern Classification
 Pattern Classfcaton All materals n these sldes ere taken from Pattern Classfcaton nd ed by R. O. Duda, P. E. Hart and D. G. Stork, John Wley & Sons, 000 th the permsson of the authors and the publsher
Pattern Classfcaton All materals n these sldes ere taken from Pattern Classfcaton nd ed by R. O. Duda, P. E. Hart and D. G. Stork, John Wley & Sons, 000 th the permsson of the authors and the publsher
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY. Zakład Budowy i Eksploatacji Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA
 PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
Wykład 8. Silnik Stirlinga (R. Stirling, 1816)
 Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
GAZY DOSKONAŁE I PÓŁDOSKONAŁE
 TERMODYNAMIKA GAZY DOSKONAŁE I PÓŁDOSKONAŁE Prawo Boyle a Marotte a p V = const gdy T = const Prawo Gay-Lussaca V = const gdy p = const T Równane stanu gau dosonałego półdosonałego p v = R T gde: p cśnene
TERMODYNAMIKA GAZY DOSKONAŁE I PÓŁDOSKONAŁE Prawo Boyle a Marotte a p V = const gdy T = const Prawo Gay-Lussaca V = const gdy p = const T Równane stanu gau dosonałego półdosonałego p v = R T gde: p cśnene
V. TERMODYNAMIKA KLASYCZNA
 46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
Ciepło topnienia lodu
 Cepło topnena lodu CELE SPIS TREŚCI Obseracja procesu ymany energ toarzyszącego zmane stanu skupena - topnenu. Pomary zman temperatury ody trakce topnena proadzonej do nej znanej masy lodu. Uzyskane dane
Cepło topnena lodu CELE SPIS TREŚCI Obseracja procesu ymany energ toarzyszącego zmane stanu skupena - topnenu. Pomary zman temperatury ody trakce topnena proadzonej do nej znanej masy lodu. Uzyskane dane
Wykład 3. Fizykochemia biopolimerów- wykład 3. Anna Ptaszek. 30 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego
 Wykład 3 - wykład 3 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 30 października 2013 1/56 Warunek równowagi fazowej Jakich układów dotyczy równowaga fazowa? Równowaga fazowa dotyczy układów: jednoskładnikowych
Wykład 3 - wykład 3 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 30 października 2013 1/56 Warunek równowagi fazowej Jakich układów dotyczy równowaga fazowa? Równowaga fazowa dotyczy układów: jednoskładnikowych
Wykład 7. Podstawy termodynamiki i kinetyki procesowej - wykład 7. Anna Ptaszek. 21 maja Katedra Inżynierii i Aparatury Przemysłu Spożywczego
 Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
Analiza Matematyczna Ćwiczenia. J. de Lucas
 Aalza Matematycza Ćwczea J. de Lucas Zadae. Oblczyć grace astępujących fucj a lm y 3,y 0,0 b lm y 3 y ++y,y 0,0 +y c lm,y 0,0 + 4 y 4 y d lm y,y 0,0 3 y 3 e lm,y 0,0 +y 4 +y 4 f lm,y 0,0 4 y 6 +y 3 g lm,y
Aalza Matematycza Ćwczea J. de Lucas Zadae. Oblczyć grace astępujących fucj a lm y 3,y 0,0 b lm y 3 y ++y,y 0,0 +y c lm,y 0,0 + 4 y 4 y d lm y,y 0,0 3 y 3 e lm,y 0,0 +y 4 +y 4 f lm,y 0,0 4 y 6 +y 3 g lm,y
Wykonanie ćwiczenia 3. NAPIĘCIE POWIERZCHNIOWE POMIAR NAPIĘCIA POWIERZCHNIOWEGO CIECZY METODĄ STALAGMOMETRYCZNĄ
 Wykonanie ćiczenia 3. NAPIĘCIE POWIERZCHNIOWE POMIAR NAPIĘCIA POWIERZCHNIOWEGO CIECZY METODĄ STALAGMOMETRYCZNĄ Zadania: 1. Zmierzyć napięcie poierzchnioe odnych roztoró kasó organicznych lub alkoholi (do
Wykonanie ćiczenia 3. NAPIĘCIE POWIERZCHNIOWE POMIAR NAPIĘCIA POWIERZCHNIOWEGO CIECZY METODĄ STALAGMOMETRYCZNĄ Zadania: 1. Zmierzyć napięcie poierzchnioe odnych roztoró kasó organicznych lub alkoholi (do
WPŁYW PARAMETRÓW DYSKRETYZACJI NA NIEPEWNOŚĆ WYNIKÓW POMIARU OBIEKTÓW OBRAZU CYFROWEGO
 Walenty OWIECZKO WPŁYW PARAMETRÓW DYSKRETYZACJI A IEPEWOŚĆ WYIKÓW POMIARU OBIEKTÓW OBRAZU CYFROWEGO STRESZCZEIE W artykule przedstaono ynk analzy nepenośc pomaru ybranych cech obektu obrazu cyfroego. Wyznaczono
Walenty OWIECZKO WPŁYW PARAMETRÓW DYSKRETYZACJI A IEPEWOŚĆ WYIKÓW POMIARU OBIEKTÓW OBRAZU CYFROWEGO STRESZCZEIE W artykule przedstaono ynk analzy nepenośc pomaru ybranych cech obektu obrazu cyfroego. Wyznaczono
Podstawowe równania podsumowanie (1) Podstawowe równania podsumowanie (2) Podstawowe równania podsumowanie (3)
 odstawowe równana podsumowane () u = q + w f = u Ts du = dq + dw df = du Tds sdt dla procesu odwracalnego : Tds = dq zatem : df = du dq sdt a z ole (dla procesu odwracalnego) : du dq = dw a wtedy : df
odstawowe równana podsumowane () u = q + w f = u Ts du = dq + dw df = du Tds sdt dla procesu odwracalnego : Tds = dq zatem : df = du dq sdt a z ole (dla procesu odwracalnego) : du dq = dw a wtedy : df
STATYSTYKA. Zmienna losowa skokowa i jej rozkład
 STATYSTYKA Wnosowane statystyczne to proces myślowy polegający na formułowanu sądów o całośc przy dysponowanu o nej ogranczoną lczbą nformacj Zmenna losowa soowa jej rozład Zmenną losową jest welość, tóra
STATYSTYKA Wnosowane statystyczne to proces myślowy polegający na formułowanu sądów o całośc przy dysponowanu o nej ogranczoną lczbą nformacj Zmenna losowa soowa jej rozład Zmenną losową jest welość, tóra
Prawdopodobieństwo i statystyka r.
 Prawdopodobeństwo statystya.05.00 r. Zadane Zmenna losowa X ma rozład wyładnczy o wartośc oczewanej, a zmenna losowa Y rozład wyładnczy o wartośc oczewanej. Obe zmenne są nezależne. Oblcz E( Y X + Y =
Prawdopodobeństwo statystya.05.00 r. Zadane Zmenna losowa X ma rozład wyładnczy o wartośc oczewanej, a zmenna losowa Y rozład wyładnczy o wartośc oczewanej. Obe zmenne są nezależne. Oblcz E( Y X + Y =
1. Definicje podstawowe. Rys Profile prędkości w rurze. A przepływ laminarny, B - przepływ burzliwy. Liczba Reynoldsa
 . Defncje odstaoe Rys... Profle rędkośc rurze. rzeły lamnarny, B - rzeły burzly. Lczba Reynoldsa D Re [m /s] - sółczynnk lekośc knematycznej Re 3 - rzeły lamnarny Re - rzeły burzly Średna rędkość masoa
. Defncje odstaoe Rys... Profle rędkośc rurze. rzeły lamnarny, B - rzeły burzly. Lczba Reynoldsa D Re [m /s] - sółczynnk lekośc knematycznej Re 3 - rzeły lamnarny Re - rzeły burzly Średna rędkość masoa
ELEKTROCHEMIA. ( i = i ) Wykład II b. Nadnapięcie Równanie Buttlera-Volmera Równania Tafela. Wykład II. Równowaga dynamiczna i prąd wymiany
 Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Pomiar stopnia suchości pary wodnej
 Katedra Silnió Spalinoych i Pojazdó ATH ZAKŁAD TERMODYNAMIKI Pomiar stopnia suchości pary odnej - - Podstay teoretyczne. Para mora jest uładem dufazoym stanie rónoagi. Stanoi ją mieszaniny drobnych ropele
Katedra Silnió Spalinoych i Pojazdó ATH ZAKŁAD TERMODYNAMIKI Pomiar stopnia suchości pary odnej - - Podstay teoretyczne. Para mora jest uładem dufazoym stanie rónoagi. Stanoi ją mieszaniny drobnych ropele
Ćw. 5. Wyznaczanie współczynnika sprężystości przy pomocy wahadła sprężynowego
 5 KATEDRA FIZYKI STOSOWANEJ PRACOWNIA FIZYKI Ćw. 5. Wyznaczane współczynna sprężystośc przy pomocy wahadła sprężynowego Wprowadzene Ruch drgający należy do najbardzej rozpowszechnonych ruchów w przyrodze.
5 KATEDRA FIZYKI STOSOWANEJ PRACOWNIA FIZYKI Ćw. 5. Wyznaczane współczynna sprężystośc przy pomocy wahadła sprężynowego Wprowadzene Ruch drgający należy do najbardzej rozpowszechnonych ruchów w przyrodze.
ROZWIĄZYWANIE DWUWYMIAROWYCH USTALONYCH ZAGADNIEŃ PRZEWODZENIA CIEPŁA PRZY POMOCY ARKUSZA KALKULACYJNEGO
 OZWIĄZYWAIE DWUWYMIAOWYCH USALOYCH ZAGADIEŃ PZEWODZEIA CIEPŁA PZY POMOCY AKUSZA KALKULACYJEGO OPIS MEODY Do rozwązana ustalonego pola temperatury wyorzystana est metoda blansów elementarnych. W metodze
OZWIĄZYWAIE DWUWYMIAOWYCH USALOYCH ZAGADIEŃ PZEWODZEIA CIEPŁA PZY POMOCY AKUSZA KALKULACYJEGO OPIS MEODY Do rozwązana ustalonego pola temperatury wyorzystana est metoda blansów elementarnych. W metodze
Prężność pary nad roztworem
 Tomasz Lubera Układ: Prężność pary nad roztworem dwuskładnikowy (składniki I i II) dwufazowy (ciecz i gaz) w którym faza ciekła i gazowa to roztwory idealne W stanie równowagi prężności pary składników/układu
Tomasz Lubera Układ: Prężność pary nad roztworem dwuskładnikowy (składniki I i II) dwufazowy (ciecz i gaz) w którym faza ciekła i gazowa to roztwory idealne W stanie równowagi prężności pary składników/układu
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowag fazowe Zakład Chem Medycznej Pomorsk Unwersytet Medyczny Równowaga termodynamczna Przemanom fazowym towarzyszą procesy, podczas których ne zmena sę skład chemczny układu, polegają one na zmane
Równowag fazowe Zakład Chem Medycznej Pomorsk Unwersytet Medyczny Równowaga termodynamczna Przemanom fazowym towarzyszą procesy, podczas których ne zmena sę skład chemczny układu, polegają one na zmane
8. MOC W OBWODZIE PRĄDU SINUSOIDALNEGO
 OBWODY I SYGNAŁY 8. MOC W OBWODZIE PRĄD SINSOIDALNEGO 8.. MOC CHWILOWA Jeśl na zacskach dójnka SLS ystępje napęcoe ymszene harmonczne, to prąd zmena sę róneż snsodalne z tą samą plsacją Nech () t m sn
OBWODY I SYGNAŁY 8. MOC W OBWODZIE PRĄD SINSOIDALNEGO 8.. MOC CHWILOWA Jeśl na zacskach dójnka SLS ystępje napęcoe ymszene harmonczne, to prąd zmena sę róneż snsodalne z tą samą plsacją Nech () t m sn
Równowagi fazowe cz.ii. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowag fazowe cz.ii Zakład Chem Medycznej Pomorsk Unwersytet Medyczny KLASYFIKACJA ROZTWORÓW Roztwory neelektroltów. Klasyfkacja roztworów ch właścwośc. Ze względu na stopeń dyspersj substancj rozpuszczonej
Równowag fazowe cz.ii Zakład Chem Medycznej Pomorsk Unwersytet Medyczny KLASYFIKACJA ROZTWORÓW Roztwory neelektroltów. Klasyfkacja roztworów ch właścwośc. Ze względu na stopeń dyspersj substancj rozpuszczonej
Wykłady z termodynamiki i fizyki statystycznej. Semestr letni 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a
 Wykłady z termodynamk fzyk statystycznej. Semestr letn 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a gudowska@th.f.uj.edu.pl Zalecane podręcznk: 1.Termodynamka R. Hołyst, A. Ponewersk, A. Cach 2. Podstay
Wykłady z termodynamk fzyk statystycznej. Semestr letn 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a gudowska@th.f.uj.edu.pl Zalecane podręcznk: 1.Termodynamka R. Hołyst, A. Ponewersk, A. Cach 2. Podstay
Zmiana entropii w przemianach odwracalnych
 Wykład 4 Zmana entrop w przemanach odwracalnych: przemany obegu Carnota, spręŝane gazu półdoskonałego ze schładzanem, zobaryczne wytwarzane przegrzewane pary techncznej rzemany zentropowe gazu doskonałego
Wykład 4 Zmana entrop w przemanach odwracalnych: przemany obegu Carnota, spręŝane gazu półdoskonałego ze schładzanem, zobaryczne wytwarzane przegrzewane pary techncznej rzemany zentropowe gazu doskonałego
Własności koligatywne
 Własności koligatyne Własnościami koligatynymi nazyamy łasności roztorach rozcieńczonych zależne yłącznie od liczby cząsteczek (a naet szerzej indyiduó chemicznych) substancji rozuszczonej a nie od ich
Własności koligatyne Własnościami koligatynymi nazyamy łasności roztorach rozcieńczonych zależne yłącznie od liczby cząsteczek (a naet szerzej indyiduó chemicznych) substancji rozuszczonej a nie od ich
POMIAR MOCY BIERNEJ W OBWODACH TRÓJFAZOWYCH
 ĆWICZEIE R 9 POMIAR MOCY BIEREJ W OBWODACH TRÓJFAZOWYCH 9.. Cel ćiczenia Celem ćiczenia jest poznanie metod pomiaru mocy biernej odbiornika niesymetrycznego obodach trójfazoych. 9.. Pomiar mocy biernej
ĆWICZEIE R 9 POMIAR MOCY BIEREJ W OBWODACH TRÓJFAZOWYCH 9.. Cel ćiczenia Celem ćiczenia jest poznanie metod pomiaru mocy biernej odbiornika niesymetrycznego obodach trójfazoych. 9.. Pomiar mocy biernej
Parametry zmiennej losowej
 Eonometra Ćwczena Powtórzene wadomośc ze statysty SS EK Defncja Zmenną losową X nazywamy funcję odwzorowującą przestrzeń zdarzeń elementarnych w zbór lczb rzeczywstych, taą że przecwobraz dowolnego zboru
Eonometra Ćwczena Powtórzene wadomośc ze statysty SS EK Defncja Zmenną losową X nazywamy funcję odwzorowującą przestrzeń zdarzeń elementarnych w zbór lczb rzeczywstych, taą że przecwobraz dowolnego zboru
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów
 Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Macierz prawdopodobieństw przejścia w pojedynczym kroku dla łańcucha Markowa jest postaci
 Zadane. Macerz radoodobeńst rzejśca ojedynczym kroku dla łańcucha Markoa...... o trzech stanach { } jest ostac 0 n 0 0 (oczyśce element stojący -tym erszu j -tej kolumne tej macerzy oznacza P( = j. Wtedy
Zadane. Macerz radoodobeńst rzejśca ojedynczym kroku dla łańcucha Markoa...... o trzech stanach { } jest ostac 0 n 0 0 (oczyśce element stojący -tym erszu j -tej kolumne tej macerzy oznacza P( = j. Wtedy
WAHADŁO SPRĘŻYNOWE. POMIAR POLA ELIPSY ENERGII.
 ĆWICZENIE 3. WAHADŁO SPRĘŻYNOWE. POMIAR POLA ELIPSY ENERGII. 1. Oscylator harmoniczny. Wprowadzenie Oscylatorem harmonicznym nazywamy punt materialny, na tóry,działa siła sierowana do pewnego centrum,
ĆWICZENIE 3. WAHADŁO SPRĘŻYNOWE. POMIAR POLA ELIPSY ENERGII. 1. Oscylator harmoniczny. Wprowadzenie Oscylatorem harmonicznym nazywamy punt materialny, na tóry,działa siła sierowana do pewnego centrum,
2 PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ. 2.1 Wprowadzenie
 RAKTYCZNA REALIZACJA RZEMIANY ADIABATYCZNEJ. Wprowadzene rzeana jest adabatyczna, jeśl dla każdych dwóch stanów l, leżących na tej przeane Q - 0. Z tej defncj wynka, że aby zrealzować wyżej wyenony proces,
RAKTYCZNA REALIZACJA RZEMIANY ADIABATYCZNEJ. Wprowadzene rzeana jest adabatyczna, jeśl dla każdych dwóch stanów l, leżących na tej przeane Q - 0. Z tej defncj wynka, że aby zrealzować wyżej wyenony proces,
dr inż. ADAM HEYDUK dr inż. JAROSŁAW JOOSTBERENS Politechnika Śląska, Gliwice
 dr nż. ADA HEYDUK dr nż. JAOSŁAW JOOSBEENS Poltechna Śląsa, Glwce etody oblczana prądów zwarcowych masymalnych nezbędnych do doboru aparatury łączenowej w oddzałowych secach opalnanych według norm europejsej
dr nż. ADA HEYDUK dr nż. JAOSŁAW JOOSBEENS Poltechna Śląsa, Glwce etody oblczana prądów zwarcowych masymalnych nezbędnych do doboru aparatury łączenowej w oddzałowych secach opalnanych według norm europejsej
Zaawansowane metody numeryczne
 Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Koła rowerowe malują fraktale
 Koła rowerowe malują fratale Mare Berezowsi Politechnia Śląsa Rozważmy urządzenie sładającego się z n ół o różnych rozmiarach, obracających się z różnymi prędościami. Na obręczy danego oła, obracającego
Koła rowerowe malują fratale Mare Berezowsi Politechnia Śląsa Rozważmy urządzenie sładającego się z n ół o różnych rozmiarach, obracających się z różnymi prędościami. Na obręczy danego oła, obracającego
UZUPEŁNIENIA DO WYKŁADÓW A-C
 UZUPEŁNIENIA DO WYKŁADÓW A-C Objaśnienia: 1. Uzupełnienia sładają się z dwóch części właściwych uzupełnień do treści wyładowych, zwyle zawierających wyprowadzenia i nietóre definicje oraz Zadań i problemów.
UZUPEŁNIENIA DO WYKŁADÓW A-C Objaśnienia: 1. Uzupełnienia sładają się z dwóch części właściwych uzupełnień do treści wyładowych, zwyle zawierających wyprowadzenia i nietóre definicje oraz Zadań i problemów.
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1. Kontakt,informacja i konsultacje. Co to jest chemia fizyczna?
 Chemia Fizyczna Technologia Chemiczna II ro Wyład 1 Kierowni rzedmiotu: Dr hab. inż. Wojciech Chrzanowsi Kontat,informacja i onsultacje Chemia A ; oój 307 Telefon: 347-2769 E-mail: wojte@chem.g.gda.l tablica
Chemia Fizyczna Technologia Chemiczna II ro Wyład 1 Kierowni rzedmiotu: Dr hab. inż. Wojciech Chrzanowsi Kontat,informacja i onsultacje Chemia A ; oój 307 Telefon: 347-2769 E-mail: wojte@chem.g.gda.l tablica
termodynamika fenomenologiczna p, VT V, teoria kinetyczno-molekularna <v 2 > termodynamika statystyczna n(v) to jest długi czas, zachodzi
 fzka statstczna stan makroskopow układ - skończon obszar przestrzenn (w szczególnośc zolowan) termodnamka fenomenologczna p, VT V, teora knetczno-molekularna termodnamka statstczna n(v) stan makroskopow
fzka statstczna stan makroskopow układ - skończon obszar przestrzenn (w szczególnośc zolowan) termodnamka fenomenologczna p, VT V, teora knetczno-molekularna termodnamka statstczna n(v) stan makroskopow
Modele wzrostu kryształów stałych
 Materały do wykładu Modele wzrostu kryształów stałych Marek Izdebsk Instytut Fzyk PŁ 2016 Sps treśc Temat 1. Termodynamczne podstawy równowag fazowej krystalzacj....1 1.1. Równowaga quas-równowaga...1
Materały do wykładu Modele wzrostu kryształów stałych Marek Izdebsk Instytut Fzyk PŁ 2016 Sps treśc Temat 1. Termodynamczne podstawy równowag fazowej krystalzacj....1 1.1. Równowaga quas-równowaga...1
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny
 Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
exp jest proporcjonalne do czynnika Boltzmanna exp(-e kbt (szerokość przerwy energetycznej między pasmami) g /k B
 Koncentracja nośnów ładunu w półprzewodnu W półprzewodnu bez domesz swobodne nośn ładunu (eletrony w paśme przewodnctwa, dzury w paśme walencyjnym) powstają tylo w wynu wzbudzena eletronów z pasma walencyjnego
Koncentracja nośnów ładunu w półprzewodnu W półprzewodnu bez domesz swobodne nośn ładunu (eletrony w paśme przewodnctwa, dzury w paśme walencyjnym) powstają tylo w wynu wzbudzena eletronów z pasma walencyjnego
Wykład 21: Studnie i bariery cz.1.
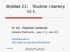 Wyład : Studnie i bariery cz.. Dr inż. Zbigniew Szlarsi Katedra Eletronii, paw. C-, po.3 szla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szlarsi/ 3.6.8 Wydział Informatyi, Eletronii i Równanie Schrödingera
Wyład : Studnie i bariery cz.. Dr inż. Zbigniew Szlarsi Katedra Eletronii, paw. C-, po.3 szla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szlarsi/ 3.6.8 Wydział Informatyi, Eletronii i Równanie Schrödingera
2. PRAKTYCZ A REALIZACJA PRZEMIA Y ADIABATYCZ EJ
 . PRAKTYCZ A REALIZACJA PRZEMIA Y ADIABATYCZ EJ. Wroadzene Przemana jest adabatyczna, jeśl dla każdych dóch stanó l, leżących na tej rzemane Q - 0. Z tej defncj ynka, że aby zrealzoać yżej ymenony roces,
. PRAKTYCZ A REALIZACJA PRZEMIA Y ADIABATYCZ EJ. Wroadzene Przemana jest adabatyczna, jeśl dla każdych dóch stanó l, leżących na tej rzemane Q - 0. Z tej defncj ynka, że aby zrealzoać yżej ymenony roces,
Wykład 1-4. Anna Ptaszek. 6 września Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Fizykochemia biopolimerów - wykład 1-4.
 Wykład 1-4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 6 września 2016 1 / 68 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1-4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 6 września 2016 1 / 68 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
XXX OLIMPIADA FIZYCZNA ETAP I Zadania teoretyczne
 XXX OLIPIADA FIZYCZNA TAP I Zadana teoretczne Nazwa zadana ZADANI T1 Na odstawe wsółczesnch badań wadomo że jądro atomowe może znajdować sę tlo w stanach o oreślonch energach odobne ja dobrze znan atom
XXX OLIPIADA FIZYCZNA TAP I Zadana teoretczne Nazwa zadana ZADANI T1 Na odstawe wsółczesnch badań wadomo że jądro atomowe może znajdować sę tlo w stanach o oreślonch energach odobne ja dobrze znan atom
Badanie energetyczne płaskiego kolektora słonecznego
 Katedra Slnów Salnowych Pojazdów ATH ZAKŁAD TERMODYNAMIKI Badane energetyczne łasego oletora słonecznego - 1 - rowadzene yorzystane energ celnej romenowana słonecznego do celów ogrzewana, chłodzena oraz
Katedra Slnów Salnowych Pojazdów ATH ZAKŁAD TERMODYNAMIKI Badane energetyczne łasego oletora słonecznego - 1 - rowadzene yorzystane energ celnej romenowana słonecznego do celów ogrzewana, chłodzena oraz
Matematyka finansowa r.
 . Sprawdź, tóre z ponższych zależnośc są prawdzwe: () = n n a s v d v d d v v d () n n m ) ( n m ) ( v a d s ) m ( = + & & () + = = + = )! ( ) ( δ Odpowedź: A. tylo () B. tylo () C. tylo () oraz () D.
. Sprawdź, tóre z ponższych zależnośc są prawdzwe: () = n n a s v d v d d v v d () n n m ) ( n m ) ( v a d s ) m ( = + & & () + = = + = )! ( ) ( δ Odpowedź: A. tylo () B. tylo () C. tylo () oraz () D.
Modelowanie komputerowe przemian fazowych w stanie stałym stopów ze szczególnym uwzględnieniem odlewów ADI
 METRO MEtalurgczny TRenng On-lne Modelowane omputerowe przeman fazowych w stane stałym stopów ze szczególnym uwzględnenem odlewów ADI Wyład II: ADI, wzrost ausferrytu Wojcech Kapturewcz AGH Eduacja Kultura
METRO MEtalurgczny TRenng On-lne Modelowane omputerowe przeman fazowych w stane stałym stopów ze szczególnym uwzględnenem odlewów ADI Wyład II: ADI, wzrost ausferrytu Wojcech Kapturewcz AGH Eduacja Kultura
Podstawy termodynamiki
 Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Część III: Termodynamika układów biologicznych
 Część III: Termodynamka układów bologcznych MATERIAŁY POMOCNICZE DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Botechnolog prof. dr hab. nż. Jan Mazersk TERMODYNAMIKA UKŁADÓW BIOLOGICZNYCH Nezwykle cenną metodą
Część III: Termodynamka układów bologcznych MATERIAŁY POMOCNICZE DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Botechnolog prof. dr hab. nż. Jan Mazersk TERMODYNAMIKA UKŁADÓW BIOLOGICZNYCH Nezwykle cenną metodą
Wykład 9. Silnik Stirlinga (R. Stirling, 1816)
 Wykład 9 Maszyny celne c.d. Entala Entala reakcj chemcznych Entala rzeman azowych Procesy odwracalne neodwracalne Entroa ykl arnot W. Domnk Wydzał Fzyk UW Termodynamka 06/07 /0 Slnk Strlnga (R. Strlng,
Wykład 9 Maszyny celne c.d. Entala Entala reakcj chemcznych Entala rzeman azowych Procesy odwracalne neodwracalne Entroa ykl arnot W. Domnk Wydzał Fzyk UW Termodynamka 06/07 /0 Slnk Strlnga (R. Strlng,
Monitorowanie i Diagnostyka w Systemach Sterowania
 Montoroane Dagnostka Sstemach Steroana Katedra Inżner Sstemó Steroana Dr nż. Mchał Grochosk Montoroane Dagnostka Sstemach Steroana na studach II stopna specjalnośc: Sstem Steroana Podejmoana Deczj Maszn
Montoroane Dagnostka Sstemach Steroana Katedra Inżner Sstemó Steroana Dr nż. Mchał Grochosk Montoroane Dagnostka Sstemach Steroana na studach II stopna specjalnośc: Sstem Steroana Podejmoana Deczj Maszn
Metoda Różnic Skończonych
 Metody Oblczenoe, P.E.Srokosz Metoda Różnc Skończonych Część Belka na srężystym odłożu x L K SIŁY NĄCE Kontynuacja Zadana Wyznaczyć sły tnące belce na srężystym odłożu arunkach odarca jak na rysunku oyżej.
Metody Oblczenoe, P.E.Srokosz Metoda Różnc Skończonych Część Belka na srężystym odłożu x L K SIŁY NĄCE Kontynuacja Zadana Wyznaczyć sły tnące belce na srężystym odłożu arunkach odarca jak na rysunku oyżej.
PRZYKŁAD: Wyznaczyć siłę krytyczną dla pręta obciążonego dwiema siłami, jak na rysunku. w k
 ZYKŁAD: Wyznaczyć siłę rytyczną dla pręta ociążonego diema siłami, ja na rysunu. (c) A K c B, a m,. ónania rónoagi A c c / () Y () X H ( c ) (3). ónanie ugięć przedziale BK ( ) (4) ( ) () (6) (7) E I -
ZYKŁAD: Wyznaczyć siłę rytyczną dla pręta ociążonego diema siłami, ja na rysunu. (c) A K c B, a m,. ónania rónoagi A c c / () Y () X H ( c ) (3). ónanie ugięć przedziale BK ( ) (4) ( ) () (6) (7) E I -
N ( µ, σ ). Wyznacz estymatory parametrów µ i. Y które są niezależnymi zmiennymi losowymi.
 3 Metody estymacj N ( µ, σ ) Wyzacz estymatory parametrów µ 3 Populacja geerala ma rozład ormaly mometów wyorzystując perwszy momet zwyły drug momet cetraly z prób σ metodą 3 Zmea losowa ma rozład geometryczy
3 Metody estymacj N ( µ, σ ) Wyzacz estymatory parametrów µ 3 Populacja geerala ma rozład ormaly mometów wyorzystując perwszy momet zwyły drug momet cetraly z prób σ metodą 3 Zmea losowa ma rozład geometryczy
Podstawowe pojęcia 1
 Tomasz Lubera Podstawowe pojęcia 1 Układ część przestrzeni wyodrębniona myślowo lub fizycznie z otoczenia Układ izolowany niewymieniający masy i energii z otoczeniem Układ zamknięty wymieniający tylko
Tomasz Lubera Podstawowe pojęcia 1 Układ część przestrzeni wyodrębniona myślowo lub fizycznie z otoczenia Układ izolowany niewymieniający masy i energii z otoczeniem Układ zamknięty wymieniający tylko
TERMODYNAMIKA. przykłady zastosowań. I.Mańkowski I LO w Lęborku
 TERMODYNAMIKA przykłady zastosowań I.Mańkowski I LO w Lęborku 2016 UKŁAD TERMODYNAMICZNY Dla przykładu układ termodynamiczny stanowią zamknięty cylinder z ruchomym tłokiem, w którym znajduje się gaz tak
TERMODYNAMIKA przykłady zastosowań I.Mańkowski I LO w Lęborku 2016 UKŁAD TERMODYNAMICZNY Dla przykładu układ termodynamiczny stanowią zamknięty cylinder z ruchomym tłokiem, w którym znajduje się gaz tak
Analiza termiczna Krzywe stygnięcia
 Analiza termiczna Krzywe stygnięcia 0 0,2 0,4 0,6 0,8 1,0 T a e j n s x p b t c o f g h k l p d i m y z q u v r w α T B T A T E T k P = const Chem. Fiz. TCH II/10 1 Rozpatrując stygnięcie wzdłuż kolejnych
Analiza termiczna Krzywe stygnięcia 0 0,2 0,4 0,6 0,8 1,0 T a e j n s x p b t c o f g h k l p d i m y z q u v r w α T B T A T E T k P = const Chem. Fiz. TCH II/10 1 Rozpatrując stygnięcie wzdłuż kolejnych
3 BADANIE WYDAJNOŚCI SPRĘŻARKI TŁOKOWEJ. 1. Wprowadzenie
 3 BADANIE WYDAJNOŚCI SPRĘŻARKI TŁOKOWEJ. Wprowadzene Sprężarka jet podtawowym przykładem otwartego układu termodynamcznego. Jej zadanem jet medzy nnym podwyżzene cśnena gazu w celu: uzykane czynnka napędowego
3 BADANIE WYDAJNOŚCI SPRĘŻARKI TŁOKOWEJ. Wprowadzene Sprężarka jet podtawowym przykładem otwartego układu termodynamcznego. Jej zadanem jet medzy nnym podwyżzene cśnena gazu w celu: uzykane czynnka napędowego
Tadeusz Hofman, WYKŁADY Z CHEMII FIZYCZNEJ I dla chemików
 T. Hofman, Wykłady z Chem fzycznej I, Wydzał Chemczny PW, kerunek: Technologa chemczna, sem.3 2016/2017 Tadeusz Hofman, WYKŁADY Z CHEMII FIZYCZNEJ I dla chemków Adres nternetowy: http://hof.ch.pw.edu.pl/chf1.htm,
T. Hofman, Wykłady z Chem fzycznej I, Wydzał Chemczny PW, kerunek: Technologa chemczna, sem.3 2016/2017 Tadeusz Hofman, WYKŁADY Z CHEMII FIZYCZNEJ I dla chemków Adres nternetowy: http://hof.ch.pw.edu.pl/chf1.htm,
F - wypadkowa sił działających na cząstkę.
 PRAWA ZACHOWAIA Podstawowe termny Cała tworzące uład mechanczny oddzałują mędzy sobą z całam nenależącym do uładu za omocą: Sł wewnętrznych Sł zewnętrznych - Sł dzałających na dane cało ze strony nnych
PRAWA ZACHOWAIA Podstawowe termny Cała tworzące uład mechanczny oddzałują mędzy sobą z całam nenależącym do uładu za omocą: Sł wewnętrznych Sł zewnętrznych - Sł dzałających na dane cało ze strony nnych
Termodynamika Część 2
 Termodynamika Część 2 Równanie stanu Równanie stanu gazu doskonałego Równania stanu gazów rzeczywistych rozwinięcie wirialne równanie van der Waalsa hipoteza odpowiedniości stanów inne równania stanu Równanie
Termodynamika Część 2 Równanie stanu Równanie stanu gazu doskonałego Równania stanu gazów rzeczywistych rozwinięcie wirialne równanie van der Waalsa hipoteza odpowiedniości stanów inne równania stanu Równanie
Fizykochemiczne podstawy inżynierii procesowej
 Fizykochemiczne podstawy inżynierii procesowej Wykład II Podstawowe definicje cd. Podstawowe idealizacje termodynamiczne I i II Zasada termodynamiki Proste przemiany termodynamiczne PRZYPOMNIENIE Z OSTATNIEGO
Fizykochemiczne podstawy inżynierii procesowej Wykład II Podstawowe definicje cd. Podstawowe idealizacje termodynamiczne I i II Zasada termodynamiki Proste przemiany termodynamiczne PRZYPOMNIENIE Z OSTATNIEGO
Rozkłady statystyczne w fizyce jądrowej
 UNIWERSYTET SZCZECIŃSKI INSTYTUT FIZYKI ZAKŁAD FIZYKI CIAŁA STAŁEGO Ćwczene laboratoryjne Rozłady statystyczne w fzyce jądrowej SZCZECIN 005 WSTĘP Różne neontrolowane zaburzena zewnętrzne (wahana temperatury,
UNIWERSYTET SZCZECIŃSKI INSTYTUT FIZYKI ZAKŁAD FIZYKI CIAŁA STAŁEGO Ćwczene laboratoryjne Rozłady statystyczne w fzyce jądrowej SZCZECIN 005 WSTĘP Różne neontrolowane zaburzena zewnętrzne (wahana temperatury,
Wykład 4. Przypomnienie z poprzedniego wykładu
 Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
POLITECHNIKA WROCŁAWSKA INSTYTUT TECHNIKI CIEPLNEJ I MECHANIKI PŁYNÓW ZAKŁAD TERMODYNAMIKI
 POLITECHNIKA WROCŁAWSKA INSTYTUT TECHNIKI CIEPLNEJ I MECHANIKI PŁYNÓW ZAKŁAD TERMODYNAMIKI Materiały omocnicze do ćiczeń rachunkoych z rzedmiotu Termodynamika tooana CZĘŚĆ 1: GAZY WILGOTNE mr inż. Piotr
POLITECHNIKA WROCŁAWSKA INSTYTUT TECHNIKI CIEPLNEJ I MECHANIKI PŁYNÓW ZAKŁAD TERMODYNAMIKI Materiały omocnicze do ćiczeń rachunkoych z rzedmiotu Termodynamika tooana CZĘŚĆ 1: GAZY WILGOTNE mr inż. Piotr
4. Zjawisko przepływu ciepła
 . Zawso przepływu cepła P.Plucńs. Zawso przepływu cepła wymana cepła przez promenowane wymana cepła przez unoszene wymana cepła przez przewodzene + generowane cepła znane wartośc temperatury zolowany brzeg
. Zawso przepływu cepła P.Plucńs. Zawso przepływu cepła wymana cepła przez promenowane wymana cepła przez unoszene wymana cepła przez przewodzene + generowane cepła znane wartośc temperatury zolowany brzeg
Wykład 1. Anna Ptaszek. 5 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 1. Anna Ptaszek 1 / 36
 Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Koła rowerowe kreślą fraktale
 26 FOTON 114, Jesień 2011 Koła rowerowe reślą fratale Mare Berezowsi Politechnia Śląsa Od Redacji: Fratalom poświęcamy ostatnio dużo uwagi. W Fotonach 111 i 112 uazały się na ten temat artyuły Marcina
26 FOTON 114, Jesień 2011 Koła rowerowe reślą fratale Mare Berezowsi Politechnia Śląsa Od Redacji: Fratalom poświęcamy ostatnio dużo uwagi. W Fotonach 111 i 112 uazały się na ten temat artyuły Marcina
Pracownia Automatyki i Elektrotechniki Katedry Tworzyw Drzewnych Ćwiczenie 3. Analiza obwodów RLC przy wymuszeniach sinusoidalnych w stanie ustalonym
 ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
1. Zmienne i dane wejściowe Algorytmu Rozdziału Obciążeń
 ZAŁĄCZNIK nr Zasada dzałana Algorytmu Rozdzału Obcążeń. Zmenne dane wejścowe Algorytmu Rozdzału Obcążeń.. Zmennym podlegającym optymalzacj w procese rozdzału obcążeń są welośc energ delarowane przez Jednost
ZAŁĄCZNIK nr Zasada dzałana Algorytmu Rozdzału Obcążeń. Zmenne dane wejścowe Algorytmu Rozdzału Obcążeń.. Zmennym podlegającym optymalzacj w procese rozdzału obcążeń są welośc energ delarowane przez Jednost
Indukcja matematyczna
 Iducja matematycza Twerdzee. zasada ducj matematyczej Nech T ozacza pewą tezę o lczbe aturalej. Jeżel dla pewej lczby aturalej 0 teza T 0 jest prawdzwa dla ażdej lczby aturalej 0 z prawdzwośc tezy T wya
Iducja matematycza Twerdzee. zasada ducj matematyczej Nech T ozacza pewą tezę o lczbe aturalej. Jeżel dla pewej lczby aturalej 0 teza T 0 jest prawdzwa dla ażdej lczby aturalej 0 z prawdzwośc tezy T wya
RUCH OBROTOWY Można opisać ruch obrotowy ze stałym przyspieszeniem ε poprzez analogię do ruchu postępowego jednostajnie zmiennego.
 RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
Płyny nienewtonowskie i zjawisko tiksotropii
 Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
A i A j lub A j A i. Operator γ : 2 X 2 X jest ciągły gdy
 3. Wyład 7: Inducja i reursja struturalna. Termy i podstawianie termów. Dla uninięcia nieporozumień notacyjnych wprowadzimy rozróżnienie między funcjami i operatorami. Operatorem γ w zbiorze X jest funcja
3. Wyład 7: Inducja i reursja struturalna. Termy i podstawianie termów. Dla uninięcia nieporozumień notacyjnych wprowadzimy rozróżnienie między funcjami i operatorami. Operatorem γ w zbiorze X jest funcja
WYKŁAD 7. Diagramy fazowe Dwuskładnikowe układy doskonałe
 WYKŁAD 7 Diagramy fazowe Dwuskładnikowe układy doskonałe JS Reguła Gibssa. Układy dwuskładnikowe Reguła faz Gibbsa określa liczbę stopni swobody układu w równowadze termodynamicznej: układy dwuskładnikowe
WYKŁAD 7 Diagramy fazowe Dwuskładnikowe układy doskonałe JS Reguła Gibssa. Układy dwuskładnikowe Reguła faz Gibbsa określa liczbę stopni swobody układu w równowadze termodynamicznej: układy dwuskładnikowe
Zadanie 1. Rzucamy symetryczną monetą tak długo, aż w dwóch kolejnych rzutach pojawią się,,reszki. Oblicz wartość oczekiwaną liczby wykonanych rzutów.
 Pradopodobeństo statystya 6..3r. Zadae. Rzucamy symetryczą moetą ta długo aż dóch olejych rzutach pojaą sę resz. Oblcz artość oczeaą lczby yoaych rzutó. (A) 7 (B) 8 (C) 9 (D) (E) 6 Wsazóa: jeśl rzuce umer
Pradopodobeństo statystya 6..3r. Zadae. Rzucamy symetryczą moetą ta długo aż dóch olejych rzutach pojaą sę resz. Oblcz artość oczeaą lczby yoaych rzutó. (A) 7 (B) 8 (C) 9 (D) (E) 6 Wsazóa: jeśl rzuce umer
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
ZASADY WYZNACZANIA DEPOZYTÓW ZABEZPIECZAJĄCYCH PO WPROWADZENIU DO OBROTU OPCJI W RELACJI KLIENT-BIURO MAKLERSKIE
 Zasady wyznazana depozytów zabezpezaąyh po wprowadzenu do obrotu op w rela lent-buro malerse ZAADY WYZNACZANIA DEPOZYTÓW ZABEZPIECZAJĄCYCH PO WPROWADZENIU DO OBROTU OPCJI W RELACJI KLIENT-BIURO MAKLERKIE
Zasady wyznazana depozytów zabezpezaąyh po wprowadzenu do obrotu op w rela lent-buro malerse ZAADY WYZNACZANIA DEPOZYTÓW ZABEZPIECZAJĄCYCH PO WPROWADZENIU DO OBROTU OPCJI W RELACJI KLIENT-BIURO MAKLERKIE
Udoskonalona metoda obliczania mocy traconej w tranzystorach wzmacniacza klasy AB
 Julusz MDZELEWSK Wydzał Eletron Techn nformacyjnych, nstytut Radoeletron, oltechna Warszawsa do:0.599/48.05.09.36 dosonalona metoda oblczana mocy traconej w tranzystorach wzmacnacza lasy AB Streszczene.
Julusz MDZELEWSK Wydzał Eletron Techn nformacyjnych, nstytut Radoeletron, oltechna Warszawsa do:0.599/48.05.09.36 dosonalona metoda oblczana mocy traconej w tranzystorach wzmacnacza lasy AB Streszczene.
relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
 1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
Wykład 2. Anna Ptaszek. 7 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 2. Anna Ptaszek 1 / 1
 Wykład 2 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 7 października 2015 1 / 1 Zjawiska koligatywne Rozpuszczenie w wodzie substancji nielotnej powoduje obniżenie prężności pary nasyconej P woda
Wykład 2 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 7 października 2015 1 / 1 Zjawiska koligatywne Rozpuszczenie w wodzie substancji nielotnej powoduje obniżenie prężności pary nasyconej P woda
chemia wykład 3 Przemiany fazowe
 Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Nieliniowe zadanie optymalizacji bez ograniczeń numeryczne metody iteracyjne optymalizacji
 Nelnowe zadane optymalzacj bez ogranczeń numeryczne metody teracyjne optymalzacj mn R n f ( ) = f Algorytmy poszuwana mnmum loalnego zadana programowana nelnowego: Bez ogranczeń Z ogranczenam Algorytmy
Nelnowe zadane optymalzacj bez ogranczeń numeryczne metody teracyjne optymalzacj mn R n f ( ) = f Algorytmy poszuwana mnmum loalnego zadana programowana nelnowego: Bez ogranczeń Z ogranczenam Algorytmy
obliczenie różnicy kwadratów odległości punktów po i przed odkształceniem - różniczka zupełna u i, j =1, 2, 3
 TEORI STNU ODKSZTŁCENI. WEKTOR RZEMIESZCZENI x u r r ' ' x stan p defrmacj x stan przed defrmacją płżene pt. przed defrmacją ( r) ( x, x, x ) płżene pt. p defrmacj ( r ) ( x, x, x ) przemeszczene puntu
TEORI STNU ODKSZTŁCENI. WEKTOR RZEMIESZCZENI x u r r ' ' x stan p defrmacj x stan przed defrmacją płżene pt. przed defrmacją ( r) ( x, x, x ) płżene pt. p defrmacj ( r ) ( x, x, x ) przemeszczene puntu
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
Wykład 5. przemysłu spożywczego- wykład 5
 Wykład spożywczego- wykład Katedra Inżynierii i Aparatury Przemysłu Spożywczego 4maja2014 1/1 Układy gaz-ciecz Rozpuszczalnośćwybranychgazówwcieczachw20 o Cw g/100g cieczy CIECZ H 2 N 2 O 2 CO 2 H 2 S
Wykład spożywczego- wykład Katedra Inżynierii i Aparatury Przemysłu Spożywczego 4maja2014 1/1 Układy gaz-ciecz Rozpuszczalnośćwybranychgazówwcieczachw20 o Cw g/100g cieczy CIECZ H 2 N 2 O 2 CO 2 H 2 S
Co to jest elektrochemia?
 Co to jest elektrochea? Dzał che zajujący sę reakcja checzny, który towarzyszy przenesene ładunku elektrycznego. Autoatyczne towarzyszą teu take zjawska, jak: Przepływ prądu elektrycznego, Powstawane gradentu
Co to jest elektrochea? Dzał che zajujący sę reakcja checzny, który towarzyszy przenesene ładunku elektrycznego. Autoatyczne towarzyszą teu take zjawska, jak: Przepływ prądu elektrycznego, Powstawane gradentu
OPTYMALIZACJA KOSZTÓW PRZEBUDOWY PORTFELA JAKO ZADANIE TRANSPORTOWE. 1. Problem badawczy
 B A D A N I A O P E R A C Y J N E I D E C Y Z J E Nr 2 2004 Krzysztof PIASECKI* OPTYALIZACJA KOSZTÓW PRZEBUDOWY PORTFELA JAKO ZADANIE TRANSPORTOWE Wszyste oszty generowane przez prowze malerse są włączone
B A D A N I A O P E R A C Y J N E I D E C Y Z J E Nr 2 2004 Krzysztof PIASECKI* OPTYALIZACJA KOSZTÓW PRZEBUDOWY PORTFELA JAKO ZADANIE TRANSPORTOWE Wszyste oszty generowane przez prowze malerse są włączone
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
ĆWICZENIE 1 BADANIE WYBRANYCH PROCEDUR I STRATEGII EKSPLOATACYJNYCH
 ĆWICNI BADANI WYBANYCH POCDU I STATGII KSPLOATACYJNYCH Cel ćwczena: - lustracja zagadneń zwązanych z zarządzanem esploatacją; - lustracja zależnośc mędzy dagnostyą nezawodnoścą a efetem procesu esploatacj.
ĆWICNI BADANI WYBANYCH POCDU I STATGII KSPLOATACYJNYCH Cel ćwczena: - lustracja zagadneń zwązanych z zarządzanem esploatacją; - lustracja zależnośc mędzy dagnostyą nezawodnoścą a efetem procesu esploatacj.
Część 1 7. TWIERDZENIA O WZAJEMNOŚCI 1 7. TWIERDZENIA O WZAJEMNOŚCI Twierdzenie Bettiego (o wzajemności prac)
 Część 1 7. TWIERDZENIA O WZAJEMNOŚCI 1 7. 7. TWIERDZENIA O WZAJEMNOŚCI 7.1. Twerdzene Bettego (o wzajemnośc prac) Nech na dowolny uład ramowy statyczne wyznaczalny lub newyznaczalny, ale o nepodatnych
Część 1 7. TWIERDZENIA O WZAJEMNOŚCI 1 7. 7. TWIERDZENIA O WZAJEMNOŚCI 7.1. Twerdzene Bettego (o wzajemnośc prac) Nech na dowolny uład ramowy statyczne wyznaczalny lub newyznaczalny, ale o nepodatnych
