Teresa Łuczak WYZNACZANIE MOLOWEJ ENTALPII REAKCJI ZOBOJĘTNIANIA
|
|
|
- Bogusław Krupa
- 8 lat temu
- Przeglądów:
Transkrypt
1 Ćwicni 2 Trsa Łuca WYZNACZANIE MOLOWE ENTALPII REAKCI ZOBOĘTNIANIA Zagadninia: Podstawow ojęcia trodynaicn: uład (iolowany, anięty, otwarty), otocni uładu, aratry stanu, wilości intnsywn i stnsywn, funcj stanu. Enrgia wwnętrna uładu i irwsa asada trodynaii. Entalia i równani irwsj asady trodynaii wyrażon a oocą ntalii. Efty nrgtycn w rianach gaów dosonałych: riana iobarycna, iochorycna, adiabatycna. Równani trochicn. Doświadcaln tody wynacania ciła racji orytria. Prawo Hssa (wyrowadni). Zalżność ciła racji od tratury. Entalia rouscania, hydratacji, rocińcania, obojętniania. Każdj racji chicnj towarysy obirani lub wydilani nrgii r uład. Badania ftów cilnych towarysących racjo chicny oirają się na rawach trochicnych, wyniających irwsj asady trodynaii. Enrgia wwnętrna uładu (U ) jst funcją aratrów stanu, natoiast raca i ciło w wilu rianach alżą od drogi dango rocsu i ni osiadają właściwości funcji stanu. Matatycn sforułowani irwsj asady trodynaii dla riany lntarnj achodącj w uładi anięty rdstawia równani: du = đ q + đ w + đ w (1) obj gdi đ q, đ wobj, đ w onacają odowidnio ciło, racę objętościową i racę niobjętościową w riani lntarnj (riani nisońcni ałj). Praca i ciło ni są funcjai stanu i at ich różnica jst niułna ( đ ). Zgodni ryjętą asadą naowania, dodatnią wartością dv wiąż się ujna wartość racy: đ w obj = dv (2) gdi, V onacają odowidnio ciśnini i objętość, natoiast dv = V V gdi: V, V to objętość odowidnio w stani ocątowy i ońcowy. Zat: du = đ q dv + đ w (3) W ryadu rocsu achodącgo w warunach iochorycnych ( d V = 0) b racy niobjętościowj ( w ), równani irwsj asady trodynaii urasca się do ostaci: d U = (đ q) = d (4) V q V Onaca to, ż iana nrgii wwnętrnj uładu równa jst wartości ciła wyiniongo otocni ( q V ). W ty ryadu ( V = const, w = 0 ) ciło uysuj właściwości funcji stanu i dla danj riany alży jdyni od stanu ocątowgo i stanu ońcowgo uładu. W ratyc więsość rian, a własca rocsy chicn, rowadi się od stały ciśnini. Stan uładu w rocsach iobarycnych dogodni jst oisywać a oocą funcji trodynaicnj wanj ntalią, dfiniowanj jao: H = U + V (5) 1
2 Entalia, odobni ja nrgia wwnętrna, jst funcją aratrów stanu i w riani sońconj alży tylo od stanu ocątowgo i ońcowgo uładu. Matatycn sforułowani irwsj asady trodynaii dla riany lntarnj achodącj w uładi anięty rdstawia równani: d H = đ q + V d + đ w (6) Gdy rocs rbiga w warunach iobarycnych ( d = 0 ) i ni wystęuj w ni raca niobjętościowa ( w = 0 ). Wówcas równani to ryjuj ostać: d H = (đ q) = d (7) q Z równania tgo ora irwsj asady trodynaii wynia, ż ry = const i w = 0, iana ntalii uładu jst równa wartości ciła wyiniongo otocni ( ). Onaca to, ż ciło uysuj właściwości funcji stanu i ni alży od drogi riany, a jdyni od stanu ocątowgo i ońcowgo uładu. żli w uładi rbiga racja chicna, T i V są stał, i w = 0, to różnica ułna nrgii wwnętrnj uładu U ( T, V, ξ) jst dana wor: U du d ξ (8) T,V gdi ξ licba ostęu racji. Z ołącnia uroscongo równania irwsj asady trodynaii (4) i równania (8) wynia: q q T, V d q d ξ T, V U T, V = r U [ ol 1 ] (9) Pochodna wyraża ilość ciła wyiniongo otocni r uład, w tóry achodi racja chicna, gdy achowan są waruni stałości tratury i objętości, a licba ostęu racji inia się o jdnostę. Stąd tę wilość ożna utożsaiać cił racji ry uładu T,V (d ξ q /d ) T, V U / ) T, V q T, V = const. Analogicni, ochodna ( ξ jst równa iani nrgii wwnętrnj ( ru), wiąanj rbigi racji chicnj, ry r U = ν U gdi nrgia wwnętrna dango ragnta. Roważając ntalię ragującgo uładu ( T,, ξ) T, = const, w = 0 otryujy: T, V = const i ξ = 1, ry cy ν wsółcynni stchiotrycny ragnta, U cąstowa olowa H i rouując analogicni ja wyżj, dla H d H d ξ (10) T, q T, d q d ξ T, H T, = r H [ ol 1 ] (11) Pochodna (d /d ξ) q T, rdstawia ilość ciła wyiniongo otocni r uład, w tóry achodi racja chicna w warunach stałości tratury i ciśninia, ry jdnostowj iani licby ostęu racji. Wilość ta jst utożsaiana cił racji q T, ry T, = const. dnocśni ochodna ( / ξ) jst równa iani ntalii uładu ( H) H T, wiąanj rbigi racji chicnj ry T, = const i ξ = 1. Z równania (11) wynia, ż 2
3 ciło racji q ry T, = const i ry ξ = 1 jst równ ntalii racji, ry cy H = ν H r T, gdi H cąstowa ntalia olowa ragnta. Równania (9) i (11) stanowią atatycną ostać odstawowgo rawa trochii rawa Hssa, tór ówi, ż ciło racji chicnj w warunach iotricno-iochorycnych lub iotricno-iobarycnych ry w = 0 ni alży od drogi rjścia lc od stanu ocątowgo i ońcowgo racji. Doładny oiar ciła racji ożliwy jst tylo dla niwilu tyów racji chicnych. Prcyyjn oiary orytrycn ożna wyonywać jdyni w ryadu racji rbigających sybo, do ońca i b rocsów ubocnych. Sybość racji owinna być taa, aby wydilani lub ochłaniani ciła nastęowało w róti orsi casu. Do taich racji nalży racja obojętniania. Procs obojętniania ocngo wasu ocną asadą, lub odwrotni, jst w istoci racją oiędy jonai H + i OH utworni cąstci wody H + (aq) + OH (aq) H 2 O(c) gdi indsy (aq) i (c) odnosą się odowidnio do rocińcongo rotworu wodngo i stanu ciłgo. Obsrwowany ft cilny w tj racji od stały ciśnini i w stałj tratur otocnia jst równy iani ntalii racji. Molową ntalię obojętniania (owstawania 1 ola + wody jonów H (aq) i OH (aq) onacono sybol H2 H. Eft cilny towarysący racji rotworu ocngo wasu rotwor ocnj asady jst wiąany ratycni wyłącni owstawani wody, a at ni alży od charatru chicngo ragujących sobą substancji, a wartość stałą. Natoiast odcas obojętniania rotworu słabj asady rotwor słabgo wasu lub odwrotni, suarycny ft cilny alży od rodaju ragujących sobą substancji bowi obo racji owstawania wody achodą rocsy ubocn, tai ja dysocjacja cy asocjacja. Dodatowo w obu ryadach ni ożna oinąć ftu nrgtycngo, tóry towarysy rocsowi rouscania ragntów (niscni sici rystalograficnj, solwatacja). Suarycny ft cilny obsrwowany w tai ryadu, odcas dodawania wasu do asady, lub odwrotni o rlicniu na 1 ol obojętnianj substancji onacono sybol H. Procs rouscania różni się od racji chicnj brai orślonych stosunów stchiotrycnych iędy sładniai rotworu. Rouscani substancji stałj w ciły rouscalniu jst suą dwóch rocsów cąstowych, ianowici: burnia sici rystalicnj substancji stałj ora solwatacji uwolnionych lntów sici. Pirwsy rocs wiąany jst ochłaniani ciła (ft nrgtycny onacany jao dodatni), ry cy użyta nrgia jst licbowo bliżona do ciła toninia cystj substancji. Natoiast rocs solwatacji jst wiąany oddawani ciła (ft nrgtycny onacany jao ujny). Zalżni więc od rwagi jdngo bądź drugigo rocsu suarycny ft cilny rouscania ciał stałych w ciłych rouscalniach będi dodatni lub ujny. Natoiast ry rouscaniu substancji ciłj w ciły rouscalniu nastęuj aws wydilani ciła wiąan rocs solwatacji (ft nrgtycny onacany jao ujny). Ciło wyinion odcas rouscania rlica się na 1 ol substancji rousconj. go wartość alży od charatru isanych substancji. Całowity ft cilny isania sładniów cystych ry T, = const równa się ntalii rocsu rouscania i naywany jst ntalią rouscania ( H ): o o = n H ( aq) H () roh = 1 [ o gdi H (, aq) standardowa ntalia sładnia w rotwor wodny, H o () standardowa ntalia cystgo sładnia, licba oli sładnia. n O ro, ] (12) 3
4 Wartości licbow ntalii rouscania roh otryuj się w bośrdni oiar orytrycny. Gdy ft nrgtycny wiąany badany rocs jst nacny, a jdnocśni rocs rbiga dużą sybością (ja n. rocs rouscania cy racja obojętniania), wówcas w oiarach rowadonych ry użyciu orytru diatricngo ożna anidbać straty lub ys ciła otocnia. żli owyżsy warun jst słniony, a rocsowi rouscania danj substancji w rouscalniu najdujący się w orytr towarysy ochłaniani nrgii na sosób ciła, to orślan jao dodatni ciło rouscania ( roh ) jst równ licbowo ciłu oddanu r uład orytrycny ( H), tóru ryisuj się na ujny. Gdy oli rocsowi rouscania substancji towarysy wydilani nrgii na sosób ciła, to orślan jao ujn ciło rouscania ( roh) jst równ licbowo ciłu obranu r uład orytrycny, tóru ryisuj się na dodatni ( H). Poniważ H = H (13) i H = c T = c ( T T ) ro (14) to H = c T = c T T ) (15) ro ( Powyżs roważania stosują się równiż ry wynacaniu ciła obojętniania. Wyonani ćwicnia Cl ćwicnia jst wynacni olowj ntalii obojętniania ( H ) siarowgo (VI) asadą otasową. Cl tn ożna raliować r: c, 1) wynacni śrdnij ojności cilnj orytru ( ) w racji wasu H 2 O 2) wynacni olowj ntalii rouscania wasu siarowgo (VI) ( H ), ro H2SO 4, 3) wynacni suarycngo ftu cilngo towarysącgo dodawaniu wasu siarowgo (VI) do rotworu asady otasowj, w rlicniu na 1 ol wasu siarowgo (VI) ( ). H Poiary rrowada się używając nacynia Dwara (łniącgo rolę orytru), wyosażongo w trotr i isadło. Ad 1) Wynacani śrdnij ojności cilnj orytru ( c ) Śrdnią ojność cilną uładu orytrycngo, wynaca się irąc ianę tratury uładu odcas rouscania substancji, jżli nana jst jj olowa ntalia rouscania. ro H roh c = c = (16) T gdi c ciło właściw atriałów, cęści sładowych uładu orytrycngo, o asi. W ćwicniu orysta się substancji o nanych wartościach olowj ntalii rouscania, n. NH 4 Cl i KCl: substancja olowa ntalia rouscania H [ ol 1 ] ro, alcana ilość substancji [g] NH 4 Cl 15,99 12 KCl 18,
5 Do nacynia Dwara wlwa się 300 c 3 wody dstylowanj i iry się jj traturę w odstęach co 10 s. Po ustalniu się tratury odcytuj się wartość T 0. Nastęni do nacynia Dwara wsyuj się odważoną ilość jdnj odanych w tabli 1 substancji (odważoną substancję rd wsyani do nacynia nalży rotrć w oźdiru) i ry ciągły isaniu notuj się traturę uładu co 10 s, aż do ontu jj ustalnia (uład osiąga traturę T 1 ). Odcyty tratury w casi rocsu rouscania uisca się w tabli. Ad 2) Wynacani olowj ntalii rouscania wasu siarowgo (VI) Do nacynia Dwara wlwa się 300 c 3 wody dstylowanj i iry się jj traturę co 10 s. Po ustalniu się tratury odcytuj się wartość T 0. Nastęni używając cylindra iarowgo wrowada się do nacynia Dwara 5 c3 stężongo wasu siarowgo (VI) ( ρ = 1,84 g c 3). Ziany tratury iron co 10 s w casi rocsu rouscania uisca się w tabli, odobni ja w unci 1. Ad 3) Wynacani olowj ntalii obojętniania w racji: H 2 SO KOH K2SO H 2 O Do lwi na 500 c 3 wlwa się 300 c 3 wody dstylowanj i rousca się w nij KOH w ilości otrbnj do obojętninia użytj ordnio ilości H 2 SO 4. Prygotowany rotwór KOH rlwa się do nacynia Dwara i ry ciągły isaniu notuj się traturę uładu co 10 s, aż do ontu jj ustalnia (T 0 ). Nastęni do nacynia Dwara wrowada się 5 c3 H 2 SO 4 i w sosób odany owyżj notuj się iany tratury aż do ustalnia się wartości T 1. Uwagi: W casi oiaru orywa nacynia Dwara usi być anięta. Kwas siarowy (VI) nalży wrowadać r otwór środowy orywy. Ilość wody użyta w oljnych onacniach usi być jdnaowa. Oblicnia 1) Oblicani śrdnij ojności cilnj orytru ( c ). Z woru (16) wynia, ż ft cilny roh wiąany rouscani substancji oisuj wyrażni: ro H = c T (17) Pry uwględniniu alżności (12): roh = n roh, i n = ntalię olową M rouscania użytj substancji, oisuj wyrażni: gdi n, M, M T roh, = c (18) onacają odowidnio licbę oli, asę [g] ora asę olową [g ol 1] użytj substancji (NH 4 Cl lub KCl). Z rstałcnia tgo woru wynia: roh, c = (19) M T W clu nalinia wartości T = 1T sorąda się wyrs alżności tratury (T ) od casu ( t ). Z wyrsu odcytuj się 1T jao różnicę T1 T0 w rocsi rouscania soli sosób odany na rys. 1 i oisany oniżj. B wględu na rodaj orytru, oiar orytrycny słada się trch orsów: ocątowgo, główngo i ońcowgo. Ors ocątowy to cas od roocęcia obsrwacji 5
6 ian tratury do aocątowania badanj riany. Od tj chwili do uysania asyalnj tratury trwa ors główny. Bośrdnio o ni nastęuj ors ońcowy, tóry trwa do chwili aońcnia odcytów tratury. Aby wynacyć wartość T = 1T sorąda się wyrs alżności tratury T od casu t (rywa abcd ), a nastęni wyrśla się dwi stycn równolgł do tj rywj rchodąc r unty odowiadając orsowi ocątowu (odcin ab ) i ońcowu (odcin cd ). Wyrślon stycn rdłuża się odowidnio stronę więsych i nijsych wartości casu uysując rost oocnic I i II, tór nastęni łący się rostą f orowadoną rostoadl do osi odciętych. Wyrśla się środową odcina f w tai sosób, aby długości odcinów g i gf były równ. Wynacony w tn sosób odcin f jdnonacni orśla wartość T = 1T = T 1 T 0. Wartości tratur w untach (T 0 ) i f ( T 1 ) odcytuj się wyrsu o straolacji do t = 0. T 1 II c d T [K] g T 0 a b f I t [s] Rys. 1. Graficny sosób wynacania T = T 1 T0 2) Oblicani olowj ntalii rouscania wasu siarowgo (VI) ( H ). ro H2SO 4, Wartość tę wynaca się orystając woru (18) i orślając wartość 2 T r sorądni wyrsu rdstawiającgo ianę tratury w rocsi rouscania wasu siarowgo (VI) od casu. 3) Oblicani olowj ntalii obojętniania w racji wasu siarowgo (VI) asadą otasową. Na suarycny ft cilny towarysący dodawaniu H 2 SO 4 do rotworu KOH (w słada się rlicniu na 1 ol wasu siarowgo (VI), onacany sybol ( ) H ntalia olowa rouscania wasu siarowgo (VI) ( ) i ntalia roh H2 SO 4, owstawania 2 oli wody. W wor 20 sybol H2 H onacono olową ntalię owstawania 1 ola H2O. Zat: H = rohh2so 4, + H2O 2 H Po odcytaniu 3 T wyrsu ian tratury od casu (analogicni ja w untach 1 i 2) oblica się suarycny ft cilny odcas dodawania wasu siarowgo (VI) do rotworu asady otasowj: O (20) 6
7 cmh2so 4 3T H = (21) H2SO 4 Korystając orślonych sryntalni wartości woru (20) ożna wylicyć H2 H. O i H o rstałcniu H ro H2SO 4, Uysan w untach 1, 2, i 3 wynii stawia się w tabli. Nalży ałożyć, ż główny źródł błędów odcas wynacania c, H, H2 OH są błędy wyniając oiarów ro H2SO 4, wilości T (w t. 1, 2 i 3), a inn wilości wynacan są błędai anidbywani ałyi. 7
CIŚNIENIE W PŁASKIM ŁOŻYSKU ŚLIZGOWYM PRZY NIESTACJONARNYM LAMINARNYM SMAROWANIU
 MODEOWANIE INŻYNIERSIE ISSN 896-77X, s. -6, Gliwic 7 CIŚNIENIE W PŁASIM ŁOŻYSU ŚIZGOWYM PRZY NIESTACJONARNYM AMINARNYM SMAROWANIU PAWEŁ RASOWSI atdra Podstaw Tcnii, Aadmia Morsa -mail: awras@am.gdynia.l
MODEOWANIE INŻYNIERSIE ISSN 896-77X, s. -6, Gliwic 7 CIŚNIENIE W PŁASIM ŁOŻYSU ŚIZGOWYM PRZY NIESTACJONARNYM AMINARNYM SMAROWANIU PAWEŁ RASOWSI atdra Podstaw Tcnii, Aadmia Morsa -mail: awras@am.gdynia.l
ćwiczenie 211 Hardware'owa realizacja automatu z parametrem wewnętrznym 1. Synteza strukturalna automatu z parametrem wewnętrznym
 ATEDA INFOMATYI TEHNIZNE Ćwicnia laoratoryjn Logiki Układów yfrowych ćwicni Tmat: Hardwarowa raliacja automatu paramtrm wwnętrnym. ynta strukturalna automatu paramtrm wwnętrnym Punktm wyjścia synty strukturalnj
ATEDA INFOMATYI TEHNIZNE Ćwicnia laoratoryjn Logiki Układów yfrowych ćwicni Tmat: Hardwarowa raliacja automatu paramtrm wwnętrnym. ynta strukturalna automatu paramtrm wwnętrnym Punktm wyjścia synty strukturalnj
Termodynamika. Część 10. Elementy fizyki statystycznej klasyczny gaz doskonały. Janusz Brzychczyk, Instytut Fizyki UJ
 Trodynaika Część 1 Elnty fizyki statystycznj klasyczny gaz doskonały Janusz Brzychczyk, Instytut Fizyki UJ Użytczn całki ax2 dx = 1 2 a x ax2 dx = 1 2a ax2 dx = a a x 2 ax2 dx = 1 4a a x 3 ax2 dx = 1 2a
Trodynaika Część 1 Elnty fizyki statystycznj klasyczny gaz doskonały Janusz Brzychczyk, Instytut Fizyki UJ Użytczn całki ax2 dx = 1 2 a x ax2 dx = 1 2a ax2 dx = a a x 2 ax2 dx = 1 4a a x 3 ax2 dx = 1 2a
Róża wiatrów - zestawienie tabelaryczne częstości występowania sytuacji meteorologicznych dla 12 głównych kierunków wiatru. Sytuacje meteorologiczne
 OBLICZENIA POZIOMÓW SUBSTANCJI W POWIETRZU (METODYKA REFERENCYJNA) Dan do oblicń oioów sbstancji w owitr Lokaliacja obikt rodaj obsar ora ty okrycia trn, rodaj abdowy (ilość i wysokość kondygnacji), granic
OBLICZENIA POZIOMÓW SUBSTANCJI W POWIETRZU (METODYKA REFERENCYJNA) Dan do oblicń oioów sbstancji w owitr Lokaliacja obikt rodaj obsar ora ty okrycia trn, rodaj abdowy (ilość i wysokość kondygnacji), granic
Układ termodynamiczny
 Uład terodynaiczny Uład terodynaiczny to ciało lub zbiór rozważanych ciał, w tóry obo wszelich innych zjawis (echanicznych, eletrycznych, agnetycznych itd.) uwzględniay zjawisa cieplne. Stan uładu charateryzuje
Uład terodynaiczny Uład terodynaiczny to ciało lub zbiór rozważanych ciał, w tóry obo wszelich innych zjawis (echanicznych, eletrycznych, agnetycznych itd.) uwzględniay zjawisa cieplne. Stan uładu charateryzuje
W-24 (Jaroszewicz) 22 slajdy Na podstawie prezentacji prof. J. Rutkowskiego. Cząstka w studni potencjału. przykłady efektu tunelowego
 Kyongju, Kora, April 999 W-4 (Jaroszwicz) slajdy Na podstawi przntacji prof. J. Rutowsigo Fizya wantowa 3 Cząsta w studni potncjału sończona studnia potncjału barira potncjału barira potncjału o sończonj
Kyongju, Kora, April 999 W-4 (Jaroszwicz) slajdy Na podstawi przntacji prof. J. Rutowsigo Fizya wantowa 3 Cząsta w studni potncjału sończona studnia potncjału barira potncjału barira potncjału o sończonj
Wykład Przemiany gazu idealnego
 Wykład 4 2.6 Przmiany gazu idalngo Zmiana stanu gazu idalngo moż odbywać się rzy różnych warunkach narzuconych na odstawow aramtry oisując stan gazu. Ogólną rzmianę gazu rzy zmiani rzynajmnij dwóch aramtrów
Wykład 4 2.6 Przmiany gazu idalngo Zmiana stanu gazu idalngo moż odbywać się rzy różnych warunkach narzuconych na odstawow aramtry oisując stan gazu. Ogólną rzmianę gazu rzy zmiani rzynajmnij dwóch aramtrów
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1. Kontakt,informacja i konsultacje. Co to jest chemia fizyczna?
 Chemia Fizyczna Technologia Chemiczna II ro Wyład 1 Kierowni rzedmiotu: Dr hab. inż. Wojciech Chrzanowsi Kontat,informacja i onsultacje Chemia A ; oój 307 Telefon: 347-2769 E-mail: wojte@chem.g.gda.l tablica
Chemia Fizyczna Technologia Chemiczna II ro Wyład 1 Kierowni rzedmiotu: Dr hab. inż. Wojciech Chrzanowsi Kontat,informacja i onsultacje Chemia A ; oój 307 Telefon: 347-2769 E-mail: wojte@chem.g.gda.l tablica
ZASTOSOWANIE SZTUCZNYCH SIECI NEURONOWYCH W DOBORZE FUNKCJI NAPĘDOWYCH ŻURAWI NA PODATNYM PODŁOŻU
 acta chanica t autoatica vol. no. () ZASOSOWAI SZUCZYCH SICI UROOWYCH W DOBORZ FUKCJI APĘDOWYCH ŻURAWI A PODAYM PODŁOŻU Andr URBAŚ * Mar SZCZOKA * * Katdra Inforatyi Stosowan Wydiał Zarądania i Inforatyi
acta chanica t autoatica vol. no. () ZASOSOWAI SZUCZYCH SICI UROOWYCH W DOBORZ FUKCJI APĘDOWYCH ŻURAWI A PODAYM PODŁOŻU Andr URBAŚ * Mar SZCZOKA * * Katdra Inforatyi Stosowan Wydiał Zarądania i Inforatyi
UZUPEŁNIENIA DO WYKŁADÓW A-C
 UZUPEŁNIENIA DO WYKŁADÓW A-C Objaśnienia: 1. Uzupełnienia sładają się z dwóch części właściwych uzupełnień do treści wyładowych, zwyle zawierających wyprowadzenia i nietóre definicje oraz Zadań i problemów.
UZUPEŁNIENIA DO WYKŁADÓW A-C Objaśnienia: 1. Uzupełnienia sładają się z dwóch części właściwych uzupełnień do treści wyładowych, zwyle zawierających wyprowadzenia i nietóre definicje oraz Zadań i problemów.
Iwona śak, Paweł Niemiec
 8. ROZTWORY BUFOROWE Iwona śa, Paweł Niemiec Rotwory buforowe posiadają dolność buforowania, tn. preciwstawiania się nacnym mianom ph po dodaniu do nich niewielich ilości mocnego wasu lub mocnej asady.
8. ROZTWORY BUFOROWE Iwona śa, Paweł Niemiec Rotwory buforowe posiadają dolność buforowania, tn. preciwstawiania się nacnym mianom ph po dodaniu do nich niewielich ilości mocnego wasu lub mocnej asady.
3. Kinematyka podstawowe pojęcia i wielkości
 3. Kinematya odstawowe ojęcia i wielości Kinematya zajmuje się oisem ruchu ciał. Ruch ciała oisujemy w ten sosób, że odajemy ołożenie tego ciała w ażdej chwili względem wybranego uładu wsółrzędnych. Porawny
3. Kinematya odstawowe ojęcia i wielości Kinematya zajmuje się oisem ruchu ciał. Ruch ciała oisujemy w ten sosób, że odajemy ołożenie tego ciała w ażdej chwili względem wybranego uładu wsółrzędnych. Porawny
Dodawanie i mnożenie liczb zespolonych są działaniami wewnętrznymi tzn., że ich wynikiem jest liczba zespolona.
 Wykład - LICZBY ZESPOLONE Algebra licb espolonych, repreentacja algebraicna i geometrycna, geometria licb espolonych. Moduł, argument, postać trygonometrycna, wór de Moivre a.' Zbiór Licb Zespolonych Niech
Wykład - LICZBY ZESPOLONE Algebra licb espolonych, repreentacja algebraicna i geometrycna, geometria licb espolonych. Moduł, argument, postać trygonometrycna, wór de Moivre a.' Zbiór Licb Zespolonych Niech
Rozkład Maxwell a prędkości cząsteczek gazu Prędkości poszczególnych cząsteczek mogą być w danej chwili dowolne
 Rozkład Maxwll a rędkośi ząstzk gazu 9-9. Rozkład Maxwll a rędkośi ząstzk gazu Prędkośi oszzgólnyh ząstzk ogą być w danj hwili dowoln 3 a tylko rędkość śrdnia kwadratowa wynosi sk. Można się jdnak sodziwać,
Rozkład Maxwll a rędkośi ząstzk gazu 9-9. Rozkład Maxwll a rędkośi ząstzk gazu Prędkośi oszzgólnyh ząstzk ogą być w danj hwili dowoln 3 a tylko rędkość śrdnia kwadratowa wynosi sk. Można się jdnak sodziwać,
Ćw. 5. Badanie ruchu wahadła sprężynowego sprawdzenie wzoru na okres drgań
 KAEDRA FIZYKI SOSOWANEJ PRACOWNIA 5 FIZYKI Ćw. 5. Badanie ruchu wahadła sprężynowego sprawdzenie wzoru na ores drgań Wprowadzenie Ruch drgający naeży do najbardziej rozpowszechnionych ruchów w przyrodzie.
KAEDRA FIZYKI SOSOWANEJ PRACOWNIA 5 FIZYKI Ćw. 5. Badanie ruchu wahadła sprężynowego sprawdzenie wzoru na ores drgań Wprowadzenie Ruch drgający naeży do najbardziej rozpowszechnionych ruchów w przyrodzie.
Entalpia swobodna (potencjał termodynamiczny)
 Entalia swobodna otencjał termodynamiczny. Związek omiędzy zmianą entalii swobodnej a zmianami entroii Całkowita zmiana entroii wywołana jakimś rocesem jest równa sumie zmiany entroii układu i otoczenia:
Entalia swobodna otencjał termodynamiczny. Związek omiędzy zmianą entalii swobodnej a zmianami entroii Całkowita zmiana entroii wywołana jakimś rocesem jest równa sumie zmiany entroii układu i otoczenia:
WAHADŁO SPRĘŻYNOWE. POMIAR POLA ELIPSY ENERGII.
 ĆWICZENIE 3. WAHADŁO SPRĘŻYNOWE. POMIAR POLA ELIPSY ENERGII. 1. Oscylator harmoniczny. Wprowadzenie Oscylatorem harmonicznym nazywamy punt materialny, na tóry,działa siła sierowana do pewnego centrum,
ĆWICZENIE 3. WAHADŁO SPRĘŻYNOWE. POMIAR POLA ELIPSY ENERGII. 1. Oscylator harmoniczny. Wprowadzenie Oscylatorem harmonicznym nazywamy punt materialny, na tóry,działa siła sierowana do pewnego centrum,
MASA ATOMOWA STECHIOMETRIA
 MASA ATOMOWA wzorce: J. Dalton wodór J.J. Berzelius tlen od 1961 r. skala oparta na węglu 12 { 12 98,89%; 13 1,11%} 12 6 ato 6n + 6p + 6e Jednostka asy atoowej jest to 1 / 12 asy atou węgla 12 j..a. 1
MASA ATOMOWA wzorce: J. Dalton wodór J.J. Berzelius tlen od 1961 r. skala oparta na węglu 12 { 12 98,89%; 13 1,11%} 12 6 ato 6n + 6p + 6e Jednostka asy atoowej jest to 1 / 12 asy atou węgla 12 j..a. 1
(Ćwiczenie nr 4) Wpływ siły jonowej roztworu na stałą szybkości reakcji.
 (Ćwiczenie nr 4) Wpływ siły jonowej roztworu na stałą szybości reacji Wstęp Rozpatrzmy reację zachodzącą w roztworze pomiędzy jonami i w wyniu tórej powstaje produt D: D stała szybości reacji () Gdy reacja
(Ćwiczenie nr 4) Wpływ siły jonowej roztworu na stałą szybości reacji Wstęp Rozpatrzmy reację zachodzącą w roztworze pomiędzy jonami i w wyniu tórej powstaje produt D: D stała szybości reacji () Gdy reacja
Algebra liniowa z geometrią analityczną
 WYKŁAD. Elmtar fucj mij spoloj: wilomiay, pirwiasti jdości, fucja: pirwiast stopia, fucja wyładica, fucja logarytmica. Podstawow własości wilomiaów: podilość, twirdi Bout, podstawow twirdi algbry, suai
WYKŁAD. Elmtar fucj mij spoloj: wilomiay, pirwiasti jdości, fucja: pirwiast stopia, fucja wyładica, fucja logarytmica. Podstawow własości wilomiaów: podilość, twirdi Bout, podstawow twirdi algbry, suai
WARSZTATY olimpijskie. Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna Kinetyka
 WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
Swobodny spadek ciał w ośrodku stawiającym opór
 Ryszard Chybici Swobodny spad ciał w ośrodu stawiający opór (Posłuiwani się przz osoby trzci ty artyuł lub jo istotnyi frantai bz widzy autora jst wzbronion) Milc, 005 Swobodny spad ciała ośrodu stawiający
Ryszard Chybici Swobodny spad ciał w ośrodu stawiający opór (Posłuiwani się przz osoby trzci ty artyuł lub jo istotnyi frantai bz widzy autora jst wzbronion) Milc, 005 Swobodny spad ciała ośrodu stawiający
( ) + ( ) T ( ) + E IE E E. Obliczanie gradientu błędu metodą układu dołączonego
 Obliczanie gradientu błędu metodą uładu dołączonego /9 Obliczanie gradientu błędu metodą uładu dołączonego Chodzi o wyznaczenie pochodnych cząstowych funcji błędu E względem parametrów elementów uładu
Obliczanie gradientu błędu metodą uładu dołączonego /9 Obliczanie gradientu błędu metodą uładu dołączonego Chodzi o wyznaczenie pochodnych cząstowych funcji błędu E względem parametrów elementów uładu
GAZY DOSKONAŁE I PÓŁDOSKONAŁE
 TERMODYNAMIKA GAZY DOSKONAŁE I PÓŁDOSKONAŁE Prawo Boyle a Marotte a p V = const gdy T = const Prawo Gay-Lussaca V = const gdy p = const T Równane stanu gau dosonałego półdosonałego p v = R T gde: p cśnene
TERMODYNAMIKA GAZY DOSKONAŁE I PÓŁDOSKONAŁE Prawo Boyle a Marotte a p V = const gdy T = const Prawo Gay-Lussaca V = const gdy p = const T Równane stanu gau dosonałego półdosonałego p v = R T gde: p cśnene
STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia!
 STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia! 001 Obliczyć stężenie molowe jonów Ca 2+ w roztworze zawierającym 2,22g CaCl2 w 100 ml roztworu, przyjmując a = 100%. 002
STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia! 001 Obliczyć stężenie molowe jonów Ca 2+ w roztworze zawierającym 2,22g CaCl2 w 100 ml roztworu, przyjmując a = 100%. 002
PLAN WYKŁADU. Sposoby dochodzenia do stanu nasycenia. Procesy izobaryczne
 PLAN WYKŁADU Sooby dochodznia do tanu naycnia Procy izobaryczn Ochładzani izobaryczn (mratura unktu roy) Ochładzani rzz izobaryczn i adiabatyczn wyarowani/kondnację wody (mratura wilgotngo trmomtru, mratura
PLAN WYKŁADU Sooby dochodznia do tanu naycnia Procy izobaryczn Ochładzani izobaryczn (mratura unktu roy) Ochładzani rzz izobaryczn i adiabatyczn wyarowani/kondnację wody (mratura wilgotngo trmomtru, mratura
Ciśnienie i nośność w płaskim łożysku ślizgowym przy niestacjonarnym laminarnym smarowaniu
 TRIBOOGIA ZAGADNIENIA EKSPOATACJI MASZYN Zesyt (5) 7 PAWEŁ KRASOWSKI Ciśnienie i nośność w łasim łożysu śligowym ry niestacjonarnym laminarnym smarowaniu Słowa lucowe Płasie łożyso śligowe, laminarne niestacjonarne
TRIBOOGIA ZAGADNIENIA EKSPOATACJI MASZYN Zesyt (5) 7 PAWEŁ KRASOWSKI Ciśnienie i nośność w łasim łożysu śligowym ry niestacjonarnym laminarnym smarowaniu Słowa lucowe Płasie łożyso śligowe, laminarne niestacjonarne
Temat: Prawo Hooke a. Oscylacje harmoniczne. Zagadnienia: prawa dynamiki Newtona, siła sprężysta, prawo Hooke a, oscylacje harmoniczne,
 sg M 6-1 - Teat: Prawo Hooe a. Oscylacje haroniczne. Zagadnienia: prawa dynaii Newtona, siła sprężysta, prawo Hooe a, oscylacje haroniczne, ores oscylacji. Koncepcja: Sprężyna obciążana różnyi asai wydłuża
sg M 6-1 - Teat: Prawo Hooe a. Oscylacje haroniczne. Zagadnienia: prawa dynaii Newtona, siła sprężysta, prawo Hooe a, oscylacje haroniczne, ores oscylacji. Koncepcja: Sprężyna obciążana różnyi asai wydłuża
M A N I P U L A T O R Y Przestrzenne Analiza kinematyczna
 N I P U L O Y Prstrnn nalia inmatcna Wsółrędn absolutn (artańsi) aniulator łasi r r r r r r acir rotaci Wrsor r r r r Prstałcni dnorodn q wtor wsółrędnch absolutnch KINEYK NIPULOÓW PZESZENNYCH 5 Wsółrędn
N I P U L O Y Prstrnn nalia inmatcna Wsółrędn absolutn (artańsi) aniulator łasi r r r r r r acir rotaci Wrsor r r r r Prstałcni dnorodn q wtor wsółrędnch absolutnch KINEYK NIPULOÓW PZESZENNYCH 5 Wsółrędn
relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
 1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
PODSTAWY AUTOMATYKI 9. Wskaźniki jakości regulacji
 Politchnia Warawa Intytut Automatyi i obotyi Prof. dr hab. inż. Jan Macij Kościlny PDSTAWY AUTMATYKI 9. Waźnii jaości rgulacji Wymagania tawian uładom rgulacji 2 Stabilność Wymagania tatycn Wymagania dynamicn
Politchnia Warawa Intytut Automatyi i obotyi Prof. dr hab. inż. Jan Macij Kościlny PDSTAWY AUTMATYKI 9. Waźnii jaości rgulacji Wymagania tawian uładom rgulacji 2 Stabilność Wymagania tatycn Wymagania dynamicn
Granica funkcji - Lucjan Kowalski GRANICA FUNKCJI
 GRANICA FUNKCJI Granica uncji. - dowolna liczba rzczywista. O, = - ; + - otoczni liczby puntu o prominiu, S, = - ;, + - sąsidztwo liczby puntu o prominiu, Nich uncja będzi orślona w sąsidztwi puntu, g
GRANICA FUNKCJI Granica uncji. - dowolna liczba rzczywista. O, = - ; + - otoczni liczby puntu o prominiu, S, = - ;, + - sąsidztwo liczby puntu o prominiu, Nich uncja będzi orślona w sąsidztwi puntu, g
Ćw. 22: Pomiary magnetyczne
 Wydiał: EAIiE Kierune: Iię i naio (e ail): Ro:. (00/0) Grua: Zeół: Data yonania: Zalienie: odi roadąego: agi: LABORATORIM METROLOGII Ć. : oiary agnetyne Wtę Cele ćienia jet aonanie ię etodai oiaru ybrany
Wydiał: EAIiE Kierune: Iię i naio (e ail): Ro:. (00/0) Grua: Zeół: Data yonania: Zalienie: odi roadąego: agi: LABORATORIM METROLOGII Ć. : oiary agnetyne Wtę Cele ćienia jet aonanie ię etodai oiaru ybrany
RUCH DRGAJĄCY. Ruch harmoniczny. dt A zatem równanie różniczkowe ruchu oscylatora ma postać:
 RUCH DRGAJĄCY Ruch haroniczny Ruch, tóry owtarza się w regularnych odstęach czasu, nazyway ruche oresowy (eriodyczny). Szczególny rzyadie ruchu oresowego jest ruch haroniczny: zależność rzeieszczenia od
RUCH DRGAJĄCY Ruch haroniczny Ruch, tóry owtarza się w regularnych odstęach czasu, nazyway ruche oresowy (eriodyczny). Szczególny rzyadie ruchu oresowego jest ruch haroniczny: zależność rzeieszczenia od
Oddziaływanie elektronu z materią
 Oddiaływani lktronu matrią p p X-ray p wt wt A wt p - lktron pirwotny, 0-3000V. wt - lktron wtórny, 0-0 V. A- lktron Augr a, 0-000V. X-ray- proiowani X, 000-000V. - plamon, 0-80 V. - fonon, 0,0-0,5V. Zdrni
Oddiaływani lktronu matrią p p X-ray p wt wt A wt p - lktron pirwotny, 0-3000V. wt - lktron wtórny, 0-0 V. A- lktron Augr a, 0-000V. X-ray- proiowani X, 000-000V. - plamon, 0-80 V. - fonon, 0,0-0,5V. Zdrni
Metody probabilistyczne Rozwiązania zadań
 Metody robabilistyczne Rozwiązania zadań 6. Momenty zmiennych losowych 8.11.2018 Zadanie 1. Poaż, że jeśli X Bn, to EX n. Odowiedź: X rzyjmuje wartości w zbiorze {0, 1,..., n} z rawdoodobieństwami zadanymi
Metody robabilistyczne Rozwiązania zadań 6. Momenty zmiennych losowych 8.11.2018 Zadanie 1. Poaż, że jeśli X Bn, to EX n. Odowiedź: X rzyjmuje wartości w zbiorze {0, 1,..., n} z rawdoodobieństwami zadanymi
SYSTEMY ROZPOZNANIA I WALKI ELEKTRONICZNEJ SOCZEWKA CZERWCA 2006
 SYSTMY ROZPOZNANA WALK LKTRONCZNJ SOCZWKA CZRWCA 6 WYKORZYSTAN FKTU OPPLRA W SYSTMACH LOKALZACJ ŹRÓŁ PROMNOWANA FAL RAOWYCH dr inż. Cary ZÓŁKOWSK pro. dr hab. inż. Władysław KOŁOSOWSK mr inż. Jan M. KLNR
SYSTMY ROZPOZNANA WALK LKTRONCZNJ SOCZWKA CZRWCA 6 WYKORZYSTAN FKTU OPPLRA W SYSTMACH LOKALZACJ ŹRÓŁ PROMNOWANA FAL RAOWYCH dr inż. Cary ZÓŁKOWSK pro. dr hab. inż. Władysław KOŁOSOWSK mr inż. Jan M. KLNR
W MIARECZKOWANIU MOCNEGO KWASU MOCNĄ ZASADĄ W MIARECZKOWANIU SŁABEGO KWASU MOCNĄ ZASADĄ
 miareowanie W MIARECZKOWANIU MOCNEGO KWASU MOCNĄ ZASADĄ PUNKT RÓWNOWAŻNIKOWY OSIĄGA SIĘ PO ZRÓWNOWAŻENIU STĘŻEŃ REAGENTÓW PRODUKTEM JEST SÓL MOCNEGO KWASU I MOCNEJ ZASADY, A w PUNKCIE RÓWNOWAŻNIKOWYM WYNOSI
miareowanie W MIARECZKOWANIU MOCNEGO KWASU MOCNĄ ZASADĄ PUNKT RÓWNOWAŻNIKOWY OSIĄGA SIĘ PO ZRÓWNOWAŻENIU STĘŻEŃ REAGENTÓW PRODUKTEM JEST SÓL MOCNEGO KWASU I MOCNEJ ZASADY, A w PUNKCIE RÓWNOWAŻNIKOWYM WYNOSI
Reakcje chemiczne. Typ reakcji Schemat Przykłady Reakcja syntezy
 Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
TEORIA OBWODÓW I SYGNAŁÓW LABORATORIUM
 EORI OBWODÓW I SYGNŁÓW LBORORIUM KDEMI MORSK Katedra eleomuniacji Morsiej Ćwiczenie nr 2: eoria obwodów i sygnałów laboratorium ĆWICZENIE 2 BDNIE WIDM SYGNŁÓW OKRESOWYCH. Cel ćwiczenia Celem ćwiczenia
EORI OBWODÓW I SYGNŁÓW LBORORIUM KDEMI MORSK Katedra eleomuniacji Morsiej Ćwiczenie nr 2: eoria obwodów i sygnałów laboratorium ĆWICZENIE 2 BDNIE WIDM SYGNŁÓW OKRESOWYCH. Cel ćwiczenia Celem ćwiczenia
... Nazwisko, imię zawodnika; Klasa Liczba punktów. ... Nazwa szkoły, miejscowość. I Podkarpacki Konkurs Chemiczny 2008/09
 ......... Nazwisko, imię zawodnika; Klasa Liczba punktów KOPKCh... Nazwa szkoły, miejscowość I Podkarpacki Konkurs Chemiczny 2008/09 ETAP III 28.02.2009 r. Godz. 10.00-13.00 Zadanie 1 (10 pkt.) ( postaw
......... Nazwisko, imię zawodnika; Klasa Liczba punktów KOPKCh... Nazwa szkoły, miejscowość I Podkarpacki Konkurs Chemiczny 2008/09 ETAP III 28.02.2009 r. Godz. 10.00-13.00 Zadanie 1 (10 pkt.) ( postaw
TWIERDZENIA O WZAJEMNOŚCIACH
 1 Olga Kopac, Adam Łodygows, Wojcech Pawłows, Mchał Płotowa, Krystof Tymber Konsultacje nauowe: prof. dr hab. JERZY RAKOWSKI Ponań 2002/2003 MECHANIKA BUDOWI 7 ACH TWIERDZENIE BETTIEGO (o wajemnośc prac)
1 Olga Kopac, Adam Łodygows, Wojcech Pawłows, Mchał Płotowa, Krystof Tymber Konsultacje nauowe: prof. dr hab. JERZY RAKOWSKI Ponań 2002/2003 MECHANIKA BUDOWI 7 ACH TWIERDZENIE BETTIEGO (o wajemnośc prac)
CHARAKTERYSTYKI CZASOWE UKŁADÓW DYNAMICZNYCH
 CHARAKERYSYKI CZASOWE UKŁADÓW DYNAMICZNYCH Zadani Chararyyi czaow uładów. Odpowidź oową wyznacza ię z wzoru: { } Problm: h L G X Wyznaczyć odpowidz oową i impulową całującgo z inrcją G h L G gdzi: Y X
CHARAKERYSYKI CZASOWE UKŁADÓW DYNAMICZNYCH Zadani Chararyyi czaow uładów. Odpowidź oową wyznacza ię z wzoru: { } Problm: h L G X Wyznaczyć odpowidz oową i impulową całującgo z inrcją G h L G gdzi: Y X
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyi i Ochrony Środowisa Studia stacjonarne, Ro I, Semestr zimowy 01/14 Dr hab. inż. Tomasz Brylewsi e-mail: brylew@agh.edu.pl tel. 1-617-59 atedra Fizyochemii
Chemia - laboratorium Wydział Geologii, Geofizyi i Ochrony Środowisa Studia stacjonarne, Ro I, Semestr zimowy 01/14 Dr hab. inż. Tomasz Brylewsi e-mail: brylew@agh.edu.pl tel. 1-617-59 atedra Fizyochemii
Opracowała: mgr inż. Ewelina Nowak
 Mateiały dydaktyczne na zajęcia wyównawcze z cheii dla studentów piewszego oku kieunku zaawianego Inżynieia Śodowiska w aach pojektu Ea inżyniea pewna lokata na pzyszłość Opacowała: g inż. Ewelina Nowak
Mateiały dydaktyczne na zajęcia wyównawcze z cheii dla studentów piewszego oku kieunku zaawianego Inżynieia Śodowiska w aach pojektu Ea inżyniea pewna lokata na pzyszłość Opacowała: g inż. Ewelina Nowak
Ćwiczenie PA6. Badanie działania regulatora PID zaimplementowanego w sterowniku S7-1200 firmy Siemens
 INSYU AUOMAYKI i ROBOYKI WYDZIAŁ MECHARONIKI - laboratorium Ćwiczni PA6 Badani działania rgulatora PID zaimplmntowango w strowniu S7-00 firmy Simns Instrucja laboratoryjna Opracowani : dr inż. Danuta Holjo
INSYU AUOMAYKI i ROBOYKI WYDZIAŁ MECHARONIKI - laboratorium Ćwiczni PA6 Badani działania rgulatora PID zaimplmntowango w strowniu S7-00 firmy Simns Instrucja laboratoryjna Opracowani : dr inż. Danuta Holjo
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
Przejścia międzypasmowe
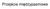 Pzjścia iędzypasow Funcja diltyczna Pzjścia iędzypasow związan są z polayzacją cuy ltonowj wwnątz dzni atoowyc - są odpowidzialn za część funcji diltycznj ε Wóćy do foalizu funcji diltycznj: ε las N (
Pzjścia iędzypasow Funcja diltyczna Pzjścia iędzypasow związan są z polayzacją cuy ltonowj wwnątz dzni atoowyc - są odpowidzialn za część funcji diltycznj ε Wóćy do foalizu funcji diltycznj: ε las N (
Wykres linii ciśnień i linii energii (wykres Ancony)
 Wyres linii ciśnień i linii energii (wyres Ancony) W wyorzystywanej przez nas do rozwiązywania problemów inżyniersich postaci równania Bernoulliego występuje wysoość prędości (= /g), wysoość ciśnienia
Wyres linii ciśnień i linii energii (wyres Ancony) W wyorzystywanej przez nas do rozwiązywania problemów inżyniersich postaci równania Bernoulliego występuje wysoość prędości (= /g), wysoość ciśnienia
Podstawy Automatyki Zbiór zadań dla studentów II roku AiR oraz MiBM
 Aademia GórniczoHutnicza im. St. Staszica w Kraowie Wydział Inżynierii Mechanicznej i Robotyi Katedra Automatyzacji Procesów Podstawy Automatyi Zbiór zadań dla studentów II rou AiR oraz MiBM Tomasz Łuomsi
Aademia GórniczoHutnicza im. St. Staszica w Kraowie Wydział Inżynierii Mechanicznej i Robotyi Katedra Automatyzacji Procesów Podstawy Automatyi Zbiór zadań dla studentów II rou AiR oraz MiBM Tomasz Łuomsi
Ćwiczenie 10. Wyznaczanie współczynnika rozpraszania zwrotnego promieniowania beta.
 Ćwicenie 1 Wynacanie współcynnika roprasania wrotnego promieniowania beta. Płytki roprasające Ustawienie licnika Geigera-Műllera w ołowianym domku Student winien wykaać się najomością następujących agadnień:
Ćwicenie 1 Wynacanie współcynnika roprasania wrotnego promieniowania beta. Płytki roprasające Ustawienie licnika Geigera-Műllera w ołowianym domku Student winien wykaać się najomością następujących agadnień:
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
13. TERMODYNAMIKA WYZNACZANIE ENTALPII REAKCJI ZOBOJĘTNIANIA MOCNEJ ZASADY MOCNYMI KWASAMI I ENTALPII PROCESU ROZPUSZCZANIA SOLI
 Wykonanie ćwiczenia 13. TERMODYNAMIKA WYZNACZANIE ENTALPII REAKCJI ZOBOJĘTNIANIA MOCNEJ ZASADY MOCNYMI KWASAMI I ENTALPII PROCESU ROZPUSZCZANIA SOLI Zadania do wykonania: 1. Wykonać pomiar temperatury
Wykonanie ćwiczenia 13. TERMODYNAMIKA WYZNACZANIE ENTALPII REAKCJI ZOBOJĘTNIANIA MOCNEJ ZASADY MOCNYMI KWASAMI I ENTALPII PROCESU ROZPUSZCZANIA SOLI Zadania do wykonania: 1. Wykonać pomiar temperatury
Ekscytony Wanniera Motta
 ozpatrzmy oddziaływani lktronu o wktorz falowym bliskim minimum pasma przwodnictwa oraz dziury z obszaru blisko wirzcołka pasma walncyjngo. Zakładamy, ż oba pasma są sfryczni symtryczn, a ic kstrma znajdują
ozpatrzmy oddziaływani lktronu o wktorz falowym bliskim minimum pasma przwodnictwa oraz dziury z obszaru blisko wirzcołka pasma walncyjngo. Zakładamy, ż oba pasma są sfryczni symtryczn, a ic kstrma znajdują
Praca objętościowa - pv (wymiana energii na sposób pracy) Ciepło reakcji Q (wymiana energii na sposób ciepła) Energia wewnętrzna
 Energia - zdolność danego układu do wykonania dowolnej pracy. Potencjalna praca, którą układ może w przyszłości wykonać. Praca wykonana przez układ jak i przeniesienie energii może manifestować się na
Energia - zdolność danego układu do wykonania dowolnej pracy. Potencjalna praca, którą układ może w przyszłości wykonać. Praca wykonana przez układ jak i przeniesienie energii może manifestować się na
9. Sprzężenie zwrotne własności
 9. Sprzężenie zwrotne własności 9.. Wprowadzenie Sprzężenie zwrotne w uładzie eletronicznym realizuje się przez sumowanie części sygnału wyjściowego z sygnałem wejściowym i użycie zmodyiowanego w ten sposób
9. Sprzężenie zwrotne własności 9.. Wprowadzenie Sprzężenie zwrotne w uładzie eletronicznym realizuje się przez sumowanie części sygnału wyjściowego z sygnałem wejściowym i użycie zmodyiowanego w ten sposób
OBLICZENIA W POMIARACH POŚREDNICH
 ROZDZAŁ 6 OBLCZENA W POMARACH POŚREDNCH Stefan ubisa Zachodniopoorsi niwersytet Technologiczny. Wstęp Poiar pośredni to tai w tóry wartość wielości ierzonej wielości wyjściowej ezurandu y oblicza się z
ROZDZAŁ 6 OBLCZENA W POMARACH POŚREDNCH Stefan ubisa Zachodniopoorsi niwersytet Technologiczny. Wstęp Poiar pośredni to tai w tóry wartość wielości ierzonej wielości wyjściowej ezurandu y oblicza się z
1.7 Zagadnienia szczegółowe związane z równaniem ruchu Moment bezwładności i moment zamachowy
 .7 Zagadnna zczgółow zwązan z równan ruchu.7. ont bzwładnośc ont zaachowy Równan równowag ł dzałających na lnt ay d poazany na ry..8 będz ało potać: df a tąd lntarny ont dynaczny: d d ϑ d r * d d ϑ r d
.7 Zagadnna zczgółow zwązan z równan ruchu.7. ont bzwładnośc ont zaachowy Równan równowag ł dzałających na lnt ay d poazany na ry..8 będz ało potać: df a tąd lntarny ont dynaczny: d d ϑ d r * d d ϑ r d
Fizyka promieniowania jonizującego. Zygmunt Szefliński
 Fizyka prominiowania jonizującgo ygmunt Szfliński 1 Wykład 10 Rozpady Rozpady - warunki nrgtyczn Ściżka stabilności Nad ściżką znajdują się jądra prominiotwórcz, ulgając rozpadowi -, zaś pod nią - jądra
Fizyka prominiowania jonizującgo ygmunt Szfliński 1 Wykład 10 Rozpady Rozpady - warunki nrgtyczn Ściżka stabilności Nad ściżką znajdują się jądra prominiotwórcz, ulgając rozpadowi -, zaś pod nią - jądra
Ćwiczenia do wykładu Fizyka Statystyczna i Termodynamika
 Ćwiczenia do wykładu Fizyka tatystyczna i ermodynamika Prowadzący dr gata Fronczak Zestaw 5. ermodynamika rzejść fazowych: równanie lausiusa-laeyrona, własności gazu Van der Waalsa 3.1 Rozważ tyowy diagram
Ćwiczenia do wykładu Fizyka tatystyczna i ermodynamika Prowadzący dr gata Fronczak Zestaw 5. ermodynamika rzejść fazowych: równanie lausiusa-laeyrona, własności gazu Van der Waalsa 3.1 Rozważ tyowy diagram
INSTYTUT ANALIZ REGIONALNYCH
 wwwiarl Oracowanie dla jednoste samorądu terytorialnego wsierające ich dążenia o wrost subwencji oświatowej na 2012 r raca odlega ustawie o rawie autorsim i rawach orewnych i międy innymi: orystając niej
wwwiarl Oracowanie dla jednoste samorądu terytorialnego wsierające ich dążenia o wrost subwencji oświatowej na 2012 r raca odlega ustawie o rawie autorsim i rawach orewnych i międy innymi: orystając niej
LABORATORIUM Z KATALIZY HOMOGENICZNEJ I HETEROGENICZNEJ KINETYKA POLIKONDENSACJI POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDA FIZYKOCHEMII I TECHNOLOGII POLIMEÓW Prowadzący: Joanna Strzezi Miejsce ćwiczenia: Załad Chemii Fizycznej, sala 5 LABOATOIUM Z KATALIZY HOMOGENICZNEJ I HETEOGENICZNEJ
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDA FIZYKOCHEMII I TECHNOLOGII POLIMEÓW Prowadzący: Joanna Strzezi Miejsce ćwiczenia: Załad Chemii Fizycznej, sala 5 LABOATOIUM Z KATALIZY HOMOGENICZNEJ I HETEOGENICZNEJ
Wykład 13 Druga zasada termodynamiki
 Wyład 3 Druga zasada termodynamii Entroia W rzyadu silnia Carnota z gazem dosonałym otrzymaliśmy Q =. (3.) Q Z tego wzoru wynia, że wielość Q Q = (3.) dla silnia Carnota jest wielością inwariantną (niezmienniczą).
Wyład 3 Druga zasada termodynamii Entroia W rzyadu silnia Carnota z gazem dosonałym otrzymaliśmy Q =. (3.) Q Z tego wzoru wynia, że wielość Q Q = (3.) dla silnia Carnota jest wielością inwariantną (niezmienniczą).
Wyznaczanie ciepła topnienia lodu lub ciepła właściwego wybranego ciała
 dla specjalnośći Biofizya moleularna Wyznaczanie ciepła topnienia lodu lub ciepła właściwego wybranego ciała I. WSTĘP C 1 C 4 Ciepło jest wielością charateryzującą przepływ energii (analogiczną do pracy
dla specjalnośći Biofizya moleularna Wyznaczanie ciepła topnienia lodu lub ciepła właściwego wybranego ciała I. WSTĘP C 1 C 4 Ciepło jest wielością charateryzującą przepływ energii (analogiczną do pracy
3. Zapas stabilności układów regulacji 3.1. Wprowadzenie
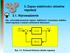 3. Zapas stabilności układów regulacji 3.. Wprowadenie Dla scharakteryowania apasu stabilności roważymy stabilny układ regulacji o nanym schemacie blokowym: Ws () Gs () Ys () Hs () Rys. 3.. Schemat blokowy
3. Zapas stabilności układów regulacji 3.. Wprowadenie Dla scharakteryowania apasu stabilności roważymy stabilny układ regulacji o nanym schemacie blokowym: Ws () Gs () Ys () Hs () Rys. 3.. Schemat blokowy
Dysocjacja elektrolityczna, przewodność elektryczna roztworów
 tester woda destylowana tester Ćwiczenie 1a woda wodociągowa tester 5% roztwór cukru tester 0,1 M HCl tester 0,1 M CH 3 COOH tester 0,1 M tester 0,1 M NH 4 OH tester 0,1 M NaCl Dysocjacja elektrolityczna,
tester woda destylowana tester Ćwiczenie 1a woda wodociągowa tester 5% roztwór cukru tester 0,1 M HCl tester 0,1 M CH 3 COOH tester 0,1 M tester 0,1 M NH 4 OH tester 0,1 M NaCl Dysocjacja elektrolityczna,
Wyznaczanie ciepła właściwego powietrza metodą rozładowa- nia kondensatora I. Cel ćwiczenia: II. Przyrządy: III. Literatura: IV.
 Ćwiczenie -5 Wyznaczanie cieła właściwego owietrza etodą rozładowania kondensatora I. el ćwiczenia: oznanie jednej z etod oiaru cieła właściwego gazów, zjawiska rozładowania kondensatora i sosobu oiaru
Ćwiczenie -5 Wyznaczanie cieła właściwego owietrza etodą rozładowania kondensatora I. el ćwiczenia: oznanie jednej z etod oiaru cieła właściwego gazów, zjawiska rozładowania kondensatora i sosobu oiaru
Zalecenia nawozowe dla pomidora w uprawie na podłożach inertnych
 INSTYTUT OGRODNICTWA ZAKŁAD UPRAWY I NAWOŻENIA ROŚLIN OGRODNICZYCH Pracownia Uprawy i Nawożenia Roślin Warzywnych 96-100 Sierniewice, ul. Rybiciego 15/17 tel./fax: 46 84666 e-mail: Jace.Dyso@inhort.pl
INSTYTUT OGRODNICTWA ZAKŁAD UPRAWY I NAWOŻENIA ROŚLIN OGRODNICZYCH Pracownia Uprawy i Nawożenia Roślin Warzywnych 96-100 Sierniewice, ul. Rybiciego 15/17 tel./fax: 46 84666 e-mail: Jace.Dyso@inhort.pl
2015-01-15. Edycja pierwsza 2014/1015. dla kierunku fizyka medyczna, I rok, studia magisterskie
 05-0-5. Opis różnicę pomiędy błędem pierwsego rodaju a błędem drugiego rodaju Wyniki eksperymentu składamy w dwie hipotey statystycne: H0 versus H, tak, by H0 odrucić i pryjąć H. Jeśli decydujemy, że pryjmujemy
05-0-5. Opis różnicę pomiędy błędem pierwsego rodaju a błędem drugiego rodaju Wyniki eksperymentu składamy w dwie hipotey statystycne: H0 versus H, tak, by H0 odrucić i pryjąć H. Jeśli decydujemy, że pryjmujemy
WYKŁAD 5 METODY OPTYMALIZACJI NIELINIOWEJ BEZ OGRANICZEŃ
 WYKŁAD 5 METODY OPTYMALIZACJI NIELINIOWEJ BEZ OGRANICZEŃ Wstęp. Za wyjątie nielicznych funcji, najczęściej w postaci wieloianów, dla tórych ożna znaleźć iniu na drodze analitycznej, pozostała więszość
WYKŁAD 5 METODY OPTYMALIZACJI NIELINIOWEJ BEZ OGRANICZEŃ Wstęp. Za wyjątie nielicznych funcji, najczęściej w postaci wieloianów, dla tórych ożna znaleźć iniu na drodze analitycznej, pozostała więszość
Obliczenia chemiczne. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
ĆWICZENIE 3 CIEPŁO ROZPUSZCZANIA I NEUTRALIZACJI
 ĆWICZENIE 3 CIEPŁO ROZPUSZCZANIA I NEUTRALIZACJI Przybory i odczynniki Kalorymetr NaOH w granulkach Mieszadło KOH w granulkach Cylinder miarowy 50 ml 4n HCl 4 Szkiełka zegarowe 4N HNO 3 Termometr (dokładność
ĆWICZENIE 3 CIEPŁO ROZPUSZCZANIA I NEUTRALIZACJI Przybory i odczynniki Kalorymetr NaOH w granulkach Mieszadło KOH w granulkach Cylinder miarowy 50 ml 4n HCl 4 Szkiełka zegarowe 4N HNO 3 Termometr (dokładność
Konkurs Chemiczny dla gimnazjalistów województwa zachodniopomorskiego w roku szkolnym 2018/2019. Etap wojewódzki
 Konkurs Chemiczny dla gimnazjalistów województwa zachodniopomorskiego w roku szkolnym 08/09 Etap wojewódzki Klucz odpowiedzi i schemat punktowania Część I. Test jednokrotnego wyboru z jedną poprawną odpowiedzią
Konkurs Chemiczny dla gimnazjalistów województwa zachodniopomorskiego w roku szkolnym 08/09 Etap wojewódzki Klucz odpowiedzi i schemat punktowania Część I. Test jednokrotnego wyboru z jedną poprawną odpowiedzią
6. ph i ELEKTROLITY. 6. ph i elektrolity
 6. ph i ELEKTROLITY 31 6. ph i elektrolity 6.1. Oblicz ph roztworu zawierającego 0,365 g HCl w 1,0 dm 3 roztworu. Odp 2,00 6.2. Oblicz ph 0,0050 molowego roztworu wodorotlenku baru (α = 1,00). Odp. 12,00
6. ph i ELEKTROLITY 31 6. ph i elektrolity 6.1. Oblicz ph roztworu zawierającego 0,365 g HCl w 1,0 dm 3 roztworu. Odp 2,00 6.2. Oblicz ph 0,0050 molowego roztworu wodorotlenku baru (α = 1,00). Odp. 12,00
III Podkarpacki Konkurs Chemiczny 2010/2011. ETAP I r. Godz Zadanie 1
 III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
KRYTERIA OCENIANIA ODPOWIEDZI Próbna Matura z OPERONEM. Chemia Poziom rozszerzony
 KRYTERIA OCENIANIA ODPOWIEDZI Próbna Matura z OPERONEM Chemia Poziom rozszerzony Listopad 01 W niniejszym schemacie oceniania zadań otwartych są prezentowane przykładowe poprawne odpowiedzi. W tego typu
KRYTERIA OCENIANIA ODPOWIEDZI Próbna Matura z OPERONEM Chemia Poziom rozszerzony Listopad 01 W niniejszym schemacie oceniania zadań otwartych są prezentowane przykładowe poprawne odpowiedzi. W tego typu
F - wypadkowa sił działających na cząstkę.
 PRAWA ZACHOWAIA Podstawowe termny Cała tworzące uład mechanczny oddzałują mędzy sobą z całam nenależącym do uładu za omocą: Sł wewnętrznych Sł zewnętrznych - Sł dzałających na dane cało ze strony nnych
PRAWA ZACHOWAIA Podstawowe termny Cała tworzące uład mechanczny oddzałują mędzy sobą z całam nenależącym do uładu za omocą: Sł wewnętrznych Sł zewnętrznych - Sł dzałających na dane cało ze strony nnych
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph
 Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
PODSTAWY TERMODYNAMIKI
 ODAWY ERMODYNAMIKI ( punkty (OŚ_3--7 Zad.. W zbiorniku zamkniętym tłokiem znajduje się moli metanu, który można z powodzeniem potraktować jako az doskonały. emperatura początkowa metanu wynosi 5 C a ciśnienie
ODAWY ERMODYNAMIKI ( punkty (OŚ_3--7 Zad.. W zbiorniku zamkniętym tłokiem znajduje się moli metanu, który można z powodzeniem potraktować jako az doskonały. emperatura początkowa metanu wynosi 5 C a ciśnienie
REFERAT PRACY MAGISTERSKIEJ Symulacja estymacji stanu zanieczyszczeń rzeki z wykorzystaniem sztucznych sieci neuronowych.
 REFERAT PRACY MAGISTERSKIEJ Symulacja estymacji stanu zanieczyszczeń rzei z wyorzystaniem sztucznych sieci neuronowych. Godło autora pracy: EwGron. Wprowadzenie. O poziomie cywilizacyjnym raju, obo wielu
REFERAT PRACY MAGISTERSKIEJ Symulacja estymacji stanu zanieczyszczeń rzei z wyorzystaniem sztucznych sieci neuronowych. Godło autora pracy: EwGron. Wprowadzenie. O poziomie cywilizacyjnym raju, obo wielu
Jak mierzyć i jak liczyć efekty cieplne reakcji?
 Jak mierzyć i jak liczyć efekty cieplne reakcji? Energia Zdolność do wykonywania pracy lub do produkowania ciepła Praca objętościowa praca siła odległość 06_73 P F A W F h N m J P F A Area A ciśnienie
Jak mierzyć i jak liczyć efekty cieplne reakcji? Energia Zdolność do wykonywania pracy lub do produkowania ciepła Praca objętościowa praca siła odległość 06_73 P F A W F h N m J P F A Area A ciśnienie
Alkacymetria ANALIZA OBJĘTOŚCIOWA. Substancje podstawowe wykorzystywane w alkacymetrii: 1. H 2 C 2 O 4 + 2 NaOH = Na 2 C 2 O 4 + 2 H 2 O
 ANALIZA BJĘTŚCIWA Alaymetria Sustaje podstawowe wyorystywae w alaymetrii: 1. C 4 + Na = Na C 4 +. C 6 5 C + Na = C 6 5 CNa + C 4. Na B 4 7 + Cl + 5 4 B + NaCl M M C Na B 10 81, 7 4 4 16, 06g mol 7 1 g
ANALIZA BJĘTŚCIWA Alaymetria Sustaje podstawowe wyorystywae w alaymetrii: 1. C 4 + Na = Na C 4 +. C 6 5 C + Na = C 6 5 CNa + C 4. Na B 4 7 + Cl + 5 4 B + NaCl M M C Na B 10 81, 7 4 4 16, 06g mol 7 1 g
Prawa Zachowania. Zasady zachowania odgrywaj w fizyce szczególn rol.
 izya 1: Wyad II Prawa Zachowania 1 Zasady zachowania odgrywaj w fizyce szczególn rol. Orócz zasad zachowania oznanych w szole: zasady zachowania du zasady zachowania momentu du zasady zachowania energii
izya 1: Wyad II Prawa Zachowania 1 Zasady zachowania odgrywaj w fizyce szczególn rol. Orócz zasad zachowania oznanych w szole: zasady zachowania du zasady zachowania momentu du zasady zachowania energii
Algebra liniowa z geometrią analityczną
 WYKŁAD. Własności zbiorów liczbowych. Podzielność liczb całowitych, relacja przystawania modulo, twierdzenie chińsie o resztach. Liczby całowite Liczby 0,±,±,±3,... nazywamy liczbami całowitymi. Zbiór
WYKŁAD. Własności zbiorów liczbowych. Podzielność liczb całowitych, relacja przystawania modulo, twierdzenie chińsie o resztach. Liczby całowite Liczby 0,±,±,±3,... nazywamy liczbami całowitymi. Zbiór
2009 ZARZĄDZANIE. LUTY 2009
 Wybran zstawy gzaminacyjn kursu Matmatyka na Wydzial ZF Uniwrsyttu Ekonomiczngo w Wrocławiu w latach 009 06 Zstawy dotyczą trybu stacjonarngo Niktór zstawy zawirają kompltn rozwiązania Zakrs matriału w
Wybran zstawy gzaminacyjn kursu Matmatyka na Wydzial ZF Uniwrsyttu Ekonomiczngo w Wrocławiu w latach 009 06 Zstawy dotyczą trybu stacjonarngo Niktór zstawy zawirają kompltn rozwiązania Zakrs matriału w
( ) gdzie: σ z naprężenie pionowe w gruncie, σ z = γz, [kpa] K a współczynnik parcia czynnego
![( ) gdzie: σ z naprężenie pionowe w gruncie, σ z = γz, [kpa] K a współczynnik parcia czynnego ( ) gdzie: σ z naprężenie pionowe w gruncie, σ z = γz, [kpa] K a współczynnik parcia czynnego](/thumbs/58/41397246.jpg) PARCI CZYNN I BIRN GRUNTU Prci gruntu jst jgo oddiływnim n konstrukcję odirjącą (ściny i mury oorow, ścinki scln, it). Znjomość wrtości tgo oddiływni jst konicn ry rojktowniu tych konstrukcji. Podn oniżj
PARCI CZYNN I BIRN GRUNTU Prci gruntu jst jgo oddiływnim n konstrukcję odirjącą (ściny i mury oorow, ścinki scln, it). Znjomość wrtości tgo oddiływni jst konicn ry rojktowniu tych konstrukcji. Podn oniżj
ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa
 Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Fizyka 1- Mechanika. Wykład 6 9.XI Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów
 izya 1- Mechania Wyład 6 9.XI.17 Zygun Szeflińsi Środowisowe Laboraoriu Ciężich Jonów szef@fuw.edu.l h://www.fuw.edu.l/~szef/ Równania ruchu ole agneyczne,, r,, v Sałe jednorodne ole w chwili = w uncie
izya 1- Mechania Wyład 6 9.XI.17 Zygun Szeflińsi Środowisowe Laboraoriu Ciężich Jonów szef@fuw.edu.l h://www.fuw.edu.l/~szef/ Równania ruchu ole agneyczne,, r,, v Sałe jednorodne ole w chwili = w uncie
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 2
 PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
MECHANIKA PŁYNÓW Płyn
 MECHANIKA PŁYNÓW Płyn - Każda substancja, która może płynąć, tj. pod wpływem znikomo małych sił dowolnie zmieniać swój kształt w zależności od naczynia, w którym się znajduje, oraz może swobodnie się przemieszczać
MECHANIKA PŁYNÓW Płyn - Każda substancja, która może płynąć, tj. pod wpływem znikomo małych sił dowolnie zmieniać swój kształt w zależności od naczynia, w którym się znajduje, oraz może swobodnie się przemieszczać
RÓWNOWAGI W UKŁADACH WIELOFAZOWYCH
 RÓWNOWAGI W UKŁADACH WIELOFAZOWYCH 321 Pojęcia podstawowe 322 erodynaika równowag fazowych reguła faz Gibbsa 323 Równanie Clausiusa-Clapeyrona 324 Przeiany fazowe I i II rodzaju 31 erodynaika równowag
RÓWNOWAGI W UKŁADACH WIELOFAZOWYCH 321 Pojęcia podstawowe 322 erodynaika równowag fazowych reguła faz Gibbsa 323 Równanie Clausiusa-Clapeyrona 324 Przeiany fazowe I i II rodzaju 31 erodynaika równowag
WYZNACZANIE PRZEWODNICTWA GRANICZNEGO ELEKTROLITÓW
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY WYZNACZANIE PRZEWODNICTWA GRANICZNEGO ELEKTROLITÓW Opiekun: Miejsce ćwiczenia: Karoń Krzysztof Katedra Fizykocheii i Technologii Polierów ul. M. Strzody 9, p. II,
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY WYZNACZANIE PRZEWODNICTWA GRANICZNEGO ELEKTROLITÓW Opiekun: Miejsce ćwiczenia: Karoń Krzysztof Katedra Fizykocheii i Technologii Polierów ul. M. Strzody 9, p. II,
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 01/1 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 01/1 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Problemy do samodzielnego rozwiązania
 Problemy do samodzielnego rozwiązania 1. Napisz równania reakcji dysocjacji elektrolitycznej, uwzględniając w zapisie czy jest to dysocjacja mocnego elektrolitu, słabego elektrolitu, czy też dysocjacja
Problemy do samodzielnego rozwiązania 1. Napisz równania reakcji dysocjacji elektrolitycznej, uwzględniając w zapisie czy jest to dysocjacja mocnego elektrolitu, słabego elektrolitu, czy też dysocjacja
TERMODYNAMIKA. Termodynamika jest to dział nauk przyrodniczych zajmujący się własnościami
 TERMODYNAMIKA Termodynamika jest to dział nauk rzyrodniczych zajmujący się własnościami energetycznymi ciał. Przy badaniu i objaśnianiu własności układów fizycznych termodynamika osługuje się ojęciami
TERMODYNAMIKA Termodynamika jest to dział nauk rzyrodniczych zajmujący się własnościami energetycznymi ciał. Przy badaniu i objaśnianiu własności układów fizycznych termodynamika osługuje się ojęciami
1. OBSERWACJE WSTĘPNE
 SPRAWOZDANIE 8 Imię i nazwisko:.. Data:... Kierunek studiów i nr grupy: Nr próby...... PRÓBKA 1 1. OBSERWACJE WSTĘPNE Właściwość fizyczna substancji Barwa Rodzaj mieszaniny (jednorodna, niejednorodna)
SPRAWOZDANIE 8 Imię i nazwisko:.. Data:... Kierunek studiów i nr grupy: Nr próby...... PRÓBKA 1 1. OBSERWACJE WSTĘPNE Właściwość fizyczna substancji Barwa Rodzaj mieszaniny (jednorodna, niejednorodna)
A4: Filtry aktywne rzędu II i IV
 A4: Filtry atywne rzędu II i IV Jace Grela, Radosław Strzała 3 maja 29 1 Wstęp 1.1 Wzory Poniżej zamieszczamy podstawowe wzory i definicje, tórych używaliśmy w obliczeniach: 1. Związe między stałą czasową
A4: Filtry atywne rzędu II i IV Jace Grela, Radosław Strzała 3 maja 29 1 Wstęp 1.1 Wzory Poniżej zamieszczamy podstawowe wzory i definicje, tórych używaliśmy w obliczeniach: 1. Związe między stałą czasową
13 TERMODYNAMIKA. Sprawdzono w roku 2017 przez A. Chomickiego
 13 TERMODYNAMIKA Zagadnienia teoretyczne Układ i otoczenie. Wielkości intensywne i ekstensywne. Pojęcie energii, ciepła, pracy, temperatury. Zasady termodynamiki (pierwsza, druga, trzecia). Funkcje termodynamiczne
13 TERMODYNAMIKA Zagadnienia teoretyczne Układ i otoczenie. Wielkości intensywne i ekstensywne. Pojęcie energii, ciepła, pracy, temperatury. Zasady termodynamiki (pierwsza, druga, trzecia). Funkcje termodynamiczne
MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA
 Copyright by ZamKor P. Sagnowski i Wspólnicy spółka jawna, Kraków 0 MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA Poziom rozszerzony Zadanie Odpowiedzi Uwagi. za poprawne uzupełnienie wiersza tabeli: Wartości
Copyright by ZamKor P. Sagnowski i Wspólnicy spółka jawna, Kraków 0 MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA Poziom rozszerzony Zadanie Odpowiedzi Uwagi. za poprawne uzupełnienie wiersza tabeli: Wartości
VII Podkarpacki Konkurs Chemiczny 2014/15. ETAP II r. Godz Zadanie 1 (11 pkt)
 VII Podkarpacki Konkurs heiczny 2014/15 KPKh ETAP II 20.12.2014 r. Godz. 10.302.30...... Nazwisko, iię Szkoła, iejscowość Rec. I Rec. II Tabela wyników Zad.1 Zad.2 Zad.3 Sua Wynik końcowy Uwaga! Masy olowe
VII Podkarpacki Konkurs heiczny 2014/15 KPKh ETAP II 20.12.2014 r. Godz. 10.302.30...... Nazwisko, iię Szkoła, iejscowość Rec. I Rec. II Tabela wyników Zad.1 Zad.2 Zad.3 Sua Wynik końcowy Uwaga! Masy olowe
