ANALIZA WŁAŚCIWOŚCI PALNYCH PODSTAWOWYCH GRUP ZWIĄZKÓW ORGANICZNYCH
|
|
|
- Rafał Chrzanowski
- 7 lat temu
- Przeglądów:
Transkrypt
1 dr Tomasz WĘSIERSKI CNBOP ANALIZA WŁAŚCIWOŚCI PALNYCH PODSTAWOWYCH GRUP ZWIĄZKÓW ORGANICZNYCH Analyss of the combuston characterstcs of the man groups of organc compounds Streszczene Analza właścwośc pożarowych zwązków chemcznych stanow nezwykle ważne zagadnene w aspekce ochrony przecwpożarowej. Określene charakterystyk pożarowych daje nam możlwość przewdzena zachowana sę rozpatrywanej substancj w żądanych warunkach a zatem staje sę realne właścwe określene ryzyka pożarowego. W sytuacjach kedy nektóre dane dotyczące substancj są nedostępne, stneje możlwość przewdzena teoretycznego wybranych parametrów takch jak temperatura zapłonu, temperatura samozapłonu, dolna górna granca wybuchowośc. W nnejszej publkacj zawarto równeż ops charakterystyk pomocnczych oraz sposobu ch nterpretacj dla takch parametrów jak lczba F, lczba RF oraz współczynnk R. Parametry te mogą być równeż bardzo pomocne przy projektowanu cząsteczek posadających wewnętrzny mechanzm nhbcj procesu spalana co ma stotne znaczene przy poszukwanu środków ognochronnych. Summary Analyss of the fre characterstcs of the chemcal compounds s a very mportant ssue n terms of fre protecton. Determnaton of ths characterstcs gves us the ablty to predct the behavor of the substances present n the desred condtons and thus a real proper determnaton of fre rsk. In stuatons where some data are unavalable, t s possble to predct some of the theoretcal parameters such as flash pont, auto-gnton temperature, flammablty lmts. Ths publcaton contans also a descrpton of secondary characterstcs such us F-number, RF-number R-ndex and ther nterpretaton. They can be also very helpful n desgnng of molecules havng nternal combuston nhbton mechansm what s mportant n retardants research.
2 Słowa kluczowe: Analza właścwośc pożarowych; charakterystyk pożarowe, lczba F, lczba RF, współczynnk R Key words: Analyss of fre charakterstcs, fre charakterstcs, F number, RF number, R ndex; Wstęp Baza danych CAS Regstry zawera obecne ok. 25 mlonów dobrze zdentyfkowanych zwązków chemcznych oraz około 50 mlonów produktów pośrednch, czyl zwązków, które ne zostały wyzolowane w postac czystej ale prawdopodobne stneją. Lczbę tę w pewnym przyblżenu można uznać za całkowtą lczbę wszystkch znanych obecne zwązków chemcznych przy czym codzenne do bazy dopsywane jest około 4000 nowych zwązków. Borąc pod uwagę, ż zdecydowaną wększość tych substancj stanową zwązk organczne od razu ujawna nam sę skala problemu analzy ch właścwośc pożarowych. Aby tego dokonać należy dla analzowanego zwązku wząć pod uwagę mędzy nnym jego masę cząsteczkową, skład atomowy, obecność oraz rodzaj grup funkcyjnych wązań nenasyconych, rozkład podstawnków, kształt cząsteczk, a nawet rozważyć rodzaj ewentualnych zaneczyszczeń, które mogą znaczne zwększyć nebezpeczeństwo nekontrolowanego zapłonu [1]. Analzując te dane jesteśmy w stane przewdzeć domnujący typ oddzaływań mędzycząsteczkowych, stan skupena, a także oszacować nektóre parametry pożarowe take jak dolna (L) oraz górna (U) granca wybuchowośc [2-6], czy temperatura zapłonu oraz samozapłonu [6]. Jedną z cekawych metod scharakteryzowana palnośc substancj chemcznych tworzących meszanny palne z powetrzem jest oznaczene lczby F, dla której postać matematyczną przedstawono w równanu 1: 0,5 L F = 1 1) U Wartość lczy F przyjmuje wartośc pomędzy zero a jednoścą w zależnośc od przyjętego stopna palnośc substancj. Klasyfkacja substancj względem lczby F przedstawa sę następująco:
3 a. F < 0,2; praktyczne nezapalne; b. 0,2 < F < 0,4; słabo zapalne; c. 0,4 < F < 0,6; o normalnej zapalnośc; d. 0,6 < F < 0,8; o podwyższonej zapalnośc; e. F > 0,8; ekstremalne łatwo zapalne. Wartość F można wyznaczyć teoretyczne dla neznanej substancj na podstawe elementów strukturalnych obecnych w cząsteczce. Posadając oznaczoną teoretyczne lczbę F możemy wyznaczyć dolną oraz górną grancę wybuchowośc. Analtyczny tok oblczeń zostane przedstawony w następnej częśc artykułu. Innym parametrem określającym właścwośc pożarowe jest współczynnk R defnowany jako loraz stężena stechometrycznego (C st ) dla reakcj przebegającej w warunkach całkowtego spalana do dolnej grancy wybuchowośc (L) (równane 2): Cst R = 2) L Jeśl lcznk oraz manownk pomnożymy przez molowe cepło spalana wartość lcznka reprezentuje nam maksymalną wartość cepła jaka sę wydzel podczas spalana jednostkowej objętośc meszanny palnej natomast wartość manownka mnmalną lość cepła wydzelającą sę w trakce spalana jednostkowej objętośc meszanny palnej. Dlatego też m wyższa wartość współczynnka R, tym palwo jest określane jako bardzej energetyczne. Jednakże ten parametr równeż ne daje nam całoścowej oceny nebezpeczeństwa zwązanego z zapłonem par palnych substancj. W perwszym przyblżenu wydaje sę, ż prawdopodobeństwo zapłonu jest proporcjonalne do welkośc przedzału pomędzy dolną a górną grancą wybuchowośc. Z drugej strony jednakże, m mnejsza jest wartość stężena odpowadająca dolnej grancy wybuchowośc, tym łatwejsze wydaje sę być osągnęce tej grancy. Zakłada sę, ż prawdopodobeństwo powstana zapłonu dane jest przez loraz różncy średnej geometrycznej dolnej oraz górnej grancy wybuchowośc (UL) 0,5 pomnejszonej o wartość dolnej grancy wybuchowośc (L), do wartośc dolnej grancy wybuchowośc (L) wg równana 3: ( UL) L 0,5 L U = L 0,5 F 1 = 1 F 3)
4 Mnożąc wartość prawdopodobeństwa zapłonu przez loraz molowego cepła spalana (Q) masy molowej (M) otrzymuje sę wartość lczby RF (wzór 4): RF ( UL) = L 0,5 L Q M U = L 0,5 1 Q M F = F 1 Q M 4) Wartość RF jest dodatkowym parametrem oprócz lczby F, który wyraża nam nebezpeczeństwo zastnena zapłonu [5]. Klasyfkacja substancj względem lczby RF przedstawa sę następująco: a. RF < 30; słabo zapalne b. 30 < RF < 150; o normalnej zapalnośc c. RF>150; slne zapalne Empryczne charakterystyk dla węglowodorów Podstawową najprostszą grupą zwązków organcznych są węglowodory. Grupa te ze względu na najmnej skomplkowaną strukturę słabych oddzaływań mędzycząsteczkowych oraz bogatą bazę danych lteraturowych wydaje sę najłatwejsza do analzy. Ze względu na obecność w swej strukturze tylko atomów węgla wodoru, wszystke węglowodory w obecnośc tlenu przy oddzaływanu źródeł zapłonu ulegają łańcuchowej reakcj spalana po osągnęcu odpowednej prężnośc par w temperaturze zwanej temperaturą zapłonu. Proste zależnośc funkcyjne ne uwzględnające elementów struktury Temperatura zapłonu Welu autorów zauważyło [7-10], ż stneje prosta korelacja pomędzy temperaturą wrzena (T b ) a temperaturą zapłonu palw węglowodorowych (T f ) wyznaczoną metodą tygla zamknętego. Lnowa zależność T f = f(t b ) w skal temperatur Celsjusza przedstawł Bodhurtha (wzór 5); T f = 0,683T b 71,7 5) Zależność kwadratową w skal temperatur Kelvna została podana natomast przez Patla (wzór 6);
5 T f = 4, ,844T b 0,234x10-3 T b 2 6) Satyanarayana Kakat [10] w swoch oblczenach uwzględnl równeż cężar właścwy (d wl ) co przedstawa wzór 7: T 0,1118x10-3 f = - 83, ,5811Tb , 734d wl 7) Tb Współczynnk korelacj równana oraz wartość odchylena średnego wskazuje, ż z przedstawonych prostych zależnośc emprycznych określających temperaturę zapłonu najlepsze rezultaty daje zastosowane równana Bodhurtha [3]. Grance wybuchowośc Przyblżona zależność określająca dolną grancę wybuchowośc (L) mów, ż wartość ta jest odwrotne proporcjonalna do standardowego molowego cepła spalana H sp [3], co przedstawa równane 8: L = 4354 H sp 8) Otrzymana zależność charakteryzuje sę jednak dość nskm współczynnkem korelacj (R 2 = 0,83) oraz wysoką wartoścą odchylena średnego co potwerdza jedyne przyblżony charakter zależnośc. Neco lepsze wynk daje metoda przewdywana dolnej grancy wybuchowośc uwzględnająca wartość stężena stechometrycznego (C st ) substancj ulegającej spalanu [3] wg równana 9: L = 0,55C st 9) Podobną zależność opracowano dla przewdywana wartośc górnej grancy wybuchowośc (U) (równane 10), jednakże przyblżene to wykazuje zdecydowane mnejszą korelację z danym eksperymentalnym nż ma to mejsce w przypadku oznaczana dolnej grancy wybuchowośc.
6 U = 3,5C st 10) Zależnośc funkcyjne uwzględnające elementy strukturalne Jak wcześnej wspomnano własnośc makroskopowe zwązków chemcznych są funkcją ch struktury. To założene sugeruje, ż te własnośc mogą zostać oblczone uwzględnając udzał poszczególnych elementów strukturalnych w cząsteczce, co stanow podstawę teoretyczną metodyk SGC (structural group contrbuton). Charakterystyka danej właścwośc zwązku może być dokonana poprzez określene wkładu wagowego dla danego parametru dla poszczególnych atomów, grup atomów, typów wązań, grup funkcyjnych oraz nnych elementów ważnych dla właścwego sparametryzowana wpływu struktury zwązku na badaną cechę. Nelnowe zależnośc przedstawone w pracy Alabahr`ego [3] wykazały, ż z dużą dokładnoścą stneje możlwość przewdzena pożarowych właścwośc węglowodorów, bazując jedyne na strukturze rozpatrywanego zwązku. Ogólna postać zależnośc dającej możlwość przewdzena temperatury zapłonu, temperatury samozapłonu oraz granc wybuchowośc przedstawa równane 11: Φ = a + b ( Φ) ) + c ( Φ) ) + d ( Φ) ) + e ( Φ) ) 11) gdze: Φ oznacza poszukwany parametr natomast Σ(Φ) określa sumę wkładów poszczególnych elementów struktury. Temperatura zapłonu Szczegółowe badana temperatury zapłonu przeprowadzone przez T. Albahr [3] dla 287 węglowodorów wykazały skomplkowaną zależność T f od struktury rozpatrywanego zwązku [3]. I tak np. dla lnowych przedstawcel alkanów wykazano, ż temperatura zapłonu jest lnową funkcją lośc atomów węgla obecnych w strukturze. Dla bardzej skomplkowanych zomerów obserwuje sę natomast zależność T f od stopna rozgałęzena zwązku w sense lośc oraz długośc łańcuchów bocznych oraz położena w łańcuchu głównym. T f dla lnowych węglowodorów jest wyższa nż T f dla zwązków rozgałęzonych o tej samej lczne atomów węgla. W przypadku olefn zaobserwowano zależność temperatury zapłonu od lośc wązań welokrotnych, ch typu, a nawet konfguracj cs/trans. Ne
7 zaobserwowano natomast wększego wpływu położena netermnalnego wązana nenasyconego wzdłuż łańcucha na wartość T f. Dla zwązków aromatycznych stotnym elementem wpływającym na wartość temperatury zapłonu jest lość perścen aromatycznych oraz ch typ sprzężena. Ważną rolę grają równeż rodzaje podstawnków alklowych pod kątem ch położena, długośc łańcucha usecowena. Funkcję określającą zależność temperatury zapłonu od elementów strukturalnych przedstawa równane 12: T = + Φ Φ + Φ f 84,65 64,18 ( ) ) 5,6345 ( ) ) 0,36 ( ) ) 0,01 ( Φ) ) 12) Wag elementów strukturalnych charakteryzujących temperaturę zapłonu przedstawono natomast w tabel 1. Wag elementów strukturalnych wpływające na temperaturę zapłonu [3] Tab. 1. Typ zwązku Grupa Waga grupy Typ zwązku Grupa Waga grupy Alkany -CH 3 0,4832 węglowodory >CH 2 0,6080 > CH 2 0,5603 cyklczne >CH- 0, >CH- 0,5275 nearomatyczne - >CH- cs 0, >CH- 0, >CH- trans 0, >CH- 0, >CH- cs 0, >CH- 0, >CH- trans 0, >C< 0, >CH- cs 0, >C< 0, >CH- trans 0, C 2 H 5 (rozg) 1,0370 >C< 0,1847 Olefny =CH 2 0,4078 =CH- 0,5287 =CH 0,6037 =CH (cs) 0,5913 węglowodory =CH- 0,6205 =CH (trans) 0,6216 aromatyczne >CH 2 1, >C= 0,7135 >C= (skum) 0, >C= 0,6550 >C= 0,6150 =C= 0,8659 >C= orto 0,7535 CH 0,4475 >C= meta 0,7384 C- 0,8387 >C= para 0,7675 Oblczene przykładowe temperatury zapłonu Zwązkem dla którego przedstawono przykładowe oblczena jest p-detylobenzen. W jego strukturze można wyróżnć następujące składnk: dwe grupy etylowe (-C 2 H 5 ), cztery
8 elementy układu aromatycznego (=CH-), jeden nesprzężony element (>C=) oraz jeden element nesprzężony aromatyczny (>C=) w pozycj para względem poprzednego. A zatem korzystając z tabel 1. otrzymujemy oraz równana 12 otrzymujemy: ΣΦ I = 2 x 1, x 0, x 0, x 0,7675 = 5,9385 T f = [ 84, ,18( 5,9385) 5,6345( 5,9385) + 0,36( 5,9385) 0,01( 5,9385) ] =329,9 K Otrzymana wartość temperatury zapłonu p-detylobenzenu różn sę zaledwe o 0,1 K od wartośc tabelarycznej. Temperatura samozapłonu (T AIT ) Podobne jak w przypadku temperatury zapłonu w tym przypadku obserwuje sę wyraźny efekt wpływu struktury na temperaturę samozapłonu. Analza dokonana przez T. Albahr [3] obejmuje grupę kontrolną 131 zwązków. U lekkch n-parafn o lczbe atomów węgla do sedmu T AIT spada wyraźne wraz ze zwększanem sę lczby atomów węgla w cząsteczce. Dla lczby atomów węgla pomędzy 7 a 16 różnce te są już newelke T AIT wahają sę w zakrese 473 do 479 K. Podobną tendencję da sę zauważyć u 1-alkenów. Obserwuje sę wyraźny spadek temperatury zapłonu dla 1-alkenów o lczne atomów węgla ne wększej nż 5, a następne T AIT zmena sę neznaczne dla przedstawcel pomędzy C 6 a C 18 oscylując w grancach od 503 do 526 K. Wpływ konfguracj cs-/trans można uznać za zanedbywalny. Temperatura samozapłonu zwązków aromatycznych meśc sę ogólne w zakrese pomędzy 700 a 840 K jest zdecydowane wyższa nż dla przedstawcel parafn oraz olefn o tej samej lośc atomów węgla. Dla zwązków aromatycznych można zauważyć wpływ lośc perścen, ch rodzaj (sprzężone, nesprzężone), położena podstawnków alfatycznych (orto-, meta-, para-). Temperatura samozapłonu zwązków cyklcznych meśc sę natomast pomędzy temperaturą samozapłonu zwązków necyklcznych a aromatycznych o odpowednej m lczbe atomów węgla w cząsteczce. Dla wększośc zwązków tej grupy wartość ta meśc sę w przedzale K. Podobne jak w przypadku zwązków aromatycznych ne obserwuje sę natomast wyraźnej korelacj pomędzy T AIT a temperaturą wrzena jak równeż loścą atomów węgla w cząsteczce. Funkcję określającą zależność temperatury samozapłonu od elementów strukturalnych przedstawa równane 13:
9 2 3 4 T = 780,42+ 26,78 ( Φ) ) 2,5887 ( Φ) ) 0,3195 ( Φ) ) 0, ( Φ) ) 13) AIT Wag elementów strukturalnych charakteryzujących temperaturę samozapłonu przedstawono natomast w tabel 2. Wag elementów strukturalnych wpływające na temperaturę samozapłonu [3] Tab. 2. Typ zwązku Grupa Waga grupy Typ zwązku Grupa Waga grupy Alkany -CH 3-0,8516 węglowodory >CH 2-1,1600 > CH 2-1,4207 cyklczne >CH- 0,0372 >CH- 0,0249 nearomatyczne >C< 8,9600 >C< 2,3226 =CH- 0,0037 >C= -12,3300 Olefny =CH 2 0,4682 węglowodory =CH- 0,4547 =CH -1,9356 aromatyczne >C= (skum) 0,0246 >C= -2,2420 >C= -1,8890 CH -3,1180 >C= orto 0,9125 C- -1,1360 >C= meta 2,4650 >C= para 2,0970 Oblczene przykładowe temperatury samozapłonu Przykładowym zwązkem dla którego przedstawono oblczena jest 1-okten. W jego strukturze można wyróżnć następujące składnk: jedną termnalną grupę CH 2 =, jedną grupę (=CH-), pęć grup alfatycznych >CH 2, jedna termnalna grupa CH 3. A zatem korzystając z tabel 2 otrzymujemy oraz równana 13 otrzymujemy: ΣΦ I = 1 x 0, x 1, x 1, x 0,8516 = -9,4225 T AIT = [ 780,42+ 26,78( 9,4225) 2,5887( 9,4225) 0,3195( 9,4225) 0,007825( 9,4225) ] =503,87 K Otrzymana wartość temperatury zapłonu 1-oktenu różn sę zaledwe o 0,57 K od wartośc tabelarycznej. Górna (U) oraz dolna (L) granca wybuchowośc Badana przeprowadzone pod kątem górnej oraz dolnej grancy wybuchowośc przez T. Alabahr [3] obejmowały odpowedno grupę 464 oraz 454 węglowodorów. Obydwa parametry wykazują podobną zależność od tych samych elementów strukturalnych. Stąd też
10 wag grup zestawono sumaryczne w jednej tabel (tabela 3). Stwerdzono, ż wartośc górnej oraz dolnej grancy wybuchowośc dla zoparafn są ne tylko zależne od całkowtej lośc atomów węgla w cząsteczce, ale równeż od lośc, typu oraz stopna rozgałęzeń w cząsteczce. Położene rozgałęzena ma jednak margnalny wpływ na te grance. Podobne w przypadku zwązków aromatycznych oraz olefn położene bocznej grupy alklowej ne mało wększego znaczena na wartość U oraz L. W przypadku olefn ne stwerdzono równeż wyraźnego wpływu konfguracj cs-/trans-. Funkcję określającą zależność dolnej oraz górnej grancy wybuchowośc od elementów strukturalnych przedstawają równana 14 oraz 15: = 5 L 4,174+ 0,8093 ( Φ) ) + 0,0689 ( Φ) ) + 0,00265 ( Φ) ) + 3,76 10 ( Φ) ) 14) = 4 U 18,14+ 3,4135 ( Φ) ) + 0,3587 ( Φ) ) + 0,01747 ( Φ) ) + 3, ( Φ) ) 15) Wag elementów strukturalnych wpływające na górną (U) oraz dolną (L) grancę wybuchowośc [3] Typ zwązku Grupa Waga grupy (U) Waga grupy (L) alkany -CH 3-0,8394-1,4407 > CH 2-1,1219-0,8736 >CH- -1,2598-0,2925 >C< -2,1941 0,2747 olefny =CH 2 0,2479-1,3126 =CH -0,3016-0,7679 >C= -0,6524-0,2016 =C= 0,0675-0,4473 CH 3,8518-1,2849 C- 1,3924-0,4396 węglowodory >CH 2-0,8386-1,0035 cyklczne >CH- -0,9648-0,4955 nearomatyczne >C< -2,2754 0,1058 =CH- -0,0821-0,8700 >C= -0,1252-0,5283 węglowodory =CH- -1,2966-0,8891 aromatyczne >CH 2-1,6166-1,0884 >C= (skum) -1,4722-0,3694 >C= 0,6649-0,2847 Tab. 3.
11 Oblczena górnej oraz dolnej grancy wybuchowośc wyglądają analogczne jak przytoczone przykłady dla temperatury zapłonu oraz samozapłonu. W tym celu należy skorzystać z wag elementów strukturalnych zawartych w tabel 3 oraz wzorów 14 oraz 15. Lczba F Tak jak wspomnano wcześnej, jedną z form scharakteryzowana właścwośc palnych substancj jest określene lczby F. Eksperymentalne jej wartość można wyznaczyć mając do dyspozycj wartość dolnej oraz górnej grancy wybuchowośc zgodne ze wzorem 1. Natomast jej wartość teoretyczną można określć na podstawe elementów strukturalnych stanowących cząsteczkę badaną Wpływ na jej welkość ma długość łańcucha, obecność wązań nenasyconych, obecność perścen aromatycznych lub alfatycznych, obecność oraz lość grup funkcyjnych takch jak grupa OH, -NO 2, -NH 2, -CN, -COOH zgodne ze wzorem 16 podanym przez Kondo współpracownków [2]. F=p 1 (1+p 2 C 1 +p 3 R OE +p 4 R CO +p 5 R COO +p 6 R NH +p 7 R RNG +p 8 R ARM +p 9 R US )(1+p 10 R F +p 11 R Cl + p 12 R Br +p 13 R OH +p 14 R NO2 +p 15 R NH2 +p 16 R CN +p 17 R COOH ) 16) gdze: p 1 p 17 parametry równana określone eksperymentalne zestawone w tabel 4; C 1 wartość parametru wynosząca jeden dla zwązków monowęglowych, zero dla pozostałych przypadków. Dla pochodnych metanu zawerających grupy CO, COO, CN, COOH wartość ta równeż wynos zero; R OE wartość otrzymana przez podzelene lośc grup eterowych zawartych w cząsteczce do sumarycznej lośc atomów węgla stanowących szkelet; R CO wartość otrzymana przez podzelene lośc grup karbonylowych zawartych w cząsteczce do sumarycznej lośc atomów węgla stanowących szkelet; R COO wartość otrzymana przez podzelene lośc grup estrowych zawartych w cząsteczce do sumarycznej lośc atomów węgla stanowących szkelet; R NH wartość otrzymana przez podzelene lośc grup mnowych zawartych w cząsteczce do sumarycznej lośc atomów węgla stanowących szkelet; R RNG wartość otrzymana przez podzelene lośc perścen alfatycznych zawartych w cząsteczce do sumarycznej lośc atomów węgla stanowących szkelet; R ARM wartość otrzymana przez podzelene lośc perścen aromatycznych zawartych w cząsteczce do sumarycznej lośc atomów węgla stanowących szkelet; R US wartość otrzymana przez podzelene stopna nenasycena cząsteczk (uwzględnającego równeż układy aromatyczne) do sumarycznej lośc atomów węgla stanowących szkelet;
12 R F wartość otrzymana przez podzelene lość atomów fluoru zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową; R Cl wartość otrzymana przez podzelene lość atomów chloru zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową; R Br wartość otrzymana przez podzelene lość atomów bromu zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową; R OH wartość otrzymana przez podzelene lość grup -OH zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową; R NO2 wartość otrzymana przez podzelene lość grup NO 2 zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową; R NH2 wartość otrzymana przez podzelene lość grup NH 2 zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową; R CN wartość otrzymana przez podzelene lość grup -CN zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową; R COOH wartość otrzymana przez podzelene lość grup -COOH zawartych w cząsteczce do sumarycznej lośc atomów wodoru w węglowodorze stanowącym cząsteczkę podstawową. Wartośc parametrów równana Kondo współpracownków służące oszacowanu Parametr lczby F [2] Ops parametru Wartość parametru p 1 Współczynnk główny 0,581 p 2 dla jednego węgla -0,194 p 3 grupa eterowa 0,134 p 4 grupa karbonylowa 0,028 p 5 grupa estrowa -0,097 p 6 grupa mnowa -0,014 p 7 perśceń alfatyczny 0,299 p 8 perśceń nenasycony -0,125 p 9 nenasycene 0,290 p 10 Fluor -0,344 p 11 Chlor -0,985 p 12 Brom -3,160 p 13 grupa hydroksylowa 0,284 p 14 grupa ntrowa 0,527 p 15 grupa amnowa -0,344 p 16 grupa cyjankowa -0,566 p 17 grupa karboksylowa -0,850 Tab. 4.
13 Tak węc wyraźne wdać, ż lość szkeletowych atomów węgla w cząsteczce lub też atomów wodoru w nepodstawonym węglowodorze zawarta jest przy określanu parametrów R X, gdze X oznacza rozpatrywany element struktury lub grupę. Analzując tabelę 4 można zauważyć efekt podstawnkowy poszczególnych elementów strukturalnych na palność zwązków [2]. Dodatna wartość parametru wskazuje na zwększene palnośc zwązku, gdyż wąże sę to ze zwększenem wartośc lczby F. Ujemna wartość parametru natomast wskazuje na element zmnejszający palność substancj. I tak np. wprowadzene grupy karbonylowej lub eterowej teoretyczne zwększa palność zwązku podobne jak pojawene sę perścena alfatycznego, grupy hydroksylowej, ntrowej czy też wązań welokrotnych. Założena te w pewnych przypadkach są zgodne z danym lteraturowym, co wyraźne wdać porównując właścwośc palne alkanów do np. alkenów, a zwłaszcza alknów, a także eterów cyklcznych, ntrozwązków. Wprowadzene natomast fluorowców, w rozważanym przypadku w szczególnośc bromu powoduje obnżene palnośc. W rzeczywstośc efekt ten jest najwększy w przypadku jodu, który w ponższej analze ne był rozpatrywany. Korzystając z równana 1 można w drugą stronę oblczyć górną (U) oraz dolną (L) grancę wybuchowośc przy czym wartość (UL) 0,5 w przyblżenu można uznać za stechometryczne stężene substancj w procese spalana. Nnejsze zależnośc podaje równane 17 oraz 18. L = (UL) 0,5 (1-F) 17) U = (UL) 0,5 /(1-F) 18) Stężene stechometryczne substancj zależy od typu reakcj przebegającej w palwe. I tak np. jeśl lczba atomów wodoru (j) w cząsteczce palwa jest wększa lub równa sume lośc atomów fluoru lub chloru (l+m) stneje duże prawdopodobeństwo, ż zawarte w palwe atomy chloru fluoru utworzą chlorowodór lub fluorowodór, podczas gdy bromopochodne węglowodorów, jako produkt spalana, będą tworzyły brom. W przypadku zwązków zawerających azot w wększośc przypadków produktem spalana będze azot. Równane reakcj dla rozpatrywanej sytuacj przedstawa sę następująco: C H j O k F l Cl m Br n N p +[+0,25(j-l-m-2k)O 2 = CO 2 +0,5(j-l-m)H 2 O+lHF+mHCl+0,5nBr 2 +0,5pN 2 19)
14 A węc stężene stechometryczne w jednostkach bezwymarowych będze wynosć: C st = ,773[ + 0,25( j l m 2k) 20) W przypadku, gdy lczba atomów wodoru (j) w cząsteczce jest mnejsza nż sumaryczna lość atomów chloru oraz fluoru (l+m) jako produkt procesu utlenana tworzy sę w przeważającej lośc chlor wg równana 21: C H j O k F l Cl m Br n N p +[+0,25(j-l-2k)O 2 = CO 2 +0,5(j-l-m)H 2 O+lHF+0,5mCl 2 +0,5nBr 2 +0,5pN 2 21) stężene stechometryczne w takej sytuacj wynos: C st = ,773[ + 0,25( j l 2k) 22) W szczególnym przypadku, gdy lczba atomów wodoru jest mnejsza nawet od lczby samych atomów fluoru w wynku reakcj spalana ne tworzy sę woda, a oprócz fluorowodoru powstaje równeż tetrafluorek węgla wg reakcj: C H j O k F l Cl m Br n N p +[+0,25(j-l-2k)O 2 = [-0,25(l-j)CO 2 +0,25(l-j)CF 4 +jhf+0,5mcl 2 +0,5nBr 2 +0,5pN 2 23) Stężene stechometryczne substancj jest określone podobne jak w przypadku poprzednm poprzez równane 22. Ne zawsze jednak wartość stężena stechometrycznego dobrze odwzorowuje (UL) 0,5, co wynka z selektywnej dyfuzj cząsteczek palwa oraz tlenu. Błąd względny pomędzy wartoścą (UL) 0,5 a stężenem stechometrycznym można zapsać zgodne z równanem 24: 0,5 ( UL) C = C st st 24) Z dość dobrym przyblżenem wartość nepewnośc jest lnową funkcja masy molowej wg równana 25:
15 = 0,00472(M-32) 25) Oblczena przykładowe dla lczby F Zwązkem przykładowym przyjętym do oblczeń lczby F jest chlorooctan metylu ClCH 2 COOCH 3. Korzystając z równana 16 oraz tabel 4 oraz borąc pod uwagę budowę chemczna rozpatrywanej cząsteczk oblczena teoretyczne lczby F przedstawają sę następująco: Ilość szkeletowych atomów węgla w cząsteczce 2 (ne wlczamy atomu węgla grupy funkcyjnej) Ilość atomów wodoru w węglowodorze podstawowym (szkeletowym) 6 (etan) Ilość grup estrowych 1 R COO = 1/2 = 0,5 Ilość atomów chloru -1 R Cl = 1/6= 0,167 F calc =0,581(1-0,097R COO )(1-0,985R Cl )= 0,581(1-0,097 x 0,5)(1 0,985 x 0,167) = 0,462 Wartość lczby F oznaczona na podstawe danych eksperymentalnych przy wykorzystanu wzoru 1 wynos natomast: F obs = 1 L U 0,5 = 1 7,5 18,5 0,5 = 0,363 Tak węc można zauważyć, ż akurat w tym przypadku stneje dość duża rozbeżność pomędzy wartoścą wylczoną na podstawe symulacj a wartoścą oznaczoną na podstawe danych eksperymentalnych. Borąc pod uwagę analzowane przez Kondo współpracownków dane 238 zwązków chemcznych odchylene średne wylczena dla lczby F calc względem F obs wynos 0,047, co stanow średno 9,2% wartośc [2]. Stosowany wzór służący do oszacowana wartośc F calc ma zatem charakter wysoce orentacyjny. Przykładowe oblczane dolnej (L) oraz górnej (U) grancy wybuchowośc z wykorzystanem oszacowana lczby F Nnejsze oblczena stosuje sę wtedy, gdy ne mamy do dyspozycj tabelarycznych wartośc górnej oraz dolnej grancy wybuchowośc. Oblczamy teoretyczne lczbę F calc
16 analogczne jak w punkce Oblczena przykładowe dla lczby F, w następnej kolejnośc wyznaczamy stężene stechometryczne C st dla danego zwązku. W tym przypadku rozpatrzmy podobne jak w podpunkce poprzednm chlorooctan metylu dla którego pełna reakcja spalana przedstawa sę następująco: ClCH 2 COOCH O 2 = 3 CO H 2 O + HCl Zważywszy na to, ż lczba atomów wodoru jest wększa nż lczba atomów chloru spodzewanym produktem spalana będze chlorowodór zgodne z równanem 19. Stężene stechometryczne wynos natomast: 1 1 C st = = =0,0653=6,53% 1+ 4,773[3 + 0,25(5 1 2x2) 15,319 Uwzględnając masę molową zwązku (M=108,5 g/mol) poprawka wynos: = 0,00472 (M-32) = 0,00472 (108,5-32) = 0,361 Po przekształcenu wzoru 24 otrzymujemy teoretyczną wartość średnej geometrycznej granc wybuchowośc (UL) 0,5 : (UL) 0,5 = C st + C st = 0,361 x 0, ,0653 = 0,0889 A zatem na podstawe wzoru 17 oraz 18 oszacowana wartość górnej oraz dolnej grancy wybuchowośc wynos: L = (UL) 0,5 (1-F) = 0,0889(1-0,462) = 0,0478 = 4,78% U = (UL) 0,5 /(1-F) = 0,0889/(1-0,462) = 0,165 = 16,5% Wartośc obserwowane dolnej górnej grancy wybuchowośc wynoszą odpowedno 7,5% oraz 18,5%. Dla tej metodyk oblczeń, podobne jak w przypadku teoretycznego szacowana lczby F, teoretyczne wartośc dolnej oraz górnej grancy wybuchowośc należy traktować jedyne jako przyblżone.
17 Równana udokładnane (szczególne) Dla nektórych grup zwązków chemcznych wyznaczono równana udokładnane charakteryzujące sę dużo lepszym odwzorowanem wartośc oblczonych względem obserwowanych. Jedną z takch grup są fluorowane pochodne węglowodorów oraz prostych eterów [6]. Mechanzm analzy jest bardzo podobny z tą różncą, ż dotyczy szczególnych elementów strukturalnych, a przewdywana wartość średnej geometrycznej granc wybuchowośc jest opsany bardzej złożoną zależnoścą. Wartość teoretyczna lczby F określona jest następującym równanem: F=a 1 (1+a 2 C 1 +a 3 P OE +a 4 P US +a 5 E F +a 6 P sf3 +a 7 P df +a 8 P dfc +a 9 P df2 +a 10 P of +a 11 P of2 +a 12 P of3 ) 26) Średna geometryczna granc wybuchowośc wynos natomast: UL 0,5 = C st [1+q 1 (M-32)+q 2 C 1 +q 3 P OE +q 4 P US +q 5 R F +q 6 P df +q 7 P dfc +q 8 P df2 ] 27) przy czym: R F C 1 zgodne z opsem równana ogólnego omówonego wcześnej. Dla uproszczena R F można dla omówonej sytuacj zdefnować równeż jako lczbę atomów fluoru podzeloną przez sumę atomów wodoru fluoru w cząsteczce. Wartość lczbowa C 1 dla równań 26 oraz 27 jest nna, co pokazują tabele 5 oraz 6; P OE lość eterowych atomów tlenu podzelona przez lość szkeletowych atomów węgla pomnejszonych o jeden. I tak np. dla eteru d etylowego P OE = 1; P US oznacza stopeń nenasycena szkeletu węglowego podzelony przez lczbę szkeletowych atomów węgla pomnejszoną o jeden. I tak np. dla etylenu P US =1, dla acetylenu P US =2, dla butadenu P US =2/3. E F jest funkcją R F wyrażoną zgodne z równanem 28: E F = dla R F 0,625 28) 2 1 2,56RF E F = 0 dla R F > 0,625 Badana wykazały, ż w przeważającej wększośc zwązk o R F > 0,625 są nepalne; P sf3 oznacza lczbę atomów fluoru należącą do grup CF 3 -C, podzeloną przez sumę atomów wodoru oraz fluoru w cząsteczce. Np. dla CF 3 CH 3, P sf3 =3/6=0,5;
18 P df - oznacza lczbę atomów fluoru należącą do grup CHF=C, podzeloną przez sumę atomów wodoru oraz fluoru w cząsteczce. Np. dla CH 2 =CHF, P df =1/4; P dfc - oznacza lczbę atomów fluoru należącą do grup C-CF=C, podzeloną przez sumę atomów wodoru oraz fluoru w cząsteczce. Np. dla CH 2 =CF-CF 3, P dfc =1/6; P df2 - oznacza lczbę atomów fluoru należącą do grup CF 2 =C, podzeloną przez sumę atomów wodoru oraz fluoru w cząsteczce. Np. dla CF 2 =CHCF 3, P df2 =2/6=0,(3); P of - oznacza lczbę pojedynczych atomów fluoru przyłączonych do atomów węgla sąsadujących bezpośredno z eterowym atomem tlenu, podzeloną przez sumę atomów wodoru oraz fluoru w cząsteczce. Np. dla CH 3 CHFOCH 3, P of =1/8=0,125; P of2 - oznacza lczbę podwójnych atomów fluoru przyłączonych do atomów węgla sąsadujących bezpośredno z eterowym atomem tlenu, podzeloną przez sumę atomów wodoru oraz fluoru w cząsteczce. Np. dla CH 3 CF 2 OCH 3, P of =2/8=0,25; P of3 - oznacza lczbę atomów fluoru należącą do grup CF 3 -O, podzeloną przez sumę atomów wodoru oraz fluoru w cząsteczce. Np. dla CHF 2 CH 2 OCF 3, P of =3/8. Parametry równana służące do wylczena lczy F oraz UL 0,5 podano odpowedno w tabel 5 oraz 6. Tab. 5. Wartośc parametrów równana lczny F dla fluorowanych węglowodorów eterów [6] Parametr Ops parametru Wartość a 1 współczynnk główny 0,232 a 2 C 1-0,441 a 3 ugrupowane eterowe 0,619 a 4 Nenasycene 0,651 a 5 F 1,337 a 6 sf3 0,131 a 7 Df -0,682 a 8 Dfc -0,580 a 9 df2-0,360 a 10 Of 0,091 a 11 of2 0,175 a 12 of3-2,194
19 Tab. 6. Wartośc parametrów równana dla średnej geometrycznej granc wybuchowośc (UL) 0,5 fluorowanych węglowodorów eterów [6] Parametr Ops parametru Wartość q 1 (M-32) 0,0029 q 2 C 1-0,0210 q 3 Ugrupowane eterowe -0,0150 q 4 Nenasycene 0,4760 q 5 F 0,0180 q 6 Df -1,5050 q 7 Dfc -2,0040 q 8 df2-1,0220 Porównane wartośc eksperymentalnych z oblczonym teoretyczne na podstawe równań 26 oraz 27 wykazały bardzo dobrą dokładność dla zwązków o R F 0,625. Średna wartość błędu ne przekraczała w tym przypadku 0,55 % objętoścowego (średna maksymalna - fluorowane etery) dla dolnej grancy wybuchowośc oraz 1,25% objętoścowego (średna maksymalna -fluorowane węglowodory) dla górnej grancy wybuchowośc. Porównane charakterystyk pożarowych wybranych grup zwązków organcznych W tabel 7 zestawono przykładowe charakterystyk wybranych zwązków z grupy węglowodorów oraz ch pochodnych. Omówone zostaną efekty podstawena tylko nektórych grup funkcyjnych, dla których stneje dostateczne duża baza danych lteraturowych. Wybrane charakterystyk pożarowe dla różnych zwązków organcznych [5] wzór chemczny metan jego pochodne masa cząsteczkowa [g/mol] Tab. 7. lczba F współczynnk R lczba RF [kj/g] CH 4 16,04 0,46 1,94 39,5 CH 3 F 34,03 0,42 1,8 14,4 CH3CI 50,49 0,36 1,49 7,3 CH 3 Br 94,94 0,21 1,23 1,8 CH 2 F 2 52,02 0,33 1,3 4,6
20 CH 2 ClF 68,48 0,26 1,2 2,6 CH 2 Cl 2 84,93 0,18 1,23 1,2 etan jego pochodne CH 3 CH 3 30,07 0,51 1,88 49,4 CH 3 CH 2 Cl 64,51 0,5 1,72 19,6 CH 3 CH 2 Br 108,97 0,08 0,96 1 CH 3 CHF 2 66,05 0,47 1,61 14,9 CH 3 CHCl 2 98,96 0,35 1,38 5,9 CH 3 CF 3 84,04 0,39 1,35 6,7 CH 3 CClF 2 100,5 0,32 1,22 4,1 CH 3 CCl 2 F 116,95 0,24 1,05 2,4 CH 3 CCl 3 133,4 0,23 1,26 2 nne węglowodory CH 3 CH 2 CH 3 44,1 0,53 1,92 52,2 CH 3 CH 2 CH 2 CH 3 58,12 0,56 1,95 59 CH(CH 3 ) 3 58,12 0,54 1,73 52,9 CH 3 (CH 2 ) 3 CH 3 72,15 0,56 1,7 58,1 CH(CH 3 ) 2 CH 2 CH 3 72,15 0,57 1,82 60,2 węglowodory cyklczne (CH 2 ) 5 70,13 0,51 1,81 50,6 zwązk zawerające tlen C 2 H 5 OH 46,07 0,58 1,98 38,8 (CH 3 ) 2 CHOH 60,1 0,6 2,22 47,4 CH 3 OCH 3 46,07 0,65 1,92 52,4 CH 3 OCF 3 100,04 0,3 1,17 3,3 CH 3 OC 2 H 5 60,1 0,56 2,22 40,1 CH 3 OC 2 F 5 150,05 0,12 0,9 0,9 C 2 H 5 OC 2 H 5 74,12 0,77 1,78 114,5 CH 2 COC 2 H 5 72,11 0,65 2,62 59,1 HCOOCH 3 60,05 0,56 2,11 19,3 zwązk zawerające azot CH 3 NH 2 31,06 0,51 1,74 33,1 CH 3 CH 2 (NH 2 ) 45,08 0,5 0,51 35,2 zwązk nenasycone CH 2 =CH 2 28,05 0,73 2, CH 2 =CHF 46,04 0,65 2,97 47,6 CH 2 =CHCl 62,5 0,67 2,15 37,5 CH 2 =CF 2 64,03 0,49 1,72 15,1 CH 2 =CCl 2 96,94 0,35 1,46 5,5 CHCl=CHCl 96,94 0,34 1,69 5,2 CHCl=CCl 2 131,39 0,13 1,19 1 CF 2 =CF 2 100,02 0,55 1,73 8,3 CF 2 =CFCl 116,47 0,28 1,71 2,1 CH 3 CH=CH 2 42,08 0,58 2,22 62,1
21 C 2 H 2 26,04 0,84 3,09 256,8 zwązk neorganczne H 2 2,02 0,77 7,4 401,5 NH 3 17,03 0,27 1,46 6,9 CO 28,01 0,59 2,37 14,5 SH 4 32,12 0,88 6,92 335,6 Efekt wprowadzena halogenu Wyraźne da sę zauważyć, ż wprowadzene halogenu zmnejsza wartośc lczbowe F, R oraz RF, co wskazuje na zmnejszene stopna palnośc po wprowadzenu podstawnka halogenowego. Wartość efektu wzrasta proporcjonalne do masy molowej halogenu, co dla pochodnych metanu przedstawono na podstawe analzy lczby RF na rycne 1. Jest to zwązane mędzy nnym z malejącą energą dysocjacj wązana węgel halogen, która wynos odpowedno: CH 3 -F (453 kj/mol), CH 3 -Cl (352 kj/mol), CH 3 -Br (293 (kj/mol), CH 3 -J (235 kj/mol). Zwększene lczby atomów halogenu równeż wyraźne wypływa na obnżene palnośc zwązku, co najlepej wdać porównując wartośc lczby RF (ry 2) ,5 30 RF [kj/g] 20 14,4 10 7,3 1,8 0 metan fluormetan chlorometan bromometan Ryc 1. Wpływ typu halogenu na wartość lczby RF dla monohalogenometanów
22 50 40 RF [kj/g] X = Cl X = F n X Ryc. 2. Wpływ lośc atomów halogenu n X (chloru oraz fluoru) dla halogenopochodnych etanu na wartość lczby RF. Efekt wprowadzena wązana olefnowego Wprowadzene wązana nenasyconego wyraźne zwększa wartość lczby RF pod warunkem, ż ne tworzy sę układ aromatyczny. Szczególne jest to wdoczne w przypadku dwuwęglowych węglowodorów (ryc. 3). Efekt ten spada wraz ze wzrostem lośc atomów węgla co wdać wyraźne już dla trojwęglowych węglowodorów, dla których wartośc RF wynoszą odpowedno: propan RF = 52,2; propen RF=62,1; propyn RF = 77,6.
23 RF [kj/g] ,4 0 etan eten etyn Ryc 3. Wpływ typu wązana mędzy atomam węgla na wartość lczby RF dla dwuwęglowych węglowodorów Efekt wprowadzena układu aromatycznego Wprowadzene układu aromatycznego zmnejsza wartość lczby RF, a zatem zwększa odporność układu na czynnk termczne. Wynka to ze stablzacj układu aromatycznego poprzez delokalzacje elektronów π perścena. Analza wartośc lczby F ne wykazuje jednak poważnych różnc. Dla sztandarowego przykładu porównawczego benzenu oraz heksanu lczby te wynoszą odpowedno: heksan F=0,617 RF=77,9; benzen F=0,594 RF=61,24. Efekt wprowadzena perścena alfatycznego Wartość lczby RF, F oraz współczynnka R dla cykloheksanu oraz cyklopentanu jest nższa nż ch nasyconych lnowych odpowednków. A zatem pojawene sę perścena pęco- sześcoczłonowego stablzuje układ, jednakże ne tak, jak ma to mejsce w przypadku perścena aromatycznego. Wartość lczby RF dla cyklopentanu oraz cykloheksanu wynos odpowedno 50,6 oraz 69, natomast wartośc dla pentanu oraz heksanu
24 wynoszą odpowedno 58,1 oraz 77,9. Sytuacja sę dametralne zmena w przypadku pojawena sę układów małoperścenowych. Dla cyklopropanu wartość lczby RF wynos aż 167 w stosunku do 52,2 odpowadającej propanow. Wynka to z faktu bardzo dużych naprężeń sterycznych perścena trójczłonowego. Badana prowadzone przez Kondo [2] dają dodatn parametr p 7 dla układów perścenowych. Wartość ta jednak jest zbyt ogólna wskutek nerozróżnana przez autora welkośc perścen, co ma stotne znaczene przy rozpatrywanu problemu. Efekt wprowadzena grupy amnowej Wprowadzene grupy amnowej powoduje wyraźny spadek wartośc RF. W przypadku metyloamny wartość ta wynos 33,1, natomast etyloamny 35. Podobne rezultaty można wycągnąć analzując współczynnk R, który jest wyraźne mnejszy dla amn. Badana dotyczące lczby F przeprowadzone przez Kondo [2] wykazują ujemną wartość parametru p 15, co równeż potwerdza nhbcyjny charakter grupy amnowej. W przypadku metylo- oraz etyloamny wartośc lczby F są jednak bardzo zblżone do sebe. Efekt wprowadzena grupy hydroksylowej Efekt wprowadzena grupy hydroksylowej powoduje neznaczne zwększene wartośc lczby F oraz współczynnka R. Obserwuje sę jednak zmnejszene wartośc RF dla alkohol nskocząsteczkowych. Począwszy od butanol RF alkohol jest wyższe nż odpowada to węglowodorow podstawowemu. Zatem wprowadzene grupy OH generalne zwększa palność zwązku chemcznego. Dane porównawcze dla wybranych alkohol odpowadających m węglowodorów zestawono w tabel 8. Wybrane charakterystyk pożarowe dla węglowodorów oraz ch pochodnych hydroksylowych Tab. 8. wzór chemczny masa cząsteczkowa [g/mol] lczba F współczynnk R lczba RF [kj/g] CH ,46 1,94 39,5 CH 3 OH 32 0,42 1,8 32,9 C 2 H ,51 1,88 49,4 C 2 H 5 OH 46 0,58 1,98 38,8 C 3 H ,53 1,92 52,2
25 n-c 3 H 7 OH 60 0,6 2,12 46,3 n-c 4 H ,56 1,95 59,0 n-c 4 H 9 OH 74 0,65 2,41 65,9 n-c 5 H ,56 1,7 58,1 n-c 5 H 11 OH 88 0,65 2,27 71,3 zo-c 4 H ,54 1,73 52,9 zo-c 4 H 9 OH 74 0,60 1,99 54,0 zo-c 5 H ,57 1,82 60,2 zo-c 5 H 11 OH 72 0,63 1,82 65,7 Efekt wprowadzena grupy karboksylowej Wprowadzene grupy karboksylowej powoduje wyraźne obnżene lczby RF. Tendencja ta jest szczególne wdoczna dla nskocząsteczkowych kwasów karboksylowych. Jest to łatwe do przewdzena, gdyż w etape dekompozycj tworzy sę CO 2 a m wększy % udzału grypy karboksylowej w zwązku tym efekt będze slnejszy. Wybrane charakterystyk pożarowe dla kwasów karboksylowych Tab. 8. masa cząsteczkowa wzór chemczny [g/mol] lczba F współczynnk R lczba RF [kj/g] HCOOH 46 0,44 1,64 4,3 CH 3 COOH 60 0,55 2,38 17,9 C 2 H 5 COOH 74 0,51 1,95 21,5 n-c 3 H 7 COOH 88 0,55 1,82 30,7 n-c 4 H 9 COOH 102 0,53 1,95 31,7 Podsumowane Odpowedne podejśce znajomość parametrów fzykochemcznych ma bardzo duże znaczene przy określanu ryzyka zwązanego z nepożądanym uwolnenem sę substancj chemcznej [11-14]. W publkacj zostało przedstawone z jakch parametrów możemy korzystać próbując określć charakterystyk pożarowe analzowanych substancj. Przewdywana neznanych parametrów, zwłaszcza w przypadku dolnej oraz górnej grancy wybuchowośc, można dokonać z dość dużą dokładnoścą analzując strukturę węglowodorów. Analza taka w przypadku zależnośc bazujących na wpływe danego typu podstawnka dla pochodnych węglowodorów odbywa sę już z mnejszą dokładnoścą otrzymane dokładnejszego odwzorowana rzeczywstośc wymaga zastosowana wzorów szczególnych [6]. Wynka to z faktu ogranczonej lośc dostępnych danych lteraturowych
26 oraz bardzo dużej lośc kombnacj, które należałoby uwzględnć dokonując analzy. W przypadku oblczeń teoretycznych zwązanych z lczbą F zakłada sę jedyne 17 parametrów, ne uwzględnając np. struktury perścen, co będze powodować poważne błędy w przypadku oblczeń dla zwązków małoperścenowych. Oblczena teoretyczne górnej grancy wybuchowośc przy założenu stężena stechometrycznego przy pełnym spalanu dają duże błędy przypadku zwązków o bardzo wysokej górnej grancy wybuchowośc, takch jak np. tlenek etylenu, tlenek propylenu, epchlorohydryna, eten, acetylen, eter detylowy, doksan. Zwązane jest to z błędnym założenem autorów uwzględnających reakcję pełnego spalana przy nedoborze tlenu, z jakm mamy do czynena w procese spalana przy górnej grancy wybuchowośc. Charakterystyk opsane w nnejszej publkacj sposób ch prezentacj wymaga dużego wyczuca mogą one zostać wykorzystane do określena nebezpeczeństwa pożarowego danego zwązku chemcznego, zwłaszcza do określena hpotetycznej wartośc górnej oraz dolnej grancy wybuchowośc. Właśne te parametry stanową najważnejszą charakterystykę pożarową zwązków chemcznych. Oznaczene wartośc lczby F, lczby RF oraz współczynnka R ma jedyne charakter pomocnczy, jednakże stotny pod kątem projektowana cząsteczek posadających wewnętrzny proces nhbcj procesu spalana, co ma stotne znaczene przy poszukwanu środków ognochronnych [15,16] Lteratura 1. Shepherd J. E, Perez., F. A., Kerosene lamps and cookstoves The hazards of gasolne contamnaton, Fre Safety Journal 43 (2008) pp ; 2. Kondo S., Urano Y., Tokuhash K., Takahash A., Tanaka K., Predcton of flammablty of gases by usng F-number analyss, J. Hazardous Mat. A82 (2001), pp ; 3. Albahr T. A., Flammablty characterstcs of pure hydrocarbons, Chemcal Engneerng Scence 58 (2003), pp ; 4. Kondo S., Takahash A., Tokuhash K., Expermental exploraton of dscrepances n F-number correlaton of flammablty lmts, J. Hazardous Mat. A100 (2003) pp.27 36; 5. Kondo S., Takahash A., Tokuhash K., Sekya A., RF number as ndex for assessng combuston hazard of flammable gases, J. Hazardous Mat. A93 (2002), pp ;
27 6. Kondo S., Takzawa K., Takahash A., Tokuhash K., Mzukado J., Sekya A., Flammabalty lmts of olefne and saturated fluoro-compounds, J. Hazardous Mat. 171 (2009), pp ; Bodhurtha F. P., Industral exploson preventon and protecton, Mc-Graw Hll, New York, 1980; 7. Raz M. R., Daubert T. E., Predctng flash and pour ponts, Hydrocarbon Processng, 56 (1987), pp ; 8. Patl G. S., Estmaton of flash pont, Fre and Materals, 12 (1988), pp ; 9. Satyanarayana K., Kakat M. C., Correlaton of flash ponts, Fre and Materals, 15 (1991), pp ; 10. Poft-Szczepańska M., Analza tworzena sę zagrożeń pożarowo-wybuchowych na nstalacjach przerobu ropy naftowej w wynku zapalena sę prosarczków (cz. 2). Zabezpeczene nstalacj przerobu ropy naftowej przed zagrożenam wynkającym z obecnośc parosarczków, [w:] Bezpeczeństwo Technka Pożarncza 01/2008, str ; 11. Obolewcz A., Zagrożena zwązane z transportem drogowym towarów nebezpecznych a tunele drogowe,[w:] Bezpeczeństwo Technka Pożarncza 02 (14) 2009, str ; 12. Węsersk T., Chema toksykologa epchlorohydryny pod kątem przydatnośc dla dzałań straży pożarnych. Podstawy analzy ryzyka, [w:] Bezpeczeństwo Technka Pożarncza 02 (18) 2010, str ; 13. Węsersk T., Funkcje probtowe jako narzędze oceny skutków uwolnena nebezpecznych substancj chemcznych. Symulacja oblczeń dla uwolnena sę gazowego chloru, [w:] Bezpeczeństwo Technka Pożarncza 02 (18) 2010, str ; 14. Nagrodzka M., Małozęć D., Znaczene środków ognochronnych wykorzystywanych w materałach stosowanych w budownctwe, [w:] Bezpeczeństwo Technka Pożarncza 02 (18) 2010, str ; 15. Małozęć D., Konuch A., Reakcja na ogeń. Metody badań krytera klasyfkacj, [w:] Bezpeczeństwo Technka Pożarncza 01 (17) 2010, str Recenzenc: dr nż. Waldemar Jaskółowsk dr nż. Stefan Wlczkowsk
W praktyce często zdarza się, że wyniki obu prób możemy traktować jako. wyniki pomiarów na tym samym elemencie populacji np.
 Wykład 7 Uwaga: W praktyce często zdarza sę, że wynk obu prób możemy traktować jako wynk pomarów na tym samym elemence populacj np. wynk x przed wynk y po operacj dla tego samego osobnka. Należy wówczas
Wykład 7 Uwaga: W praktyce często zdarza sę, że wynk obu prób możemy traktować jako wynk pomarów na tym samym elemence populacj np. wynk x przed wynk y po operacj dla tego samego osobnka. Należy wówczas
α i = n i /n β i = V i /V α i = β i γ i = m i /m
 Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE
 Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ],
![STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ], STATECZNOŚĆ SKARP. α - kąt nachylenia skarpy [ o ], φ - kąt tarcia wewnętrznego gruntu [ o ],](/thumbs/27/11347185.jpg) STATECZNOŚĆ SKARP W przypadku obektu wykonanego z gruntów nespostych zaprojektowane bezpecznego nachylena skarp sprowadza sę do przekształcena wzoru na współczynnk statecznośc do postac: tgφ tgα = n gdze:
STATECZNOŚĆ SKARP W przypadku obektu wykonanego z gruntów nespostych zaprojektowane bezpecznego nachylena skarp sprowadza sę do przekształcena wzoru na współczynnk statecznośc do postac: tgφ tgα = n gdze:
KURS STATYSTYKA. Lekcja 6 Regresja i linie regresji ZADANIE DOMOWE. www.etrapez.pl Strona 1
 KURS STATYSTYKA Lekcja 6 Regresja lne regresj ZADANIE DOMOWE www.etrapez.pl Strona 1 Część 1: TEST Zaznacz poprawną odpowedź (tylko jedna jest prawdzwa). Pytane 1 Funkcja regresj I rodzaju cechy Y zależnej
KURS STATYSTYKA Lekcja 6 Regresja lne regresj ZADANIE DOMOWE www.etrapez.pl Strona 1 Część 1: TEST Zaznacz poprawną odpowedź (tylko jedna jest prawdzwa). Pytane 1 Funkcja regresj I rodzaju cechy Y zależnej
Analiza rodzajów skutków i krytyczności uszkodzeń FMECA/FMEA według MIL STD - 1629A
 Analza rodzajów skutków krytycznośc uszkodzeń FMECA/FMEA według MIL STD - 629A Celem analzy krytycznośc jest szeregowane potencjalnych rodzajów uszkodzeń zdentyfkowanych zgodne z zasadam FMEA na podstawe
Analza rodzajów skutków krytycznośc uszkodzeń FMECA/FMEA według MIL STD - 629A Celem analzy krytycznośc jest szeregowane potencjalnych rodzajów uszkodzeń zdentyfkowanych zgodne z zasadam FMEA na podstawe
ELEKTROCHEMIA. ( i = i ) Wykład II b. Nadnapięcie Równanie Buttlera-Volmera Równania Tafela. Wykład II. Równowaga dynamiczna i prąd wymiany
 Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
SZACOWANIE NIEPEWNOŚCI POMIARU METODĄ PROPAGACJI ROZKŁADÓW
 SZACOWANIE NIEPEWNOŚCI POMIARU METODĄ PROPAGACJI ROZKŁADÓW Stefan WÓJTOWICZ, Katarzyna BIERNAT ZAKŁAD METROLOGII I BADAŃ NIENISZCZĄCYCH INSTYTUT ELEKTROTECHNIKI ul. Pożaryskego 8, 04-703 Warszawa tel.
SZACOWANIE NIEPEWNOŚCI POMIARU METODĄ PROPAGACJI ROZKŁADÓW Stefan WÓJTOWICZ, Katarzyna BIERNAT ZAKŁAD METROLOGII I BADAŃ NIENISZCZĄCYCH INSTYTUT ELEKTROTECHNIKI ul. Pożaryskego 8, 04-703 Warszawa tel.
Systemy Ochrony Powietrza Ćwiczenia Laboratoryjne
 ś POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr nż. Łukasz Amanowcz Systemy Ochrony Powetrza Ćwczena Laboratoryjne 2 TEMAT ĆWICZENIA: Oznaczane lczbowego rozkładu lnowych projekcyjnych
ś POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr nż. Łukasz Amanowcz Systemy Ochrony Powetrza Ćwczena Laboratoryjne 2 TEMAT ĆWICZENIA: Oznaczane lczbowego rozkładu lnowych projekcyjnych
 Zadane 1: Wyznacz średne ruchome 3-okresowe z następujących danych obrazujących zużyce energ elektrycznej [kwh] w pewnym zakładze w mesącach styczeń - lpec 1998 r.: 400; 410; 430; 40; 400; 380; 370. Zadane
Zadane 1: Wyznacz średne ruchome 3-okresowe z następujących danych obrazujących zużyce energ elektrycznej [kwh] w pewnym zakładze w mesącach styczeń - lpec 1998 r.: 400; 410; 430; 40; 400; 380; 370. Zadane
Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 1. Układy równań liniowych
 Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
OGÓLNE PODSTAWY SPEKTROSKOPII
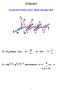 WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
Kształtowanie się firm informatycznych jako nowych elementów struktury przestrzennej przemysłu
 PRACE KOMISJI GEOGRAFII PRZEMY SŁU Nr 7 WARSZAWA KRAKÓW 2004 Akadema Pedagogczna, Kraków Kształtowane sę frm nformatycznych jako nowych elementów struktury przestrzennej przemysłu Postępujący proces rozwoju
PRACE KOMISJI GEOGRAFII PRZEMY SŁU Nr 7 WARSZAWA KRAKÓW 2004 Akadema Pedagogczna, Kraków Kształtowane sę frm nformatycznych jako nowych elementów struktury przestrzennej przemysłu Postępujący proces rozwoju
Za: Stanisław Latoś, Niwelacja trygonometryczna, [w:] Ćwiczenia z geodezji II [red.] J. Beluch
![Za: Stanisław Latoś, Niwelacja trygonometryczna, [w:] Ćwiczenia z geodezji II [red.] J. Beluch Za: Stanisław Latoś, Niwelacja trygonometryczna, [w:] Ćwiczenia z geodezji II [red.] J. Beluch](/thumbs/25/5046464.jpg) Za: Stansław Latoś, Nwelacja trygonometryczna, [w:] Ćwczena z geodezj II [red.] J. eluch 6.1. Ogólne zasady nwelacj trygonometrycznej. Wprowadzene Nwelacja trygonometryczna, zwana równeż trygonometrycznym
Za: Stansław Latoś, Nwelacja trygonometryczna, [w:] Ćwczena z geodezj II [red.] J. eluch 6.1. Ogólne zasady nwelacj trygonometrycznej. Wprowadzene Nwelacja trygonometryczna, zwana równeż trygonometrycznym
Modele wieloczynnikowe. Modele wieloczynnikowe. Modele wieloczynnikowe ogólne. α β β β ε. Analiza i Zarządzanie Portfelem cz. 4.
 Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
± Δ. Podstawowe pojęcia procesu pomiarowego. x rzeczywiste. Określenie jakości poznania rzeczywistości
 Podstawowe pojęca procesu pomarowego kreślene jakośc poznana rzeczywstośc Δ zmerzone rzeczywste 17 9 Zalety stosowana elektrycznych przyrządów 1/ 1. możlwość budowy czujnków zamenających werne każdą welkość
Podstawowe pojęca procesu pomarowego kreślene jakośc poznana rzeczywstośc Δ zmerzone rzeczywste 17 9 Zalety stosowana elektrycznych przyrządów 1/ 1. możlwość budowy czujnków zamenających werne każdą welkość
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 2(88)/2012
 ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW (88)/01 Hubert Sar, Potr Fundowcz 1 WYZNACZANIE ASOWEGO OENTU BEZWŁADNOŚCI WZGLĘDE OSI PIONOWEJ DLA SAOCHODU TYPU VAN NA PODSTAWIE WZORU EPIRYCZNEGO 1. Wstęp asowy moment
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW (88)/01 Hubert Sar, Potr Fundowcz 1 WYZNACZANIE ASOWEGO OENTU BEZWŁADNOŚCI WZGLĘDE OSI PIONOWEJ DLA SAOCHODU TYPU VAN NA PODSTAWIE WZORU EPIRYCZNEGO 1. Wstęp asowy moment
Stanisław Cichocki Natalia Nehrebecka. Zajęcia 4
 Stansław Cchock Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0-1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających Interpretacja
Stansław Cchock Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0-1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających Interpretacja
Analiza danych OGÓLNY SCHEMAT. http://zajecia.jakubw.pl/ Dane treningowe (znana decyzja) Klasyfikator. Dane testowe (znana decyzja)
 Analza danych Dane trenngowe testowe. Algorytm k najblższych sąsadów. Jakub Wróblewsk jakubw@pjwstk.edu.pl http://zajeca.jakubw.pl/ OGÓLNY SCHEMAT Mamy dany zbór danych podzelony na klasy decyzyjne, oraz
Analza danych Dane trenngowe testowe. Algorytm k najblższych sąsadów. Jakub Wróblewsk jakubw@pjwstk.edu.pl http://zajeca.jakubw.pl/ OGÓLNY SCHEMAT Mamy dany zbór danych podzelony na klasy decyzyjne, oraz
Opracowanie metody predykcji czasu życia baterii na obiekcie i oceny jej aktualnego stanu na podstawie analizy bieżących parametrów jej eksploatacji.
 Zakład Systemów Zaslana (Z-5) Opracowane nr 323/Z5 z pracy statutowej pt. Opracowane metody predykcj czasu życa bater na obekce oceny jej aktualnego stanu na podstawe analzy beżących parametrów jej eksploatacj.
Zakład Systemów Zaslana (Z-5) Opracowane nr 323/Z5 z pracy statutowej pt. Opracowane metody predykcj czasu życa bater na obekce oceny jej aktualnego stanu na podstawe analzy beżących parametrów jej eksploatacj.
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Natalia Nehrebecka. Zajęcia 4
 St ł Cchock Stansław C h k Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0 1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających
St ł Cchock Stansław C h k Natala Nehrebecka Zajęca 4 1. Interpretacja parametrów przy zmennych zerojedynkowych Zmenne 0 1 Interpretacja przy zmennej 0 1 w modelu lnowym względem zmennych objaśnających
BADANIE STABILNOŚCI WSPÓŁCZYNNIKA BETA AKCJI INDEKSU WIG20
 Darusz Letkowsk Unwersytet Łódzk BADANIE STABILNOŚCI WSPÓŁCZYNNIKA BETA AKCJI INDEKSU WIG0 Wprowadzene Teora wyboru efektywnego portfela nwestycyjnego zaproponowana przez H. Markowtza oraz jej rozwnęca
Darusz Letkowsk Unwersytet Łódzk BADANIE STABILNOŚCI WSPÓŁCZYNNIKA BETA AKCJI INDEKSU WIG0 Wprowadzene Teora wyboru efektywnego portfela nwestycyjnego zaproponowana przez H. Markowtza oraz jej rozwnęca
Węglowodory poziom podstawowy
 Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Wykład 7. Podstawy termodynamiki i kinetyki procesowej - wykład 7. Anna Ptaszek. 21 maja Katedra Inżynierii i Aparatury Przemysłu Spożywczego
 Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
Zastosowanie symulatora ChemCad do modelowania złożonych układów reakcyjnych procesów petrochemicznych
 NAFTA-GAZ styczeń 2011 ROK LXVII Anna Rembesa-Śmszek Instytut Nafty Gazu, Kraków Andrzej Wyczesany Poltechnka Krakowska, Kraków Zastosowane symulatora ChemCad do modelowana złożonych układów reakcyjnych
NAFTA-GAZ styczeń 2011 ROK LXVII Anna Rembesa-Śmszek Instytut Nafty Gazu, Kraków Andrzej Wyczesany Poltechnka Krakowska, Kraków Zastosowane symulatora ChemCad do modelowana złożonych układów reakcyjnych
Analiza danych. Analiza danych wielowymiarowych. Regresja liniowa. Dyskryminacja liniowa. PARA ZMIENNYCH LOSOWYCH
 Analza danych Analza danych welowymarowych. Regresja lnowa. Dyskrymnacja lnowa. Jakub Wróblewsk jakubw@pjwstk.edu.pl http://zajeca.jakubw.pl/ PARA ZMIENNYCH LOSOWYCH Parę zmennych losowych X, Y możemy
Analza danych Analza danych welowymarowych. Regresja lnowa. Dyskrymnacja lnowa. Jakub Wróblewsk jakubw@pjwstk.edu.pl http://zajeca.jakubw.pl/ PARA ZMIENNYCH LOSOWYCH Parę zmennych losowych X, Y możemy
Współczynnik przenikania ciepła U v. 4.00
 Współczynnk przenkana cepła U v. 4.00 1 WYMAGANIA Maksymalne wartośc współczynnków przenkana cepła U dla ścan, stropów, stropodachów, oken drzw balkonowych podano w załącznku do Rozporządzena Mnstra Infrastruktury
Współczynnk przenkana cepła U v. 4.00 1 WYMAGANIA Maksymalne wartośc współczynnków przenkana cepła U dla ścan, stropów, stropodachów, oken drzw balkonowych podano w załącznku do Rozporządzena Mnstra Infrastruktury
Teoria niepewności pomiaru (Rachunek niepewności pomiaru) Rodzaje błędów pomiaru
 Pomary fzyczne - dokonywane tylko ze skończoną dokładnoścą. Powodem - nedoskonałość przyrządów pomarowych neprecyzyjność naszych zmysłów borących udzał w obserwacjach. Podawane samego tylko wynku pomaru
Pomary fzyczne - dokonywane tylko ze skończoną dokładnoścą. Powodem - nedoskonałość przyrządów pomarowych neprecyzyjność naszych zmysłów borących udzał w obserwacjach. Podawane samego tylko wynku pomaru
Wprowadzenie. Estimation of properties hydrocarbons plus fraction
 Średna masa cząsteczkowa frakcj C+ węglowodorów jest znaczącym parametrem składu chemcznego ropy naftowej. Uzyskuje sę ją w wynku destylacj laboratoryjnej TBP próbk ropy. W artykule pokazano możlwośc wykorzystana
Średna masa cząsteczkowa frakcj C+ węglowodorów jest znaczącym parametrem składu chemcznego ropy naftowej. Uzyskuje sę ją w wynku destylacj laboratoryjnej TBP próbk ropy. W artykule pokazano możlwośc wykorzystana
Natalia Nehrebecka. Wykład 2
 Natala Nehrebecka Wykład . Model lnowy Postad modelu lnowego Zaps macerzowy modelu lnowego. Estymacja modelu Wartośd teoretyczna (dopasowana) Reszty 3. MNK przypadek jednej zmennej . Model lnowy Postad
Natala Nehrebecka Wykład . Model lnowy Postad modelu lnowego Zaps macerzowy modelu lnowego. Estymacja modelu Wartośd teoretyczna (dopasowana) Reszty 3. MNK przypadek jednej zmennej . Model lnowy Postad
ZESZYTY NAUKOWE INSTYTUTU POJAZDÓW 5(96)/2013
 ZESZYTY NAUKOWE NSTYTUTU POJAZDÓW 5(96)/2013 Hubert Sar, Potr Fundowcz 1 WYZNACZANE MASOWEGO MOMENTU BEZWŁADNOŚC WZGLĘDEM OS PODŁUŻNEJ DLA SAMOCHODU TYPU VAN NA PODSTAWE WZORÓW DOŚWADCZALNYCH 1. Wstęp
ZESZYTY NAUKOWE NSTYTUTU POJAZDÓW 5(96)/2013 Hubert Sar, Potr Fundowcz 1 WYZNACZANE MASOWEGO MOMENTU BEZWŁADNOŚC WZGLĘDEM OS PODŁUŻNEJ DLA SAMOCHODU TYPU VAN NA PODSTAWE WZORÓW DOŚWADCZALNYCH 1. Wstęp
I. Elementy analizy matematycznej
 WSTAWKA MATEMATYCZNA I. Elementy analzy matematycznej Pochodna funkcj f(x) Pochodna funkcj podaje nam prędkość zman funkcj: df f (x + x) f (x) f '(x) = = lm x 0 (1) dx x Pochodna funkcj podaje nam zarazem
WSTAWKA MATEMATYCZNA I. Elementy analzy matematycznej Pochodna funkcj f(x) Pochodna funkcj podaje nam prędkość zman funkcj: df f (x + x) f (x) f '(x) = = lm x 0 (1) dx x Pochodna funkcj podaje nam zarazem
WĘGLOWODORY POWTÓRZENIE WIADOMOŚCI
 WĘGLOWODORY POWTÓRZENIE WIADOMOŚCI 1. W kórym punkcie zapisano wyłącznie węglowodory odbarwiające wodę bromową: a) C 2 H 6 ; C 4 H 10 ; C 6 H 14 b) C 9 H 20 ; C 8 H 16 ; C 2 H 4 c) C 2 H 2 ; C 3 H 6 ;
WĘGLOWODORY POWTÓRZENIE WIADOMOŚCI 1. W kórym punkcie zapisano wyłącznie węglowodory odbarwiające wodę bromową: a) C 2 H 6 ; C 4 H 10 ; C 6 H 14 b) C 9 H 20 ; C 8 H 16 ; C 2 H 4 c) C 2 H 2 ; C 3 H 6 ;
C C CH 3. 2.Narysuj w wzory Newmana związków A, B, C. Znajdź najkorzystniejszą konformację (rozpatruj rotację wokół pogrubionego wiązania) C CH 2
 Prosemnarum 4 Podstawy hem Organcznej 14-0-2016 1. Określ le produktów monochlorowana powstane w reakcj ponższych zwązków z l 2 w obecnośc śwatła. Jake będą proporcje? Reaktywność atomów wodoru na podstawene
Prosemnarum 4 Podstawy hem Organcznej 14-0-2016 1. Określ le produktów monochlorowana powstane w reakcj ponższych zwązków z l 2 w obecnośc śwatła. Jake będą proporcje? Reaktywność atomów wodoru na podstawene
STARE A NOWE KRAJE UE KONKURENCYJNOŚĆ POLSKIEGO EKSPORTU
 Ewa Szymank Katedra Teor Ekonom Akadema Ekonomczna w Krakowe ul. Rakowcka 27, 31-510 Kraków STARE A NOWE KRAJE UE KONKURENCYJNOŚĆ POLSKIEGO EKSPORTU Abstrakt Artykuł przedstawa wynk badań konkurencyjnośc
Ewa Szymank Katedra Teor Ekonom Akadema Ekonomczna w Krakowe ul. Rakowcka 27, 31-510 Kraków STARE A NOWE KRAJE UE KONKURENCYJNOŚĆ POLSKIEGO EKSPORTU Abstrakt Artykuł przedstawa wynk badań konkurencyjnośc
Refraktometria. sin β sin β
 efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
Test kompetencji z chemii do liceum. Grupa A.
 Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
PROSTO O DOPASOWANIU PROSTYCH, CZYLI ANALIZA REGRESJI LINIOWEJ W PRAKTYCE
 PROSTO O DOPASOWANIU PROSTYCH, CZYLI ANALIZA REGRESJI LINIOWEJ W PRAKTYCE Janusz Wątroba, StatSoft Polska Sp. z o.o. W nemal wszystkch dzedznach badań emprycznych mamy do czynena ze złożonoścą zjawsk procesów.
PROSTO O DOPASOWANIU PROSTYCH, CZYLI ANALIZA REGRESJI LINIOWEJ W PRAKTYCE Janusz Wątroba, StatSoft Polska Sp. z o.o. W nemal wszystkch dzedznach badań emprycznych mamy do czynena ze złożonoścą zjawsk procesów.
Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2014/2015
 Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2014/2015 PRZYKŁADOWE ROZWIĄZANIA WRAZ Z PUNKTACJĄ Maksymalna liczba punktów możliwa do uzyskania po
Wojewódzki Konkurs Przedmiotowy z Chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2014/2015 PRZYKŁADOWE ROZWIĄZANIA WRAZ Z PUNKTACJĄ Maksymalna liczba punktów możliwa do uzyskania po
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
ZASTOSOWANIE ANALIZY HARMONICZNEJ DO OKREŚLENIA SIŁY I DŁUGOŚCI CYKLI GIEŁDOWYCH
 Grzegorz PRZEKOTA ZESZYTY NAUKOWE WYDZIAŁU NAUK EKONOMICZNYCH ZASTOSOWANIE ANALIZY HARMONICZNEJ DO OKREŚLENIA SIŁY I DŁUGOŚCI CYKLI GIEŁDOWYCH Zarys treśc: W pracy podjęto problem dentyfkacj cykl gełdowych.
Grzegorz PRZEKOTA ZESZYTY NAUKOWE WYDZIAŁU NAUK EKONOMICZNYCH ZASTOSOWANIE ANALIZY HARMONICZNEJ DO OKREŚLENIA SIŁY I DŁUGOŚCI CYKLI GIEŁDOWYCH Zarys treśc: W pracy podjęto problem dentyfkacj cykl gełdowych.
Praca podkładu kolejowego jako konstrukcji o zmiennym przekroju poprzecznym zagadnienie ekwiwalentnego przekroju
 Praca podkładu kolejowego jako konstrukcj o zmennym przekroju poprzecznym zagadnene ekwwalentnego przekroju Work of a ralway sleeper as a structure wth varable cross-secton - the ssue of an equvalent cross-secton
Praca podkładu kolejowego jako konstrukcj o zmennym przekroju poprzecznym zagadnene ekwwalentnego przekroju Work of a ralway sleeper as a structure wth varable cross-secton - the ssue of an equvalent cross-secton
Współczynniki aktywności w roztworach elektrolitów. W.a. w roztworach elektrolitów (2) W.a. w roztworach elektrolitów (3) 1 r. Przypomnienie!
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Test sprawdzający, wielostopniowy z chemii: Węglowodory
 Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
Twierdzenie Bezouta i liczby zespolone Javier de Lucas. Rozwi azanie 2. Z twierdzenia dzielenia wielomianów, mamy, że
 Twerdzene Bezouta lczby zespolone Javer de Lucas Ćwczene 1 Ustal dla których a, b R można podzelć f 1 X) = X 4 3X 2 + ax b przez f 2 X) = X 2 3X+2 Oblcz a b Z 5 jeżel zak ladamy, że f 1 f 2 s a welomanam
Twerdzene Bezouta lczby zespolone Javer de Lucas Ćwczene 1 Ustal dla których a, b R można podzelć f 1 X) = X 4 3X 2 + ax b przez f 2 X) = X 2 3X+2 Oblcz a b Z 5 jeżel zak ladamy, że f 1 f 2 s a welomanam
= σ σ. 5. CML Capital Market Line, Rynkowa Linia Kapitału
 5 CML Catal Market Lne, ynkowa Lna Katału Zbór ortolo o nalny odchylenu standardowy zbór eektywny ozważy ortolo złożone ze wszystkch aktywów stnejących na rynku Załóży, że jest ch N A * P H P Q P 3 * B
5 CML Catal Market Lne, ynkowa Lna Katału Zbór ortolo o nalny odchylenu standardowy zbór eektywny ozważy ortolo złożone ze wszystkch aktywów stnejących na rynku Załóży, że jest ch N A * P H P Q P 3 * B
Płyny nienewtonowskie i zjawisko tiksotropii
 Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Proces narodzin i śmierci
 Proces narodzn śmerc Jeżel w ewnej oulacj nowe osobnk ojawają sę w sosób losowy, rzy czym gęstość zdarzeń na jednostkę czasu jest stała w czase wynos λ, oraz lczba osobnków n, które ojawły sę od chwl do
Proces narodzn śmerc Jeżel w ewnej oulacj nowe osobnk ojawają sę w sosób losowy, rzy czym gęstość zdarzeń na jednostkę czasu jest stała w czase wynos λ, oraz lczba osobnków n, które ojawły sę od chwl do
Zapis informacji, systemy pozycyjne 1. Literatura Jerzy Grębosz, Symfonia C++ standard. Harvey M. Deitl, Paul J. Deitl, Arkana C++. Programowanie.
 Zaps nformacj, systemy pozycyjne 1 Lteratura Jerzy Grębosz, Symfona C++ standard. Harvey M. Detl, Paul J. Detl, Arkana C++. Programowane. Zaps nformacj w komputerach Wszystke elementy danych przetwarzane
Zaps nformacj, systemy pozycyjne 1 Lteratura Jerzy Grębosz, Symfona C++ standard. Harvey M. Detl, Paul J. Detl, Arkana C++. Programowane. Zaps nformacj w komputerach Wszystke elementy danych przetwarzane
APROKSYMACJA QUASIJEDNOSTAJNA
 POZNAN UNIVE RSITY OF TE CHNOLOGY ACADE MIC JOURNALS No 73 Electrcal Engneerng 213 Jan PURCZYŃSKI* APROKSYMACJA QUASIJEDNOSTAJNA W pracy wykorzystano metodę aproksymacj średnokwadratowej welomanowej, przy
POZNAN UNIVE RSITY OF TE CHNOLOGY ACADE MIC JOURNALS No 73 Electrcal Engneerng 213 Jan PURCZYŃSKI* APROKSYMACJA QUASIJEDNOSTAJNA W pracy wykorzystano metodę aproksymacj średnokwadratowej welomanowej, przy
PROGNOZOWANIE SPRZEDAŻY Z ZASTOSOWANIEM ROZKŁADU GAMMA Z KOREKCJĄ ZE WZGLĘDU NA WAHANIA SEZONOWE
 STUDIA I PRACE WYDZIAŁU NAUK EKONOMICZNYCH I ZARZĄDZANIA NR 36 Krzysztof Dmytrów * Marusz Doszyń ** Unwersytet Szczecńsk PROGNOZOWANIE SPRZEDAŻY Z ZASTOSOWANIEM ROZKŁADU GAMMA Z KOREKCJĄ ZE WZGLĘDU NA
STUDIA I PRACE WYDZIAŁU NAUK EKONOMICZNYCH I ZARZĄDZANIA NR 36 Krzysztof Dmytrów * Marusz Doszyń ** Unwersytet Szczecńsk PROGNOZOWANIE SPRZEDAŻY Z ZASTOSOWANIEM ROZKŁADU GAMMA Z KOREKCJĄ ZE WZGLĘDU NA
STATYSTYCZNA ANALIZA WYNIKÓW POMIARÓW
 Zakład Metrolog Systemów Pomarowych P o l t e c h n k a P o z n ańska ul. Jana Pawła II 4 60-965 POZAŃ (budynek Centrum Mechatronk, Bomechank anonżyner) www.zmsp.mt.put.poznan.pl tel. +48 61 665 5 70 fax
Zakład Metrolog Systemów Pomarowych P o l t e c h n k a P o z n ańska ul. Jana Pawła II 4 60-965 POZAŃ (budynek Centrum Mechatronk, Bomechank anonżyner) www.zmsp.mt.put.poznan.pl tel. +48 61 665 5 70 fax
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Temat 13. Rozszerzalność cieplna i przewodnictwo cieplne ciał stałych.
 Temat 13. Rozszerzalność ceplna przewodnctwo ceplne cał stałych. W temace 8 wykazalśmy przy wykorzystanu warunków brzegowych orna-karmana, że wyraz lnowy w rozwnęcu energ potencjalnej w szereg potęgowy
Temat 13. Rozszerzalność ceplna przewodnctwo ceplne cał stałych. W temace 8 wykazalśmy przy wykorzystanu warunków brzegowych orna-karmana, że wyraz lnowy w rozwnęcu energ potencjalnej w szereg potęgowy
ANALIZA PORÓWNAWCZA WYNIKÓW UZYSKANYCH ZA POMOCĄ MIAR SYNTETYCZNYCH: M ORAZ PRZY ZASTOSOWANIU METODY UNITARYZACJI ZEROWANEJ
 METODY ILOŚCIOWE W BADANIACH EKONOMICZNYCH Tom XVI/3, 2015, str. 248 257 ANALIZA PORÓWNAWCZA WYNIKÓW UZYSKANYCH ZA POMOCĄ MIAR SYNTETYCZNYCH: M ORAZ PRZY ZASTOSOWANIU METODY UNITARYZACJI ZEROWANEJ Sławomr
METODY ILOŚCIOWE W BADANIACH EKONOMICZNYCH Tom XVI/3, 2015, str. 248 257 ANALIZA PORÓWNAWCZA WYNIKÓW UZYSKANYCH ZA POMOCĄ MIAR SYNTETYCZNYCH: M ORAZ PRZY ZASTOSOWANIU METODY UNITARYZACJI ZEROWANEJ Sławomr
Wykład 8. Silnik Stirlinga (R. Stirling, 1816)
 Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
MATEMATYKA POZIOM ROZSZERZONY Kryteria oceniania odpowiedzi. Arkusz A II. Strona 1 z 5
 MATEMATYKA POZIOM ROZSZERZONY Krytera ocenana odpowedz Arkusz A II Strona 1 z 5 Odpowedz Pytane 1 2 3 4 5 6 7 8 9 Odpowedź D C C A B 153 135 232 333 Zad. 10. (0-3) Dana jest funkcja postac. Korzystając
MATEMATYKA POZIOM ROZSZERZONY Krytera ocenana odpowedz Arkusz A II Strona 1 z 5 Odpowedz Pytane 1 2 3 4 5 6 7 8 9 Odpowedź D C C A B 153 135 232 333 Zad. 10. (0-3) Dana jest funkcja postac. Korzystając
Regulamin promocji upalne lato 2014 2.0
 upalne lato 2014 2.0 strona 1/5 Regulamn promocj upalne lato 2014 2.0 1. Organzatorem promocj upalne lato 2014 2.0, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa
upalne lato 2014 2.0 strona 1/5 Regulamn promocj upalne lato 2014 2.0 1. Organzatorem promocj upalne lato 2014 2.0, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa
dy dx stąd w przybliżeniu: y
 Przykłady do funkcj nelnowych funkcj Törnqusta Proszę sprawdzć uzasadnć, które z podanych zdań są prawdzwe, a które fałszywe: Przykład 1. Mesęczne wydatk na warzywa (y, w jednostkach penężnych, jp) w zależnośc
Przykłady do funkcj nelnowych funkcj Törnqusta Proszę sprawdzć uzasadnć, które z podanych zdań są prawdzwe, a które fałszywe: Przykład 1. Mesęczne wydatk na warzywa (y, w jednostkach penężnych, jp) w zależnośc
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 13 stycznia 2017 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości.
 Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości. Cel główny: przypomnienie i utrwalenie wiadomości dotyczących węglowodorów i pochodnych
Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości. Cel główny: przypomnienie i utrwalenie wiadomości dotyczących węglowodorów i pochodnych
Instrukcja do ćwiczeń laboratoryjnych
 UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracowna studencka Katedry Analzy Środowska Instrukcja do ćwczeń laboratoryjnych Ćwczene nr 2 WYZNACZANIE WSPÓŁCZYNNIKA PDZIAŁU WYBRANYCH ZANIECZYSZCZEŃ RGANICZNYCH ŚRDWISKA
UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracowna studencka Katedry Analzy Środowska Instrukcja do ćwczeń laboratoryjnych Ćwczene nr 2 WYZNACZANIE WSPÓŁCZYNNIKA PDZIAŁU WYBRANYCH ZANIECZYSZCZEŃ RGANICZNYCH ŚRDWISKA
XXX OLIMPIADA FIZYCZNA ETAP III Zadanie doświadczalne
 XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
SYMULACJA KOMPUTEROWA NAPRĘŻEŃ DYNAMICZNYCH WE WRĘGACH MASOWCA NA FALI NIEREGULARNEJ
 Jan JANKOWSKI *), Maran BOGDANIUK *),**) SYMULACJA KOMPUTEROWA NAPRĘŻEŃ DYNAMICZNYCH WE WRĘGACH MASOWCA NA FALI NIEREGULARNEJ W referace przedstawono równana ruchu statku w warunkach falowana morza oraz
Jan JANKOWSKI *), Maran BOGDANIUK *),**) SYMULACJA KOMPUTEROWA NAPRĘŻEŃ DYNAMICZNYCH WE WRĘGACH MASOWCA NA FALI NIEREGULARNEJ W referace przedstawono równana ruchu statku w warunkach falowana morza oraz
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie) Kod ucznia Suma punktów Witamy Cię na trzecim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie) Kod ucznia Suma punktów Witamy Cię na trzecim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Twórcza szkoła dla twórczego ucznia Projekt współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 SCENARIUSZ LEKCJI PRZEDMIOT: CHEMIA TEMAT: POWTÓRZENIE WIADOMOŚCI O WĘGLU I WĘGLOWODORACH AUTOR SCENARIUSZA: mgr Ewa Gryczman OPRACOWANIE ELEKTRONICZNO GRAFICZNE : mgr Beata Rusin TEMAT LEKCJI Powtórzenie
SCENARIUSZ LEKCJI PRZEDMIOT: CHEMIA TEMAT: POWTÓRZENIE WIADOMOŚCI O WĘGLU I WĘGLOWODORACH AUTOR SCENARIUSZA: mgr Ewa Gryczman OPRACOWANIE ELEKTRONICZNO GRAFICZNE : mgr Beata Rusin TEMAT LEKCJI Powtórzenie
Michal Strzeszewski Piotr Wereszczynski. poradnik. Norma PN-EN 12831. Nowa metoda. obliczania projektowego. obciazenia cieplnego
 Mchal Strzeszewsk Potr Wereszczynsk Norma PN-EN 12831 Nowa metoda oblczana projektowego. obcazena ceplnego poradnk Mchał Strzeszewsk Potr Wereszczyńsk Norma PN EN 12831 Nowa metoda oblczana projektowego
Mchal Strzeszewsk Potr Wereszczynsk Norma PN-EN 12831 Nowa metoda oblczana projektowego. obcazena ceplnego poradnk Mchał Strzeszewsk Potr Wereszczyńsk Norma PN EN 12831 Nowa metoda oblczana projektowego
Teoria niepewności pomiaru (Rachunek niepewności pomiaru) Rodzaje błędów pomiaru
 Pomary fzyczne - dokonywane tylko ze skończoną dokładnoścą. Powodem - nedoskonałość przyrządów pomarowych neprecyzyjność naszych zmysłów borących udzał w obserwacjach. Podawane samego tylko wynku pomaru
Pomary fzyczne - dokonywane tylko ze skończoną dokładnoścą. Powodem - nedoskonałość przyrządów pomarowych neprecyzyjność naszych zmysłów borących udzał w obserwacjach. Podawane samego tylko wynku pomaru
Wskaż grupy reakcji, do których można zaliczyć proces opisany w informacji wstępnej. A. I i III B. I i IV C. II i III D. II i IV
 Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
MECHANIKA 2 MOMENT BEZWŁADNOŚCI. Wykład Nr 10. Prowadzący: dr Krzysztof Polko
 MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
Procedura normalizacji
 Metody Badań w Geograf Społeczno Ekonomcznej Procedura normalzacj Budowane macerzy danych geografcznych mgr Marcn Semczuk Zakład Przedsęborczośc Gospodark Przestrzennej Instytut Geograf Unwersytet Pedagogczny
Metody Badań w Geograf Społeczno Ekonomcznej Procedura normalzacj Budowane macerzy danych geografcznych mgr Marcn Semczuk Zakład Przedsęborczośc Gospodark Przestrzennej Instytut Geograf Unwersytet Pedagogczny
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
odbarwia wodę bromową
 Zadanie 1. (0 1) W którym wierszu tabeli poprawnie scharakteryzowano wymienione węglowodory? Wybierz odpowiedź spośród podanych. Metan Eten Etyn A. jest gazem jest gazem jest cieczą B. w jego cząsteczce
Zadanie 1. (0 1) W którym wierszu tabeli poprawnie scharakteryzowano wymienione węglowodory? Wybierz odpowiedź spośród podanych. Metan Eten Etyn A. jest gazem jest gazem jest cieczą B. w jego cząsteczce
Regulamin promocji 14 wiosna
 promocja_14_wosna strona 1/5 Regulamn promocj 14 wosna 1. Organzatorem promocj 14 wosna, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa od 01 lutego 2014 do 30
promocja_14_wosna strona 1/5 Regulamn promocj 14 wosna 1. Organzatorem promocj 14 wosna, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa od 01 lutego 2014 do 30
POŁOŻENIA SYGNAŁÓW PROTONÓW POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA
 POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
Statystyka Opisowa 2014 część 2. Katarzyna Lubnauer
 Statystyka Opsowa 2014 część 2 Katarzyna Lubnauer Lteratura: 1. Statystyka w Zarządzanu Admr D. Aczel 2. Statystyka Opsowa od Podstaw Ewa Waslewska 3. Statystyka, Lucjan Kowalsk. 4. Statystyka opsowa,
Statystyka Opsowa 2014 część 2 Katarzyna Lubnauer Lteratura: 1. Statystyka w Zarządzanu Admr D. Aczel 2. Statystyka Opsowa od Podstaw Ewa Waslewska 3. Statystyka, Lucjan Kowalsk. 4. Statystyka opsowa,
Rozwiązywanie zadań optymalizacji w środowisku programu MATLAB
 Rozwązywane zadań optymalzacj w środowsku programu MATLAB Zagadnene optymalzacj polega na znajdowanu najlepszego, względem ustalonego kryterum, rozwązana należącego do zboru rozwązań dopuszczalnych. Standardowe
Rozwązywane zadań optymalzacj w środowsku programu MATLAB Zagadnene optymalzacj polega na znajdowanu najlepszego, względem ustalonego kryterum, rozwązana należącego do zboru rozwązań dopuszczalnych. Standardowe
Metody predykcji analiza regresji
 Metody predykcj analza regresj TPD 008/009 JERZY STEFANOWSKI Instytut Informatyk Poltechnka Poznańska Przebeg wykładu. Predykcja z wykorzystanem analzy regresj.. Przypomnene wadomośc z poprzednch przedmotów..
Metody predykcj analza regresj TPD 008/009 JERZY STEFANOWSKI Instytut Informatyk Poltechnka Poznańska Przebeg wykładu. Predykcja z wykorzystanem analzy regresj.. Przypomnene wadomośc z poprzednch przedmotów..
Pomiary parametrów akustycznych wnętrz.
 Pomary parametrów akustycznych wnętrz. Ocena obektywna wnętrz pod względem akustycznym dokonywana jest na podstawe wartośc następujących parametrów: czasu pogłosu, wczesnego czasu pogłosu ED, wskaźnków
Pomary parametrów akustycznych wnętrz. Ocena obektywna wnętrz pod względem akustycznym dokonywana jest na podstawe wartośc następujących parametrów: czasu pogłosu, wczesnego czasu pogłosu ED, wskaźnków
Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). C. alkiny D. areny
 Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
ANALIZA KORELACJI WYDATKÓW NA KULTURĘ Z BUDŻETU GMIN ORAZ WYKSZTAŁCENIA RADNYCH
 Potr Mchalsk Węzeł Centralny OŻK-SB 25.12.2013 rok ANALIZA KORELACJI WYDATKÓW NA KULTURĘ Z BUDŻETU GMIN ORAZ WYKSZTAŁCENIA RADNYCH Celem ponższej analzy jest odpowedź na pytane: czy wykształcene radnych
Potr Mchalsk Węzeł Centralny OŻK-SB 25.12.2013 rok ANALIZA KORELACJI WYDATKÓW NA KULTURĘ Z BUDŻETU GMIN ORAZ WYKSZTAŁCENIA RADNYCH Celem ponższej analzy jest odpowedź na pytane: czy wykształcene radnych
Stanisław Cichocki. Natalia Nehrebecka. Wykład 6
 Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Interpretacja parametrów przy zmennych objaśnających cągłych Semelastyczność 2. Zastosowane modelu potęgowego Model potęgowy 3. Zmenne cągłe za zmenne dyskretne
Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Interpretacja parametrów przy zmennych objaśnających cągłych Semelastyczność 2. Zastosowane modelu potęgowego Model potęgowy 3. Zmenne cągłe za zmenne dyskretne
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
LABORATORIUM PODSTAW ELEKTROTECHNIKI Badanie obwodów prądu sinusoidalnie zmiennego
 Ćwczene 1 Wydzał Geonżyner, Górnctwa Geolog ABORATORUM PODSTAW EEKTROTECHNK Badane obwodów prądu snusodalne zmennego Opracował: Grzegorz Wśnewsk Zagadnena do przygotowana Ops elementów RC zaslanych prądem
Ćwczene 1 Wydzał Geonżyner, Górnctwa Geolog ABORATORUM PODSTAW EEKTROTECHNK Badane obwodów prądu snusodalne zmennego Opracował: Grzegorz Wśnewsk Zagadnena do przygotowana Ops elementów RC zaslanych prądem
Wykład Turbina parowa kondensacyjna
 Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Portfele zawierające walor pozbawiony ryzyka. Elementy teorii rynku kapitałowego
 Portel nwestycyjny ćwczena Na podst. Wtold Jurek: Konstrukcja analza rozdzał 5 dr chał Konopczyńsk Portele zawerające walor pozbawony ryzyka. lementy teor rynku kaptałowego 1. Pożyczane penędzy amy dwa
Portel nwestycyjny ćwczena Na podst. Wtold Jurek: Konstrukcja analza rozdzał 5 dr chał Konopczyńsk Portele zawerające walor pozbawony ryzyka. lementy teor rynku kaptałowego 1. Pożyczane penędzy amy dwa
Regulamin promocji zimowa piętnastka
 zmowa pętnastka strona 1/5 Regulamn promocj zmowa pętnastka 1. Organzatorem promocj zmowa pętnastka, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa od 01 grudna
zmowa pętnastka strona 1/5 Regulamn promocj zmowa pętnastka 1. Organzatorem promocj zmowa pętnastka, zwanej dalej promocją, jest JPK Jarosław Paweł Krzymn, zwany dalej JPK. 2. Promocja trwa od 01 grudna
Zdzisław Głowacki. Zakres podstawowy i rozszerzony. Odpowiedzi i rozwiązania zadań. Rozdział 2. Strona Linia zadanie Jest Powinno być
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 2 Errata do drugiego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 52 Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 2 Errata do drugiego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 52 Zadanie
Węgiel i jego związki z wodorem
 Węgiel i jego związki z wodorem 1. Związki organiczne i nieorganiczne są to związki chemiczne, które w swoich cząsteczkach zawierają atomy węgla są to związki chemiczne, które w swoich cząsteczkach nie
Węgiel i jego związki z wodorem 1. Związki organiczne i nieorganiczne są to związki chemiczne, które w swoich cząsteczkach zawierają atomy węgla są to związki chemiczne, które w swoich cząsteczkach nie
ZWIĘKSZANIE POJEMNOŚCI ADSORBENTÓW WĘGLOWYCH W PROCESIE ADSORPCYJNEGO MAGAZYNOWANIA WODORU
 Węgel aktywny w ochrone środowska przemyśle (26) LESZEK CZEPIRSKI, BRONISŁAW BUCZEK Akadema Górnczo-Hutncza m. S. Staszca, Wydzał Palw Energ al. Mckewcza 3, 3-59 Kraków ZWIĘKSZANIE POJEMNOŚCI ADSORBENTÓW
Węgel aktywny w ochrone środowska przemyśle (26) LESZEK CZEPIRSKI, BRONISŁAW BUCZEK Akadema Górnczo-Hutncza m. S. Staszca, Wydzał Palw Energ al. Mckewcza 3, 3-59 Kraków ZWIĘKSZANIE POJEMNOŚCI ADSORBENTÓW
Laboratorium ochrony danych
 Laboratorum ochrony danych Ćwczene nr Temat ćwczena: Cała skończone rozszerzone Cel dydaktyczny: Opanowane programowej metody konstruowana cał skończonych rozszerzonych GF(pm), poznane ch własnośc oraz
Laboratorum ochrony danych Ćwczene nr Temat ćwczena: Cała skończone rozszerzone Cel dydaktyczny: Opanowane programowej metody konstruowana cał skończonych rozszerzonych GF(pm), poznane ch własnośc oraz
METODA UNITARYZACJI ZEROWANEJ Porównanie obiektów przy ocenie wielokryterialnej. Ranking obiektów.
 Opracowane: Dorota Mszczyńska METODA UNITARYZACJI ZEROWANEJ Porównane obektów przy ocene welokryteralnej. Rankng obektów. Porównane wybranych obektów (warantów decyzyjnych) ze względu na różne cechy (krytera)
Opracowane: Dorota Mszczyńska METODA UNITARYZACJI ZEROWANEJ Porównane obektów przy ocene welokryteralnej. Rankng obektów. Porównane wybranych obektów (warantów decyzyjnych) ze względu na różne cechy (krytera)
System Przeciwdziałania Powstawaniu Bezrobocia na Terenach Słabo Zurbanizowanych SPRAWOZDANIE Z BADAŃ Autor: Joanna Wójcik
 Opracowane w ramach projektu System Przecwdzałana Powstawanu Bezroboca na Terenach Słabo Zurbanzowanych ze środków Europejskego Funduszu Społecznego w ramach Incjatywy Wspólnotowej EQUAL PARTNERSTWO NA
Opracowane w ramach projektu System Przecwdzałana Powstawanu Bezroboca na Terenach Słabo Zurbanzowanych ze środków Europejskego Funduszu Społecznego w ramach Incjatywy Wspólnotowej EQUAL PARTNERSTWO NA
Zaawansowane metody numeryczne
 Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Stanisław Cichocki. Natalia Nehrebecka. Wykład 7
 Stansław Cchock Natala Nehrebecka Wykład 7 1 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy zmennych dyskretnych 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy
Stansław Cchock Natala Nehrebecka Wykład 7 1 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy zmennych dyskretnych 1. Zmenne cągłe a zmenne dyskretne 2. Interpretacja parametrów przy
Badania sondażowe. Braki danych Konstrukcja wag. Agnieszka Zięba. Zakład Badań Marketingowych Instytut Statystyki i Demografii Szkoła Główna Handlowa
 Badana sondażowe Brak danych Konstrukcja wag Agneszka Zęba Zakład Badań Marketngowych Instytut Statystyk Demograf Szkoła Główna Handlowa 1 Błędy braku odpowedz Całkowty brak odpowedz (UNIT nonresponse)
Badana sondażowe Brak danych Konstrukcja wag Agneszka Zęba Zakład Badań Marketngowych Instytut Statystyk Demograf Szkoła Główna Handlowa 1 Błędy braku odpowedz Całkowty brak odpowedz (UNIT nonresponse)
DIAGNOSTYKA WYMIENNIKÓW CIEPŁA Z UWIARYGODNIENIEM WYNIKÓW POMIARÓW EKPLOATACYJNYCH
 RYNEK CIEŁA 03 DIANOSYKA YMIENNIKÓ CIEŁA Z UIARYODNIENIEM YNIKÓ OMIARÓ EKLOAACYJNYCH Autorzy: rof. dr hab. nż. Henryk Rusnowsk Dr nż. Adam Mlejsk Mgr nż. Marcn ls Nałęczów, 6-8 paźdzernka 03 SĘ Elementam
RYNEK CIEŁA 03 DIANOSYKA YMIENNIKÓ CIEŁA Z UIARYODNIENIEM YNIKÓ OMIARÓ EKLOAACYJNYCH Autorzy: rof. dr hab. nż. Henryk Rusnowsk Dr nż. Adam Mlejsk Mgr nż. Marcn ls Nałęczów, 6-8 paźdzernka 03 SĘ Elementam
TRANZYSTOR BIPOLARNY CHARAKTERYSTYKI STATYCZNE
 POLITHNIKA RZSZOWSKA Katedra Podstaw lektronk Instrkcja Nr4 F 00/003 sem. letn TRANZYSTOR IPOLARNY HARAKTRYSTYKI STATYZN elem ćwczena jest pomar charakterystyk statycznych tranzystora bpolarnego npn lb
POLITHNIKA RZSZOWSKA Katedra Podstaw lektronk Instrkcja Nr4 F 00/003 sem. letn TRANZYSTOR IPOLARNY HARAKTRYSTYKI STATYZN elem ćwczena jest pomar charakterystyk statycznych tranzystora bpolarnego npn lb
