Aminy. Aminy 1 0 RNH 2 NH. Aminy 3 0 R 3
|
|
|
- Judyta Żukowska
- 7 lat temu
- Przeglądów:
Transkrypt
1 Aminy Aminy 1 0 R 2 Aminy 2 0 R 2 Aminy 3 0 R 3 C 3 C 3 C C 3 C 3 C 3 C 2 C 3 C 3 C 3 C 3 alkohol 3 o amina 1 o amina 3 o Czwartorzędowa sól amoniowa: R R R R X 1
2 Aminy alifatyczne ( wszystkie podstawniki węglowe na atomie azotu mają charakter alifatyczny) C 3 7 C 2 5 Aminy aromatyczne przynajmniej jeden z podstawników bezpośrednio związany z azotem jest aromatyczny C 2 5 C 3 7 C 2 5 2
3 azewnictwo: Aminy pierwszorzędowe (R 2 ) można zgodnie z nazewnictwem IUPAC, nazywać na kilka sposobów, w zależności od ich struktury. 1. Przyrostek amina dołączany jest do nazwy podstawnika alkilowego C 3 C 3 C 2 2 C 3 tert - butyloamina cykloheksyloamina 3
4 2. Przyrostek amina można dołączyć do nazwy związku macierzystego, wstawiając między obydwa człony literę o C 3 C 3 2 4,4-dimetylocykloheksanoamina 2 C 2 C 2 C 2 C 2 2 1,4-butanodiamina 4
5 Symetryczne aminy drugo-(r 2 ) i trzeciorzędowe (R 3 ) noszą nazwy utworzone przez dodanie przedrostka di- lub trido grupy alkilowej: C 3 C 3 C 3 difenyloamina trimetyloamina 5
6 Podstawione niesymetrycznie drugo- (RR ) i trzeciorzędowe aminy (RR R ) są określane jako -podstawione aminy pierwszorzędowe. Jako nazwę macierzystą wybiera się nazwę największej grupy alkilowej C 3 C 2 C 3 C 3,-dimetyloetyloamina C 3 C 2 C 3 -etylo--metylocykloheksyloamina 6
7 Aminy o więcej niż jednej grupie funkcyjnej noszą nazwę traktującą grupę 2 jako podstawnik aminowy przy związku macierzystym np.: C 2 C aminoetanol 2 C 3 C 2 CC kwas 2-aminobutanowy 2 C 3 CC 2 CC 3 4-amino-2-pentanon 7
8 Dopuszczone nazwy zwyczajowe: 2 2C3 2 anilina o-toluidyna C 3 8
9 2 m-toluidyna amina aromatyczna 1 o C 3 C 3 -metyloanilina amina aromatyczna 2 o C 2 2 benzyloamina amina alifatyczna 1 o 9
10 Ważność grup funkcyjnych w nazewnictwie: kwasy > bezwodniki > estry > halogenki acyli > amidy > nitryle > aldehydy > ketony > alkohole > fenole > aminy > etery > > alkeny > alkiny > halogenki, alkile 10
11 Aminy heterocykliczne pirydyna pirol chinolina imidazol indol pirymidyna puryna pirolidyna piperydyna 11
12 Właściwości fizyczne amin: Aminy o < C 5 podobnie jak alkohole są rozpuszczalne w 2 Aminy 1 0 i 2 0 tworzą wiązania wodorowe i są silne zasocjowane. W efekcie aminy wykazują wyższe temperatury wrzenia niż alkany o podobnej masie cząsteczkowej. 12
13 Aminy niskocząsteczkowe wykazują wyróżniającą ich woń zapach nieświeżych ryb. Putrescyna (1,4-butanodiamina) jedna z ptoamin (jady trupie), zawdzięcza swą nazwę procesom gnicia podczas, których się wydziela ( łac, putrescere gnić) Kadaweryna (1,5-pentanodiamina) jedna z ptoamin amina biogenna będąca produktem dekarboksylacji lizyny, 2 -(C 2 ) 4 -C(C)- 2 (lizyna) 2 -(C 2 ) C 2 Ma silny nieprzyjemny zapach rozkładających się zwłok i jest szkodliwa dla zdrowia (uszkadza układ krążenia) (łac. cadaver - trup, zwłoki). 13
14 Zasadowość Amin + A + A amina (zasada Lewisa) kwas sól Aminy są bardziej zasadowe niż alkohole, etery i woda. 14
15 Zasadowość Amin R 2 2 R [ R 3 ] [ ] K= [R2 ] [ 2 ] Kb = K[ 2 ] = [ R 3 ] [ ] [R 2 ] Zasadowość amin: R 2 > R 2 > 3 >> aminy aromatyczne ArR 2 > ArR > Ar 2 > Ar 2 > Ar 3 15
16 Zasadowość amin aromatycznych 2 Y Podstawniki oddające elektrony, takie jak C 3, - 2, -C 3, które zwiększają reaktywność pierścienia wobec substytucji elektrofilowej zwiększają również zasadowość aryloaminy. 2 Y Podstwaniki wyciągające elektrony, takie jak Cl, - 2, -C, które zmniejszają reaktywność pierścienia wobec substytucji elektrofilowej, zmniejszają również zasadowość aryloaminy. 16
17 trzymywanie amin Reakcje S 2 halogenków alkilu z amoniakiem otrzymuje się mieszaninę produktów. 3 R X + R 3 X a R 2 R 2 + R X R 2 2 X a R 2 R 2 R X + R 3 X a R 3 R 3 + R X R 4 X 17
18 trzymywanie amin Reakcja redukcji związków zawierających azot: RC 1. LiAl RC 2 2 RC 1. LiAl 4 RC C Fe, Cl C a / C
19 trzymywanie amin Reakcja aminowania redukcyjnego ketonów i aldehydów: w reakcji tej mogą być stosowane amoniak, aminy 1 o i 2 o (-) dając odpowiednio: aminy 1 o, 2 o i 3 o. 3 2 / kat 2 RCR' amina 1 o RCR' R" 2 2 / kat R" RCR' amina 2 o R" 2 2 / kat R" 2 RCR' amina 3 o 19
20 trzymywanie amin trzymywanie amin aromatycznych: redukcja nitrobenzenów Fe, Cl 2. a x Przegrupowanie ofmanna: RC 2 Br 2 a R 2 20
21 Reakcje amin 1. Reakcja alkilowania (synteza amin) : R 2 + R' X RR' 2 X a RR' 2. Reakcja acylowania C R' Cl R 2 pirydyna 2 C 3 CCl pirydyna R' C R C C 3 acetanilid 21
22 3. Reakcje z kwasem azotowym ( III ) a 2 + Cl + acl = ietrwały kation nitrozoniowy ma właściwości elektrofilowe i przyłącza się do aminy. Wynik reakcji zależy od rzędowości aminy, jej struktury ( czy jest to amina alifatyczna czy aromatyczna), oraz od warunków prowadzenia reakcji. 22
23 Aminy 1 o R 2 + R 2 -nitrozoamina - 2 R kation diazoniowy z anionem kwasu tworzy sól 23
24 Aminy alifatyczne 1 o Powstająca sól diazoniowa R 2+ X - jest nietrwała w warunkach reakcji < 5 o C R - 2 R W wyniku rozpadu soli diazoniowej powstaje karbokation, który może ulec przegrupowaniu, reakcji eliminacji lub podstawienia obecnymi w środowisku reakcji nukleofilami : wodą lub anionem kwasu. Powstaje mieszanina produktów, wydziela się 2. 24
25 Aminy aromatyczne 1 o a S 4, t < 5 o C 2 S 4 sól diazoniowa trwała w warunkach reakcji t< 5 o C 2 X a 2 t<5 o C 2 X 2 S 4 + u u 25
26 2 X + u u CuCl Cl 2 X CuBr Br reakcje Sandmeyera CuC C C 26
27 KI I 2 X 2, t BF 4 F 3 P 2 27
28 Reakcja sprzęgania diazoniowego Sole diazoniowe aromatyczne ulegają reakcji sprzęgania z zaktywowanymi pierścieniami aromatycznymi ( S E Ar ), dając barwne azozwiązki, Ar-=-Ar 2 + Y Y Y = lub R 2 28
29 CRMFR, grupa chromoforowa, układ chromoforowy Grupa atomów w cząsteczce związku organicznego absorbująca promieniowanie w zakresie światła widzialnego (powodująca zabarwienie związku) i nadfioletu. Zawiera wiązanie wielokrotne lub kilka wiązań w układzie sprzężonym. Typowymi chromoforami występującymi w barwnikach są układy chinoidowe (chinony), grupa azowa -=-, nitrozowa =, nitrowa 2, karbonylowa C=. Grupa auksochromowa podstawnik, który wzbogacając układ w dodatkowe pary elektronów powoduje przesunięcie pasma absorpcji w kierunku dłuższych fal (efekt batochromowy) (np.: -, - 2, -R 2, -C 3, -CC 3, -Br, -Cl) 29
30 oranż metylowy a 3 S (C 3 ) 2 czerwień Kongo 2 2 S 3 S 3 30
31 2 2 chryzoidyna pomarańczowy barwnik do papieru i skóry a 3 S a 2 C S 3 a E 102 Tartrazyna żółty barwnik napoje w proszku, esencje owocowe, miód sztuczny, musztarda Tartrazyna jest czynnikiem uwalniającym histaminę, dlatego po jej spożyciu astmatycy mogą odczuwać wzmożone objawy choroby ( grozi również poronieniem). U dzieci, w połączeniu z benzoesanami(e ) może powodować trudności w nauce, a nawet wystąpienie syndromu ADD. 31
32 a 3 S S 3 a E 110 żółcień pomarańczowa FCF (Sunset Yellow FCF) prawdopodobnie kancerogenna marmolady, żele, guma do żucia, powłoki tabletek 3 S C 3 C 3 S 3 E 129 Czerwień Allura AC (Allura Red AC) jest kancerogenna Pomimo że Unia Europejska dopuszcza jej użycie jako barwnika spożywczego, w Danii, Belgii, Szwajcarii, Francji i Szwecji jej stosowanie jest zakazane. 32
33 Aminy 2 o alifatyczne i aromatyczne w reakcji z kwasem azotowym (III) tworzą stosunkowo trwałe -nitrozoaminy. a 2 Cl Aminy 3 o alifatyczne nie reagują na zimno z kwasem azotowym (III) - aromatyczne dają p-nitrozoaminy R 2 a 2 R Cl 2 p-nitrozoamina 33
34 Alkaloidy Alkaloidy (arabskie: alkali - potaż i greckie: eidos -postać czyli "przyjmujący postać zasady") to związki pochodzenia roślinnego, zawierające układy heterocykliczne z co najmniej jednym zasadowym atomem azotu w pierścieniu. Ich biosynteza oparta jest o aminokwasy. Alkaloidy wykazują zwykle silne działanie fizjologiczne. 34
35 Alkaloidy chinolina C 3 Lek przeciwmalaryczny chinina C 3 Jest najstarszym lekiem przeciwarytmicznym chinidyna ba te alkaloidy są w stosunku do siebie diastereoizomerami, różnią się jedynie konfiguracją absolutną na dwóch atomach węgla : * łączącym ugrupowania chinolinowe i chinuklidynowe oraz na jeszcze jednym *. 35
36 Alkaloidy izochinolina x C 3 C 3 papaweryna C 3 C 3 Papaweryna ma silne działanie przeciwskurczowe, występuje w opium, ale nie ma działania narkotycznego. 36
37 Alkaloidy pirydyna x nikotyna nornikotyna azwa nikotyny pochodzi od nazwiska lekarza, Jeana icot, który w XVI wieku zalecał tytoń jako lek. 37
38 Alkaloidy x piperydyna lobelina Lobelina (też: lobelia) środek o działaniu wymiotnym oraz pobudzającym ośrodek oddechowy, także środek przeciwastmatyczny. Lobelina jest podawana palaczom gdyż działa wymiotnie tuż po zapaleniu papierosa. Piperyna - występuje w pieprzu czarnym (piper nigrum). piperyna 38
39 Alkaloidy tropan atropina kokaina Atropina występuje głównie w roślinach z rodziny psiankowatych, np. pokrzyku wilczej jagodzie (Atropa belladonna). Kokaina - jedna z najsilniej działających substancji pobudzających pochodzenia roślinnego. dznacza się bardzo dużym potencjałem uzależniającym. trzymywany z liści krasnodrzewu pospolitego (koki), który pierwotnie porastał tereny Andów. skopolamina Skopolamina, hioscyna - otrzymywana m.in. z liści bielunia kędzierzawy. Wykazuje słabsze działanie ośrodkowe od atropiny. 39
40 Alkaloidy puryna C 3 C 3 Kofeina, znana również jako teina gdy pochodzi z herbaty. Jest stosowana jako dodatek do wielu napojów takich jak coca-cola czy redbull. C 3 kofeina C 3 C 3 teobromina Działa silnie diuretycznie i spazmolitycznie. gólnie jej działanie jest zbliżone do kofeiny, ale dużo słabsze. Gorzka czekolada zawiera około 10 gramów teobrominy na kilogram, mleczna - około 5 gramów. Teobromina jest szkodliwa dla niektórych zwierząt, miedzy innymi dla psów i koni. Dla psa ważącego 25 kg zjedzenie dwóch tabliczek czekolady może okazać się śmiertelne. 40
41 Alkaloidy indol P C 2 C 2 (C 3 ) 2 Psylocybina -- psychoaktywny alkaloid obecny w grzybach halucynogennych, rytualny psychodelik stosowany przez Indian od 4 tysięcy lat. psylocybina C 3 C Johimbina - uzyskiwana z kory lub liści drzewa Yohimbe, rosnących w Kamerunie. johimbina 41
42 Alkaloidy C 3 C 3 C morfina C3 kodeina C3 C 3 C heroina C3 42
43 Alkaloidy 2 2-fenyloetyloamina β fenyloetyloamina fenyloetyloamina (PEA) fenetyloamina Endogenny alkaloid wytwarzany między innymi w organizmach ludzkich w stanach emocjonalnych określanych jako zakochanie C3 C 3 efedryna Efedryna (występuje między innymi w cisie) była stosowana od tysięcy lat w medycynie chińskiej (ma huang) w celu leczenia przeziębień i astmy. 43
44 Kapsaicyna alkaloid odpowiedzialny za ostry, piekący smak papryki chili, działa na receptory bólu (nocyceptory) oraz błonę śluzową. strość smaku mierzy się w skali Scoville a (SU -Scoville eat Units) czysta kapsaicyna to SU dla porównania klasyczny sos Tabasco ma SU 44
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
Slajd 1. Slajd 2. Aminy. trietyloamina. amoniak. chlorofil
 Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Aminy - budowa. R alkil Alkiloamina Amina alifatyczna. Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA III - RZĘDOWA AMINA II - RZĘDOWA
 Aminy Aminy - budowa R alkil Alkiloamina Amina alifatyczna Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA II - RZĘDOWA AMINA III - RZĘDOWA Aminy - budowa ALKILOAMINY PIRAMIDA TRYGONALNA ARYLOAMINY
Aminy Aminy - budowa R alkil Alkiloamina Amina alifatyczna Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA II - RZĘDOWA AMINA III - RZĘDOWA Aminy - budowa ALKILOAMINY PIRAMIDA TRYGONALNA ARYLOAMINY
AMINY. tytoń szlachetny. nikotyna. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania
 Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
AMINY I ICH POCHODNE
 AMIY I I PDE rganiczne pochodne amoniaku. 4/5 powietrza azot. W naturze: aminokwasy, peptydy, białka, alkaloidy (kokaina, nikotyna, morfina, meskalina ), neurotransmitery, stymulanty, kwasy nukleinowe
AMIY I I PDE rganiczne pochodne amoniaku. 4/5 powietrza azot. W naturze: aminokwasy, peptydy, białka, alkaloidy (kokaina, nikotyna, morfina, meskalina ), neurotransmitery, stymulanty, kwasy nukleinowe
amoniak amina 1 amina 2 amina 3
 AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego. ĆWICZENIE 6 i 7. Aminy i amidy kwasowe
 ĆWICZENIE 6 i 7 Aminy i amidy kwasowe Do amin zaliczamy związki organiczne, których wzór można wyprowadzić ze wzoru amoniaku przez podstawienie w nim atomu lub atomów wodoru grupą lub grupami alkilowymi
ĆWICZENIE 6 i 7 Aminy i amidy kwasowe Do amin zaliczamy związki organiczne, których wzór można wyprowadzić ze wzoru amoniaku przez podstawienie w nim atomu lub atomów wodoru grupą lub grupami alkilowymi
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Kilka wskazówek ułatwiających analizę widm w podczerwieni
 Kilka wskazówek ułatwiających analizę widm w podczerwieni Opracowanie wg dostępnej literatury spektroskopowej: Dr Alina T. Dubis e-mail: alina@uwb.edu.pl Instytut Chemii Uniwersytet w Białymstoku Al. J.
Kilka wskazówek ułatwiających analizę widm w podczerwieni Opracowanie wg dostępnej literatury spektroskopowej: Dr Alina T. Dubis e-mail: alina@uwb.edu.pl Instytut Chemii Uniwersytet w Białymstoku Al. J.
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
R 2 III-rzędowe R 1 N R 3
 ZWIĄZKI ZAWIERAJĄE AZT W GRUPA FUKYJY I. Wprowadzenie teoretyczne Ważniejsze związki organiczne zawierające azot w grupie funkcyjnej to aminy, aminokwasy, związki nitrowe oraz hydrazyna i jej pochodne.
ZWIĄZKI ZAWIERAJĄE AZT W GRUPA FUKYJY I. Wprowadzenie teoretyczne Ważniejsze związki organiczne zawierające azot w grupie funkcyjnej to aminy, aminokwasy, związki nitrowe oraz hydrazyna i jej pochodne.
Jak analizować widmo IR?
 Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
Węglowodory nomenklatura Pochodne chlorowcowe węglowodorów
 Węglowodory nomenklatura 1. Alkany: a) otrzymywanie metodą Wurtza, ze związków Gringarda, z halogenków alkilów, przez elektrolizę soli kwasów karboksylowych. b) Własności: halogenowanie, spalanie, piroliza,
Węglowodory nomenklatura 1. Alkany: a) otrzymywanie metodą Wurtza, ze związków Gringarda, z halogenków alkilów, przez elektrolizę soli kwasów karboksylowych. b) Własności: halogenowanie, spalanie, piroliza,
fenol ninhydryna difenyloamina kwas octowy Określ ph amin: n-butyloamina dietyloamina difenyloamina anilina N,N-dimetyloanilina
 REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna (0310-CH-S1-026) Nazwa wariantu modułu (opcjonalnie):
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Podział związków organicznych
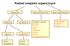 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
RJC A-B A + B. Slides 1 to 27
 Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Chemia organiczna. Związki zawierające azot. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
C H N O L B I O T E ORGANICZNA I A. Nomenklatura
 B T E L EMA G GAZA A omenklatura B T E L EMA G GAZA A Synteza AMY -rzędowe ' 2 2 2 ' 2 0 0 0 1 2 3 Typy amin -rzędowych w zależności od rzędowości atomu węgla związanego z grupą aminową METDY EDUKYJE
B T E L EMA G GAZA A omenklatura B T E L EMA G GAZA A Synteza AMY -rzędowe ' 2 2 2 ' 2 0 0 0 1 2 3 Typy amin -rzędowych w zależności od rzędowości atomu węgla związanego z grupą aminową METDY EDUKYJE
Widma UV charakterystyczne cechy ułatwiające określanie struktury pirydyny i pochodnych
 Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Kierunek i poziom studiów: Biotechnologia, pierwszy. Nazwa wariantu modułu (opcjonalnie): nie dotyczy
 Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka
 REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
Chemia organiczna. Związki zawierające azot. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 2
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
WĘGLOWODORY AROMATYCZNE
 WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
MIKROANALIZY WĘGLOWODORY. W1 Utlenianie węglowodorów nadmanganianem potasu w środowisku kwaśnym (w temp. pokojowej) RÓWNANIA REAKCJI: OBSERWACJE:
 MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
Zarys Chemii Organicznej
 Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Aminy pochodne amoniaku, w których
 A M I N Y Aminy pochodne amoniaku, w których jeden (aminy 1 o ), dwa (aminy 2 o ) lub trzy (aminy 3 o ) atomy wodoru zostały zastąpione resztami organicznymi (alifatycznymi bądź aromatycznymi). Przykłady
A M I N Y Aminy pochodne amoniaku, w których jeden (aminy 1 o ), dwa (aminy 2 o ) lub trzy (aminy 3 o ) atomy wodoru zostały zastąpione resztami organicznymi (alifatycznymi bądź aromatycznymi). Przykłady
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Identyfikacja płomieniowa tworzyw sztucznych Iloczyny rozpuszczalności trudno rozpuszczalnych związków w wodzie w temperaturze pokojowej
 Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych:
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Układy pięcioczłonowe z jednym heteroatomem
 WYKŁAD 7 Układy pięcioczłonowe z jednym heteroatomem Furan 1-Pirol Tiofen Benzofuran 1-Indol Benzo[b]tiofen Tetrahydrofuran Pirolidyna Tiolan 1 1. Muskaryna (I, muscarine) Alkaloid pochodzenia naturalnego
WYKŁAD 7 Układy pięcioczłonowe z jednym heteroatomem Furan 1-Pirol Tiofen Benzofuran 1-Indol Benzo[b]tiofen Tetrahydrofuran Pirolidyna Tiolan 1 1. Muskaryna (I, muscarine) Alkaloid pochodzenia naturalnego
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Ćwiczenie 4. Reakcja aminokwasów z ninhydryną. Opisz typy reakcji przebiegających w tym procesie i zaznacz ich miejsca przebiegu.
 azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
Węglowodory Aromatyczne
 Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Slajd 1. Etery i epoksydy. Slajd 2. Wprowadzenie. Wzór R-O-R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: CH 3 O CH 3 O CH 3
 Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Program wykładu Chemia Organiczna I
 Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
1. Napisz schematy reakcji otrzymywania z 1-bromo-2-fenyloetanu i z dowolnych innych reagentów następujących amin: 2-fenyloetyloaminy
 REPETYTORIUM A Z zakresu aminy alifatyczne i aromatyczne, związki heterocykliczne, związki karbopolicykliczne, węglowodany, aminokwasy i peptydy, terpeny, steroidy, lipidy 1. Napisz schematy reakcji otrzymywania
REPETYTORIUM A Z zakresu aminy alifatyczne i aromatyczne, związki heterocykliczne, związki karbopolicykliczne, węglowodany, aminokwasy i peptydy, terpeny, steroidy, lipidy 1. Napisz schematy reakcji otrzymywania
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII Instrukcja do ćwiczeń laboratoryjnych WŁAŚCIWOŚCI KWASOWOZASADOWE ZWIĄZKÓW ORGANICZNYCH; BADANIE ROZPUSZCZALNOŚCI
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII Instrukcja do ćwiczeń laboratoryjnych WŁAŚCIWOŚCI KWASOWOZASADOWE ZWIĄZKÓW ORGANICZNYCH; BADANIE ROZPUSZCZALNOŚCI
KARTA KURSU. Student posiada podstawową wiedzę z zakresu fizyki, matematyki i chemii nieorganicznej.
 Kierunek, stopień, tok studiów, rok akademicki, semestr Biologia, licencjat, studia stacjonarne, 2017/2018, II KARTA KURSU Nazwa Chemia organiczna I Nazwa w j. ang. Koordynator dr Waldemar Tejchman Zespół
Kierunek, stopień, tok studiów, rok akademicki, semestr Biologia, licencjat, studia stacjonarne, 2017/2018, II KARTA KURSU Nazwa Chemia organiczna I Nazwa w j. ang. Koordynator dr Waldemar Tejchman Zespół
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
S Y L A B U S P R Z E D M I O T U
 "Z A T W I E R D Z A M" Dziekan Wydziału Nowych Technologii i Chemii Dr hab. inż. Stanisław CUDZIŁO, prof. WAT Warszawa, dnia... S Y L A B U S P R Z E D M I O T U NAZWA PRZEDMIOTU:..CHEMIA ORGANICZNA SUBJECT
"Z A T W I E R D Z A M" Dziekan Wydziału Nowych Technologii i Chemii Dr hab. inż. Stanisław CUDZIŁO, prof. WAT Warszawa, dnia... S Y L A B U S P R Z E D M I O T U NAZWA PRZEDMIOTU:..CHEMIA ORGANICZNA SUBJECT
Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
 Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Oranż β-naftolu; C 16 H 10 N 2 Na 2 O 4 S, M = 372,32 g/mol; proszek lub
 Laboratorium Chemii rganicznej, Synteza oranżu β-naftolu, 1-5 Synteza oranżu β-naftolu Wydział Chemii UMCS w Lublinie 1. Właściwości fizyczne i chemiczne oranżu β-naftolu S 3 a ranż β-naftolu; C 16 10
Laboratorium Chemii rganicznej, Synteza oranżu β-naftolu, 1-5 Synteza oranżu β-naftolu Wydział Chemii UMCS w Lublinie 1. Właściwości fizyczne i chemiczne oranżu β-naftolu S 3 a ranż β-naftolu; C 16 10
Azotowe związki organiczne
 strona 1/1 Azotowe związki organiczne Krystyna Bogdanowicz-Szwed Procesy zachodzące w żywych organizmach są ściśle związane z chemią wielofunkcyjnych związków organicznych zawierających w swoich cząsteczkach
strona 1/1 Azotowe związki organiczne Krystyna Bogdanowicz-Szwed Procesy zachodzące w żywych organizmach są ściśle związane z chemią wielofunkcyjnych związków organicznych zawierających w swoich cząsteczkach
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
Lek od pomysłu do wdrożenia
 Lek od pomysłu do wdrożenia Lek od pomysłu do wdrożenia KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU
Lek od pomysłu do wdrożenia Lek od pomysłu do wdrożenia KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU KRÓTKA HISTORIA LEKU
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Barwniki azowe Dwuazotypia Aminy i kwas azotawy. A + Sole dwuazoniowe, Kwas azotawy Związki dwuazoaminowe Dwuazowanie.
 Barwniki azowe (1958 P. Griss: odkrycie reakcji diazowania i pierwszy barwnik: żółcień anilinowa) to barwniki syntetyczne zawierające jedną lub kilka grup azowych (jako chromofor). W zależności od ilości
Barwniki azowe (1958 P. Griss: odkrycie reakcji diazowania i pierwszy barwnik: żółcień anilinowa) to barwniki syntetyczne zawierające jedną lub kilka grup azowych (jako chromofor). W zależności od ilości
Właściwości chemiczne nukleozydów pirymidynowych i purynowych
 Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
CHEMIA ORGANICZNA. Chemia Organiczna. Zakład Chemii Organicznej. Prof. dr hab. Dorota Maciejewska. pierwszy. drugi. podstawowy TAK.
 CHEMIA ORGANICZNA 1. Metryczka Nazwa Wydziału: Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Program kształcenia Analityka medyczna, studia stacjonarne Rok akademicki: 2018/2019 Nazwa modułu/przedmiotu:
CHEMIA ORGANICZNA 1. Metryczka Nazwa Wydziału: Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Program kształcenia Analityka medyczna, studia stacjonarne Rok akademicki: 2018/2019 Nazwa modułu/przedmiotu:
Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, Spis treści
 Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, 2010 Spis treści Część II. Zagadnienia wybrane 25. Halogenki arylów. Substytucja nukleofilowa w pierścieniu
Chemia organiczna. T. 2 / Robert Thornton Morrison, Robert Neilson Boyd. wyd. 5, 3 dodr. Warszawa, 2010 Spis treści Część II. Zagadnienia wybrane 25. Halogenki arylów. Substytucja nukleofilowa w pierścieniu
BARWY W CHEMII Dr Emilia Obijalska Katedra Chemii Organicznej i Stosowanej UŁ
 BARWY W CHEMII Dr Emilia bijalska Katedra Chemii rganicznej i Stosowanej UŁ Akademia Ciekawej Chemii Czym jest światło? Wzrok człowieka reaguje na fale elektromagnetyczne w zakresie 380-760nm. Potocznie
BARWY W CHEMII Dr Emilia bijalska Katedra Chemii rganicznej i Stosowanej UŁ Akademia Ciekawej Chemii Czym jest światło? Wzrok człowieka reaguje na fale elektromagnetyczne w zakresie 380-760nm. Potocznie
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14):
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Organiczne związki azotu
 Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
