1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
|
|
|
- Kazimiera Pietrzak
- 6 lat temu
- Przeglądów:
Transkrypt
1 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych. eakcje te mają następujące zalety: A. Biegną często w łagodnych warunkach (temperatura wrzenia eteru dietylowego lub TF-u). B. trzymywanie związku magnezoorganicznego jest standardową, dobrze opracowaną reakcją, przebiegającą z wysokim stopniem przereagowania. C. Związek magnezoorganiczny otrzymuje się in situ w postaci roztworu (najczęściej eterowego), który zużywa się następnie do dalszej reakcji dwa następcze procesy biegną zatem w jednym naczyniu reakcyjnym. D. eakcja związku magnezoorganicznego jest energiczna, biegnie szybko i na ogół z wysoką wydajnością. E. bróbka mieszaniny poreakcyjnej jest standardowa i polega na oddzieleniu fazy eterowej od warstwy wodnej uzyskanej po hydrolizie, przepłukaniu wodą, suszeniu i destylacji bądź krystalizacji. eaktywność związków magnezoorganicznych wiąże się ze znaczną polaryzacją wiązania węgielmagnez, co prowadzi do wytworzenia bardzo reaktywnego centrum o charakterze karboanionu. Centrum to wykazuje powinowactwo do związków o charakterze elektrofilowym np. proton lub grupa karbonylowa. Niżej przedstawione są najważniejsze wykorzystywane w syntezie organicznej reakcje związków magnezoorganicznych: 1. EAKCJA ZE ZWIĄZKAMI PSIADAJĄCYMI KWASWY ATM WDU: Związki magnezoorganiczne rozkładane są przez większość związków posiadających kwasowy atom wodoru (nawet przez bardzo słabe kwasy np. amoniak lub aminy). W reakcji tej, z grupy zawartej w związku magnezoorganicznym tworzy się odpowiedni węglowodór. eakcja biegnie według następującego schematu: Przykłady: C 3 MgCl 2 C 4 Mg()Cl C 2 MgI C 2 5 C 3 C 2 5 MgI MgBr N 2 NMgBr C 3 CC 3 MgCl C 3 C 2 C 2 C C C 3 C 2 C 2 C C MgCl C 3 C 2 C 3
2 2. EAKCJE ADDYCJI D GUPY KABNYLWEJ Związki magnezoorganiczne reagują ze wszystkimi związkami posiadającymi grupę karbonylową. Grupa katbonylowa jest spolaryzowana, przy czym na karbonylowym atomie węgla występuje deficyt elektronów jest on zatem obiektem ataku grupy węglowej zawartej w związku magnezoorganicznym (posiadającej cząstkowy ładunek ujemny). eakcja biegnie według następującego schematu: W wyniku hydrolizy otrzymanego adduktu otrzymuje się z dobrą wydajnością związek organiczny stanowiący połączenie grupy węglowej zawartej w związku magnezoorganicznym oraz fragmentu zawierającego grupę karbonylową. W syntezie organicznej znajdują zastosowanie następujące reakcje: a) reakcja z aldehydami W reakcji z aldehydem mrówkowym (formaldehydem) tworzy się po hydrolizie alkohol pierwszorzędowy zawierający grupę ze związku magnezoorganicznego przedłużoną o jeden atom węgla. C C 2, C 2 W reakcji z pozostałymi aldehydami tworzą się po hydrolizie alkohole drugorzędowe. 1 C 2, Gdy grupy i 1 są różne, w reakcji tworzy się mieszanina racemiczna (z uwagi na jednakowe prawdopodobieństwo addycji z obu stron do płaskiej grupy karbonylowej) b) reakcja z ketonami C 1 2, W analogicznej reakcji związków magnezoorganicznych z ketonami otrzymuje się alkohole trzeciorzędowe. Podobnie jak w przypadku reakcji z aldehydami, gdy grupy, 1 i 2 są różne tworzy się racemiczny produkt.
3 c) reakcja z estrami eakcja ta przebiega dwuetapowo. Addukt powstający w wyniku reakcji estru z cząsteczką związku magnezoorganicznego eliminuje cząsteczkę alkoholanu tworząc keton. 1 C Keton Wspomniana reakcja eliminacji przebiega samorzutnie w środowisku reakcji (przed etapem hydrolizy) stąd możliwa jest następcza reakcja tworzącego się ketonu z cząsteczką związku magnezoorganicznego C 1 2, Sumarycznie przebiega zatem następująca reakcja: 2 1 C 2 Mg()X W reakcji tej można zatem otrzymywać trzeciorzędowe alkohole zawierające dwie takie same grupy przy atomie węgla związanym z grupą hydroksylową. d) reakcja z C2 Ditlenek węgla jako związek zawierający grupę karbonylową reaguje również energicznie ze związkami magnezoorganicznymi tworząc po hydrolizie kwas karboksylowy. eakcja ta pozwala na wbudowanie funkcji karboksylowej do cząsteczki związku organicznego. C C 2, C 3. EAKCJE ADDYCJI D NITYLI Grupa cyjanowa (-CN) jest także spolaryzowana co powoduje, iż ze związkami magnezoorganicznymi reaguje w sposób analogiczny jak grupa karboksylowa. W wyniku hydrolizy adduktu tworzą się ketony.
4 4. EAKCJE Z EPKSYDAMI Związki magnezoorganiczne reagują z oksiranem (tlenkiem etylenu) oraz jego pochodnymi (np. tlenkiem propylenu). eakcję tę można traktować jako w pewnej mierze analogiczną do reakjcji addycji do grupy karbonylowej. Wiązanie bananowe w oksiranie ma bowiem charakter pośredni między wiązaniem i wiązaniem i jest spolaryzowane w kierunku atomu tlenu (na atomie węgla istnieje zatem deficyt elektronowy). W reakcji następuje rozpad wiązania epoksydowego i tworzy się addukt, który po hydrolizie przechodzi w alkohol I-rzędowy zawierający układ węglowy (grupy ze związku magnezoorganicznego) przedłużony o dwa atomy węgla. W przypadku tlenku propylenu (2-metylooksiranu) addycja grupy - ze związku magnezoorganicznego następuje do mniej osłoniętego pierwszorzędowego atomu węgla. W wyniku tej reakcji otrzymuje się alkohol drugorzędowy. 5. EAKCJA Z ALGENPCDNYMI TYPU ALLILWEG I BENZYLWEG Związki magnezoorganiczne nie reagują na ogół z halogenopochodnymi typu alkilowego. Nie przebiegają zatem reakcje: MgBr X reakcja NIE PZEBIEGA gdy jest grupą alkilową nasyconą (Cn2n1) a tym bardziej winylową lub arylową eakcje takie są możliwe do przeprowadzenia jedynie w nielicznych przypadkach, np: a) jest grupą typu allilowego lub benzylowego (czyli reakcja przebiega z fluorowcopochodnymi zawierającymi bardzo ruchliwy atom halogenu).
5 b) jest grupą typu 1-alkinylowego zaś 1 jest grupą typu allilowego, benzylowego lub propargilowego (stosuje się sole miedzi I jako katalizatory): 6. EAKCJA Z SIAKĄ Związki magnezoorganiczne reagują z siarką tworząc tiole. - 2, S S S 7. EAKCJA Z TLENEM Związki magnezoorganiczne reagują również z tlenem, tworząc w początkowej fazie sól wodoronadtlenku, a następnie w reakcji z drugą cząsteczką związku magnezoorganicznego sól alkoholanu. Po hydrolizie mieszaniny reakcyjnej uzyskuje się alkohol. - 2, 2
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
Mg I. I Mg. Nie można ich jednak otrzymać ze związków, które posiadają grupy chlorowcowe w tak zwanym ustawieniu wicynalnym.
 nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Materiały dodatkowe związki karbonylowe
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podział związków organicznych
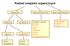 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
(57)1. Sposób wytwarzania nitrowych pochodnych
 RZECZPOSPOLITA POLSKA Urząd Patentowy Rzeczypospolitej Polskiej (12) OPIS PATENTOWY (19) PL (11) 185862 (21) Numer zgłoszenia: 319445 (22) Data zgłoszenia: 11.04.1997 (13) B1 (51) IntCl7 C07D 209/08 C07D
RZECZPOSPOLITA POLSKA Urząd Patentowy Rzeczypospolitej Polskiej (12) OPIS PATENTOWY (19) PL (11) 185862 (21) Numer zgłoszenia: 319445 (22) Data zgłoszenia: 11.04.1997 (13) B1 (51) IntCl7 C07D 209/08 C07D
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Zadanie 2. (2 pkt) Roztwór kwasu solnego o ph = 5 rozcieńczono 1000 krotnie wodą. Oblicz ph roztworu po rozcieńczeniu.
 Zadanie 1. (2 pkt) Oblicz, z jakiej objętości powietrza odmierzonego w temperaturze 285K i pod ciśnieniem 1029 hpa można usunąć tlen i azot dysponując 14 g magnezu. Magnez w tych warunkach tworzy tlenek
Zadanie 1. (2 pkt) Oblicz, z jakiej objętości powietrza odmierzonego w temperaturze 285K i pod ciśnieniem 1029 hpa można usunąć tlen i azot dysponując 14 g magnezu. Magnez w tych warunkach tworzy tlenek
Sprawdzian 3. CHEMIA. Przed próbną maturą (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 34. Imię i nazwisko ...
 CEMIA Przed próbną maturą 2017 Sprawdzian 3. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 34 Imię i nazwisko Liczba punktów Procent 2 Zadanie 1. (0 1) Związki krzemu z wodorem noszą
CEMIA Przed próbną maturą 2017 Sprawdzian 3. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 34 Imię i nazwisko Liczba punktów Procent 2 Zadanie 1. (0 1) Związki krzemu z wodorem noszą
Reakcje związków karbonylowych. Maria Burgieł R R C O. C O + Nu E C
 eakcje związków karbonylowych Maria Burgieł Związki zawierające grupę = nazywamy związkami karbonylowymi. Do najprostszych związków karbonylowych należą aldehydy, w których grupa = jest połączona z jedną
eakcje związków karbonylowych Maria Burgieł Związki zawierające grupę = nazywamy związkami karbonylowymi. Do najprostszych związków karbonylowych należą aldehydy, w których grupa = jest połączona z jedną
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Mechanizm dehydratacji alkoholi
 Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Właściwości chemiczne nukleozydów pirymidynowych i purynowych
 Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
WĘGLOWODORY. Uczeń: Przykłady wymagań nadobowiązkowych Uczeń:
 WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Materiały dodatkowe - węglowodory
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe - węglowodory Alkany 1. Hybrydyzacja atomu węgla Mnogość związków, jakie mogą powstać z udziałem atomów węgla,
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe - węglowodory Alkany 1. Hybrydyzacja atomu węgla Mnogość związków, jakie mogą powstać z udziałem atomów węgla,
Chemia węgla. Chemia Wydział SiMR, kierunek IPEiH I rok I stopnia studiów, semestr I. Chemia organiczna - podstawy
 hemia Wydział SiMR, kierunek IPEi I rok I stopnia studiów, semestr I dr inż. Leszek iedzicki hemia organiczna - podstawy hemia węgla hemia organiczna to chemia związków węgla. Inne pierwiastki, które zwykle
hemia Wydział SiMR, kierunek IPEi I rok I stopnia studiów, semestr I dr inż. Leszek iedzicki hemia organiczna - podstawy hemia węgla hemia organiczna to chemia związków węgla. Inne pierwiastki, które zwykle
ALKENY WĘGLOWODORY NIENASYCONE
 Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
 Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 2002 BYŁA DZISIAJ CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY ARKUSZ EGZAMINACYJNY I
 MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem
 Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna
 Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
CHEMIA KLASA Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
1. Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
Wpływ czynników utleniających na przebieg modelowego procesu utleniania cykloheksanolu i cykloheksanonu
 PLITENIKA ŚLĄSKA WYDZIAŁ EMIZNY KATEDRA TENLGII EMIZNEJ RGANIZNEJ I PETREMII INSTRUKJA D ĆWIZEŃ LABRATRYJNY: Wpływ czynników utleniających na przebieg modelowego procesu utleniania cykloheksanolu i cykloheksanonu
PLITENIKA ŚLĄSKA WYDZIAŁ EMIZNY KATEDRA TENLGII EMIZNEJ RGANIZNEJ I PETREMII INSTRUKJA D ĆWIZEŃ LABRATRYJNY: Wpływ czynników utleniających na przebieg modelowego procesu utleniania cykloheksanolu i cykloheksanonu
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/55/35935976.jpg) KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny)
 DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Test kompetencji z chemii do liceum. Grupa A.
 Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
CHARAKTERYSTYKA KARBOKSYLANÓW
 AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
b) Podaj liczbę moli chloru cząsteczkowego, która całkowicie przereaguje z jednym molem glinu.
 Informacja do zadań 1 i 2 Chlorek glinu otrzymuje się w reakcji glinu z chlorowodorem lub działając chlorem na glin. Związek ten tworzy kryształy, rozpuszczalne w wodzie zakwaszonej kwasem solnym. Z roztworów
Informacja do zadań 1 i 2 Chlorek glinu otrzymuje się w reakcji glinu z chlorowodorem lub działając chlorem na glin. Związek ten tworzy kryształy, rozpuszczalne w wodzie zakwaszonej kwasem solnym. Z roztworów
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Slajd 1. Alkohole i fenole. Cholesterol. Slajd 2. Budowa alkoholi. metanol. metanol. Grupą funkcyjną jest (OH) Tlen posiada hybrydyzacjęsp 3
 Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony
 CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY
 WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego. II Etap - 18 stycznia 2016
 XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego II Etap - 18 stycznia 2016 Nazwisko i imię ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
XIV Konkurs Chemiczny dla uczniów gimnazjum województwa świętokrzyskiego II Etap - 18 stycznia 2016 Nazwisko i imię ucznia: Liczba uzyskanych punktów: Drogi Uczniu, przeczytaj uważnie instrukcję i postaraj
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne:
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
I. Węgiel i jego związki z wodorem
 NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Spektrometria mas (1)
 pracował: Wojciech Augustyniak Spektrometria mas (1) Spektrometr masowy ma źródło jonów, które jonizuje próbkę Jony wędrują w polu elektromagnetycznym do detektora Metody jonizacji: - elektronowa (EI)
pracował: Wojciech Augustyniak Spektrometria mas (1) Spektrometr masowy ma źródło jonów, które jonizuje próbkę Jony wędrują w polu elektromagnetycznym do detektora Metody jonizacji: - elektronowa (EI)
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony.
 WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
Beata Mendak fakultety z chemii II tura PYTANIA Z KLASY PIERWSZEJ
 Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Zadanie: 2 (4 pkt) Napisz, uzgodnij i opisz równania reakcji, które zaszły w probówkach:
 Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze:
 Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze: Mentol w wyniku reakcji utleniania roztworem K 2 Cr 2 O 7 w środowisku kwaśnym daje związek należący do ketonów cyklicznych.
Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze: Mentol w wyniku reakcji utleniania roztworem K 2 Cr 2 O 7 w środowisku kwaśnym daje związek należący do ketonów cyklicznych.
Zadanie: 1 (1 pkt) Czy piorąc w wodzie miękkiej i twardej zużywa się jednakowe ilości mydła?
 Zadanie: 1 (1 pkt) Czy piorąc w wodzie miękkiej i twardej zużywa się jednakowe ilości mydła? Zadanie: 2 (1 pkt) Woda twarda powoduje tworzenie się kamienia kotłowego. Uzasadnij, pisząc odpowiednie równania
Zadanie: 1 (1 pkt) Czy piorąc w wodzie miękkiej i twardej zużywa się jednakowe ilości mydła? Zadanie: 2 (1 pkt) Woda twarda powoduje tworzenie się kamienia kotłowego. Uzasadnij, pisząc odpowiednie równania
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO kod Uzyskane punkty..... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII... DLA UCZNIÓW GIMNAZJÓW - rok szkolny 2011/2012 eliminacje wojewódzkie
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
Szanowne koleżanki i koledzy nauczyciele chemii!
 Szanowne koleżanki i koledzy nauczyciele chemii! Chciałabym podzielić się z Wami moimi spostrzeżeniami dotyczącymi poziomu wiedzy z chemii uczniów rozpoczynających naukę w Liceum Ogólnokształcącym. Co
Szanowne koleżanki i koledzy nauczyciele chemii! Chciałabym podzielić się z Wami moimi spostrzeżeniami dotyczącymi poziomu wiedzy z chemii uczniów rozpoczynających naukę w Liceum Ogólnokształcącym. Co
PRÓBNY II ETAP OLIMPIADY CHEMICZNEJ. Gimnazjum i Liceum Akademickie w Toruniu. Toruń, 9.01.2013
 PRÓBNY II ETAP OLIMPIADY CHEMICZNEJ Gimnazjum i Liceum Akademickie w Toruniu Toruń, 9.01.2013 ZADANIE 1 Synteza fragmentu pewnego sterydu i reakcja annulacji Robinsona. W typowej kondensacji aldolowej
PRÓBNY II ETAP OLIMPIADY CHEMICZNEJ Gimnazjum i Liceum Akademickie w Toruniu Toruń, 9.01.2013 ZADANIE 1 Synteza fragmentu pewnego sterydu i reakcja annulacji Robinsona. W typowej kondensacji aldolowej
Zad. 1. Br 2 + Zad. 2
 Zad. 1 ajszybciej, już bez dostępu światła, reaguje styren obecność winylowego wiązania podwójnego czyni go podatnym na reakcję addycji 2 (probówka 1). Etylobenzen i toluen ulegają reakcji wolnorodnikowej
Zad. 1 ajszybciej, już bez dostępu światła, reaguje styren obecność winylowego wiązania podwójnego czyni go podatnym na reakcję addycji 2 (probówka 1). Etylobenzen i toluen ulegają reakcji wolnorodnikowej
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Budowa przestrzenna alkanów
 Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
Różnorodny świat izomerów powtórzenie wiadomości przed maturą
 Różnorodny świat izomerów powtórzenie wiadomości przed maturą Maria Kluz Klasa III, profil biologiczno-chemiczny i matematyczno-chemiczny 1 godzina lekcyjna, praca w grupie 16-osobowej. Cele edukacyjne:
Różnorodny świat izomerów powtórzenie wiadomości przed maturą Maria Kluz Klasa III, profil biologiczno-chemiczny i matematyczno-chemiczny 1 godzina lekcyjna, praca w grupie 16-osobowej. Cele edukacyjne:
Sprawdzian 1. CHEMIA. Przed próbną maturą. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 32. Imię i nazwisko ...
 CHEMIA Przed próbną maturą Sprawdzian 1. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 32 Imię i nazwisko Liczba punktów Procent 2 Zadanie 1. Cząsteczka pewnej substancji chemicznej
CHEMIA Przed próbną maturą Sprawdzian 1. (poziom rozszerzony) Czas pracy: 90 minut Maksymalna liczba punktów: 32 Imię i nazwisko Liczba punktów Procent 2 Zadanie 1. Cząsteczka pewnej substancji chemicznej
Materiały dodatkowe alkohole, fenole, etery
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1.
 1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
EGZAMIN MATURALNY Z CHEMII
 Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO MCH-W1D1P-021 EGZAMIN MATURALNY Z CHEMII Instrukcja dla zdającego Czas pracy 90 minut 1. Proszę sprawdzić, czy arkusz
Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO MCH-W1D1P-021 EGZAMIN MATURALNY Z CHEMII Instrukcja dla zdającego Czas pracy 90 minut 1. Proszę sprawdzić, czy arkusz
Regulamin Przedmiotowy. XII Wojewódzkiego Konkursu Chemicznego. dla uczniów szkół gimnazjalnych województwa świętokrzyskiego
 Regulamin Przedmiotowy XII Wojewódzkiego Konkursu Chemicznego dla uczniów szkół gimnazjalnych województwa świętokrzyskiego w roku szkolnym 2014/ 2015 I. Informacje ogólne 1. Niniejszy Regulamin określa
Regulamin Przedmiotowy XII Wojewódzkiego Konkursu Chemicznego dla uczniów szkół gimnazjalnych województwa świętokrzyskiego w roku szkolnym 2014/ 2015 I. Informacje ogólne 1. Niniejszy Regulamin określa
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Spis treści Podstawowe dane Podział alkoholi alifatycznych Nazewnictwo systematyczne alkoholi Izomeria alkoholi Alkohole nasycone monohydroksylowe
 Spis treści Podstawowe dane Podział alkoholi alifatycznych Nazewnictwo systematyczne alkoholi Izomeria alkoholi Alkohole nasycone monohydroksylowe Właściwości fizyczne Otrzymywanie Przemysłowe metody otrzymywania
Spis treści Podstawowe dane Podział alkoholi alifatycznych Nazewnictwo systematyczne alkoholi Izomeria alkoholi Alkohole nasycone monohydroksylowe Właściwości fizyczne Otrzymywanie Przemysłowe metody otrzymywania
