HCOOH kwas metanowy ( mrówkowy ) CH 3. COOH kwas etanowy ( octowy ) CH 2
|
|
|
- Jolanta Urbaniak
- 7 lat temu
- Przeglądów:
Transkrypt
1 Kwasy karboksylowe, Ar Nazewnictwo: Kwasy, które są pochodnymi alkanów o otwartych łańcuchach, są nazywane w sposób systematyczny przez dodanie nazwy kwas i dodanie końcówki owy do alkanu - kwas alkanowy kwas metanowy ( mrówkowy ) 3 kwas etanowy ( octowy ) 3 2 kwas propanowy ( propionowy ) kwas butanowy ( masłowy ) 2 kwas propenowy ( akrylowy ) 2 3 kwas 2-metylopropenowy ( metakrylowy ) 2 kwas fenyloetanowy ( fenylooctowy ) 1
2 Kwasy aromatyczne Ar mają końcówkę -esowy kwas benzoesowy kwas 1-naftoesowy kwas 2-naftoesowy 2
3 azwę kwasu można też utworzyć wyłączając grupę karboksylową tedy nazwa będzie brzmiała kwas alkanokarboksylowy kwas pentanowy kwas butanokarboksylowy kwas cykloheksanokarboksylowy kwas benzenokarboksylowy kwas benzoesowy 3
4 Kwasy dikarboksylowe 2 kwas etanodiowy kwas propanodiowy (szczawiowy) (malonowy) 2 2 kwas butanodiowy (bursztynowy) 4
5 Kwasy dikarboksylowe kwas ftalowy kwas tereftalowy kwas 1,4-benzenodikarboksylowy 5
6 ydroksykwasy 2 3 kwas glikolowy kwas hydroksyoctowy kwas mlekowy kwas 2-hydroksypropanowy () 2 2 kwas jabłkowy kwas 2-hydroksybutanodiowy () () kwas winowy 6
7 ydroksykwasy 2 2 kwas cytrynowy kwas 2-hydroksy-1,2,3-propanotrikarboksylowy kwas 2-hydroksybenzoesowy kwas salicylowy 7
8 Ketokwasy 3 kwas pirogronowy kwas 2-oksopropanowy 3 2 kwas acetylooctowy kwas 3-oksobutanowy 8
9 Właściwości fizyczne kwasów karboksylowych 9
10 Kwas Struktura Temp. topn. Temp. wrz. [ o ] [ o ] mrówkowy 8,4 100,7 octowy 3 16,6 117,9 propanowy ,8 141 benzoesowy ,
11 trzymywanie kwasów karboksylowych 1. Utlenianie 1 o alkoholi lub aldehydów 2 r 3 2 S 4 AgN 3 N 4 2. Utlenianie alkilobenzenów 2 3 KMn 4 11
12 3. ydroliza nitryli 2 N 3 t 2 4. Karboksylowanie związków Grignarda reakcja addycji odczynnika Grignarda do 2 MgX / + 2 Br NaN 2 N 3 t 2 Mg eter 2 MgBr /
13 eakcje kwasów karboksylowych Właściwości kwasowe oddysocjowanie protonu edukcja 13
14 Substytucja nukleofilowa grupy acylowej S N Ac Y Substytucja w położeniu α X 14
15 Kwasowość grupy karboksylowej K = [ ] [ 3 ] [] [ 2 ] K a = K [ 2 ] = [ ] [ 3 ] [] Dla większości kwasów karboksylowych K a ~ 10 5 K a (l) > K a ( 3 ) > K a (Ph) > K a ( 2 5 ) 15
16 - 1/2-1/2 o 1,20 A o 1,34 A o 1,27 A Moc kwasu karboksylowego zależy od tego, w jakim stopniu stabilizowany jest anion karboksylanowy. 16
17 Podstawniki elektrodonorowe (jak grupy alkilowe) poprzez dostarczanie dodatkowego ładunku destabilizują anion karboksylanowy, dysocjacja zachodzi w mniejszym stopniu, a więc kwas jest słabszy. 2 K () > K ( 3 ) > K ( 2 5 ) > K (
18 Podstawniki elektronoakceptorowe (jak np. halogenki) przejmują na siebie część ładunku ujemnego i tym samym przyczyniają się do większej stabilizacji anionu karboksylanowego, a więc kwas jest mocniejszy. 2 l > 3 K (l 3 ) > K (l 2 ) > K ( 2 l) K ( 2 F) > K ( 2 l) > K ( 2 Br) 3 2 l > 3 2 > x l l 18
19 Kwasowość kwasów dikarboksylowych ( 2 ) n ( 2 ) n + K 1 = [anion I] [ ] [kwas] kwas anion I ( 2 ) n anion I ( 2 ) n + K 2 = anion II [ anion II ] [ ] [ anion I ] K 1 > K 2 19
20 edukcja kwasów karboksylowych 1. LiAl 4, TF B 3, TF Nie ulegają redukcji pod wpływem NaB 4 20
21 Substytucja w pozycji α 1. l 2, Pl l 1. Br 2, PBr Br 21
22 Substytucja nukleofilowa grupy acylowej S N Ac Sl 2 l chlorek kwasowy ' ' ester Ο bezwodnik N 2 amid 22
23 Pochodne kwasów karboksylowych: Y Y = l, Br, I N 2 halogenki kwasowe bezwodniki estry amidy 1 o 23
24 Substytucja nukleofilowa grupy acylowej - mechanizm Y + Nu Y Nu Nu + Y 24
25 Substytucja nukleofilowa grupy acylowej eaktywność pochodnych kwasowych: halogenki kwasowe > bezwodniki kwasowe > estry > amidy Wzajemne przemiany pochodnych kwasów karboksylowych: halogenek kwasowy bezwodnik kwasowy ester amid W naturze nie występują chlorki kwasowe i bezwodniki są zbyt reaktywne. 25
26 alogenki kwasowe Nazewnictwo: 1. Podając rodzaj atomu halogenku i nazwę kwasu macierzystego halogenek kwasu karboksylowego np. chlorek kwasu octowego bromek kwasu propanowego 3 l 3 2 Br 26
27 2. Jako halogenek acylu: l chlorek kwasu mrówkowego chlorek metanoilu (formylu) 3 Br bromek kwasu octowego bromek etanoilu (acetylu) 6 5 l chlorek kwasu benzoesowego chlorek benzoilu 27
28 alogenki kwasowe trzymywanie: Sl 2 l PBr 3 Br 28
29 eakcje halogenków kwasowych 1. ydroliza - S N Ac l 2 2. Alkoholiza - S N Ac l ' pirydyna ' 29
30 3. Aminoliza - reakcja z amoniakiem lub aminą 1 o i 2 o -S N Ac l 2N 3 N 2 + N 4 l l 2 'N 2 + 'N N' 3 l l 2 ' 2 N N' 2 + ' 2 N 2 l 30
31 4. edukcja - S N Ac l 1. LiAl eakcja z odczynnikiem Grignarda - S N Ac l 1. 2'MgX ' ' 6. Acylowanie Friedel a - raftsa l All 3 31
32 Bezwodniki kwasowe Nazewnictwo: 1. Dodając słowo bezwodnik do nazwy kwasu np. bezwodnik kwasu pentanowego bezwodnik kwasu mrówkowego 2. Zastępując słowo kwas słowem bezwodnik np. bezwodnik octowy 3 3 bezwodnik mrówkowo - octowy 3 32
33 Bezwodniki kwasowe Niektóre kwasy dikarboksylowe tworzą bezwodniki cykliczne: kwas ftalowy bezwodnik ftalowy kwas bursztynowy bezwodnik bursztynowy 33
34 Bezwodniki kwasowe - otrzymywanie 1. Sól kwasu + chlorek kwasowy Na + l Bezwodniki cykliczne przez ogrzewanie kwasów 230 o 34
35 eakcje bezwodników kwasowych 1. ydroliza - S N Ac Alkoholiza - S N Ac ' ' + ester kwas 3. Aminoliza - reakcja z amoniakiem lub aminą 1 o i 2 o -S N Ac N 3 N 2 + amid kwas 35
36 4. edukcja - S N Ac 1. LiAl eakcja Friedel a - raftsa () 2 All 3 36
37 Estry Nazewnictwo 1. Dla estrów kwasów alkanowych część kwasową określa się dodając do nazwy alkanu końcówkę ian i podając dalej nazwę podstawnika alkoholowego w dopełniaczu alkanian alkilu propanian etylu 37
38 2. Dla kwasów aromatycznych stosuje się końcówkę -esan 3 benzoesan metylu Estry kwasu ftalowego nazywamy ftalanami ftalan dietylu 38
39 3 3 etanian metylu octan metylu butanian etylu maślan etylu 3 3 metanian izopropylu mrówczan izopropylu 3 m-nitrobenzoesan metylu N 2 39
40 trzymywanie estrów 1. eakcja bezpośredniej estryfikacji z kwasu i alkoholu (tylko w środowisku kwaśnym) ' ' 2. z soli kwasu i halogenku alkilu ( tylko dla X 1 o ) 1. Na 2. 'X ' 'X tylko 1 o 40
41 3. z chlorków kwasowych l ' pirydyna ' 4. z bezwodników kwas salicylowy bezwodnik octowy kwas acetylosalicylowy aspiryna 41
42 Mechanizm estryfikacji + + ' ' ' - 2 ' ' ' - ' 42
43 Dowodem na powyższy mechanizm była reakcja estryfikacji przeprowadzona ze znaczonym tlenem w alkoholu
44 eakcje estrów 1. ydroliza kwaśna reakcja odwracalna ' 2 + ' Mechanizm jest odwrotnością reakcji estryfikacji 44
45 45 ' + ' ' ' + ' ' ' -' -
46 eakcje estrów 2. ydroliza zasadowa reakcja nieodwracalna - S N Ac δ δ+ + ' ' + ' + ' + ' mocniejszy kwas słabszy kwas 46
47 3. Transestryfikacja eakcje estrów ' " " + ' ' " Na " + ' Na 4. Aminoliza reakcja z amoniakiem lub aminą 1 o i 2 o ' N 3 N 2 + ' 47
48 eakcje estrów 5. eakcja z odczynnikiem Grignarda ' 1. 2"MgX 2. 2 " " + ' 6. edukcja ' 1. LiAl ' 48
49 Amidy N 2 N' N' 2 amid 1 o amid 2 o amid 3 o 49
50 N 2 amid 1 o Nazewnictwo 1. Dodając do nazwy alkanu końcówkę -amid - alkanoamid 3 2 N 2 2. amid kwasu... propanoamid 3 N 2 N 2 amid kwasu octowego acetamid amid kwasu benzoesowego benzamid 50
51 N' N' 2 Nazwy podstawionych amidów ( 2 o i 3 o ) poprzedza się podaniem podstawników grupy amidowej z lokantem N N( 3 ) 2 N,N-dimetyloformamid DMF 51
52 Amidy - otrzymywanie 1. eakcja chlorków kwasowych z amoniakiem - amidy 1 o lub aminami 1 o i 2 o -amidy 2 o i 3 o 2. eakcja bezwodników eakcja estrów - 4. ydroliza nitryli - amidy 1 o N 2 N 2 N 2 N 2 52
53 5. dwodnienie (dehydratacja) soli amonowych N 3 N 4 sól amonowa P 2 5 N 2 53
54 Amidy - reakcje 1. ydroliza w środowisku kwaśnym N N 4 2. ydroliza w środowisku zasadowym N 2 3. edukcja 2 + N 3 N 2 1. LiAl 4 2 N
55 4. Przegrupowanie ofmanna N 2 Br 2 Na N 2 5. dwodnienie (dehydratacja) N 2 Pl 3-2 N 55
56 Amidy zasadowość azotu Azot w amidach nie wykazuje właściwości zasadowych. N 2 N 2 Amidy protonowane są na tlenie: N 2 N 2 56
57 Nitryle N Nazewnictwo 1. Do nazwy alkanu (włączając w to atom węgla grupy N) dodaje się końcówkę nitryl 3 N etanonitryl N butanonitryl 57
58 2. Grupa N jest traktowana jako podstawnik alkanu i określana słowem cyjanek. Wtedy w nazwie łańcucha węglowego pomija się atom węgla grupy N. 3 N cyjanek metylu ; etanonitryl; acetonitryl N cyjanek fenylu; benzonitryl N cyjanek propylu; butanonitryl 58
59 Nitryle N - otrzymywanie 1. W reakcjach podstawienia nukleofilowego S N z halogenków alkilowych NaN 2 X 2 N 2. dwodnienie amidów 1 o lub oksymów aldehydów N 2 Pl 3-2 N N P N 59
60 Nitryle - reakcje Nitryle są bardzo użytecznymi odczynnikami chemicznymi. Grupa N stanowi równoważnik grupy karboksylowej, ponieważłatwo może być przekształcona w nią lub jej pochodną. 1. ydroliza N 2 N 2 2 N 2 N N 3 60
61 2. Alkoholiza N ' N 2 ' karbaminian 2 ester ' 3. edukcja 1. LiAl 4 N 2 N eakcja z odczynnikiem Grignarda N 1. 'MgX 2. 2 N MgX ' 2 ' 61
62 4. Aminoliza N N 3 N 2 N 2 amidyna N 'N 2 N' N 2 N-podstawiona amidyna 62
63 ydroksykwasy - reakcje γ - hydroksy oraz δ - hydroksykwasy bardzo łatwo ulegają wewnątrzcząsteczkowej reakcji estryfikacji, tworząc cykliczne estry, zwane laktonami lakton δ -hydroksykwas Ο lakton γ hydroksykwas 63
64 Kumaryna - o przyjemnym zapachu świeżego siana. Występuje w turówce wonnej gatunku trawy nazywanej potocznie żubrówką stosowaną jako przyprawa do wódki δ -hydroksykwas β γ α δ δ -lakton kwas cynamonowy 64
65 β hydroksykwasy łatwo eliminują cząsteczkę wody, tworząc kwasy nienasycone (α,β-nienasycone) 65
66 α- hydroksykwasy tworzą charakterystyczne podwójne laktony - laktydy 2 α - hydroksykwas laktyd 66
67 Polilaktyd (poli(kwas mlekowy), PLA z ang. polylactic acid, polylactide) - w pełni biodegradowalny polimer. PLA otrzymuje się w wyniku polimeryzacji z otwarciem pierścienia laktydu: n Polilaktyd jest używany głównie dla celów biomedycznych, m.in. do produkcji implantów dentystycznych i resorbowalnych nici chirurgicznych. 67
68 γ i δ - aminokwasy łatwo ulegają reakcji cyklizacji dając wewnętrzne amidy zwane laktamami 2 N - 2 N laktam Imidy podwójne amidy kwasów dikarboksylowych N imid kwasy ftalowego ftalimid N N imid kwasu butanodiowego sukcynimid 68
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
KWASY KARBOKSYLOWE i ich pochodne (by Aleksandra Kołodziejczyk, UG)
 KWASY KABKSYLWE i ich pochodne (by Aleksandra Kołodziejczyk, UG) metanowy (mrówkowy) 3 etanowy (octowy) 3 2 propanowy (propionowy) 3 2 2 butanowy (masłowy) 3 ( 2 ) 3 (walerianowy Br l kwas 2-hydroksybenzoesowy
KWASY KABKSYLWE i ich pochodne (by Aleksandra Kołodziejczyk, UG) metanowy (mrówkowy) 3 etanowy (octowy) 3 2 propanowy (propionowy) 3 2 2 butanowy (masłowy) 3 ( 2 ) 3 (walerianowy Br l kwas 2-hydroksybenzoesowy
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Pochodne kwasów karboksylowych. Krystyna Dzierzbicka
 Pochodne kwasów karboksylowych Krystyna Dzierzbicka halogenki kwasowe X X = l, Br, I bezwodniki kwasowe ' estry ' amidy N 2 sole nitryle N Nazwy grup acylowych 3 3 2 acyl metanoil formyl etanoil acetyl
Pochodne kwasów karboksylowych Krystyna Dzierzbicka halogenki kwasowe X X = l, Br, I bezwodniki kwasowe ' estry ' amidy N 2 sole nitryle N Nazwy grup acylowych 3 3 2 acyl metanoil formyl etanoil acetyl
KWASY KARBOKSYLOWE. Krystyna Dzierzbicka
 KWASY KARBKSYLWE Krystyna Dzierzbicka Kwasy karboksylowe są związkami organicznymi zawierającymi grupę karboksylową - zbudowaną z grupy karbonylowej () i hydroksylowej (). R (Ar) karboksylowy Możemy je
KWASY KARBKSYLWE Krystyna Dzierzbicka Kwasy karboksylowe są związkami organicznymi zawierającymi grupę karboksylową - zbudowaną z grupy karbonylowej () i hydroksylowej (). R (Ar) karboksylowy Możemy je
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
Kwasy karboksylowe C O OH OH C CH 2 H OH CH 2 C CH 3 C OH C OH C OH. propionowy. mrówkowy. akrylowy. octowy. masłowy metakrylowy.
 Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
13. B E Z W O D N I K I I H A L O G E N K I K W A S O W E Aleksander Kołodziejczyk sierpień 2007
 13. B E Z W D N I K I I A L G E N K I K W A S W E Aleksander Kołodziejczyk sierpień 2007 A L G E N K I K W A S W E alogenki kwasowe są pochodnymi kwasów karboksylowych, w których funkcja hydroksylowa została
13. B E Z W D N I K I I A L G E N K I K W A S W E Aleksander Kołodziejczyk sierpień 2007 A L G E N K I K W A S W E alogenki kwasowe są pochodnymi kwasów karboksylowych, w których funkcja hydroksylowa została
Kwasy organiczne. 1. Narysuj wzory półstrukturalne poniższych kwasów:
 Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy f. akrylowy g. jabłkowy h. walerianowy i. fosfoenolopirogronowy
Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy f. akrylowy g. jabłkowy h. walerianowy i. fosfoenolopirogronowy
Kwasy organiczne G. H. I. J. K. ONa L. Ł. O OH
 ollegium Medicum UJ, Katedra hemii rganicznej, Barbara Drożdż Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy
ollegium Medicum UJ, Katedra hemii rganicznej, Barbara Drożdż Kwasy organiczne 1. arysuj wzory półstrukturalne poniższych kwasów: a. glicerynowy b. cytrynowy c. szczawiooctowy d. bursztynowy e. cynamonowy
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Spis treści. Nazewnictwo kwasów karboksylowych.
 Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
KWASY KARBOKSYLOWE. Krystyna Dzierzbicka
 KWASY KARBKSYLWE Krystyna Dzierzbicka Kwasy karboksylowe są związkami organicznymi zawierającymi grupę karboksylową -H zbudowaną z grupy karbonylowej () i hydroksylowej (H). R (Ar) H karboksylowy Możemy
KWASY KARBKSYLWE Krystyna Dzierzbicka Kwasy karboksylowe są związkami organicznymi zawierającymi grupę karboksylową -H zbudowaną z grupy karbonylowej () i hydroksylowej (H). R (Ar) H karboksylowy Możemy
l. at C Wzór sumaryczny pół strukturalny Nazwa systematyczna Nazwa zwyczajowa 1 HCOOH
 KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
Kwasy karboksylowe. 1. Cele lekcji. 2. Metoda i forma pracy. 3. Środki dydaktyczne. 4. Przebieg lekcji. a) Wiadomości.
 Kwasy karboksylowe 1. Cele lekcji a) Wiadomości Uczeń zna budowę kwasów karboksylowych, nazewnictwo kwasów karboksylowych, podział kwasów karboksylowych, sposoby otrzymywania kwasów karboksylowych, właściwości
Kwasy karboksylowe 1. Cele lekcji a) Wiadomości Uczeń zna budowę kwasów karboksylowych, nazewnictwo kwasów karboksylowych, podział kwasów karboksylowych, sposoby otrzymywania kwasów karboksylowych, właściwości
Aldehydy i Ketony. Grupa karbonylowa: Keton. Aldehyd R H CO R 1 R 2
 Aldehydy i Ketony Grupa karbonylowa: Aldehyd Keton R R 1 R 2 1 Aldehyd = alcohol dehydrogenatus alkohol odwodorniony Nazewnictwo: 1. alkan + al grupa aldehydowa = lokant 1 propanal 3 2 1,3-propanodial
Aldehydy i Ketony Grupa karbonylowa: Aldehyd Keton R R 1 R 2 1 Aldehyd = alcohol dehydrogenatus alkohol odwodorniony Nazewnictwo: 1. alkan + al grupa aldehydowa = lokant 1 propanal 3 2 1,3-propanodial
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Grupa karboksylowa DŁUGOŚĆ WIĄZAŃ
 Kwasy karboksylowe Grupa karboksylowa DŁUGOŚĆ WIĄZAŃ KĄT Grupa karboksylowa REZONANS W GRUPIE KARBOKSYLOWEJ Grupa karboksylowa WŁAŚCIWOŚCI FIZYKOCHEMICZNE Grupa karboksylowa KWASOWOŚĆ JONIZACJA ETANOLU
Kwasy karboksylowe Grupa karboksylowa DŁUGOŚĆ WIĄZAŃ KĄT Grupa karboksylowa REZONANS W GRUPIE KARBOKSYLOWEJ Grupa karboksylowa WŁAŚCIWOŚCI FIZYKOCHEMICZNE Grupa karboksylowa KWASOWOŚĆ JONIZACJA ETANOLU
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Kwasy karboksylowe to jednofunkcyjne pochodne węglowodorów o grupie funkcyjnej -COOH zwanej grupą karboksylową.
 Spis treści: Charakterystyka grupy karboksylowej Podział kwasów karboksylowych Nazewnictwo kwasy monokarboksylowe alifatyczne nasycone kwasy monokarboksylowe alifatyczne nienasycone kwasy dikarboksylowe
Spis treści: Charakterystyka grupy karboksylowej Podział kwasów karboksylowych Nazewnictwo kwasy monokarboksylowe alifatyczne nasycone kwasy monokarboksylowe alifatyczne nienasycone kwasy dikarboksylowe
Zadanie: 3 (1 pkt) W poniższej tabeli podano temperatury wrzenia czterech pierwszych w szeregu homologicznym kwasów monokarboksylowych.
 Zadanie: 1 (2 pkt) Pewien kwas karboksylowy zawiera 40% pierwiastka C. Oblicz masę cząsteczkową tego kwasu. Podaj jego wzór sumaryczny i nazwę Zadanie: 2 (1 pkt) Kwas salicylowy ma właściwości antyseptyczne.
Zadanie: 1 (2 pkt) Pewien kwas karboksylowy zawiera 40% pierwiastka C. Oblicz masę cząsteczkową tego kwasu. Podaj jego wzór sumaryczny i nazwę Zadanie: 2 (1 pkt) Kwas salicylowy ma właściwości antyseptyczne.
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 2
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Zadanie: 2 (4 pkt) Napisz, uzgodnij i opisz równania reakcji, które zaszły w probówkach:
 Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Chemia organiczna. Związki zawierające grupę karbonylową. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające grupę karbonylową Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Grupy związków zawierających grupę karbonylową C=O aldehyd ester keton kwasy karboksylowy
Chemia organiczna Związki zawierające grupę karbonylową Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Grupy związków zawierających grupę karbonylową C=O aldehyd ester keton kwasy karboksylowy
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Reakcje aldehydów i ketonów. grupa karbonylowa Z = H, aldehyd Z = R (czyli at. C), keton
 30-33. Reakcje aldehydów i ketonów grupa karbonylowa Z =, aldehyd Z = R (czyli at. C), keton Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 15.1. Nazewnictwo Aldehyd
30-33. Reakcje aldehydów i ketonów grupa karbonylowa Z =, aldehyd Z = R (czyli at. C), keton Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 15.1. Nazewnictwo Aldehyd
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
17. DODATKI Tabela 1. Symbole okre laj ce wielokrotno ci i podwielokrotno ci ułamków dziesi tnych Symbol Okre lenie Wielokrotno Tabela 2.
 17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
Materiał powtórzeniowy do sprawdzianu - kwasy karboksylowe, estry, glicerydy - tłuszcze, mydła + przykładowe zadania z rozwiązaniami
 Materiał powtórzeniowy do sprawdzianu - kwasy karboksylowe, estry, glicerydy - tłuszcze, mydła + przykładowe zadania z rozwiązaniami I. Kwasy karboksylowe 1. Budowa i klasyfikacja kwasów karboksylowych
Materiał powtórzeniowy do sprawdzianu - kwasy karboksylowe, estry, glicerydy - tłuszcze, mydła + przykładowe zadania z rozwiązaniami I. Kwasy karboksylowe 1. Budowa i klasyfikacja kwasów karboksylowych
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
CHEMIA ORGANICZNA. dr hab. Włodzimierz Gałęzowski Wydział Chemii UAM (61)
 EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
Slajd 1. Slajd 2. Aminy. trietyloamina. amoniak. chlorofil
 Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
a) I i II b) II i III c) I i III d) I, II, III
 TEST estry 1) Kwasem karboksylowym, który powstanie w wyniku hydrolizy maślanu etylu jest: a) kwas etanowy b) kwas butanowy c) CH 3 CH 2 COOH d) HCOOH 2) Nienasycony ester, którego polimer jest wykorzystywany
TEST estry 1) Kwasem karboksylowym, który powstanie w wyniku hydrolizy maślanu etylu jest: a) kwas etanowy b) kwas butanowy c) CH 3 CH 2 COOH d) HCOOH 2) Nienasycony ester, którego polimer jest wykorzystywany
Wykład 9. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 9 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Reakcje fenoli c.d. 4. Substytucja w pierścieniu. a) Nitrowanie b) sulfonowanie Reakcje fenoli c) Halogenowanie d) alkilowanie
Wykład 9 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Reakcje fenoli c.d. 4. Substytucja w pierścieniu. a) Nitrowanie b) sulfonowanie Reakcje fenoli c) Halogenowanie d) alkilowanie
CH 3 OH C 2 H 5 OH H 3 C CH 2 CH 2 OH H 3 C CH CH 3 OH metanol etanol propan-1-ol propan-2-ol H 2 C CH 2 OH OH H 2 C CH CH 2 OH OH OH
 Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
GRUPA KARBOKSYLOWA - budowa płaska. Długości wiązań. 132 pm. Długości wiązań: C O i C=O świadczą o występowaniu sprzężenia (w alkoholach długość.
 B I T E N L EMIA G GANIZNA I A Budowa GUPA KABKSYLWA - budowa płaska Kąty między wiązaniami 124 o o 111 o 125 106 o Długości wiązań 110 pm 123 pm 132 pm 97 pm Długości wiązań: i = świadczą o występowaniu
B I T E N L EMIA G GANIZNA I A Budowa GUPA KABKSYLWA - budowa płaska Kąty między wiązaniami 124 o o 111 o 125 106 o Długości wiązań 110 pm 123 pm 132 pm 97 pm Długości wiązań: i = świadczą o występowaniu
Rozdział 7. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 7 Errata do siódmego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 187 Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 7 Errata do siódmego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 187 Zadanie
ORGANICZNE POCHODNE KWASU WĘGLOWEGO. Krystyna Dzierzbicka
 RGANIZNE PDNE KWASU WĘGLWEG Krystyna Dzierzbicka Kwas węglowy ( 2 3 ) słaby kwas nieorganiczny, istnieje tylko w wodnych roztworach. 2 == + kwas węglowy Trwałą nieorganiczną pochodną kwasu węglowego jest
RGANIZNE PDNE KWASU WĘGLWEG Krystyna Dzierzbicka Kwas węglowy ( 2 3 ) słaby kwas nieorganiczny, istnieje tylko w wodnych roztworach. 2 == + kwas węglowy Trwałą nieorganiczną pochodną kwasu węglowego jest
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
Pochodne węglowodorów
 Pochodne węglowodorów 1. Pochodne węglowodorów To związki chemiczne pochodzące od węglowodorów, które w cząsteczkach oprócz węgla, wodoru mają inne pierwiastki chemiczne, np. tlen, azot, chlor. Pochodne
Pochodne węglowodorów 1. Pochodne węglowodorów To związki chemiczne pochodzące od węglowodorów, które w cząsteczkach oprócz węgla, wodoru mają inne pierwiastki chemiczne, np. tlen, azot, chlor. Pochodne
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Chemia związków węgla
 strona 1/7 hemia związków węgla Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Węgiel i jego związki. Proste węglowodory nasycone i nienasycone, alkohole, kwasy karboksylowe,
strona 1/7 hemia związków węgla Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Węgiel i jego związki. Proste węglowodory nasycone i nienasycone, alkohole, kwasy karboksylowe,
Przed sprawdzianem z pochodnych węglowodorów karta powtórzeniowa.
 Przed sprawdzianem z pochodnych węglowodorów karta powtórzeniowa. Grupa związków Grupa funkcyjna wzór nazwa Wzór i nazwa przedstawiciela 1. Znajomość pojęć takich jak: fermentacja alkoholowa i octowa,
Przed sprawdzianem z pochodnych węglowodorów karta powtórzeniowa. Grupa związków Grupa funkcyjna wzór nazwa Wzór i nazwa przedstawiciela 1. Znajomość pojęć takich jak: fermentacja alkoholowa i octowa,
Kwasy Karboksylowe i Nitryle. Według McMurry s Organic Chemistry, 6 th edition
 Kwasy Karboksylowe i Nitryle Według McMurry s Organic Chemistry, 6 th edition Znaczenie Kwasów Karboksylowych (RCO 2 H) Materiał wyjściowy dla pochodnych acylowych (estrów, amidów, chlorków kwasowych)
Kwasy Karboksylowe i Nitryle Według McMurry s Organic Chemistry, 6 th edition Znaczenie Kwasów Karboksylowych (RCO 2 H) Materiał wyjściowy dla pochodnych acylowych (estrów, amidów, chlorków kwasowych)
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
PRZYKŁADOWE ZADANIA KWASY
 PRZYKŁADOWE ZADANIA KWASY Zadanie 1014 (3 pkt) Pr.XII/2004 A2 Określ typ podanych niżej reakcji: I. C 17 H 33 COOH + Br 2 C 17 H 33 Br 2 COOH Al 2O 3, temp II. C 2 H 5 OH C 2 H 4 + H 2 O hγ III. CH 4 +
PRZYKŁADOWE ZADANIA KWASY Zadanie 1014 (3 pkt) Pr.XII/2004 A2 Określ typ podanych niżej reakcji: I. C 17 H 33 COOH + Br 2 C 17 H 33 Br 2 COOH Al 2O 3, temp II. C 2 H 5 OH C 2 H 4 + H 2 O hγ III. CH 4 +
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
Scenariusz lekcji pokazowej z chemii
 Scenariusz lekcji pokazowej z chemii 16.12.2009r. klasa II b prowadząca: Ewa Siennicka dział: Jedno- i wielofunkcyjne pochodne węglowodorów. TEMAT: Kwasy karboksylowe nazewnictwo i właściwości. 1. Cele
Scenariusz lekcji pokazowej z chemii 16.12.2009r. klasa II b prowadząca: Ewa Siennicka dział: Jedno- i wielofunkcyjne pochodne węglowodorów. TEMAT: Kwasy karboksylowe nazewnictwo i właściwości. 1. Cele
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Slajd 1. Etery i epoksydy. Slajd 2. Wprowadzenie. Wzór R-O-R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: CH 3 O CH 3 O CH 3
 Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności
 Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
Podział związków organicznych
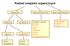 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
KRYTERIA OCENIANIA ZESTAW ZADAŃ DLA KLAS REALIZUJĄCYCH CHEMIĘ W WYMIARZE MINIMUM 8 GODZIN W CYKLU KSZTAŁCENIA.
 MTUR PRÓBN 22 KRĘGW K M I S J EGZMINYJN w KRKWIE HEMI KRYTERI ENINI ZESTW ZDŃ DL KLS RELIZUJĄYH HEMIĘ W WYMIRZE MINIMUM 8 GDZIN W YKLU KSZTŁENI. 55 kręgowa Komisja Egzaminacyjna w Krakowie Matura próbna
MTUR PRÓBN 22 KRĘGW K M I S J EGZMINYJN w KRKWIE HEMI KRYTERI ENINI ZESTW ZDŃ DL KLS RELIZUJĄYH HEMIĘ W WYMIRZE MINIMUM 8 GDZIN W YKLU KSZTŁENI. 55 kręgowa Komisja Egzaminacyjna w Krakowie Matura próbna
STRUKTURA określa w jaki sposób poszczególne atomy połączone są w cząsteczce
 Jakie zagadnienia będą poruszane podczas zgłębiania chemii związków węgla, czyli chemii organicznej? STRUKTURA określa w jaki sposób poszczególne atomy połączone są w cząsteczce MEANIZM - w jaki sposób
Jakie zagadnienia będą poruszane podczas zgłębiania chemii związków węgla, czyli chemii organicznej? STRUKTURA określa w jaki sposób poszczególne atomy połączone są w cząsteczce MEANIZM - w jaki sposób
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
REAKCJE JONÓW ENOLANOWYCH
 REKCJE JÓW ELWYC Część I MTERIŁY PRZYGTWUJĄCE D CLLQUIUM KŃCWEG PRCWI ZWSW CEMI RGICZ zasada Dr artosz Trzewik Kraków, 9 listopada 2013 r. 1 Spis treści: 1. Kwasowość atomów wodoru α, jony enolanowe 2.
REKCJE JÓW ELWYC Część I MTERIŁY PRZYGTWUJĄCE D CLLQUIUM KŃCWEG PRCWI ZWSW CEMI RGICZ zasada Dr artosz Trzewik Kraków, 9 listopada 2013 r. 1 Spis treści: 1. Kwasowość atomów wodoru α, jony enolanowe 2.
Błędy w skrypcie: Chemia organiczna Kurs podstawowy. str. 4 (tytuł podrozdziału 5.2.7.) jest (reakcja Karasha), powinno być (reakcja Kharascha)
 1 Błędy w skrypcie: hemia organiczna Kurs podstawowy str. 4 (tytuł podrozdziału 5.2.7.) jest (reakcja Karasha), powinno być (reakcja Kharascha) str. 13 (1. wiersz od góry) ( 3 () ) str. 13 (12. wiersz
1 Błędy w skrypcie: hemia organiczna Kurs podstawowy str. 4 (tytuł podrozdziału 5.2.7.) jest (reakcja Karasha), powinno być (reakcja Kharascha) str. 13 (1. wiersz od góry) ( 3 () ) str. 13 (12. wiersz
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
WYMAGANIA EDUKACYJNE
 SZKOŁA PODSTAWOWA W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie 8 Szkoły Podstawowej Wymagania edukacyjne niezbędne
SZKOŁA PODSTAWOWA W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie 8 Szkoły Podstawowej Wymagania edukacyjne niezbędne
Rodzaje wiązań chemicznych
 Rodzaje wiązań chemicznych Teoria Lewisa (1916) atomy łączą się ze sobą przez przeniesienie (1 lub więcej) elektronów z jednego atomu na drugi wiązanie jonowe lub przez uwspólnienie par elektronowych aby
Rodzaje wiązań chemicznych Teoria Lewisa (1916) atomy łączą się ze sobą przez przeniesienie (1 lub więcej) elektronów z jednego atomu na drugi wiązanie jonowe lub przez uwspólnienie par elektronowych aby
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Program wykładu Chemia Organiczna I
 Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Substytucja nukleofilowa
 Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Alkeny. Wzór ogólny alkenów C n H 2n. (Uwaga identyczny wzór ogólny mają cykloakany!!!)
 Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
ZWIĄZKI WĘGLA Z WODOREM 1) Uzupełnij i uzgodnij równania reakcji spalania całkowitego alkanów, alkenów i alkinów.
 Nauczanie domowe WIEM, CO TRZEBA Klasa VIII Chemia od listopada do czerwca aktualizacja 05.10.2018 ZWIĄZKI WĘGLA Z WODOREM 1) Uzupełnij i uzgodnij równania reakcji spalania całkowitego alkanów, alkenów
Nauczanie domowe WIEM, CO TRZEBA Klasa VIII Chemia od listopada do czerwca aktualizacja 05.10.2018 ZWIĄZKI WĘGLA Z WODOREM 1) Uzupełnij i uzgodnij równania reakcji spalania całkowitego alkanów, alkenów
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Materiały dodatkowe związki karbonylowe
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem
 Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. COH
 Alkohole R Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. C Alkohole można uważać za organiczne pochodne wody --, w której jeden z atomów
Alkohole R Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. C Alkohole można uważać za organiczne pochodne wody --, w której jeden z atomów
I. Węgiel i jego związki z wodorem
 NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Narysuj stereoizomery cis i trans dla 1,2-dibromocyklobutanu. Czy ulegają one wzajemnej przemianie, odpowiedź uzasadnij.
 WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
NOMENKLATURA ZWIĄZKÓW ORGANICZNYCH
 MEKLATURA ZWIĄZKÓW RGAIZY AZEWITW ALKAÓW Tabela. azwy alkanów prostych o danej liczbie atomów węgla. Liczba atomów węgla metan etan propan butan pentan 6 heksan 7 heptan 8 oktan 9 nonan 0 dekan undekan
MEKLATURA ZWIĄZKÓW RGAIZY AZEWITW ALKAÓW Tabela. azwy alkanów prostych o danej liczbie atomów węgla. Liczba atomów węgla metan etan propan butan pentan 6 heksan 7 heptan 8 oktan 9 nonan 0 dekan undekan
wzory skrócone Kwasy aromatyczne grupa arylowa połączona z grupą karboksylową. kwas benzoesowy
 KWASY KARBKSYLWE wzór ogólny wzory skrócone grupa karboksylowa Kwasy alifatyczne grupa alkilowa połączona z grupą karboksylową kwas propionowy kwas mrówkowy Kwasy aromatyczne grupa arylowa połączona z
KWASY KARBKSYLWE wzór ogólny wzory skrócone grupa karboksylowa Kwasy alifatyczne grupa alkilowa połączona z grupą karboksylową kwas propionowy kwas mrówkowy Kwasy aromatyczne grupa arylowa połączona z
REAKCJE W CHEMII ORGANICZNEJ
 Katedra Biochemii ul. Akademicka 12, 20-033 Lublin tel. 081 445 66 08 www.biochwet.up.lublin.pl REAKCJE W CHEMII ORGANICZNEJ I. Reakcje utleniania na przykładzie różnych związków organicznych. 1. Utlenienie
Katedra Biochemii ul. Akademicka 12, 20-033 Lublin tel. 081 445 66 08 www.biochwet.up.lublin.pl REAKCJE W CHEMII ORGANICZNEJ I. Reakcje utleniania na przykładzie różnych związków organicznych. 1. Utlenienie
