Fizyka Wyk ad W8 1. Fizyka Statystyczna
|
|
|
- Lech Andrzejewski
- 6 lat temu
- Przeglądów:
Transkrypt
1 Fizyka Wykad W8 Fizyka Statystyczna W dotychczas zrealizowanym kursie fizyki skupilimy si na ukadach fizycznych o niewielkiej liczbie stopni swobody tj. liczbie zmiennych niezalenych potrzebnych do opisania zjawisk w ukadzie. Dziaem fizyki, który zajmuje si ukadami o bardzo duej liczbie stopni swobody jest fizyka statystyczna. Posuguje si ona metodami probabilistycznymi: dlatego warunkiem koniecznym stosowalnoci metod z tej dziedziny jest ogromna liczba czstek - dla ustalenia skali - liczba Avogadro tj cząsteczek w gramorównoważniku substancji (w molu). Nie jest to warunek wystarczajcy bo np. dla bryy doskonale sztywnej liczba czstek jest bardzo dua ale liczba stopni swobody maa i metody statystyczne s nieodpowiednie. Natomiast aby okreli rozszerzalno bryy lub drgania jej atomów trzeba stosowa metody fizyki statystycznej
2 Fizyka Wykad W8 2 U podoa tej dziedziny - jak w przypadku wikszoci innych dziaów fizyki - ley ruch mechaniczny ale w specyficzny sposób: nie mona rozwiza ukadu równa ruchu dla tak wielu stopni swobody (rzdu np ) ale mona okreli pewne prawidowoci odnoszce si do ukadu jako caoci Prawa fizyki statystycznej wyróniaj si tym, e najczciej wystpuje w nich temperatura T. Podobnie jest w pokrewnej dziedzinie zwanej termodynamik Rónica midzy tymi dwoma dziedzinami jest taka, e termodynamika jest dziedzin fenomenologiczn powsta z obserwacji wyników dowiadcze fizyka statystyczna wywodzi te same zjawiska, które s omawiane w termodynamice, ale wychodzc z mikroskopowych zalenoci (mówimy: z zasad pierwszych ) Aby tego dokona potrzebne jest w fizyce statystycznej rozrónienie stan mikroskopowy (mikrostan): jest to stan wszystkich czstek ukadu Q( r,r 2,...,r N, p, p2,...,pn, t)
3 Fizyka Wykad W8 3 Na ogó stan mikroskopowy Q zmienia si w czasie: zapisujemy te zmiany w 6N wymiarowej przestrzeni fazowej wszystki pooe oraz pdów. Symbolicznie mona tak ewolucj przedstawi tak: w trakcie ewolucji mokrostany poruszaj sie po trajektorii w przestrzeni fazowej makrostan (stan makroskopowy): kademu mikrostanowi odpowiadaj charakterytyki okrelajce stan caoci ukadu Przykady energia wewnętrzna, magnetyzacja, koncentracja noników adunku Makrostan moe zmieni si w czasie tj. makroskopowa charakterystyka A(t) = A(Q(t)).
4 Fizyka Wykad W8 4 Zwiazek makrostanu A z mikrostanem Q jest znany jedynie w sensie statystycznym gdy mikrostanów nie jestemy w stanie ledzi. Dokadno wyznaczania charakterystyki makrostanu jest zwizana z liczb czstek N: gdzie A < A> <A> oznacza redni wartoc A 2 2 A= <(A- < A> ) = < A 2 >-< A> jest odchyleniem rednim standardowym Przykad: wida od razu, e dla niewielkiej liczby czstek (stopni swobody) bd metod fizyki statystycznej jest duy. Tak wic posiadamy oraz dobre metody fizyki dla niewielkiej liczby stopni swobody (mechanika) dla bardzo duej liczby stopni swobody ale dla ukadów mezoskopowych (średniej skali) mamy kopoty! Widzimy kluczow dla fizyki statystycznej potrzeb okrelenia charakterystyki makroskopowej A N wielkoci sredniej danej
5 Fizyka Wykad W8 5 Najbardziej naturalna średnia to średnia w czasie: < A>= gdzie τ jest czasem urednienia. A( Q ( Jeli <A> jest stae w czasie to mamy do czynienia ze 0 t ) ) dt stanem równowagi ze wzgldu na zmienn makroskopow A. Ukad odosobniony (tj. taki, który nie wymienia ani czstek ani ciepa z otoczeniem) to po pewnym czasie (czas relaksacji) osiga stan równowagi. Podzia fizyki statystycznej fizyka statystyczna stanów równowagi przykad zagadnienia: wyznaczanie temperatury ciaa fizyka statystyczna stanów nierównowagi przykad zagadnienia: przepyw prdu elektrycznego
6 Fizyka Wykad W8 6 Zagadnienia równowagi nie naley myli z zagadnieniem stacjonarnoci: Przepyw prdu elektrycznego jest zjawiskiem nierównowagowym ale moe by stacjonarny lub niestacjonarny Zespoy statystyczne Gibbsa Obliczanie redniej obserwabli A jako redniej po czasie: Aśr = A( Q ( t ) ) dt 0 To jest bardzo dobra definicja redniej ale nie jest praktyczn receptą na jej obliczenie. Zazwyczaj trzeba czekać długo aby średnia osiągnęła stałą wartość (znamiona stanu równowagi!) Znacznie skuteczniejszym sposobem jest wykorzystanie koncepcji zespou statystycznego Gibbsa. Przykad: przypumy, e chcemy wyznaczy warto redni jakiego procesu przypadkowego np. rzutu monet lub kostk. Moemy: rzuca jedn monet tak dugo a bdziemy mieli dostatecznie du prób wyników rzutu by obliczy redni po czasie. Dla monety to nie zajmie duo czasu ale dla skomplikowanych procesów przypadkowych jak np. ruch Browna (ruch czstki kurzu w powietrzu) wyznaczenie rzetelnej redniej moe wymaga duej cierpliwoci
7 Fizyka Wykad W8 7 rzuci jednoczenie i w taki sam sposób bardzo wielk liczb identycznych monet (zespó monet) raz a nastpnie obliczy redni wyniku. < A>= P(Q) A(Q) Q P(Q) jest prawdopodobiestwem (ściślej gęstością prawdopodobieństwa) otrzymania stanu mikroskopowego Q (np. ora). P(Q) wyraa si jako procent tych ukadów zespou Gibbsa, które znajduj si w stanie Q. Podstawowy postulat fizyki statystycznej stanów równowagi Aśr =< A > U podstaw tego postulatu ley nastpujcy fakt: Stany mikroskopowe ukadu termodynamicznego s od siebie niezalene jeli odstp czasu pomidzy pomiarami tych stanów jest dostatecznie duy. Tak jest w zdecydowanej wikszoci sytuacji eksperymentalnych - pomiar zawsze wprowadza urednienie po pewnym czasie. Funkcje stanu W fizyce statystycznej (jak równiez w termodynamice) okrela si funkcje stanu ukadu termodynamicznego.
8 Fizyka Wykad W8 8 Oczywistym i najprostszym przykadem takiej funkcji jest rednia energia <E> ukadu rozumiana jako rednia energii po zespole statystycznym wszystkich mikrostanów ukadu (jest to tzw. energia wewntrzna ukadu). Okazuje si, e mona zdefiniowa wiele funkcji stanu. Jedn z najwaniejszych takich funkcji stanu jest entropia. Pojcie to powstao w termodynamice, gdzie wnioskujc z obserwacji wprowadzono Q pojcie entropii termodynamicznej S = T Q jest ciepem wymieniany z otoczenie w trakcie obserwowanego zjawiska T jest temperatur w jakiej ta wymiana zachodzi. Entropia termodynamiczna jest więc ciepłem zredukowanym (obliczanym na stopień temperatury) Boltzmann wprowadzi wyraenie na entropi wychodzc z przesanek fizyki statystycznej: S = k B ln g gdzie g liczb moliwych mikrostanów relizujcych dany makrostan, a k B =, J/K jest sta fizyczn (staa Boltzmanna) potrzebn po to aby entropia tak zdefiniowana bya równa entropii termodynamicznej. Tak zdefiniowana entropia ma wymiar energii na stopień temperatury. Entropia wskazuje kierunek przebiegu procesów termodynamicznych (tj. kierunek zmian stanu termodynamicznego).
9 Fizyka Wykad W8 9 Przykład: mao prawdopodobne jest aby gaz w pudeku spontanicznie zebra si w jednym naroniku zbiornika. Proces taki wymagałby zmniejszenia entropii czego zabraniaj prawa termodynamiki procesów równowagowych. Entropia Boltzmanna wie si z entropi wprowadzon znacznie póniej (lata 20-te i 40-te XX w.) w teorii informacji (informacja Shannona lub entropia Shannona). Przykad: Przypumy, e mamy g jednakowo prawdopodobnych mikrostanów (dla monety g=2, dla kostki do gry g=6, dla alfabetu Morse a g=2 a waciwie 3 itd.) Jeeli nie wykonalimy adnych pomiarów (np. rzutów kostk) to nasza niewiedza jest najwiksza i tym większa im wiksze jest liczba stanów g. Uwaamy, e nasza informacja I = 0. Po dokonaniu rzutu nasza informacja I 0 i znamy mikrostan. Chcemy teraz zwiza informacj I z liczb stanów g.
10 Fizyka Wykad W8 0 Wymagamy jednak aby informacja bya addytywna tj. aby gdy mamy dwa niezalene procesy (np. dwie kostki do gry) i liczba stanów g = g g 2 to aby I( g g )= I( g )+ I( g ) 2 2 Tak bdzie wtedy i tylko wtedy gdy I = K ln g przy czym w teorii informacji na ogó przyjmuje si K = /ln 2 = log 2 e. Ostatecznie informacja i wyraana jest w bitach. I = log 2 g Przykad: Przypumy, e mamy sowo o dugoci N skadajce si ze znaków Morse a: N kresek i N 2 kropek (pomijamy spacje!). Liczba stanów g wynosi N N! g = = ; N = N + N 2 n N! N 2! g jest w tym wypadku liczb moliwych sów, jakie mona przekaza takim alfabetem za pomoc N kresek i N 2 kropek.
11 Fizyka Wykad W8 Chcemy okreli informacj na symbol i = I/N Wstawiajc wyraenie na g do wzoru na informacj I oraz stosujc wzór Stirlinga ln Q! Q (ln Q - ) poprawny dla Q > 00 otrzymuje si przyblione wyraenie I N N N 2 N 2 i -K ln + ln N N N N N Wprowadzajc prawdopodobiestwo mikrostanu i: N i p = i N otrzymujemy wyraenie na informacj, dla 2 symboli. i = -K ( p ln p + p ln p ) 2 2 To wyraenie na informacj mona uogólni na przypadek wikszej liczby zdarze (symboli) i= - K p p i i ln i Uwaga na koniec przykadów: czsto odrónia si entropi informacyjn (miar niewiedzy) od informacji tj. czsto przyjmuje się S = -I.
12 Fizyka Wykad W8 2 Istniej trzy podstawowe zespoy statystyczne Gibbsa: zespó mikrokanoniczny, zespó kanoniczny i wielki zespó kanoniczny kady z nich reprezentowany jest przez odrbny rozkad statystyczny P(Q) zespó mikrokanoniczny: Szczególna rol w zrozumieniu zjawisk odgrywaj ukady izolowane od otocznia tj. takie, które nie wymieniaj ani energii ani czstek z otoczeniem. Dla takiego ukadu wszystkie mikrostany Q s jednakowo prawdopobne tj. P(Q) = const. Warto tej staej wynika z unormowania rozkadu statystycznego tj. P(Q)=, gdzie suma jest po wszystkich mikrostanach Q. To, e energia i liczba czstek ukadu izolowanego si nie zmienia to nie oznacza, e wiele innych wielkoci fizycznych w takim ukadzie nie moe si zmienia. Przykad: Rozpatrzmy entropi w przykadzie ze sowem zapisanym za pomoc alfebetu Morse a. Moe to by dowolny inny ukad o zawierajcy N elementów mogcych si znajdowa w 2 mikrostanach np. czstki o spinie /2 ). Q
13 Fizyka Wykad W8 3 Niech n bdzie liczb obiektów znajdujcych si w stanie A (np. kropek). Zgodnie z definicj Boltzmanna entropia S = k B ln g W naszym przypadku g jest dane przez zasady kombinatoryki jako N N! g = = n n! (N - n)! N To wyraenie ma maksimum dla n =. 2 Wniosek: liczba stanów jest najwiksza gdy poowa czstek ukadu znajduje si w stanie A a poowa w B. entropia takiego stanu jest najwiksza Wida, e ukad bdzie si znajdowa w takim makrostanie, dla którego entropia jest maksymalna! makrostanowi temu odpowiada najwiksza liczba mikrostanów, którego go realizuj - jest wic najbardziej prawdopodobny. Std bierze si interpretacja entropii jako miary chaotycznoci (nieuporzdkowania): gdy liczba równowanych realizacji danego makrostanu jest najwiksza najwieksza jest te nieokrelono mikrostanu w jakim ukad si znajduje.
14 Fizyka Wykad W8 4 warunki równowagi dwóch ukadów Równowaga w mechanice: E wystarczy zarzda = 0 gdzie E jest całkowitą energią układu jest zmienn wzgldem, której równowaga ma by osignita Równowaga w sensie fizyki statystycznej jest o wiele bardziej skomplikowanym pojciem: wymaga uwzgldnienia oprócz minimum energii jeszcze liczby stanów mikroskopowych g przy zadanym stanie makroskopowym. Na ogó im wiksza energia danego makrostanu tym wiksza liczba stanów mikroskopowych, które je realizuj. Oznacza to, e prawdopodobienstwo takiego stanu bdzie wiksze. Jak określi stan równowagi ukadu odosobnionego? Przyjmuje si, e jest to stan jaki ustala si po dostatecznie dugim czasie. Staoc naley tu rozumie w sensie staoci redniej statystycznej charakterystyk makroskopowych ukadu. okazuje si, e takie okrelenie dobrze odzwierciedla obserwacje. naturalnym kryterium równowagi ukadu odosobnionego jest wic stan o najwikszej entropii
15 Fizyka Wykad W8 5 A jaka bdzie równowaga w ukadzie odosobnionym, który skada si z dwóch podukadów termodynamicznych w kontakcie ze sob? Dla ustalenia uwagi wybieramy najbardziej naturalne wielkoci makroskopowe: energi E objto V liczb czstek w ukadzie N Ukad jako cao jest odosobniony wic jest w równowadze termodynamicznej E+ E2= E V +V 2= V N + N 2= N Pomidzy podukadami moe zachodzi wymiana energii, objtoci oraz liczby czstek ale w taki sposób aby równowaga caoci nie bya naruszona: E= - E2 ; V = - V 2 ; N= - N 2
16 Fizyka Wykad W8 6 W stanie równowagi caego ukadu entropia jest maksymalna (ekstremum): ds = ds ds2 =0 S S ds = de+ E E2 de2 + S S dv + V V 2 dv 2 + S S dn + N N 2 dn 2= 0 W analogii do termodynamiki definiuje si w fizyce statystycznej: S temperatur = T E S cinienie p=t V S potencja chemiczny = - T N Potencja chemiczny jest to energia potrzebna na dodanie (odjcie) jednej czstki w ukadzie. Dla póprzewodników (i w całej fizyce ciała stałego) potencja chemiczny jest równy energii Fermiego.
17 Fizyka Wykad W8 7 Po podstawieniu tych definicji ds = T - T 2 de dn = 0 T T 2 gdzie energia E, objto V oraz liczba czstek N s zmiennymi niezalenymi. Jak wida warunkiem równowagi dwóch podukładów jest wyrównanie temperatury podukadów (T = T 2 ), cinienia (p = p 2 ) oraz potencjaów chemicznych (μ = μ 2 ). Ten ostatni warunek spełniony zostaje przez przekazanie odpowiedniej liczby cząstek z jednego podukładu do drugiego. + p T - p T 2 2 dv Uwagi: bardzo wiele przyrzdów póprzewodnikowych opiera swoje dziaanie na zjawisku równowagi termodynamicznej przy zmiennej liczbie czstek czsto dwa podukady w równowadze nie s rozdzielone fizycznie np. jednym podukadem mogą by elektrony naleące do jednego pasma a drugim - elektrony znajdujce si w drugim paśmie.
Wykład 8 i 9. Hipoteza ergodyczna, rozkład mikrokanoniczny, wzór Boltzmanna
 Wykład 8 i 9 Hipoteza ergodyczna, rozkład mikrokanoniczny, wzór Boltzmanna dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW)
Wykład 8 i 9 Hipoteza ergodyczna, rozkład mikrokanoniczny, wzór Boltzmanna dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW)
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron
 Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
Układy statystyczne. Jacek Jurkowski, Fizyka Statystyczna. Instytut Fizyki
 Instytut Fizyki 2015 Stany mikroskopowe i makroskopowe w układzie wielopoziomowym Stany mikroskopowe i makroskopowe w układzie wielopoziomowym N rozróżnialnych cząstek, z których każda może mieć energię
Instytut Fizyki 2015 Stany mikroskopowe i makroskopowe w układzie wielopoziomowym Stany mikroskopowe i makroskopowe w układzie wielopoziomowym N rozróżnialnych cząstek, z których każda może mieć energię
Elementy termodynamiki i wprowadzenie do zespołów statystycznych. Katarzyna Sznajd-Weron
 Elementy termodynamiki i wprowadzenie do zespołów statystycznych Katarzyna Sznajd-Weron Wielkości makroskopowe - termodynamika Termodynamika - metoda fenomenologiczna Fenomenologia w fizyce: widzimy jak
Elementy termodynamiki i wprowadzenie do zespołów statystycznych Katarzyna Sznajd-Weron Wielkości makroskopowe - termodynamika Termodynamika - metoda fenomenologiczna Fenomenologia w fizyce: widzimy jak
S ścianki naczynia w jednostce czasu przekazywany
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
Teoria kinetyczno cząsteczkowa
 Teoria kinetyczno cząsteczkowa Założenie Gaz składa się z wielkiej liczby cząstek znajdujących się w ciągłym, chaotycznym ruchu i doznających zderzeń (dwucząstkowych) Cel: Wyprowadzić obserwowane (makroskopowe)
Teoria kinetyczno cząsteczkowa Założenie Gaz składa się z wielkiej liczby cząstek znajdujących się w ciągłym, chaotycznym ruchu i doznających zderzeń (dwucząstkowych) Cel: Wyprowadzić obserwowane (makroskopowe)
Elementy termodynamiki
 Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 5 stycznia 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 5 stycznia 2019 1 / 27 Wielkości
Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 5 stycznia 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 5 stycznia 2019 1 / 27 Wielkości
Wstęp do fizyki statystycznej: krytyczność i przejścia fazowe. Katarzyna Sznajd-Weron
 Wstęp do fizyki statystycznej: krytyczność i przejścia fazowe Katarzyna Sznajd-Weron Co to jest fizyka statystyczna? Termodynamika poziom makroskopowy Fizyka statystyczna poziom mikroskopowy Marcin Weron
Wstęp do fizyki statystycznej: krytyczność i przejścia fazowe Katarzyna Sznajd-Weron Co to jest fizyka statystyczna? Termodynamika poziom makroskopowy Fizyka statystyczna poziom mikroskopowy Marcin Weron
FIZYKA STATYSTYCZNA. d dp. jest sumaryczną zmianą pędu cząsteczek zachodzącą na powierzchni S w
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
6.2. Baza i wymiar. V nazywamy baz-
 62 Baza i wymiar V nazywamy baz- Definicja 66 Niech V bdzie przestrzeni, liniow, nad cia/em F Podzbiór B przestrzeni V, je2eli: () B jest liniowo niezale2ny, (2) B jest generuj,cy, tzn lin(b) =V Przyk/ady:
62 Baza i wymiar V nazywamy baz- Definicja 66 Niech V bdzie przestrzeni, liniow, nad cia/em F Podzbiór B przestrzeni V, je2eli: () B jest liniowo niezale2ny, (2) B jest generuj,cy, tzn lin(b) =V Przyk/ady:
= = Budowa materii. Stany skupienia materii. Ilość materii (substancji) n - ilość moli, N liczba molekuł (atomów, cząstek), N A
 Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
Wykład 1 i 2. Termodynamika klasyczna, gaz doskonały
 Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Termodynamika. Część 4. Procesy izoparametryczne Entropia Druga zasada termodynamiki. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Dynamika Uk adów Nieliniowych 2009 Wykład 11 1 Synchronizacja uk adów chaotycznych O synchronizacji mówiliśmy przy okazji języków Arnolda.
 Dynamika Ukadów Nieliniowych 2009 Wykład 11 1 Synchronizacja ukadów chaotycznych O synchronizacji mówiliśmy przy okazji języków Arnolda. Wtedy była to synchronizacja stanów periodycznych. Wiecej na ten
Dynamika Ukadów Nieliniowych 2009 Wykład 11 1 Synchronizacja ukadów chaotycznych O synchronizacji mówiliśmy przy okazji języków Arnolda. Wtedy była to synchronizacja stanów periodycznych. Wiecej na ten
Fizyka statystyczna doskona ego gazu bozonów
 Fizyka statystyczna doskonaego gazu bozonów Kazimierz Rzewski Centrum Fizyki Teoretycznej PAN oraz Uniwersytet Kardynaa Stefana Wyszyskiego w Warszawie Fizyka statystyczna doskonaego gazu bozonów Kazimierz
Fizyka statystyczna doskonaego gazu bozonów Kazimierz Rzewski Centrum Fizyki Teoretycznej PAN oraz Uniwersytet Kardynaa Stefana Wyszyskiego w Warszawie Fizyka statystyczna doskonaego gazu bozonów Kazimierz
Fizyka statystyczna Termodynamika bliskiej nierównowagi. P. F. Góra
 Fizyka statystyczna Termodynamika bliskiej nierównowagi P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Nasze wszystkie dotychczasowe rozważania dotyczyły układów w równowadze termodynamicznej lub
Fizyka statystyczna Termodynamika bliskiej nierównowagi P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Nasze wszystkie dotychczasowe rozważania dotyczyły układów w równowadze termodynamicznej lub
Występują fluktuacje w stanie równowagi Proces przejścia do stanu równowagi jest nieodwracalny proces powrotny jest bardzo mało prawdopodobny.
 Wykład 14: Fizyka statystyczna Zajmuje sie układami makroskopowymi (typowy układ makroskopowy składa się z ok. 10 25 atomów), czyli ok 10 25 równań Newtona? Musimy dopasować inne pojęcia do opisu takich
Wykład 14: Fizyka statystyczna Zajmuje sie układami makroskopowymi (typowy układ makroskopowy składa się z ok. 10 25 atomów), czyli ok 10 25 równań Newtona? Musimy dopasować inne pojęcia do opisu takich
Teoria ergodyczności: co to jest? Średniowanie po czasie vs. średniowanie po rozkładach Twierdzenie Poincare o powrocie Twierdzenie ergodyczne
 WYKŁAD 23 1 Teoria ergodyczności: co to jest? Średniowanie po czasie vs. średniowanie po rozkładach Twierdzenie Poincare o powrocie Twierdzenie ergodyczne (Birkhoff, Ter Haar) Hipoteza semi-ergodyczna
WYKŁAD 23 1 Teoria ergodyczności: co to jest? Średniowanie po czasie vs. średniowanie po rozkładach Twierdzenie Poincare o powrocie Twierdzenie ergodyczne (Birkhoff, Ter Haar) Hipoteza semi-ergodyczna
Elementy termodynamiki
 Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 marca 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 marca 2019 1 / 37 Dwa poziomy
Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 marca 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 marca 2019 1 / 37 Dwa poziomy
Klasyczna mechanika statystyczna Gibbsa I
 Wykład III Mechanika statystyczna Klasyczna mechanika statystyczna Gibbsa I Wstępne uwagi Materia nas otaczająca, w szczególności gazy będące centralnym obiektem naszego zainteresowania, zbudowane są z
Wykład III Mechanika statystyczna Klasyczna mechanika statystyczna Gibbsa I Wstępne uwagi Materia nas otaczająca, w szczególności gazy będące centralnym obiektem naszego zainteresowania, zbudowane są z
5. (8 punktów) EGZAMIN MAGISTERSKI, r Matematyka w ekonomii i ubezpieczeniach
 Matematyka w ekonomii i ubezpieczeniach ( Niezale»ne szkody maja rozkªady P (X i = k) = exp( 1)/k!, P (Y i = k) = 4+k ) k (1/3) 5 (/3) k, k = 0, 1,.... Niech S = X 1 +... + X 500 + Y 1 +... + Y 500. Skªadka
Matematyka w ekonomii i ubezpieczeniach ( Niezale»ne szkody maja rozkªady P (X i = k) = exp( 1)/k!, P (Y i = k) = 4+k ) k (1/3) 5 (/3) k, k = 0, 1,.... Niech S = X 1 +... + X 500 + Y 1 +... + Y 500. Skªadka
Co to jest model Isinga?
 Co to jest model Isinga? Fakty eksperymentalne W pewnych metalach (np. Fe, Ni) następuje spontaniczne ustawianie się spinów wzdłuż pewnego kierunku, powodując powstanie makroskopowego pola magnetycznego.
Co to jest model Isinga? Fakty eksperymentalne W pewnych metalach (np. Fe, Ni) następuje spontaniczne ustawianie się spinów wzdłuż pewnego kierunku, powodując powstanie makroskopowego pola magnetycznego.
Wykład 3. Entropia i potencjały termodynamiczne
 Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Elementy fizyki statystycznej
 5-- lementy fizyki statystycznej ermodynamika Gęstości stanów Funkcje rozkładu Gaz elektronów ermodynamika [K] 9 wszechświat tuż po powstaniu ermodynamika to dział fizyki zajmujący się energią termiczną
5-- lementy fizyki statystycznej ermodynamika Gęstości stanów Funkcje rozkładu Gaz elektronów ermodynamika [K] 9 wszechświat tuż po powstaniu ermodynamika to dział fizyki zajmujący się energią termiczną
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12
 Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny
 Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Równania kinetyczne prostych reakcji.
 Szybko reakcji chemicznej definiowana jest jako ubytek stenia substratu lub przyrost stenia produktu w jednostce czasu. W definicjach szybkoci innych zjawisk wana jest wielko okrelajca kinetyk w danej
Szybko reakcji chemicznej definiowana jest jako ubytek stenia substratu lub przyrost stenia produktu w jednostce czasu. W definicjach szybkoci innych zjawisk wana jest wielko okrelajca kinetyk w danej
Rozkłady: Kanoniczny, Wielki Kanoniczny, Izobaryczno-Izotermiczny
 Rozkłady: Kanoniczny, Wielki Kanoniczny, Izobaryczno-Izotermiczny 1 Rozkład Mikrokanoniczny (przypomnienie) S= k B ln( (E,V,{x i },{N j }) ) Z fenomenologii: Niestety, rachunki przy użyciu rozkładu mikrokanonicznego
Rozkłady: Kanoniczny, Wielki Kanoniczny, Izobaryczno-Izotermiczny 1 Rozkład Mikrokanoniczny (przypomnienie) S= k B ln( (E,V,{x i },{N j }) ) Z fenomenologii: Niestety, rachunki przy użyciu rozkładu mikrokanonicznego
Krótki przegląd termodynamiki
 Wykład I Przejścia fazowe 1 Krótki przegląd termodynamiki Termodynamika fenomenologiczna oferuje makroskopowy opis układów statystycznych w stanie równowagi termodynamicznej bądź w stanach jemu bliskich.
Wykład I Przejścia fazowe 1 Krótki przegląd termodynamiki Termodynamika fenomenologiczna oferuje makroskopowy opis układów statystycznych w stanie równowagi termodynamicznej bądź w stanach jemu bliskich.
KLUCZ PUNKTOWANIA ODPOWIEDZI
 Egzamin maturalny maj 009 MATEMATYKA POZIOM PODSTAWOWY KLUCZ PUNKTOWANIA ODPOWIEDZI Zadanie 1. Matematyka poziom podstawowy Wyznaczanie wartoci funkcji dla danych argumentów i jej miejsca zerowego. Zdajcy
Egzamin maturalny maj 009 MATEMATYKA POZIOM PODSTAWOWY KLUCZ PUNKTOWANIA ODPOWIEDZI Zadanie 1. Matematyka poziom podstawowy Wyznaczanie wartoci funkcji dla danych argumentów i jej miejsca zerowego. Zdajcy
Termodynamika. Część 11. Układ wielki kanoniczny Statystyki kwantowe Gaz fotonowy Ruchy Browna. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 11 Układ wielki kanoniczny Statystyki kwantowe Gaz fotonowy Ruchy Browna Janusz Brzychczyk, Instytut Fizyki UJ Układ otwarty rozkład wielki kanoniczny Rozważamy układ w równowadze termicznej
Termodynamika Część 11 Układ wielki kanoniczny Statystyki kwantowe Gaz fotonowy Ruchy Browna Janusz Brzychczyk, Instytut Fizyki UJ Układ otwarty rozkład wielki kanoniczny Rozważamy układ w równowadze termicznej
( ) Pochodne. Załómy, e funkcja f jest okrelona w pewnym otoczeniu punktu x 0. Liczb
 Pocodne Załómy, e unkcja jest okrelona w pewnym otoczeniu punktu. Liczb ( + ) ( ) nazywamy ilorazem rónicowym unkcji w punkcie dla przyrostu. Pocodn ( ) unkcji w punkcie nazywamy granic ilorazu rónicowego,
Pocodne Załómy, e unkcja jest okrelona w pewnym otoczeniu punktu. Liczb ( + ) ( ) nazywamy ilorazem rónicowym unkcji w punkcie dla przyrostu. Pocodn ( ) unkcji w punkcie nazywamy granic ilorazu rónicowego,
ODPOWIEDZI I SCHEMAT PUNKTOWANIA ZESTAW NR 2 POZIOM PODSTAWOWY. 1. x y x y
 Nr zadania Nr czynnoci Przykadowy zestaw zada nr z matematyki ODPOWIEDZI I SCHEMAT PUNKTOWANIA ZESTAW NR POZIOM PODSTAWOWY Etapy rozwizania zadania. Podanie dziedziny funkcji f: 6, 8.. Podanie wszystkich
Nr zadania Nr czynnoci Przykadowy zestaw zada nr z matematyki ODPOWIEDZI I SCHEMAT PUNKTOWANIA ZESTAW NR POZIOM PODSTAWOWY Etapy rozwizania zadania. Podanie dziedziny funkcji f: 6, 8.. Podanie wszystkich
WYKŁAD 9: Rozkład mikrokanoniczny i entropia Boltzmanna
 WYKŁAD 9: Rozkład mikrokanoniczny i entropia Boltzmanna (Zadaniem Fizyki Statystycznej jest zrozumienie własności (równowagowych i nierównowagowych materii w oparciu o oddziaływania międzymolekularne)
WYKŁAD 9: Rozkład mikrokanoniczny i entropia Boltzmanna (Zadaniem Fizyki Statystycznej jest zrozumienie własności (równowagowych i nierównowagowych materii w oparciu o oddziaływania międzymolekularne)
TERMODYNAMIKA FENOMENOLOGICZNA
 TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
Arkusz zawiera informacje prawnie chronione do momentu rozpocz cia egzaminu.
 Ukad graficzny CKE 2013 KOD Centralna Komisja Egzaminacyjna Arkusz zawiera informacje prawnie chronione do momentu rozpoczcia egzaminu. WPISUJE ZDAJCY PESEL Miejsce na naklejk z kodem dysleksja EGZAMIN
Ukad graficzny CKE 2013 KOD Centralna Komisja Egzaminacyjna Arkusz zawiera informacje prawnie chronione do momentu rozpoczcia egzaminu. WPISUJE ZDAJCY PESEL Miejsce na naklejk z kodem dysleksja EGZAMIN
Podstawy termodynamiki
 Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
n p 2 i = R 2 (8.1) i=1
 8.9 Rozkład Maxwella Jest to rozkład prędkości cząstek w gazie doskonałym. Wielkość f (p) jest gęstością prawdopodobieństwa znalezienia cząstki o pędzie p. Różnica pomiędzy rozkładem Maxwella i rozkładem
8.9 Rozkład Maxwella Jest to rozkład prędkości cząstek w gazie doskonałym. Wielkość f (p) jest gęstością prawdopodobieństwa znalezienia cząstki o pędzie p. Różnica pomiędzy rozkładem Maxwella i rozkładem
1. Wspó czynnik absorpcji materia u zale y od d ugo ci fali wiat a w nast puj cy sposób:
 Wstp do Optyki i Fizyki Materii Skondensowanej Zadania domowe 1/11 Jakiej dugoci fale wietlne s cakowicie odbijane od metalowego lustra? Zaoy, e atomy uoone s w prost sie kubiczn o staej a =.4 nm i kady
Wstp do Optyki i Fizyki Materii Skondensowanej Zadania domowe 1/11 Jakiej dugoci fale wietlne s cakowicie odbijane od metalowego lustra? Zaoy, e atomy uoone s w prost sie kubiczn o staej a =.4 nm i kady
Termodynamika. Energia wewnętrzna ciał
 ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
Cia!a sta!e. W!asno"ci elektryczne cia! sta!ych. Inne w!asno"ci
 Cia!a sta!e Podstawowe w!asno"ci cia! sta!ych Struktura cia! sta!ych Przewodnictwo elektryczne teoria Drudego Poziomy energetyczne w krysztale: struktura pasmowa Metale: poziom Fermiego, potencja! kontaktowy
Cia!a sta!e Podstawowe w!asno"ci cia! sta!ych Struktura cia! sta!ych Przewodnictwo elektryczne teoria Drudego Poziomy energetyczne w krysztale: struktura pasmowa Metale: poziom Fermiego, potencja! kontaktowy
Wykład 4, 5 i 6. Elementy rachunku prawdopodobieństwa i kombinatoryki w fizyce statystycznej
 Wykład 4, 5 i 6 Elementy rachunku prawdopodobieństwa i kombinatoryki w fizyce statystycznej dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak
Wykład 4, 5 i 6 Elementy rachunku prawdopodobieństwa i kombinatoryki w fizyce statystycznej dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak
Wykład FIZYKA I. 14. Termodynamika fenomenologiczna cz.ii. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
Wielki rozkład kanoniczny
 , granica termodynamiczna i przejścia fazowe Instytut Fizyki 2015 Podukład otwarty Podukład otwarty S opisywany układ + rezerwuar R Podukład otwarty S opisywany układ + rezerwuar R układ S + R jest izolowany
, granica termodynamiczna i przejścia fazowe Instytut Fizyki 2015 Podukład otwarty Podukład otwarty S opisywany układ + rezerwuar R Podukład otwarty S opisywany układ + rezerwuar R układ S + R jest izolowany
1 Rachunek prawdopodobieństwa
 1 Rachunek prawdopodobieństwa 1. Obliczyć średnią i wariancję rozkładu Bernouliego 2. Wykonać przejście graniczne p 0, N w rozkładzie Bernouliego przy zachowaniu stałej wartości średniej: λ = N p = const
1 Rachunek prawdopodobieństwa 1. Obliczyć średnią i wariancję rozkładu Bernouliego 2. Wykonać przejście graniczne p 0, N w rozkładzie Bernouliego przy zachowaniu stałej wartości średniej: λ = N p = const
FIZYKA STATYSTYCZNA. Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych
 FIZYKA STATYSTYCZA Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych elementów takich jak atomy czy cząsteczki. Badanie ruchów pojedynczych cząstek byłoby bardzo trudnym
FIZYKA STATYSTYCZA Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych elementów takich jak atomy czy cząsteczki. Badanie ruchów pojedynczych cząstek byłoby bardzo trudnym
Fizykochemiczne podstawy inżynierii procesowej
 Fizykochemiczne podstawy inżynierii procesowej Wykład I - 1 Sprawy formalne 2 Fizykochemiczne podstawy inżynierii procesowej Sprawy formalne: Forma: Wykład w postaci prezentacji komputerowych Przeznaczenie:
Fizykochemiczne podstawy inżynierii procesowej Wykład I - 1 Sprawy formalne 2 Fizykochemiczne podstawy inżynierii procesowej Sprawy formalne: Forma: Wykład w postaci prezentacji komputerowych Przeznaczenie:
Planowanie adresacji IP dla przedsibiorstwa.
 Planowanie adresacji IP dla przedsibiorstwa. Wstp Przy podejciu do planowania adresacji IP moemy spotka si z 2 głównymi przypadkami: planowanie za pomoc adresów sieci prywatnej przypadek, w którym jeeli
Planowanie adresacji IP dla przedsibiorstwa. Wstp Przy podejciu do planowania adresacji IP moemy spotka si z 2 głównymi przypadkami: planowanie za pomoc adresów sieci prywatnej przypadek, w którym jeeli
OCENIANIE ARKUSZA POZIOM ROZSZERZONY
 Numer zadania... Etapy rozwizania zadania Przeksztacenie wzoru funkcji do danej postaci f ( x) lub f ( x) x x. I sposób rozwizania podpunktu b). Zapisanie wzoru funkcji w postaci sumy OCENIANIE ARKUSZA
Numer zadania... Etapy rozwizania zadania Przeksztacenie wzoru funkcji do danej postaci f ( x) lub f ( x) x x. I sposób rozwizania podpunktu b). Zapisanie wzoru funkcji w postaci sumy OCENIANIE ARKUSZA
TERMODYNAMIKA I FIZYKA STATYSTYCZNA
 TERMODYNAMIKA I FIZYKA STATYSTYCZNA Lech Longa pok. D.2.49, II piętro, sektor D Zakład Fizyki Statystycznej e-mail: lech.longa@uj.edu.pl Dyżury: poniedziałki 14-15.50 można się umówić wysyłając e-maila
TERMODYNAMIKA I FIZYKA STATYSTYCZNA Lech Longa pok. D.2.49, II piętro, sektor D Zakład Fizyki Statystycznej e-mail: lech.longa@uj.edu.pl Dyżury: poniedziałki 14-15.50 można się umówić wysyłając e-maila
Wykład 12. Rozkład wielki kanoniczny i statystyki kwantowe
 Wykład 12 Rozkład wielki kanoniczny i statystyki kwantowe dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy
Wykład 12 Rozkład wielki kanoniczny i statystyki kwantowe dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy
WYKŁAD 15. Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego
 WYKŁAD 15 Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego 1 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bosony
WYKŁAD 15 Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego 1 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bosony
Przegląd termodynamiki II
 Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
Wykład FIZYKA I. 15. Termodynamika statystyczna. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 15. Termodynamika statystyczna Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html TERMODYNAMIKA KLASYCZNA I TEORIA
Wykład FIZYKA I 15. Termodynamika statystyczna Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html TERMODYNAMIKA KLASYCZNA I TEORIA
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Termodynamika. Cel. Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa. William Thomson 1. Baron Kelvin
 Cel Termodynamika Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa Nicolas Léonard Sadi Carnot 1796 1832 Rudolf Clausius 1822 1888 William Thomson 1. Baron Kelvin 1824 1907 i inni...
Cel Termodynamika Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa Nicolas Léonard Sadi Carnot 1796 1832 Rudolf Clausius 1822 1888 William Thomson 1. Baron Kelvin 1824 1907 i inni...
Termodynamika Część 3
 Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
Fizyka statystyczna i termodynamika Wykład 1: Wstęp. Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej
 Fizyka statystyczna i termodynamika Wykład 1: Wstęp Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej http://www.if.pwr.wroc.pl/~katarzynaweron/ Mój plan zajęć Strona kursu Kim jestem? Prof. dr hab. Katarzyna
Fizyka statystyczna i termodynamika Wykład 1: Wstęp Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej http://www.if.pwr.wroc.pl/~katarzynaweron/ Mój plan zajęć Strona kursu Kim jestem? Prof. dr hab. Katarzyna
Entropia, demon Maxwella i maszyna Turinga
 Entropia, demon Maxwella i maszyna Turinga P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 14 lutego 2013 Pojęcia z dwu różnych dyscyplin Fizyka Informatyka Demon Maxwella Maszyna Turinga podstawy termodynamiki
Entropia, demon Maxwella i maszyna Turinga P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 14 lutego 2013 Pojęcia z dwu różnych dyscyplin Fizyka Informatyka Demon Maxwella Maszyna Turinga podstawy termodynamiki
Zespó kanoniczny W licznych uk adach fizycznych nastepuje wymiana ciep a z otoczeniem.
 Zespó kanoniczny W licznych uk adach fizycznych nastepuje wymiana ciep a z otoczeniem. Wyk ad W0 Niech b dzie dany uk ad izolowany tj. opisany zespo em mikrokanonicznym Gibbsa: prawdopodobie stwo mikrostanów
Zespó kanoniczny W licznych uk adach fizycznych nastepuje wymiana ciep a z otoczeniem. Wyk ad W0 Niech b dzie dany uk ad izolowany tj. opisany zespo em mikrokanonicznym Gibbsa: prawdopodobie stwo mikrostanów
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Fizyka statystyczna Zasady Termodynamiki. P. F. Góra
 Fizyka statystyczna Zasady Termodynamiki P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Stan układu Fizyka statystyczna (i termodynamika) zajmuje się przede wszystkim układami dużymi, liczacymi sobie
Fizyka statystyczna Zasady Termodynamiki P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Stan układu Fizyka statystyczna (i termodynamika) zajmuje się przede wszystkim układami dużymi, liczacymi sobie
17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 17 KLASYCZNA DYNAMIKA MOLEKULARNA 17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek Rozważamy układ N punktowych cząstek
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 17 KLASYCZNA DYNAMIKA MOLEKULARNA 17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek Rozważamy układ N punktowych cząstek
Elementy pneumatyczne
 POLITECHNIKA LSKA W GLIWICACH WYDZIAŁ INYNIERII RODOWISKA i ENERGETYKI INSTYTUT MASZYN i URZDZE ENERGETYCZNYCH Elementy pneumatyczne Laboratorium automatyki (A 3) Opracował: dr in. Jacek Łyczko Sprawdził:
POLITECHNIKA LSKA W GLIWICACH WYDZIAŁ INYNIERII RODOWISKA i ENERGETYKI INSTYTUT MASZYN i URZDZE ENERGETYCZNYCH Elementy pneumatyczne Laboratorium automatyki (A 3) Opracował: dr in. Jacek Łyczko Sprawdził:
Teoria kinetyczna gazów
 Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
Fizyka statystyczna Zerowa Zasada Termodynamiki. P. F. Góra
 Fizyka statystyczna Zerowa Zasada Termodynamiki P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Stan układu Fizyka statystyczna (i termodynamika) zajmuje się przede wszystkim układami dużymi, liczacymi
Fizyka statystyczna Zerowa Zasada Termodynamiki P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Stan układu Fizyka statystyczna (i termodynamika) zajmuje się przede wszystkim układami dużymi, liczacymi
Termodynamika (1) Bogdan Walkowiak. Zakład Biofizyki Instytut Inżynierii Materiałowej Politechnika Łódzka. poniedziałek, 23 października 2017
 Wykład 1 Termodynamika (1) Bogdan Walkowiak Zakład Biofizyki Instytut Inżynierii Materiałowej Politechnika Łódzka Biofizyka 1 Zaliczenie Aby zaliczyć przedmiot należy: uzyskać pozytywną ocenę z laboratorium
Wykład 1 Termodynamika (1) Bogdan Walkowiak Zakład Biofizyki Instytut Inżynierii Materiałowej Politechnika Łódzka Biofizyka 1 Zaliczenie Aby zaliczyć przedmiot należy: uzyskać pozytywną ocenę z laboratorium
Agata Fronczak Elementy fizyki statystycznej
 Agata Fronczak Elementy fizyki statystycznej Skrypt do wykładu i ćwiczeń rachunkowych dla kierunku Fotonika (rok III, semestr 5) na Wydziale Fizyki PW Warszawa 2016 Spis treści 1. Termodynamika klasyczna,
Agata Fronczak Elementy fizyki statystycznej Skrypt do wykładu i ćwiczeń rachunkowych dla kierunku Fotonika (rok III, semestr 5) na Wydziale Fizyki PW Warszawa 2016 Spis treści 1. Termodynamika klasyczna,
Ekonometria - wykªad 8
 Ekonometria - wykªad 8 3.1 Specykacja i werykacja modelu liniowego dobór zmiennych obja±niaj cych - cz ± 1 Barbara Jasiulis-Goªdyn 11.04.2014, 25.04.2014 2013/2014 Wprowadzenie Ideologia Y zmienna obja±niana
Ekonometria - wykªad 8 3.1 Specykacja i werykacja modelu liniowego dobór zmiennych obja±niaj cych - cz ± 1 Barbara Jasiulis-Goªdyn 11.04.2014, 25.04.2014 2013/2014 Wprowadzenie Ideologia Y zmienna obja±niana
Zasady termodynamiki
 Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Termodynamika program wykładu
 Termodynamika program wykładu Wiadomości wstępne: fizyka statystyczna a termodynamika masa i rozmiary cząstek stan układu, przemiany energia wewnętrzna pierwsza zasada termodynamiki praca wykonana przez
Termodynamika program wykładu Wiadomości wstępne: fizyka statystyczna a termodynamika masa i rozmiary cząstek stan układu, przemiany energia wewnętrzna pierwsza zasada termodynamiki praca wykonana przez
Wykład FIZYKA I. 5. Energia, praca, moc. http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 5. Energia, praca, moc Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html ENERGIA, PRACA, MOC Siła to wielkość
Wykład FIZYKA I 5. Energia, praca, moc Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html ENERGIA, PRACA, MOC Siła to wielkość
Układ termodynamiczny Parametry układu termodynamicznego Proces termodynamiczny Układ izolowany Układ zamknięty Stan równowagi termodynamicznej
 termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
MATERIAŁ WICZENIOWY Z MATEMATYKI
 Miejsce na naklejk POZNA MATERIAŁ WICZENIOWY Z MATEMATYKI STYCZE 010 POZIOM PODSTAWOWY Czas pracy 170 minut Instrukcja dla zdajcego 1. Sprawd, czy arkusz zawiera 16 stron (zadania 1 9). Ewentualny brak
Miejsce na naklejk POZNA MATERIAŁ WICZENIOWY Z MATEMATYKI STYCZE 010 POZIOM PODSTAWOWY Czas pracy 170 minut Instrukcja dla zdajcego 1. Sprawd, czy arkusz zawiera 16 stron (zadania 1 9). Ewentualny brak
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
EGZAMIN MATURALNY Z MATEMATYKI
 Miejsce na naklejk z kodem szkoy dysleksja MMA-R1_1P-07 EGZAMIN MATURALNY Z MATEMATYKI POZIOM ROZSZERZONY Czas pracy 180 minut Instrukcja dla zdajcego 1. Sprawd, czy arkusz egzaminacyjny zawiera 15 stron
Miejsce na naklejk z kodem szkoy dysleksja MMA-R1_1P-07 EGZAMIN MATURALNY Z MATEMATYKI POZIOM ROZSZERZONY Czas pracy 180 minut Instrukcja dla zdajcego 1. Sprawd, czy arkusz egzaminacyjny zawiera 15 stron
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów
 Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1. Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski
 Chemia Fizyczna Technologia Chemiczna II rok Wykład 1 Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski Kontakt,informacja i konsultacje Chemia A ; pokój 307 Telefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1 Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski Kontakt,informacja i konsultacje Chemia A ; pokój 307 Telefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl
TERMODYNAMIKA I TERMOCHEMIA
 TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
Problem decyzyjny naley do klasy NP. (Polynomial), jeeli moe by rozwizany w czasie conajwyej wielomianowym przez algorytm A dla DTM.
 WYKŁAD : Teoria NP-zupełnoci. Problem decyzyjny naley do klasy P (Polynomial), jeeli moe by rozwizany w czasie conajwyej wielomianowym przez algorytm A dla DTM. (przynaleno ta jest zachowana równie dla
WYKŁAD : Teoria NP-zupełnoci. Problem decyzyjny naley do klasy P (Polynomial), jeeli moe by rozwizany w czasie conajwyej wielomianowym przez algorytm A dla DTM. (przynaleno ta jest zachowana równie dla
Podstawy fizyki sezon 1 X. Elementy termodynamiki
 Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
Enzymologia I. Kinetyka - program Gepasi. Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu
 Enzymologia I Kinetyka - program Gepasi Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu I zasada + II zasada termodynamiki zmiana entalpii i entropii może zostać wyrażona ilościowo
Enzymologia I Kinetyka - program Gepasi Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu I zasada + II zasada termodynamiki zmiana entalpii i entropii może zostać wyrażona ilościowo
Wykład 2. Przykład zastosowania teorii prawdopodobieństwa: procesy stochastyczne (Markova)
 Wykład 2 Przykład zastosowania teorii prawdopodobieństwa: procesy stochastyczne (Markova) 1. Procesy Markova: definicja 2. Równanie Chapmana-Kołmogorowa-Smoluchowskiego 3. Przykład dyfuzji w kapilarze
Wykład 2 Przykład zastosowania teorii prawdopodobieństwa: procesy stochastyczne (Markova) 1. Procesy Markova: definicja 2. Równanie Chapmana-Kołmogorowa-Smoluchowskiego 3. Przykład dyfuzji w kapilarze
Miejsce biofizyki we współczesnej nauce. Obszary zainteresowania biofizyki. - Powrót do współczesności. - obiekty mikroświata.
 Zakład Biofizyki Miejsce biofizyki we współczesnej nauce - trochę historii - Powrót do współczesności Obszary zainteresowania biofizyki - ekosystemy - obiekty makroświata - obiekty mikroświata - język
Zakład Biofizyki Miejsce biofizyki we współczesnej nauce - trochę historii - Powrót do współczesności Obszary zainteresowania biofizyki - ekosystemy - obiekty makroświata - obiekty mikroświata - język
Sposoby przekazywania parametrów w metodach.
 Temat: Definiowanie i wywoływanie metod. Zmienne lokalne w metodach. Sposoby przekazywania parametrów w metodach. Pojcia klasy i obiektu wprowadzenie. 1. Definiowanie i wywoływanie metod W dotychczas omawianych
Temat: Definiowanie i wywoływanie metod. Zmienne lokalne w metodach. Sposoby przekazywania parametrów w metodach. Pojcia klasy i obiektu wprowadzenie. 1. Definiowanie i wywoływanie metod W dotychczas omawianych
Wstp. Warto przepływu to
 177 Maksymalny przepływ Załoenia: sie przepływow (np. przepływ cieczy, prdu, danych w sieci itp.) bdziemy modelowa za pomoc grafów skierowanych łuki grafu odpowiadaj kanałom wierzchołki to miejsca połcze
177 Maksymalny przepływ Załoenia: sie przepływow (np. przepływ cieczy, prdu, danych w sieci itp.) bdziemy modelowa za pomoc grafów skierowanych łuki grafu odpowiadaj kanałom wierzchołki to miejsca połcze
I piętro p. 131 A, 138
 CHEMIA NIEORGANICZNA Dr hab. Andrzej Kotarba Zakład Chemii Nieorganicznej Wydział Chemii I piętro p. 131 A, 138 WYKŁAD - 4 RÓWNOWAGA Termochemia i termodynamika funkcje termodynamiczne, prawa termodynamiki,
CHEMIA NIEORGANICZNA Dr hab. Andrzej Kotarba Zakład Chemii Nieorganicznej Wydział Chemii I piętro p. 131 A, 138 WYKŁAD - 4 RÓWNOWAGA Termochemia i termodynamika funkcje termodynamiczne, prawa termodynamiki,
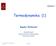
Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }
![Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] } Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }](/thumbs/64/51033976.jpg) Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
ZMIENNE LOSOWE. Zmienna losowa (ZL) X( ) jest funkcją przekształcającą przestrzeń zdarzeń elementarnych w zbiór liczb rzeczywistych R 1 tzn. X: R 1.
 Opracowała: Joanna Kisielińska ZMIENNE LOSOWE Zmienna losowa (ZL) X( ) jest funkcją przekształcającą przestrzeń zdarzeń elementarnych w zbiór liczb rzeczywistych R tzn. X: R. Realizacją zmiennej losowej
Opracowała: Joanna Kisielińska ZMIENNE LOSOWE Zmienna losowa (ZL) X( ) jest funkcją przekształcającą przestrzeń zdarzeń elementarnych w zbiór liczb rzeczywistych R tzn. X: R. Realizacją zmiennej losowej
Karta punktowania egzaminu do kursu Fizyka 1 dla studentów Wydziału Inż. Śr., kier. Inż. Śr. oraz WPPT IB. Zagadnienie 1.
 Karta punktowania egzaminu do kursu Fizyka 1 dla studentów Wydziału Inż. Śr., kier. Inż. Śr. oraz WPPT IB. Zagadnienie 1. 3 PKT. Wzorcowa odpowiedź ad I zasada zaczerpnięta z podręcznika HRW lub równoważna
Karta punktowania egzaminu do kursu Fizyka 1 dla studentów Wydziału Inż. Śr., kier. Inż. Śr. oraz WPPT IB. Zagadnienie 1. 3 PKT. Wzorcowa odpowiedź ad I zasada zaczerpnięta z podręcznika HRW lub równoważna
Rozkłady zmiennych losowych
 Rozkłady zmiennych losowych Wprowadzenie Badamy pewną zbiorowość czyli populację pod względem występowania jakiejś cechy. Pobieramy próbę i na podstawie tej próby wyznaczamy pewne charakterystyki. Jeśli
Rozkłady zmiennych losowych Wprowadzenie Badamy pewną zbiorowość czyli populację pod względem występowania jakiejś cechy. Pobieramy próbę i na podstawie tej próby wyznaczamy pewne charakterystyki. Jeśli
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
TERMODYNAMIKA I FIZYKA STATYSTYCZNA
 TERMODYNAMIKA I FIZYKA STATYSTYCZNA Lech Longa pok. D.2.49, II piętro, sektor D Zakład Fizyki Statystycznej e-mail: lech.longa@uj.edu.pl Dyżury: poniedziałki 13-14 można się umówić wysyłając e-maila 1
TERMODYNAMIKA I FIZYKA STATYSTYCZNA Lech Longa pok. D.2.49, II piętro, sektor D Zakład Fizyki Statystycznej e-mail: lech.longa@uj.edu.pl Dyżury: poniedziałki 13-14 można się umówić wysyłając e-maila 1
Wstęp do Fizyki Statystycznej
 Wstęp do Fizyki Statystycznej Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 października 2016 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 października 2016
Wstęp do Fizyki Statystycznej Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 października 2016 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 października 2016
Wykład 3. Zerowa i pierwsza zasada termodynamiki:
 Wykład 3 Zerowa i pierwsza zasada termodynamiki: Termodynamiczne funkcje stanu. Parametry extensywne i intensywne. Pojęcie równowagi termodynamicznej. Tranzytywność stanu równowagi i pojęcie temperatury
Wykład 3 Zerowa i pierwsza zasada termodynamiki: Termodynamiczne funkcje stanu. Parametry extensywne i intensywne. Pojęcie równowagi termodynamicznej. Tranzytywność stanu równowagi i pojęcie temperatury
Weryfikacja hipotez statystycznych
 Weryfikacja hipotez statystycznych Hipoteza Test statystyczny Poziom istotności Testy jednostronne i dwustronne Testowanie równości wariancji test F-Fishera Testowanie równości wartości średnich test t-studenta
Weryfikacja hipotez statystycznych Hipoteza Test statystyczny Poziom istotności Testy jednostronne i dwustronne Testowanie równości wariancji test F-Fishera Testowanie równości wartości średnich test t-studenta
In»ynierskie zastosowania statystyki wiczenia
 Uwagi: 27012014 poprawiono kilka literówek, zwi zanych z przedziaªami ufno±ci dla wariancji i odchylenia standardowego In»ynierskie zastosowania statystyki wiczenia Przedziaªy wiarygodno±ci, testowanie
Uwagi: 27012014 poprawiono kilka literówek, zwi zanych z przedziaªami ufno±ci dla wariancji i odchylenia standardowego In»ynierskie zastosowania statystyki wiczenia Przedziaªy wiarygodno±ci, testowanie
