Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
|
|
|
- Maja Elżbieta Adamska
- 4 lat temu
- Przeglądów:
Transkrypt
1 Równowag fazowe Zakład Chem Medycznej Pomorsk Unwersytet Medyczny
2 Równowaga termodynamczna Przemanom fazowym towarzyszą procesy, podczas których ne zmena sę skład chemczny układu, polegają one na zmane stanu skupena dotyczą układów prostych jednoskładnkowych, jak bardzej złożonych weloskładnkowych. Układ znajdujący sę w warunkach stałego cśnena stałej temperatury dąży do zmnejszena jego potencjału termodynamcznego. Za termodynamczne trwały stan skupena danej substancj przyjmuje sę stan, w którym w danych warunkach cśnena, temperatury składu, wartość jej potencjału termodynamcznego jest najmnejsza.
3 SUBSTANCJE CZYSTE
4 SUBSTANCJE CZYSTE
5 RÓWNOWAGI FAZOWE Fazą danej substancj nazywamy postać mater która charakteryzuje sę jednorodnym składem chemcznym stanem fzycznym. Przemana fazowa to samorzutna przemana jednej fazy w drugą, dla danego cśnena zachodz w charakterystycznej temperaturze. Temperatura przejśca fazowego T p.f. odpowada temperaturze, w której potencjały chemczne obu faz są sobe równe, a fazy znajdują sę w równowadze pod danym cśnenem. Fazy metastablne to fazy netrwałe termodynamczne, które stneją dzęk temu, ż przemana jest zahamowana knetyczne. Schematyczna zależność potencjału chemcznego fazy stałej, cekłej gazowej substancj od temperatury.
6 RÓWNOWAGI FAZOWE Dagram fazowy substancj pokazuje obszar cśnena temperatury, w których różne jej fazy są termodynamczne trwałe. Lne równowag faz to grance pomędzy obszaram, określają wartośc p T, dla których dwe fazy współstneją ze sobą w równowadze. Prężność par substancj występuje gdy cśnene gazu jest w stane równowag z fazą cekłą w danej temperaturze. Punkt potrójny zbór warunków, w których trzy różne fazy współstneją w równowadze - spotykają sę trzy lne równowag faz. Ogólny schemat dagramu fazowego przedstawający obszary trwałośc cała stałego, ceczy gazu.
7 RÓWNOWAGI FAZOWE Prężność pary Wrzene to proces swobodnego parowana zachodzący w całej objętośc ceczy. Cecz lub cało stałe Temperatura wrzena w danym cśnenu to temperatura, w której prężność pary ceczy równa jest cśnenu zewnętrznemu. Jeśl wynos ono 1 atm, temp. wrzena nazywamy normalną temperaturą wrzena lub normalnym punktem wrzena. Jeśl cśnene zew. wyrażone jest jako 1 bar, wówczas mówmy o standardowej temp.wrzena. Temperatura krytyczna T kr to temperatura, w której powerzchna granczna znka. Prężność pary w temp. krytycznej nos nazwę cśnena krytycznego p kr W temp. krytycznej powyżej nej naczyne wypełna pojedyncza jednorodna faza zwana płynem nadkrytycznym. Prężność pary ceczy lub cała stałego odpowada cśnenu wyweranemu przez gaz znajdujący sę w równowadze z fazą skondensowaną.
8 RÓWNOWAGI FAZOWE Temperatura topnena T t to temperatura, w której pod danym cśnenem cecz cało stałe współstneją ze sobą w równowadze. Jeśl cśnene wynos 1 atm, mówmy o normalnej temperaturze topnena. Jeśl cśnene wynos 1 bar- standardowej temperaturze topnena. Substancje topą sę w tej samej temperaturze, w której krzepną, temperatura topnena substancj jest taka sama jak ch temperatury krzepnęca.
9 RÓWNOWAGI FAZOWE Przemany fazowe wg Ehrenfesta: 1. Perwszego rodzaju: - perwsze pochodne potencjału chemcznego względem cśnena temperatury wykazują necągłość w punkce przemany - dla neskończene małych zman temperatury, zmana entalp jest skończona - neskończona pojemność ceplna w temperaturze przemany - dostarczone cepło zużywane jest na przeprowadzene samej przemany, a ne na podnesene temperatury układu 2. Drugego rodzaju: - perwsza pochodna potencjału chemcznego względem temperatury jest cągła, natomast necągła jest druga pochodna - cągłe nachylene µ, oznacza że objętość entropa w trakce przemany fazowej ne zmenają sę - pojemność ceplna jest necągła, ale ne neskończona 3. Przejśce λ - stosuje sę do przeman fazowych, które ne są perwszego rodzaju, ale dla których pojemność ceplna staje sę neskończona w temperaturze przemany
10 RÓWNOWAGI FAZOWE
11 RÓWNOWAGI FAZOWE Temperatura topnena T t to temperatura, w której pod danym cśnenem cecz cało stałe współstneją ze sobą w równowadze. Jeśl cśnene wynos 1 atm, mówmy o normalnej temperaturze topnena. Jeśl cśnene wynos 1 bar- standardowej temperaturze topnena. Substancje topą sę w tej samej temperaturze, w której krzepną, temperatura topnena substancj jest taka sama jak ch temperatury krzepnęca. Układ cecz- para
12 RÓWNOWAGI FAZOWE Wpływ wzrostu cśnena na wartośc potencjałów chemcznych fazy stałej cekłej oraz zwązaną z nm temperaturę topnena. Molowa objętość fazy stałej jest mnejsza nż cekłej µ(s) rośne słabej nż µ(c), w wynku czego temperatura krzepnęca sę podwyższa. Molowa objętość fazy stałej jest wększa nż cekłej, zatem µ(s) rośne slnej nż µ(c), a temperatura krzepnęca sę obnża.
13 RÓWNOWAGI FAZOWE Wpływ cśnena na prężność pary Cząstkowe cśnene pary danej substancj, to cśnene cząstkowe pary w warunkach równowag z fazą skondensowaną. Solwatacja gazu to przyłączene cząsteczek ceczy do cząsteczek fazy gazowej. Cśnene na fazę skondensowaną można wywerać przez: a) ścskane fazy skondensowanej b) Poddając ją dzałanu sprężonego gazu obojętnego.
14 RÓWNOWAGI FAZOWE Cepło przemany fazowej. Występującym w układach przemanom fazowym towarzyszą zmany funkcj termodynamcznych. Warunkem równowag zotermczno-zobarycznej mędzy dwoma fazam w układze jednoskładnkowym jest równość molowych potencjałów termodynamcznych składnka w obu fazach. Jeżel na układ będący w równowadze z otoczenem podzała czynnk zewnętrzny zwększy sę temperatura układu, to nastąp równeż zmana cśnena zwązana z tym zmana molowych entalp swobodnych obu faz.
15 RÓWNOWAGI FAZOWE Cepło przemany fazowej wybranych substancj Substancja Temp. Wrzena [K] Molowe cepło parowana [kj/ mol] Temp.topnena [K] aceton 329,1 29,1 177,8 5,7 argon 87,3 6, ,2 amonak 239,7 23,4 195,3 5,6 etanol 351,5 43,5 158,7 4,6 rtęć 629,7 59,3 234,3 2,3 woda 373,2 40,7 273,2 6,0 Molowe cepło topnena [kj/mol] Molowe cepło parowana jest dużo wększe nż molowe cepło topnena. Cząsteczk substancj, aby przejść w stan pary muszą być całkowce od sebe oddzelone. W procese topnena wązana mędzycząsteczkowe są jedyne rozluźnone wymaga to w porównanu z procesem parowana znaczne mnejszej energ.
16 RÓWNOWAGI FAZOWE 1. Zaburzene stanu równowag poprzez zwększene cśnena dp 2. Przywrócene stanu równowag poprzez wzrost temperatury dt 3. Układ pozostaje w równowadze, gdy jeden z parametrów dp lub dt ulegne zmane
17 RÓWNANIE CLAPEYRONA-CLAUSIUSACLAUSIUSA Równane Clapyerona-Claususa dotyczy dowolnej przemany fazowej w układze jednoskładnkowym, np. przejśca ceczy w parę, cała stałego w cecz lub cała stałego w parę. Z równana można oblczyć:- molowe cepło przemany - temperaturę przemany - zmany cśnena
18 RÓWNANIE CLAPEYRONA-CLAUSIUSACLAUSIUSA Równane Clapeyrona- Claususa dp / dt = Δ p.f. S / Δ p.f. V Δ p.f Δ p.f oznaczają odpowedno zmany molowych entrop objętośc, jake towarzyszą przemane Równane Clapeyrona jest równanem ścsłym, opsującym nachylene ln równowag, stosuje sę go do każdej równowag fazowej dowolnej substancj czystej. Grafczna lustracja równana Claususa- Clapeyrona na przykładze wody (objętość molowa lodu > objętość molowa ceczy)
19 RÓWNANIE CLAPEYRONA Potencjał chemczny określony jest jako dµ= -S m dt + V m dp poneważ dµ α = dµ β węc, dla każdej fazy możemy zapsać -S α,m dt + V α, m dp = -S β, m dt + V β, m dp gdze: S α,m S β, m są molową entropą danej fazy stąd V α, m V β, m to objętośc molowe (V β,m V α,m ) dp = (S β,m S α,m )dt Otrzymujemy równane Clapeyrona dp / dt = Δ p.f. S / Δ p.f. V Δ p.f Δ p.f oznaczają odpowedno zmany molowych entrop objętośc, jake towarzyszą przemane Równane Clapeyrona jest równanem ścsłym, opsującym nachylene ln równowag, stosuje sę go do każdej równowag fazowej dowolnej substancj czystej.
20 REGUŁA FAZ GIBBSA Układ weloskładnkowy znajduje sę w równowadze wówczas, gdy potencjały chemczne każdego składnka osobno, we wszystkch fazach będą równe. Gbbs wyprowadzł w 1876 r. regułę faz, będącą zależnoścą mędzy lczbą zmennych nezależnych (temp., cśnene, stężene), a lczbą faz (stała, cekła, gazowa) występującą w układze znajdującym sę w równowadze, zawerającym określoną lczbę składnków. Reguła ta podaje ogólny zwązek pomędzy lczbą stopn swobody F, lczbą składnków nezależnych C oraz lczbą faz P dla układów o dowolnym składze w stane równowag F = C P + 2
21 RÓWNOWAGI FAZOWE Lczba składnków to najmnejsza lczba nezależnych substancj nezbędnych do opsana składu wszystkch faz układu znajdującego sę w stane równowag. Np.: meszanna trójfazowa lodu, wody pary wodnej wynos 1, poneważ skład wszystkch trzech faz jest określony przez substancję chemczną H2O Lczba stopn swobody to lczba ntensywnych parametrów opsujących stan układu, nezależnych od masy układu (temperatura, cśnene, stężene, gęstość, lepkość tp.), które można nezależne zmenać bez naruszena stanu równowag fazowej (zanku lub tworzena sę nowych faz).
22 RÓWNOWAGI FAZOWE Np.: układ jednofazowy jednoskładnkowy para wodna, lczba stopn swobody wynos 2 (S=1-1+2=2) 2 parametry np. cśnene temperatura mogą być zmenane nezależne. Układ stanow woda (cecz) w równowadze z parą wodną to jest to układ dwufazowy; lczba stopn swobody wynos 1 (S= 1-2+2=1), oznacza to, że cśnene ne może być dowolne zmenane w tym układze, jeśl równocześne chce sę zmenć temperaturę układu. Zmana cśnena mus być połączona z określoną zmaną temperatury. Układ, w którym w równowadze znajdują sę 3 fazy: woda, para wodna lód; lczba stopn swobody wynos 0 (S=1-3+2=0); układ może występować wyłączne przy jednej, ścśle określonej, wartośc temperatury cśnena.
23 REGUŁA FAZ GIBBSA Wzrost lczby składnków w układze zwększa lczbę stopn swobody. Obszary dagramu fazowego dla układu jednoskładnkowego: -lne określają warunk, w jakch fazy pozostają w równowadze. -punkty określają jedyny zestaw warunków, w których trzy fazy współstneją ze sobą w stane równowag. -cztery fazy ne mogą współstneć w równowadze.
24 UKŁADY JEDNOSKŁADNIKOWE Przemany fazowe w układach jednoskładnkowych Schematyczna zależność cśnena od temperatury dla fazy stałej, cekłej gazowej substancj.
25 UKŁADY JEDNOSKŁADNIKOWE Równowaga cecz-cało stałe
26 RÓWNOWAGI FAZOWE Lna równowag cało stałe cecz: 1. Begne stromo w górę 2. Wzrost cśnena powoduje wzrost temperatury topnena 3. Wększość substancj zachowuje sę w tak sposób Lna równowag cecz gaz: 1. Wykres prężnośc pary od temperatury 2. Lna równowag wykazuje odwrotną krzywznę 3. Lna granczna kończy sę w punkce krytycznym
27 RÓWNOWAGI FAZOWE Lna granczna cało stałe gaz: 1. Punkt potrójny 2. Lna cało stałe- gaz ma wększe nachylene nż cecz gaz 3. Entalpa sublmacj jest wększa od entalp parowana 4. Wartośc temperatury w równanu opsującym nachylene są podobne
28 UKŁADY JEDNOSKŁADNIKOWE 1. Tylko jedna faza F = 2 - można zmenać nezależne p T ne powodując zmany lczby faz - pojedyncza faza na dagrame to cała powerzchna 2. Dwe fazy w równowadze F = 1 - przy ustalonej temperaturze ne można zmenć cśnena w dowolny sposób - jeśl ustalmy cśnene zamast temperatury, to w określonej temperaturze dwe fazy są w równowadze np. krzepnęce zachodz przy danym cśnenu temperaturze - na dagrame fazowym równowaga dwóch faz określona jest za pomocą ln 3. Trzy fazy w równowadze F = 0 - układ nwarantny - równowagę określa punkt potrójny Dagram fazowy wody: 4. Cztery fazy w równowadze zabronone T 3 temperatura punktu potrójnego T w normalna temperatura wrzena T k normalna temperatura krzepnęca
29 UKŁADY JEDNOSKŁADNIKOWE Krzywa chłodzena dla zobary: a chłodzene próbk pod stałym cśnenem faza gazowa b dwe fazy w równowadze gazowa cekła c jednofazowy obszar ceczy d zachodz egzotermczna przemana fazowa perwszego rodzaju (krzepnęce)
30 ROZTWORY DOSKONAŁE Roztwory doskonałe to roztwory, których składnk podczas tworzena roztworu jedyne ulegają rozceńczenu, ne zmenając przy tym swoch właścwośc. Przy tworzenu sę takch roztworów ne występuje pochłanane lub uwalnane cepła Całkowta objętość roztworu jest sumą objętośc poszczególnych składnków Roztwory doskonałe tworzą substancje o podobnych właścwoścach np. benzen toluen. Termodynamczne roztwory doskonałe to roztwory, w których potencjał chemczny każdego składnka spełna w całym zakrese stężeń wzór (T, p) = (T, p) + RT lnx 0< x < 1 Roztwór dealne rozceńczony to tak roztwór, który zawerając rozpuszczalnk w dużych stężenach spełna powyższe równane.
31 MIESZANINY GAZÓW Meszannę gazów uważa sę za roztwór doskonały, jeśl: Roztwór gazowy spełna prawo Daltona Meszanu sę gazów ne towarzyszy efekt ceplny (brak poberana wydzelana) PRAWO DALTONA Cśnene wywerane przez meszannę gazów doskonałych jest sumą cśneń wyweranych przez poszczególne gazy zajmujące, każdy z osobna, taką sama objętość, jaką zajmuje meszanna. Prawo to spełna sę wyłączne w przypadku meszanny gazów doskonałych lub gazów rzeczywstych, przy tak nskch cśnenach, że gazy te zachowują sę jak gazy doskonałe.
32 PRAWO DALTONA I zbornk = tlen II zbornk = azot W obu zbornkach jest taka sama objętość taka sama temperatura. Po zmeszanu gazy będą zajmować tą samą objętość w tej samej temperaturze, a cśnene całkowte jake wywrze meszanna gazów będze sumą cśneń ze zbornka I II.
33 PRAWO DALTONA 1. Całkowte cśnene meszanny gazów jest suma cśneń cząstkowych wszystkch występujących w meszanne gazów 2. Cząstkowe cśnene każdego gazu jest równe cśnenu, jake wywerałby ten gaz, jeśl zajmowałby zbornk oddzelne.
34 ROZPUSZCZALNOŚĆ GAZÓW W CIECZACH Dyfuzja proces samorzutnego przemeszczana sę cząstek z przestrzen o stężenu wyższym do przestrzen o stężenu nższym. Szybkość dyfuzj gazów rośne wraz ze wzrostem: temperatury, powerzchn wymany, gradentu stężeń pomędzy gazem nad ceczą w ceczy Szybkość dyfuzj gazów maleje wraz ze wzrostem: wymaru cząsteczek, które są proporcjonalne do masy gazu, lepkośc ceczy, długośc drog dyfuzyjnej 34
35 ROZPUSZCZALNOŚĆ GAZÓW W CIECZACH Rozpuszczalność gazów w ceczy zależy od: rodzaju obu substancj, gazu rozpuszczalnka, podobne rozpuszcza sę w podobnym, reakcj towarzyszących rozpuszczanu temperatury cśnena: PRAWO HENRY EGO Masa gazu rozpuszczonego w określonej objętośc ceczy jest wprost proporcjonalna do cśnena parcjalnego gazu znajdującego sę nad roztworem. ze wzrostem temperatury maleje rozpuszczalność gazów w ceczach 35
36 PRAWO RAOULTA Zdefnowane w 1887 roku, dotyczące cząstkowej prężnośc par każdego składnka meszanny. Prężność pary danego składnka nad roztworem jest równa loczynow prężnośc pary czystego składnka jego ułamka molowego w roztworze. N lczba mol rozpuszczalnka n lczba mol nelotnej substancj rozpuszczonej p o prężność pary nasyconej czystego rozpuszczalnka p prężność pary nad roztworem p o -p = Dp obnżene prężnośc pary Dp/p o względne obnżene prężnośc pary Prawo Raoulta spełnają roztwory doskonałe w całym zakrese stężeń. Roztwory rzeczywste ne spełnają prawa Raoulta.
37 PRAWO RAOULTA - ODCHYLENIA Dodatne odchylena : Jeśl oddzaływana medzy cząsteczkam tej samej substancj A-A B-B przewyższają oddzaływana medzy cząsteczkam dwóch różnych substancj A-B, rzeczywsta prężność pary nad roztworem tych substancj jest wększa nż wynka to z prawa Raoulta. Np.benzen etanol dsarczek węgla aceton chloroform etanol etanol woda metanol aceton azeotropa dodatna Newelke dodatne odchylena od prawa Raoulta
38 PRAWO RAOULTA Ujemne odchylena: Gdy sły oddzaływana medzy cząsteczkam dwóch różnych substancj tego samego rodzaju A-A B-B są mnejsze nż mędzy cząsteczkam dwóch różnych substancj A-B np. aceton chloroform azeotropa ujemna Prężność par nad nemeszającym sę ceczam
39 UKŁADY DWUSKŁADNIKOWE RÓWNOWAGA CIECZ-PARA DLA UKŁADÓW DWUSKŁADNIKOWYCH 1. Aby jednoznaczne określć stan układu potrzeba znać: cśnene, temperaturę skład układu 2. Układ dwuskładnkowy ma najwększą lczbę stopn swobody, gdy ma najmnejszą lczbę faz 3. Stan układu charakteryzuje dagram fazowy o współrzędnych cśnene-skład lub temperatura-skład 4. I PRAWO KONOWAŁŁOWA Para pozostająca w równowadze z roztworem jest bogatsza w ten składnk, którego dodane do roztworu zwększa sumaryczną prężność pary nad nm.
40 UKŁADY DWUSKŁADNIKOWE Zależność całkowtej prężnośc pary roztworu dealnego od ułamka molowego substancj A w układze. Punkty leżące pomędzy lnam odpowadają współstnenu ceczy pary, natomast poza tym obszarem stneje tylko jedna faza. Punkty dagramu cśnene- skład. Lna ponowa przechodząca przez punkt a jest zopletą, czyl lną stałego składu całego układu
41 UKŁADY DWUSKŁADNIKOWE 1. Dwe fazy w równowadze F = 1 dla wszystkch punktów w obszarze dwoma lnam. 2. Dla danego cśnena lczba stopn swobody wynos 0, faza cekła gazowa mają ścśle określone składy. Dagram prężnośc par
42 UKŁAD DWUSKŁADNIKOWE Reguła dźwgn: 1. Określa względne lośc obu faz będących ze sobą w równowadze. 1. Na podstawe odcnków l α l β można wyznaczyć wzajemny stosunek lośc pozostających w równowadze faz α (np.cecz) β (np. para) 2. Reguła dźwgn wąże dwe masy znajdujące sę na obu końcach dźwgn z ch odległoścam od punktu podparca
43 DESTYLACJA MIESZANIN a 1 roztwór perwotny, który wrze w temp. T 2 a 2 - para będąca w równowadze z wrzącą ceczą T 3 - temperatura wrzena ceczy a 3 - para z wrzącej ceczy w temp.t 3 II PRAWO KONOWAŁŁOWA W maksmum lub mnmum temperatury wrzena skład ceczy skład pary są jednakowe. Meszanny o takm składze noszą nazwę azeotropowych.
44 DESTYLACJA MIESZANIN Metoda rozdzału zwana destylacją frakcyjną. Następujące po sobe procesy wrzena kondensacj ceczy o początkowym składze a 1 prowadzą do destylatu, którym jest czysta substancja A. Dagram temperatura skład dla dealnej meszanny, w której składnk A jest bardzej lotny nż B
45 DESTYLACJA MIESZANIN W destylacj frakcyjnej procesy wrzena kondensacj powtarzają sę sukcesywne. Sprawność kolumny rektyfkacyjnej wyraża sę lczbą półek teoretycznych Lczba półek teoretycznych to lczba procesów parowana kondensacj nezbędnych do osągnęca określonego stopna rozdzału dwóch składnków meszanny przykłady odpowadają a) trzem b) pęcu półkom teoretycznym
46 DESTYLACJA MIESZANIN Destylacja z parą wodną destylacja z użycem strumena nasyconej lub przegrzanej pary wodnej, prowadząca do otrzymywana kondensatów dwufazowych (faza wodna organczna), odberanych w temperaturze nższej od temperatury wrzena najnżej wrzącego składnka meszanny (heteroazeotrop).
47 MIESZANINA AZEOTROPOWA AZEOTROP cekła meszanna wykazująca azeotropę, czyl destylująca bez zmany składu, co oznacza, że ne można uzyskać rozdzelena jej na składnk czyste. Meszanna azeotropowa wykazująca maksmum na krzywej wrzena. Gdy cecz o składze a ulega destylacj, jej skład zmena sę, lecz tylko do punktu b, po czym pozostaje nezmenny. Meszanna azeotropowa wykazująca mnmum na krzywej temperatury wrzena. Gdy cecz o składze a ulega destylacj frakcyjnej równowagowy skład pary w kolumne rektyfkacyjnej zmena sę tylko do punktu b, po czym pozostaje nezmenny.
48 UKŁADY DWUSKŁADNIKOWE Cecze częścowo meszające sę Dagram temperatura- skład dla meszanny dwuskładnkowej. Nezależne od składu górna temperatura krytyczna rozpuszczalnośc jest nższa od temperatury wrzena. Meszanna tworzy azeotrop wykazujący mnmum temperatury wrzena. Składnk meszają sę przed osągnęcem Punktu wrzena.
49 UKŁADY DWUSKŁADNIKOWE UKŁAD HEKSAN / NITROBENZEN 1. Punkt o współrzędnych x=0,41 T=290 K leży w obszarze dwufazowym dagramu 2. Pozoma lna konugacj przecna lnę granczną faz w x= 0,35 x= 0,83 3. Stosunek lośc każdej fazy równy jest stosunkow długośc odcnków lα lβ wynos 7 4. W układze jest około sedem razy węcej fazy bogatej w ntrobenzen nż fazy bogatej w heksan 5. Układ jest jednofazowy po ogrzanu do temperatury 292K
50 UKŁADY DWUSKŁADNIKOWE I TEMPERATURY KRYTYCZNE ROZPUSZCZALNOŚCI IV IV II III Dagram temperatura- skład dla wody nkotyny. 1. Górna temperatura krytyczna rozpuszczalnośc T gkr to najwyższa temperatura, w której występuje rozdzelene faz. 2. Dolna temperatura krytyczna rozpuszczalnośc T dkr, ponżej tej temperatury oba składnk meszają sę w każdym stosunku, natomast powyżej stneją w dwóch fazach. I nenasycony roztwór nkotyny w wodze, układ jednofazowy II- nasycony roztwór wody w nkotyne nkotyny w wodze, układ dwufazowy III- nenasycony roztwór wody w nkotyne, układ jednofazowy IV- neogranczona meszalność wody nkotyny, układ jednofazowy
51 UKŁADY DWUSKŁADNIKOWE DIAGRAM FAZOWY CIECZ- CIAŁO STAŁE 1. Składnk układu prawe ne rozpuszczają sę w faze stałej, a rozpuszczają sę całkowce w faze cekłej 2. Izopleta przechodząca przez punkt e odpowada składow eutektycznemu, czyl meszanne o najnższej temperaturze wrzena. 3. a 1 a 2 układ wchodz w obszar dwufazowy 4. a 2 a 3 tworzy sę węcej substancj stałej 5. a 3 a 4 cecz krzepne, układ dwufazowy
52 UKŁAD TRÓJSKŁADNIKOWY KRZYWE STYGNIĘCIA a) Przebeg stygnęca substancj czystej b) Przebeg stygnęca meszanny, w której 2 wykazują całkowtą meszalność w obu fazach c) Przebeg procesu stygnęca układu eutektycznego prostego
53 UKŁADY TRÓJSKŁADNIKOWE Meszanna eutektyczna to meszanna kryształów o określonym składze, która wydzela sę z roztworów cekłych w określonej temperaturze zwanej temp. eutektyczną. Temp. eutektyczna jest na ogół nższa od temp. Krzepnęca czystych składnków. T A, E, T B lna LIKWIDUSA, odpowada współstnenu w stane równowag fazy cekłej z fazą stałą. T A, E opsuje zależność mędzy składem fazy cekłej a temperaturą krystalzacj składnka A T B, E nadmar rozpuszczalnka B, krystalzuje jako perwszy z roztworu T A, DEH, T B lna SOLIDUSA, ograncza od góry obszar stnena faz stałych
54 UKŁADY TRÓJSKŁADNIKOWE
55 UKŁAD TRÓJSKŁADNIKOWY Do opsu układów trójskładnkowych służy PRAWO PODZIAŁU NERNSTA. W układze trójskładnkowym, w którym dwa składnk to rozpuszczalnk o ogranczonej rozpuszczalnośc wzajemnej (ne meszające sę ze sobą) a trzeca to substancja stała, cekła lub gazowa dobrze rozpuszczająca sę w obydwu poprzednch. W warunkach równowag termodynamcznej, (stała temperatura cśnene), stosunek aktywnośc rozpuszczonej substancj w obydwu rozpuszczalnkach jest welkoścą stałą zwaną współczynnkem podzału K N współczynnk podzału Nernsta (a C ) α aktywność substancj rozpuszczonej w faze α (a C ) β aktywność substancj rozpuszczonej w faze β
56 PRAWO PODZIAŁU NERNSTA faza cekła faza cekła faza cekła faza cekła faza cekła faza cekła faza cekła faza cekła faza cekła faza cekła opsuje rozdzał substancj mędzy dwe ne meszające sę ze sobą fazy cekłe. substancja ( ) W stane równowag fazowej, dla T, p = const: - standardowy potencjał chemczny składnka odpowedno w faze - aktywność składnka odpowedno w faze β α α Θ α α a R T ln β Θ β β a R T ln, β α a, a β α W stane równowag fazowej, dla T, p = const: - standardowy potencjał chemczny składnka odpowedno w faze - aktywność składnka odpowedno w faze β α α Θ α α a R T ln β Θ β β a R T ln, β α a, a β α β α α Θ α α a R T ln β Θ β β a R T ln, β α a, a β α
57 PRAWO PODZIAŁU NERNSTA α β W warunkach T, p = const: Θ α R T ln a α = Θ β R T lna β Θ β - R T Θ α const R T lna α - R T lna β Θ β - Θ α czyl: lna α - lna β Θ β - R T Θ α e Θ β - Θ α R T const K a ln a a a α β α β e Θ β - R T Θ α Θ β Θ α - R T K a a α α β / β K a a α β
58 PRAWO PODZIAŁU NERNSTA WSPÓŁCZYNNIK PODZIAŁU NERNSTA JEST RÓWNY ILORAZOWI STĘŻEŃ SUBSTANCJI ROZPUSZCZONEJ W DWÓCH NIEMIESZAJĄCYCH SIĘ FAZACH CIEKŁYCH,W STANIE RÓWNOWAGI FAZOWEJ, W STAŁEJ TEMPERATURZE. Roztwór dealny (f = 1): K X X / Roztwór rozceńczony: K α / β c c α β
59 PRAWO PODZIAŁU NERNSTA Równana słuszne gdy: cecze ne meszają sę ( lub meszają sę ogranczene ) stężene substancj rozpuszczonej w obu fazach ne jest duże ( roztwory rozceńczone ) ne zachodz dysocjacja an asocjacja cząsteczek substancj rozpuszczonej w żadnej z faz stała temperatura Wartość współczynnka podzału ( K ): zależy od rodzaju składnków układu (ceczy substancj) oraz od temperatury ne zależy od lośc substancj rozpuszczonej objętośc ceczy
60 PRAWO PODZIAŁU NERNSTA ZASTOSOWANIE WSPÓŁCZYNNIKA PODZIAŁU NERNSTA 1. określane właścwośc substancj > 1 substancja ma charakter lpoflny (co > cw) (wększe pownowactwo do fazy olejowej) < 1 substancja ma charakter hydroflny (co < cw) (wększe pownowactwo do fazy wodnej) 2. QSAR (Quanttatve Structure-Actvty Relatonshps) 3. proces ekstrakcj (przewdywane najkorzystnejszych warunków ekstrakcj - dobór odpowednego rozpuszczalnka, przewdywane stopna rozdzału składnków)
61 NAPIĘCIE POWIERZCHNIOWE 1. Napęce powerzchnowe to zjawsko występujące na grancy faz. 2. Cząstka znajdująca sę wewnątrz fazy podlega jednakowym oddzaływanom ze wszystkch stron, a wypadkowa tych dzałań jest równa zero. 3. Sły dzałające na cząstkę znajdującą sę w warstwe powerzchnowej ne są zrównoważone. 4. na grancy fazy cekłej gazowej wypadkowa sł dzałających na cząstkę jest prostopadła do powerzchn fazy skerowana do wnętrza ceczy. 5. Cząstk z powerzchn fazy są wcągane w głąb ceczy. 6. Napęce powerzchnowe to praca L potrzebna do utworzena jednostkowej powerzchn mędzyfazowej A
62 NAPIĘCIE POWIERZCHNIOWE loraz pracy powerzchn równa sę stosunkow sły/długośc równoważny wymar napęca powerzchnowego SENS FIZYCZNY: Napęce powerzchnowe równa sę lczbowo sle F dzałającej styczne do powerzchn grancznej przypadającej na jednostkę długośc l przekroju lnowego tej powerzchn. Napęce powerzchnowe roztworu różn sę na ogół od napęca powerzchnowego czystego rozpuszczalnka zależy od rodzaju dodanej substancj jej stężena.
63 ADSORPCJA 1. Gdy stężene substancj w warstwe powerzchnowej jest wększe od jej stężena w głęb roztworu, zjawsko nazywa sę ADSORPCJĄ DODATNIĄ napęce powerzchnowe < napęce powerzchnowe czystego roztworu rozpuszczalnka 2. Gdy cząsteczk rozpuszczalnka przycągają sę słabej nż cząsteczk substancj rozpuszczonej z cząsteczkam rozpuszczalnka, to substancja gromadz sę w głęb roztworu jej stężene na powerzchn jest bardzo małe, a zjawsko nos nazwę ADSORPCJI UJEMNEJ substancja rozpuszczona jest powerzchnowo neczynna
64 ADSORPCJA Substancje powerzchnowo- czynne w roztworach wodnych: - mają na ogół budowę asymetryczną - zwązk organczne: mydła, wyższe kwasy tłuszczowe, alkohole, estry, sole, kwasy sulfonowe, sole amn - cząsteczk zwązku zawerają co najmnej jedną grupę hydroflową oraz hydrofobowy łańcuch węglowy - zdolność zmnejszana napęca powerzchnowego nazywana jest aktywnoścą powerzchnową. Równane Gbbsa adsorpcja zależy od aktywnośc powerzchnowej substancj. Г jest nadmarem powerzchnowym oznacza lość substancj zaadsorbowanej z roztworu, przypadającą na jednostkę powerzchn
65 LEPKOŚĆ Lepkość to zjawsko tarca wewnętrznego powstałe, w wynku dzałana sł mędzycząsteczkowych podczas ruchu poszczególnych warstw ceczy względem sebe. Wzór Newtona gdze η współczynnk proporcjonalnośc zwany lepkoścą dynamczną A pole powerzchn ulegającej przesuwanu Cecze, których lepkość jest stała w danej temperaturze to cecze newtonowske, natomast te które wykazują odchylena od tej reguły to cecze nenewtonowske.
66 LEPKOŚĆ Lepkość roztworów to funkcja zmerzonych współczynnków lepkośc rozpuszczalnka η o roztworu η. lepkość względna- lepkość ceczy wyrażona w stosunku do lepkośc nnej nż ceczy uważanej za wzorcową. lepkość właścwa lepkość zredukowana lepkość właścwa odnesona do jednostkowego stężena lepkość granczna- lepkość zredukowana ekstrapolowana do rozceńczena neskończene dużego
67 EKSTRAKCJA EKSTRAKCJA SUBSTANCJI Z FAZY CIEKŁEJ α DO FAZY CIEKŁEJ β faza cekła v faza cekła v m m stan równowag m o początkowa masa substancj w faze α Zgodne z prawem podzału Nernsta: K α / β m v m v α β β α m α, m β masa substancj zawarta w faze α β ( w stane równowag fazowej) V α, V β objętośc fazy α β
68 EKSTRAKCJA Po jednorazowej ekstrakcj: m 1 masa substancj w faze α (m o m 1 ) masa substancj w faze β m ο m v - m v 1 α β 1 m K 1 α / β m ο K K α/β α α/β v v α v β Po kolejnych ekstrakcjach w faze α pozostaje m 1, m 2...m n gramów substancj. Masa substancj pozostała w faze α po n- krotnej ekstrakcj: n α Kα/β v mn mο α β Kα/β v v Ilość przeprowadzonej substancj z fazy α do fazy β zależy od: - lczby powtarzanych ekstrakcj - objętośc użytych ceczy - wększą wydajność uzyskuje sę po welokrotnej ekstrakcj, stosując wytrząsane małym porcjam fazy β
69 EKSTRAKCJA Wyodrębnane substancj z jednej fazy do drugej można przeprowadzć za pomocą: 1. Ekstrakcja prosta przeprowadzana jest w rozdzelaczach 2. Ekstrakcja cągła w ekstraktorach Różne rodzaje rozdzelaczy a- za pomocą ceczy lżejszej od wody b- ceczy cęższej od wody c- aparat Soxhleta do ekstrakcj substancj z cał stałych a b c
Równowagi fazowe cz.ii. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowag fazowe cz.ii Zakład Chem Medycznej Pomorsk Unwersytet Medyczny KLASYFIKACJA ROZTWORÓW Roztwory neelektroltów. Klasyfkacja roztworów ch właścwośc. Ze względu na stopeń dyspersj substancj rozpuszczonej
Równowag fazowe cz.ii Zakład Chem Medycznej Pomorsk Unwersytet Medyczny KLASYFIKACJA ROZTWORÓW Roztwory neelektroltów. Klasyfkacja roztworów ch właścwośc. Ze względu na stopeń dyspersj substancj rozpuszczonej
Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Chemia fizyczna. Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia fizyczna Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny SUBSTANCJE CZYSTE SUBSTANCJE CZYSTE RÓWNOWAGI FAZOWE Fazą danej substancji nazywamy postać materii, która charakteryzuje
Chemia fizyczna Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny SUBSTANCJE CZYSTE SUBSTANCJE CZYSTE RÓWNOWAGI FAZOWE Fazą danej substancji nazywamy postać materii, która charakteryzuje
Wykład 7. Podstawy termodynamiki i kinetyki procesowej - wykład 7. Anna Ptaszek. 21 maja Katedra Inżynierii i Aparatury Przemysłu Spożywczego
 Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
Wykład 7 knetyk knetyk procesowej - Katedra Inżyner Aparatury Przemysłu Spożywczego 21 maja 2018 1 / 31 Układ weloskładnkowy dwufazowy knetyk P woda 1 atm lód woda cek a woda + substancja nelotna para
chemia wykład 3 Przemiany fazowe
 Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
TERMODYNAMIKA TECHNICZNA I CHEMICZNA
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
Wykład Turbina parowa kondensacyjna
 Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Wykład 3. Fizykochemia biopolimerów- wykład 3. Anna Ptaszek. 30 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego
 Wykład 3 - wykład 3 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 30 października 2013 1/56 Warunek równowagi fazowej Jakich układów dotyczy równowaga fazowa? Równowaga fazowa dotyczy układów: jednoskładnikowych
Wykład 3 - wykład 3 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 30 października 2013 1/56 Warunek równowagi fazowej Jakich układów dotyczy równowaga fazowa? Równowaga fazowa dotyczy układów: jednoskładnikowych
Podstawy termodynamiki
 Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
V. TERMODYNAMIKA KLASYCZNA
 46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
α i = n i /n β i = V i /V α i = β i γ i = m i /m
 Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
ELEKTROCHEMIA. ( i = i ) Wykład II b. Nadnapięcie Równanie Buttlera-Volmera Równania Tafela. Wykład II. Równowaga dynamiczna i prąd wymiany
 Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Modele wzrostu kryształów stałych
 Materały do wykładu Modele wzrostu kryształów stałych Marek Izdebsk Instytut Fzyk PŁ 2016 Sps treśc Temat 1. Termodynamczne podstawy równowag fazowej krystalzacj....1 1.1. Równowaga quas-równowaga...1
Materały do wykładu Modele wzrostu kryształów stałych Marek Izdebsk Instytut Fzyk PŁ 2016 Sps treśc Temat 1. Termodynamczne podstawy równowag fazowej krystalzacj....1 1.1. Równowaga quas-równowaga...1
Wykład 8B. Układy o ograniczonej mieszalności
 Wykład 8B Układy o ograniczonej mieszalności Układy o ograniczonej mieszalności Jeżeli dla pewnego składu entalpia swobodna mieszania ( Gmiesz> 0) jest dodatnia, to mieszanie nie jest procesem samorzutnym
Wykład 8B Układy o ograniczonej mieszalności Układy o ograniczonej mieszalności Jeżeli dla pewnego składu entalpia swobodna mieszania ( Gmiesz> 0) jest dodatnia, to mieszanie nie jest procesem samorzutnym
Wykład 6. Klasyfikacja przemian fazowych
 Wykład 6 Klasyfikacja przemian fazowych JS Klasyfikacja Ehrenfesta Ehrenfest klasyfikuje przemiany fazowe w oparciu o potencjał chemiczny. nieciągłość Przemiany fazowe pierwszego rodzaju pochodne potencjału
Wykład 6 Klasyfikacja przemian fazowych JS Klasyfikacja Ehrenfesta Ehrenfest klasyfikuje przemiany fazowe w oparciu o potencjał chemiczny. nieciągłość Przemiany fazowe pierwszego rodzaju pochodne potencjału
Wykład 8. Silnik Stirlinga (R. Stirling, 1816)
 Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
Wykład 8 Maszyny ceplne c.d. Rozkład Maxwella -wstęp Entalpa Entalpa reakcj chemcznych Entalpa przeman azowych Procesy odwracalne neodwracalne Entropa W. Domnk Wydzał Fzyk UW Termodynamka 018/019 1/6 Slnk
Wykład 2. Anna Ptaszek. 7 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 2. Anna Ptaszek 1 / 1
 Wykład 2 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 7 października 2015 1 / 1 Zjawiska koligatywne Rozpuszczenie w wodzie substancji nielotnej powoduje obniżenie prężności pary nasyconej P woda
Wykład 2 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 7 października 2015 1 / 1 Zjawiska koligatywne Rozpuszczenie w wodzie substancji nielotnej powoduje obniżenie prężności pary nasyconej P woda
Zmiana entropii w przemianach odwracalnych
 Wykład 4 Zmana entrop w przemanach odwracalnych: przemany obegu Carnota, spręŝane gazu półdoskonałego ze schładzanem, zobaryczne wytwarzane przegrzewane pary techncznej rzemany zentropowe gazu doskonałego
Wykład 4 Zmana entrop w przemanach odwracalnych: przemany obegu Carnota, spręŝane gazu półdoskonałego ze schładzanem, zobaryczne wytwarzane przegrzewane pary techncznej rzemany zentropowe gazu doskonałego
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY. Zakład Budowy i Eksploatacji Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA
 PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
Termodynamika równowag fazowych w układach dwuskładnikowych
 Termodynamika równowag fazowych w układach dwuskładnikowych 3.3.1. Równowaga ciecz-para: skład pary nad roztworem, prawo Roulta, Henry ego, destylacja baryczna oraz termiczna 3.3.2. Równowaga ciecz-ciecz
Termodynamika równowag fazowych w układach dwuskładnikowych 3.3.1. Równowaga ciecz-para: skład pary nad roztworem, prawo Roulta, Henry ego, destylacja baryczna oraz termiczna 3.3.2. Równowaga ciecz-ciecz
Analiza termiczna Krzywe stygnięcia
 Analiza termiczna Krzywe stygnięcia 0 0,2 0,4 0,6 0,8 1,0 T a e j n s x p b t c o f g h k l p d i m y z q u v r w α T B T A T E T k P = const Chem. Fiz. TCH II/10 1 Rozpatrując stygnięcie wzdłuż kolejnych
Analiza termiczna Krzywe stygnięcia 0 0,2 0,4 0,6 0,8 1,0 T a e j n s x p b t c o f g h k l p d i m y z q u v r w α T B T A T E T k P = const Chem. Fiz. TCH II/10 1 Rozpatrując stygnięcie wzdłuż kolejnych
Wykład 1-4. Anna Ptaszek. 6 września Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Fizykochemia biopolimerów - wykład 1-4.
 Wykład 1-4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 6 września 2016 1 / 68 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1-4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 6 września 2016 1 / 68 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Współczynniki aktywności w roztworach elektrolitów. W.a. w roztworach elektrolitów (2) W.a. w roztworach elektrolitów (3) 1 r. Przypomnienie!
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Warunki izochoryczno-izotermiczne
 WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
Para pozostająca w równowadze z roztworem jest bogatsza w ten składnik, którego dodanie do roztworu zwiększa sumaryczną prężność pary nad nim.
 RÓWNOWAGA CIECZ-PARA DLA UKŁADÓW DWUSKŁADNIKOWYCH: 1) Zgodnie z regułą faz Gibbsa układ dwuskładnikowy osiąga największą liczbę stopni swobody (f max ), gdy znajduje się w nim najmniejsza możliwa liczba
RÓWNOWAGA CIECZ-PARA DLA UKŁADÓW DWUSKŁADNIKOWYCH: 1) Zgodnie z regułą faz Gibbsa układ dwuskładnikowy osiąga największą liczbę stopni swobody (f max ), gdy znajduje się w nim najmniejsza możliwa liczba
Prężność pary nad roztworem
 Tomasz Lubera Układ: Prężność pary nad roztworem dwuskładnikowy (składniki I i II) dwufazowy (ciecz i gaz) w którym faza ciekła i gazowa to roztwory idealne W stanie równowagi prężności pary składników/układu
Tomasz Lubera Układ: Prężność pary nad roztworem dwuskładnikowy (składniki I i II) dwufazowy (ciecz i gaz) w którym faza ciekła i gazowa to roztwory idealne W stanie równowagi prężności pary składników/układu
prof. dr hab. Małgorzata Jóźwiak
 Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Wykład 8. Równowaga fazowa Roztwory rzeczywiste
 Wykład 8 Równowaga fazowa Roztwory rzeczywiste Roztwory doskonałe Porównanie roztworów doskonałych i Roztwory Doskonałe rzeczywistych Roztwory Rzeczywiste Spełniają prawo Raoulta Mieszanie w warunkach
Wykład 8 Równowaga fazowa Roztwory rzeczywiste Roztwory doskonałe Porównanie roztworów doskonałych i Roztwory Doskonałe rzeczywistych Roztwory Rzeczywiste Spełniają prawo Raoulta Mieszanie w warunkach
WYKŁAD 7. Diagramy fazowe Dwuskładnikowe układy doskonałe
 WYKŁAD 7 Diagramy fazowe Dwuskładnikowe układy doskonałe JS Reguła Gibssa. Układy dwuskładnikowe Reguła faz Gibbsa określa liczbę stopni swobody układu w równowadze termodynamicznej: układy dwuskładnikowe
WYKŁAD 7 Diagramy fazowe Dwuskładnikowe układy doskonałe JS Reguła Gibssa. Układy dwuskładnikowe Reguła faz Gibbsa określa liczbę stopni swobody układu w równowadze termodynamicznej: układy dwuskładnikowe
IZOTERMA ADSORPCJI GIBBSA
 Ćwczene nr VII IZOTERM DSORPCJI GIBBS I. Cel ćwczena Celem ćwczena jest możlwość loścowego określena welkośc molekularnej nadmaru powerzchnowego z pomarów makroskopowych napęca powerzchnowego γ l. II.
Ćwczene nr VII IZOTERM DSORPCJI GIBBS I. Cel ćwczena Celem ćwczena jest możlwość loścowego określena welkośc molekularnej nadmaru powerzchnowego z pomarów makroskopowych napęca powerzchnowego γ l. II.
Płyny nienewtonowskie i zjawisko tiksotropii
 Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Laboratorium z chemii fizycznej. Zakres zagadnień na kolokwia
 CHEMIA semestr III Laboratorium z chemii fizycznej Zakres zagadnień na kolokwia 1. Wymagania ogólne Podstawą przygotowania do ćwiczeń jest skrypt pt. Chemia fizyczna. Ćwiczenia laboratoryjne, praca zbiorowa
CHEMIA semestr III Laboratorium z chemii fizycznej Zakres zagadnień na kolokwia 1. Wymagania ogólne Podstawą przygotowania do ćwiczeń jest skrypt pt. Chemia fizyczna. Ćwiczenia laboratoryjne, praca zbiorowa
Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE
 Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak
 Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
Kalorymetria. 1. I zasada termodynamiki, Prawo Hessa, Prawo Kirchhoffa (graficzna interpretacja), ciepło właściwe, termodynamiczne funkcje stanu.
 Kalorymetria 1. I zasada termodynamiki, Prawo Hessa, Prawo Kirchhoffa (graficzna interpretacja), ciepło właściwe, termodynamiczne funkcje stanu. 2. Rodzaje i zasady działania kalorymetrów: a) nieizotermicznego
Kalorymetria 1. I zasada termodynamiki, Prawo Hessa, Prawo Kirchhoffa (graficzna interpretacja), ciepło właściwe, termodynamiczne funkcje stanu. 2. Rodzaje i zasady działania kalorymetrów: a) nieizotermicznego
Refraktometria. sin β sin β
 efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
Zestaw zadań 4: Przestrzenie wektorowe i podprzestrzenie. Liniowa niezależność. Sumy i sumy proste podprzestrzeni.
 Zestaw zadań : Przestrzene wektorowe podprzestrzene. Lnowa nezależność. Sumy sumy proste podprzestrzen. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar :
Zestaw zadań : Przestrzene wektorowe podprzestrzene. Lnowa nezależność. Sumy sumy proste podprzestrzen. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar :
RUCH OBROTOWY Można opisać ruch obrotowy ze stałym przyspieszeniem ε poprzez analogię do ruchu postępowego jednostajnie zmiennego.
 RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
Wykład 1. Anna Ptaszek. 5 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 1. Anna Ptaszek 1 / 36
 Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Część III: Termodynamika układów biologicznych
 Część III: Termodynamka układów bologcznych MATERIAŁY POMOCNICZE DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Botechnolog prof. dr hab. nż. Jan Mazersk TERMODYNAMIKA UKŁADÓW BIOLOGICZNYCH Nezwykle cenną metodą
Część III: Termodynamka układów bologcznych MATERIAŁY POMOCNICZE DO WYKŁADÓW Z PODSTAW BIOFIZYKI IIIr. Botechnolog prof. dr hab. nż. Jan Mazersk TERMODYNAMIKA UKŁADÓW BIOLOGICZNYCH Nezwykle cenną metodą
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda-kwas octowychloroform metodą potencjometryczną ćwczene nr 9 Opracowała dr hab. Małgorzata Jóźwak Zakres
Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda-kwas octowychloroform metodą potencjometryczną ćwczene nr 9 Opracowała dr hab. Małgorzata Jóźwak Zakres
INDUKCJA ELEKTROMAGNETYCZNA. - Prąd powstający w wyniku indukcji elektro-magnetycznej.
 INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
Termodynamiczne modelowanie procesów spalania, wybuchu i detonacji nieidealnych układów wysokoenergetycznych
 BIULETYN WAT VOL. LIX, NR 3, 2010 Termodynamczne modelowane procesów spalana, wybuchu detonacj nedealnych układów wysokoenergetycznych SEBASTIAN GRYS, WALDEMAR A. TRZCIŃSKI Wojskowa Akadema Technczna,
BIULETYN WAT VOL. LIX, NR 3, 2010 Termodynamczne modelowane procesów spalana, wybuchu detonacj nedealnych układów wysokoenergetycznych SEBASTIAN GRYS, WALDEMAR A. TRZCIŃSKI Wojskowa Akadema Technczna,
Wykład 13. Rozkład kanoniczny Boltzmanna Rozkład Maxwella-Boltzmanna III Zasada Termodynamiki. Rozkład Boltzmanna!!!
 Wykład 13 Rozkład kanonczny Boltzmanna Rozkład Maxwella-Boltzmanna III Zasada Termodynamk W. Domnk Wydzał Fzyk UW Termodynamka 2018/2019 1/30 Rozkład Boltzmanna!!! termostat T E n układ P n exp E n Z warunku
Wykład 13 Rozkład kanonczny Boltzmanna Rozkład Maxwella-Boltzmanna III Zasada Termodynamk W. Domnk Wydzał Fzyk UW Termodynamka 2018/2019 1/30 Rozkład Boltzmanna!!! termostat T E n układ P n exp E n Z warunku
Wykłady z termodynamiki i fizyki statystycznej. Semestr letni 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a
 Wykłady z termodynamk fzyk statystycznej. Semestr letn 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a gudowska@th.f.uj.edu.pl Zalecane podręcznk: 1.Termodynamka R. Hołyst, A. Ponewersk, A. Cach 2. Podstay
Wykłady z termodynamk fzyk statystycznej. Semestr letn 2009/2010 Ewa Gudowska-Nowak, IFUJ, p.441 a gudowska@th.f.uj.edu.pl Zalecane podręcznk: 1.Termodynamka R. Hołyst, A. Ponewersk, A. Cach 2. Podstay
ANALIZA TERMODYNAMICZNA STOPÓW ODLEWNICZYCH PRZY UŻYCIU PROGRAMU THERMOCALC
 171/18 ARCHIWUM ODLEWNICTWA Rok 2006, Rocznk 6, Nr 18 (2/2) ARCHIVES OF FOUNDRY Year 2006, Volume 6, N o 18 (2/2) PAN Katowce PL ISSN 1642-5308 ANALIZA TERMODYNAMICZNA STOPÓW ODLEWNICZYCH PRZY UŻYCIU PROGRAMU
171/18 ARCHIWUM ODLEWNICTWA Rok 2006, Rocznk 6, Nr 18 (2/2) ARCHIVES OF FOUNDRY Year 2006, Volume 6, N o 18 (2/2) PAN Katowce PL ISSN 1642-5308 ANALIZA TERMODYNAMICZNA STOPÓW ODLEWNICZYCH PRZY UŻYCIU PROGRAMU
Wykład 5. przemysłu spożywczego- wykład 5
 Wykład spożywczego- wykład Katedra Inżynierii i Aparatury Przemysłu Spożywczego 4maja2014 1/1 Układy gaz-ciecz Rozpuszczalnośćwybranychgazówwcieczachw20 o Cw g/100g cieczy CIECZ H 2 N 2 O 2 CO 2 H 2 S
Wykład spożywczego- wykład Katedra Inżynierii i Aparatury Przemysłu Spożywczego 4maja2014 1/1 Układy gaz-ciecz Rozpuszczalnośćwybranychgazówwcieczachw20 o Cw g/100g cieczy CIECZ H 2 N 2 O 2 CO 2 H 2 S
INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH
 INSTYTUT MASZYN I URZĄDZEŃ ENERGETYCZNYCH Politechnika Śląska w Gliwicach INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH WYZNACZANIE WYKRESU RÓWNOWAGI FAZOWEJ (dla stopów dwuskładnikowych) Instrukcja przeznaczona
INSTYTUT MASZYN I URZĄDZEŃ ENERGETYCZNYCH Politechnika Śląska w Gliwicach INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH WYZNACZANIE WYKRESU RÓWNOWAGI FAZOWEJ (dla stopów dwuskładnikowych) Instrukcja przeznaczona
Wykład Mikroskopowa interpretacja ciepła i pracy Entropia
 Wykład 7 5.13 Mkroskopowa nterpretacja cepła pracy. 5.14 Entropa 5.15 Funkcja rozdzału 6 II zasada termodynamk 6.1 Sformułowane Claususa oraz Kelvna-Plancka II zasady termodynamk 6.2 Procesy odwracalne
Wykład 7 5.13 Mkroskopowa nterpretacja cepła pracy. 5.14 Entropa 5.15 Funkcja rozdzału 6 II zasada termodynamk 6.1 Sformułowane Claususa oraz Kelvna-Plancka II zasady termodynamk 6.2 Procesy odwracalne
SYMULACJA KRZEPNIĘCIA OBJĘTOŚCIOWEGO METALI Z UWZGLĘDNIENIEM PRZECHŁODZENIA TEMPERATUROWEGO
 49/14 Archves of Foundry, Year 2004, Volume 4, 14 Archwum O dlewnctwa, Rok 2004, Rocznk 4, Nr 14 PAN Katowce PL ISSN 1642-5308 SYMULACJA KRZEPNIĘCIA OBJĘTOŚCIOWEGO METALI Z UWZGLĘDNIENIEM PRZECHŁODZENIA
49/14 Archves of Foundry, Year 2004, Volume 4, 14 Archwum O dlewnctwa, Rok 2004, Rocznk 4, Nr 14 PAN Katowce PL ISSN 1642-5308 SYMULACJA KRZEPNIĘCIA OBJĘTOŚCIOWEGO METALI Z UWZGLĘDNIENIEM PRZECHŁODZENIA
Roztwory. Homogeniczne jednorodne (jedno-fazowe) mieszaniny dwóch lub więcej składników.
 Roztwory Homogeniczne jednorodne (jedno-fazowe) mieszaniny dwóch lub więcej składników. Własności fizyczne roztworów są związane z równowagę pomiędzy siłami wiążącymi cząsteczki wody i substancji rozpuszczonej.
Roztwory Homogeniczne jednorodne (jedno-fazowe) mieszaniny dwóch lub więcej składników. Własności fizyczne roztworów są związane z równowagę pomiędzy siłami wiążącymi cząsteczki wody i substancji rozpuszczonej.
Termodynamika Techniczna dla MWT, Rozdział 14. AJ Wojtowicz IF UMK. 5.2. Generacja entropii; transfer ciepła przy skończonej róŝnicy temperatur
 ermodynamka echnczna dla MW, Rozdzał 4. AJ Wojtowcz IF UMK Rozdzał 4. Zmana entrop w przemanach odwracalnych.. rzemany obegu Carnota.. SpręŜane gazu półdoskonałego ze schładzanem.3. Izobaryczne wytwarzane
ermodynamka echnczna dla MW, Rozdzał 4. AJ Wojtowcz IF UMK Rozdzał 4. Zmana entrop w przemanach odwracalnych.. rzemany obegu Carnota.. SpręŜane gazu półdoskonałego ze schładzanem.3. Izobaryczne wytwarzane
Zadania treningowe na kolokwium
 Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
5. Pochodna funkcji. lim. x c x c. (x c) = lim. g(c + h) g(c) = lim
 5. Pocodna funkcj Defncja 5.1 Nec f: (a, b) R nec c (a, b). Jeśl stneje granca lm x c x c to nazywamy ją pocodną funkcj f w punkce c oznaczamy symbolem f (c) Twerdzene 5.1 Jeśl funkcja f: (a, b) R ma pocodną
5. Pocodna funkcj Defncja 5.1 Nec f: (a, b) R nec c (a, b). Jeśl stneje granca lm x c x c to nazywamy ją pocodną funkcj f w punkce c oznaczamy symbolem f (c) Twerdzene 5.1 Jeśl funkcja f: (a, b) R ma pocodną
Zastosowanie symulatora ChemCad do modelowania złożonych układów reakcyjnych procesów petrochemicznych
 NAFTA-GAZ styczeń 2011 ROK LXVII Anna Rembesa-Śmszek Instytut Nafty Gazu, Kraków Andrzej Wyczesany Poltechnka Krakowska, Kraków Zastosowane symulatora ChemCad do modelowana złożonych układów reakcyjnych
NAFTA-GAZ styczeń 2011 ROK LXVII Anna Rembesa-Śmszek Instytut Nafty Gazu, Kraków Andrzej Wyczesany Poltechnka Krakowska, Kraków Zastosowane symulatora ChemCad do modelowana złożonych układów reakcyjnych
MECHANIKA 2 MOMENT BEZWŁADNOŚCI. Wykład Nr 10. Prowadzący: dr Krzysztof Polko
 MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
I. Elementy analizy matematycznej
 WSTAWKA MATEMATYCZNA I. Elementy analzy matematycznej Pochodna funkcj f(x) Pochodna funkcj podaje nam prędkość zman funkcj: df f (x + x) f (x) f '(x) = = lm x 0 (1) dx x Pochodna funkcj podaje nam zarazem
WSTAWKA MATEMATYCZNA I. Elementy analzy matematycznej Pochodna funkcj f(x) Pochodna funkcj podaje nam prędkość zman funkcj: df f (x + x) f (x) f '(x) = = lm x 0 (1) dx x Pochodna funkcj podaje nam zarazem
Model ASAD. ceny i płace mogą ulegać zmianom (w odróżnieniu od poprzednio omawianych modeli)
 Model odstawowe założena modelu: ceny płace mogą ulegać zmanom (w odróżnenu od poprzedno omawanych model) punktem odnesena analzy jest obserwacja pozomu produkcj cen (a ne stopy procentowej jak w modelu
Model odstawowe założena modelu: ceny płace mogą ulegać zmanom (w odróżnenu od poprzedno omawanych model) punktem odnesena analzy jest obserwacja pozomu produkcj cen (a ne stopy procentowej jak w modelu
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2016/17)
 Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2016/17) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
Ćwiczenia audytoryjne z Chemii fizycznej 1 Zalecane zadania kolokwium 1. (2016/17) Uwaga! Uzyskane wyniki mogą się nieco różnić od podanych w materiałach, ze względu na uaktualnianie wartości zapisanych
Termodynamiczny opis przejść fazowych pierwszego rodzaju
 Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
MATEMATYKA POZIOM ROZSZERZONY Kryteria oceniania odpowiedzi. Arkusz A II. Strona 1 z 5
 MATEMATYKA POZIOM ROZSZERZONY Krytera ocenana odpowedz Arkusz A II Strona 1 z 5 Odpowedz Pytane 1 2 3 4 5 6 7 8 9 Odpowedź D C C A B 153 135 232 333 Zad. 10. (0-3) Dana jest funkcja postac. Korzystając
MATEMATYKA POZIOM ROZSZERZONY Krytera ocenana odpowedz Arkusz A II Strona 1 z 5 Odpowedz Pytane 1 2 3 4 5 6 7 8 9 Odpowedź D C C A B 153 135 232 333 Zad. 10. (0-3) Dana jest funkcja postac. Korzystając
Pokazać, że wyżej zdefiniowana struktura algebraiczna jest przestrzenią wektorową nad ciałem
 Zestaw zadań : Przestrzene wektorowe. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar : C C C, (z, v) z v := z v jest przestrzeną lnową nad całem lczb zespolonych
Zestaw zadań : Przestrzene wektorowe. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar : C C C, (z, v) z v := z v jest przestrzeną lnową nad całem lczb zespolonych
2 PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ. 2.1 Wprowadzenie
 RAKTYCZNA REALIZACJA RZEMIANY ADIABATYCZNEJ. Wprowadzene rzeana jest adabatyczna, jeśl dla każdych dwóch stanów l, leżących na tej przeane Q - 0. Z tej defncj wynka, że aby zrealzować wyżej wyenony proces,
RAKTYCZNA REALIZACJA RZEMIANY ADIABATYCZNEJ. Wprowadzene rzeana jest adabatyczna, jeśl dla każdych dwóch stanów l, leżących na tej przeane Q - 0. Z tej defncj wynka, że aby zrealzować wyżej wyenony proces,
3. ŁUK ELEKTRYCZNY PRĄDU STAŁEGO I PRZEMIENNEGO
 3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
Kwantowa natura promieniowania elektromagnetycznego
 Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadanie teoretyczne
 XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
OGÓLNE PODSTAWY SPEKTROSKOPII
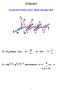 WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH
 WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
Wykład 4. Przypomnienie z poprzedniego wykładu
 Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
TERMODYNAMIKA. Andrzej Syrwid. Kraków 2011 r.
 ERMODYNAMIKA Andrzej Syrwd Kraków 011 r. Sps treśc 1 Podstawowe pojęca 5 Zasady termodynamk 6 3 Podstawowe skale temperatur 6 4 Podstawowe zależnośc pomędzy parametram opsującym układ 7 5 Gaz doskonały
ERMODYNAMIKA Andrzej Syrwd Kraków 011 r. Sps treśc 1 Podstawowe pojęca 5 Zasady termodynamk 6 3 Podstawowe skale temperatur 6 4 Podstawowe zależnośc pomędzy parametram opsującym układ 7 5 Gaz doskonały
Modele wieloczynnikowe. Modele wieloczynnikowe. Modele wieloczynnikowe ogólne. α β β β ε. Analiza i Zarządzanie Portfelem cz. 4.
 Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 ANALIZA TERMICZNA WSTĘP Zespół ciał (substancji) stanowiący w danej chwili przedmiot naszych badań nazywamy układem, a wszystko co znajduje się na zewnątrz niego, otoczeniem. Poszczególne jednolite części
ANALIZA TERMICZNA WSTĘP Zespół ciał (substancji) stanowiący w danej chwili przedmiot naszych badań nazywamy układem, a wszystko co znajduje się na zewnątrz niego, otoczeniem. Poszczególne jednolite części
Diagonalizacja macierzy kwadratowej
 Dagonalzacja macerzy kwadratowej Dana jest macerz A nân. Jej wartośc własne wektory własne spełnają równane Ax x dla,..., n Każde z równań własnych osobno można zapsać w postac: a a an x x a a an x x an
Dagonalzacja macerzy kwadratowej Dana jest macerz A nân. Jej wartośc własne wektory własne spełnają równane Ax x dla,..., n Każde z równań własnych osobno można zapsać w postac: a a an x x a a an x x an
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Trójkąt Gibbsa Równowagi układów z ograniczoną mieszalnością składników Prawo podziału Nernsta
 Termodynamiczny opis równowag w układach trójskładnikowych 3.4.1. Trójkąt Gibbsa 3.4.2. Równowagi układów z ograniczoną mieszalnością składników 3.4.3. Prawo podziału Nernsta Układy trójskładnikowe Liczba
Termodynamiczny opis równowag w układach trójskładnikowych 3.4.1. Trójkąt Gibbsa 3.4.2. Równowagi układów z ograniczoną mieszalnością składników 3.4.3. Prawo podziału Nernsta Układy trójskładnikowe Liczba
PROCESY JEDNOSTKOWE W TECHNOLOGIACH ŚRODOWISKOWYCH DESTYLACJA
 KIiChŚ PROCESY JEDNOSTKOWE W TECHNOLOGIACH ŚRODOWISKOWYCH Ćwiczenie nr 5 DESTYLACJA Cel ćwiczenia Doświadczalne wyznaczenie krzywych równowagi ciecz-para dla układu woda-kwas octowy. Wprowadzenie Destylacja
KIiChŚ PROCESY JEDNOSTKOWE W TECHNOLOGIACH ŚRODOWISKOWYCH Ćwiczenie nr 5 DESTYLACJA Cel ćwiczenia Doświadczalne wyznaczenie krzywych równowagi ciecz-para dla układu woda-kwas octowy. Wprowadzenie Destylacja
Mieszaniny substancji
 Mieszaniny substancji Wykład 8 Mieszaniny Mieszanina układ dwóch lub więcej pierwiastków lub związków chemicznych zmieszanych z sobą w dowolnym stosunku i wykazujących swoje indywidualne właściwości. Mieszaniny
Mieszaniny substancji Wykład 8 Mieszaniny Mieszanina układ dwóch lub więcej pierwiastków lub związków chemicznych zmieszanych z sobą w dowolnym stosunku i wykazujących swoje indywidualne właściwości. Mieszaniny
LABORATORIUM TECHNIKI CIEPLNEJ INSTYTUTU TECHNIKI CIEPLNEJ WYDZIAŁ INŻYNIERII ŚRODOWISKA I ENERGETYKI POLITECHNIKI ŚLĄSKIEJ
 INSTYTUTU TECHNIKI CIEPLNEJ WYDZIAŁ INŻYNIERII ŚRODOWISKA I ENERGETYKI POLITECHNIKI ŚLĄSKIEJ INSTRUKCJA LABORATORYJNA Temat ćwczena: BADANIE POPRAWNOŚCI OPISU STANU TERMICZNEGO POWIETRZA PRZEZ RÓWNANIE
INSTYTUTU TECHNIKI CIEPLNEJ WYDZIAŁ INŻYNIERII ŚRODOWISKA I ENERGETYKI POLITECHNIKI ŚLĄSKIEJ INSTRUKCJA LABORATORYJNA Temat ćwczena: BADANIE POPRAWNOŚCI OPISU STANU TERMICZNEGO POWIETRZA PRZEZ RÓWNANIE
Energia potencjalna jest energią zgromadzoną w układzie. Energia potencjalna może być zmieniona w inną formę energii (na przykład energię kinetyczną)
 1 Enega potencjalna jest enegą zgomadzoną w układze. Enega potencjalna może być zmenona w nną omę eneg (na pzykład enegę knetyczną) może być wykozystana do wykonana pacy. Sumę eneg potencjalnej knetycznej
1 Enega potencjalna jest enegą zgomadzoną w układze. Enega potencjalna może być zmenona w nną omę eneg (na pzykład enegę knetyczną) może być wykozystana do wykonana pacy. Sumę eneg potencjalnej knetycznej
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1
 Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Model ISLM. Inwestycje - w modelu ISLM przyjmujemy, że inwestycje przyjmują postać funkcji liniowej:
 dr Bartłomej Rokck Ćwczena z Makroekonom I Model ISLM Podstawowe założena modelu: penądz odgrywa ważną rolę przy determnowanu pozomu dochodu zatrudnena nwestycje ne mają charakteru autonomcznego, a ch
dr Bartłomej Rokck Ćwczena z Makroekonom I Model ISLM Podstawowe założena modelu: penądz odgrywa ważną rolę przy determnowanu pozomu dochodu zatrudnena nwestycje ne mają charakteru autonomcznego, a ch
Temat 13. Rozszerzalność cieplna i przewodnictwo cieplne ciał stałych.
 Temat 13. Rozszerzalność ceplna przewodnctwo ceplne cał stałych. W temace 8 wykazalśmy przy wykorzystanu warunków brzegowych orna-karmana, że wyraz lnowy w rozwnęcu energ potencjalnej w szereg potęgowy
Temat 13. Rozszerzalność ceplna przewodnctwo ceplne cał stałych. W temace 8 wykazalśmy przy wykorzystanu warunków brzegowych orna-karmana, że wyraz lnowy w rozwnęcu energ potencjalnej w szereg potęgowy
Seminarium 4 Obliczenia z wykorzystaniem przekształcania wzorów fizykochemicznych
 Seminarium 4 Obliczenia z wykorzystaniem przekształcania wzorów fizykochemicznych Zad. 1 Przekształć w odpowiedni sposób podane poniżej wzory aby wyliczyć: a) a lub m 2 b) m zred h E a 8ma E osc h 4 2
Seminarium 4 Obliczenia z wykorzystaniem przekształcania wzorów fizykochemicznych Zad. 1 Przekształć w odpowiedni sposób podane poniżej wzory aby wyliczyć: a) a lub m 2 b) m zred h E a 8ma E osc h 4 2
Systemy Ochrony Powietrza Ćwiczenia Laboratoryjne
 ś POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr nż. Łukasz Amanowcz Systemy Ochrony Powetrza Ćwczena Laboratoryjne 2 TEMAT ĆWICZENIA: Oznaczane lczbowego rozkładu lnowych projekcyjnych
ś POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr nż. Łukasz Amanowcz Systemy Ochrony Powetrza Ćwczena Laboratoryjne 2 TEMAT ĆWICZENIA: Oznaczane lczbowego rozkładu lnowych projekcyjnych
relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
 1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
Prowadzący. http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5)
 Tomasz Lubera dr Tomasz Lubera mail: luberski@interia.pl Prowadzący http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5) Konsultacje: we wtorki
Tomasz Lubera dr Tomasz Lubera mail: luberski@interia.pl Prowadzący http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5) Konsultacje: we wtorki
TRANZYSTOR BIPOLARNY CHARAKTERYSTYKI STATYCZNE
 POLITHNIKA RZSZOWSKA Katedra Podstaw lektronk Instrkcja Nr4 F 00/003 sem. letn TRANZYSTOR IPOLARNY HARAKTRYSTYKI STATYZN elem ćwczena jest pomar charakterystyk statycznych tranzystora bpolarnego npn lb
POLITHNIKA RZSZOWSKA Katedra Podstaw lektronk Instrkcja Nr4 F 00/003 sem. letn TRANZYSTOR IPOLARNY HARAKTRYSTYKI STATYZN elem ćwczena jest pomar charakterystyk statycznych tranzystora bpolarnego npn lb
Badanie współzależności dwóch cech ilościowych X i Y. Analiza korelacji prostej
 Badane współzależnośc dwóch cech loścowych X Y. Analza korelacj prostej Kody znaków: żółte wyróżnene nowe pojęce czerwony uwaga kursywa komentarz 1 Zagadnena 1. Zwązek determnstyczny (funkcyjny) a korelacyjny.
Badane współzależnośc dwóch cech loścowych X Y. Analza korelacj prostej Kody znaków: żółte wyróżnene nowe pojęce czerwony uwaga kursywa komentarz 1 Zagadnena 1. Zwązek determnstyczny (funkcyjny) a korelacyjny.
ZADANIE 9.5. p p T. Dla dwuatomowego gazu doskonałego wykładnik izentropy = 1,4 (patrz tablica 1). Temperaturę spiętrzenia obliczymy następująco
 ZADANIE 9.5. Do dyszy Bendemanna o rzekroju wylotowym A = mm doływa owetrze o cśnenu =,85 MPa temeraturze t = C, z rędkoścą w = 5 m/s. Cśnene owetrza w rzestrzen, do której wyływa owetrze z dyszy wynos
ZADANIE 9.5. Do dyszy Bendemanna o rzekroju wylotowym A = mm doływa owetrze o cśnenu =,85 MPa temeraturze t = C, z rędkoścą w = 5 m/s. Cśnene owetrza w rzestrzen, do której wyływa owetrze z dyszy wynos
Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 1. Układy równań liniowych
 Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Fazy i ich przemiany
 Układy i fazy Fazy i ich przemiany Co to jest faza? 1. Faza to forma występowania materii jednolita w całej objętości pod względem składu chemicznego i właściwości fizycznych (Atkins) 2. Faza to część
Układy i fazy Fazy i ich przemiany Co to jest faza? 1. Faza to forma występowania materii jednolita w całej objętości pod względem składu chemicznego i właściwości fizycznych (Atkins) 2. Faza to część
W praktyce często zdarza się, że wyniki obu prób możemy traktować jako. wyniki pomiarów na tym samym elemencie populacji np.
 Wykład 7 Uwaga: W praktyce często zdarza sę, że wynk obu prób możemy traktować jako wynk pomarów na tym samym elemence populacj np. wynk x przed wynk y po operacj dla tego samego osobnka. Należy wówczas
Wykład 7 Uwaga: W praktyce często zdarza sę, że wynk obu prób możemy traktować jako wynk pomarów na tym samym elemence populacj np. wynk x przed wynk y po operacj dla tego samego osobnka. Należy wówczas
Wykład 3. Diagramy fazowe P-v-T dla substancji czystych w trzech stanach. skupienia. skupienia
 Wykład 3 Substancje proste i czyste Przemiany w systemie dwufazowym woda para wodna Diagram T-v dla przejścia fazowego woda para wodna Diagramy T-v i P-v dla wody Punkt krytyczny Temperatura nasycenia
Wykład 3 Substancje proste i czyste Przemiany w systemie dwufazowym woda para wodna Diagram T-v dla przejścia fazowego woda para wodna Diagramy T-v i P-v dla wody Punkt krytyczny Temperatura nasycenia
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Natalia Nehrebecka. Wykład 2
 Natala Nehrebecka Wykład . Model lnowy Postad modelu lnowego Zaps macerzowy modelu lnowego. Estymacja modelu Wartośd teoretyczna (dopasowana) Reszty 3. MNK przypadek jednej zmennej . Model lnowy Postad
Natala Nehrebecka Wykład . Model lnowy Postad modelu lnowego Zaps macerzowy modelu lnowego. Estymacja modelu Wartośd teoretyczna (dopasowana) Reszty 3. MNK przypadek jednej zmennej . Model lnowy Postad
