Warunki równowagi i rozkład kanoniczny. H0 E 1 EL 8E 1 < W i HE i L ~ E i W 2 E - E 1 W 1 E 1. iloczyn W 2 HE - E 1 L W 1 HE 1 L E 1 = E
|
|
|
- Michalina Chmiel
- 6 lat temu
- Przeglądów:
Transkrypt
1 Warunki równowagi i rozkład kanoniczny. W HEL = W 1 HE 1 L W 2 HE - E 1 L 8E 1 < H0 E 1 EL W i HE i L ~ E i N W 2 E - E 1 W 1 E 1 iloczyn W 2 HE - E 1 L W 1 HE 1 L E 1 = 0 E 1 = E
2 W 2 HE - E 1 L W 1 HE 1 L ma bardzo ostre maksimum dla pewnego podziału: E 1 = E * 1, E 2 = E - E * 1. PokaŜemy obecnie, Ŝe ten podział odpowiada równowadze pomiędzy podukładami. E * 1 określone jest przez warunek : W 1 HE 1 L W 2 HE 2 L = max przy E 1 + E 2 = E = const lub równowaŝnie S 1 HE 1 Lêk B S 2 HE 2 Lêk B 1 HE 1 L+S 2 HE 2 LDêk B = max î S 1 HE 1 L + S 2 HE 2 L = max przy E 1 + E 2 = E = const
3 ZauwaŜmy równieŝ, Ŝe W 1 HE * 1 L W 2 HE - E * 1 L W HEL i j E k D y z W 1 HE * 1 L W 2 HE - E * 1 L { lub Odległość między poziomami N a Maksymalna ilość moŝliwych wartości E 1 ln W 1 HE 1 * L + ln W 2 HE - E 1 * L ln W HEL a ln N + ln W 1 HE 1 * L + ln W 2 HE - E 1 * L
4 Tzn. w granicy termodynamicznej; w równowadze: ln W HEL > ln W 1 HE * 1 L + ln W 2 HE - E * 1 L tzn. S = S 1 + S 2 : addytywność entropii liczonej dla E * * 1, E - E 1 To co pokazaliśmy moŝna streścić następująco: 9 W HEL> W 1 HE 1 * L W 2 H E 2 * L S HEL> S 1 H E 1 * L + S 2 H E 2 * L gdzie E 1 * maksymalizuje wyraŝenie 9 W 1 HE 1 L W 2 H E 2 L S 1 H E 1 L + S 2 H E 2 L przy ograniczeniu E 1 + E 2 = const
5 mamy więc S 1 H E 1 L + S 2 H E 2 L = max przy E 1 + E 2 = const = E fi d@ S 1 H E 1 L + S 2 H E 2 LD = 0 przy d E 1 + de 2 = 0 î i j k S 1 E 1 ƒ E * 1=E 1 - S 2 E 2 ƒ E * 2=E 2 y z de 1 = 0 " de 1 { Ω Ω Ø Ø 1 1 T 1 T 2 î T 1 = T 2 Odtworzyliśmy więc warunki równowagi układ-otoczenie(podukład) w przypadku osłony adiabatycznej
6 Podobnie moŝna wyprowadzić warunki równowagi w przypadku, gdy istnieje moŝliwość wymiany cząstek oraz gdy ścianki są ruchome. wtedy partycja równowagowa określona jest przez E 1 = E 1 *, E 2 = E 2 * = E - E 1 *, N 1 = N 1 *, N 2 = N 2 * = N - N 1 *, V 1 = V 1 *, V 2 = V 2 * = V -V 1 * î T 1 = T 2, m 1 = m 2, p 1 = p 2 - dodatkowo pokazaliśmy wcześniej addytywność entropii dla stanu równowagi
7 Wzrost entropii przy zdąŝaniu układów do równowagi Mamy dwa oddzielne podukłady ' 1' i ' 2 ' z partycjami IE 0 1, N 0 1, V 0 1 M oraz IE 0 2, N 0 2, V 0 2 M, które są róŝne od partycji równowagowej : HE 1 *, N 1 *, V 1 *, E 2 *, N 2 *, V 2 * L Jeśli teraz pozwolim y na wym ianę energii, cząstek oraz na zm iany objętości wtedy system jako całość osiągnie stan równowagi. W tym nowym stanie równowagowym entropia całego układu spełnia następujący związek : S 1+2 HE, V, NL = S 1 HE 1 *, N 1 *, V 1 * L + S 2 HE 2 *, N 2 *, V 2 * L S 1 IE 1 0, N 1 0, V 1 0 M + S 2 IE 2 0, N 2 0, V 2 0 M = S pocz S końcowa S początkowa
8 E(i) : i-zbiór liczb kw. charakteryzujący mikrostan układu Otoczenie- termostat układ Otoczenie izolacja adiabatyczna: DQ =0 E c = const Układ moŝe wymieniać energię z otoczeniem Policzymy prawdopodobieństwo P(i) tego, Ŝe układ znajduje się w mikrostanie o energii E(i). 12
9 Zanim przystąpimy do rachunków posłuŝymy się przykładem = 12 Białe kostki: termostat Czerwona kostka: układ Wynik na kostce czerwonej monitorujemy jedynie wtedy gdy suma wszystkich oczek = reprezentuje tutaj stałość energii U+O. Pytamy o częstość wystąpienia 1,2,3,4,5,6 na k. cz. P H1L = 2 25 P H2L = P H5L = P H6L = 5 25 P HiL = W O HE C - E HiLL W O+U HE C L
10 P HiL = W O HE C - E HiLL W O+U HE C L S O HE C -E HiLL- S O+U HE C L = k B Wzór wynika z częstościowej def. prawdopodobieństwa i z załoŝenia równego, a priori prawdopodobieństwa wszystkich mikrostanów U + O (załoŝenie moleku- -larnego chaosu). ZałóŜmy obecnie, Ŝe w równowadze średnia energia układu wynosi UH EL, a otoczenia E C - U. Przy tym podpodziale S O+U HE C L = S O HE C - UL + S U HUL Hpatrz poprzednie rozwaŝanial Podobnie, e S O HE C - E HiLL = S O H E C - U + U - E HiL L = Hrozwijamy wokół połoŝenia równowagi L = S O HE C - UL + S O e ƒ e=e C-U HU - E HiLL +
11 UWAGA: opuszczone wyrazy znikają w granicy termodynamicznej ( wziętej po M-cząstkach całości tj. U+O; Termostat ma nieskończenie więcej stopni swobody niŝ układ- z definicji-: S O+U HE C L = S O HE C - UL + S U HUL S O HE C - E HiLL = S O HE C - UL + S O e ƒ e=e C-U HU - E HiLL = S O HE C - UL + U - E HiL T O P HiL = W O HE C - E HiLL W O+U HE C L = S O HE C -E HiLL- S O+U HE C L k B U - E HiL (wyraŝenie pod eksponentą) T O - S U HUL
12 Stąd P HiL = S O HE C -E HiLL- S O+U HE C L k B = U- T O S U HE U L k B T O â - E HiL k B T O H'L ślad po termostacie pozostał jedynie jako T O H+ warunki term alizacjil H''L czynnik 1 k B T O występuje tak często, Ŝe pomija się ' O' oraz oznacza 1 k B T O przez b : 1 k B T O 1 k B T b U- T O S U HE U L = F Hrównowagowypotencjał Helmholtza ukł.l
13 P HiL = bf - b E HiL ó Hpełni rolę niezaleŝnej od stanu układu stałej normalizacyjnej rozkładu L P HiL = 1 = bf - b E HiL stąd dalej Z F-cja rozdziału rozkładu kanonicznego bf Z = 1 î F = - b -1 ln Z
14 Rozkład kanoniczny podsumowanie : P i = Z -1 - b E HiL, b = Z = - b E HiL 1 k B T F = U - TS = - b -1 ln Z + warunki termalizacji
15 Średnia energia U dana jest przez: U = E HiL P HiL = E HiL Z -1 - b E HiL = Z -1 E HiL - b E HiL = Z -1i j - k b - b E HiLy z { = Z -1i j - k b Z y z = - { ln ZD = F - T H Fê TL = H F + TSL Hco bardzo dobrze znamyl
16 Model dwustanowy liczony rozkładem kanonicznym + E 0 HN + - cząstekl - E 0 HN - - cząstekl E = E O s, gdzie s = ± 1; s: stopień swobody parametry - -zujący stan pojedynczej cząstki Z = - b E HiL 8 i< = 8 s 1, s 2,..., s N < s a = ± 1 =... = 8s 1 = ±1< 8s 2 = ±1< 8s N = ±1< E HiL E Hs 1, s 2,..., s N L = E O a=1,..,n s a S
17 stąd Z = 8s 1 = ±1< 8s 2 = ±1<... 8s N = ±1< e - b E O Hs 1 + s s N L = = i j k8s 1 = ±1< e -b E O s 1 y z { i j k 8s 2 = ±1< y e - b E O s 2 z... i j { k 8s N = ±1< y e - b E O s N z { = Z 1 N gdzie Z 1 = 8s 1 = ±1< e -b E O s 1 = e - be O + e be 0 = 2 coshhb E O L
18 Zatem Z coshhb E O LD N i mamy F = -k B T N ln@2 coshhb E O LD U = - Z -1 b Z = -N E O tanh HbE O L itd. Otrzymalismy wzory identyczne z mikrokanonicznymi poza ujemną temperaturą- bowiem tutaj T jest temperaturą otoczenia; Musimy dołączyć warunek termalizacji- w przeciwnym razie nie mamy równowagi
19 Wielki rozkład kanoniczny Otoczenie- termostat Otoczenie układ E C = const N C = const V C = const Układ moŝe wymieniać energię i cząstki z otoczeniem P Hi, NL = W O HE C - E Hi, NLL W O+U HE C, N C L S O HE C -E Hi,NL, N C - NL- S O+U HE C,N C L = k B 24
20 P Hi, NL = W O HE C - E Hi, NLL W O+U HE C, N C L S O HE C -E Hi,NL, N C - NL- S O+U HE C,N C L = k B ZałóŜmy, Ŝe w równowadze U+O: energia układu: U energia otoczenia: E C - U liczba cząstek w ukł. N U liczba cząstek w otoczeniu: N C - N U S O+U H E C, N C L = S O HE C -U, N C - N U L + S U HU, N U L Jak poprzednio, rozwijamy entropię otoczenia wokół stanu równowagi: S O HE C -E Hi, NL, N C - NL = S O H E C - U + U - E Hi, NL, N C - N U + N U - NL
21 S O HE C -E Hi,NL, N C - NL- S O+U HE C,N C L k B S O HE C - E Hi, NL, N C - NL = S O H E C - U + U - E Hi, NL, N C - N U + N U - NL S O+U H E C, N C L = S O HE C - U, N C - N U L + S U HU, N U L S O HE C - E Hi, NL, N C - NL = S O HE C - U, N C - N U L + 1 T O + S O e ƒ e=e C-U, h=n C -N U HU - E Hi, NLL - m O T O + S O h ƒ e=e C-U, h=n C -N U HN U - NL = S O HE C - U, N C - N U L + U - E Hi, NL T O - m O T O HN U - NL
22 S O HE C -E Hi,NL, N C - NL - S O+U HE C,N C L P Hi, NL = k B S O HE C - E Hi, NL, N C - NL - S O+U H E C, N C L = U - E Hi, NL T O - m O T O HN U - NL - S U HU, N U L i wstawiając do wyjściowego rozkładu otrzymamy: P Hi, NL = U- T O S U HE U L- m O N U k B T O â - E Hi,NL-m O N k B T O = Z -1 - E Hi,NL-m O N k B T O U - T O S U HE U L - m O N U = F - G = X = -p O V U HponiewaŜ wielkości określone są w równowadze - opuszczamy indeks ' O'L
23 P Hi, NL = U- T O S U HE U L- m O N U k B T O â - E Hi,NL-m O N k B T O = Z -1 - E Hi,NL-m O N k B T O U - T O S U HE U L - m O N U = F - G = X = -p O V U HponiewaŜ wielkości określone są w równowadze - opuszczamy indeks ' O'L Rozkład wielki kanoniczny: P Hi, NL = - bpv - b@e Hi,NL -mnd = Z -1 - b@e Hi,NL -mnd Z = - b@e Hi,NL-mND = 8i, N< 8N< b mn - b E Hi,NL X = -pv = - b -1 ln Z + warunki termalizacji
24 Rozkład izobaryczno-izotermiczny Rozkład izobaryczno - izotermiczny : Dopuszczamy zmianę objętości (N=const) P Hi, VL = b@u- T O S U HE U L + p O V U D - b@e Hi,VL +p O VD = bg - b@e Hi,VL + pvd = Z -1 - b@e Hi,VL + pvd Z = V - b@e Hi,NL + pvd = V - b pv - b E Hi,VL G = - b -1 ln Z (wyprowadzić) + warunki termalizacji
25 Czy moŝna wyeliminować wszystkie ograniczenia i pozwolić na: wymianę energii, wymianę cząstek i fluktuację objętości? Odpowiedź: Taka procedura nie prowadzi do nowego rozkładu bowiem T, m oraz p nie są niezaleŝne!
26 P Hi, NL = b@u- T O S U HE U L - m O N U D P Hi, VL = b@u- T O S U HE U L + p O V U D -b@e Hi,VL - m O ND -b@e Hi,VL +p O VD P Hi, N, VL = b@u- T O S U HE U L - m O N U + p O V U D -b@e Hi,N,VL - m O N + p O VD P Hi, N, VL = -b@e Hi,VL - m O N + p O VD V N - b@e Hi, N, VL - m O N + p O VD = 1 Hodpowiednik relacji Gibbsa - DuhemaL
27 Związek między rozkładem kanonicznym i mikrokanonicznym W W HE, V, NL = df E HiL = E 1 = d H E - E HiL L î Z = - b E HiL = EO d HE - E HiLL - b E E = i = EO j k ZHT, V, NL = d HE - E HiLL y z - b E E = { EO W HE, N, VL -b E E EO W HE, N, VL - b E E Htr. Laplace' a rozkładu mikrol
28 Przykład: Klasyczny gaz doskonały N E H = j=1 p j2 2 m p j Hp x,j, p y,j, p z,j L Z HN, V, TL = 1 h 3 N N! 3 p p N 3 r r N e - b H = V N h 3 N N! e - p m k B T 3 p 1... e - p N 2 2 m k B T 3 p N = VN N! i j k H2 p mk B TL 3ê2 h 3 y z { N = V N N! H2 pl 3 Nê2 l 3 N
29 Z HN, V, TL = VN N! ih2 p mk B TL 3ê2 j k h 3 y z { N H1L Energia swobodna: F = -k B T ln Z = -k B T i jn ln V + 3 N k 2 ln 2 pmk B T - ln N! y z h 2 { > -k B T i jn ln V + 3 N k 2 ln 2 pmk B T - N ln N + N y z h 2 { = -k B T N i j ln V k N + H2L równanie stanu: 3 2 ln 2 pmk B T + 1 y z h 2 { p = - i j F k V y z { T,N = Nk B T V î pv = N k B T
30 F > -k B T N i j ln V k N ln 2 pmk B T + 1 y z h 2 { H3L entropia: S = - i j F k T y z { V,N = k B N i j ln V k N ln 2 pmk B T y z h 2 2{ H4L energia wewnętrzna: U = F + TS = 3 2 N k B T i j 3 k 2 pvy z HU nie zaleŝy od VL { H5L C V = i j U k T y z { V = 3 2 N k B (niezgodne z III zasadą t. -nieuwzględnienie efektów kwantowych)
Warunki równowagi. Rozkłady: kanoniczny, wielki kanoniczny, izobaryczno-izotermiczny
 Warunki równowagi. Rozkłady: kanoniczny, wielki kanoniczny, izobaryczno-izotermiczny 1 Niestety, rachunki przy użyciu rozkładu mikrokanonicznego nie są łatwe. Wprowadzimy teraz inne rozkłady, przy pomocy
Warunki równowagi. Rozkłady: kanoniczny, wielki kanoniczny, izobaryczno-izotermiczny 1 Niestety, rachunki przy użyciu rozkładu mikrokanonicznego nie są łatwe. Wprowadzimy teraz inne rozkłady, przy pomocy
Rozkłady: Kanoniczny, Wielki Kanoniczny, Izobaryczno-Izotermiczny
 Rozkłady: Kanoniczny, Wielki Kanoniczny, Izobaryczno-Izotermiczny 1 Rozkład Mikrokanoniczny (przypomnienie) S= k B ln( (E,V,{x i },{N j }) ) Z fenomenologii: Niestety, rachunki przy użyciu rozkładu mikrokanonicznego
Rozkłady: Kanoniczny, Wielki Kanoniczny, Izobaryczno-Izotermiczny 1 Rozkład Mikrokanoniczny (przypomnienie) S= k B ln( (E,V,{x i },{N j }) ) Z fenomenologii: Niestety, rachunki przy użyciu rozkładu mikrokanonicznego
Statystyka nieoddziaływujących gazów Bosego i Fermiego
 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bozony: fotony (kwanty pola elektromagnetycznego, których liczba nie jest zachowana mogą być pojedynczo pochłaniane lub tworzone. W konsekwencji,
Statystyka nieoddziaływujących gazów Bosego i Fermiego Bozony: fotony (kwanty pola elektromagnetycznego, których liczba nie jest zachowana mogą być pojedynczo pochłaniane lub tworzone. W konsekwencji,
Wykład 3. Entropia i potencjały termodynamiczne
 Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
WYKŁAD 9: Rozkład mikrokanoniczny i entropia Boltzmanna
 WYKŁAD 9: Rozkład mikrokanoniczny i entropia Boltzmanna (Zadaniem Fizyki Statystycznej jest zrozumienie własności (równowagowych i nierównowagowych materii w oparciu o oddziaływania międzymolekularne)
WYKŁAD 9: Rozkład mikrokanoniczny i entropia Boltzmanna (Zadaniem Fizyki Statystycznej jest zrozumienie własności (równowagowych i nierównowagowych materii w oparciu o oddziaływania międzymolekularne)
Wykład 12. Rozkład wielki kanoniczny i statystyki kwantowe
 Wykład 12 Rozkład wielki kanoniczny i statystyki kwantowe dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy
Wykład 12 Rozkład wielki kanoniczny i statystyki kwantowe dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny
 Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Elementy termodynamiki i wprowadzenie do zespołów statystycznych. Katarzyna Sznajd-Weron
 Elementy termodynamiki i wprowadzenie do zespołów statystycznych Katarzyna Sznajd-Weron Wielkości makroskopowe - termodynamika Termodynamika - metoda fenomenologiczna Fenomenologia w fizyce: widzimy jak
Elementy termodynamiki i wprowadzenie do zespołów statystycznych Katarzyna Sznajd-Weron Wielkości makroskopowe - termodynamika Termodynamika - metoda fenomenologiczna Fenomenologia w fizyce: widzimy jak
Wykład 1 i 2. Termodynamika klasyczna, gaz doskonały
 Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
II Zasada Termodynamiki c.d.
 Wykład 5 II Zasada Termodynamiki c.d. Pojęcie entropii i temperatury absolutnej II zasada termodynamiki dla procesów nierównowagowych Równania Gibbsa dla procesów quasistatycznych Równania Eulera Relacje
Wykład 5 II Zasada Termodynamiki c.d. Pojęcie entropii i temperatury absolutnej II zasada termodynamiki dla procesów nierównowagowych Równania Gibbsa dla procesów quasistatycznych Równania Eulera Relacje
Wykład 8 i 9. Hipoteza ergodyczna, rozkład mikrokanoniczny, wzór Boltzmanna
 Wykład 8 i 9 Hipoteza ergodyczna, rozkład mikrokanoniczny, wzór Boltzmanna dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW)
Wykład 8 i 9 Hipoteza ergodyczna, rozkład mikrokanoniczny, wzór Boltzmanna dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW)
Elementy termodynamiki
 Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 5 stycznia 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 5 stycznia 2019 1 / 27 Wielkości
Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 5 stycznia 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 5 stycznia 2019 1 / 27 Wielkości
Wielki rozkład kanoniczny
 , granica termodynamiczna i przejścia fazowe Instytut Fizyki 2015 Podukład otwarty Podukład otwarty S opisywany układ + rezerwuar R Podukład otwarty S opisywany układ + rezerwuar R układ S + R jest izolowany
, granica termodynamiczna i przejścia fazowe Instytut Fizyki 2015 Podukład otwarty Podukład otwarty S opisywany układ + rezerwuar R Podukład otwarty S opisywany układ + rezerwuar R układ S + R jest izolowany
Termodynamika. Część 11. Układ wielki kanoniczny Statystyki kwantowe Gaz fotonowy Ruchy Browna. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 11 Układ wielki kanoniczny Statystyki kwantowe Gaz fotonowy Ruchy Browna Janusz Brzychczyk, Instytut Fizyki UJ Układ otwarty rozkład wielki kanoniczny Rozważamy układ w równowadze termicznej
Termodynamika Część 11 Układ wielki kanoniczny Statystyki kwantowe Gaz fotonowy Ruchy Browna Janusz Brzychczyk, Instytut Fizyki UJ Układ otwarty rozkład wielki kanoniczny Rozważamy układ w równowadze termicznej
Fizyka statystyczna Zespół kanoniczny i wielki zespół kanoniczny Statystyki kwantowe. P. F. Góra
 Fizyka statystyczna Zespół kanoniczny i wielki zespół kanoniczny Statystyki kwantowe P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Zespół kanoniczny Zespół mikrokanoniczny jest (przynajmniej w warstwie
Fizyka statystyczna Zespół kanoniczny i wielki zespół kanoniczny Statystyki kwantowe P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Zespół kanoniczny Zespół mikrokanoniczny jest (przynajmniej w warstwie
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Teoria kinetyczno cząsteczkowa
 Teoria kinetyczno cząsteczkowa Założenie Gaz składa się z wielkiej liczby cząstek znajdujących się w ciągłym, chaotycznym ruchu i doznających zderzeń (dwucząstkowych) Cel: Wyprowadzić obserwowane (makroskopowe)
Teoria kinetyczno cząsteczkowa Założenie Gaz składa się z wielkiej liczby cząstek znajdujących się w ciągłym, chaotycznym ruchu i doznających zderzeń (dwucząstkowych) Cel: Wyprowadzić obserwowane (makroskopowe)
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów
 Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
= = Budowa materii. Stany skupienia materii. Ilość materii (substancji) n - ilość moli, N liczba molekuł (atomów, cząstek), N A
 Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
Wykład FIZYKA I. 14. Termodynamika fenomenologiczna cz.ii. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
TERMODYNAMIKA FENOMENOLOGICZNA
 TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
Teoria ergodyczności: co to jest? Średniowanie po czasie vs. średniowanie po rozkładach Twierdzenie Poincare o powrocie Twierdzenie ergodyczne
 WYKŁAD 23 1 Teoria ergodyczności: co to jest? Średniowanie po czasie vs. średniowanie po rozkładach Twierdzenie Poincare o powrocie Twierdzenie ergodyczne (Birkhoff, Ter Haar) Hipoteza semi-ergodyczna
WYKŁAD 23 1 Teoria ergodyczności: co to jest? Średniowanie po czasie vs. średniowanie po rozkładach Twierdzenie Poincare o powrocie Twierdzenie ergodyczne (Birkhoff, Ter Haar) Hipoteza semi-ergodyczna
Agata Fronczak Elementy fizyki statystycznej
 Agata Fronczak Elementy fizyki statystycznej Skrypt do wykładu i ćwiczeń rachunkowych dla kierunku Fotonika (rok III, semestr 5) na Wydziale Fizyki PW Warszawa 2016 Spis treści 1. Termodynamika klasyczna,
Agata Fronczak Elementy fizyki statystycznej Skrypt do wykładu i ćwiczeń rachunkowych dla kierunku Fotonika (rok III, semestr 5) na Wydziale Fizyki PW Warszawa 2016 Spis treści 1. Termodynamika klasyczna,
S ścianki naczynia w jednostce czasu przekazywany
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
Ogólny schemat postępowania
 Ogólny schemat postępowania 1. Należy zdecydować, który rozkład prawdopodobieństwa chcemy badać. Rozkład oznaczamy przez P; zależy od zespołu statystycznego. 2. Narzucamy warunek równowagi szczegółowej,
Ogólny schemat postępowania 1. Należy zdecydować, który rozkład prawdopodobieństwa chcemy badać. Rozkład oznaczamy przez P; zależy od zespołu statystycznego. 2. Narzucamy warunek równowagi szczegółowej,
Podstawy termodynamiki
 Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Wykład 3. Zerowa i pierwsza zasada termodynamiki:
 Wykład 3 Zerowa i pierwsza zasada termodynamiki: Termodynamiczne funkcje stanu. Parametry extensywne i intensywne. Pojęcie równowagi termodynamicznej. Tranzytywność stanu równowagi i pojęcie temperatury
Wykład 3 Zerowa i pierwsza zasada termodynamiki: Termodynamiczne funkcje stanu. Parametry extensywne i intensywne. Pojęcie równowagi termodynamicznej. Tranzytywność stanu równowagi i pojęcie temperatury
Elementy fizyki statystycznej
 5-- lementy fizyki statystycznej ermodynamika Gęstości stanów Funkcje rozkładu Gaz elektronów ermodynamika [K] 9 wszechświat tuż po powstaniu ermodynamika to dział fizyki zajmujący się energią termiczną
5-- lementy fizyki statystycznej ermodynamika Gęstości stanów Funkcje rozkładu Gaz elektronów ermodynamika [K] 9 wszechświat tuż po powstaniu ermodynamika to dział fizyki zajmujący się energią termiczną
FIZYKA STATYSTYCZNA. d dp. jest sumaryczną zmianą pędu cząsteczek zachodzącą na powierzchni S w
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
Układy statystyczne. Jacek Jurkowski, Fizyka Statystyczna. Instytut Fizyki
 Instytut Fizyki 2015 Stany mikroskopowe i makroskopowe w układzie wielopoziomowym Stany mikroskopowe i makroskopowe w układzie wielopoziomowym N rozróżnialnych cząstek, z których każda może mieć energię
Instytut Fizyki 2015 Stany mikroskopowe i makroskopowe w układzie wielopoziomowym Stany mikroskopowe i makroskopowe w układzie wielopoziomowym N rozróżnialnych cząstek, z których każda może mieć energię
Elementy termodynamiki
 Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 marca 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 marca 2019 1 / 37 Dwa poziomy
Elementy termodynamiki Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 marca 2019 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 marca 2019 1 / 37 Dwa poziomy
Zasady Termodynamiki
 Zasady Termodynamiki I-sza zasada termodynamiki: - bilans energii w procesie przejścia układu ze stanu A do stanu B - identyfikacja kanałów przekazu B A W oparciu o I-szą zasadę wiemy, Ŝe Przekaz moŝe
Zasady Termodynamiki I-sza zasada termodynamiki: - bilans energii w procesie przejścia układu ze stanu A do stanu B - identyfikacja kanałów przekazu B A W oparciu o I-szą zasadę wiemy, Ŝe Przekaz moŝe
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron
 Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
Równowaga w układach termodynamicznych. Katarzyna Sznajd-Weron Zagadka na początek wykładu Diagram fazowy wody w powiększeniu, problem metastabilności aktualny (Nature, 2011) Niższa temperatura topnienia
Co to jest model Isinga?
 Co to jest model Isinga? Fakty eksperymentalne W pewnych metalach (np. Fe, Ni) następuje spontaniczne ustawianie się spinów wzdłuż pewnego kierunku, powodując powstanie makroskopowego pola magnetycznego.
Co to jest model Isinga? Fakty eksperymentalne W pewnych metalach (np. Fe, Ni) następuje spontaniczne ustawianie się spinów wzdłuż pewnego kierunku, powodując powstanie makroskopowego pola magnetycznego.
FIZYKA STATYSTYCZNA. Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych
 FIZYKA STATYSTYCZA Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych elementów takich jak atomy czy cząsteczki. Badanie ruchów pojedynczych cząstek byłoby bardzo trudnym
FIZYKA STATYSTYCZA Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych elementów takich jak atomy czy cząsteczki. Badanie ruchów pojedynczych cząstek byłoby bardzo trudnym
Fizyka statystyczna Zwyrodniały gaz Fermiego. P. F. Góra
 Fizyka statystyczna Zwyrodniały gaz Fermiego P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Fermiony w niskich temperaturach Wychodzimy ze znanego już wtrażenia na wielka sumę statystyczna: Ξ = i=0
Fizyka statystyczna Zwyrodniały gaz Fermiego P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Fermiony w niskich temperaturach Wychodzimy ze znanego już wtrażenia na wielka sumę statystyczna: Ξ = i=0
Wykład 4. II Zasada Termodynamiki
 Wykład 4 II Zasada Termodynamiki Ogólne sformułowanie: istnienie strzałki czasu Pojęcie entropii i temperatury absolutnej Ćwiczenia: Formy różniczkowe Pfaffa 1 I sza Zasada Termodynamiki: I-sza zasada
Wykład 4 II Zasada Termodynamiki Ogólne sformułowanie: istnienie strzałki czasu Pojęcie entropii i temperatury absolutnej Ćwiczenia: Formy różniczkowe Pfaffa 1 I sza Zasada Termodynamiki: I-sza zasada
Przegląd termodynamiki II
 Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
Zasady termodynamiki
 Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Termodynamika. Cel. Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa. William Thomson 1. Baron Kelvin
 Cel Termodynamika Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa Nicolas Léonard Sadi Carnot 1796 1832 Rudolf Clausius 1822 1888 William Thomson 1. Baron Kelvin 1824 1907 i inni...
Cel Termodynamika Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa Nicolas Léonard Sadi Carnot 1796 1832 Rudolf Clausius 1822 1888 William Thomson 1. Baron Kelvin 1824 1907 i inni...
Statystyka nieoddziaływujących gazów Bosego: kondensacja Bosego- Einsteina
 Statystyka nieoddziaływujących gazów Bosego: kondensacja Bosego- Einsteina Silnie zwyrodniały gaz bozonów o niezerowej masie spoczynkowej Gdy liczba cząstek nie jest zachowywana, termodynamika nieoddziaływujących
Statystyka nieoddziaływujących gazów Bosego: kondensacja Bosego- Einsteina Silnie zwyrodniały gaz bozonów o niezerowej masie spoczynkowej Gdy liczba cząstek nie jest zachowywana, termodynamika nieoddziaływujących
e E Z = P = 1 Z e E Kanoniczna suma stanów Prawdopodobieństwo wystąpienia mikrostanu U E = =Z 1 Wartość średnia energii
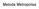 Metoda Metropolisa Z = e E P = 1 Z e E Kanoniczna suma stanów Prawdopodobieństwo wystąpienia mikrostanu U E = P E =Z 1 E e E Wartość średnia energii Średnia wartość A = d r N A r N exp[ U r N ] d r N exp[
Metoda Metropolisa Z = e E P = 1 Z e E Kanoniczna suma stanów Prawdopodobieństwo wystąpienia mikrostanu U E = P E =Z 1 E e E Wartość średnia energii Średnia wartość A = d r N A r N exp[ U r N ] d r N exp[
ę ą ę ó ń ń ń ó ń ó ó ń ź ą ę Ń ą ó ę ą ó ą ą ć ś ą ó ś ó ń ó ą Ń Ą ś ę ńś Ą ń ó ń ó ńś ó ś Ą ś ś ó ó ś ś ó ą ń ó ń Ę ń ć ńś ę ó ś ś Ę ń Ł ó ń ź ń ś ę
 ń ę ś Ą Ń ó ę ą ń ą ś Ł ń ń ź ń ś ó ń ę ę ę Ń ą ą ń ą ź ą ź ń ć ę ó ó ę ś ą ść ńś ś ę ź ó ń ó ń ę ń ą ń ś ę ó ó Ę ó ń ę ń ó ń ń ń ą Ę ą ź ą ą ń ó ą ę ó ć ą ś ę ó ą ń ś ę ą ę ó ń ń ń ó ń ó ó ń ź ą ę Ń ą
ń ę ś Ą Ń ó ę ą ń ą ś Ł ń ń ź ń ś ó ń ę ę ę Ń ą ą ń ą ź ą ź ń ć ę ó ó ę ś ą ść ńś ś ę ź ó ń ó ń ę ń ą ń ś ę ó ó Ę ó ń ę ń ó ń ń ń ą Ę ą ź ą ą ń ó ą ę ó ć ą ś ę ó ą ń ś ę ą ę ó ń ń ń ó ń ó ó ń ź ą ę Ń ą
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12
 Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
N a l e W y u n i k a ć d ł u g o t r w a ł e g o k o n t a k t u p o l a k i e r o w a n y c h p o w i e r z c h n i z w y s o k i m i t e m p e r a
 J L G 3 6 6 P A W I L O N O G R O D O W Y J L G 3 6 6 I N S T R U K C J A M O N T A V U I B E Z P I E C Z E Ń S T W A S z a n o w n i P a s t w o, D z i ę k u j e m y z a z a k u p p a w i l o n u o g
J L G 3 6 6 P A W I L O N O G R O D O W Y J L G 3 6 6 I N S T R U K C J A M O N T A V U I B E Z P I E C Z E Ń S T W A S z a n o w n i P a s t w o, D z i ę k u j e m y z a z a k u p p a w i l o n u o g
Termodynamika. Część 4. Procesy izoparametryczne Entropia Druga zasada termodynamiki. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Fizyka, technologia oraz modelowanie wzrostu kryształów
 Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Statystyki kwantowe. P. F. Góra
 Statystyki kwantowe P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Statystyki kwantowe Rozpatrujemy gaz doskonały o Hamiltonianie H = N i=1 p i 2 2m. (1) Zamykamy czastki w bardzo dużym pudle o idealnie
Statystyki kwantowe P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Statystyki kwantowe Rozpatrujemy gaz doskonały o Hamiltonianie H = N i=1 p i 2 2m. (1) Zamykamy czastki w bardzo dużym pudle o idealnie
Wielki rozkład kanoniczny
 Ćwiczenia nr 0 Wielki rozkład kanoniczny Jest to rozkład prawdopodobieństwa dla układu o zmiennej liczbie cząstek N. Liczbę cząstek możemy potraktować jako dodatkową liczbą kwantową układu. ψ jest to stan
Ćwiczenia nr 0 Wielki rozkład kanoniczny Jest to rozkład prawdopodobieństwa dla układu o zmiennej liczbie cząstek N. Liczbę cząstek możemy potraktować jako dodatkową liczbą kwantową układu. ψ jest to stan
Miejsce biofizyki we współczesnej nauce. Obszary zainteresowania biofizyki. - Powrót do współczesności. - obiekty mikroświata.
 Zakład Biofizyki Miejsce biofizyki we współczesnej nauce - trochę historii - Powrót do współczesności Obszary zainteresowania biofizyki - ekosystemy - obiekty makroświata - obiekty mikroświata - język
Zakład Biofizyki Miejsce biofizyki we współczesnej nauce - trochę historii - Powrót do współczesności Obszary zainteresowania biofizyki - ekosystemy - obiekty makroświata - obiekty mikroświata - język
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Obraz statyczny układu
 Termodynamika Obraz statyczny układu energia kinetyczna E k = mv 2 / 2 energia wewnetrzna energia powierzchniowa inne energie U inne parametry: T, m, P, V, S... Ep= mgh energia potencjalna STAN I PRZEMIANA
Termodynamika Obraz statyczny układu energia kinetyczna E k = mv 2 / 2 energia wewnetrzna energia powierzchniowa inne energie U inne parametry: T, m, P, V, S... Ep= mgh energia potencjalna STAN I PRZEMIANA
Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }
![Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] } Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }](/thumbs/64/51033976.jpg) Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
Fizyka statystyczna. This Book Is Generated By Wb2PDF. using
 http://pl.wikibooks.org/wiki/fizyka_statystyczna This Book Is Generated By Wb2PDF using RenderX XEP, XML to PDF XSL-FO Formatter 18-05-2014 Table of Contents 1. Fizyka statystyczna...4 Spis treści..........................................................................?
http://pl.wikibooks.org/wiki/fizyka_statystyczna This Book Is Generated By Wb2PDF using RenderX XEP, XML to PDF XSL-FO Formatter 18-05-2014 Table of Contents 1. Fizyka statystyczna...4 Spis treści..........................................................................?
Klasyczna mechanika statystyczna Gibbsa I
 Wykład III Mechanika statystyczna Klasyczna mechanika statystyczna Gibbsa I Wstępne uwagi Materia nas otaczająca, w szczególności gazy będące centralnym obiektem naszego zainteresowania, zbudowane są z
Wykład III Mechanika statystyczna Klasyczna mechanika statystyczna Gibbsa I Wstępne uwagi Materia nas otaczająca, w szczególności gazy będące centralnym obiektem naszego zainteresowania, zbudowane są z
Jednostki podstawowe. Tuż po Wielkim Wybuchu temperatura K Teraz ok. 3K. Długość metr m
 TERMODYNAMIKA Jednostki podstawowe Wielkość Nazwa Symbol Długość metr m Masa kilogramkg Czas sekunda s Natężenieprąduelektrycznego amper A Temperaturatermodynamicznakelwin K Ilość materii mol mol Światłość
TERMODYNAMIKA Jednostki podstawowe Wielkość Nazwa Symbol Długość metr m Masa kilogramkg Czas sekunda s Natężenieprąduelektrycznego amper A Temperaturatermodynamicznakelwin K Ilość materii mol mol Światłość
4 Przekształcenia pochodnych termodynamicznych
 4 Przekształcenia pochodnych termodynamicznych 4.1 Relacje Maxwella Pierwsza zasada termodynamiki może być zapisana w postaci niezależnej od reprezentacji jako warunek znikania formy Pfaffa: Stąd musi
4 Przekształcenia pochodnych termodynamicznych 4.1 Relacje Maxwella Pierwsza zasada termodynamiki może być zapisana w postaci niezależnej od reprezentacji jako warunek znikania formy Pfaffa: Stąd musi
Układ termodynamiczny Parametry układu termodynamicznego Proces termodynamiczny Układ izolowany Układ zamknięty Stan równowagi termodynamicznej
 termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
W8 40. Para. Równanie Van der Waalsa Temperatura krytyczna ci Przemiany pary. Termodynamika techniczna
 W8 40 Równanie Van der Waalsa Temperatura krytyczna Stopień suchości ci Przemiany pary 1 p T 1 =const T 2 =const 2 Oddziaływanie międzycz dzycząsteczkowe jest odwrotnie proporcjonalne do odległości (liczonej
W8 40 Równanie Van der Waalsa Temperatura krytyczna Stopień suchości ci Przemiany pary 1 p T 1 =const T 2 =const 2 Oddziaływanie międzycz dzycząsteczkowe jest odwrotnie proporcjonalne do odległości (liczonej
r. akad. 2005/ 2006 Jan Królikowski Fizyka IBC
 VIII.1 Pojęcia mikrostanu i makrostanu układu N punktów materialnych. Prawdopodobieństwo termodynamiczne. Entropia. VIII. Rozkład Boltzmanna VIII.3 Twierdzenie o wiriale Jan Królikowski Fizyka IBC 1 Uwagi
VIII.1 Pojęcia mikrostanu i makrostanu układu N punktów materialnych. Prawdopodobieństwo termodynamiczne. Entropia. VIII. Rozkład Boltzmanna VIII.3 Twierdzenie o wiriale Jan Królikowski Fizyka IBC 1 Uwagi
3 Potencjały termodynamiczne i transformacja Legendre a
 3 Potencjały termodynamiczne i transformacja Legendre a literatura: Ingarden, Jamiołkowski i Mrugała, Fizyka Statystyczna i ermodynamika, 9 W.I Arnold, Metody matematyczne mechaniki klasycznej, 14 3.1
3 Potencjały termodynamiczne i transformacja Legendre a literatura: Ingarden, Jamiołkowski i Mrugała, Fizyka Statystyczna i ermodynamika, 9 W.I Arnold, Metody matematyczne mechaniki klasycznej, 14 3.1
Wykład 2. Przykład zastosowania teorii prawdopodobieństwa: procesy stochastyczne (Markova)
 Wykład 2 Przykład zastosowania teorii prawdopodobieństwa: procesy stochastyczne (Markova) 1. Procesy Markova: definicja 2. Równanie Chapmana-Kołmogorowa-Smoluchowskiego 3. Przykład dyfuzji w kapilarze
Wykład 2 Przykład zastosowania teorii prawdopodobieństwa: procesy stochastyczne (Markova) 1. Procesy Markova: definicja 2. Równanie Chapmana-Kołmogorowa-Smoluchowskiego 3. Przykład dyfuzji w kapilarze
WYKŁAD 15. Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego
 WYKŁAD 15 Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego 1 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bosony
WYKŁAD 15 Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego 1 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bosony
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Termodynamika Część 3
 Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
Podstawy fizyki sezon 1 X. Elementy termodynamiki
 Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
Wykład 6 Ciepło właściwe substancji prostych Ciepło właściwe gazów doskonałych Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C )
 Wykład 6 Ciepło właściwe substancji prostych Ciepło właściwe gazów doskonałych Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C ) ZaleŜność stosunku R od temperatury dla gazu doskonałego
Wykład 6 Ciepło właściwe substancji prostych Ciepło właściwe gazów doskonałych Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C ) ZaleŜność stosunku R od temperatury dla gazu doskonałego
Druga zasada termodynamiki
 Waldemar Ufnalski Wprowadzenie do termodynamiki chemicznej Wykład 4 Druga zasada termodynamiki. Carnot L. Boltzmann 1 Wykład 4 4.1. Fakty doświadczalne i sformułowanie drugiej zasady termodynamiki 2 Wszystkie
Waldemar Ufnalski Wprowadzenie do termodynamiki chemicznej Wykład 4 Druga zasada termodynamiki. Carnot L. Boltzmann 1 Wykład 4 4.1. Fakty doświadczalne i sformułowanie drugiej zasady termodynamiki 2 Wszystkie
ĺ ą Ł ĺĺ ĺ ĺĺĺ ĺ ĺ ę Żĺ ĺĺĺĺ ę ĺ ĺ ĺĺ ĺ ą ę ś Ść Ą ę ę ś ś ś ę ý ś ż ę ś ý ę ę ń ę ą Ż ę ę ý ś ń ą ĺ ż ż ś ć ż Ż ś ć ś ś ś ą ę ś ę ę Ś ęś ś ś ś ę ęć ż
 Ą ą ą ż ą ę ń ĺ Ą ą ĺ ń ą ú ĺ ń ĺ Ż ĺ ĺ Ą ę ś ę ę ń ĺ ĺ ĺ ĺ ą ĺ ń ś đ ę ą ĺ ń ą Ż ę ĺ ż í ĺĺ ż ę ĺ ĺ ĺ Ź ę ĺ Ż Ż ĺ ĺ ą Ł ĺĺ ĺ ĺĺĺ ĺ ĺ ę Żĺ ĺĺĺĺ ę ĺ ĺ ĺĺ ĺ ą ę ś Ść Ą ę ę ś ś ś ę ý ś ż ę ś ý ę ę ń ę ą Ż
Ą ą ą ż ą ę ń ĺ Ą ą ĺ ń ą ú ĺ ń ĺ Ż ĺ ĺ Ą ę ś ę ę ń ĺ ĺ ĺ ĺ ą ĺ ń ś đ ę ą ĺ ń ą Ż ę ĺ ż í ĺĺ ż ę ĺ ĺ ĺ Ź ę ĺ Ż Ż ĺ ĺ ą Ł ĺĺ ĺ ĺĺĺ ĺ ĺ ę Żĺ ĺĺĺĺ ę ĺ ĺ ĺĺ ĺ ą ę ś Ść Ą ę ę ś ś ś ę ý ś ż ę ś ý ę ę ń ę ą Ż
Kinetyczna teoria gazów Termodynamika. dr Mikołaj Szopa Wykład
 Kinetyczna teoria gazów Termodynamika dr Mikołaj Szopa Wykład 7.11.015 Kinetyczna teoria gazów Kinetyczna teoria gazów. Termodynamika Termodynamika klasyczna opisuje tylko wielkości makroskopowe takie
Kinetyczna teoria gazów Termodynamika dr Mikołaj Szopa Wykład 7.11.015 Kinetyczna teoria gazów Kinetyczna teoria gazów. Termodynamika Termodynamika klasyczna opisuje tylko wielkości makroskopowe takie
Wstęp do fizyki statystycznej: krytyczność i przejścia fazowe. Katarzyna Sznajd-Weron
 Wstęp do fizyki statystycznej: krytyczność i przejścia fazowe Katarzyna Sznajd-Weron Co to jest fizyka statystyczna? Termodynamika poziom makroskopowy Fizyka statystyczna poziom mikroskopowy Marcin Weron
Wstęp do fizyki statystycznej: krytyczność i przejścia fazowe Katarzyna Sznajd-Weron Co to jest fizyka statystyczna? Termodynamika poziom makroskopowy Fizyka statystyczna poziom mikroskopowy Marcin Weron
Í ń ę ń Í ę ź ę ń ľ ń ć ę ę ľ ń ę ľ ć
 ń Í ń ę ń Í ę ź ę ń ľ ń ć ę ę ľ ń ę ľ ć Í ń Ó Ń Ń Ń Ó ľ ęż Ń Á ęż Ń Ą ę Ż ć ę ę Ż ć ę ć Ś ę ę Ś Ż Ż Ż Ż ę ę Ż ń Ż ń ę ę ć Ś ę Ż ć Ż ć Ż Ż ć ń Ż ľ ę ę ę ę Ś ę ę ľ ę Ę Ĺ Í ľ ď ý Ę ń ľ ę ń Ó Ń ć Í ô Ó ľ ü
ń Í ń ę ń Í ę ź ę ń ľ ń ć ę ę ľ ń ę ľ ć Í ń Ó Ń Ń Ń Ó ľ ęż Ń Á ęż Ń Ą ę Ż ć ę ę Ż ć ę ć Ś ę ę Ś Ż Ż Ż Ż ę ę Ż ń Ż ń ę ę ć Ś ę Ż ć Ż ć Ż Ż ć ń Ż ľ ę ę ę ę Ś ę ę ľ ę Ę Ĺ Í ľ ď ý Ę ń ľ ę ń Ó Ń ć Í ô Ó ľ ü
Biofizyka. wykład: dr hab. Jerzy Nakielski. Katedra Biofizyki i Morfogenezy Roślin
 Biofizyka wykład: dr hab. Jerzy Nakielski Katedra Biofizyki i Morfogenezy Roślin Biofizyka - wykłady Biotechnologia III rok Tematyka (15 godz.): dr hab. Jerzy Nakielski dr Joanna Szymanowska-Pułka dr
Biofizyka wykład: dr hab. Jerzy Nakielski Katedra Biofizyki i Morfogenezy Roślin Biofizyka - wykłady Biotechnologia III rok Tematyka (15 godz.): dr hab. Jerzy Nakielski dr Joanna Szymanowska-Pułka dr
n p 2 i = R 2 (8.1) i=1
 8.9 Rozkład Maxwella Jest to rozkład prędkości cząstek w gazie doskonałym. Wielkość f (p) jest gęstością prawdopodobieństwa znalezienia cząstki o pędzie p. Różnica pomiędzy rozkładem Maxwella i rozkładem
8.9 Rozkład Maxwella Jest to rozkład prędkości cząstek w gazie doskonałym. Wielkość f (p) jest gęstością prawdopodobieństwa znalezienia cząstki o pędzie p. Różnica pomiędzy rozkładem Maxwella i rozkładem
Wykład FIZYKA I. 15. Termodynamika statystyczna. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 15. Termodynamika statystyczna Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html TERMODYNAMIKA KLASYCZNA I TEORIA
Wykład FIZYKA I 15. Termodynamika statystyczna Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html TERMODYNAMIKA KLASYCZNA I TEORIA
P r a w d o p o d o b i eństwo Lekcja 1 Temat: Lekcja organizacyjna. Program. Kontrakt.
 P r a w d o p o d o b i eństwo Lekcja 1 Temat: Lekcja organizacyjna. Program. Kontrakt. Lekcja 2 Temat: Podstawowe pojęcia związane z prawdopodobieństwem. Str. 10-21 1. Doświadczenie losowe jest to doświadczenie,
P r a w d o p o d o b i eństwo Lekcja 1 Temat: Lekcja organizacyjna. Program. Kontrakt. Lekcja 2 Temat: Podstawowe pojęcia związane z prawdopodobieństwem. Str. 10-21 1. Doświadczenie losowe jest to doświadczenie,
Krótki przegląd termodynamiki
 Wykład I Przejścia fazowe 1 Krótki przegląd termodynamiki Termodynamika fenomenologiczna oferuje makroskopowy opis układów statystycznych w stanie równowagi termodynamicznej bądź w stanach jemu bliskich.
Wykład I Przejścia fazowe 1 Krótki przegląd termodynamiki Termodynamika fenomenologiczna oferuje makroskopowy opis układów statystycznych w stanie równowagi termodynamicznej bądź w stanach jemu bliskich.
Fizyka statystyczna Potencjały termodynamiczne i warunki równowagi Geometria Drugiej Zasady Termodynamiki
 Fizyka statystyczna Potencjały termodynamiczne i warunki równowagi Geometria Drugiej Zasady Termodynamiki P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Energia wewnętrzna jako funkcja jednorodna
Fizyka statystyczna Potencjały termodynamiczne i warunki równowagi Geometria Drugiej Zasady Termodynamiki P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2016 Energia wewnętrzna jako funkcja jednorodna
Stany materii. Masa i rozmiary cząstek. Masa i rozmiary cząstek. m n mol. n = Gaz doskonały. N A = 6.022x10 23
 Stany materii Masa i rozmiary cząstek Masą atomową ierwiastka chemicznego nazywamy stosunek masy atomu tego ierwiastka do masy / atomu węgla C ( C - izoto węgla o liczbie masowej ). Masą cząsteczkową nazywamy
Stany materii Masa i rozmiary cząstek Masą atomową ierwiastka chemicznego nazywamy stosunek masy atomu tego ierwiastka do masy / atomu węgla C ( C - izoto węgla o liczbie masowej ). Masą cząsteczkową nazywamy
1 Rachunek prawdopodobieństwa
 1 Rachunek prawdopodobieństwa 1. Obliczyć średnią i wariancję rozkładu Bernouliego 2. Wykonać przejście graniczne p 0, N w rozkładzie Bernouliego przy zachowaniu stałej wartości średniej: λ = N p = const
1 Rachunek prawdopodobieństwa 1. Obliczyć średnią i wariancję rozkładu Bernouliego 2. Wykonać przejście graniczne p 0, N w rozkładzie Bernouliego przy zachowaniu stałej wartości średniej: λ = N p = const
Politechnika Wrocławska Katedra Fizyki Teoretycznej. Katarzyna Sznajd-Weron. Fizyka Statystyczna
 Politechnika Wrocławska Katedra Fizyki Teoretycznej Katarzyna Sznajd-Weron Fizyka Statystyczna Skrypt dla studentów Wrocław 2016 2 Spis treści 1 Elementy termodynamiki 1 1.1 Wielkości termodynamiczne..........................
Politechnika Wrocławska Katedra Fizyki Teoretycznej Katarzyna Sznajd-Weron Fizyka Statystyczna Skrypt dla studentów Wrocław 2016 2 Spis treści 1 Elementy termodynamiki 1 1.1 Wielkości termodynamiczne..........................
Teoria kinetyczna gazów
 Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
10. FALE, ELEMENTY TERMODYNAMIKI I HYDRODY- NAMIKI.
 0. FALE, ELEMENY ERMODYNAMIKI I HYDRODY- NAMIKI. 0.9. Podstawy termodynamiki i raw gazowych. Podstawowe ojęcia Gaz doskonały: - cząsteczki są unktami materialnymi, - nie oddziałują ze sobą siłami międzycząsteczkowymi,
0. FALE, ELEMENY ERMODYNAMIKI I HYDRODY- NAMIKI. 0.9. Podstawy termodynamiki i raw gazowych. Podstawowe ojęcia Gaz doskonały: - cząsteczki są unktami materialnymi, - nie oddziałują ze sobą siłami międzycząsteczkowymi,
Spis treści. Przedmowa Obraz makroskopowy Ciepło i entropia Zastosowania termodynamiki... 29
 Przedmowa... XI 1. Obraz makroskopowy... 1 1.1. Termodynamika... 1 1.2. Parametry termodynamiczne... 2 1.3. Granica termodynamiczna... 3 1.4. Procesy termodynamiczne... 4 1.5. Klasycznygazdoskonały...
Przedmowa... XI 1. Obraz makroskopowy... 1 1.1. Termodynamika... 1 1.2. Parametry termodynamiczne... 2 1.3. Granica termodynamiczna... 3 1.4. Procesy termodynamiczne... 4 1.5. Klasycznygazdoskonały...
Występują fluktuacje w stanie równowagi Proces przejścia do stanu równowagi jest nieodwracalny proces powrotny jest bardzo mało prawdopodobny.
 Wykład 14: Fizyka statystyczna Zajmuje sie układami makroskopowymi (typowy układ makroskopowy składa się z ok. 10 25 atomów), czyli ok 10 25 równań Newtona? Musimy dopasować inne pojęcia do opisu takich
Wykład 14: Fizyka statystyczna Zajmuje sie układami makroskopowymi (typowy układ makroskopowy składa się z ok. 10 25 atomów), czyli ok 10 25 równań Newtona? Musimy dopasować inne pojęcia do opisu takich
Wstęp do Fizyki Statystycznej
 Wstęp do Fizyki Statystycznej Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 października 2016 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 października 2016
Wstęp do Fizyki Statystycznej Katarzyna Sznajd-Weron Katedra Fizyki Teoretycznej Politechnika Wrocławska 11 października 2016 Katarzyna Sznajd-Weron (K4) Wstęp do Fizyki Statystycznej 11 października 2016
Ć Ę Ę ż ŁĄ
 Ó Ń Ń Ń Ą Ę Ź ŚĘ Ś Ć Ę Ę ż ŁĄ ż Ą Ś Ą Ś ź ż ź Ś Ę Ę ź Ą Ę ż Ą ż ż ż Ą Ś ż ż ż ć ż ż ć ż ż ć ć ż ż Ą ż ż ż Ę Ę Ę ż Ś ż Ą Ę Ź Ą ż Ą Ę ż ż Ś ż ż ż ż Ł Ę ć ż Ś ż ż ż ż ż Ś Ę ż ż Ę Ę ż Ę ć ż ż ż Ś ż ż ć ż Ę
Ó Ń Ń Ń Ą Ę Ź ŚĘ Ś Ć Ę Ę ż ŁĄ ż Ą Ś Ą Ś ź ż ź Ś Ę Ę ź Ą Ę ż Ą ż ż ż Ą Ś ż ż ż ć ż ż ć ż ż ć ć ż ż Ą ż ż ż Ę Ę Ę ż Ś ż Ą Ę Ź Ą ż Ą Ę ż ż Ś ż ż ż ż Ł Ę ć ż Ś ż ż ż ż ż Ś Ę ż ż Ę Ę ż Ę ć ż ż ż Ś ż ż ć ż Ę
Fizykochemiczne podstawy inżynierii procesowej
 Fizykochemiczne podstawy inżynierii procesowej Wykład I - 1 Sprawy formalne 2 Fizykochemiczne podstawy inżynierii procesowej Sprawy formalne: Forma: Wykład w postaci prezentacji komputerowych Przeznaczenie:
Fizykochemiczne podstawy inżynierii procesowej Wykład I - 1 Sprawy formalne 2 Fizykochemiczne podstawy inżynierii procesowej Sprawy formalne: Forma: Wykład w postaci prezentacji komputerowych Przeznaczenie:
C V dla róŝnych gazów. Widzimy C C dla wszystkich gazów jest, zgodnie z przewidywaniami równa w
 Wykład z fizyki, Piotr Posmykiewicz 7 P dt dt + nrdt i w rezultacie: nr 4-7 P + Dla gazu doskonałego pojemność cieplna przy stałym ciśnieniu jest większa od pojemności cieplnej przy stałej objętości o
Wykład z fizyki, Piotr Posmykiewicz 7 P dt dt + nrdt i w rezultacie: nr 4-7 P + Dla gazu doskonałego pojemność cieplna przy stałym ciśnieniu jest większa od pojemności cieplnej przy stałej objętości o
Maszyny cieplne i II zasada termodynamiki
 Maszyny cieplne i II zasada termodynamiki Maszyny cieplne, chłodnie i pompy tlenowe II zasada termodynamiki Cykl Carnot a Entropia termodynamiczna definicja II zasada termodynamiki i entropia Cykle termodynamiczne.
Maszyny cieplne i II zasada termodynamiki Maszyny cieplne, chłodnie i pompy tlenowe II zasada termodynamiki Cykl Carnot a Entropia termodynamiczna definicja II zasada termodynamiki i entropia Cykle termodynamiczne.
9.1 Rozkład kanoniczny dla układów kwantowych
 9 Rozkład kanoniczny 9.1 Rozkład kanoniczny dla układów kwantowych Jest to funkcja rozkładu w stanie równowagi termodynamicznej, dla układu mogącego wymieniać ciepło z otoczeniem. Układ znajduje się w
9 Rozkład kanoniczny 9.1 Rozkład kanoniczny dla układów kwantowych Jest to funkcja rozkładu w stanie równowagi termodynamicznej, dla układu mogącego wymieniać ciepło z otoczeniem. Układ znajduje się w
, , , , 0
 S T E R O W N I K G R E E N M I L L A Q U A S Y S T E M 2 4 V 4 S E K C J I G B 6 9 6 4 C, 8 S E K C J I G B 6 9 6 8 C I n s t r u k c j a i n s t a l a c j i i o b s ł u g i P r z e d r o z p o c z ę
S T E R O W N I K G R E E N M I L L A Q U A S Y S T E M 2 4 V 4 S E K C J I G B 6 9 6 4 C, 8 S E K C J I G B 6 9 6 8 C I n s t r u k c j a i n s t a l a c j i i o b s ł u g i P r z e d r o z p o c z ę
Wstęp do probabilistyki i statystyki Wykład 3. Prawdopodobieństwo i algebra zdarzeń
 Wstęp do probabilistyki i statystyki Wykład 3. Prawdopodobieństwo i algebra zdarzeń dr inż. Krystyna Schneider, Katedra Elektroniki, AGH e-mail: kryschna@agh.edu.pl http://home.agh.edu.pl/~kryschna 1 Plan:
Wstęp do probabilistyki i statystyki Wykład 3. Prawdopodobieństwo i algebra zdarzeń dr inż. Krystyna Schneider, Katedra Elektroniki, AGH e-mail: kryschna@agh.edu.pl http://home.agh.edu.pl/~kryschna 1 Plan:
Zarządzenia i informacje 1.1. Zarządzenia
 C h o r ą g i e w D o l n o l ą s k a Z H P W r o c ł a w, 3 0 l i s t o p a d 2 0 r. Z w i ą z e k H a r c e r s t w a P o l s k i e g o K o m e n d a n t C h o r ą g w i D o l n o 6 l ą s k i e j Z H
C h o r ą g i e w D o l n o l ą s k a Z H P W r o c ł a w, 3 0 l i s t o p a d 2 0 r. Z w i ą z e k H a r c e r s t w a P o l s k i e g o K o m e n d a n t C h o r ą g w i D o l n o 6 l ą s k i e j Z H






