ALKOHOLE (by Aleksandra Kołodziejczyk, UG)
|
|
|
- Robert Kaczmarczyk
- 7 lat temu
- Przeglądów:
Transkrypt
1 ALKLE (by Aleksandra Kołodziejczyk, UG) -: alkohol/fenol/enol Typowy alkohol gr. przy o hybrydyzacji sp 3 Nazewnictwo: alkanol - jak najniższy lokant podstawnika hydroksylowego Alkohole 1, 2, propan-1-ol (1 ) 3 () 2 3 butan-2-ol = alkohol sec-butylowy (2 ) = 4,4,7-trimetylooktan-3-ol (2 ) cis-3-chlorocyklopentanol (2 ) l Właściwości: hybrydyzacja sp 3 atomu tlenu, - silniejsze, krótsze niż - Związki polarne: μ Wiązania wodorowe t.t., t.wrz., rozpuszczalność w wodzie - wyższe niż w alkanach i halogenoalkanach. Woda - 100! zęść hydrofobowa i hydrofilowa Alkohole są amfoteryczne Kwasowość - zbliżona do wody jon alkoksylowy 1
2 3 + NaN 2 Na 3 + N 3 pk a = 15.5 pk a = 35 Kwasowość: 3 < 2 < 1 < 3 Steryczne utrudnienie solwatacji jonu alkoksylowego: Efekt indukcyjny przenoszenie ładunku przez wiązania (stabilizacja anionu). Wpływ na kwasowość: pk a ( 3 ) l F F Zasadowość: -- silny kwas -- [ 3 2 ] + pk a = -2.2 jon alkoksoniowy Metody otrzymywania alkoholi: 1. Przemysłowe: katalityczna redukcja (gaz syntezowy), hydratacja etenu, 5% - fermentacja 2. Substytucja nukleofilowa halogenoalkanów: zadko, częściej odwrotnie; uboczna reakcja eliminacji (E2) Na Br NaBr 3. edukcja ketonów i aldehydów redukcja utlenienie 1 ' redukcja utlenienie ' 2 a. Wodorowanie (hydrogenacja); kataliza heterogeniczna , Pd
3 b. edukcja wodorkami NaB 4, LiAl 4 ; Li, Na gorzej rozpuszczalne Na 3 B Na 3B( 2 3 ) 4. Synteza z użyciem związków organometalicznych Związki organometaliczne: 3 Br + Li Et 2, 0 3 Li + LiBr TF ( 3 ) 2 I + Mg ( 3 ) 2 MgI + LiBr Zw. magnezoorganiczne = zw. Grignarda jodek 1-metyloetylomagnezowy X + Mg ( 3 2 ) 2 Mg X M M- M - metal alogenoalkan alkan: Mg -Br -Mg-Br - Aplikacja otrzymywanie deuteropochodnych: ( 3 ) 3 -l 1. Mg 2. D 2 ( 3 ) 3 -D Związki metaloorganiczne w syntezie alkoholi: - M + M 3
4 aldehyd mrówkowy 1 alkohole Et 2 3 ( 2 ) 2 2 MgBr ( 2 ) MgBr +, 2 3 ( 2 ) Mg()Br aldehydy 2 alkohole MgBr -MgBr + ' ' ' + Mg()Br ketony 3 alkohole 3 3 ( 2 ) 2 2 MgBr Et 2 +, 2 3 ( 2 ) Mg()Br eakcje z estrami i chlorkami kwasowymi 3 alkohole 3 2 podstawniki pochodzące od zw. Grignarda! mrówczany 2 alkohole 5. edukcja kwasów/estrów: 1. LiAl 4, eter - 2 ' 2. +, 2 =, alkil, aryl NaB 4 tylko estry 4
5 6. ydratacja alkenów a. bezpośrednia: ' b. pośrednia: '' +, 2 ' '' EAKJE ALKLI 1. eakcje z silnymi zasadami: A. z metalami alkalicznymi (Na, Li, K, s) Na 2 Na Na 2 - Na ( 3 ) 3-2 ( 3 ) 3 - K eaktywność: 3 > 1 > 2 > 3 - M + - aniony alkoholanowe/alkoksylowe - silne Nu/B z silnymi zasadami (silniejsze od - ): NaN 2, Na, MgX, Li 3 + K pka = K + - pka = ( 2 ) 3 Li 3 Li + 3 ( 2 ) 2 3 pk a = 50 ( 3 ) Li N 3 Li + ( 3 ) 2 2. eakcje z silnymi kwasami podstawienie/dehydratacja (S N, E1): N ( 3 ) 2 ( 3 ) 2 pk a = A. trzymywanie halogenoalkanów z 1 : 5
6 2 + X 2 + X S N 2 2 X + 2 X = Br, I anion chloru za słabym Nu; Sl 2, PBr 3 otrzymywanie chlorków, bromków B. eakcje z 2 i 3 S N 1, E1; przegrupowanie kationów: Gdy dobry Nu S N 1: ( 3 ) 3 + Br ( 3 ) 3 Br + 2 ( 3 ) 3 + Br ( 3 ) Br ( 3 ) Br ( 3 ) 3 Br + 2 W wyższych temperaturach E = dehydratacja alkoholi 2 2 S 4, T S N 2-1 rz. X + 2 X, S N 1 X - 2, 3 rz. E1 alken Przegrupowania karbokationów/podstawienie: Br 0 3 Br Br główny produkt 6
7 E1 - przegrupowanie anionu wodorkowego/alkilu: Br 3 Br S T 2 S Gdy brak odpowiedniego 2 lub 3 atomu wodoru migracja alkilu: Br Br Br Szybkość migracji większa gdy prowadzi do 3 karbokationu. Alkohole 1 też mogą ulegać przegrupowaniom - równoczesna z odejściem wody migracja alkilu (podstawienie utrudnia duże zatłoczenie): alkohol neopentylowy Br
8 3. eakcje z kwasami organicznymi i tlenowymi kwasami nieorganicznymi i ich pochodnymi estry r P S ' r P S ' Estryfikacja: Estry kwasów nieorganicznych jako droga do halogenoalkanów Br P Br 2 --PBr 2 + Br S N 2 2 Br + PBr 2 Br bromofosforan (III) PBr Br + 3 P 3 chlorki Sl 2, jodki P + I l S l 2 S l trzymywanie sulfonianów (wszechstronnych substratów) S N l 2 l + S 2 + l Sulfoniany krystaliczne, łatwo oczyszczać Sl Py S- 3 + Py x l -S-' Nu -Nu + 'S 3 8
9 3 - S S ( 3) 2S S 3 4. Utlenianie A. Alkohole 1 aldehydy/ kwasy utl. utl. 2 aldehydy tylko wtedy gdy można je usuwać z roztworu lub selektywny utleniacz (r 3 w acetonie, chlorochromian pirydyny (P) = r 3 + l + Py) KMn 4, K 2 r 2 7 kwasy B. Alkohole 2 ketony ' K 2 r 2 7 ' Silne utleniacze - destrukcja. Alkohole 3 - nie utleniają się (brak ) Ar, IUPA benzenole FENLE Elektrony π nakładają się z orb. p atomu tlenu. Delokalizacja jak w anionie benzylowym. Fenol kwas karbolowy dezinfektant, polimery Kopolimer fenolu i aldehydu mrówkowego żywice fenolanowe (np. Bakelit) trans - resweratrol 9
10 Kwasowość pk a = 8 10 (kwasy 3 5, alkohole 16 18) + Sprzężona zasada stabilizowany rezonansowo anion fenolanowy 4-nitrofenol pk a = ,4,6-trinitrofenol pk a = 0.25 (kwas pikrynowy) Na Na N trzymywanie fenoli Przez S E b.trudno I. Przemysłowe otrzymywanie fenolu: utlenianie kumenu; chlorobenzen + Na - S N (Ar) Nukleofilowe podstawienie aromatyczne - S N (Ar) l Nu N 2 N2 + Nu + l N 2 N 2 Nu =, N 2, N 3 Dwa etapy: addycja + eliminacja (jak pochodne kwasów) Mechanizm A-E: Konieczne podst. akceptorowe (stabilizacja anionu); o-, p- l Nu N 2 l Nu N l Nu N... - l Nu N 2 N 2 N 2 N 2 N 2 Podstawniki meta nie wspomagają rezonansowej stabilizacji. 10
11 Mechanizm E-A: alogenoareny, które nie mają podstawników elektronoakceptorowych mogą reagować przez benzyn II. trzymywanie fenoli z soli diazoniowych: N 2 N N NaN 2,, 2 T - N 2 EAKJE FENLI Jak inne alkohole: 1. Estryfikacja z kwasami endotermiczna; chlorki kwasowe: 2 5 Na, Nal l 3 2. Synteza eterów (Williamsona): Br Na, 2 + NaBr l l S E Silna aktywacja o- i p-. Nawet rozc. N 3 powoduje nitrowanie. eakcję F.-. komplikuje estryfikacja. eakcja Kolbego: + 2 K 3, p K 3 salicylan potasu kw. salicylowy inhibicja tromboxanu A 2 (prostaglandyna) 1997 r. 100-lecie aspiryny octan kwasu 2-hydroksybenzoesowego (kwas acetylosalicylowy) 11
12 3. Utlenianie fenoli Mechanizm transferu 1e diony [] [] benzeno-1,4-diol cykloheksa-2,5-dien-1,4-dion ( hydrochinon) (chinon) Para redoksowa benzochinon utleniania w naturze. hydrochinon w realizacji równowagowych procesów 3 3 ( 2 = 2 ) n ubichinony (koenzym Q) reakcje redoksowe w łańcuchu oddechowym aerobów (przeniesienie elektronów z reduktazy NAD-Q do reduktazy cytochromowej) 3 3 n = 6, 8, 10 ubichinon (Q) ubichinol (Q 2 ) Sumarycznie: Naturalny antyoksydant (fenol) witamina E redukcja i protonowanie rodników 3 - -lipid lipid 3 odnik -tokoferolu stosunkowo mało reaktywny (zatłoczenie, delokalizacja); redukowany np. przez wit., metabolity wydalane. Syntetyczne analogi witaminy E konserwanty: n 2n+2, -- ETEY nazewnictwo IUPA alkoksyalkany lub eter np.dialkilowy sp 3, α = 112º (eter dimetylowy) etoksy-2-metylopropan metoksyetan = eter etylowometylowy 12
13 ,2-dimetoksyetan (eter dimetylowy glikolu) oksolan cis-1-etoksy-2-metoksycyklopentan 1,4-dioksan tetrahydrofuran, TF) Etery heterocykliczne ykliczne polietery etery koronowe Właściwości: Brak wiązań wodorowych niskie t.wrz., słaba rozpuszczalność w 2 Solwatowanie kationów rozpuszczanie soli nieorganicznych w rozp. niepolarnych KMn 4 K Mn eagenty transportujące jony: etery koronowe, kryptandy (trójwymiarowe etery policykliczne) K > b > Na > s > Li K(K + ) = K(Li + ) = 100 Jonofory związki otaczające przykoordynowany kation Synteza Williamsona Synteza eterów - - dobry Nu, silna B tylko 1 czynniki alkilujące (konkurencja eliminacji) 13
14 Wewnątrzcząsteczkowa r. Willamsona: -( 2 ) 4 2 Br k 3 > k 5 > k 6 > k 4 > k 7 > k 8 + alogenohydryna + Na epoksyd/ oksiran 2 czynniki entropowe + naprężenie pierścienia (kompromis) oksan (tetrahydropiran) Wewnątrzcząsteczkowa reakcja Williamsona może być stereospecyficzna. 2. Działanie kwasów mineralnych na alkohole symetr. etery głównie 1 o alkoholi S Najsilniejszym Nu niesprotonowany alkohol, S N 2, konkurencja: E S 4 E2, S 4 3 ( 3 ) 2 --( 3 ) , 3 S N 1 2-(1-metyloetoksy)propan 3. Alkoholiza halogenoalkanów/ sulfonianów - halogenki 2, 3 3 l l 14
15 EAKJE ETEÓW Tworzenie nadtlenków - rodnikowe utlenienie na powietrzu wodoronadtlenek eteru ozszczepienie przez silne kwasy (Br, I) nadtlenek eteru Br Br --' -Br + '- -Br + '-Br Ph Ph Br Ph 2 Br Jony oksoniowe zawierające 3 alkil karbokationy (S N 1, E1), gdy 1 lub 2 - S N 2 I, 2 + I TFA + EAKJE EPKSYDÓW epoksyd = oksiran = 1,2-epoksyetan = tlenek glikolu 1. Nukleofilowe otwieranie pierścienia pochodne alkoholi + 3 S 2 2 S S N 2 nietypowe. Napęd likwidacja naprężenia. 15
16 3, egioselektywność zawada steryczna, stereoselektywność - anti eakcje z wodorkami i zw. organometalicznymi: 1. LiAl 4, Et 2 2., 2 ydroksyetylowanie: MgBr Kwaśno katalizowane otwieranie pierścienia epoksydowego ' '? regiospecyficzność ' ' 3 ' 3 TILE i SULFIDY siarkowe analogi alkoholi i eterów Nazewnictwo: alkanotiole/merkaptany: 3 S metanotiol -S gr. merkaptanowa 16
17 S 3 S cykloheksanotiol 2-metylopentano-3-tiol S merkaptoetanol (niższa preferencja S) Tioetery = sulfidy 3 S- alkilotio- 3 S( 2 ) S 3 S 2 3 etylometylosulfid 3 1,1-dimetyloetyloheptylosulfid jon metanotiolanowy sulfid dimetylowy = siarczek dimetylu Właściwości: Atom S większy rozmiar, słabo spolaryzowane S- słabe wiązania wodorowe. Lotność S jak X, a nie. Zapach! Słabe wiązanie S-, pk a = 9 12 S + S + atom S bardziej nukleofilowy niż at. EAKJE: ( 3 ) 2 -Br + Na S Et ( 3 ) 2 -S + NaBr Alkilowanie tioli sulfidy Na S + 'Br S' + NaBr + 2 S N 2 Nukleofilowość sulfidów sole trialkilosulfoniowe 3 3 S + 3 I S + I Sole sulfoniowe S N na atom (sulfid grupą opuszczającą) 3 + S S( 3 ) 2 3 Utlenienie a/ łagodne disulfidy: 17
18 b/ drastyczne kwasy sulfonowe: 3 S KMn 4 ( 2 2 ) 3 S- kwas metanosulfonowy S S S- 3 sulfid dimetylowy sulfotlenek dimetylowy DMS sulfon dimetylowy Zastosowanie, fizjologiczna rola alkoholi, eterów 3 rozpuszczalnik, paliwo, toksyczny dodatek do Et, 30 ml dawka śmiertelna ( 2 = zaburza proces widzenia), ewent. prekursor benzyny 3 2 składnik napojów alkoholowych (depresant), rozpuszczalnik (perfumy, politury ) dawki okołotoksyczne przy zatruciach metanolem czy etano-1,2-diolem spożywczy: ( enzymy enzymy ) n metabolizm 10ml/h (wątroba 2 ) Etano-1,2-diol (glikol etylenowy) 2 2 [] Niska t.t (-11,5 ), wysoka t.wrz. (198 ), pełna mieszalność z wodą płyny przeciw zamarzaniu. Propano-1,2,3-triol (gliceryna, glicerol) Źródłem zasadowa hydroliza triglicerydów; nietoksyczna, lepka, rozpuszczalna w wodzie ciecz (przemysł kosmetyczny, farmaceutyczny, skórzany) Estry fosforowe fosfoglicerydy (membrany komórkowe) Triester kw. azotowego = nitrogliceryna Naturalne alkohole ważne fizjologicznie: dialkohol - morfina (diacetylowa pochodna heroina), tetrahydrokanabinol, cholesterol cholesterol 18
C OH ALKOHOLE ETERY R OH R O R R' O FENOLE. Ar OH NOMENKLATURA ALKOHOLE ZWIĄZKI ORGANICZNE ZAWIERAJĄCE W STRUKTURZE ATOMY TLENU C O C OH CH 3 OH
 ZWIĄZKI GANIZNE ZAWIEAJĄE W STUKTUZE ATMY TLENU 8 1s2 2s 2 2p 4 okres 2; grupa VI w związkach jest dwuwiążący, z dwoma niewiążącymi parami elektronów drugi w skali elektroujemności Paulinga 3.5 (za fluorem)
ZWIĄZKI GANIZNE ZAWIEAJĄE W STUKTUZE ATMY TLENU 8 1s2 2s 2 2p 4 okres 2; grupa VI w związkach jest dwuwiążący, z dwoma niewiążącymi parami elektronów drugi w skali elektroujemności Paulinga 3.5 (za fluorem)
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. COH
 Alkohole R Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. C Alkohole można uważać za organiczne pochodne wody --, w której jeden z atomów
Alkohole R Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. C Alkohole można uważać za organiczne pochodne wody --, w której jeden z atomów
Slajd 1. Etery i epoksydy. Slajd 2. Wprowadzenie. Wzór R-O-R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: CH 3 O CH 3 O CH 3
 Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu. F Br H 3 C
 alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Slajd 1. Alkohole i fenole. Cholesterol. Slajd 2. Budowa alkoholi. metanol. metanol. Grupą funkcyjną jest (OH) Tlen posiada hybrydyzacjęsp 3
 Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
1. Substytucja nukleofilowa we fluorowcopochodnych
 B T E L EMA G GAZA A Synteza 1. Substytucja nukleofilowa we fluorowcopochodnych 1a) Etery dialkilowe można otrzymywać w reakcji pierwszorzędowych fluorowcopochodnych z ALKLAAM. Jest to reakcja Williamsona.
B T E L EMA G GAZA A Synteza 1. Substytucja nukleofilowa we fluorowcopochodnych 1a) Etery dialkilowe można otrzymywać w reakcji pierwszorzędowych fluorowcopochodnych z ALKLAAM. Jest to reakcja Williamsona.
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Materiały dodatkowe alkohole, fenole, etery
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Alkohole i fenole. Opracowanie: Bartłomiej SIEPSIAK klasa 3d Opiekun: p. Teresa Gębicka
 Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Mg I. I Mg. Nie można ich jednak otrzymać ze związków, które posiadają grupy chlorowcowe w tak zwanym ustawieniu wicynalnym.
 nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
CH 3 OH C 2 H 5 OH H 3 C CH 2 CH 2 OH H 3 C CH CH 3 OH metanol etanol propan-1-ol propan-2-ol H 2 C CH 2 OH OH H 2 C CH CH 2 OH OH OH
 Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Klasyfikacja i przykłady ETERY
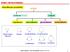 ETERY I EPKSYZWIĄZKI Klasyfikacja i przykłady ETERY acykliczne R--R cykliczne trójczłonowe czteroczłonowe pięcioczłonowe sześcioczłonowe tlenek etylenu (oksiran) oksetan tetrahydrofuran tetrahydropiran
ETERY I EPKSYZWIĄZKI Klasyfikacja i przykłady ETERY acykliczne R--R cykliczne trójczłonowe czteroczłonowe pięcioczłonowe sześcioczłonowe tlenek etylenu (oksiran) oksetan tetrahydrofuran tetrahydropiran
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2
![liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2 liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2](/thumbs/65/54124071.jpg) Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
ALKOHOLE, FENOLE, ALDEHYDY, KETONY
 LKOHOLE, FENOLE, LDEHYDY, KETONY ZDNIE DOMOWE ZDNIE 1. (2 P.): Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. Określ typ każdej reakcji (1. 4.) z powyższego schematu,
LKOHOLE, FENOLE, LDEHYDY, KETONY ZDNIE DOMOWE ZDNIE 1. (2 P.): Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. Określ typ każdej reakcji (1. 4.) z powyższego schematu,
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
HCOOH kwas metanowy ( mrówkowy ) CH 3. COOH kwas etanowy ( octowy ) CH 2
 Kwasy karboksylowe, Ar Nazewnictwo: Kwasy, które są pochodnymi alkanów o otwartych łańcuchach, są nazywane w sposób systematyczny przez dodanie nazwy kwas i dodanie końcówki owy do alkanu - kwas alkanowy
Kwasy karboksylowe, Ar Nazewnictwo: Kwasy, które są pochodnymi alkanów o otwartych łańcuchach, są nazywane w sposób systematyczny przez dodanie nazwy kwas i dodanie końcówki owy do alkanu - kwas alkanowy
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
10. Eliminacja halogenków alkili
 10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
20 i 21. Eliminacja halogenków alkili
 20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
Podział związków organicznych
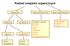 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Wykład 8. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 8 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) ALKOHOLE I FENOLE Związki o wzorze ogólnym R-OH. W fenolach grupa OH jest bezpośrednio związana z pierścieniem aromatycznum.
Wykład 8 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) ALKOHOLE I FENOLE Związki o wzorze ogólnym R-OH. W fenolach grupa OH jest bezpośrednio związana z pierścieniem aromatycznum.
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 1
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
trzeciorzędowe (3 ) (CH 3 ) 3 COH tert-butanol
 ALKOLE I FENOLE ALKOLE - KLASYFIKACJA pierwszorzędowe (1 ) drugorzędowe (2 ) trzeciorzędowe (3 ) allilowe benzylowe CH 2 etanol ( ) 2 CH alkohol izopropylowy ( ) 3 C tert-butanol CH 2 =CHCH 2 alkohol allilowy
ALKOLE I FENOLE ALKOLE - KLASYFIKACJA pierwszorzędowe (1 ) drugorzędowe (2 ) trzeciorzędowe (3 ) allilowe benzylowe CH 2 etanol ( ) 2 CH alkohol izopropylowy ( ) 3 C tert-butanol CH 2 =CHCH 2 alkohol allilowy
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
13. B E Z W O D N I K I I H A L O G E N K I K W A S O W E Aleksander Kołodziejczyk sierpień 2007
 13. B E Z W D N I K I I A L G E N K I K W A S W E Aleksander Kołodziejczyk sierpień 2007 A L G E N K I K W A S W E alogenki kwasowe są pochodnymi kwasów karboksylowych, w których funkcja hydroksylowa została
13. B E Z W D N I K I I A L G E N K I K W A S W E Aleksander Kołodziejczyk sierpień 2007 A L G E N K I K W A S W E alogenki kwasowe są pochodnymi kwasów karboksylowych, w których funkcja hydroksylowa została
Długość [pm] Energia [kj/mol] C O H wynosi (zarówno w fenolach, jak i alkoholach) około 109 o
![Długość [pm] Energia [kj/mol] C O H wynosi (zarówno w fenolach, jak i alkoholach) około 109 o Długość [pm] Energia [kj/mol] C O H wynosi (zarówno w fenolach, jak i alkoholach) około 109 o](/thumbs/66/55340837.jpg) B I T E N L EMIA G GANIZNA I A Budowa ALKLE zawierające atom TLENU związany z atomem węgla sp 3 mają budowę przestrzenną TETAEDYZNĄ zbliżoną do budowy węglowodorów. Wiązanie węgiel - tlen utworzone jest
B I T E N L EMIA G GANIZNA I A Budowa ALKLE zawierające atom TLENU związany z atomem węgla sp 3 mają budowę przestrzenną TETAEDYZNĄ zbliżoną do budowy węglowodorów. Wiązanie węgiel - tlen utworzone jest
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
A B C D A B C 4. D A B C D
 1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
Program wykładu Chemia Organiczna I
 Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Kwasy karboksylowe C O OH OH C CH 2 H OH CH 2 C CH 3 C OH C OH C OH. propionowy. mrówkowy. akrylowy. octowy. masłowy metakrylowy.
 Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Fenole związki organiczne, w których grupa hydroksylowa związana jest bezpośrednio z atomem węgla układu aromatycznego (z węglem o hybrydyzacji sp 2 ). Przykłady i -naftol -naftol
Krystyna Dzierzbicka Fenole związki organiczne, w których grupa hydroksylowa związana jest bezpośrednio z atomem węgla układu aromatycznego (z węglem o hybrydyzacji sp 2 ). Przykłady i -naftol -naftol
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Lista zagadnień do egzaminu licencjackiego
 Lista zagadnień do egzaminu licencjackiego Przedmiot Podstawy chemii : 1. Historia odkryć subatomowej struktury materii i znajomość kluczowych eksperymentów, dowodzących istnienia elektronów, protonów
Lista zagadnień do egzaminu licencjackiego Przedmiot Podstawy chemii : 1. Historia odkryć subatomowej struktury materii i znajomość kluczowych eksperymentów, dowodzących istnienia elektronów, protonów
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Grupy główne wg malejcego pierwszestwa. Alkohole i fenole Grupa funkcyjna OH
 Alkohole i fenole Grupa funkcyjna OH Alkohole - zwizki posiadajce grup funkcyjn "z prawdziwego zdarzenia" - grup główn. Wizanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale w nazwie
Alkohole i fenole Grupa funkcyjna OH Alkohole - zwizki posiadajce grup funkcyjn "z prawdziwego zdarzenia" - grup główn. Wizanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale w nazwie
Znane są alkohole nienasycone i aromatyczne (nazwy zwyczajowe), ale w nich grupa -OH nie jest związana z C sp 2 : -OH
 A L K L E I E T E Y Aleksander Kołodziejczyk grudzień 2007 ALKLE Alkoholami nazywane są związki organiczne zawierające grupę hydroksylową (-) związaną z nasyconym atomem węgla, tzn. z atomem węgla o hybrydyzacji
A L K L E I E T E Y Aleksander Kołodziejczyk grudzień 2007 ALKLE Alkoholami nazywane są związki organiczne zawierające grupę hydroksylową (-) związaną z nasyconym atomem węgla, tzn. z atomem węgla o hybrydyzacji
Jednofunkcyjno pochodne węglowodorów - cząsteczki węglowodoru, w których atom lub atomy wodoru zastały podstawione (zastąpiono) grupą funkcyjną.
 Materiał powtórzeniowy do sprawdzianu - jednofunkcyjne pochodne węglowodorów - halogenowęglowodory, alkohole, fenole, aldehydy, ketony + przykładowe zadania - Cz. I I. Jednofunkcyjne pochodne i grupy funkcyjne
Materiał powtórzeniowy do sprawdzianu - jednofunkcyjne pochodne węglowodorów - halogenowęglowodory, alkohole, fenole, aldehydy, ketony + przykładowe zadania - Cz. I I. Jednofunkcyjne pochodne i grupy funkcyjne
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
CHEMIA ORGANICZNA. dr hab. Włodzimierz Gałęzowski Wydział Chemii UAM (61)
 EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
Mat. powtórzeniowy: zad. dot. procesów wieloetapowych w chemii organicznej
 Mat. powtórzeniowy: zad. dot. procesów wieloetapowych w chemii organicznej Zad.1. Zapisz równania reakcji przedstawionych na poniższym schemacie, określ typ rekcji w chemii organicznej, nadaj nazwy systematyczne
Mat. powtórzeniowy: zad. dot. procesów wieloetapowych w chemii organicznej Zad.1. Zapisz równania reakcji przedstawionych na poniższym schemacie, określ typ rekcji w chemii organicznej, nadaj nazwy systematyczne
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
ALKENY. Dodaj do nazwy podstawniki starając się, aby miały jak najniższe lokanty; Zidentyfikuj stereoizomery, oznacz je jako cis/trans (Z/E):
 WĘGLWDY NIENASYNE (by Aleksandra Kołodziejczyk, UG) alkeny (=); alkiny ( ); węglowodory skondensowane (==); węglowodory sprzężone (=-=); węglowodory o izolowanych wiązaniach wielokrotnych (=--=) ALKENY
WĘGLWDY NIENASYNE (by Aleksandra Kołodziejczyk, UG) alkeny (=); alkiny ( ); węglowodory skondensowane (==); węglowodory sprzężone (=-=); węglowodory o izolowanych wiązaniach wielokrotnych (=--=) ALKENY
wykład: Alkohole, Etery i Fenole
 wykład: Alkohole, Etery i Fenole Alkohole Alkohole związki organiczne o wzorze ogólnym R- w których grupa hydroksylowa połączona jest z atomem węgla z łańcucha węglowego. Alkohole nasycone Alkohole nienasycone
wykład: Alkohole, Etery i Fenole Alkohole Alkohole związki organiczne o wzorze ogólnym R- w których grupa hydroksylowa połączona jest z atomem węgla z łańcucha węglowego. Alkohole nasycone Alkohole nienasycone
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
KATALIZA I KATALIZATORY
 AKADEMIA CIEKAWEJ CEMII 2010/2011 KATALIZA I KATALIZATRY WYKŁAD IV dr Anna Zawisza Katedra Chemii rganicznej i Stosowanej UŁ 12.01.2011 REAKCJE CEMICZNE SZYBKIE WLNE TERIA ZDERZEŃ musi dochodzić do zderzeń
AKADEMIA CIEKAWEJ CEMII 2010/2011 KATALIZA I KATALIZATRY WYKŁAD IV dr Anna Zawisza Katedra Chemii rganicznej i Stosowanej UŁ 12.01.2011 REAKCJE CEMICZNE SZYBKIE WLNE TERIA ZDERZEŃ musi dochodzić do zderzeń
Zdzisław Głowacki Chemia organiczna 2b Zakres podstawowy i rozszerzony Odpowiedzi i rozwiązania zadań Rozdział 5
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 5 Errata do piątego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 109 Str.
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 5 Errata do piątego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 109 Str.
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII Instrukcja do ćwiczeń laboratoryjnych WŁAŚCIWOŚCI KWASOWOZASADOWE ZWIĄZKÓW ORGANICZNYCH; BADANIE ROZPUSZCZALNOŚCI
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII Instrukcja do ćwiczeń laboratoryjnych WŁAŚCIWOŚCI KWASOWOZASADOWE ZWIĄZKÓW ORGANICZNYCH; BADANIE ROZPUSZCZALNOŚCI
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna (0310-CH-S1-026) Nazwa wariantu modułu (opcjonalnie):
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Kartkówka nr 1 Imię i Nazwisko:.. Nr albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1.
 Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Spis treści Podstawowe dane Podział alkoholi alifatycznych Nazewnictwo systematyczne alkoholi Izomeria alkoholi Alkohole nasycone monohydroksylowe
 Spis treści Podstawowe dane Podział alkoholi alifatycznych Nazewnictwo systematyczne alkoholi Izomeria alkoholi Alkohole nasycone monohydroksylowe Właściwości fizyczne Otrzymywanie Przemysłowe metody otrzymywania
Spis treści Podstawowe dane Podział alkoholi alifatycznych Nazewnictwo systematyczne alkoholi Izomeria alkoholi Alkohole nasycone monohydroksylowe Właściwości fizyczne Otrzymywanie Przemysłowe metody otrzymywania
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
ALKENY WĘGLOWODORY NIENASYCONE
 Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE
 PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
Alkohole i fenole Grupa funkcyjna OH
 Alkohole i fenole Grupa funkcyjna OH Alkohole - związki posiadające grupę funkcyjną "z prawdziwego zdarzenia" - grupę główną. Wiązanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale
Alkohole i fenole Grupa funkcyjna OH Alkohole - związki posiadające grupę funkcyjną "z prawdziwego zdarzenia" - grupę główną. Wiązanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Kierunek i poziom studiów: Biotechnologia, pierwszy. Nazwa wariantu modułu (opcjonalnie): nie dotyczy
 Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Reakcje aldehydów i ketonów. grupa karbonylowa Z = H, aldehyd Z = R (czyli at. C), keton
 30-33. Reakcje aldehydów i ketonów grupa karbonylowa Z =, aldehyd Z = R (czyli at. C), keton Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 15.1. Nazewnictwo Aldehyd
30-33. Reakcje aldehydów i ketonów grupa karbonylowa Z =, aldehyd Z = R (czyli at. C), keton Chemia rganiczna, dr hab. inż. Mariola Koszytkowska-Stawińska, WChem PW; 2017/2018 1 15.1. Nazewnictwo Aldehyd
