18. Reakcje benzenu i jego pochodnych
|
|
|
- Anna Laskowska
- 6 lat temu
- Przeglądów:
Transkrypt
1 18. Reakcje benzenu i jego pochodnych 1
2 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy w roli podstawnika metylenofenyl w roli podstawnika 2
3 18.2. Elektrofilowe podstawienie aromatyczne (S E Ar) wymiana protonu (H+) reagent, z którego zostaje wygenerowany elektrofil elektrofil sp 2 sp 3 aromatyczny produkt podstawienia protonu (H + ) jest trwalszy termodynamiczne nukleofil pełni rolę zasady odrywa proton od at. C(sp 3 ) hipotetyczny produkt addycji niearomatyczny, mniej trwały termodynamicznie 3
4 S E Ar mechanizm reakcji 2 E H Energia poten ncjalna 4
5 Powszechnie stosowane reakcje S E Ar Fluorowanie w reakcji S E Ar zachodzi gwałtownie trudna kontrola reakcji at. F wstawia się w reakcji soli diazoniowych (Ar-N 2+ ) (uwaga: to nie jest reakcja S E Ar) 5
6 18.3. S E Ar halogenowanie wytworzenie elektrofila (X = Cl, Br) podstawienie w praktyce stosuje się Fe, ze względu na higroskopijność FeX 3 2 Fe + 3 X 2 2 FeX 3 wytworzenie elektrofila podczas jodowania 6
7 18.4. S E Ar nitrowanie W praktyce: mieszanina stęż. HNO 3 i stęż. H 2 SO 4 tzw. mieszanina nitrująca wytworzenie elektrofila kationu nitroniowego (NO 2+ ) HNO 3 (słabszy kwas) pełni rolę zasady (formalnie) protonowanie HNO 3 sprzyja wytworzeniu NO 2 + bez dodatku H 2 SO 4 nitrowanie zachodzi wolno kation nitroniowy podstawienie 7
8 18.5. S E Ar sulfonowanie wytworzenie elektrofila podstawienie 8
9 S E Ar sulfonowanie, odwracalność reakcji sulfonowanie de-sulfonowanie sulfonowanie jest stosowane w praktyce jako zabezpieczenie określonej pozycji w pierścieniu benzenowym 9
10 18.6. S E Ar acylowanie Friedela-Craftsa wytworzenie kationu acyliowego (elektrofila w wiekszości zbadanych reakcjach acylowania) podstawienie występowanie produktu w postaci kompleksu z AlCl 3 ma konsekwencje w praktyce 10
11 S E Ar acylowanie Friedela-Craftsa, praktyka Konsekwencje w praktyce tworzenia kompleksów R(O)Cl-AlCl 3 i keton-alcl 3 : 1. konieczność użycia R(O)Cl i AlCl 3 w odpowiedniej proporcji molowej 2. konieczność rozkładu kompleksu keton-alcl 3 w celu wydzielenia produktu reakcji (ketonu) 11
12 S E Ar acylowanie Friedela-Craftsa, stosowanie bezwodników kwasowych wytworzenie kationu acyliowego bezwodniki kwasowe mniej reaktywne niż chlorki kwasowe cykliczne bezwodniki kwasowe są stosowane do syntezy kwasów oksokarboksylowych podstawienie (jak w przypadku użycia chlorku kwasowego) konsekwencje w praktyce użycia (RCO) 2 O:
13 18.7. S E Ar alkilowanie Friedela-Craftsa wytworzenie elektrofila (karbokationu alkilowego) karbokation może ulec przegrupowaniu (jak w innych poznanych reakcjach) najpoważniejsza (nie jedyna) wada metody podstawienie odtwarza się katalizator nie jest wiązany przez produkt (jak w acylowaniu) może być stosowany w ilości katalitycznej (zaleta metody) 13
14 18.8. S E Ar rada na przegrupowanie karbokationu w alkilowaniu Friedela-Craftsa produkt spodziewany produkt główny (lub jedyny) przyczyna niepowodzenia sposób na otrzymanie spodziewanego związku warunki redukcji redukcja Wolffa-Kiżnera NH 2 NH 2 /OH /DT lub redukcja Clemmensena Zn(Hg)/HCl/DT 14
15 Dobór warunków redukcji ketonu alkilowo-arylowego grupy funkcyjne wrażliwe na warunki redukujące też mogą ulegać przemianie CO 2 R, CHO, NO 2, C=C modyfikacja Huanga-Minlona: NH 2 NH 2 /OH-(CH 2 ) 2 -OH/DT t-buok/dmso/temp. pok. 15
16 Wady Alkilowanie i acylowanie Friedela-Craftsa, zestawienie wad i zalet Alkilowanie Friedela-Craftsa 1. Przegrupowanie karbokationu alkilowego (elektrofila) 2. Polialkilowanie - grupa alkilowa ma charakter elektronodonorowy - wprowadzenie pierwszej grupy alkilowej zwiększa podatność pierścienia benzenowego na dalsze podstawienie elektrofilowe; polialkilowanie ogranicza stosowanie dużego nadmiaru benzenu w stosunku do RCl 3. Reakcji ulegają tylko pochodne benzenu z podstawnikami: -R alkil; -OR alkoksyl X halogen (-Cl, -Br, -F) Zalety 1. Stosowanie kwasu Lewisa w małej ilości Wady Zalety Acylowanie Friedela-Craftsa 1. Stosowanie kwasu Lewisa w ilości ponadstechiometrycznej 2. Niemożność syntezy aldehydu benzoesowego (chlorek formylu nie istnieje), syntezę trzeba wykonać w innych warunkach (patrz pkt 18.10) 3. Reakcji ulegają tylko pochodne benzenu z podstawnikami: -R alkil -OR alkoksyl X halogen (-Cl, -Br, -F) 1. Brak przegrupowania kationu acyliowego (elektrofila) 2. Brak poliacylowania - grupa acylowy ma charakter elektronoakceptorowy - wprowadzenie pierwszej grupy acylowej zmniejsza podatność pierścienia benzenowego na dalsze podstawienie elektrofilowe 3. Możliwość redukcji ketonów alkilowo-arylowych do odpowiednich alkilobenzenów (niedostępnych przez alkilowanie F.-C. z powodu przegrupowania karbokationu) (pokazana w pkt 18.8 i 18.1, ale patrz też pkt 18.11) 16
17 Reakcja Gattermana-Kocha - formylowanie pierścienia benzenowego równomolowa mieszanina metoda ograniczona do benzenu i alkilobenzenów 17
18 Nazewnictwo di- i polipodstawionych pochodnych benzenu dipodstawienie o-, m-, p- tylko (!) w piśmie orto (o) 2 R 1 2 orto (o) polipodstawienie poli liczba R = 3-6 dipodstawienie meta (m) 3 R' 4 3 para (p) meta (m) R = R numeracja i kolejność zgodna z alfabetem nazwa zwyczajowa zw. monopodst. podstawą nazwy ale pochodne toluenu, to podstawione metylobenzeny 1 2 Br Br 1,2-dibromobenzen orto-dibromobenzen 2 1 CH 3 Br 1-bromometylobenzen orto-bromometylobenzen polipodstawienie jak najniższe lokanty, kolejność nazw podstawników - alfabetyczna 18
19 Względna reaktywność benzenu i jego pochodnych w S E Ar benzen przeważa efekt wzbogacania (zasada nie obowiązuje, kiedy Z = F, Cl, Br, I) obydwa efekty się sumują 19
20 Względna reaktywność benzenu i jego pochodnych w S E Ar, przykłady 20
21 Względna reaktywność benzenu i jego pochodnych w S E Ar, zestawienie podstawniki aktywujące na S E Ar benzen podstawnik aktywacja efekt kierujący silna średnia słaba orto, para podstawniki deaktywujące na S E Ar podstawnik deaktywacja słaba średnia silna efekt kierujący orto, para meta 21
22 Efekt kierujący podstawnika w S E Ar, grupa alkoksylowa rozkład ładunków podstawienie: orto para meta 22
23 Efekt kierujący podstawnika w S E Ar, grupa nitrowa rozkład ładunków podstawienie: meta orto para 23
24 Efekt kierujący podstawnika w S E Ar, przykłady 24
25 Efekt kierujący podstawnika w S E Ar, przykłady aktywniejszy pierścień O O NO 2 O HNO 3 H 2 SO 4 O + O O NO 2 O HNO 3 H 2 SO 4 O 2 N O H 3 C O H 3 C O OCH 3 OCH 3 NO 2 NO 2 O Br 2, Fe Br O H 3 C H 3 C 25
26 Efekt kierujący podstawnika w S E Ar, proporcja molowa produktów HNO 3 H 2 SO NO podstawniki kierujące pozycję orto i para im podstawnik bardziej rozbudowany przestrzennie, tym większe zatłoczenie steryczne w pozycji orto NO 2 61% 39% tym większa skłonność podstawnika do kierowania w pozycję para HNO 3 H 2 SO NO NO 2 50% 50% HNO 3 H 2 SO NO NO 2 18% 82% 26
27 Efekt kierujący podstawnika w S E Ar, synteza trójpodstawionych benzenów podstawniki tego samego rodzaju (kierują w takie same pozycje) efekt kierujący - zgodny efekt kierujący - niezgodny ** CH 3 CH HNO 3 3 ** H 2 SO 4 ** CH 3 CH 3 NO 2 podstawniki różnego rodzaju (nie kierują w takie same pozycje) efekt kierujący - zgodny efekt kierujący - niezgodny CH 3 CH HNO 3 3 H ** ** 2 SO 4 NO 2 NO 2 NO 2 27
28 Nukleofilowe podstawienie aromatyczne (S N Ar) wymiana halogenu Podstawienie halogenu (ale nie tylko) wiązanego z aromatycznym at. C(sp 2 ) umożliwia obecność podstawnika silnie elektronoakceptorowego (co najmniej jednego) w pozycji orto i/lub para do grupy odchodzącej 28
29 S N Ar reakcja addycji-eliminacji, a reakcja eliminacji-addycji reakcja addycji-eliminacji eliminacja addycja reakcja eliminacji-addycji Podstawienie halogenu wiązanego z aromatycznym at. C(sp 2 ) w nieobecności podstawnika silnie elektronoakceptorowego w pozycji orto i/lub para do grupy odchodzącej eliminacja addycja 29
30 Reakcje pochodnych benzenu, zachodzące w łańcuchu bocznym 30
31 Materiały uzupełniające, przypomnienia 31
32 S E Ar reagenty i elektrofile, podsumowanie halogenowanie Reakcja S E Ar Reagenty Elektrofil chlorowanie Cl 2, Fe Cl + bromowanie Br 2, Fe Br + jodowanie I 2, HNO 3 lub I 2, H 2 O 2 /H 2 SO 4 I + nitrowanie HNO 3 st., H 2 SO 4 st. sulfonowanie H 2 SO 4 st. lub oleum SO 3 NO 2+ (kation nitroniowy) acylowanie Friedela-Craftsa RC(O)Cl, AlCl 3 lub (RCO) 2 O), AlCl 3 kation acyliowy alkilowanie Friedela-Craftsa RX, AlCl 3 R + (karbokation) formylowanie Gattermana- Kocha CO/HCl, AlCl 3 kation formylowy 32
33 Sposoby otrzymania alkilobenzenów, alternatywne do alkilowania F.-C. przypomnienie reakcja Suzuki reakcja z udziałem R 2 CuLi 33
34 Wpływ podstawnika w pierścieniu benzenowym na kwasowość zw. organicznych, kwasy karboksylowe Podstawniki elektronoakceptorowe w pozycjach orto i para w stosunku do grupy karboksylowej zwiększają kwasowość aromatycznych kwasów karboksylowych. Podstawniki elektronodonorowe w pozycjach orto i para w stosunku do grupy karboksylowej zmniejszają kwasowość aromatycznych kwasów karboksylowych. Prawie wszystkie podstawniki w położeniu orto wywierają taki sam wpływ (wyjątkowo duży) - zwiększają kwasowość, niezależnie od skłonności do przyciągania lub uwalniania elektronów. 34
35 Wpływ podstawnika w pierścieniu benzenowym na kwasowość zw. organicznych, fenole Podstawniki elektronoakceptorowe w pozycjach orto i para w stosunku do grupy hydroksylowej zwiększają kwasowość fenoli. Podstawniki elektronodonorowe w pozycjach orto i para w stosunku do grupy hydroksylowej zmniejszają kwasowość fenoli. Ta prawidłowość jest nie zawsze spełniona w przypadku podstawników elektronodonorowych w pozycji meta. 35
36 Wpływ podstawnika w pierścieniu benzenowym na kwasowość zw. organicznych, aminy aromatyczne Aminy aromatyczne są słabszymi zasadami od amin alifatycznych tej samej rzędowości. Podstawniki elektronoakceptorowe w pozycjach orto i para względem grupy aminowej obniżają zasadowość amin aromatycznych. Podstawniki elektronodonorowe w pozycjach orto i para względem grupy aminowej zwiększają zasadowość amin aromatycznych. 36
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
WĘGLOWODORY AROMATYCZNE
 WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
Laboratorium. Podstawowe procesy jednostkowe w technologii chemicznej
 Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Wykład 6. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego ĆWICZENIE 5. Związki aromatyczne
 ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania
 Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
AMINY. tytoń szlachetny. nikotyna. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
BENZEN - własności chemiczne
 B I T N L MIA G GANIZNA I A BNZN - własności chemiczne 1) edukcja katalityczna wodorem PD WYSKIM IŚNINIM (do cykloheksanu). Jako katalizatory najczęściej stosowane są: Pt, Pd, Ni / Ni 2 p = 100 atm. T
B I T N L MIA G GANIZNA I A BNZN - własności chemiczne 1) edukcja katalityczna wodorem PD WYSKIM IŚNINIM (do cykloheksanu). Jako katalizatory najczęściej stosowane są: Pt, Pd, Ni / Ni 2 p = 100 atm. T
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Zakres materiału do sprawdzianu - alkeny, alkiny i areny + przykładowe zadania
 Zakres materiału do sprawdzianu - alkeny, alkiny i areny + przykładowe zadania I. Węglowodory nienasycone 1. Alkeny - węglowodory nienasycone w cząsteczkach których między atomami węgla występuje jedno
Zakres materiału do sprawdzianu - alkeny, alkiny i areny + przykładowe zadania I. Węglowodory nienasycone 1. Alkeny - węglowodory nienasycone w cząsteczkach których między atomami węgla występuje jedno
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
10. Alkeny wiadomości wstępne
 0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
Benzen 2C 6 H 6 + 3O 2 12C + 6H 2 O
 Benzen Najprostszym arenem, jest benzen o wzorze sumarycznym C 6 H 6. To bezbarwna, lotna ciecz, topniejąca w temperaturze 5,533 C, a wrząca w temperaturze 80,09 C. Gęstość benzenu w temperaturze 20 C,
Benzen Najprostszym arenem, jest benzen o wzorze sumarycznym C 6 H 6. To bezbarwna, lotna ciecz, topniejąca w temperaturze 5,533 C, a wrząca w temperaturze 80,09 C. Gęstość benzenu w temperaturze 20 C,
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Wykład 7. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 7 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Otrzymywanie węglowodorów aromatycznych 1. z katalitycznego reformingu (frakcje C 6 -C 10 ) 2. synteza alkilowych pochodnych
Wykład 7 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Otrzymywanie węglowodorów aromatycznych 1. z katalitycznego reformingu (frakcje C 6 -C 10 ) 2. synteza alkilowych pochodnych
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
20 i 21. Eliminacja halogenków alkili
 20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
Slajd 1. Slajd 2. Aminy. trietyloamina. amoniak. chlorofil
 Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
8. Delokalizacja elektronów i reaktywność dienów sprzężonych
 8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
10. Eliminacja halogenków alkili
 10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
amoniak amina 1 amina 2 amina 3
 AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
Związki aromatyczne CH 3 NH 2 OH CN. toluen anilina fenol benzonitryl O CHO CCH 3 COOH CH CH 2. kwas benzoesowy. acetofenon. benzaldehyd.
 Związki aromatyczne Cl NO 2 C 2 C 3 benzen chlorobenzen nitrobenzen etylobenzen C 3 N 2 O CN toluen anilina fenol benzonitryl O CO CC 3 COO C C 2 benzaldehyd acetofenon kwas benzoesowy styren 1 C 3 C 3
Związki aromatyczne Cl NO 2 C 2 C 3 benzen chlorobenzen nitrobenzen etylobenzen C 3 N 2 O CN toluen anilina fenol benzonitryl O CO CC 3 COO C C 2 benzaldehyd acetofenon kwas benzoesowy styren 1 C 3 C 3
Wykład 19 XII 2018 Żywienie
 Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Substytucja elektrofilowa
 Substytucja elektrofilowa Katarzyna strowska Reakcja substytucji elektrofilowej w układach aromatycznych zachodzi z wymianą atomu wodoru na reagent elektrofilowy. Związki aromatyczne są płaskimi związkami
Substytucja elektrofilowa Katarzyna strowska Reakcja substytucji elektrofilowej w układach aromatycznych zachodzi z wymianą atomu wodoru na reagent elektrofilowy. Związki aromatyczne są płaskimi związkami
Węglowodory Aromatyczne
 Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Materiały dodatkowe węglowodory aromatyczne, halogenopochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodory aromatyczne, halogenopochodne Areny 1. Aromatyczność związków niebenzoidowe związki aromatyczne. Benzen
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodory aromatyczne, halogenopochodne Areny 1. Aromatyczność związków niebenzoidowe związki aromatyczne. Benzen
Slajd 1. Reakcje alkinów
 Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Procesy jednostkowe. Reakcje halogenowania
 Procesy jednostkowe Reakcje halogenowania Procesy jednostkowe Klasyfikacja procesów technologicznych przeprowadzanych w przemyśle organicznym. Nazwa procesu jednostkowego pochodzi od nazwy typu reakcji
Procesy jednostkowe Reakcje halogenowania Procesy jednostkowe Klasyfikacja procesów technologicznych przeprowadzanych w przemyśle organicznym. Nazwa procesu jednostkowego pochodzi od nazwy typu reakcji
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych:
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Zadanie 1. (3 pkt) a) Dokończ poniższe równanie reakcji (stosunek molowy substratów wynosi 1:1).
 Zadanie 1. (3 pkt) a) Dokończ poniższe równanie reakcji (stosunek molowy substratów wynosi 1:1). b) Podaj nazwę systematyczną związku organicznego otrzymanego w tej reakcji. c) Określ, jaką rolę w tej
Zadanie 1. (3 pkt) a) Dokończ poniższe równanie reakcji (stosunek molowy substratów wynosi 1:1). b) Podaj nazwę systematyczną związku organicznego otrzymanego w tej reakcji. c) Określ, jaką rolę w tej
Materiały dodatkowe alkohole, fenole, etery
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14):
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Kierunek i poziom studiów: Biotechnologia, pierwszy. Nazwa wariantu modułu (opcjonalnie): nie dotyczy
 Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Spis treści. Nazewnictwo kwasów karboksylowych.
 Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
RJC Y R R Y R R R H R H. Slides 1 to 24
 JC eakcje Eliminacji (E1 & E2) B δ B δ B Slides 1 to 24 JC eakcje Eliminacji Dwa mechanizmy są moŝliwe wtedy, kiedy zasada (B - ) atakuje halogenek alkilowy z atomem w pozycji α; ; zachodząca reakcja eliminacji
JC eakcje Eliminacji (E1 & E2) B δ B δ B Slides 1 to 24 JC eakcje Eliminacji Dwa mechanizmy są moŝliwe wtedy, kiedy zasada (B - ) atakuje halogenek alkilowy z atomem w pozycji α; ; zachodząca reakcja eliminacji
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
PROGRAM ĆWICZEŃ Program ćwiczeń z chemii organicznej obejmuje wykonanie jedenastu zadań praktycznych i zdanie czterech kolokwiów.
 Wrocław 2019-10-01 REGULAMIN PRZEDMIOTU CHEMIA ORGANICZNA DLA STUDENTÓW II ROKU WYDZIAŁU FARMACEUTYCZNEGO UMW WE WROCŁAWIU (150 godzin ćwiczeń, 60 godzin wykładów) w roku akademickim 2019/ 2020 PROGRAM
Wrocław 2019-10-01 REGULAMIN PRZEDMIOTU CHEMIA ORGANICZNA DLA STUDENTÓW II ROKU WYDZIAŁU FARMACEUTYCZNEGO UMW WE WROCŁAWIU (150 godzin ćwiczeń, 60 godzin wykładów) w roku akademickim 2019/ 2020 PROGRAM
EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III
 Miejsce na naklejkę z kodem szkoły iejsce na naklejkę z kodem szkoły dysleksja Liczba pkt: Wynik %: Ocena: MCH-R1A1P-062 EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III ARKUSZ II Arkusz
Miejsce na naklejkę z kodem szkoły iejsce na naklejkę z kodem szkoły dysleksja Liczba pkt: Wynik %: Ocena: MCH-R1A1P-062 EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III ARKUSZ II Arkusz
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka
 Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
WĘGLOWODORY AROMATYCZNE.
 Spis treści 1 WĘGLOWODORY AROMATYCZNE. 2 Budowa i nomenklatura węglowodorów aromatycznych 3 Efekt mezomeryczny 4 Substytucja elektrofilowa w układach aromatycznych 4.1 Profil energetyczny reakcji. 4.2
Spis treści 1 WĘGLOWODORY AROMATYCZNE. 2 Budowa i nomenklatura węglowodorów aromatycznych 3 Efekt mezomeryczny 4 Substytucja elektrofilowa w układach aromatycznych 4.1 Profil energetyczny reakcji. 4.2
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 2
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Kartkówka nr 1 Imię i Nazwisko:.. Nr albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1.
 Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
Chemia organiczna. Związki zawierające azot. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Program wykładu Chemia Organiczna I
 Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Stereochemia Ułożenie atomów w przestrzeni
 Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
+ HCl + + CHLOROWCOWANIE
 CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Podział związków organicznych
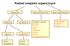 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
POŁOŻENIA SYGNAŁÓW PROTONÓW POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA
 POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna (0310-CH-S1-026) Nazwa wariantu modułu (opcjonalnie):
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
Wykład 8. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 8 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) ALKOHOLE I FENOLE Związki o wzorze ogólnym R-OH. W fenolach grupa OH jest bezpośrednio związana z pierścieniem aromatycznum.
Wykład 8 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) ALKOHOLE I FENOLE Związki o wzorze ogólnym R-OH. W fenolach grupa OH jest bezpośrednio związana z pierścieniem aromatycznum.
ROZWIĄZANIA ZADAŃ II ETAPU XXII KONKURSU CHEMICZNEGO DLA UCZNIÓW SZKÓŁ PONADGIMNAZJALNYCH
 ROZWIĄZANIA ZADAŃ II ETAPU XXII KONKURSU CHEMICZNEGO DLA UCZNIÓW SZKÓŁ PONADGIMNAZJALNYCH Zadanie 1 A PbCO 3 węglan ołowiu(ii); B Pb 3 O 4 tlenek diołowiu(ii) ołowiu(iv), tetratlenek triołowiu; C PbO tlenek
ROZWIĄZANIA ZADAŃ II ETAPU XXII KONKURSU CHEMICZNEGO DLA UCZNIÓW SZKÓŁ PONADGIMNAZJALNYCH Zadanie 1 A PbCO 3 węglan ołowiu(ii); B Pb 3 O 4 tlenek diołowiu(ii) ołowiu(iv), tetratlenek triołowiu; C PbO tlenek
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu. F Br H 3 C
 alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
Maria Bełtowska-Brzezinska, Tomasz Węsierski
 Ćwiczenie 28 Maria Bełtowska-Brzezinska, Tomasz Węsierski BADANIE ELEKTRONODONOROWYCH I ELEKTRONOAKCEPTOROWYCH WŁAŚCIWOŚCI PODSTAWNIKÓW W OPARCIU O RÓWNANIE HAMMETTA Zagadnienia: Korelacja Hammetta, korelacja
Ćwiczenie 28 Maria Bełtowska-Brzezinska, Tomasz Węsierski BADANIE ELEKTRONODONOROWYCH I ELEKTRONOAKCEPTOROWYCH WŁAŚCIWOŚCI PODSTAWNIKÓW W OPARCIU O RÓWNANIE HAMMETTA Zagadnienia: Korelacja Hammetta, korelacja
ALKENY WĘGLOWODORY NIENASYCONE
 Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
CH 3 OH C 2 H 5 OH H 3 C CH 2 CH 2 OH H 3 C CH CH 3 OH metanol etanol propan-1-ol propan-2-ol H 2 C CH 2 OH OH H 2 C CH CH 2 OH OH OH
 Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
MECHANIZMY FRAGMENTACJI ZWIĄZKÓW ORGANICZNYCH. Copyright 2003 Witold Danikiewicz
 MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
