13. B E Z W O D N I K I I H A L O G E N K I K W A S O W E Aleksander Kołodziejczyk sierpień 2007
|
|
|
- Aleksandra Adamska
- 8 lat temu
- Przeglądów:
Transkrypt
1 13. B E Z W D N I K I I A L G E N K I K W A S W E Aleksander Kołodziejczyk sierpień 2007 A L G E N K I K W A S W E alogenki kwasowe są pochodnymi kwasów karboksylowych, w których funkcja hydroksylowa została zastąpiona przez halogen. X X : F; l; Br; I Występowanie alogenki kwasowe nie występują w stanie naturalnym, ponieważ są bardzo reaktywnymi związkami. Wszystkie zostały otrzymywane syntetycznie. W praktyce laboratoryjnej i w przemyśle zastosowanie znalazły głównie chlorki kwasowe. Nomenklatura Nazwę halogenków kwasowych tworzy się przez dodanie do nazwy halogenku (fluorku, chlorku, bromku lub jodku) nazwę reszty acylowej, np. chlorek acetylu. 3 chlorek acetylu l 2 5 Br bromek propionylu chlorek cykloheksanokarbonylu l bromek benzoilu Br trzymywanie alogenki kwasowe otrzymuje się z kwasów karboksylowych. Najczęściej stosowanym odczynnikiem do przekształcania kwasów w chlorki kwasowe jest chlorek tionylu (Sl 2 ). Zaletą, oprócz niskiej ceny odczynnika i dobrej wydajności jest to, że obok chlorku kwasowego powstają łatwe do usunięcia produkty gazowe (S 2 i l). Podobne zalety wykazuje chlorek oksalilu ll. S 2 l S l % 3 kwas 2,4,6-trimetylobenzoesowy chlorek 2,4,6-trimetylobenzoilu l ll l 2 kwas 3-fenylopropanowy chlorek 3-fenylopropanoilu (95%) eakcja kwasów karboksylowych z chlorkiem tionylu biegnie zgodnie z mechanizmem S N. W wyniku addycji Sl 2 do acylowego atomu węgla powstaje chlorosiarczyn acylu, który pod wpływem anionu chlorkowego traci cząsteczkę S 2 i przekształca się w chlorek kwasowy. 1
2 - l : : : : : S : S l S l : : l - S 2 l - l l : l : kwas karboksylowy chlorosiarczyn chlorek kwasowy hlorki kwasowe można również otrzymywać za pomocą pochodnych fosforu takich, jak Pl 3, Pl 3, Pl 5. Bromki kwasowe syntezuje się z kwasów i PBr 3 lub PBr 3, zaś jodki kwasowe powstają z chlorków kwasowych pod wpływem jodowodoru, a fluorki kwasowe z bezwodników i bezwodnego fluorowodoru. 2 3 Na PBr Br NaP 3 NaBr octan sodu bromek acetylu (65%) l kwas p-nitrobenzoesowy Pl 5 N 2 (95%) N 2 Pl 3 l chlorek p-nitrobenzolilu Właściwości fizyczne i fizjologiczne alogenki kwasowe o niskich ciężarach cząsteczkowych są cieczami; chlorek acetylu wrze w temperaturze 52 o, chlorek propionylu w 78 o, a chlorek benzoilu w 198 o. hlorek p- nitrobenzoilu jest krystaliczny, topnieje w temperaturze 73 o. alogenki kwasowe są nierozpuszczalne w wodzie, ale reagują z nią ulegając rozkładowi do kwasów karboksylowych. Po wlaniu do wody opadają na dno i w niskiej temperaturze wolno hydrolizują z wydzielaniem l. Niższe halogenki kwasowe reagują z wodą energiczniej, a bardzo gwałtownie z alkoholami (rozpuszczają się w nich). alogenki kwasowe mają intensywny, gryzący zapach; nawet te niskolotne są duszące dymią na powietrzu. Właściwości chemiczne alogenki kwasowe są bardzo reaktywne, ulegają rozkładowi (lizie) pod wpływem wielu odczynników. Z wodą zachodzi hydroliza do kwasów karboksylowych, z alkoholami w wyniku alkoholizy powstają estry, z amoniakiem (amonoliza) tworzą się amidy niepodstawione, z aminami (aminoliza) amidy podstawione, a z solami kwasów karboksylowych bezwodniki kwasowe. 1. ydroliza hlorki kwasowe w reakcji z wodą ulegają hydrolizie do kwasów karboksylowych. Im mniejsza masa cząsteczkowa chlorku tym szybciej reaguje on z wodą. - : : : : : - B l : :.... l - l - B: chlorek benzoilu kwas benzoesowy W praktyce hydroliza chlorków kwasowych nie jest wykorzystywana do otrzymywania kwasów karboksylowych, gdyż to z kwasów otrzymuje się chlorki kwasowe. Należy jednak pamiętać o tym, że chlorki kwasowe są wrażliwe na wilgoć. Powinno się, zatem przechowywać je w 2
3 szczelnie zamkniętych naczyniach, a reakcje z nimi prowadzić w warunkach bezwodnych. Wyższe chlorki kwasowe są mniej reaktywne i można ich roztwory w rozpuszczalniku niemieszającym się z wodą przemywać zimną wodą w celu oczyszczenia, a następnie suszyć (usuwać resztki wody). 2. Alkoholiza eakcja chlorków kwasowych z alkoholami, zwana reakcją alkoholizy, czyli rozkładu pod wpływem alkoholu jest szeroko stosowana do otrzymywania estrów. Py ( 2 3 l - l 3 ( chlorek acetylu butan-1-ol octan butylu (90%) l Py - l chlorek benzoilu cykoheksanol benzoesan cykloheksylu (97%) eakcję prowadzi się wobec zasad, np. pirydyny (Py), Na lub NEt 3, które pochłaniają wydzielający się chlorowodór. Alkoholiza chlorków kwasowych biegnie zwykle gwałtowniej niż ich hydroliza, ponieważ są one rozpuszczalne w alkoholach. Z tego powodu alkoholizę należy prowadzić ostrożnie, w obniżonej temperaturze, wkraplając chlorek do środowiska reakcji. Szybkość alkoholizy chlorków kwasowych w dużym stopniu zależy od rzędowości reagującego alkoholu. Alkohole 1 o reagują znacznie szybciej niż 2 o, dlatego wykorzystując tę zależność można alkohole niżej rzędowe selektywnie acylować w obecności wyżej rzędowych. l Py l chlorek benzolilu 4-hydroksymetylocykloheksanol 4-benzoiloksymetylocykloheksanol (80%) 3. Amonoliza i aminoliza alogenki kwasowe w obecności amoniaku ulegają amonolizie, a pod wpływem amin 1 o i 2 o aminolizie. W obu reakcja tworzą się amidy, z wysokimi wydajnością, odpowiednio niepodstawione lub podstawione. Zarówno amonoliza jak i aminoliza niskocząsteczkowych chlorków kwasowyych biegnie gwałtownie. ( 3 l 2 :N 3 ( 3 N 2 N 4 l chlorek 2-metylopropanoilu 2-metylopropanoamid (83%) l N 2 Na N chlorek benzoilu anilina benzanilid (75%) eakcja aminolizy chlorków i bezwodników kwasowych w wodzie wobec Na znana jest pod nazwą reakcji Schottena-Baumanna. 3
4 arl Schotten ( ), ur. w Marburgu, Niemcy; doktorat u ofmanna w Berlinie; prof. na Uniwersytecie w Berlinie. eakcja Schottena-Baumanna wykorzystywana jest zarówno laboratoryjne, jak i w przemyśle. Przykładem praktycznego zastosowania amonolizy chlorku kwasowego może być synteza leku uspokajającego trimetozyny. chlorek 3,4,5-trimetoksybenzolilu l N morfolina Na/ N trimetozyna Syntetyczna trimetozyna jest analogiem (podobna w budowie) do meskaliny, narkotyku wytwarzanego przez pejot, kaktus rosnący w Meksyku i na południu USA N 2 meskalina Meskalina, silny, halucynogenny narkotyk wywołuje zaburzenie poczucia czasu i miejsca przebywania oraz barwne wizje. Zażywana wielokrotnie powoduje uzależnienie i zmiany psychiczne przypominające schizofrenię. Na przełomie XIX i XX w. była popularna pośród malarzy, którzy pod jej wpływem tworzyli obrazy zawierające niezwykłe kształty i barwy (Witkacy). Natomiast morfolina, pomimo podobieństwa w nazwie do morfiny nie jest narkotykiem. 4. edukcja Przez długi czas chlorki kwasowe stanowiły cenny substrat do otrzymywania aldehydów. Pierwotnym ich substratem były łatwo dostępne kwasy karboksylowe, których przekształcenie w chlorki kwasowe nie nastręczało trudności. Problem stanowiła ich redukcja, ponieważ łatwiej jest zredukować chlorki kwasowe do alkoholi 1 o, niż do aldehydów. Przez długi czas jedynym dostępnym sposobem redukcji chlorków kwasowych było ich uwodornienie wodorem w obecności katalizatora palladowego zatrutego związkami siarki. eakcję tę znaną pod nazwą reakcji osenmunda prowadziło się we wrzącym ksylenie. Nie cieszyła się powodzeniem ze względu na stosunkowo niskie wydajności i niezbyt dogodne warunki jej prowadzenia. Pd/S -l 2 - l ksylen, tw becnie chlorki kwasowe najdogodniej przeprowadza się w aldehydy za pomocą tri-tertbutyloksyhydroglinianu litu. l chlorek kwasowy 1. LiAl[( 3 ] 3 2. / aldehyd Ten selektywny reduktor otrzymuje się w reakcji t-butanolu z tetrahydroglinianem litu. 3 ( 3 LiAl 4 LiAl[( 3 ] Tri-tert-butyloksyhydroglinian litu selektywnie redukuje chlorki kwasowe, ponieważ ma słabsze zdolności redukujące niż LiAl 4, a jego rozbudowana przestrzennie cząsteczka zawiera tylko jeden atom. dczynnik ten pozwala redukować chlorki kwasowe w obecności grupy nitrowej. 4
5 l l chlorek p-nitrobenzoilu N 2 1. LiAl[( 3 ] 3 2. / N 2 (81%) p-nitrobenzaldehyd czywiście nie ma zalet bez wad, tri-tert-butyloksyhydroglinian litu w porównaniu do LiAl 4 jest mniej wydajny (stechiometrycznie redukuje cztery razy mniej chlorku). W takim przypadku mówimy o niskiej wydajności atomowej reakcji. Z powodów ekonomicznych ten sposób syntezy aldehydów jest stosowany jedynie w badaniach naukowych i do wytwarzania drogich produktów. Tetrahydroglinian litu redukuje chlorki kwasowe do alkoholi 1 o. l 2 chlorek benzoilu 1. LiAl 4 2. / 96% alkohol benzylowy eduktorem w tej reakcji jest anion wodorkowy: -. eakcja biegnie wg mechanizmu S N. Przejściowo powstaje aldehyd, ale reakcja nie zatrzymuje się na tym etapie i biegnie dalej do alkoholu. : - : : - : : : l : - / - l : l - alkohol 1 o chlorek kwasowy W praktyce chlorki kwasowe rzadko redukowane są za pomocą LiAl 4, ponieważ te same produkty można otrzymać z kwasu, niepotrzebny jest, więc etap przekształcania kwasów w chlorki kwasowe. 5. eakcje ze związkami metaloorganicznymi hlorki kwasowe reagują z dwoma molami związku Grignarda (2 mole/1 mol chlorku), ponieważ powstający przejściowo keton ulega w warunkach reakcji kolejnej addycji i po hydrolizie tworzy się alkohol 3 o. eakcja biegnie mechanizmem S N. : : : Mgl : l 3 Mgl 3 3 chlorek l benzoilu chlorek metylomagnezowy acetofenon - Mgl 2 / 3 Mgl fenylopropan-2-ol (92%) eakcję można zatrzymać na etapie ketonu pod warunkiem, że użyje się mniej reaktywnych reagentów, takich jak odczynniki Gilmana czy związki kadmoorganiczne. dczynniki Gilmana nie reagują z estrami, ani z bezwodnikami. Dietylomiedzian litu został wykorzystany do otrzymywania manikonu, feromonu alarmowego mrówek Manica. 5
6 3 2 Zadanie: nazwij systematycznie manikon 3 l ( 3 2 uli eter, -78 o chlorek 2,4-dimetyloheks-2-enoilu manikon (92%) 2 3 Związki kadmoorganiczne są też mniej reaktywne od magnezoorganicznych i służą do otrzymywania ketonów z chlorków kwasowych. Powstają one ze związków Grignarda w reakcji w chlorkiem kadmu. 2 MgX dl 2 2 d 2 MgXl 2 d 2 'l 2 --' dl 2 Mniejsza reaktywność związków kadmoorganicznych pozwala na selektywne przyłączanie reszt alkilowych wobec innych reaktywnych grup. l - 3 chlorek p-nitrobenzoilu 2 ( 3 d 2 - dl 2 N 2 dimetylokadm N 2 keton metylowo-p-nitrofenylowy ównież estry nie reagują ze związkami kadmoorganicznymi. chlorek 3-metoksykarbonylopropanoilu l [( ] 2 d ( 3 - dl 2 bis(3-metylobutylo)kadm 4-oksy-7-metylooktanoilan metylu Zadanie: nazwij ten związek przyjmując, że keton stanowi główną grupę 6. Acylowanie Firedla - raftsa hlorki kwasowe służą nie tylko do -acylowania (otrzymywania estrów) i N-acylowania (otrzymywania amidów) ale również do -acylowania prowadzącego do ketonów. Pośród reakcji -acylowania najbardziej znaną jest reakcja Friedla - raftsa polegająca na działaniu chlorku kwasowego na związek aromatyczny w obecności bezwodnego chlorku glinu. W procesie tym następuje wymiana protonu związane z aromatycznym pierścieniem na resztę acylową. eakcja biegnie wg mechanizmu S E. hlorek glinu ułatwia wytworzenie kationu acyliowego z chlorku kwasowego. chlorek propanolilu 3 2 l All All 4 kation propanoliowy W obecności związków aromatycznych dochodzi do utworzenia ketonu poprzez podstawienie aromatycznego protonu kationem acyliowym. benzen kation propanoliowy propiofenon eakcja Friedla - raftsa jest szeroko wykorzystywana w syntezie organicznej. Zamiast chlorków kwasowych stosuje się też bezwodniki kwasowe. 6
7 B E Z W D N I K I K W A S W E Bezwodniki są pochodnymi kwasów karboksylowych, w których atom wodoru funkcji hydroksylowej został podstawiony reszta acylową. Ich nazwa wywodzi się z reakcji ich powstawania, polegającej na kondensacji dwóch cząsteczek kwasu karboksylowego (kwasów), podczas której wydziela się cząsteczka wody. Wzór sumaryczny produktu różni się od dwóch cząsteczek kwasów, z których powstał, brakiem cząsteczki wody, stąd bezwodnik. - ' ' kwas karboksylowy kwas karboksylowy bezwodnik Bezwodniki mogą być symetryczne ( = ), jeżeli zbudowane są z reszt tego samego kwasu bądź niesymetryczne jeżeli powstały z cząsteczek dwóch różnych kwasów ( ). Występowanie Bezwodniki kwasowe nie występują w naturze, są otrzymywane syntetycznie. Nomenklatura Nazwy bezwodników tworzone są od nazw kwasów, z których się wywodzą, przy czym w nazwie bezwodnika symetrycznego po słowie bezwodnik występuje nazwa kwasu w formie przymiotnikowej, np. bezwodnik octowy, bezwodnik ftalowy itd. Bezwodniki niesymetryczne nazywa się podobnie jak ketony, tzn. po słowie bezwodnik podaje się w porządku alfabetycznym przymiotnikowe nazwy macierzystych kwasów, np. bezwodnik mrówkowo-octowy czy masłowo-propionowy. (l bezwodnik octowy bezwodnik ftalowy bezwodnik chlorooctowy bezwodnik masłowo-propionowy W nazwach bezwodników stosuje się również systematyczne nazwy kwasów. ( trzymywanie bezwodnik heksanowy bezwodnik cykloheksanokarboksylowy 1. Acylowanie soli kwasów Typowy sposób otrzymywania bezwodników, zarówno symetrycznych, jak i niesymetrycznych polega na reakcji soli kwasu z chlorkiem kwasowym. - Nal Na l 3 3 mrówczan sodu chlorek acetylu bezwodnik mrówkowooctowy (64%) 2. Przemysłowa produkcja bezwodnika octowego Przemysłowa metoda otrzymywania bezwodnika octowego polega na reakcji ketenu z kwasem octowym. Keten powstaje w wyniku wysokotemperaturowej dehydratacji kwasu octowego. 7
8 keten kwas octowy bezwodnik octowy 3. Za pomocą D Dogodnym laboratoryjnym sposobem otrzymywania bezwodników jest reakcja odwodnienia kwasów za pomocą dicykloheksylokarbodiimidu (D). dczynnik ten wykorzystuje się często w chemii peptydów do tworzenia wiązania peptydowego. Z N-chronionych aminokwasów można otrzymywać symetryczne lub niesymetryczne bezwodniki, które służą do acylowania - chronionych aminokwasów. D kwas 2 - ( bezwodnik - 4. Dehydratacja termiczna kwasów dikarboksylowych Bezwodniki cykliczne powstają w trakcie termicznej dehydratacji kwasów dikarboksylowych. kwas ftalowy o bezwodnik ftalowy kwas bursztynowy o bezwodnik bursztynowy Właściwości chemiczne Bezwodniki kwasowe swoimi właściwościami przypominają chlorki kwasowe, są jednak trochę mniej reaktywne. Ulegają one reakcjom hydrolizy, alkoholizy, amonolizy, aminolizy i redukcji, wchodzą w reakcję ze związkami metaloorganicznymi i służą do -acylowania. 1. ydroliza Bezwodniki hydrolizują w obecności wody do kwasu (kwasów), z którego się wywodzą. Nie jest to jednak metoda otrzymywania kwasów. Należy jedynie pamiętać o możliwości hydrolizy bezwodników podczas pracy z nimi. ( 2 ydroliza bezwodników biegnie wg mechanizmu typowego dla pochodnych kwasów, czyli jest to złożona substytucja nukleofilowa. W pierwszym etapie następuje addycja do acylowego atomu węgla, po czym dochodzi do eliminacji grupy odchodzącej, w tym wypadku cząsteczki kwasu. : : -.. : bezwodnik kwas 2. Alkoholiza W wyniku reakcji alkoholu z bezwodnikiem tworzy się ester i wydziela cząsteczka kwasu. ( 8
9 Nie jest wydajny sposób otrzymywania estrów, ponieważ połowa cząsteczki bezwodnika jest marnowana, jako produkt uboczny wydziela się kwas karboksylowy. Niektóre bezwodniki są jednak powszechnie stosowane, gdyż są tanie i wygodniejsze w użyciu niż chlorki kwasowe. Należą do nich bezwodnik octowy i benzoesowy. eakcja alkoholizy bezwodników jest katalizowana zarówno przez kwasy jak i zasady. Mechanizm: ' : : ' -.. ' : bezwodnik alkohol ester kwas Zarówno podczas hydrolizy, jak i alkoholizy bezwodników dochodzi do autokatalizy, ponieważ powstający w reakcji kwas katalizuje te reakcje. Wykorzystywanie tylko połowy cząsteczki bezwodnika do acylowania jest dogodnym sposobem otrzymywania monoestrów kwasów dikarboksylowych z bezwodników cyklicznych. Et : bezwodnik bursztynowy wodorobursztynian etylu bezwodnik ftalowy alkohol sec-butylowy wodoroftalan sec-butylu Acylowanie za pomocą bezwodników w środowisku wody z udziałem Na, podobnie jak dla chlorków kwasowych, nazywa się reakcją Schottena-Baumanna. Bezwodnik octowy jest wykorzystywany w produkcji aspiryny, czyli kwasu acetylosalicylowego. kwas salicylowy Zadanie: nazwij systematycznie substrat i produkt Ac 2 Na Ac aspiryna AcNa 3. Amonoliza (aminoliza) W reakcji bezwodników z amoniakiem lub aminami 1 o lub 2 o tworzą się amidy, odpowiednio niepodstawione lub podstawione oraz sól. Wymagane są dwa mole aminy na 1 mol bezwodnika lub użycie innej zasady do wiązania tworzącego się kwasu. Powstający w reakcji kwas tworzy z aminą sól, a amina w postaci soli nie ulega acylowaniu. ( 2 N 2 N 2 - N 2 2 Mechanizm: ' N - N' 2 - : : N' 2 N' 2 ' 2 : bezwodnik sól ':, alkil lub aryl ' 2 N amid Bezwodnik octowy jest często stosowany do reakcji N-acylowania, prowadzącej do amidów. Grupa aminowa jest bardziej podatna na acylowanie niż hydroksylowa, dlatego też można 9
10 selektywnie acylować aminy wobec alkoholi (fenoli). W ten sposób otrzymuje się p- acetamidofenol, powszechnie stosowany lek przeciwbólowy, znany pod nazwą paracetamolu. Za pomocą bardziej reaktywnych chlorków kwasowych trudniej przeprowadzać acylowanie selektywne. p-aminofenol N 2 Ac 2 Na NAc AcNa p-acetamidofenol (paracetamol) Podobnie jak w przypadku -acylowania (alkoholizy bezwodników) podczas ich amonolizy także wydziela się l mol kwasu; w tym przypadku w postaci soli. Amonoliza bezwodników cyklicznych jest dogodnym sposobem otrzymywania monoamidów kwasów dikarboksylowych. - 2 N 4 N : bezwodnik N 2 N 3 2 / bursztynowy monoamin sól kwasu bursztynowego Użycie bezwodnika bursztynowego i amoniaku w stosunku molowym 1 : 1 nie prowadzi do imidu; w tych warunkach powstaje także monoamid. Imid kwasu bursztynowego (sukcynoimid) jest powszechnie stosowanym, komercyjnym odczynnikiem. Jego otrzymywanie polega na termicznym rozkładzie soli amonowej kwasu bursztynowego N bursztynian 4 N N 3 2 diaminu sukcynoimid (82%) Podobne reakcje zachodzą z bezwodnikiem ftalowym. Użycie aminy 1 o do reakcji z cyklicznymi bezwodnikami prowadzi bezpośrednio do imidu (Npodstawionego). bezwodnik EtN 2 N-Et ftalowy etyloamina N-etyloftalimid (>90%) 4. edukcja edukowanie bezwodników tetrahydroglinianem litu prowadzi do alkoholi. Z jednego mola bezwodnika symetrycznego otrzymuje się 2 mole alkoholu. ekcja ta nie ma większego znaczenia praktycznego, ponieważ bezpośrednio z kwasu można otrzymać ten sam produkt. ( LiAl 4 1. eter 2. / eakcja ze związkami Grignarda Bezwodniki reagują ze związkami Grignarda podobnie jak inne związki zawierające grupę karbonylową. eakcja ta nie ma większego znaczenia, ponieważ podobne produkty otrzymuje się z łatwiej dostępnych estrów. 10
11 6. Acylowanie Friedla-raftsa Bezwodniki, podobnie jak chlorki kwasowe używane są do -acylowania arenów. eakcja biegnie w obecności chlorku glinu, który ułatwia powstawanie kationu acyliowego. benzen 3 3 bezwodnik octowy All 3 3 Ac acetofenon (83%) 3 mezytylen 3 ( 3 All 3 3 bezwodnik octowy Ac acetylomezytylen 3 Acylowanie arenów cyklicznymi bezwodnikami prowadzi do oksokwasów. benzen All 3 bezwodnik ftalowy 2-karboksybenzofenon benzen All 3 bezwodnik bursztynowy (94%) kwas β-benzoilopropionowy Właściwości chemiczne bezwodników Schemat 13.1 redukcja [] hydroliza [] ' alkoholiza (-acylowanie) Ar/All 3 N' 2 Ar reakcja Friedla-raftsa (-acylowanie) amonoliza (N-acylowanie) -' N' 2 11
Kwasy karboksylowe C O OH OH C CH 2 H OH CH 2 C CH 3 C OH C OH C OH. propionowy. mrówkowy. akrylowy. octowy. masłowy metakrylowy.
 Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Mg I. I Mg. Nie można ich jednak otrzymać ze związków, które posiadają grupy chlorowcowe w tak zwanym ustawieniu wicynalnym.
 nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
HCOOH kwas metanowy ( mrówkowy ) CH 3. COOH kwas etanowy ( octowy ) CH 2
 Kwasy karboksylowe, Ar Nazewnictwo: Kwasy, które są pochodnymi alkanów o otwartych łańcuchach, są nazywane w sposób systematyczny przez dodanie nazwy kwas i dodanie końcówki owy do alkanu - kwas alkanowy
Kwasy karboksylowe, Ar Nazewnictwo: Kwasy, które są pochodnymi alkanów o otwartych łańcuchach, są nazywane w sposób systematyczny przez dodanie nazwy kwas i dodanie końcówki owy do alkanu - kwas alkanowy
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Pochodne kwasów karboksylowych. Krystyna Dzierzbicka
 Pochodne kwasów karboksylowych Krystyna Dzierzbicka halogenki kwasowe X X = l, Br, I bezwodniki kwasowe ' estry ' amidy N 2 sole nitryle N Nazwy grup acylowych 3 3 2 acyl metanoil formyl etanoil acetyl
Pochodne kwasów karboksylowych Krystyna Dzierzbicka halogenki kwasowe X X = l, Br, I bezwodniki kwasowe ' estry ' amidy N 2 sole nitryle N Nazwy grup acylowych 3 3 2 acyl metanoil formyl etanoil acetyl
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Zadanie: 2 (4 pkt) Napisz, uzgodnij i opisz równania reakcji, które zaszły w probówkach:
 Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Technologia chemiczna. Dwiczenie nr 4. OTRZYMYWANIE OCTANU n-butylu
 Technologia chemiczna Dwiczenie nr 4 OTRZYMYWANIE OCTANU n-butylu Wrocław, 2010 ESTRY BUDOWA, WŁAŚCIWOŚCI, OTRZYMYWANIE Estry to związki organiczne, które są pochodnymi kwasów karboksylowych (lub nieorganicznych)
Technologia chemiczna Dwiczenie nr 4 OTRZYMYWANIE OCTANU n-butylu Wrocław, 2010 ESTRY BUDOWA, WŁAŚCIWOŚCI, OTRZYMYWANIE Estry to związki organiczne, które są pochodnymi kwasów karboksylowych (lub nieorganicznych)
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
ORGANICZNE POCHODNE KWASU WĘGLOWEGO. Krystyna Dzierzbicka
 RGANIZNE PDNE KWASU WĘGLWEG Krystyna Dzierzbicka Kwas węglowy ( 2 3 ) słaby kwas nieorganiczny, istnieje tylko w wodnych roztworach. 2 == + kwas węglowy Trwałą nieorganiczną pochodną kwasu węglowego jest
RGANIZNE PDNE KWASU WĘGLWEG Krystyna Dzierzbicka Kwas węglowy ( 2 3 ) słaby kwas nieorganiczny, istnieje tylko w wodnych roztworach. 2 == + kwas węglowy Trwałą nieorganiczną pochodną kwasu węglowego jest
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Substytucja nukleofilowa
 Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
Narysuj stereoizomery cis i trans dla 1,2-dibromocyklobutanu. Czy ulegają one wzajemnej przemianie, odpowiedź uzasadnij.
 WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
Podział związków organicznych
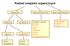 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
WĘGLOWODORY AROMATYCZNE
 WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
+ HCl + + CHLOROWCOWANIE
 CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
WĘGLOWODORY, ALKOHOLE, FENOLE. I. Wprowadzenie teoretyczne
 WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
WĘGLWDRY, ALKHLE, FENLE I. Wprowadzenie teoretyczne Węglowodory Węglowodory są to połączenia organiczne zbudowane z atomów węgla i wodoru. Ze względu na różne sposoby łączenia się atomów węgla w tych związkach
Węglowodory poziom podstawowy
 Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Materiały dodatkowe związki karbonylowe
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
Br Br. Br Br OH 2 OH NH NH 2 2. Zakład Chemii Organicznej: kopiowanie zabronione
 Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
UJ - Collegium Medicum, KChO, Pracownia chemii organicznej S. Acylacja. Symbol Nazwa otrzymywanego preparatu strona. Acylacja część teoretyczna 2
 UJ - Collegium Medicum, KCh, Pracownia chemii organicznej S Symbol Nazwa otrzymywanego preparatu strona część teoretyczna 2 A1 Aspiryna I 5 A2 Aspiryna II 6 A3 Acetanilid 7 A4 N-acetylo-p-toluidyna 8 A5
UJ - Collegium Medicum, KCh, Pracownia chemii organicznej S Symbol Nazwa otrzymywanego preparatu strona część teoretyczna 2 A1 Aspiryna I 5 A2 Aspiryna II 6 A3 Acetanilid 7 A4 N-acetylo-p-toluidyna 8 A5
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 2
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2
![liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2 liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2](/thumbs/65/54124071.jpg) Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Zadanie 4. Mrówczan metylu ma taki sam wzór sumaryczny jak: A. octan etylu. C. kwas mrówkowy. B. octan metylu. D. kwas octowy.
 Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 3 marca 2011 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 3 marca 2011 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Kwasy Karboksylowe i Nitryle. Według McMurry s Organic Chemistry, 6 th edition
 Kwasy Karboksylowe i Nitryle Według McMurry s Organic Chemistry, 6 th edition Znaczenie Kwasów Karboksylowych (RCO 2 H) Materiał wyjściowy dla pochodnych acylowych (estrów, amidów, chlorków kwasowych)
Kwasy Karboksylowe i Nitryle Według McMurry s Organic Chemistry, 6 th edition Znaczenie Kwasów Karboksylowych (RCO 2 H) Materiał wyjściowy dla pochodnych acylowych (estrów, amidów, chlorków kwasowych)
Acylacja. Symbol Nazwa otrzymywanego preparatu strona. Acylacja część teoretyczna 2. A1 Aspiryna I 5. A2 Aspiryna II 6.
 UJ - Collegium Medicum, KCh, Pracownia chemii organicznej Symbol Nazwa otrzymywanego preparatu strona część teoretyczna 2 A1 Aspiryna I 5 A2 Aspiryna II 6 A3 Acetanilid 7 A4 N-acetylo-p-toluidyna 8 A5
UJ - Collegium Medicum, KCh, Pracownia chemii organicznej Symbol Nazwa otrzymywanego preparatu strona część teoretyczna 2 A1 Aspiryna I 5 A2 Aspiryna II 6 A3 Acetanilid 7 A4 N-acetylo-p-toluidyna 8 A5
b) Podaj liczbę moli chloru cząsteczkowego, która całkowicie przereaguje z jednym molem glinu.
 Informacja do zadań 1 i 2 Chlorek glinu otrzymuje się w reakcji glinu z chlorowodorem lub działając chlorem na glin. Związek ten tworzy kryształy, rozpuszczalne w wodzie zakwaszonej kwasem solnym. Z roztworów
Informacja do zadań 1 i 2 Chlorek glinu otrzymuje się w reakcji glinu z chlorowodorem lub działając chlorem na glin. Związek ten tworzy kryształy, rozpuszczalne w wodzie zakwaszonej kwasem solnym. Z roztworów
Slajd 1. Alkohole i fenole. Cholesterol. Slajd 2. Budowa alkoholi. metanol. metanol. Grupą funkcyjną jest (OH) Tlen posiada hybrydyzacjęsp 3
 Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
l. at C Wzór sumaryczny pół strukturalny Nazwa systematyczna Nazwa zwyczajowa 1 HCOOH
 KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
EGZAMIN WSTĘPNY NA STUDIUM DOKTORANCKIE W CBMIM PAN W ŁODZI. Zestaw pytań z chemii organicznej
 EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
Budowa tłuszczów // // H 2 C O H HO C R 1 H 2 C O C R 1 // // HC O H + HO C R 2 HC - O C R 2 + 3H 2 O
 Tłuszcze (glicerydy) - Budowa i podział tłuszczów, - Wyższe kwasy tłuszczowe, - Hydroliza (zmydlanie) tłuszczów - Utwardzanie tłuszczów -Próba akroleinowa -Liczba zmydlania, liczba jodowa Budowa tłuszczów
Tłuszcze (glicerydy) - Budowa i podział tłuszczów, - Wyższe kwasy tłuszczowe, - Hydroliza (zmydlanie) tłuszczów - Utwardzanie tłuszczów -Próba akroleinowa -Liczba zmydlania, liczba jodowa Budowa tłuszczów
Chemia organiczna. Związki zawierające grupę karbonylową. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające grupę karbonylową Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Grupy związków zawierających grupę karbonylową C=O aldehyd ester keton kwasy karboksylowy
Chemia organiczna Związki zawierające grupę karbonylową Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Grupy związków zawierających grupę karbonylową C=O aldehyd ester keton kwasy karboksylowy
Skala ocen: ndst 0 20, dst , dst , db , db , bdb Informacja:
 Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Kuratorium Oświaty w Lublinie
 Kuratorium Oświaty w Lublinie KOD UCZNIA ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 ETAP WOJEWÓDZKI Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
Kuratorium Oświaty w Lublinie KOD UCZNIA ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 ETAP WOJEWÓDZKI Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
NIEBEZPIECZNE REAKCJE CHEMICZNE
 NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Estry. 1. Cele lekcji. 2. Metoda i forma pracy. 3. Środki dydaktyczne. a) Wiadomości. b) Umiejętności
 Estry 1. Cele lekcji a) Wiadomości Uczeń: wie, jak zbudowane są cząsteczki estrów, wie, jakie jest zastosowanie estrów, wie, jakie są właściwości fizyczne octanu etylu zna pojęcia: stan równowagi dynamicznej,
Estry 1. Cele lekcji a) Wiadomości Uczeń: wie, jak zbudowane są cząsteczki estrów, wie, jakie jest zastosowanie estrów, wie, jakie są właściwości fizyczne octanu etylu zna pojęcia: stan równowagi dynamicznej,
Właściwości chemiczne nukleozydów pirymidynowych i purynowych
 Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Ćwiczenie 1. Ćwiczenie Temat: Podstawowe reakcje nieorganiczne. Obliczenia stechiometryczne.
 PROGRAM ĆWICZEŃ LABORATORYJNYCH Z CHEMII (SEMESTR LETNI) OCHRONA ŚRODOWISKA Literatura zalecana 1. P. Szlachcic, J. Szymońska, B. Jarosz, E. Drozdek, O. Michalski, A. Wisła-Świder, Chemia I: Skrypt do
PROGRAM ĆWICZEŃ LABORATORYJNYCH Z CHEMII (SEMESTR LETNI) OCHRONA ŚRODOWISKA Literatura zalecana 1. P. Szlachcic, J. Szymońska, B. Jarosz, E. Drozdek, O. Michalski, A. Wisła-Świder, Chemia I: Skrypt do
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
ĆWICZENIE III. Reakcje charakterystyczne na węglowodory (alifatyczne, aromatyczne), alkohole, aldehydy i ketony
 ĆWIZENIE III eakcje charakterystyczne na węglowodory (alifatyczne, aromatyczne), alkohole, aldehydy i ketony I. eakcje charakterystyczne odróżniające węglowodory alifatyczne nasycone od nienasyconych 1.
ĆWIZENIE III eakcje charakterystyczne na węglowodory (alifatyczne, aromatyczne), alkohole, aldehydy i ketony I. eakcje charakterystyczne odróżniające węglowodory alifatyczne nasycone od nienasyconych 1.
Alkohole i fenole. Opracowanie: Bartłomiej SIEPSIAK klasa 3d Opiekun: p. Teresa Gębicka
 Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
ROLNICTWO. Ćwiczenie 1
 PROGRAM ĆWICZEŃ LABORATORYJNYCH Z CHEMII (SEMESTR ZIMOWY) ROLNICTWO Ćwiczenie 1 1. Organizacja ćwiczeń. Regulamin pracowni chemicznej i przepisy BHP (Literatura zalecana, pozycja 1, rozdz. 1.1.). Zasady
PROGRAM ĆWICZEŃ LABORATORYJNYCH Z CHEMII (SEMESTR ZIMOWY) ROLNICTWO Ćwiczenie 1 1. Organizacja ćwiczeń. Regulamin pracowni chemicznej i przepisy BHP (Literatura zalecana, pozycja 1, rozdz. 1.1.). Zasady
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PROGRAM ĆWICZEŃ LABORATORYJNYCH Z CHEMII (SEMESTR LETNI) OCHRONA ŚRODOWISKA
 PROGRAM ĆWICZEŃ LABORATORYJNYCH Z CHEMII (SEMESTR LETNI) OCHRONA ŚRODOWISKA Ćwiczenie 1 (Karta pracy - 1a, 1b, 1c, 1d, 1e) 1. Organizacja ćwiczeń. Regulamin pracowni chemicznej i przepisy BHP (Literatura
PROGRAM ĆWICZEŃ LABORATORYJNYCH Z CHEMII (SEMESTR LETNI) OCHRONA ŚRODOWISKA Ćwiczenie 1 (Karta pracy - 1a, 1b, 1c, 1d, 1e) 1. Organizacja ćwiczeń. Regulamin pracowni chemicznej i przepisy BHP (Literatura
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
Krystyna Dzierzbicka Aldehydy i ketony są pochodnymi węglowodorów zawierającymi grupę karbonylową =. Aldehydy związki zawierające grupę formylową (-) połączoną z atomem węgla: R(Ar)-, R reszta alkilowa;
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
 Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA
 SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
Reakcje charakterystyczne amin i aminokwasów
 eakcje charakterystyczne amin i aminokwasów Maria Jamrozik Zastąpienie atomów wodoru w amoniaku grupami alkilowymi lub arylowymi prowadzi do powstania związków, zawierających jedno, dwa lub trzy wiązania
eakcje charakterystyczne amin i aminokwasów Maria Jamrozik Zastąpienie atomów wodoru w amoniaku grupami alkilowymi lub arylowymi prowadzi do powstania związków, zawierających jedno, dwa lub trzy wiązania
Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1.
 1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
59 Olimpiada Chemiczna I etap PRÓBA. 10 października 2012, 10:00 15:00. redagowanie treści: Kuba Skrzeczkowski
 59 Olimpiada Chemiczna I etap PRÓBA 10 października 2012, 10:00 15:00 redagowanie treści: Kuba Skrzeczkowski ZADANIE 1. Dwa problemy z kinetyki chemicznej A. W podwyższonej temperaturze izomery geometryczne
59 Olimpiada Chemiczna I etap PRÓBA 10 października 2012, 10:00 15:00 redagowanie treści: Kuba Skrzeczkowski ZADANIE 1. Dwa problemy z kinetyki chemicznej A. W podwyższonej temperaturze izomery geometryczne
Organiczne związki azotu
 Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Reakcje związków karbonylowych. Maria Burgieł R R C O. C O + Nu E C
 eakcje związków karbonylowych Maria Burgieł Związki zawierające grupę = nazywamy związkami karbonylowymi. Do najprostszych związków karbonylowych należą aldehydy, w których grupa = jest połączona z jedną
eakcje związków karbonylowych Maria Burgieł Związki zawierające grupę = nazywamy związkami karbonylowymi. Do najprostszych związków karbonylowych należą aldehydy, w których grupa = jest połączona z jedną
Kwasy karboksylowe. 1. Cele lekcji. 2. Metoda i forma pracy. 3. Środki dydaktyczne. 4. Przebieg lekcji. a) Wiadomości.
 Kwasy karboksylowe 1. Cele lekcji a) Wiadomości Uczeń zna budowę kwasów karboksylowych, nazewnictwo kwasów karboksylowych, podział kwasów karboksylowych, sposoby otrzymywania kwasów karboksylowych, właściwości
Kwasy karboksylowe 1. Cele lekcji a) Wiadomości Uczeń zna budowę kwasów karboksylowych, nazewnictwo kwasów karboksylowych, podział kwasów karboksylowych, sposoby otrzymywania kwasów karboksylowych, właściwości
Konkurs przedmiotowy z chemii dla uczniów szkół podstawowych
 Kod ucznia Konkurs przedmiotowy z chemii dla uczniów szkół podstawowych Suma punktów 13 marca 2019 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie konkursu chemicznego. Podczas rozwiązywania
Kod ucznia Konkurs przedmiotowy z chemii dla uczniów szkół podstawowych Suma punktów 13 marca 2019 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie konkursu chemicznego. Podczas rozwiązywania
I. Węgiel i jego związki z wodorem
 NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
