AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
|
|
|
- Eleonora Sadowska
- 6 lat temu
- Przeglądów:
Transkrypt
1 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1
2 KLASYFIKACJA AMIN 2
3 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3
4 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI 4
5 ZASADOWOŚĆ AMIN toluidyna p-nitrotoluen T wrz. 200 C T wrz. 238 C 5
6 STAŁA RÓWNOWAGI REAKCJI AMIN Z WODĄ i pk b jako miara ich zasadowości amina kation amoniowy miara zasadowości amin STAŁA RÓWNOWAGI REAKCJI KATIONU AMONIOWEGO Z WODĄ I pk a JAKO MIARA JEGO KWASOWOŚCI pk a = log K a miara kwasowości kationu amoniowego pk a + pk b = 14 pk b = 14 pk a 6
7 PORÓWNANIE ZASADOWOŚCI AMIN W ROZTWORACH WODNYCH CH 3 CH 3 CH 3 NH CH 3 NH 2 CH 3 N CH 3 NH 3 amina: amoniak pk a: zasadowość: 2 > 1 > 3 > NH 3 NH 2 NH 2 NH 2 CH 3 NH 2 OCH 3 NO 2 pk a :
8 NOMENKLATURA AMIN Ogólna nazwa aminy obejmuje związki o budowie RNH 2, RR NH i RR R N, które klasyfikuje się jako odpowiednio pierwszorzędowe, drugorzędowe i trzeciorzędowe Aminy pierwszorzędowe Nazwy pierwszorzędowych amin tworzy się dodając przyrostek amina: do nazwy grupy R (alkilowej, arylowej, itd.) lub do nazwy macierzystego układu RH CH 3 CH 3 CH 3 CHNH 2 CH 3 CH 2 NH 2 CH 3 CH 2 CHNH 2 etyloamina 1-metylopropyloamina sec-butyloamina 1-metyloetyloamina izopropyloamina CH 3 NH 2 CH 3 CNH 2 C 6 H 5 CH 2 NH 2 NH 2 NH 2 NH 2 CH 3 CH 3 CHCH 2 CH 2 CHCH 3 1,1-dimetyloetyloamina tert-butyloamina benzyloamina cykloheksyloamina 2-naftyloamina heksano-2,5-diamina NH 2 NH 2 Zachowuje się nazwy zwyczajowe następujących amin aromatycznych: anilina CH 3 m-toluidyna (orazizomery orto i para) NH 2 OCH 3 o-anizydyna (orazizomery meta i para) 8
9 NOMENKLATURA AMIN Aminy drugo- i trzeciorzędowe Nazwy symetrycznych amin drugorzędowych i trzeciorzędowych tworzy się dodając przed nazwą grupy przedrostek di lub tri. (CH 3 ) 2 NH dimetyloamina (CH 3 CH 2 CH 2 ) 2 NH (CH 3 CH 2 ) 3 N dipropyloamina trietyloamina (C 6 H 5 CH 2 ) 2 NH dibenzyloamina Niesymetryczne drugorzędowe i trzeciorzędowe aminy nazywa się jako N-podstawione (lub N,N-dwupodstawione) pochodne amin pierwszorzędowych. Jako podstawę nazwy macierzystej aminy wybiera się najbardziej złożoną spośród grup związanych z atomem azotu. CH 3 CH CH CH 3 CH 2 CH 2 CH 2 N(CH 3 ) N CH 3 CH 2 CHN CH N,N-dimetylobutyloamina 2 CH CH 3 3 N,N-dimetylo-(1-metylopropylo)amina N-etylo-N-metyloanilina W przypadku, gdy grupy aminowe nie są grupami głównymi (są podstawnikami), nazywa się je przy pomocy przedrostków: grupa NH 2 amino-, HOOC N(CH grupa NHR alkiloamino-, 3 ) 2 grupa N(R) 2 dialkiloamino-. kwas p-dimetyloaminobenzoesowy 9
10 NOMENKLATURA AMIN Sole amoniowe (aminiowe) Sole i wodorotlenki zawierające czterowiązalny atom azotu (R 4 N + X ), w których R oznacza takie same lub różne grupy, nazywa się dodając do wymienionych alfabetycznie nazw podstawników związanych z atomem azotu przyrostek amoniowy i podając na początku nazwę anionu (jako oddzielne słowo). [C 6 H 5 CH 2 N(CH 3 ) 3 ] + OH wodorotlenek benzylotrimetyloamoniowy [(CH 3 ) 4 N] + I [(CH 3 CH 2 ) 2 NH 2 ] + Cl jodek tetrametyloamoniowy chlorek dietyloamoniowy W przypadkach, gdy nazwa aminy nie kończy się na amina, czwartorzędowy charakter związku określa się dodając do nazwy tej zasady końcówkę iowy (z pominięciem końcowej litery a (jeśli ta samogłoska jest na końcu aminy) i podając na początku nazwę anionu. [C 6 H 5 NH 3 ] + Cl chlorek aniliniowy [C 6 H 5 NH 2 (CH 3 )] + Br bromek N-metyloaniliniowy 10
11 PRZEMYSŁOWA METODA OTRZYMYWANIA AMIN - alkilowanie amoniaku i amin metyloamina (amina 1 ) Nie można otrzymać danej aminy bez domieszek amin o wyższej rzędowości! 11
12 METODY LABORATORYJNE OTRZYMYWANIA AMIN 1 12
13 METODY LABORATORYJNE OTRZYMYWANIA AMIN 1 nitryl amina 1 13
14 METODY LABORATORYJNE OTRZYMYWANIA AMIN 1 azydek alkilowy amina 1 14
15 METODY LABORATORYJNE OTRZYMYWANIA AMIN 1 15
16 METODY LABORATORYJNE OTRZYMYWANIA AMIN 1 amina 1 16
17 METODY LABORATORYJNE OTRZYMYWANIA AMIN 1 amid 1 amina 1 17
18 METODY LABORATORYJNE OTRZYMYWANIA AMIN 1 R O LiAlH 4 C R NH 2 CH 2 NH 2 + H 2 O amid 1 amina 1 aldehyd lub keton imina amina 1 (1) NH 3 (2) H 2 /Ni, T, p 18
19 METODY LABORATORYJNE OTRZYMYWANIA AMIN 2 O LiAlH 4 C R CH 2 NH R' + H 2 O R NH R' amid 2 amina 2 (amina 1 ) aldehyd lub keton imina amina 2 19
20 METODY LABORATORYJNE OTRZYMYWANIA AMIN 3 amina 2 O R' LiAlH C R' 4 R CH 2 N R'' + H 2 O R N amid 3 amina 3 R'' 20
21 REAKCJE AMIN AROMATYCZNYCH REAKCJE AROMATYCZNEJ SUBSTYTUCJI ELEKTROFILOWEJ Z UDZIAŁEM ANILINY SULFONOWANIE H 2 O NITROWANIE Aniliny nie poddaje się bezpośredniemu nitrowaniu, ponieważ kwas azotowy ma właściwości utleniające, a pierścień aromatyczny wzbogacony w elektrony jest szczególnie podatny na utlenianie, które prowadzi do jego destrukcji. BROMOWANIE 21
22 REAKCJE POCHODNYCH AMIN AROMATYCZNYCH REAKCJE AROMATYCZNEJ SUBSTYTUCJI ELEKTROFILOWEJ ALKILOWANIE LUB ACYLOWANIE FRIEDLA-CRAFTSA NITROWANIE i BROMOWANIE ANILIDÓW 22
23 REAKCJE POCHODNYCH AMIN AROMATYCZNYCH UTLENIANIE AMIN ELIMINACJA HOFMANNA eliminacja 4 wodorotlenków amoniowych + 23
24 REAKCJA 1 AMIN AROMATYCZNYCH Z KWASEM AZOTAWYM aromatyczne sole diazoniowe nitryle chlorki arylowe fenole (deaminacja) Bromki arylowe jodki arylowe Fluorki arylowe 24
25 WYKORZYSTANIE AROMATYCZNYCH SOLI DIAZONIOWYCH 25
26 WYKORZYSTANIE AROMATYCZNYCH SOLI DIAZONIOWYCH o-toluidyna o-toluonitryl kwas o-toluilowy m-aminoacetofenon m-hydroksyacetofenon 26
27 WYKORZYSTANIE AROMATYCZNYCH SOLI DIAZONIOWYCH SPRZĘGANIE AROMATYCZNYCH SOLI DIAZOMIOWYCH otrzymywanie barwników azowych 27
28 OTRZYMYWANIE BARWNIKÓW AZOWYCH wskaźnik kwasowo-zasadowy w roztworze zasadowym 28 w roztworze kwaśnym
AMINY. tytoń szlachetny. nikotyna. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
amoniak amina 1 amina 2 amina 3
 AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
Slajd 1. Slajd 2. Aminy. trietyloamina. amoniak. chlorofil
 Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego. ĆWICZENIE 6 i 7. Aminy i amidy kwasowe
 ĆWICZENIE 6 i 7 Aminy i amidy kwasowe Do amin zaliczamy związki organiczne, których wzór można wyprowadzić ze wzoru amoniaku przez podstawienie w nim atomu lub atomów wodoru grupą lub grupami alkilowymi
ĆWICZENIE 6 i 7 Aminy i amidy kwasowe Do amin zaliczamy związki organiczne, których wzór można wyprowadzić ze wzoru amoniaku przez podstawienie w nim atomu lub atomów wodoru grupą lub grupami alkilowymi
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
WĘGLOWODORY AROMATYCZNE
 WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
Aminy pochodne amoniaku, w których
 A M I N Y Aminy pochodne amoniaku, w których jeden (aminy 1 o ), dwa (aminy 2 o ) lub trzy (aminy 3 o ) atomy wodoru zostały zastąpione resztami organicznymi (alifatycznymi bądź aromatycznymi). Przykłady
A M I N Y Aminy pochodne amoniaku, w których jeden (aminy 1 o ), dwa (aminy 2 o ) lub trzy (aminy 3 o ) atomy wodoru zostały zastąpione resztami organicznymi (alifatycznymi bądź aromatycznymi). Przykłady
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania
 Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Aminy - budowa. R alkil Alkiloamina Amina alifatyczna. Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA III - RZĘDOWA AMINA II - RZĘDOWA
 Aminy Aminy - budowa R alkil Alkiloamina Amina alifatyczna Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA II - RZĘDOWA AMINA III - RZĘDOWA Aminy - budowa ALKILOAMINY PIRAMIDA TRYGONALNA ARYLOAMINY
Aminy Aminy - budowa R alkil Alkiloamina Amina alifatyczna Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA II - RZĘDOWA AMINA III - RZĘDOWA Aminy - budowa ALKILOAMINY PIRAMIDA TRYGONALNA ARYLOAMINY
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
C H N O L B I O T E ORGANICZNA I A. Nomenklatura
 B T E L EMA G GAZA A omenklatura B T E L EMA G GAZA A Synteza AMY -rzędowe ' 2 2 2 ' 2 0 0 0 1 2 3 Typy amin -rzędowych w zależności od rzędowości atomu węgla związanego z grupą aminową METDY EDUKYJE
B T E L EMA G GAZA A omenklatura B T E L EMA G GAZA A Synteza AMY -rzędowe ' 2 2 2 ' 2 0 0 0 1 2 3 Typy amin -rzędowych w zależności od rzędowości atomu węgla związanego z grupą aminową METDY EDUKYJE
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Organiczne związki azotu
 Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Chemia organiczna. Związki zawierające azot. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Aminy. Aminy 1 0 RNH 2 NH. Aminy 3 0 R 3
 Aminy Aminy 1 0 R 2 Aminy 2 0 R 2 Aminy 3 0 R 3 C 3 C 3 C C 3 C 3 C 3 C 2 C 3 C 3 C 3 C 3 alkohol 3 o amina 1 o amina 3 o Czwartorzędowa sól amoniowa: R R R R X 1 Aminy alifatyczne ( wszystkie podstawniki
Aminy Aminy 1 0 R 2 Aminy 2 0 R 2 Aminy 3 0 R 3 C 3 C 3 C C 3 C 3 C 3 C 2 C 3 C 3 C 3 C 3 alkohol 3 o amina 1 o amina 3 o Czwartorzędowa sól amoniowa: R R R R X 1 Aminy alifatyczne ( wszystkie podstawniki
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka
 REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
fenol ninhydryna difenyloamina kwas octowy Określ ph amin: n-butyloamina dietyloamina difenyloamina anilina N,N-dimetyloanilina
 REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
Chemia organiczna. Związki zawierające azot. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
AMINY I ICH POCHODNE
 AMIY I I PDE rganiczne pochodne amoniaku. 4/5 powietrza azot. W naturze: aminokwasy, peptydy, białka, alkaloidy (kokaina, nikotyna, morfina, meskalina ), neurotransmitery, stymulanty, kwasy nukleinowe
AMIY I I PDE rganiczne pochodne amoniaku. 4/5 powietrza azot. W naturze: aminokwasy, peptydy, białka, alkaloidy (kokaina, nikotyna, morfina, meskalina ), neurotransmitery, stymulanty, kwasy nukleinowe
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 2
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych:
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
Ćwiczenie 6 Aminokwasy
 Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
POŁOŻENIA SYGNAŁÓW PROTONÓW POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA
 POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
POŁOŻENIA SYGNAŁÓW PROTONÓW SPEKTROSKOPIA NMR OH, NH alkeny kwasy aromatyczne aldehydy alkiny alkile przy heteroatomach alkile δ ppm 11 10 9 8 7 6 5 4 3 2 1 POŁOŻENIA SYGNAŁÓW ATOMÓW WĘGLA alkeny alkile
MIKROANALIZY WĘGLOWODORY. W1 Utlenianie węglowodorów nadmanganianem potasu w środowisku kwaśnym (w temp. pokojowej) RÓWNANIA REAKCJI: OBSERWACJE:
 MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14):
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Reakcje charakterystyczne amin i aminokwasów
 eakcje charakterystyczne amin i aminokwasów Maria Jamrozik Zastąpienie atomów wodoru w amoniaku grupami alkilowymi lub arylowymi prowadzi do powstania związków, zawierających jedno, dwa lub trzy wiązania
eakcje charakterystyczne amin i aminokwasów Maria Jamrozik Zastąpienie atomów wodoru w amoniaku grupami alkilowymi lub arylowymi prowadzi do powstania związków, zawierających jedno, dwa lub trzy wiązania
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII Instrukcja do ćwiczeń laboratoryjnych WŁAŚCIWOŚCI KWASOWOZASADOWE ZWIĄZKÓW ORGANICZNYCH; BADANIE ROZPUSZCZALNOŚCI
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA CHEMII ORGANICZNEJ, BIOORGANICZNEJ I BIOTECHNOLOGII Instrukcja do ćwiczeń laboratoryjnych WŁAŚCIWOŚCI KWASOWOZASADOWE ZWIĄZKÓW ORGANICZNYCH; BADANIE ROZPUSZCZALNOŚCI
Wykład 7. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 7 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Otrzymywanie węglowodorów aromatycznych 1. z katalitycznego reformingu (frakcje C 6 -C 10 ) 2. synteza alkilowych pochodnych
Wykład 7 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Otrzymywanie węglowodorów aromatycznych 1. z katalitycznego reformingu (frakcje C 6 -C 10 ) 2. synteza alkilowych pochodnych
Kwasy karboksylowe C O OH OH C CH 2 H OH CH 2 C CH 3 C OH C OH C OH. propionowy. mrówkowy. akrylowy. octowy. masłowy metakrylowy.
 Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Kwasy karboksylowe Największą kwasowość spośród związków organicznych wykazują kwasy karboksylowe. Związki te zawierają w cząsteczce grupę karboksylową H, połączoną albo z grupą alkilową R (RH) albo grupą
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Węglowodory Aromatyczne
 Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
NAZEWNICTWO WYBRANYCH KLAS ZWIĄZKÓW ORGANICZNYCH 1 ALKANY
 NAZEWNITW WYBRANYH KLAS ZWIĄZKÓW RGANIZNYH ALKANY Pierwsze cztery nierozgałęzione alkany mają nazwy zwyczajowe: metan, etan, propan, butan. Nazwy wyższych członów szeregu homologicznego składają się z
NAZEWNITW WYBRANYH KLAS ZWIĄZKÓW RGANIZNYH ALKANY Pierwsze cztery nierozgałęzione alkany mają nazwy zwyczajowe: metan, etan, propan, butan. Nazwy wyższych członów szeregu homologicznego składają się z
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Slajd 1. Reakcje alkinów
 Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Węglowodory nomenklatura Pochodne chlorowcowe węglowodorów
 Węglowodory nomenklatura 1. Alkany: a) otrzymywanie metodą Wurtza, ze związków Gringarda, z halogenków alkilów, przez elektrolizę soli kwasów karboksylowych. b) Własności: halogenowanie, spalanie, piroliza,
Węglowodory nomenklatura 1. Alkany: a) otrzymywanie metodą Wurtza, ze związków Gringarda, z halogenków alkilów, przez elektrolizę soli kwasów karboksylowych. b) Własności: halogenowanie, spalanie, piroliza,
RJC. 1 Kwasy i Zasady. Kwasy i zasady Brønsteda Stabilizacja Rezonansowa Kwasy i Zasady Lewisa HA + B: A - + BH + Slides 1 to 35
 1 Kwasy i Zasady Kwasy i zasady Brønsteda Stabilizacja Rezonansowa Kwasy i Zasady Lewisa HA + B: A - + BH + Slides 1 to 35 2 Kwas : Definicja Brønsteda Kwasem jest taki związek zek chemiczny, który moŝe
1 Kwasy i Zasady Kwasy i zasady Brønsteda Stabilizacja Rezonansowa Kwasy i Zasady Lewisa HA + B: A - + BH + Slides 1 to 35 2 Kwas : Definicja Brønsteda Kwasem jest taki związek zek chemiczny, który moŝe
Proseminarium identyfikacji związków organicznych
 Proseminarium identyfikacji związków organicznych pracował: Wojciech Augustyniak Dr Wojciech Augustyniak Pracownia Peptydów Gmach Chemii p. 230 (tel. wew. 509) Gmach Radiochemii p. 118, 122, 165, 169 (wew.
Proseminarium identyfikacji związków organicznych pracował: Wojciech Augustyniak Dr Wojciech Augustyniak Pracownia Peptydów Gmach Chemii p. 230 (tel. wew. 509) Gmach Radiochemii p. 118, 122, 165, 169 (wew.
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Program wykładu Chemia Organiczna I
 Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Krystyna Dzierzbicka
 Krystyna Dzierzbicka Fenole związki organiczne, w których grupa hydroksylowa związana jest bezpośrednio z atomem węgla układu aromatycznego (z węglem o hybrydyzacji sp 2 ). Przykłady i -naftol -naftol
Krystyna Dzierzbicka Fenole związki organiczne, w których grupa hydroksylowa związana jest bezpośrednio z atomem węgla układu aromatycznego (z węglem o hybrydyzacji sp 2 ). Przykłady i -naftol -naftol
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
BENZEN - własności chemiczne
 B I T N L MIA G GANIZNA I A BNZN - własności chemiczne 1) edukcja katalityczna wodorem PD WYSKIM IŚNINIM (do cykloheksanu). Jako katalizatory najczęściej stosowane są: Pt, Pd, Ni / Ni 2 p = 100 atm. T
B I T N L MIA G GANIZNA I A BNZN - własności chemiczne 1) edukcja katalityczna wodorem PD WYSKIM IŚNINIM (do cykloheksanu). Jako katalizatory najczęściej stosowane są: Pt, Pd, Ni / Ni 2 p = 100 atm. T
(57)1. Sposób wytwarzania nitrowych pochodnych
 RZECZPOSPOLITA POLSKA Urząd Patentowy Rzeczypospolitej Polskiej (12) OPIS PATENTOWY (19) PL (11) 185862 (21) Numer zgłoszenia: 319445 (22) Data zgłoszenia: 11.04.1997 (13) B1 (51) IntCl7 C07D 209/08 C07D
RZECZPOSPOLITA POLSKA Urząd Patentowy Rzeczypospolitej Polskiej (12) OPIS PATENTOWY (19) PL (11) 185862 (21) Numer zgłoszenia: 319445 (22) Data zgłoszenia: 11.04.1997 (13) B1 (51) IntCl7 C07D 209/08 C07D
Laboratorium. Podstawowe procesy jednostkowe w technologii chemicznej
 Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
PROGRAM ĆWICZEŃ Program ćwiczeń z chemii organicznej obejmuje wykonanie jedenastu zadań praktycznych i zdanie czterech kolokwiów.
 Wrocław 2019-10-01 REGULAMIN PRZEDMIOTU CHEMIA ORGANICZNA DLA STUDENTÓW II ROKU WYDZIAŁU FARMACEUTYCZNEGO UMW WE WROCŁAWIU (150 godzin ćwiczeń, 60 godzin wykładów) w roku akademickim 2019/ 2020 PROGRAM
Wrocław 2019-10-01 REGULAMIN PRZEDMIOTU CHEMIA ORGANICZNA DLA STUDENTÓW II ROKU WYDZIAŁU FARMACEUTYCZNEGO UMW WE WROCŁAWIU (150 godzin ćwiczeń, 60 godzin wykładów) w roku akademickim 2019/ 2020 PROGRAM
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
CHEMIA BUDOWLANA ĆWICZENIE NR 3
 CHEMIA BUDOWLANA ĆWICZENIE NR 3 HYDROLIZA SOLI I WYZNACZANIE ph ROZTWORÓW WSTĘP TEORETYCZNY Kwasy są to substancje zdolne do oddawania protonów. Zasady są zdolne do wiązania protonów. Definicję kwasów
CHEMIA BUDOWLANA ĆWICZENIE NR 3 HYDROLIZA SOLI I WYZNACZANIE ph ROZTWORÓW WSTĘP TEORETYCZNY Kwasy są to substancje zdolne do oddawania protonów. Zasady są zdolne do wiązania protonów. Definicję kwasów
R 2 III-rzędowe R 1 N R 3
 ZWIĄZKI ZAWIERAJĄE AZT W GRUPA FUKYJY I. Wprowadzenie teoretyczne Ważniejsze związki organiczne zawierające azot w grupie funkcyjnej to aminy, aminokwasy, związki nitrowe oraz hydrazyna i jej pochodne.
ZWIĄZKI ZAWIERAJĄE AZT W GRUPA FUKYJY I. Wprowadzenie teoretyczne Ważniejsze związki organiczne zawierające azot w grupie funkcyjnej to aminy, aminokwasy, związki nitrowe oraz hydrazyna i jej pochodne.
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
WARSZTATY olimpijskie. Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna Kinetyka
 WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
1. Substytucja nukleofilowa we fluorowcopochodnych
 B T E L EMA G GAZA A Synteza 1. Substytucja nukleofilowa we fluorowcopochodnych 1a) Etery dialkilowe można otrzymywać w reakcji pierwszorzędowych fluorowcopochodnych z ALKLAAM. Jest to reakcja Williamsona.
B T E L EMA G GAZA A Synteza 1. Substytucja nukleofilowa we fluorowcopochodnych 1a) Etery dialkilowe można otrzymywać w reakcji pierwszorzędowych fluorowcopochodnych z ALKLAAM. Jest to reakcja Williamsona.
Kierunek i poziom studiów: Biotechnologia, pierwszy. Nazwa wariantu modułu (opcjonalnie): nie dotyczy
 Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Podział związków organicznych
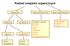 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Jak analizować widmo IR?
 Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Substytucja elektrofilowa
 Substytucja elektrofilowa Katarzyna strowska Reakcja substytucji elektrofilowej w układach aromatycznych zachodzi z wymianą atomu wodoru na reagent elektrofilowy. Związki aromatyczne są płaskimi związkami
Substytucja elektrofilowa Katarzyna strowska Reakcja substytucji elektrofilowej w układach aromatycznych zachodzi z wymianą atomu wodoru na reagent elektrofilowy. Związki aromatyczne są płaskimi związkami
węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny)
 DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
Z a d a n i a t e o r e t y c z n e
 O L I M P I A D A 45 1954 1998 Z a d a n i a t e o r e t y c z n e C H EM I C Z N A zmiana ph roztworów ZADANIE 1 Jak zmieni się stężenie jonów wodorotlenowych przy przejściu od roztworu A do roztworu
O L I M P I A D A 45 1954 1998 Z a d a n i a t e o r e t y c z n e C H EM I C Z N A zmiana ph roztworów ZADANIE 1 Jak zmieni się stężenie jonów wodorotlenowych przy przejściu od roztworu A do roztworu
Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna (0310-CH-S1-026) Nazwa wariantu modułu (opcjonalnie):
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, poziom kształcenia pierwszy Kierunek i poziom studiów: Sylabus modułu: Chemia organiczna () Nazwa wariantu modułu (opcjonalnie):
Barwniki azowe Dwuazotypia Aminy i kwas azotawy. A + Sole dwuazoniowe, Kwas azotawy Związki dwuazoaminowe Dwuazowanie.
 Barwniki azowe (1958 P. Griss: odkrycie reakcji diazowania i pierwszy barwnik: żółcień anilinowa) to barwniki syntetyczne zawierające jedną lub kilka grup azowych (jako chromofor). W zależności od ilości
Barwniki azowe (1958 P. Griss: odkrycie reakcji diazowania i pierwszy barwnik: żółcień anilinowa) to barwniki syntetyczne zawierające jedną lub kilka grup azowych (jako chromofor). W zależności od ilości
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
3. Wprowadzenie do nazewnictwa związków organicznych
 3. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową (C
3. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową (C
S Y L A B U S P R Z E D M I O T U
 "Z A T W I E R D Z A M" Dziekan Wydziału Nowych Technologii i Chemii Dr hab. inż. Stanisław CUDZIŁO, prof. WAT Warszawa, dnia... S Y L A B U S P R Z E D M I O T U NAZWA PRZEDMIOTU:..CHEMIA ORGANICZNA SUBJECT
"Z A T W I E R D Z A M" Dziekan Wydziału Nowych Technologii i Chemii Dr hab. inż. Stanisław CUDZIŁO, prof. WAT Warszawa, dnia... S Y L A B U S P R Z E D M I O T U NAZWA PRZEDMIOTU:..CHEMIA ORGANICZNA SUBJECT
Identyfikacja płomieniowa tworzyw sztucznych Iloczyny rozpuszczalności trudno rozpuszczalnych związków w wodzie w temperaturze pokojowej
 Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
Jeśli ktoś jest w posiadaniu tablic chemicznych, to bardzo prosilibyśmy, aby nam je nadesłał (na adres któregoś z administratorów, najlepiej w formie pliku *.doc; *.pdf; *.jpg) - na pewno je zamieścimy.
