Definicja szybkości reakcji
|
|
|
- Patryk Wrona
- 7 lat temu
- Przeglądów:
Transkrypt
1 Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia tej zmiany v n x d dt x Chem. Fiz. TCH II/7
2 Szybkośi reakji Jednostki szybkośi reakji: [mol dm -3 s - ], [mol dm -3 min - ], [mmol dm -3 s - ], itp. [Pa/s] (dla reakji w fazie gazowej) [A], [ma], [µa] (dla reakji elektrodowyh) Szybkość hwilowa reakji oznaza szybkość w dowolnie wybranym momenie jej trwania, po upływie zasu t od momentu rozpozęia reakji. Przypadek szzególny, gdy t, vv, nazywamy szybkośią pozątkową reakji. Chem. Fiz. TCH II/7
3 Równanie kinetyzne vk i r i i reakji Szybkość reakji dana jest wzorem: k m A n B o C... m, n, o, r i są ząstkowymi rzędami reakji, odpowiednio względem reagenta i (A, B, C). Całkowity rząd reakji o szybkośi zdefiniowanej powyższym równaniem wynosi: i ri m + n + o... Chem. Fiz. TCH II/7 3
4 Rząd reakji, stała szybkośi Rzędem reakji względem reagenta nazywamy wykładnik potęgi, do której stężenie tego reagenta jest podniesione w równaniu kinetyznym, opisująym zależność hwilowej szybkośi reakji od stężenia tego reagenta. Ogólny rząd reakji jest równy sumie wykładników przy stężeniah w równaniu kinetyznym reakji. NIE jest to suma współzynników stehiometryznyh reakji. Współzynnik proporjonalnośi w równaniu kinetyznym k, zwany stałą szybkośi reakji,nie zależy od stężenia. Zależy ona wyłąznie od reakji (jest to wielkość harakterystyzna dla reakji) i od temperatury. Chem. Fiz. TCH II/7 4
5 Równanie kinetyzne reakji () Przykłady: Równanie kinetyzne: Całkowity rząd reakji: Może się też zdarzyćże rząd reakji (ząstkowy lub ogólny) jest ujemny: v k[] [Y] / + ++?½ Jak również rząd reakji zależny od stężenia v k[a][p] produktu: Zdarza się też, że w ogóle nie można określić rzędu reakji! Chem. Fiz. TCH II/7 5
6 Sałkowane równanie kinetyzne Bezpośredni pomiar szybkośi reakji jest (poza elektrohemią, gdzie jest to pomiar prądu) trudny, jeśli nie niemożliwy. Dlatego też mierzymy razej zmiany stężenia wybranego reagenta (substratu lub produktu) w zasie. W tym elu potrzebna jest nam zależność: i f (t) Otrzymuje się ją przez sałkowanie równania kinetyznego danej reakji przy znanyh stężeniah pozątkowyh reagenta lub reagentów. Chem. Fiz. TCH II/7 6
7 Sałkowane równanie kinetyzne rząd Reakje rzędu zerowego (szybkość reakji nie zależy od stężenia substratu ) Równanie kinetyzne (różnizkowe): Krok : rozdzielenie zmiennyh: Krok : ałkowanie nieoznazone: Krok 3: korzystamy z warunków graniznyh: d k dt d kdt d k dt kt + onst t onst Chem. Fiz. TCH II/7 7
8 Sałkowane równanie kinetyzne rząd () Krok 4: podstawienie stałej: kt + kt Szybkość pozątkowa dla reakji rzędu : Przykłady reakji rzędu zerowego: gorąy drut Pt NH3 (g) N (g) + 3H (g) v k ałkowity rząd NO(g) + CO(g) NO(g) + CO(g) ałkowity rząd, rząd względem CO. Oznaza to, że stosowne równanie kinetyzne ma postać: vk[no ] Chem. Fiz. TCH II/7 8
9 Sałkowane równanie kinetyzne rząd Reakje rzędu pierwszego (szybkość reakji jest liniową funkją stężenia substratu ) Równanie kinetyzne (różnizkowe): Krok : rozdzielenie zmiennyh: Krok : ałkowanie nieoznazone: Krok 3: korzystamy z warunków graniznyh: d A d k dt kdt d k dt ln kt + onst t ln onst ln kt + ln Krok 4: podstawienie stałej: Chem. Fiz. TCH II/7 9
10 ln ln Sałkowane równanie kinetyzne rząd () Ostateznie dla reakji rzędu pierwszego kt ln Szybkość pozątkowa dla reakji rzędu : kt Przykłady reakji rzędu pierwszego: CH 6(g) CH3 (g) yklopropan propen -kt e Chem. Fiz. TCH II/7 rozpad promieniotwórzy, np. 4 C 4 N + β v k
11 Sałkowane równanie kinetyzne rząd Reakje rzędu drugiego (szybkość reakji jest kwadratową funkją stężenia substratu ) Równanie kinetyzne (różnizkowe): Krok : rozdzielenie zmiennyh: Krok : ałkowanie nieoznazone: d d Chem. Fiz. TCH II/7 dt kdt k d k dt kt + onst t Krok 3: korzystamy z warunków graniznyh: Krok 4: podstawienie stałej: onst kt
12 Sałkowane równanie kinetyzne rząd () k t k t k t + Szybkość pozątkowa dla reakji rzędu : v k Przykłady reakji rzędu drugiego: NO(g) NO(g) + O(g) I(g) +I(g) I (g) H (g) +I (g) HI(g) + H - (aq) +OH (aq) H O() Chem. Fiz. TCH II/7
13 Wykresy sałkowanyh równań kinetyznyh Chem. Fiz. TCH II/7 3
14 Czas połowiznej przemiany Czas, po którym stężenie reagenta spada do połowy swojej wartośi pozątkowej, nazywamy okresem połowiznej przemiany τ /. Odpowiednie wyrażenie wiążąe τ / z innymi parametrami kinetyznymi można wyprowadzić podstawiają konsekwenje w/w definiji (½ A zamiast A ) do sałkowanego równania kinetyznego i rozwiązują je ze względu na t, który na moy tejże definiji staje się τ /. Chem. Fiz. TCH II/7 4
15 Czas połowiznej przemiany () Rząd Rząd Rząd kt ln kt Po uwzględnieniu: τ / k x t τ / Czasy połowiznej przemiany wynoszą: τ / ln k Chem. Fiz. TCH II/7 5 τ / k Zwróćmy uwagę, że dla rzędu zas połowiznej przemiany nie zależy od stężenia pozątkowego! kt
16 Czas połowiznej przemiany (3) Przykład: NO NO + O rząd ; k.54 l/(mol s) w 573K. mo/l Znajdź zas, po którym: a) / ; b) /6 ; ) /9. a) okres połowiznej przemiany: τ /,54[l mol - - s ],[mol l - 9,6 ] [s] Chem. Fiz. TCH II/7 6
17 Czas połowiznej przemiany (4) Przykład.d.: NO NO + O rząd ; k.54 l/(mol s) w 573K. mo/l Znajdź zas, po którym: a) / ; b) /6 ; ) /9. b) wyprowadzamy: τ k 6 5 / 6 6 kt; 6 5 5τ k / 38, 9 [s] Chem. Fiz. TCH II/7 7
18 Czas połowiznej przemiany (5) Przykład.d.: NO NO + O rząd ; k.54 l/(mol s) w 573K. mo/l Znajdź zas, po którym: a) / ; b) /6 ; ) /9. ) również wyprowadzamy (analogiznie jak w pkt b) τ/ 9 8τ / 9 k k 9 74, [s] Chem. Fiz. TCH II/7 8
Definicja szybkości reakcji. Szybkości reakcji. Równanie kinetyczne reakcji ...
 Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany v zmiana stężenia zas potrzebny do zajśia dx
Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany v zmiana stężenia zas potrzebny do zajśia dx
Definicja szybkości reakcji
 Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
WYZNACZANIE STAŁEJ SZYBKOŚCI I RZĘDU REAKCJI (Utlenianie jonów Fe 2+ jonami ClO 3
 Ćwizenie nr 4b WYZNACZANIE STAŁEJ SZYBKOŚCI I RZĘDU REAKCJI (Utlenianie jonów Fe + jonami ClO 3 w środowisku kwaśnym) I. Cel ćwizenia Celem ćwizenia jest wyznazenie rzędu reakji, stałej szybkośi reakji
Ćwizenie nr 4b WYZNACZANIE STAŁEJ SZYBKOŚCI I RZĘDU REAKCJI (Utlenianie jonów Fe + jonami ClO 3 w środowisku kwaśnym) I. Cel ćwizenia Celem ćwizenia jest wyznazenie rzędu reakji, stałej szybkośi reakji
Relaksacja. Chem. Fiz. TCH II/19 1
 Relasaja Relasaja oznaza powrót uładu do stanu równowagi po zaburzeniu równowagi pierwotnej jaimś bodźem (wielośią zewnętrzną zmieniająą swoją wartość soowo, np. stężenie jednego z reagentów, iśnienie
Relasaja Relasaja oznaza powrót uładu do stanu równowagi po zaburzeniu równowagi pierwotnej jaimś bodźem (wielośią zewnętrzną zmieniająą swoją wartość soowo, np. stężenie jednego z reagentów, iśnienie
Stan równowagi chemicznej
 Stan równowagi hemiznej Równowaga hemizna to taki stan układu złożonego z roduktów i substratów dowolnej reakji odwraalnej, w którym szybkość owstawania roduktów jest równa szybkośi ih rozadu Odwraalność
Stan równowagi hemiznej Równowaga hemizna to taki stan układu złożonego z roduktów i substratów dowolnej reakji odwraalnej, w którym szybkość owstawania roduktów jest równa szybkośi ih rozadu Odwraalność
KI + Pb(NO 3 ) 2 PbI 2 + KNO 3. fermentacja alkoholowa
 Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
fermentacja alkoholowa erozja skał lata dni KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 min Karkonosze Pielgrzymy (1204 m n.p.m.)
 Kinetyka chemiczna lata erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa dni min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Kinetyka chemiczna lata erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa dni min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Kinetyka. Kinetyka. Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? energia swobodna, G. postęp reakcji.
 Kinetyka energia swobodna, G termodynamika stan 1 kinetyka termodynamika stan 2 postęp reakcji 1 Kinetyka Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 2 Jak szybko
Kinetyka energia swobodna, G termodynamika stan 1 kinetyka termodynamika stan 2 postęp reakcji 1 Kinetyka Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 2 Jak szybko
Kinetyka. energia swobodna, G. postęp reakcji. stan 1 stan 2. kinetyka
 Kinetyka postęp reakcji energia swobodna, G termodynamika kinetyka termodynamika stan 1 stan 2 Kinetyka Stawia dwa pytania: 1) Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 1) Jak szybko
Kinetyka postęp reakcji energia swobodna, G termodynamika kinetyka termodynamika stan 1 stan 2 Kinetyka Stawia dwa pytania: 1) Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 1) Jak szybko
KI + Pb(NO 3 ) 2 PbI 2 + KNO 3. fermentacja alkoholowa
 Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
1 Kinetyka reakcji chemicznych
 Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Terminy. Omówienie kolokwium I. Poprawa kolokwium I. Poprawa kolokwium II g. 15, s g. 15, s g. 15, s.
 Tomasz Lubera Omówienie kolokwium I 14.05 g. 15, s. 402 Poprawa kolokwium I 21.05 g. 15, s. 402 Poprawa kolokwium II 28.05 g. 15, s. 402 Terminy Ćwiczenia rachunkowe z chemii fizycznej - Kolokwium II 2
Tomasz Lubera Omówienie kolokwium I 14.05 g. 15, s. 402 Poprawa kolokwium I 21.05 g. 15, s. 402 Poprawa kolokwium II 28.05 g. 15, s. 402 Terminy Ćwiczenia rachunkowe z chemii fizycznej - Kolokwium II 2
Pojęcia podstawowe 1
 Tomasz Lubera Pojęcia podsawowe aa + bb + dd + pp + rr + ss + Kineyka chemiczna dział chemii fizycznej zajmujący się przebiegiem reakcji chemicznych w czasie, ich mechanizmami oraz wpływem różnych czynników
Tomasz Lubera Pojęcia podsawowe aa + bb + dd + pp + rr + ss + Kineyka chemiczna dział chemii fizycznej zajmujący się przebiegiem reakcji chemicznych w czasie, ich mechanizmami oraz wpływem różnych czynników
Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ
 Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
erozja skał lata KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 min Karkonosze Pielgrzymy (1204 m n.p.m.)
 Kinetyka chemiczna erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa lata min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Kinetyka chemiczna erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa lata min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Wzrost fazy krystalicznej
 Wzrost fazy krystalicznej Wydzielenie nowej fazy może różnić się of fazy pierwotnej : składem chemicznym strukturą krystaliczną orientacją krystalograficzną... faza pierwotna nowa faza Analogia elektryczna
Wzrost fazy krystalicznej Wydzielenie nowej fazy może różnić się of fazy pierwotnej : składem chemicznym strukturą krystaliczną orientacją krystalograficzną... faza pierwotna nowa faza Analogia elektryczna
Ćwiczenie 6. Symulacja komputerowa wybranych procesów farmakokinetycznych z uwzględnieniem farmakokinetyki bezmodelowej
 Ćwiczenie 6. Symulacja komputerowa wybranych procesów farmakokinetycznych z uwzględnieniem farmakokinetyki bezmodelowej Celem ćwiczenia jest wyznaczenie podstawowych parametrów farmakokinetycznych paracetamolu
Ćwiczenie 6. Symulacja komputerowa wybranych procesów farmakokinetycznych z uwzględnieniem farmakokinetyki bezmodelowej Celem ćwiczenia jest wyznaczenie podstawowych parametrów farmakokinetycznych paracetamolu
Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. a RT.
 Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
Odwracalność przemiany chemicznej
 Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
ELEMENTY SZCZEGÓLNEJ TEORII WZGLĘDNOŚCI. I. Zasada względności: Wszystkie prawa przyrody są takie same we wszystkich
 ELEMENTY SZCZEGÓLNEJ TEORII WZGLĘDNOŚCI Postulaty Einsteina (95 r) I Zasada względnośi: Wszystkie prawa przyrody są takie same we wszystkih inerjalnyh układah odniesienia lub : Równania wyrażająe prawa
ELEMENTY SZCZEGÓLNEJ TEORII WZGLĘDNOŚCI Postulaty Einsteina (95 r) I Zasada względnośi: Wszystkie prawa przyrody są takie same we wszystkih inerjalnyh układah odniesienia lub : Równania wyrażająe prawa
Chemia fizyczna 2 - wykład
 Chemia fizyczna 2 - wykład Dr hab. inż. Aneta Pobudkowska-Mirecka Konsultacje: środa 12.15 14.00 (p.149) Chemia Fizyczna 2 - wykład Chemia kwantowa (prof. dr hab. Andrzej Sporzyński) Procesy (dr hab. inż.
Chemia fizyczna 2 - wykład Dr hab. inż. Aneta Pobudkowska-Mirecka Konsultacje: środa 12.15 14.00 (p.149) Chemia Fizyczna 2 - wykład Chemia kwantowa (prof. dr hab. Andrzej Sporzyński) Procesy (dr hab. inż.
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 Roztwory rzeczywiste (2) Tym razem dla (CH 3 ) 2 CO () i CHCl
Roztwory rzeczywiste (1)
 Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
Roztwory rzeczywiste (1) Również w temp. 298,15K, ale dla CCl 4 () i CH 3 OH (). 2 15 1 5-5 -1-15 Τ S H,2,4,6,8 1 G -2 Chem. Fiz. TCH II/12 1 rzyczyny dodatnich i ujemnych odchyleń od prawa Raoulta konsekwencja
M10. Własności funkcji liniowej
 M10. Własności funkcji liniowej dr Artur Gola e-mail: a.gola@ajd.czest.pl pokój 3010 Definicja Funkcję określoną wzorem y = ax + b, dla x R, gdzie a i b są stałymi nazywamy funkcją liniową. Wykresem funkcji
M10. Własności funkcji liniowej dr Artur Gola e-mail: a.gola@ajd.czest.pl pokój 3010 Definicja Funkcję określoną wzorem y = ax + b, dla x R, gdzie a i b są stałymi nazywamy funkcją liniową. Wykresem funkcji
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA
 SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
REAKCJE CHEMICZNE. syntezy. analizy. wymiany AB A + B. rodzaje reakcji chemicznych reakcje: H 2 SO NaOH A + B AB 2 H 2 + O 2 = 2H 2 O
 REAKCJE CHEMICZNE rodzaje reakji hemiznyh reakje: 1. syntezy. analizy 3. wymiany 4. substytuji 5. addyji 6. eliminaji 7. polimeryzaji reakja hemizna to każdy proes w wyniku którego następuje zrywanie i/lub
REAKCJE CHEMICZNE rodzaje reakji hemiznyh reakje: 1. syntezy. analizy 3. wymiany 4. substytuji 5. addyji 6. eliminaji 7. polimeryzaji reakja hemizna to każdy proes w wyniku którego następuje zrywanie i/lub
WYKŁADY. Matematyka. dla studentów I roku Farmacji WUM. dr Justyna Kurkowiak
 WYKŁADY Matematyka dla studentów I roku Farmacji WUM dr Justyna Kurkowiak 209-0-0 WARUNKI ZALICZENIA Matematyka (I semestr) W semestrze można zdobyć 00 punktów. PUNKTACJA Kolokwium I Kolokwium II Kartkówki
WYKŁADY Matematyka dla studentów I roku Farmacji WUM dr Justyna Kurkowiak 209-0-0 WARUNKI ZALICZENIA Matematyka (I semestr) W semestrze można zdobyć 00 punktów. PUNKTACJA Kolokwium I Kolokwium II Kartkówki
Równania różniczkowe liniowe rzędu pierwszego
 Katedra Matematyki i Ekonomii Matematycznej SGH 21 kwietnia 2016 Wstęp Definicja Równanie różniczkowe + p (x) y = q (x) (1) nazywamy równaniem różniczkowym liniowym pierwszego rzędu. Jeśli q (x) 0, to
Katedra Matematyki i Ekonomii Matematycznej SGH 21 kwietnia 2016 Wstęp Definicja Równanie różniczkowe + p (x) y = q (x) (1) nazywamy równaniem różniczkowym liniowym pierwszego rzędu. Jeśli q (x) 0, to
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
Inżynieria Biomedyczna
 1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
Równania różniczkowe wyższych rzędów
 Równania różniczkowe wyższych rzędów Marcin Orchel Spis treści 1 Wstęp 1 1.1 Istnienie rozwiązań............................... 1 1. Rozwiązanie ogólne............................... 1.3 Obniżanie rzędu
Równania różniczkowe wyższych rzędów Marcin Orchel Spis treści 1 Wstęp 1 1.1 Istnienie rozwiązań............................... 1 1. Rozwiązanie ogólne............................... 1.3 Obniżanie rzędu
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych
 Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
Enzymologia I. Kinetyka - program Gepasi. Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu
 Enzymologia I Kinetyka - program Gepasi Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu I zasada + II zasada termodynamiki zmiana entalpii i entropii może zostać wyrażona ilościowo
Enzymologia I Kinetyka - program Gepasi Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu I zasada + II zasada termodynamiki zmiana entalpii i entropii może zostać wyrażona ilościowo
FUNKCJA LINIOWA. A) B) C) D) Wskaż, dla którego funkcja liniowa określona wzorem jest stała. A) B) C) D)
 FUNKCJA LINIOWA 1. Funkcja jest rosnąca, gdy 2. Wskaż, dla którego funkcja liniowa jest rosnąca Wskaż, dla którego funkcja liniowa określona wzorem jest stała. 3. Funkcja liniowa A) jest malejąca i jej
FUNKCJA LINIOWA 1. Funkcja jest rosnąca, gdy 2. Wskaż, dla którego funkcja liniowa jest rosnąca Wskaż, dla którego funkcja liniowa określona wzorem jest stała. 3. Funkcja liniowa A) jest malejąca i jej
Obliczanie wydajności reakcji
 bliczanie wydajności reakcji Wydajność reakcji chemicznej (W) jest to stosunek masy produktu (m p ) otrzymanej w wyniku przeprowadzenia reakcji chemicznej do masy tego produktu (m t ) wynikającej z równania
bliczanie wydajności reakcji Wydajność reakcji chemicznej (W) jest to stosunek masy produktu (m p ) otrzymanej w wyniku przeprowadzenia reakcji chemicznej do masy tego produktu (m t ) wynikającej z równania
Badania zostały przeprowadzone dla wybranych pochodnych metioniny. Badane związki
 7 4.2.2. Metionina i jej pohodne Badania zostały przeprowadzone dla wybranyh pohodnyh metioniny. Badane związki COO - CH 3 SCH 2 CH 2 CH NH 3 L-metionina [Met] COO - CH 3 SCH 2 CH 2 CH NH C O CH 3 N-aetylo-L-metionina
7 4.2.2. Metionina i jej pohodne Badania zostały przeprowadzone dla wybranyh pohodnyh metioniny. Badane związki COO - CH 3 SCH 2 CH 2 CH NH 3 L-metionina [Met] COO - CH 3 SCH 2 CH 2 CH NH C O CH 3 N-aetylo-L-metionina
Wykład 4. Anna Ptaszek. 27 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 4. Anna Ptaszek 1 / 31
 Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 27 października 2015 1 / 31 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 27 października 2015 1 / 31 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
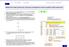 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
1 Równania różniczkowe zwyczajne o rozdzielonych zmiennych
 Równania różniczkowe zwyczajne o rozdzielonych zmiennych Definicja. Równaniem różniczkowym o rozdzielonych zmiennych nazywamy równanie postaci p(y) = q() (.) rozwiązanie równania sprowadza się do postaci
Równania różniczkowe zwyczajne o rozdzielonych zmiennych Definicja. Równaniem różniczkowym o rozdzielonych zmiennych nazywamy równanie postaci p(y) = q() (.) rozwiązanie równania sprowadza się do postaci
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
Badanie kinetyki katalitycznego rozkładu H 2 O 2
 Badanie kinetyki katalitycznego rozkładu H 2 O 2 (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zapoznanie się z prawami kinetyki chemicznej, sposobem wyznaczenia stałej szybkości i rzędu reakcji
Badanie kinetyki katalitycznego rozkładu H 2 O 2 (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zapoznanie się z prawami kinetyki chemicznej, sposobem wyznaczenia stałej szybkości i rzędu reakcji
RÓWNANIA RÓŻNICZKOWE WYKŁAD 2
 RÓWNANIA RÓŻNICZKOWE WYKŁAD 2 Równania różniczkowe o zmiennych rozdzielonych Równania sprowadzalne do równań o zmiennych rozdzielonych Niech f będzie funkcją ciągłą na przedziale (a, b), spełniającą na
RÓWNANIA RÓŻNICZKOWE WYKŁAD 2 Równania różniczkowe o zmiennych rozdzielonych Równania sprowadzalne do równań o zmiennych rozdzielonych Niech f będzie funkcją ciągłą na przedziale (a, b), spełniającą na
Logarytmy. Funkcje logarytmiczna i wykładnicza. Równania i nierówności wykładnicze i logarytmiczne.
 Logarytmy. Funkcje logarytmiczna i wykładnicza. Równania i nierówności wykładnicze i logarytmiczne. Definicja. Niech a i b będą dodatnimi liczbami rzeczywistymi i niech a. Logarytmem liczby b przy podstawie
Logarytmy. Funkcje logarytmiczna i wykładnicza. Równania i nierówności wykładnicze i logarytmiczne. Definicja. Niech a i b będą dodatnimi liczbami rzeczywistymi i niech a. Logarytmem liczby b przy podstawie
Dysocjacja kwasów i zasad. ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to:
 Stała równowagi dysocjacji: Dysocjacja kwasów i zasad HX H 2 O H 3 O X - K a [ H 3O [ X [ HX [ H O 2 ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to: K a [ H 3 O [ X [ HX Dla słabych kwasów
Stała równowagi dysocjacji: Dysocjacja kwasów i zasad HX H 2 O H 3 O X - K a [ H 3O [ X [ HX [ H O 2 ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to: K a [ H 3 O [ X [ HX Dla słabych kwasów
Funkcje i ich własności. Energetyka, sem.1 (2017/2018) Matematyka #3: Funkcje 1 / 43
 Funkcje i ich własności Energetyka, sem.1 (2017/2018) Matematyka #3: Funkcje 1 / 43 Zbiory liczbowe Zbiory Zbiór Iloczyn (część wspólna zbiorów) A B = {x : x A x B} Suma Różnica Zawieranie się A B = {x
Funkcje i ich własności Energetyka, sem.1 (2017/2018) Matematyka #3: Funkcje 1 / 43 Zbiory liczbowe Zbiory Zbiór Iloczyn (część wspólna zbiorów) A B = {x : x A x B} Suma Różnica Zawieranie się A B = {x
Inżynieria Biomedyczna
 1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
Kontakt,informacja i konsultacje
 Kontakt,informacja i konsultacje Chemia A ; pokój 307 elefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl tablica ogłoszeń Katedry Chemii Fizycznej http://www.pg.gda.pl/chem/dydaktyka/ lub http://www.pg.gda.pl/chem/katedry/fizyczna
Kontakt,informacja i konsultacje Chemia A ; pokój 307 elefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl tablica ogłoszeń Katedry Chemii Fizycznej http://www.pg.gda.pl/chem/dydaktyka/ lub http://www.pg.gda.pl/chem/katedry/fizyczna
Zakres materiału obowiązujący do egzaminu poprawkowego z matematyki klasa 1 d LO
 Zakres materiału obowiązujący do egzaminu poprawkowego z matematyki klasa 1 d LO Dział programowy. Zakres realizacji 1. Liczby, działania i procenty Liczby wymierne i liczby niewymierne-działania, kolejność
Zakres materiału obowiązujący do egzaminu poprawkowego z matematyki klasa 1 d LO Dział programowy. Zakres realizacji 1. Liczby, działania i procenty Liczby wymierne i liczby niewymierne-działania, kolejność
Wykład 4. Anna Ptaszek. 9 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 4. Anna Ptaszek 1 / 29
 Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 9 października 2015 1 / 29 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 9 października 2015 1 / 29 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych
 Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
a) 1 mol b) 0,5 mola c) 1,7 mola d) potrzebna jest znajomość objętości zbiornika, aby można było przeprowadzić obliczenia
 1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
Wykład 3 Równania rózniczkowe cd
 7 grudnia 2010 Definicja Równanie różniczkowe dy dx + p (x) y = q (x) (1) nazywamy równaniem różniczkowym liniowym pierwszego rzędu. Jeśli q (x) 0, to równanie (1) czyli równanie dy dx + p (x) y = 0 nazywamy
7 grudnia 2010 Definicja Równanie różniczkowe dy dx + p (x) y = q (x) (1) nazywamy równaniem różniczkowym liniowym pierwszego rzędu. Jeśli q (x) 0, to równanie (1) czyli równanie dy dx + p (x) y = 0 nazywamy
Matematyka licea ogólnokształcące, technika
 Matematyka licea ogólnokształcące, technika Opracowano m.in. na podstawie podręcznika MATEMATYKA w otaczającym nas świecie zakres podstawowy i rozszerzony Funkcja liniowa Funkcję f: R R określoną wzorem
Matematyka licea ogólnokształcące, technika Opracowano m.in. na podstawie podręcznika MATEMATYKA w otaczającym nas świecie zakres podstawowy i rozszerzony Funkcja liniowa Funkcję f: R R określoną wzorem
ĆWICZENIE 1. Farmakokinetyka podania dożylnego i pozanaczyniowego leku w modelu jednokompartmentowym
 ĆWICZENIE 1 Farmakokinetyka podania dożylnego i pozanaczyniowego leku w modelu jednokompartmentowym Celem ćwiczenia jest wyznaczenie parametrów farmakokinetycznych leków podanych w jednorazowych dawkach:
ĆWICZENIE 1 Farmakokinetyka podania dożylnego i pozanaczyniowego leku w modelu jednokompartmentowym Celem ćwiczenia jest wyznaczenie parametrów farmakokinetycznych leków podanych w jednorazowych dawkach:
c. Oblicz wydajność reakcji rozkładu 200 g nitrogliceryny, jeśli otrzymano w niej 6,55 g tlenu.
 Zadanie 1. Nitrogliceryna (C 3H 5N 3O 9) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: 4 C 3 H 5 N 3 O 9 (c) 6 N 2 (g) + 12 CO 2 (g) + 10 H 2 O (g) + 1 O 2 (g) H rozkładu =
Zadanie 1. Nitrogliceryna (C 3H 5N 3O 9) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: 4 C 3 H 5 N 3 O 9 (c) 6 N 2 (g) + 12 CO 2 (g) + 10 H 2 O (g) + 1 O 2 (g) H rozkładu =
IX. MECHANIKA (FIZYKA) KWANTOWA
 IX. MECHANIKA (FIZYKA) KWANTOWA IX.1. OPERACJE OBSERWACJI. a) klasycznie nie ważna kolejność, w jakiej wykonujemy pomiary. AB = BA A pomiar wielkości A B pomiar wielkości B b) kwantowo wartość obserwacji
IX. MECHANIKA (FIZYKA) KWANTOWA IX.1. OPERACJE OBSERWACJI. a) klasycznie nie ważna kolejność, w jakiej wykonujemy pomiary. AB = BA A pomiar wielkości A B pomiar wielkości B b) kwantowo wartość obserwacji
27. RÓWNANIA RÓŻNICZKOWE CZĄSTKOWE
 27. RÓWNANIA RÓŻNICZKOWE CZĄSTKOWE 27.1. Wiadomości wstępne Równaniem różniczkowym cząstkowym nazywamy związek w którym występuje funkcja niewiadoma u dwóch lub większej liczby zmiennych niezależnych i
27. RÓWNANIA RÓŻNICZKOWE CZĄSTKOWE 27.1. Wiadomości wstępne Równaniem różniczkowym cząstkowym nazywamy związek w którym występuje funkcja niewiadoma u dwóch lub większej liczby zmiennych niezależnych i
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym
 1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
RÓWNANIA RÓŻNICZKOWE ZWYCZAJNE
 RÓWNANIA RÓŻNICZKOWE ZWYCZAJNE A. RÓWNANIA RZĘDU PIERWSZEGO Uwagi ogólne Równanie różniczkowe zwyczajne rzędu pierwszego zawiera. Poza tym może zawierać oraz zmienną. Czyli ma postać ogólną Na przykład
RÓWNANIA RÓŻNICZKOWE ZWYCZAJNE A. RÓWNANIA RZĘDU PIERWSZEGO Uwagi ogólne Równanie różniczkowe zwyczajne rzędu pierwszego zawiera. Poza tym może zawierać oraz zmienną. Czyli ma postać ogólną Na przykład
FUNKCJA KWADRATOWA. 1. Definicje i przydatne wzory. lub trójmianem kwadratowym nazywamy funkcję postaci: f(x) = ax 2 + bx + c
 FUNKCJA KWADRATOWA 1. Definicje i przydatne wzory DEFINICJA 1. Funkcja kwadratowa lub trójmianem kwadratowym nazywamy funkcję postaci: f(x) = ax + bx + c taką, że a, b, c R oraz a 0. Powyższe wyrażenie
FUNKCJA KWADRATOWA 1. Definicje i przydatne wzory DEFINICJA 1. Funkcja kwadratowa lub trójmianem kwadratowym nazywamy funkcję postaci: f(x) = ax + bx + c taką, że a, b, c R oraz a 0. Powyższe wyrażenie
Dwie proste mogą być względem siebie prostopadłe, równoległe albo przecinać się pod kątem innym niż prosty..
 4. Proste równoległe i prostopadłe Dwie proste mogą być względem siebie prostopadłe, równoległe albo przecinać się pod kątem innym niż prosty.. Jeśli przecinają się w dowolnym miejscu, i to pod kątem prostym,
4. Proste równoległe i prostopadłe Dwie proste mogą być względem siebie prostopadłe, równoległe albo przecinać się pod kątem innym niż prosty.. Jeśli przecinają się w dowolnym miejscu, i to pod kątem prostym,
3. FUNKCJA LINIOWA. gdzie ; ół,.
 1 WYKŁAD 3 3. FUNKCJA LINIOWA FUNKCJĄ LINIOWĄ nazywamy funkcję typu : dla, gdzie ; ół,. Załóżmy na początek, że wyraz wolny. Wtedy mamy do czynienia z funkcją typu :.. Wykresem tej funkcji jest prosta
1 WYKŁAD 3 3. FUNKCJA LINIOWA FUNKCJĄ LINIOWĄ nazywamy funkcję typu : dla, gdzie ; ół,. Załóżmy na początek, że wyraz wolny. Wtedy mamy do czynienia z funkcją typu :.. Wykresem tej funkcji jest prosta
1. PIERWSZA I DRUGA ZASADA TERMODYNAMIKI TERMOCHEMIA
 . PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
. PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
Równania i nierówności wykładnicze i logarytmiczne
 Równania i nierówności wykładnicze i logarytmiczne Paweł Foralewski Teoria Ponieważ funkcje wykładnicza i logarytmiczna zostały wprowadzone wcześniej, tutaj przypomnimy tylko definicję logarytmu i jego
Równania i nierówności wykładnicze i logarytmiczne Paweł Foralewski Teoria Ponieważ funkcje wykładnicza i logarytmiczna zostały wprowadzone wcześniej, tutaj przypomnimy tylko definicję logarytmu i jego
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu
 Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
Kinetyka i równowaga reakcji chemicznej
 Kinetyka i równowaga reakcji chemicznej W przebiegu reakcji chemicznych interesujące są dwa aspekty zachodzących przemian: 1. rodzaj substratów i otrzymanych z nich produktów, 2. szybkość, z jaką substraty
Kinetyka i równowaga reakcji chemicznej W przebiegu reakcji chemicznych interesujące są dwa aspekty zachodzących przemian: 1. rodzaj substratów i otrzymanych z nich produktów, 2. szybkość, z jaką substraty
Funkcje IV. Wymagania egzaminacyjne:
 Wymagania egzaminacyjne: a) określa funkcję za pomocą wzoru, tabeli, wykresu, opisu słownego, b) odczytuje z wykresu funkcji: dziedzinę i zbiór wartości, miejsca zerowe, maksymalne przedziały, w których
Wymagania egzaminacyjne: a) określa funkcję za pomocą wzoru, tabeli, wykresu, opisu słownego, b) odczytuje z wykresu funkcji: dziedzinę i zbiór wartości, miejsca zerowe, maksymalne przedziały, w których
Układ Graficzny przygotowano na podstawie materiałów egzaminacyjnych CKE
 Układ Graficzny przygotowano na podstawie materiałów egzaminacyjnych CKE WPISUJE ZDAJĄCY KOD KOD PESEL PESEL Miejsce na naklejkę z kodem EGZAMIN MATURALNY Z CHEMII (KINETYKA I RÓWNOWAGA CHEMICZNA - A)
Układ Graficzny przygotowano na podstawie materiałów egzaminacyjnych CKE WPISUJE ZDAJĄCY KOD KOD PESEL PESEL Miejsce na naklejkę z kodem EGZAMIN MATURALNY Z CHEMII (KINETYKA I RÓWNOWAGA CHEMICZNA - A)
Równania różniczkowe wyższych rzędów
 Równania różniczkowe wyższych rzędów Marcin Orchel Spis treści 1 Wstęp 1 1.1 Istnienie rozwiązań............................... 1 1.2 Rozwiązanie ogólne............................... 2 1.3 Obniżanie rzędu
Równania różniczkowe wyższych rzędów Marcin Orchel Spis treści 1 Wstęp 1 1.1 Istnienie rozwiązań............................... 1 1.2 Rozwiązanie ogólne............................... 2 1.3 Obniżanie rzędu
1 Hydroliza soli. Hydroliza soli 1
 Hydroliza soli 1 1 Hydroliza soli Niektóre sole, rozpuszczone w wodzie, reagują z cząsteczkami rozpuszczalnika. Reakcja ta nosi miano hydrolizy. Reakcję hydrolizy soli o wzorze BA, można schematycznie
Hydroliza soli 1 1 Hydroliza soli Niektóre sole, rozpuszczone w wodzie, reagują z cząsteczkami rozpuszczalnika. Reakcja ta nosi miano hydrolizy. Reakcję hydrolizy soli o wzorze BA, można schematycznie
2. DZIAŁANIA NA WIELOMIANACH
 WIELOMIANY 1. Stopieo wielomianu. Działania na wielomianach 2. Równość wielomianów. 3. Pierwiastek wielomianu. Rozkład wielomianu na czynniki 4. Równania wielomianowe. 1.STOPIEŃ WIELOMIANU Wielomian to
WIELOMIANY 1. Stopieo wielomianu. Działania na wielomianach 2. Równość wielomianów. 3. Pierwiastek wielomianu. Rozkład wielomianu na czynniki 4. Równania wielomianowe. 1.STOPIEŃ WIELOMIANU Wielomian to
3. Wykład Układy równań liniowych.
 31 Układy równań liniowych 3 Wykład 3 Definicja 31 Niech F będzie ciałem Układem m równań liniowych o niewiadomych x 1,, x n, m, n N, o współczynnikach z ciała F nazywamy układ równań postaci: x 1 + +
31 Układy równań liniowych 3 Wykład 3 Definicja 31 Niech F będzie ciałem Układem m równań liniowych o niewiadomych x 1,, x n, m, n N, o współczynnikach z ciała F nazywamy układ równań postaci: x 1 + +
FUNKCJE ELEMENTARNE I ICH WŁASNOŚCI
 FUNKCJE ELEMENTARNE I ICH WŁASNOŚCI DEFINICJA (funkcji elementarnych) Podstawowymi funkcjami elementarnymi nazywamy funkcje: stałe potęgowe wykładnicze logarytmiczne trygonometryczne Funkcje, które można
FUNKCJE ELEMENTARNE I ICH WŁASNOŚCI DEFINICJA (funkcji elementarnych) Podstawowymi funkcjami elementarnymi nazywamy funkcje: stałe potęgowe wykładnicze logarytmiczne trygonometryczne Funkcje, które można
Chemia fizyczna (2013/2014) kinetyka chemiczna
 Chemia fizyczna (01/014) kinetyka chemiczna Zadanie 1. Dla reakcji rozkładu N O 5 4NO +O w roztworze CCl 4, w warunkach T,V=const w temperaturze 45 o C otrzymano następującą zależność stężenia N O 5 (A)
Chemia fizyczna (01/014) kinetyka chemiczna Zadanie 1. Dla reakcji rozkładu N O 5 4NO +O w roztworze CCl 4, w warunkach T,V=const w temperaturze 45 o C otrzymano następującą zależność stężenia N O 5 (A)
UKŁADY RÓWNAŃ LINIOWYCH
 Projekt dofinansowała Fundacja mbanku UKŁADY RÓWNAŃ LINIOWYCH CZĘŚĆ I Układ równań to przynajmniej dwa równania spięte z lewej strony klamrą, np.: x + 0 Każde z równań musi zawierać przynajmniej jedną
Projekt dofinansowała Fundacja mbanku UKŁADY RÓWNAŃ LINIOWYCH CZĘŚĆ I Układ równań to przynajmniej dwa równania spięte z lewej strony klamrą, np.: x + 0 Każde z równań musi zawierać przynajmniej jedną
A B Skąd wiadomo, że reakcja zachodzi? Co jest miarą szybkości reakcji?
 Kinetya chemiczna 3.1.1. Pojęcie szybości reacji chemicznej 3.1.. Ilościowe miary szybości 3.1.3. Reacje pierwszego rzędu 3.1.4. Reacje zerowego rzędu 3.1.5. Przyłady SZYBKOŚĆ REAKCJI HOMOGENICZNEJ A B
Kinetya chemiczna 3.1.1. Pojęcie szybości reacji chemicznej 3.1.. Ilościowe miary szybości 3.1.3. Reacje pierwszego rzędu 3.1.4. Reacje zerowego rzędu 3.1.5. Przyłady SZYBKOŚĆ REAKCJI HOMOGENICZNEJ A B
Układy równań liniowych
 Układy równań liniowych Niech K będzie ciałem. Niech n, m N. Równanie liniowe nad ciałem K z niewiadomymi (lub zmiennymi) x 1, x 2,..., x n K definiujemy jako formę zdaniową zmiennej (x 1,..., x n ) K
Układy równań liniowych Niech K będzie ciałem. Niech n, m N. Równanie liniowe nad ciałem K z niewiadomymi (lub zmiennymi) x 1, x 2,..., x n K definiujemy jako formę zdaniową zmiennej (x 1,..., x n ) K
Jak osiągnąć 100% wydajności reakcji?
 Jak osiągnąć 100% wydajnośi reakji? Stan równowagi ois termodynamizny G 0 A A G + RT ln(q)o B B C (a) (b) wówzas G - RT ln() stała równowagi a) G
Jak osiągnąć 100% wydajnośi reakji? Stan równowagi ois termodynamizny G 0 A A G + RT ln(q)o B B C (a) (b) wówzas G - RT ln() stała równowagi a) G
2. LICZBY RZECZYWISTE Własności liczb całkowitych Liczby rzeczywiste Procenty... 24
 SPIS TREŚCI WYRAŻENIA ALGEBRAICZNE RÓWNANIA I NIERÓWNOŚCI ALGEBRAICZNE 7 Wyrażenia algebraiczne 0 Równania i nierówności algebraiczne LICZBY RZECZYWISTE 4 Własności liczb całkowitych 8 Liczby rzeczywiste
SPIS TREŚCI WYRAŻENIA ALGEBRAICZNE RÓWNANIA I NIERÓWNOŚCI ALGEBRAICZNE 7 Wyrażenia algebraiczne 0 Równania i nierówności algebraiczne LICZBY RZECZYWISTE 4 Własności liczb całkowitych 8 Liczby rzeczywiste
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak)
 Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych
 CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
Analiza szeregów czasowych: 7. Liniowe modele stochastyczne
 Analiza szeregów czasowych: 7. Liniowe modele stochastyczne P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ semestr letni 2005/06 Liniowe modele stochastyczne Niech {y n } N n=1 będzie pewnym ciagiem danych
Analiza szeregów czasowych: 7. Liniowe modele stochastyczne P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ semestr letni 2005/06 Liniowe modele stochastyczne Niech {y n } N n=1 będzie pewnym ciagiem danych
Wykład 10 Równowaga chemiczna
 Wykład 10 Równowaga chemiczna REAKCJA CHEMICZNA JEST W RÓWNOWADZE, GDY NIE STWIERDZAMY TENDENCJI DO ZMIAN ILOŚCI (STĘŻEŃ) SUBSTRATÓW ANI PRODUKTÓW RÓWNOWAGA CHEMICZNA JEST RÓWNOWAGĄ DYNAMICZNĄ W rzeczywistości
Wykład 10 Równowaga chemiczna REAKCJA CHEMICZNA JEST W RÓWNOWADZE, GDY NIE STWIERDZAMY TENDENCJI DO ZMIAN ILOŚCI (STĘŻEŃ) SUBSTRATÓW ANI PRODUKTÓW RÓWNOWAGA CHEMICZNA JEST RÓWNOWAGĄ DYNAMICZNĄ W rzeczywistości
c t x v KINETYKA CHEMICZNA
 KINETYKA CHEMICZNA Prawa termodynamiki chemicznej pozwalają nam przewidzieć tylko możliwy kierunek przemian w układzie reagentów oraz ilość poszczególnych składników znajdujących się w układzie w momencie
KINETYKA CHEMICZNA Prawa termodynamiki chemicznej pozwalają nam przewidzieć tylko możliwy kierunek przemian w układzie reagentów oraz ilość poszczególnych składników znajdujących się w układzie w momencie
WYMAGANIE EDUKACYJNE Z MATEMATYKI W KLASIE II GIMNAZJUM. dopuszczającą dostateczną dobrą bardzo dobrą celującą
 1. Statystyka odczytać informacje z tabeli odczytać informacje z diagramu 2. Mnożenie i dzielenie potęg o tych samych podstawach 3. Mnożenie i dzielenie potęg o tych samych wykładnikach 4. Potęga o wykładniku
1. Statystyka odczytać informacje z tabeli odczytać informacje z diagramu 2. Mnożenie i dzielenie potęg o tych samych podstawach 3. Mnożenie i dzielenie potęg o tych samych wykładnikach 4. Potęga o wykładniku
PRACOWNIA CHEMII. Kinetyka reakcji chemicznych (Fiz1)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Kinetyka reakcji chemicznych
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Kinetyka reakcji chemicznych
STECHIOMETRIA SPALANIA
 STECHIOMETRIA SPALANIA Mole i kilomole Masa atomowa pierwiastka to średnia ważona mas wszystkich jego naturalnych izotopów w stosunku do 1/12 masy izotopu węgla: 1/12 126 C ~ 1,66 10-27 kg Liczba Avogadra
STECHIOMETRIA SPALANIA Mole i kilomole Masa atomowa pierwiastka to średnia ważona mas wszystkich jego naturalnych izotopów w stosunku do 1/12 masy izotopu węgla: 1/12 126 C ~ 1,66 10-27 kg Liczba Avogadra
Egzamin ustny z matematyki semestr II Zakres wymaganych wiadomości i umiejętności
 Egzamin ustny z matematyki semestr II Zakres wymaganych wiadomości i umiejętności I. Pojęcie funkcji definicja różne sposoby opisu funkcji określenie dziedziny, zbioru wartości, miejsc zerowych. Należy
Egzamin ustny z matematyki semestr II Zakres wymaganych wiadomości i umiejętności I. Pojęcie funkcji definicja różne sposoby opisu funkcji określenie dziedziny, zbioru wartości, miejsc zerowych. Należy
Wykład 30 Szczególne przekształcenie Lorentza
 Wykład Szzególne przekształenie Lorentza Szzególnym przekształeniem Lorentza (właśiwym, zahowująym kierunek zasu) nazywa się przekształenie między dwoma inerjalnymi układami odniesienia K i K w przypadku
Wykład Szzególne przekształenie Lorentza Szzególnym przekształeniem Lorentza (właśiwym, zahowująym kierunek zasu) nazywa się przekształenie między dwoma inerjalnymi układami odniesienia K i K w przypadku
Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 4. Równania różniczkowe zwyczajne podstawy teoretyczne
 Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 4. Równania różniczkowe zwyczajne podstawy teoretyczne P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ semestr letni 2005/06 Wstęp
Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 4. Równania różniczkowe zwyczajne podstawy teoretyczne P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ semestr letni 2005/06 Wstęp
Opracował: dr inż. Tadeusz Lemek
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria i Gospodarka Wodna w ramach projektu Era inżyniera pewna lokata na przyszłość Opracował:
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria i Gospodarka Wodna w ramach projektu Era inżyniera pewna lokata na przyszłość Opracował:
KINETYKA INWERSJI SACHAROZY
 Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Termochemia efekty energetyczne reakcji
 Termochemia efekty energetyczne reakcji 1. Podstawowe pojęcia termodynamiki chemicznej a) Układ i otoczenie Układ, to wyodrębniony obszar materii, oddzielony od otoczenia wyraźnymi granicami (np. reagenty
Termochemia efekty energetyczne reakcji 1. Podstawowe pojęcia termodynamiki chemicznej a) Układ i otoczenie Układ, to wyodrębniony obszar materii, oddzielony od otoczenia wyraźnymi granicami (np. reagenty
Finanse i Rachunkowość studia niestacjonarne/stacjonarne Model Przepływów Międzygałęziowych
 dr inż. Ryszard Rębowski 1 OPIS ZJAWISKA Finanse i Rachunkowość studia niestacjonarne/stacjonarne Model Przepływów Międzygałęziowych 8 listopada 2015 1 Opis zjawiska Będziemy obserwowali proces tworzenia
dr inż. Ryszard Rębowski 1 OPIS ZJAWISKA Finanse i Rachunkowość studia niestacjonarne/stacjonarne Model Przepływów Międzygałęziowych 8 listopada 2015 1 Opis zjawiska Będziemy obserwowali proces tworzenia
Temat wykładu: Całka nieoznaczona. Kody kolorów: żółty nowe pojęcie pomarańczowy uwaga kursywa komentarz * materiał nadobowiązkowy
 Temat wykładu: Całka nieoznazona Kody kolorów: żółty nowe pojęie pomarańzowy uwaga kursywa komentarz * materiał nadobowiązkowy A n n a R a j f u r a, M a t e m a t y k a Zagadnienia. Terminologia i oznazenia.
Temat wykładu: Całka nieoznazona Kody kolorów: żółty nowe pojęie pomarańzowy uwaga kursywa komentarz * materiał nadobowiązkowy A n n a R a j f u r a, M a t e m a t y k a Zagadnienia. Terminologia i oznazenia.
ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji
 ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji w tej temperaturze wynosi K p = 0,11. Reaktor został
ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji w tej temperaturze wynosi K p = 0,11. Reaktor został
a. Dobierz współczynniki w powyższym schemacie tak, aby stał się równaniem reakcji chemicznej.
 Zadanie 1. Nitrogliceryna (C 3 H 5 N 3 O 9 ) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: C 3 H 5 N 3 O 9 (c) N 2 (g) + CO 2 (g) + H 2 O (g) + O 2 (g) H rozkładu = - 385 kj/mol
Zadanie 1. Nitrogliceryna (C 3 H 5 N 3 O 9 ) jest środkiem wybuchowym. Jej rozkład można opisać następującym schematem: C 3 H 5 N 3 O 9 (c) N 2 (g) + CO 2 (g) + H 2 O (g) + O 2 (g) H rozkładu = - 385 kj/mol
Plan wynikowy z rozkładem materiału
 Plan wynikowy z rozkładem materiału Plan wynikowy oraz rozkład materiału nauczania są indywidualnymi dokumentami nauczycielskimi związanymi z realizowanym programem nauczania. Uwzględniają specyfikę danej
Plan wynikowy z rozkładem materiału Plan wynikowy oraz rozkład materiału nauczania są indywidualnymi dokumentami nauczycielskimi związanymi z realizowanym programem nauczania. Uwzględniają specyfikę danej
Funkcja liniowa - podsumowanie
 Funkcja liniowa - podsumowanie 1. Funkcja - wprowadzenie Założenie wyjściowe: Rozpatrywana będzie funkcja opisana w dwuwymiarowym układzie współrzędnych X. Oś X nazywana jest osią odciętych (oś zmiennych
Funkcja liniowa - podsumowanie 1. Funkcja - wprowadzenie Założenie wyjściowe: Rozpatrywana będzie funkcja opisana w dwuwymiarowym układzie współrzędnych X. Oś X nazywana jest osią odciętych (oś zmiennych
