Kinetyka i równowaga reakcji chemicznej
|
|
|
- Eleonora Świderska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Kinetyka i równowaga reakcji chemicznej
2 W przebiegu reakcji chemicznych interesujące są dwa aspekty zachodzących przemian: 1. rodzaj substratów i otrzymanych z nich produktów, 2. szybkość, z jaką substraty przetwarzane są w produkty. Badanie szybkości reakcji chemicznych oraz warunków, od których ta szybkość zależy zajmuje się kinetyka chemiczna.
3 Szybkość reakcji (v) określa stosunek nieskończenie małych zmian stężenia substratów lub produktów do nieskończenie małego przedziału czasu, w którym te zmiany stężeń zachodzą. Można to przedstawić za pomocą następujących wyrażeń: v dcs lub dt v dc dt p gdzie : v szybkość reakcji c s - stężenie substratu (mol/dm 3 ) c p - stężenie produktu (mol/dm 3 ) t - czas Znak minus w wyrażeniu pierwszym mówi o malejącym stężeniu substratów w czasie reakcji, znak plus w drugim wyrażeniu mówi o rosnącym stężeniu produktów w czasie reakcji. Oba wzory można stosować zamiennie, ponieważ stężenia substratów i produktów związane są ze sobą stechiometrycznie.
4 Ilościowo szybkość reakcji określa się jako zmianę molowego stężenia substratu lub produktu w jednostce czasu. Szybkość reakcji opisuje równanie: gdzie: v - szybkość reakcji chemicznej, ΔC - zmiana stężenia reagentów, Δt - jednostka czasu.
5 Wpływ stężenia substancji na szybkość reakcji Zależność szybkości reakcji od stężenia ujmuje prawo działania mas Guldberga i Waagego. Prawo to mówi, że: Szybkość reakcji jest wprost proporcjonalna do iloczynu stężeń substratów. Jeżeli mamy równanie reakcji chemicznej aa + bb + cc ---> dd, to szybkość reakcji opisuje równanie; v = k [A] a [B] b [C] c gdzie: k - stała szybkości reakcji, (a, b, c) - wykładnik potęgi, do której należy podnieść stężenie, odpowiednio [A], [B], [C]. W przypadku reakcji gazowych często w równaniach kinetycznych zamiast stężeń molowych stosuje się ciśnienia cząstkowe. Wykładniki a, b i c są zazwyczaj liczbami całkowitymi, ale zastosowane w równaniu mogą być niekiedy ułamkami, równać się 0 lub być liczbami ujemnymi.
6 Rzędowość reakcji chemicznej Przebieg reakcji chemicznych jest bardziej złożony niż mogłoby to wynikać z równania stechiometrycznego. Większość reakcji to reakcje kilkuetapowe. Czasami w reakcji występuje kilka substratów a, szybkość reakcji zależy tylko od stężenia jednego lub dwóch z nich. Tylko na podstawie doświadczeń można ustalić zależność między szybkością reakcji a stężeniem substratów. Dają one równanie kinetyczne danej reakcji. Suma wykładników potęg występujących w tym równaniu przy stężeniach substratów, które wpływają na szybkość reakcji określa rzędowość reakcji. Można mówić o: - reakcjach zerowego rzędu v = k - reakcjach pierwszego rzędu v = k c A - reakcjach drugiego rzędu v = k c A c B lub v = k c 2 A - reakcjach trzeciego rzędu v = k c A c B c C lub v = k c 3 A Reakcje wyższych rzędów nie są znane. Wynika to z tego, że w każdym etapie reakcji uczestniczy jedna, dwie lub co najwyżej trzy cząsteczki.
7 Rzędu reakcji nie można mylić ze współczynnikami stechiometrycznymi reakcji i tzw. cząsteczkowością reakcji. Cząsteczkowość określa liczbę cząsteczek uczestniczących w elementarnej przemianie chemicznej, natomiast reakcja jako sumaryczny zapis stechiometryczny może przebiegać poprzez szereg przemian elementarnych. Przykład: 2Br - + 2H + + H 2 O 2 --> Br 2 + H 2 O Gdyby reakcja przebiegała w jednym etapie, to musiałoby nastąpić spotkanie pięciu cząsteczek: dwóch jonów Br -, dwóch jonów H + i cząsteczki nadtlenku wodoru. W rzeczywistości mechanizm tej reakcji obejmuje dwa etapy: H + + Br - + H 2 O 2 --> HOBr + H 2 O /wolno/ HOBr + H + + Br - --> Br 2 + H 2 O /szybko/ Szybkość reakcji określa pierwsza wolna reakcja. v = k [H + ] [Br + ] [H 2 O 2 ] Jest to zatem reakcja trzeciorzędowa.
8 Różnorodność zjawisk kinetycznych, wpływ szeregu czynników na szybkość reakcji wyjaśniają najlepiej dwie teorie kinetyczne: 1. Teoria zderzeń (dotyczy tylko reakcji w fazie gazowej) 2. Teoria kompleksu aktywnego (dotyczy reakcji w fazie gazowej i ciekłej)
9 Teoria zderzeń aktywnych 1. Warunkiem zajścia reakcji są zderzenia odpowiednich drobin. Nie każde zderzenie jest efektywne chemicznie. Liczba zdarzeń efektywnych stanowi zwykle niewielki ułamek wszystkich zderzeń. Im większa liczba zderzeń tym więcej wśród nich zderzeń efektywnych, a więc i większa szybkość reakcji. 2. Reakcja chemiczna stanowi ciąg aktów elementarnych. Akt elementarny to pojedyncze zdarzenie. Wiele takich samych zderzeń stanowi etap reakcji. Sekwencja aktów elementarnych nazywana jest mechanizmem reakcji. Reakcje jednoetapowe nazywamy prostymi, a wieloetapowe złożonymi. O szybkości reakcji wieloetapowej decyduje etap najwolniejszy tzw. etap limitujący.
10 3. Pierwszym warunkiem efektywności zderzenia jest odpowiednia wartość sumy energii kinetycznych zderzających się drobin. Energia ta nie może być niższa od tzw. energii aktywacji E A. Jeżeli jest mniejsza to zderzenie kończy się sprężystym odbiciem. Energia aktywacji E A jest to minimalna wartość sumy energii kinetycznych zderzających się drobin, która umożliwia (ale nie gwarantuje) skuteczność chemicznego zderzenia. Im wyższa wartość E A tym wolniej przebiega reakcja, ponieważ tym mniej jest drobin mających odpowiednio dużą energię. W reakcji wieloetapowej etap o najwyższej E A jest etapem limitującym. 4. Drugim warunkiem efektywności zderzenia jest odpowiednia orientacja przestrzenna zderzających się drobin.
11 Teoria kompleksu aktywnego Teoria kompleksu aktywnego lepiej wyjaśnia istotę energii aktywacji. Przyjmuje ona postulaty teorii zderzeń i uzupełnia je nowymi. 1. Zderzenie drobin może doprowadzić do utworzenia nietrwałego kompleksu aktywnego zbudowanego z jąder i elektronów zderzających się drobin. Każde zderzenie chemicznie efektywne przebiega przez stadium pośrednie trwające około sekundy, np. w reakcji: A + BC AB + C, tworzy się przejściowo kompleks ABC: A + BC A B C AB + C Klasycznym przykładem jest synteza jodowodoru: H 2 + I 2 2HI H - H H --- H H H + I - I I I I I Nie jest konieczne całkowite rozerwanie wiązań w cząsteczkach substratów. To wyjaśnia, dlaczego w podanej reakcji energia aktywacji jest mniejsza od sumy energii wiązań w drobinach substratów. W kompleksie istnieją stare wiązania, choć osłabione i nowe, ale jeszcze nie w pełni trwałe.
12
13 2. Szybkość reakcji zależy od: - stężenia kompleksu aktywnego - szybkości, z jaką ulega on rozpadowi na produkty W oparciu o obie teorie kinetyczne łatwiej zrozumieć zależność szybkości reakcji od różnych czynników. Są to przede wszystkim: stężenia reagentów temperatura katalizatory ciśnienie (dla reakcji w fazie gazowej) rodzaj rozpuszczalnika stopień rozdrobnienia, mieszanie
14 Szybkość reakcji a stężenie substratów Wpływ stężenia musi być ustalony doświadczalnie. Zgodnie z teorią zderzeń im więcej drobin tym więcej zderzeń, a więc najczęściej wzrost stężenia powoduje zwiększenie szybkości reakcji. Szybkość reakcji a temperatura Szybkość reakcji prawie zawsze rośnie wraz ze wzrostem temperatury. Zależność tę określa w przybliżeniu reguła van t Hoffa, która mówi, że szybkość reakcji wzrasta krotnie wraz ze wzrostem temperatury o 10 o C. v v 2 1 t 2 t 1 10 k 10 v 2, v 1 szybkość reakcji w temp. t 1 i t 2 α - współczynnik temperaturowy szybkości reakcji, równy 2 4 k t stała szybkości reakcji w temp. t t k t
15 Szybkość reakcji Praktycznie pomiary szybkości reakcji wykazały, że szybkość reakcji nie jest stała, lecz maleje w miarę zużywania się substratów.
16 Chcąc obliczyć szybkość reakcji w określonej chwili należałoby uwzględnić bardzo mały odstęp czasu między pomiarami. Jeżeli przyrost stężenia produktów reakcji oznaczymy przez dca a odstęp czasu przez dt, to szybkość reakcji v wyrazi się równaniem. v = dca/dt W przypadku reakcji pierwszego rzędu szybkość reakcji jest proporcjonalna do stężenia jednej substancji reagującej. Szybkość reakcji w tym przypadku określa równanie. -dca/dt = k * ca Po przekształceniu otrzymujemy k = 1/t * ln(ca o /ca) = 2,303/t * log(ca o )/ca) Wielkością, która charakteryzuje szybkość reakcji, jest okres połowicznej przemiany. Jest to czas potrzebny do tego, aby połowa reagującej substancji uległa przemianie. Dla reakcji pierwszego rzędu okres połowicznej przemiany wyraża się równaniem. T1/2 = 2,303/k * log2 = 0,693/k Analogicznie wyprowadzone równania dla reakcji drugiego rzędu, gdzie v = kc2, po scałkowaniu od c0 do c, mają postać k = 1/t * (1/c - 1/c o ) T1/2 = 1/k(2/c o - 1/c o ) = 1/(kc o )
17 Wpływ katalizatora na szybkość reakcji Katalizator to substancja, której obecność w mieszaninie reakcyjnej zwiększa szybkość reakcji (kataliza). Istotne jest to, że katalizator nie przesuwa położenia stanu równowagi reakcji (a więc nie wpływa na wydajność), ale przyspiesza jego osiągnięcie.
18 Mechanizm działania katalizatora w katalizie homogennej można wyjaśnić za pomocą kompleksu aktywnego, np. gdy reakcja: A + B A B AB ze względu na wysoką energię aktywacji przebiega powoli, odpowiednio dobrany katalizator (K) spowoduje przereagowanie substratów w etapach: Etap 1: A + K A K AK Etap 2: AK + B AK B AB + K Etapy te będą wymagały niższej energii aktywacji, więc przebiegną szybciej. W katalizie heterogenicznej katalizator jest najczęściej stały, (tzw. kontakt). Istotną rolę odgrywa tu tzw. adsorpcja aktywowana reagujących cząsteczek. Na powierzchni katalizatora w tzw. centrach aktywnych adsorbują się cząsteczki substratów i tworzą związki przejściowe, co jest związane z obniżeniem energii aktywacji i zwiększeniem aktywności substratów. Aby zwiększyć ilość centrów aktywnych dąży się do rozwinięcia powierzchni katalizatora. W tym celu tworzy się jego porowate struktury. Istnieją również substancje, których obecność w mieszaninie reakcyjnej może obniżać szybkość reakcji chemicznych przez zwiększenie energii aktywacji. Niektóre substancje dezaktywują katalizatory. Są to tzw. trucizny katalityczne. Należą do nich m.in.: H 2 S, NH 3, HCN, tlenek węgla, związki ołowiu.
19 RÓWNOWAGA CHEMICZNA Wszystkie reakcje chemiczne przebiegające w układach zamkniętych są odwracalne tzn., że z substratów mogą powstać produkty i odwrotnie. Istnieje jednak wiele reakcji, których odwrócenie wymagałoby drastycznych warunków (np. wysokiej temperatury, wysokiego ciśnienia) i w zwykłych warunkach przebiegają one praktycznie jednokierunkowo. Takie reakcje nazywa się praktycznie nieodwracalnymi i zapisuje się strzałką skierowaną w jedną stronę np.: A + B AB Reakcje nieodwracalne należą do wyjątków i biegną z reguły wtedy, gdy jeden z produktów opuszcza środowisko reakcji.
20 Reakcje odwracalne zapisuje się z dwiema strzałkami skierowanymi przeciwnie np.: aa + bb cc + dd rozumiejąc, że obok reakcji aa + bb Cc + dd przebiegającej z szybkością v 1, zachodzi reakcja cc + dd aa + bb z szybkością v 2. Szybkość tych reakcji można wyrazić następująco: v 1 = k 1 [A] a [B] b v 2 = k 2 [C] c [D] d Ponieważ ubywa substratów A i B to v 1 maleje. Ponieważ przybywa produktów C i D to v 2 rośnie.
21 Stan, kiedy v 1 = v 2 nazywa się stanem równowagi. Pozornie wydaje się, że reakcja w tym stanie nie zachodzi, chociaż szybkość reakcji v 1 i v 2 może być duża. Jeżeli v 1 = v 2 to: k 1 [A] a [B] b = k 2 [C] c [D] d k k 1 2 C A c a D B d b K c gdy T = const. Jest to wzór na stałą równowagi chemicznej (K c ) wyrażający w sposób matematyczny prawo działania mas Guldberga i Waagego. Pamiętać należy, że skoro K c = k 1 / k 2 to wielkość liczbowa stałej K c wskazuje ile razy szybkość reakcji w prawo jest większa od szybkości reakcji w lewo. K c jest wielkością stałą, zależną tylko od temperatury. K c nie zależy od stężenia reagentów!
22 Poprzez stałą równowagi K c możemy m.in. opisać stan równowagi w roztworach, np. dla reakcji. C 2 H 5 OH + CH 3 COOH <=> CH 3 COOC 2 H 5 + H 2 O
23 Dla reakcji biegnącej w fazie gazowej, np. reakcji syntezy amoniaku: 3H 2 + N 2 = 2NH 3 zamiast stężeń we wzorze wygodniej jest stosować ciśnienia cząstkowe reagentów pa, pb, pe, pd Stałą Kp nazywamy ciśnieniową stałą równowagi: K c = K p (1/RT) Δn gdzie Δn = Σn moli gazowych produktów - Σn moli gazowych substratów Dla C (s) + O 2 (g) = CO 2 (g) K c = [CO 2 ]/[O 2 ] K c = K p bo Δn = 0
24 Stałe równowagi dla niektórych często spotykanych reakcji przyjęły charakterystyczne nazwy. Dla reakcji dysocjacji, np. kwasów w roztworach, nazywamy stałą dysocjacji. Np. dla reakcji: CH 3 COOH <=> CH 3 COO - + H + stała dysocjacji wynosi:
25 Reguła przekory Le Chateliera Browna Jeżeli stan równowagi chemicznej reakcji zostanie zakłócony przez jakiś czynnik zewnętrzny to w układzie rozpocznie się taka przemiana, która będzie przeciwdziałać zakłóceniom prowadząc do ponownego osiągnięcia stanu równowagi. Czynnikami mogącymi spowodować zakłócenia stanu równowagi reakcji chemicznej mogą być: a) zmiana stężenia któregokolwiek z reagentów b) zmiana temperatury c) zmiana ciśnienia dla reakcji zachodzących w fazie gazowej, jeżeli objętość zmienia się w czasie reakcji. Dokonując zmian w/w czynników można kierować reakcjami odwracalnymi w pożądanym kierunku uzyskując odpowiednią szybkość i wydajność reakcji.
26 Zmiana stężenia substratu Jeżeli do układu w stanie równowagi dodatkowo wprowadzimy pewną ilość reagentu (substratu lub produktu) to stan równowagi przesunie się w kierunku zmniejszenia jego wartości w układzie. Usuwanie produktów lub dodawanie substratów przesuwa stan równowagi reakcji w prawo. Dodawanie produktów lub usuwanie substratów przesuwa równowagę reakcji w lewo. Wpływ temperatury Jeżeli czynnikiem naruszającym równowagę chemiczną jest zmiana temperatury, to w zależności od efektu cieplnego danej reakcji należy oczekiwać dwojakiego rodzaju skutków. Podwyższenie temperatury w układzie przesunie stan równowagi na korzyść reakcji endotermicznej, której towarzyszy pochłanianie ciepła, natomiast obniżenie temperatury układu przesunie równowagę w kierunku reakcji egzotermicznej, której towarzyszy wydzielanie ciepła.
27 W przypadku reakcji endotermicznych ( pochłaniających ciepło) wzrost temperatury zwiększa szybkość reakcji w prawo. W przypadku reakcji egzotermicznych ( podczas których wydziela się ciepło), wzrost temperatury zwiększa szybkość reakcji w lewo. Obniżenie temperatury powoduje skutek odwrotny. Wpływ ciśnienia Zmiany ciśnienia mają wpływ na przebieg reakcji w układzie zamkniętym tylko wtedy, gdy reakcja przebiega ze zmianą liczby moli, a więc objętość substratów nie równa się objętości produktów. Gdy objętość substratów jest większa od objętości produktów, podwyższenie ciśnienia powoduje przesunięcie równowagi reakcji w prawo. Gdy objętość substratów jest mniejsza od objętości produktów, podwyższenie ciśnienia powoduje przesunięcie równowagi reakcji w lewo. Obniżenie ciśnienia powoduje skutek odwrotny.
Odwracalność przemiany chemicznej
 Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
Odwracalność przemiany chemicznej Na ogół wszystkie reakcje chemiczne są odwracalne, tzn. z danych substratów tworzą się produkty, a jednocześnie produkty reakcji ulegają rozkładowi na substraty. Fakt
Kinetyka reakcji chemicznych. Dr Mariola Samsonowicz
 Kinetyka reakcji chemicznych Dr Mariola Samsonowicz 1 Czym zajmuje się kinetyka chemiczna? Badaniem szybkości reakcji chemicznych poprzez analizę eksperymentalną i teoretyczną. Zdefiniowanie równania kinetycznego
Kinetyka reakcji chemicznych Dr Mariola Samsonowicz 1 Czym zajmuje się kinetyka chemiczna? Badaniem szybkości reakcji chemicznych poprzez analizę eksperymentalną i teoretyczną. Zdefiniowanie równania kinetycznego
Wykład z Chemii Ogólnej i Nieorganicznej
 Wykład z Chemii Ogólnej i Nieorganicznej Część 5 ELEMENTY STATYKI CHEMICZNEJ Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika w Toruniu Prof. dr hab. n.chem.
Wykład z Chemii Ogólnej i Nieorganicznej Część 5 ELEMENTY STATYKI CHEMICZNEJ Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika w Toruniu Prof. dr hab. n.chem.
KI + Pb(NO 3 ) 2 PbI 2 + KNO 3. fermentacja alkoholowa
 Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
1 Kinetyka reakcji chemicznych
 Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Inżynieria Biomedyczna
 1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. a RT.
 Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ
 Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA
 SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
SZYBKOŚĆ REAKCJI CHEMICZNYCH. RÓWNOWAGA CHEMICZNA Zadania dla studentów ze skryptu,,obliczenia z chemii ogólnej Wydawnictwa Uniwersytetu Gdańskiego 1. Reakcja między substancjami A i B zachodzi według
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych
 Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
Materiał powtórzeniowy do sprawdzianu - reakcje egzoenergetyczne i endoenergetyczne, szybkość reakcji chemicznych I. Reakcje egzoenergetyczne i endoenergetyczne 1. Układ i otoczenie Układ - ogół substancji
KI + Pb(NO 3 ) 2 PbI 2 + KNO 3. fermentacja alkoholowa
 Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Kinetyka chemiczna KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 fermentacja alkoholowa czynniki wpływaj ywające na szybkość reakcji chemicznych stęż ężenie reagentów w (lub ciśnienie gazów w jeżeli eli reakcja przebiega
Inżynieria Biomedyczna
 1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
1.Obliczyć przy jakim stężeniu kwasu octowego stopień dysocjacji osiągnie wartość 3.%, jeżeli wiadomo, że stopień dysocjacji 15.%-wego roztworu (d=1.2 g/cm 3 ) w 2. Do 1 cm 3 2% (d=1.2 g/cm 3 ) roztworu
Chemia ogólna nieorganiczna Wykład XII Kinetyka i statyka chemiczna
 Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
fermentacja alkoholowa erozja skał lata dni KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 min Karkonosze Pielgrzymy (1204 m n.p.m.)
 Kinetyka chemiczna lata erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa dni min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Kinetyka chemiczna lata erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa dni min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu
 Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
Wykład 21 XI 2018 Żywienie
 Wykład 21 XI 2018 Żywienie Witold Bekas SGGW Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od warunków przebiegu reakcji pomaga
Wykład 21 XI 2018 Żywienie Witold Bekas SGGW Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od warunków przebiegu reakcji pomaga
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych
 Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Kinetyka. Kinetyka. Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? energia swobodna, G. postęp reakcji.
 Kinetyka energia swobodna, G termodynamika stan 1 kinetyka termodynamika stan 2 postęp reakcji 1 Kinetyka Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 2 Jak szybko
Kinetyka energia swobodna, G termodynamika stan 1 kinetyka termodynamika stan 2 postęp reakcji 1 Kinetyka Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 2 Jak szybko
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU.
 CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
Kinetyka. energia swobodna, G. postęp reakcji. stan 1 stan 2. kinetyka
 Kinetyka postęp reakcji energia swobodna, G termodynamika kinetyka termodynamika stan 1 stan 2 Kinetyka Stawia dwa pytania: 1) Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 1) Jak szybko
Kinetyka postęp reakcji energia swobodna, G termodynamika kinetyka termodynamika stan 1 stan 2 Kinetyka Stawia dwa pytania: 1) Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 1) Jak szybko
Wykład 10 Równowaga chemiczna
 Wykład 10 Równowaga chemiczna REAKCJA CHEMICZNA JEST W RÓWNOWADZE, GDY NIE STWIERDZAMY TENDENCJI DO ZMIAN ILOŚCI (STĘŻEŃ) SUBSTRATÓW ANI PRODUKTÓW RÓWNOWAGA CHEMICZNA JEST RÓWNOWAGĄ DYNAMICZNĄ W rzeczywistości
Wykład 10 Równowaga chemiczna REAKCJA CHEMICZNA JEST W RÓWNOWADZE, GDY NIE STWIERDZAMY TENDENCJI DO ZMIAN ILOŚCI (STĘŻEŃ) SUBSTRATÓW ANI PRODUKTÓW RÓWNOWAGA CHEMICZNA JEST RÓWNOWAGĄ DYNAMICZNĄ W rzeczywistości
relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
 1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1 STECHIOMETRIA INTERPRETACJA ILOŚCIOWA ZJAWISK CHEMICZNYCH relacje ilościowe ( masowe,objętościowe i molowe ) dotyczące połączeń 1. pierwiastków w związkach chemicznych 2. związków chemicznych w reakcjach
1. Określ, w którą stronę przesunie się równowaga reakcji syntezy pary wodnej z pierwiastków przy zwiększeniu objętości zbiornika reakcyjnego:
 1. Określ, w którą stronę przesunie się równowaga reakcji syntezy pary wodnej z pierwiastków przy zwiększeniu objętości zbiornika reakcyjnego: 2. Określ w którą stronę przesunie się równowaga reakcji rozkładu
1. Określ, w którą stronę przesunie się równowaga reakcji syntezy pary wodnej z pierwiastków przy zwiększeniu objętości zbiornika reakcyjnego: 2. Określ w którą stronę przesunie się równowaga reakcji rozkładu
Wykład 4. Anna Ptaszek. 27 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 4. Anna Ptaszek 1 / 31
 Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 27 października 2015 1 / 31 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 27 października 2015 1 / 31 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym
 1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
PRACOWNIA CHEMII. Kinetyka reakcji chemicznych (Fiz1)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Kinetyka reakcji chemicznych
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Kinetyka reakcji chemicznych
Chemia fizyczna 2 - wykład
 Chemia fizyczna 2 - wykład Dr hab. inż. Aneta Pobudkowska-Mirecka Konsultacje: środa 12.15 14.00 (p.149) Chemia Fizyczna 2 - wykład Chemia kwantowa (prof. dr hab. Andrzej Sporzyński) Procesy (dr hab. inż.
Chemia fizyczna 2 - wykład Dr hab. inż. Aneta Pobudkowska-Mirecka Konsultacje: środa 12.15 14.00 (p.149) Chemia Fizyczna 2 - wykład Chemia kwantowa (prof. dr hab. Andrzej Sporzyński) Procesy (dr hab. inż.
Dysocjacja kwasów i zasad. ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to:
 Stała równowagi dysocjacji: Dysocjacja kwasów i zasad HX H 2 O H 3 O X - K a [ H 3O [ X [ HX [ H O 2 ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to: K a [ H 3 O [ X [ HX Dla słabych kwasów
Stała równowagi dysocjacji: Dysocjacja kwasów i zasad HX H 2 O H 3 O X - K a [ H 3O [ X [ HX [ H O 2 ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to: K a [ H 3 O [ X [ HX Dla słabych kwasów
ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji
 ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji w tej temperaturze wynosi K p = 0,11. Reaktor został
ZADANIE 1 W temperaturze 700 K gazowa mieszanina dwutlenku węgla i wodoru reaguje z wytworzeniem pary wodnej i tlenku węgla. Stała równowagi reakcji w tej temperaturze wynosi K p = 0,11. Reaktor został
Wykład 4. Anna Ptaszek. 9 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 4. Anna Ptaszek 1 / 29
 Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 9 października 2015 1 / 29 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Wykład 4 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 9 października 2015 1 / 29 Podstawy kinetyki chemicznej pochodna funkcji i jej interpretacja, pojęcie szybkości i prędkości, stechiometria
Równowaga to stan w którym nie obserwuje się zmian wraz z upływem czasu
 Równowaa chemiczna Równowaa to stan w którym nie obserwuje się zmian wraz z upływem czasu Reakcja chemiczna osiąa stan równowai dy stężenia substratów i produktów nie uleają zmianie pozostają stałe. ozornie
Równowaa chemiczna Równowaa to stan w którym nie obserwuje się zmian wraz z upływem czasu Reakcja chemiczna osiąa stan równowai dy stężenia substratów i produktów nie uleają zmianie pozostają stałe. ozornie
erozja skał lata KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 min Karkonosze Pielgrzymy (1204 m n.p.m.)
 Kinetyka chemiczna erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa lata min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Kinetyka chemiczna erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa lata min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
- w nawiasach kwadratowych stężenia molowe.
 Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
a) 1 mol b) 0,5 mola c) 1,7 mola d) potrzebna jest znajomość objętości zbiornika, aby można było przeprowadzić obliczenia
 1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
Podstawy kinetyki i termodynamiki chemicznej. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Podstawy kinetyki i termodynamiki chemicznej Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Układ i otoczenie Układem - część środowiska, która stanowi przedmiot naszych badań pojęcie abstrakcyjne,
Podstawy kinetyki i termodynamiki chemicznej Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Układ i otoczenie Układem - część środowiska, która stanowi przedmiot naszych badań pojęcie abstrakcyjne,
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI
 Ćwiczenie nr 4 WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej szybkości reakcji zmydlania estru etylowego w dwóch różnych temperaturach,
Ćwiczenie nr 4 WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej szybkości reakcji zmydlania estru etylowego w dwóch różnych temperaturach,
Przemiany/Reakcje chemiczne
 Przemiany/Reakcje chemiczne Przemiany/Reakcje chemiczne Reakcje chemiczne są to takie przemiany, w wyniku których z jednych substancji powstają inne substancje, o zupełnie odmiennych właściwościach fizycznych
Przemiany/Reakcje chemiczne Przemiany/Reakcje chemiczne Reakcje chemiczne są to takie przemiany, w wyniku których z jednych substancji powstają inne substancje, o zupełnie odmiennych właściwościach fizycznych
Wyznaczanie stałej szybkości reakcji wymiany jonowej
 Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych
 CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
Równowagi w roztworach wodnych
 Równowagi w roztworach wodnych V 1 A + B = C + D V 2 Szybkości reakcji: v 1 = k 1 c A c B v 2 = k 2 c C c D ogólnie Roztwory, rozpuszczalność, rodzaje stężeń, iloczyn rozpuszczalności Reakcje dysocjacji
Równowagi w roztworach wodnych V 1 A + B = C + D V 2 Szybkości reakcji: v 1 = k 1 c A c B v 2 = k 2 c C c D ogólnie Roztwory, rozpuszczalność, rodzaje stężeń, iloczyn rozpuszczalności Reakcje dysocjacji
prof. dr hab. Małgorzata Jóźwiak
 Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph
 Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
KATALITYCZNY ROZKŁAD WODY UTLENIONEJ
 Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KATALITYCZNY ROZKŁAD WODY UTLENIONEJ Wstęp teoretyczny Kataliza homo- i heterogeniczna Zwiększenie
Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KATALITYCZNY ROZKŁAD WODY UTLENIONEJ Wstęp teoretyczny Kataliza homo- i heterogeniczna Zwiększenie
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12
 Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Opracował: dr inż. Tadeusz Lemek
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria i Gospodarka Wodna w ramach projektu Era inżyniera pewna lokata na przyszłość Opracował:
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria i Gospodarka Wodna w ramach projektu Era inżyniera pewna lokata na przyszłość Opracował:
KINETYKA INWERSJI SACHAROZY
 Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
PRACOWNIA CHEMII. Równowaga chemiczna (Fiz2)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Równowaga chemiczna (Fiz2)
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Równowaga chemiczna (Fiz2)
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
TYPY REAKCJI CHEMICZNYCH
 1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
1 REAKCJA CHEMICZNA: TYPY REAKCJI CHEMICZNYCH REAKCJĄ CHEMICZNĄ NAZYWAMY PROCES, W WYNIKU KTÓREGO Z JEDNYCH SUBSTANCJI POWSTAJĄ NOWE (PRODUKTY) O INNYCH WŁAŚCIWOŚCIACH NIŻ SUBSTANCJE WYJŚCIOWE (SUBSTRATY)
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak
 Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
Czy równowaga jest procesem korzystnym? dr hab. prof. nadzw. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga ciało
dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K
![dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K](/thumbs/55/36391740.jpg) RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
a) jeżeli przedstawiona reakcja jest reakcją egzotermiczną, to jej prawidłowy przebieg jest przedstawiony na wykresie za pomocą linii...
 1. Spośród podanych reakcji wybierz reakcję egzoenergetyczną: a) Redukcja tlenku miedzi (II) wodorem b) Otrzymywanie tlenu przez rozkład chloranu (V) potasu c) Otrzymywanie wapna palonego w procesie prażenia
1. Spośród podanych reakcji wybierz reakcję egzoenergetyczną: a) Redukcja tlenku miedzi (II) wodorem b) Otrzymywanie tlenu przez rozkład chloranu (V) potasu c) Otrzymywanie wapna palonego w procesie prażenia
Podstawy termodynamiki.
 Podstawy termodynamiki. Termodynamika opisuje ogólne prawa przemian energetycznych w układach makroskopowych. Określa kierunki procesów zachodzących w przyrodzie w sposób samorzutny, jak i stanów końcowych,
Podstawy termodynamiki. Termodynamika opisuje ogólne prawa przemian energetycznych w układach makroskopowych. Określa kierunki procesów zachodzących w przyrodzie w sposób samorzutny, jak i stanów końcowych,
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej. Część IV - Elementy termodynamiki i kinetyki chemicznej
 Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Część IV - Elementy termodynamiki i kinetyki chemicznej Wydział Chemii UAM Poznań 2011 POJĘCIA CIA PODSTAWOWE UKŁAD AD pewna część
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Część IV - Elementy termodynamiki i kinetyki chemicznej Wydział Chemii UAM Poznań 2011 POJĘCIA CIA PODSTAWOWE UKŁAD AD pewna część
Roztwory elekreolitów
 Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
Równowagi w roztworach wodnych
 Równowagi w roztworach wodnych Stan i stała równowagi reakcji chemicznej ogólnie Roztwory, rozpuszczalność, rodzaje stężeń, iloczyn rozpuszczalności Reakcje dysocjacji Stopień dysocjacji Prawo rozcieńczeń
Równowagi w roztworach wodnych Stan i stała równowagi reakcji chemicznej ogólnie Roztwory, rozpuszczalność, rodzaje stężeń, iloczyn rozpuszczalności Reakcje dysocjacji Stopień dysocjacji Prawo rozcieńczeń
Badanie kinetyki katalitycznego rozkładu H 2 O 2
 Badanie kinetyki katalitycznego rozkładu H 2 O 2 (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zapoznanie się z prawami kinetyki chemicznej, sposobem wyznaczenia stałej szybkości i rzędu reakcji
Badanie kinetyki katalitycznego rozkładu H 2 O 2 (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zapoznanie się z prawami kinetyki chemicznej, sposobem wyznaczenia stałej szybkości i rzędu reakcji
ĆWICZENIE NR 11 KINETYKA WYMIANY IZOTOPOWEJ W UKŁADZIE HOMOGENICZNYM
 ĆWICZENIE NR 11 KINETYKA WYMIANY IZOTOPOWEJ W UKŁADZIE HOMOGENICZNYM Podstawy fizyczne Przez reakcję wymiany izotopowej rozumie się taką reakcję chemiczną, w czasie której izotopowe atomy określonego pierwiastka
ĆWICZENIE NR 11 KINETYKA WYMIANY IZOTOPOWEJ W UKŁADZIE HOMOGENICZNYM Podstawy fizyczne Przez reakcję wymiany izotopowej rozumie się taką reakcję chemiczną, w czasie której izotopowe atomy określonego pierwiastka
Obliczenia chemiczne. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru
 1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
CHEMIA. Wymagania szczegółowe. Wymagania ogólne
 CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
c t x v KINETYKA CHEMICZNA
 KINETYKA CHEMICZNA Prawa termodynamiki chemicznej pozwalają nam przewidzieć tylko możliwy kierunek przemian w układzie reagentów oraz ilość poszczególnych składników znajdujących się w układzie w momencie
KINETYKA CHEMICZNA Prawa termodynamiki chemicznej pozwalają nam przewidzieć tylko możliwy kierunek przemian w układzie reagentów oraz ilość poszczególnych składników znajdujących się w układzie w momencie
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Kinetyka. Szybkość reakcji. Szybkość reakcji. Szybkość reakcji
 Korozja konstrukcji stalowych dr inż. Leszek Niedzicki Kinetyka Szybki rozkład związków organicznych (wysokoenergetycznych) lub synteza wody z wodoru i tlenu. 2 Reakcja może trwać nano-mikrosekundy lub
Korozja konstrukcji stalowych dr inż. Leszek Niedzicki Kinetyka Szybki rozkład związków organicznych (wysokoenergetycznych) lub synteza wody z wodoru i tlenu. 2 Reakcja może trwać nano-mikrosekundy lub
Jak mierzyć i jak liczyć efekty cieplne reakcji?
 Jak mierzyć i jak liczyć efekty cieplne reakcji? Energia Zdolność do wykonywania pracy lub do produkowania ciepła Praca objętościowa praca siła odległość 06_73 P F A W F h N m J P F A Area A ciśnienie
Jak mierzyć i jak liczyć efekty cieplne reakcji? Energia Zdolność do wykonywania pracy lub do produkowania ciepła Praca objętościowa praca siła odległość 06_73 P F A W F h N m J P F A Area A ciśnienie
Podstawy kinetyki i termodynamiki chemicznej. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Podstawy kinetyki i termodynamiki chemicznej Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Termodynamika chemiczna i kinetyka reakcji chemicznych Termodynamika - odpowiada na pytanie czy
Podstawy kinetyki i termodynamiki chemicznej Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Termodynamika chemiczna i kinetyka reakcji chemicznych Termodynamika - odpowiada na pytanie czy
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak)
 Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Sonochemia. Schemat 1. Strefy reakcji. Rodzaje efektów sonochemicznych. Oscylujący pęcherzyk gazu. Woda w stanie nadkrytycznym?
 Schemat 1 Strefy reakcji Rodzaje efektów sonochemicznych Oscylujący pęcherzyk gazu Woda w stanie nadkrytycznym? Roztwór Znaczne gradienty ciśnienia Duże siły hydrodynamiczne Efekty mechanochemiczne Reakcje
Schemat 1 Strefy reakcji Rodzaje efektów sonochemicznych Oscylujący pęcherzyk gazu Woda w stanie nadkrytycznym? Roztwór Znaczne gradienty ciśnienia Duże siły hydrodynamiczne Efekty mechanochemiczne Reakcje
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1
 Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 2, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
imię i nazwisko, nazwa szkoły, miejscowość Zadania I etapu Konkursu Chemicznego Trzech Wydziałów PŁ V edycja
 Zadanie 1 (2 pkt.) Zmieszano 80 cm 3 roztworu CH3COOH o stężeniu 5% wag. i gęstości 1,006 g/cm 3 oraz 70 cm 3 roztworu CH3COOK o stężeniu 0,5 mol/dm 3. Obliczyć ph powstałego roztworu. Jak zmieni się ph
Zadanie 1 (2 pkt.) Zmieszano 80 cm 3 roztworu CH3COOH o stężeniu 5% wag. i gęstości 1,006 g/cm 3 oraz 70 cm 3 roztworu CH3COOK o stężeniu 0,5 mol/dm 3. Obliczyć ph powstałego roztworu. Jak zmieni się ph
Za poprawną metodę Za poprawne obliczenia wraz z podaniem zmiany ph
 Zadanie 1 ( pkt.) Zmieszano 80 cm roztworu CHCH o stężeniu 5% wag. i gęstości 1,006 g/cm oraz 70 cm roztworu CHCK o stężeniu 0,5 mol/dm. bliczyć ph powstałego roztworu. Jak zmieni się ph roztworu po wprowadzeniu
Zadanie 1 ( pkt.) Zmieszano 80 cm roztworu CHCH o stężeniu 5% wag. i gęstości 1,006 g/cm oraz 70 cm roztworu CHCK o stężeniu 0,5 mol/dm. bliczyć ph powstałego roztworu. Jak zmieni się ph roztworu po wprowadzeniu
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj.
 Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Wpływ wybranych czynników na efektywność procesu
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA TECHNOLOGII CHEMICZNEJ ORGANICZNEJ I PETROCHEMII INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH: Wpływ wybranych czynników na efektywność procesu Laboratorium z przedmiotu:
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA TECHNOLOGII CHEMICZNEJ ORGANICZNEJ I PETROCHEMII INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH: Wpływ wybranych czynników na efektywność procesu Laboratorium z przedmiotu:
Enzymologia I. Kinetyka - program Gepasi. Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu
 Enzymologia I Kinetyka - program Gepasi Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu I zasada + II zasada termodynamiki zmiana entalpii i entropii może zostać wyrażona ilościowo
Enzymologia I Kinetyka - program Gepasi Uniwersytet Warszawski Wydział Biologii Zakład Regulacji Metabolizmu I zasada + II zasada termodynamiki zmiana entalpii i entropii może zostać wyrażona ilościowo
BIOTECHNOLOGIA. Materiały do ćwiczeń rachunkowych z chemii fizycznej kinetyka chemiczna, 2014/15
 BIOTECHNOLOGIA Materiały do ćwiczeń rachunkowych z chemii fizycznej kinetyka chemiczna, 014/15 Zadanie 1. (*) W temperaturze 45 o C badano reakcję rozkładu tlenku azotu (V) w roztworze CCl4 (T, V = const.)
BIOTECHNOLOGIA Materiały do ćwiczeń rachunkowych z chemii fizycznej kinetyka chemiczna, 014/15 Zadanie 1. (*) W temperaturze 45 o C badano reakcję rozkładu tlenku azotu (V) w roztworze CCl4 (T, V = const.)
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 2
 PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
Inżynieria Środowiska
 ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
Chemia fizyczna (2013/2014) kinetyka chemiczna
 Chemia fizyczna (01/014) kinetyka chemiczna Zadanie 1. Dla reakcji rozkładu N O 5 4NO +O w roztworze CCl 4, w warunkach T,V=const w temperaturze 45 o C otrzymano następującą zależność stężenia N O 5 (A)
Chemia fizyczna (01/014) kinetyka chemiczna Zadanie 1. Dla reakcji rozkładu N O 5 4NO +O w roztworze CCl 4, w warunkach T,V=const w temperaturze 45 o C otrzymano następującą zależność stężenia N O 5 (A)
EFEKT SOLNY BRÖNSTEDA
 EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
-wszystkie substancje (pierwiastki lub zw chem) które biorą udział w reakcji chemicznej nazywamy reagentami
 Zapis reakcji chemicznej co to są przemiany chemiczne oraz w jaki sposób możemy opisać zachodzące reakcje? wokół nas bezustannie zachodzą rozmaite przemiany przemiany podczas których powstaje nowa substancja,
Zapis reakcji chemicznej co to są przemiany chemiczne oraz w jaki sposób możemy opisać zachodzące reakcje? wokół nas bezustannie zachodzą rozmaite przemiany przemiany podczas których powstaje nowa substancja,
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II
 TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
HYDROLIZA SOLI. 1. Hydroliza soli mocnej zasady i słabego kwasu. Przykładem jest octan sodu, dla którego reakcja hydrolizy przebiega następująco:
 HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks
 Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
Obliczenia stechiometryczne, bilansowanie równań reakcji redoks Materiały pomocnicze do zajęć wspomagających z chemii opracował: dr Błażej Gierczyk Wydział Chemii UAM Obliczenia stechiometryczne Podstawą
... Nazwisko, imię zawodnika; Klasa Liczba punktów. ... Nazwa szkoły, miejscowość. I Podkarpacki Konkurs Chemiczny 2008/09
 ......... Nazwisko, imię zawodnika; Klasa Liczba punktów KOPKCh... Nazwa szkoły, miejscowość I Podkarpacki Konkurs Chemiczny 2008/09 ETAP III 28.02.2009 r. Godz. 10.00-13.00 Zadanie 1 (10 pkt.) ( postaw
......... Nazwisko, imię zawodnika; Klasa Liczba punktów KOPKCh... Nazwa szkoły, miejscowość I Podkarpacki Konkurs Chemiczny 2008/09 ETAP III 28.02.2009 r. Godz. 10.00-13.00 Zadanie 1 (10 pkt.) ( postaw
Układ Graficzny przygotowano na podstawie materiałów egzaminacyjnych CKE
 Układ Graficzny przygotowano na podstawie materiałów egzaminacyjnych CKE WPISUJE ZDAJĄCY KOD KOD PESEL PESEL Miejsce na naklejkę z kodem EGZAMIN MATURALNY Z CHEMII (KINETYKA I RÓWNOWAGA CHEMICZNA - A)
Układ Graficzny przygotowano na podstawie materiałów egzaminacyjnych CKE WPISUJE ZDAJĄCY KOD KOD PESEL PESEL Miejsce na naklejkę z kodem EGZAMIN MATURALNY Z CHEMII (KINETYKA I RÓWNOWAGA CHEMICZNA - A)
MODEL ODPOWIEDZI I SCHEMAT OCENIANIA ARKUSZA II
 MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
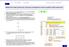 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG
 WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG Imię i nazwisko: Klasa i szkoła*: Adres e-mail: Nr telefonu: Czy uczeń jest już uczestnikiem projektu? (odp. otoczyć kółkiem) Ocena
WNIOSEK REKRUTACYJNY NA ZAJĘCIA KÓŁKO OLIMPIJSKIE Z CHEMII - poziom PG Imię i nazwisko: Klasa i szkoła*: Adres e-mail: Nr telefonu: Czy uczeń jest już uczestnikiem projektu? (odp. otoczyć kółkiem) Ocena
LABORATORIUM Z KATALIZY HOMOGENICZNEJ I HETEROGENICZNEJ WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa
 Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Równowagi w roztworach wodnych
 Równowagi w roztworach wodnych Stan i stała równowagi reakcji chemicznej ogólnie Roztwory, rozpuszczalność, rodzaje stężeń, iloczyn rozpuszczalności Reakcje dysocjacji Stopień dysocjacji Prawo rozcieńczeń
Równowagi w roztworach wodnych Stan i stała równowagi reakcji chemicznej ogólnie Roztwory, rozpuszczalność, rodzaje stężeń, iloczyn rozpuszczalności Reakcje dysocjacji Stopień dysocjacji Prawo rozcieńczeń
RÓWNOWAGI W ROZTWORACH ELEKTROLITÓW
 RÓWNOWAGI W ROZTWORACH ELETROLITÓW Opracowanie: dr Jadwiga Zawada, dr inż. rystyna Moskwa, mgr Magdalena Bisztyga 1. Dysocjacja elektrolityczna Substancje, które podczas rozpuszczania w wodzie (lub innych
RÓWNOWAGI W ROZTWORACH ELETROLITÓW Opracowanie: dr Jadwiga Zawada, dr inż. rystyna Moskwa, mgr Magdalena Bisztyga 1. Dysocjacja elektrolityczna Substancje, które podczas rozpuszczania w wodzie (lub innych
Mechanizm działania buforów *
 Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
