3. Wprowadzenie do nazewnictwa związków organicznych
|
|
|
- Liliana Bukowska
- 7 lat temu
- Przeglądów:
Transkrypt
1 3. Wprowadzenie do nazewnictwa związków organicznych 1
2 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową (C 2 ) jednostka strukturalna izo Izomery konstytucyjne ten sam wzór sumaryczny, różny sposób połączenia atomów nazwa systematyczna nazwa zwyczajowa 2
3 3.2. Nazewnictwo podstawników (pierwszorzędowy) atom węgla 4 Podstawnik metyl C 3 etyl C 3 C 2 propyl C 3 C 2 C 2 butyl C 3 C 2 C 2 C 2 itd. Węglowodór metan C 4 etan C 3 C 3 propan C 3 C 2 C 3 butan C 3 C 2 C 2 C 3 zamiana końcówki an w nazwie systematycznej węglowodoru na yl Podstawniki rozgałęzione (nazwy zwyczajowe) oznaczenie odjęcia wodoru 3
4 3.3. Nazewnictwo alkanów 4 C 3 2 najdłuższy łańcuch, tzw. główny lokant podstawnika 2-metylopentan 3-etyloheksan 4-propylooktan (najniższy z możliwych) podstawniki w porządku alfabetycznym di, tri, tetra, itd. krotność takich samych podstawników (przedrostki nie uwzględniane w porządku alfabetycznym, podobnie jak przedrostki sec- i tert-) 5-etylo-3-metylooktan 2,4-dimetyloheksan 5-etylo-2,5-dimetyoheptan lokanty są takie same w obu kierunkach numeracji - kierunek numeracji jest zgodny z porządkiem alfabetycznym podstawników 3-etylo-5-metyloheptan 4
5 3.3.cd. Nazewnictwo alkanów atom węgla podstawnika rozgałęzionego związany z łańcuchem głównym - zawsze lokant 1 w numeracji podstawnika przedrostki di, tri, tetra, itd. - część nazwy podstawnika uwzględniana w porządku alfabetycznym podstawników 4-(1-metyloetylo)heptan 6-(1,2-dimetylopropylo)-4-propylodekan dwa lub więcej łańcuchów tej samej długości łańcuch główny to ten z większą liczbą podstawników 3-etylo-2-metyloheksan 3-(1-metyloetylo)heksan nazwa prawidłowa 5
6 3.4. Nazewnictwo cykloalkanów przedrostek cyklo przed nazwą alkanu o danej liczbie atomów węgla cyklopropan cyklobutan cyklopentan cykloheksan jeden podstawnik w pierścieniu brak numeracji pierścienia metylocyklopentan etylocykloheksan większa liczba atomów węgla w podstawniku niż w pierścieniu pierścień jest podstawnikiem 1-cylobutylopentan dwa różne podstawniki kierunek numeracji pierścienia zgodny z porządkiem alfabetycznym nazw podstawników 1-etylo-2-metylocyklopentan 1-metylo-3-propylocyklopentan dwa podstawniki taki kierunek numeracji pierścienia, aby lokant drugiego podstawnika był jak najniższy 1 1,1,2-trimetylocyklopentan takie same niskie lokanty dwóch podstawników numeracja pierścienia w kierunku skutkującym jak najniższym lokantem trzeciego podstawnika 4-etylo-2-metylo-1-propylocykloheksan 6
7 3.5. Nazewnictwo halogenków alkili Atom wodoru w alkanie jest zastąpiony przez halogen związek 1 1 bromek alkilu Br Nomenklatura klasowo-funkcyjna chlorek metylu fluorek etylu 2 R C Br R 2 bromek alkilu jodek izopropylu bromek sec-butylu Nomenklatura podstawnikowa; halogen - podstawnik chlorometan fluoroetan 2-jodopropan 3 3 bromek alkilu 2-bromobutan jakikolwiek halogen jakikolwiek szkielet alkilowy Nomenklatura klasowo-funkcyjna - główną grupę charakterystyczną określa nazwa klasy związku, np.: chlorek, alkohol lub keton, pisana jako oddzielny wyraz przed nazwą macierzystego wodorku (np.: jodek metylu, keton etylowo-metylowy) lub nazwa podstawnika (np. chlorek acetylu). Nomenklatura podstawnikowa - wymiana jednego lub większej liczby atomów wodoru macierzystego wodorku lub macierzystej struktury na inny atom lub grupę atomów określanych właściwym dla nich przyrostkiem bądź przedrostkiem, np.: 1-metylonaftalen, pentan-1-ol. Macierzysty wodorek jest strukturą, której nazwa po dodaniu afiksów wskazujących podstawniki utworzy nazwę określonego związku. 2-bromo-5-metyloheptan 1-etylo-2-jodocyklopentan 1-bromo-2-chloro-4-metylocykloheksan 7
8 3.6. Nazewnictwo eterów eter symetryczny (jednakowe szkielety węglowe) eter niesymetryczny (różne szkielety węglowe) Nomenklatura klasowo-funkcyjna; eter klasa związku (do nazywania małocząsteczkowych eterów) nazwy szkieletów węglowych w porządku alfabetycznym Nomenklatura podstawnikowa (alkoksyl - podstawnik) eter etylowo-metylowy eter dietylowy eter tert-butylowo-izobutylowyy 1-tert-butoksy-2-metylopropan eter sec-butylowo-izopropylowy 2-izopropoksybutan eter cykloheksylo-izopentylowy izopentyloksycyklohexan 8
9 3.7. Nazewnictwo amin R R N R 1 amina 2 amina 3 amina rzędowość aminy liczba podstawników węglowych przy at. N Nomenklatura klasowo-funkcyjna; amina klasa związku (do nazywania małocząsteczkowych amin) podstawniki przy atomie azotu w porządku alfabetycznym etyloamina Nomenklatura podstawnikowa; grupa aminowa (N 2, RN lub R 2 N) podstawnik etanoamina metylopropyloamina N-metylopropano-1-amina dietyloamina N,N-dimetylobutano-1-amina butylodimetyloamina N-etylo-5-metyloheksano-3-amina 9
10 3.8. Nazewnictwo alkoholi R C O R 1 alkohol 2 alkohol 3 alkohol związek Nomenklatura klasowo-funkcyjna; alkohol klasa związku alkohol etylowy alkohol propylowy alkohol izopropylowy alkohol izobutylowy Nomenklatura podstawnikowa; grupa hydroksyksylowa (ol) - podstawnik etanol propan-1-ol propan-2-ol 2-metylopropan-1-ol Zasady konstruowania nazw grupowo-funkcyjnych łańcuch główny musi zawierać grupę funkcyjną (tutaj, O), a jej lokant musi być najniższy z możliwych 2-etylopentan-1-ol liczba grup O w łańcuchu głównym przedrostek di-, tri, tetra-, itd. heksano-1,2-diol pentano-2,3,4-triol 10
11 3.8.cd. Nazewnictwo alkoholi grupa O ma najniższy lokant spośród lokantów innych podstawników 3-bromobutan-1-ol 4-chlorobutan-2-ol 5,5-dimethylhexan-2-ol jeśli numeracja w obu kierunkach daje taki sam lokant grupy O, to łańcuch główny jest numerowany tak, aby lokant drugiego podstawnika był najniższy z możliwych 2-chloropentan-3-ol 3-methylcyclohexanol jeśli są dwa lub więcej podstawniki (poza grupą O), to wymienia się je w porządku alfabetycznym 7-chloro-4-etylooktan-2-ol 11
12 3.9. Wybrane właściwości fizyczne związków organicznych Temperatura wrzenia i temperatura topnienia a liczba atomów węgla 40 Temperatura wrzenia a stopień rozgałęzienia T/st. C C 3 C Liczba atomów C Tw Tt Tw/st. C pentan 2-metylobutan 2,2-dimetylopropan pentan 2-metylobutan 2,2-dimetylopropan 12
13 3.9.cd. Wybrane właściwości fizyczne związków organicznych 95 Temperatura wrzenia a klasa związku O wiązanie wodorowe nm 75 Tw/st. C N 2 O alkan eter alkohol amina nm Temperatura wrzenia a rzędowość aminy Temperatura wrzenia a rodzaj halogenku alkilu I Br Tw/st. C 50 0 N 2 N N Tw/st. C Cl F alkan fluorek chlorek bromek jodek alkilu 13
14 3.10. Pojęcie konformacji Konformacja zmiana wzajemnego ułożenia w przestrzeni elementów składowych obiektu bez zmiany konstytucji (budowy) obiektu Przemiana konformacyjna nie powoduje rozłączenia elementów obiektu najtrwalsza konformacja najmniej trwała konformacja 14
15 3.11. Równowaga konformacyjna w etanie Wzory Newmana bariera rotacji Energia pote encjalna 15
16 3.12. Wizualizacja równowagi konformacyjnej w butanie «Chem3D Embed» 16
17 3.13. Równowaga konformacyjna w butanie zmiana energii potencjalnej synperiplanarna antyklinalna antyklinalna C 3 konformacje naprzeciwległe Ener rgia potencjalna 16 kj/mol 19 kj/mol 3.6 kj/mol 3 C konformacje naprzemianległe C 3 C 3 3 C C 3 synklinalna antyperiplanarna synklinalna 17
18 3.14. Naprężenia kątowe w cykloalkanach niewielki stopień nałożenia orbitali słabe wiązanie znaczny stopień nałożenia orbitali silne wiązanie cyklopropan 27.3 cyklobutan 26.5 cyklopentan 06.2 cykloheksan 00 cykloheptan 06.2 Energia naprężeń* [kcal/mol] *zakładając, że pierścień jest płaski 18
19 3.15. Równowaga konformacyjna w cykloheksanie rodzaje wiązań C- konformacja krzesłowa minimum energii potencjalnej krok wiązania aksjalne wiązania ekwatorialne Ważne wiązania do siebie równoległe 19
20 3.16. Równowaga konformacyjna w cykloheksanie rodzaje konformacji minimum energii potencjalnej maksimum energii potencjalnej minimum energii potencjalnej wiązania ekwatorialne ten at. C pociągnąć w dół szybka konwersja wiązania aksjalne ten atom C popchnąć w górę konformacja łodziowa maksimum energii potencjalnej
21 3.17. Równowaga konformacyjna w monopodstawionych cykloheksanach trwalszy konformer oddziaływania 1,3-diaksjalne zatłoczenie steryczne Podstawnik C 3 C 2 C ponad 99.9% populacji cząsteczek w postaci konformeru z t-bu w położeniu ekwatorialnym 21
22 3.18. Równowaga konformacyjna w dimetylocykloheksanie cis-1,4-dimetylocykloheksan obie gr. C 3 po tej samej stronie pierścienia (oba wiązania skierowane w dół) trans-1,4-dimetylocykloheksan obie gr. C 3 po przeciwnych stronach pierścienia wiązanie skierowane w górę wiązanie skierowane w dół konformer (a,e) (e,a) (e,e) (a,a) Ważne Konwersja pierścienia nie powoduje zmiany rodzaju izomeru 22
23 3.19. Równowaga konformacyjna w 1-t-butylo-2-metylocykloheksanie cis-1-t-butylo-3-metylocykloheksan (e,e) (a,a) trans-1-t-butylo-3-metylocykloheksan (a,e) (e,a) 23
24 3.20. Równowaga konformacyjna w 1-t-butylo-3-metylocykloheksanie cis-1-t-butylo-2-metylocykloheksan trans-1-t-butylo-2-metylocykloheksan 24
25 3.21. Skumulowane cykloalkany trans-dekalina cis-dekalina Układ pierścieni w cząsteczkach steroidów trans-skumulowane pierścienie 25
4-6. Wprowadzenie do nazewnictwa związków organicznych
 4-6. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową
4-6. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową
Slajd 1. Wstęp do chemii organicznej. Nomenklatura, własności fizyczne, struktura. eter. mapa potencjału elektrostatycznego cząsteczki eteru etylowego
 Slajd 1 Wstęp do chemii organicznej Nomenklatura, własności fizyczne, struktura hybrydyzacja sp 3 eter mapa potencjału elektrostatycznego cząsteczki eteru etylowego Slajd 2 Alkany to węglowodory zawierające
Slajd 1 Wstęp do chemii organicznej Nomenklatura, własności fizyczne, struktura hybrydyzacja sp 3 eter mapa potencjału elektrostatycznego cząsteczki eteru etylowego Slajd 2 Alkany to węglowodory zawierające
Materiały do zajęć dokształcających z chemii organicznej
 hemia Warta Poznania - nowa JAKOŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
hemia Warta Poznania - nowa JAKOŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
Alkany i Cykloalkany C n H 2n+2
 Alkany i Cykloalkany C n H 2n+2 C n H 2n Alkany - węglowodory nasycone RH węglowodory ponieważ składają się jedynie z atomów C i H nasycone, bo zawierają jedynie pojedyncze wiązania C C i tym samym mają
Alkany i Cykloalkany C n H 2n+2 C n H 2n Alkany - węglowodory nasycone RH węglowodory ponieważ składają się jedynie z atomów C i H nasycone, bo zawierają jedynie pojedyncze wiązania C C i tym samym mają
H H H. Wzór "płaskostrukturalny": Wzór klinowy: H H. Model kulkowy cząsteczki: (obrazuje długosci wiązań, kąty między wiązaniami)
 Autor: Marek Walnik, 04 Alkany - węglowodory nasycone, parafiny. Związki węgla z wodorem, w których cząsteczkach występują wyłącznie wiązania pojedyncze. Szczególną klasę związków tego typu stanowią cykloalkany
Autor: Marek Walnik, 04 Alkany - węglowodory nasycone, parafiny. Związki węgla z wodorem, w których cząsteczkach występują wyłącznie wiązania pojedyncze. Szczególną klasę związków tego typu stanowią cykloalkany
RJC # Defin i i n c i ja
 Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Konspekt wykładu Chemia Organiczna dla studentów Wydziału Inżynierii Chemicznej i Procesowej
 Konspekt wykładu hemia Organiczna dla studentów Wydziału Inżynierii hemicznej i Procesowej ALKANY 2 godz. 1. Wzór sumaryczny: n 2n+2 (n = liczba naturalna) - węglowodory posiadające tylko wiązania pojedyncze
Konspekt wykładu hemia Organiczna dla studentów Wydziału Inżynierii hemicznej i Procesowej ALKANY 2 godz. 1. Wzór sumaryczny: n 2n+2 (n = liczba naturalna) - węglowodory posiadające tylko wiązania pojedyncze
Zdzisław Głowacki. Zakres podstawowy i rozszerzony. Odpowiedzi i rozwiązania zadań. Rozdział 1. Powinno być
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 1 Errata do pierwszego rozdziału ćwiczeń: Strona Linia / zadanie Str. 10. Linia 1. Str. 16.
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 1 Errata do pierwszego rozdziału ćwiczeń: Strona Linia / zadanie Str. 10. Linia 1. Str. 16.
ALKANY (by Aleksandra Kołodziejczyk, UG) Węglowodory: - nasycone = alkany - nienasycone (alkeny, alkiny)
 ALKANY (by Aleksandra Kołodziejczyk, UG) Węglowodory: - nasycone = alkany - nienasycone (alkeny, alkiny) C n n+, brak gr. funkcyjnych. Alkany: - nierozgałęzione; - rozgałęzione; - cykliczne. Związki homologiczne
ALKANY (by Aleksandra Kołodziejczyk, UG) Węglowodory: - nasycone = alkany - nienasycone (alkeny, alkiny) C n n+, brak gr. funkcyjnych. Alkany: - nierozgałęzione; - rozgałęzione; - cykliczne. Związki homologiczne
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Alkany i cykloalkany
 Alkany i cykloalkany ALKANY WĘGLOWODORY NASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU POJEDYNCZE WIĄZANIA WĘGIEL WĘGIEL ATOM WĘGLA W HYBRYDYZACJI sp 3 KĄTY MIĘDZY WIĄZANIAMI, DŁUGOŚCI
Alkany i cykloalkany ALKANY WĘGLOWODORY NASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU POJEDYNCZE WIĄZANIA WĘGIEL WĘGIEL ATOM WĘGLA W HYBRYDYZACJI sp 3 KĄTY MIĘDZY WIĄZANIAMI, DŁUGOŚCI
Klasyfikacja i przykłady ETERY
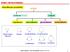 ETERY I EPKSYZWIĄZKI Klasyfikacja i przykłady ETERY acykliczne R--R cykliczne trójczłonowe czteroczłonowe pięcioczłonowe sześcioczłonowe tlenek etylenu (oksiran) oksetan tetrahydrofuran tetrahydropiran
ETERY I EPKSYZWIĄZKI Klasyfikacja i przykłady ETERY acykliczne R--R cykliczne trójczłonowe czteroczłonowe pięcioczłonowe sześcioczłonowe tlenek etylenu (oksiran) oksetan tetrahydrofuran tetrahydropiran
Spis treści. Budowa alkanów. 1 Budowa alkanów 2 Reakcje chemiczne alkanów 3 Izomeria 4 Rzędowość atomów węgla 5 Energia wewnętrzna. Konformacje.
 Spis treści 1 Budowa alkanów 2 Reakcje chemiczne alkanów 3 Izomeria 4 Rzędowość atomów węgla 5 Energia wewnętrzna. Konformacje. Budowa alkanów Poznawanie związków organicznych zaczniemy od substancji najprostszych
Spis treści 1 Budowa alkanów 2 Reakcje chemiczne alkanów 3 Izomeria 4 Rzędowość atomów węgla 5 Energia wewnętrzna. Konformacje. Budowa alkanów Poznawanie związków organicznych zaczniemy od substancji najprostszych
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Materiał powtórzeniowy do sprawdzianu - węglowodory nasycone - alkany + przykładowe zadania
 Materiał powtórzeniowy do sprawdzianu - węglowodory nasycone - alkany + przykładowe zadania I. Atom węgla w związkach organicznych i jego rzędowość 1. Hybryzdyzacja atomu węgla a) konfiguracja elektronowa
Materiał powtórzeniowy do sprawdzianu - węglowodory nasycone - alkany + przykładowe zadania I. Atom węgla w związkach organicznych i jego rzędowość 1. Hybryzdyzacja atomu węgla a) konfiguracja elektronowa
Izomerię konstytucyjną można podzielić na podgrupy a) izomeria szkieletowa, która polega na różnej budowie szkieletu węglowego cząsteczek Przykład:
 1 1) Informacje ogólne Izomery są to związki, które maja identyczne wzory sumaryczne ale różnią się sposobem lub kolejnością powiązania atomów lub rozmieszczeniem atomów w przestrzeni. rozróżnia się izomerię
1 1) Informacje ogólne Izomery są to związki, które maja identyczne wzory sumaryczne ale różnią się sposobem lub kolejnością powiązania atomów lub rozmieszczeniem atomów w przestrzeni. rozróżnia się izomerię
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
W29-W ZALICZENIE
 EMIA ORGANIZNA Zakres materiału lp wykład data temat 1 W1-W2 5.10.2018 klasy zw. org. alkany i cykloalkany 2 W3-W4 12.10. 2018 stereoizomeria 3 W5-W6 19.10. 2018 alkeny i cykloalkeny 4 W7-W8 26.10. 2018
EMIA ORGANIZNA Zakres materiału lp wykład data temat 1 W1-W2 5.10.2018 klasy zw. org. alkany i cykloalkany 2 W3-W4 12.10. 2018 stereoizomeria 3 W5-W6 19.10. 2018 alkeny i cykloalkeny 4 W7-W8 26.10. 2018
CHEMIA ORGANICZNA. Zakres materiału
 EMIA ORGANIZNA Zakres materiału lp wykład data temat 1 W1-W2 7.10.2015 klasy zw org alkany i cykloalkany 2 W3-W4 14.10.2015 stereoizomeria 3 W5-W6 21.10.2015 alkeny i cykloalkeny 4 W7-W8 28.10.2015 alkadieny
EMIA ORGANIZNA Zakres materiału lp wykład data temat 1 W1-W2 7.10.2015 klasy zw org alkany i cykloalkany 2 W3-W4 14.10.2015 stereoizomeria 3 W5-W6 21.10.2015 alkeny i cykloalkeny 4 W7-W8 28.10.2015 alkadieny
4. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
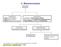 4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
-pinen (składnik terpentyny)
 ALKENY (OLEFINY) WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) WŁAŚIWOŚI FIZYZNE -pinen (składnik terpentyny) cis-trikoz-9-en (hormon płciowy
ALKENY (OLEFINY) WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) WŁAŚIWOŚI FIZYZNE -pinen (składnik terpentyny) cis-trikoz-9-en (hormon płciowy
B I O T E. p e n t a n d e k a n
 CnHn+ Węglowodory o łańcuchu prostym: B I O T E C H N O L EMIA O G ORGANICZNA I A Nomenklatura n nazwa n nazwa n nazwa n nazwa metan dodekan 9 nonakozan 90 NONAKONTAN etan tridekan 0 TRIAKONTAN 00 H E
CnHn+ Węglowodory o łańcuchu prostym: B I O T E C H N O L EMIA O G ORGANICZNA I A Nomenklatura n nazwa n nazwa n nazwa n nazwa metan dodekan 9 nonakozan 90 NONAKONTAN etan tridekan 0 TRIAKONTAN 00 H E
7-9. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
 7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
CHEMIA ORGANICZA - węglowodory. Podział węglowodorów
 EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
Alkany. Alkeny. Alkiny
 Węglowodory Alkany Alkeny Alkiny Spis treści: Podział węglowodorów. Porównanie Alkany: budowa cząsteczki, szereg homologiczny, konformacje i izomeria, nazewnictwo, właściwości fizyczne, właściwości chemiczne.
Węglowodory Alkany Alkeny Alkiny Spis treści: Podział węglowodorów. Porównanie Alkany: budowa cząsteczki, szereg homologiczny, konformacje i izomeria, nazewnictwo, właściwości fizyczne, właściwości chemiczne.
Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka
 Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
R E A K C J E E L I M I N A C J I
 E A K J E E L I M I N A J I Związki organiczne zawierające dobrą grupę odchodzącą mogą ulegać reakcji eliminacji w wyniku czego powstają alkeny: B - - - - -= + B Grupami odchodzącymi są te same jony lub
E A K J E E L I M I N A J I Związki organiczne zawierające dobrą grupę odchodzącą mogą ulegać reakcji eliminacji w wyniku czego powstają alkeny: B - - - - -= + B Grupami odchodzącymi są te same jony lub
CHEMIA ORGANICZNA. dr hab. Włodzimierz Gałęzowski Wydział Chemii UAM (61)
 EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
Slajd 1. Reakcje alkinów
 Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Konformacje cykloheksanu
 I O T E C N O L CEMI O G ORGNICZN I Konformacje cykloheksanu Konformacje cykloheksanu sposób rysowania pierścienia sześcioczłonowego Dekalina MONOPODSTWIONE pochodne cykloheksanu Konformacja krzesłowa
I O T E C N O L CEMI O G ORGNICZN I Konformacje cykloheksanu Konformacje cykloheksanu sposób rysowania pierścienia sześcioczłonowego Dekalina MONOPODSTWIONE pochodne cykloheksanu Konformacja krzesłowa
Zdzisław Głowacki. Zakres podstawowy i rozszerzony. Odpowiedzi i rozwiązania zadań. Rozdział 2. Strona Linia zadanie Jest Powinno być
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 2 Errata do drugiego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 52 Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 2 Errata do drugiego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 52 Zadanie
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Alkeny. Wzór ogólny alkenów C n H 2n. (Uwaga identyczny wzór ogólny mają cykloakany!!!)
 Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
ZASADY ZALICZENIA PRZEDMIOTU CHEMIA BIOORGANICZNA I BIOSTEREOCHEMIA
 ZASADY ZALIZENIA PZEDMIOTU EMIA BIOOGANIZNA I BIOSTEEOEMIA 35% BIOSTEEOEMIA 35% EMIA BIOOGANIZNA ELEMENTY SKŁADOWE OENY 30% SEMINAIUM ZASADY ZALIZENIA PZEDMIOTU EMIA BIOOGANIZNA I BIOSTEEOEMIA < 50% niedostateczna
ZASADY ZALIZENIA PZEDMIOTU EMIA BIOOGANIZNA I BIOSTEEOEMIA 35% BIOSTEEOEMIA 35% EMIA BIOOGANIZNA ELEMENTY SKŁADOWE OENY 30% SEMINAIUM ZASADY ZALIZENIA PZEDMIOTU EMIA BIOOGANIZNA I BIOSTEEOEMIA < 50% niedostateczna
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
ZASADY SYSTEMATYCZNEGO NAZEWNICTWA ZWIĄZKÓW ORGANICZNYCH część I. WĘGLOWODORY. 1. ALKANY i CYKLOALKANY
 ZASADY SYSTEMATYZNEG NAZEWNITWA ZWIĄZKÓW RGANIZNY część I. WĘGLWDRY 1. ALKANY i YKLALKANY Nazwy łańcuchów węglowych 1-20 : 1 - metan 6 - heksan 11 - undekan 16 - heksadekan 2 - etan 7 - heptan 12 - dodekan
ZASADY SYSTEMATYZNEG NAZEWNITWA ZWIĄZKÓW RGANIZNY część I. WĘGLWDRY 1. ALKANY i YKLALKANY Nazwy łańcuchów węglowych 1-20 : 1 - metan 6 - heksan 11 - undekan 16 - heksadekan 2 - etan 7 - heptan 12 - dodekan
Zarys Chemii Organicznej
 Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Chemia organiczna. Stereochemia. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny)
 DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
17. CH 2 CH CH 2 C CH 18. CH
 1. NAZEWNICTW ZWIĄZKÓW RGANICZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
1. NAZEWNICTW ZWIĄZKÓW RGANICZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami
 Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami I. Otrzymywanie halogenowęglowodorów 1. Reakcje halogenacji (substytucji rodnikowej halogenów (Cl, ) na
Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami I. Otrzymywanie halogenowęglowodorów 1. Reakcje halogenacji (substytucji rodnikowej halogenów (Cl, ) na
10. Alkeny wiadomości wstępne
 0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
węglowodory posiadające wiązanie podwójne (p) C=C a-pinen (składnik terpentyny)
 ALKENY (OLEFINY) węglowodory posiadające wiązanie podwójne (p) = WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) a-pinen (składnik terpentyny)
ALKENY (OLEFINY) węglowodory posiadające wiązanie podwójne (p) = WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) a-pinen (składnik terpentyny)
Wykład 1. Struktura i wiązania w cząsteczkach organicznych
 Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
NOMENKLATURA ZWIĄZKÓW ORGANICZNYCH
 MEKLATURA ZWIĄZKÓW RGAIZY AZEWITW ALKAÓW Tabela. azwy alkanów prostych o danej liczbie atomów węgla. Liczba atomów węgla metan etan propan butan pentan 6 heksan 7 heptan 8 oktan 9 nonan 0 dekan undekan
MEKLATURA ZWIĄZKÓW RGAIZY AZEWITW ALKAÓW Tabela. azwy alkanów prostych o danej liczbie atomów węgla. Liczba atomów węgla metan etan propan butan pentan 6 heksan 7 heptan 8 oktan 9 nonan 0 dekan undekan
Test sprawdzający, wielostopniowy z chemii: Węglowodory
 Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
Izomeria. isos - taki sam meros -części
 Izomeria isos - taki sam meros -części Izomery związki, które zawierają taką samą liczbę i rodzaj atomów w cząsteczce, ale różnią się sposobem ułożenia tych atomów. Mają taki sam wzór sumaryczny. 6 12
Izomeria isos - taki sam meros -części Izomery związki, które zawierają taką samą liczbę i rodzaj atomów w cząsteczce, ale różnią się sposobem ułożenia tych atomów. Mają taki sam wzór sumaryczny. 6 12
 1. NAZEWNITW ZWIĄZKÓW RGANIZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
1. NAZEWNITW ZWIĄZKÓW RGANIZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
KOLOKWIUM II - ROZWIĄZANIA Chemia organiczna B,
 KLKWIUM II - RZWIĄZANIA Chemia organiczna B, 0..008 Zad.. (0 p.) Przedstaw mechanizmy następujących reakcji. W punktach a-c należy posłużyć się wzorami przestrzennymi lub krzesłowymi. a) (R)--fenylobutan--ol
KLKWIUM II - RZWIĄZANIA Chemia organiczna B, 0..008 Zad.. (0 p.) Przedstaw mechanizmy następujących reakcji. W punktach a-c należy posłużyć się wzorami przestrzennymi lub krzesłowymi. a) (R)--fenylobutan--ol
A B C D A B C 4. D A B C D
 1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
Izomeria. isos - taki sam meros -części
 Izomeria isos - taki sam meros -części Izomery związki, które zawierają taką samą liczbę i rodzaj atomów w cząsteczce, ale różnią się sposobem ułożenia tych atomów. Mają taki sam wzór sumaryczny. 6 12
Izomeria isos - taki sam meros -części Izomery związki, które zawierają taką samą liczbę i rodzaj atomów w cząsteczce, ale różnią się sposobem ułożenia tych atomów. Mają taki sam wzór sumaryczny. 6 12
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
ZASADY SYSTEMATYCZNEGO NAZEWNICTWA ZWIĄZKÓW ORGANICZNYCH CZĘŚĆ I. WĘGLOWODORY 1. ALKANY I CYKLOALKANY
 ZASADY SYSTEMATYZEG AZEWITWA ZWIĄZKÓW GAIZY 1. ALKAY I YKLALKAY ZĘŚĆ I. WĘGLWDY azwy łańcuchów węglowych 1-20 : 1 - metan 6 - heksan 11 - undekan 16 - heksadekan 2 - etan 7 - heptan 12 - dodekan 17 - heptadekan
ZASADY SYSTEMATYZEG AZEWITWA ZWIĄZKÓW GAIZY 1. ALKAY I YKLALKAY ZĘŚĆ I. WĘGLWDY azwy łańcuchów węglowych 1-20 : 1 - metan 6 - heksan 11 - undekan 16 - heksadekan 2 - etan 7 - heptan 12 - dodekan 17 - heptadekan
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
Slajd 1. Etery i epoksydy. Slajd 2. Wprowadzenie. Wzór R-O-R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: CH 3 O CH 3 O CH 3
 Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna. Stereochemia. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
STEREOCHEMIA ORGANICZNA
 STEECEMI GNICZN Sławomir Jarosz Wykład 3 B B B B B B B B enancjomery enancjomery enancjomery enancjomery B S S S B S S B S S B S B B S B S B S S S brót o 180 Centrum pseudoasymetrii Konfiguracja względna
STEECEMI GNICZN Sławomir Jarosz Wykład 3 B B B B B B B B enancjomery enancjomery enancjomery enancjomery B S S S B S S B S S B S B B S B S B S S S brót o 180 Centrum pseudoasymetrii Konfiguracja względna
Podstawy Chemii. Zarys chemii organicznej. Dr inż. Marcin Libera
 Podstawy Chemii Zarys chemii organicznej Dr inż. Marcin Libera Zakres merytoryczny 1. Podstawowe pojęcia i prawa chemii. 2. Budowa atomu i układ okresowy pierwiastków. 3. Budowa cząsteczek (organicznych
Podstawy Chemii Zarys chemii organicznej Dr inż. Marcin Libera Zakres merytoryczny 1. Podstawowe pojęcia i prawa chemii. 2. Budowa atomu i układ okresowy pierwiastków. 3. Budowa cząsteczek (organicznych
Modele: kulkowy i czaszowy: wzór półstrukturalny: H 2 C=CH 2. Obecność wiązania podwójnego sygnalizuje końcówka nazwy "-en" Wzór strukturalny:
 Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Węglowodory poziom rozszerzony
 Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). C. alkiny D. areny
 Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Węglowodory. Michał Szewczyk Kl. IV TI
 Węglowodory Michał Szewczyk Kl. IV TI Węglowodory nasycone (Alkany) Węglowodory nasycone (Alkany)- to związki węgla z wodorem, w których pomiędzy atomami węgla występują tylko pojedyncze wiązania. Wzór
Węglowodory Michał Szewczyk Kl. IV TI Węglowodory nasycone (Alkany) Węglowodory nasycone (Alkany)- to związki węgla z wodorem, w których pomiędzy atomami węgla występują tylko pojedyncze wiązania. Wzór
11.Chemia organiczna. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu)
 11.Chemia organiczna. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Związki organiczne CHEMIA ORGANICZNA Def. 1. (Gmelin 1848, Kekule 1851 ) chemia
11.Chemia organiczna. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Związki organiczne CHEMIA ORGANICZNA Def. 1. (Gmelin 1848, Kekule 1851 ) chemia
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
Wykład 19 XII 2018 Żywienie
 Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Lista 1 (Wprowadzenie)
 Lista 1 (Wprowadzenie) 1. Dokonaj podziału reakcji na: addycję, eliminację, substytucję lub przegrupowanie: a) CH 3 Br+ KOH CH 3 OH + KBr b) CH 3 CH 2 OH H 2 C=CH 2 + H 2 O c) H 2 C=CH 2 + H 2 CH 3 CH
Lista 1 (Wprowadzenie) 1. Dokonaj podziału reakcji na: addycję, eliminację, substytucję lub przegrupowanie: a) CH 3 Br+ KOH CH 3 OH + KBr b) CH 3 CH 2 OH H 2 C=CH 2 + H 2 O c) H 2 C=CH 2 + H 2 CH 3 CH
Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze:
 Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze: Mentol w wyniku reakcji utleniania roztworem K 2 Cr 2 O 7 w środowisku kwaśnym daje związek należący do ketonów cyklicznych.
Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze: Mentol w wyniku reakcji utleniania roztworem K 2 Cr 2 O 7 w środowisku kwaśnym daje związek należący do ketonów cyklicznych.
Węglowodory Aromatyczne
 Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Stereochemia Ułożenie atomów w przestrzeni
 Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Węglowodory nienasycone
 AUTORZY SKRYPTU Szymon Michalski OPIEKUN MERYTORYCZNY mgr Adam Makówka Węglowodory nienasycone Alkeny Spis treści: 1.Określenie i wzór ogólny alkenów 2.Szereg homologiczny alkenów 3.Nazewnictwo alkenów
AUTORZY SKRYPTU Szymon Michalski OPIEKUN MERYTORYCZNY mgr Adam Makówka Węglowodory nienasycone Alkeny Spis treści: 1.Określenie i wzór ogólny alkenów 2.Szereg homologiczny alkenów 3.Nazewnictwo alkenów
Pochodne węglowodorów
 Pochodne węglowodorów 1. Pochodne węglowodorów To związki chemiczne pochodzące od węglowodorów, które w cząsteczkach oprócz węgla, wodoru mają inne pierwiastki chemiczne, np. tlen, azot, chlor. Pochodne
Pochodne węglowodorów 1. Pochodne węglowodorów To związki chemiczne pochodzące od węglowodorów, które w cząsteczkach oprócz węgla, wodoru mają inne pierwiastki chemiczne, np. tlen, azot, chlor. Pochodne
Alkohole i fenole. Opracowanie: Bartłomiej SIEPSIAK klasa 3d Opiekun: p. Teresa Gębicka
 Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
20 i 21. Eliminacja halogenków alkili
 20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
Podstawy i Metody Oceny Środowiska Pracy 2011, nr 4(70), s
 Podstawy i Metody Oceny Środowiska Pracy 2011, nr 4(70), s. 176 180 Indeks metod oznaczania najwyższych dopuszczalnych stężeń (NDS) substancji chemicznych w powietrzu oraz procedur oznaczania poziomu najwyższych
Podstawy i Metody Oceny Środowiska Pracy 2011, nr 4(70), s. 176 180 Indeks metod oznaczania najwyższych dopuszczalnych stężeń (NDS) substancji chemicznych w powietrzu oraz procedur oznaczania poziomu najwyższych
Budowa przestrzenna alkanów
 Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE
 PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
CZWARTORZĘDOWY ATOM WĘGLA CHCH 3 TRZECIORZĘDOWY ATOM WĘGLA DRUGORZĘDOWY ATOM WĘGLA
 ZASADY SYSTEMATYZNEG NAZEWNITWA ZWIĄZKÓW GANIZNY część I. Węglowodory I. WZY STUKTUALNE UPSZZNE ZWATZĘDWY ATM WĘGLA ETAN PPAN 3 3 3 3 PIEWSZZĘDWY ATM WĘGLA IZBUTAN ( 3 ) 3 TZEIZĘDWY ATM WĘGLA DUGZĘDWY
ZASADY SYSTEMATYZNEG NAZEWNITWA ZWIĄZKÓW GANIZNY część I. Węglowodory I. WZY STUKTUALNE UPSZZNE ZWATZĘDWY ATM WĘGLA ETAN PPAN 3 3 3 3 PIEWSZZĘDWY ATM WĘGLA IZBUTAN ( 3 ) 3 TZEIZĘDWY ATM WĘGLA DUGZĘDWY
R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu. F Br H 3 C
 alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
CO_05_W: Stereochemia
 CO_05_W: Stereochemia UWAGA: W tej części kursu CO_05: Stereochemia zawarto materiały i przykłady rozszerzające zagadnienia zawarte w podręcznikach: 1. H. Hart, L. E. Craine, D. J. Hart, Ch. M. Hadad Chemia
CO_05_W: Stereochemia UWAGA: W tej części kursu CO_05: Stereochemia zawarto materiały i przykłady rozszerzające zagadnienia zawarte w podręcznikach: 1. H. Hart, L. E. Craine, D. J. Hart, Ch. M. Hadad Chemia
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
DETEKTOR NIESZCZELNOŚCI GD-8
 DETEKTOR NIESZCZELNOŚCI GD-8 Przeznaczenie i ogólna charakterystyka Przenośny detektor nieszczelności GD-8 jest prostym w obsłudze, dwugazowym urządzeniem do wykrywania ulotów gazu ziemnego (CH 4 ) oraz
DETEKTOR NIESZCZELNOŚCI GD-8 Przeznaczenie i ogólna charakterystyka Przenośny detektor nieszczelności GD-8 jest prostym w obsłudze, dwugazowym urządzeniem do wykrywania ulotów gazu ziemnego (CH 4 ) oraz
10. Eliminacja halogenków alkili
 10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Wstęp do chemii organicznej - konwersatorium Baza pytań do wykorzystania.
 Wstęp do chemii organicznej - konwersatorium Baza pytań do wykorzystania. Arkusz kolokwialny powinien zawierać 30 pytań, dowolnie wybranych z bazy. Punktacja 0-14 2.0 (ndst) 15-18 3.0 (dst) 19-21 3.5 (dst+)
Wstęp do chemii organicznej - konwersatorium Baza pytań do wykorzystania. Arkusz kolokwialny powinien zawierać 30 pytań, dowolnie wybranych z bazy. Punktacja 0-14 2.0 (ndst) 15-18 3.0 (dst) 19-21 3.5 (dst+)
Rodzaje wiązań chemicznych
 Rodzaje wiązań chemicznych Teoria Lewisa (1916) atomy łączą się ze sobą przez przeniesienie (1 lub więcej) elektronów z jednego atomu na drugi wiązanie jonowe lub przez uwspólnienie par elektronowych aby
Rodzaje wiązań chemicznych Teoria Lewisa (1916) atomy łączą się ze sobą przez przeniesienie (1 lub więcej) elektronów z jednego atomu na drugi wiązanie jonowe lub przez uwspólnienie par elektronowych aby
Laboratorium. Podstawowe procesy jednostkowe w technologii chemicznej
 Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Kilka wskazówek ułatwiających analizę widm w podczerwieni
 Kilka wskazówek ułatwiających analizę widm w podczerwieni Opracowanie wg dostępnej literatury spektroskopowej: Dr Alina T. Dubis e-mail: alina@uwb.edu.pl Instytut Chemii Uniwersytet w Białymstoku Al. J.
Kilka wskazówek ułatwiających analizę widm w podczerwieni Opracowanie wg dostępnej literatury spektroskopowej: Dr Alina T. Dubis e-mail: alina@uwb.edu.pl Instytut Chemii Uniwersytet w Białymstoku Al. J.
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Materiały do zajęć dokształcających z chemii organicznej
 hemia Warta Poznania - nowa JAKŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
hemia Warta Poznania - nowa JAKŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
Alkohole i fenole Grupa funkcyjna OH
 Alkohole i fenole Grupa funkcyjna OH Alkohole - związki posiadające grupę funkcyjną "z prawdziwego zdarzenia" - grupę główną. Wiązanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale
Alkohole i fenole Grupa funkcyjna OH Alkohole - związki posiadające grupę funkcyjną "z prawdziwego zdarzenia" - grupę główną. Wiązanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale
