R E A K C J E E L I M I N A C J I
|
|
|
- Irena Dobrowolska
- 8 lat temu
- Przeglądów:
Transkrypt
1 E A K J E E L I M I N A J I Związki organiczne zawierające dobrą grupę odchodzącą mogą ulegać reakcji eliminacji w wyniku czego powstają alkeny: B = + B Grupami odchodzącymi są te same jony lub cząsteczki, które zostały omówione w reakcjach substytucji, a więc tosylanowa, halogenki, alkoksylanowa czy woda. eakcje eliminacji zachodzą pod wpływem zasad, a poniewaŝ odczynniki zasadowe mają zwykle właściwości nukleofilowe reakcje substytucji i eliminacji są wzajemnie konkurencyjne. Nu = Nu - Nu, - - eliminacja substytucja Kierunek reakcji zaleŝy zarówno od właściwości związku organicznego, właściwości odczynnika (im bardziej zasadowy tym większa tendencja do eliminacji) i warunków reakcji. eakcje eliminacji, podobnie jak substytucji mogą biec wg mechanizmu dwucząsteczkowego E eakcje eliminacji typu E B - -= + B + - W reakcjach eliminacji biegnących wg mechanizmu E szybkość reakcji zaleŝy od stęŝenia obu reagentów: eguła Zajcewa v = k[- - -]. [B - ] W produktach reakcji eliminacji halogenowodoru () z halogenków alkilowych przewaŝa bardziej rozgałęziony alken. Na + EtO = + = -bromobutan but--en (8%) but--en (9%) Na + = EtO + = -bromo--metylobutan -metylobut--en (70%) -metylobut--en (0%)
2 eakcje E zachodzą pod wpływem silnej zasady. Odrywa ona proton z atomu węgla w pozycji β, czyli z atomu sąsiadującego z atomem, do którego przyłączona jest grupa odchodząca: EtO β α β α stan przejściowy reakcji E + δ + EtO + - W stanie przejściowym, który zaistniał w wyniku ataku zasady ( ) na atom wodoru związany z β następuje rozluźnienie wiązania pomiędzy - β i α - oraz utworzenie częściowo podwójnego wiązania pomiędzy α - β. Warto zwrócić uwagę, Ŝe proton jest odrywany z pozycji trans w stosunku do grupy odchodzącej. Energia stanu przejściowego decyduje o produkcie eliminacji i racjonalnie tłumaczy regułę Zajcewa. W reakcji -bromo--metylobutanu z etanolanem sodu jest moŝliwość utworzenia dwóch struktur stanu przejściowego, w wyniku ataku zasady na proton przy lub : β α - -OEt EtO A B OEt ys.. Schemat reakcji eliminacji typu E. Preferowane jest tworzenie się alkenu bardziej rozgałęzionego, zgodnie z regułą Zajcewa, poniewaŝ stan przejściowy A jest stabilizowany przez grupy alkilowe, a B tylko przez dwie Osiągnięcie stanu przejściowego B wymaga większej energii aktywacji, jest więc mniej prawdopodobne.
3 Przykłady reakcji eliminacji (orientacja reakcji dehydrohalogenacji: KO KO l = l EtO EtO -chloropropan propen -chloropropan (chlorek n-propylu) (chlorek izopropylu) KO l = EtO -chlorobutan (chlorek n-butylu) but--en KO l = + = EtO -chlorobutan (chlorek sec-butylu) but--en (80%) but--en (0%) KO = + = EtO -bromopentan pent--en (7%) pent--en (9%) -- = + = EtO -bromo--metylobutan -metylobut--en (69%) -metylobut--en (%) Na wydajność określonego produktu alkenu wpływa nie tylko trwałość produktu pośredniego (tym samym danego alkenu), ale równieŝ liczba i reaktywność (kwasowość) atomów ulegających oderwaniu. eaktywność atomów wodoru w reakcjach eliminacji Tabela Substrat produkt Względna szybkość Względna szybkość w przeliczeniu na atom - =,0,0 (cztery ) =, 5,0 (dwa ) - = 9,,7 (sześć ) ( ) ( ) 0 0 (dziewięć ) Wraz ze wzrostem rzędowości atomów, z którymi związany jest halogen rośnie kwasowość wodorów na sąsiadujących atomach węgla, a tym samym ich reaktywność w reakcjach eliminacji E, równocześnie ten czynnik (rzędowość atomów ) sprzyja powstawaniu bardziej rozgałęzionych alkenów. eaktywność halogenków alkilowych w reakcjach dehydrohalogenacji rośnie wraz ze wzrostem ich rzędowości: o < o < o.
4 eakcje eliminacji halogenowodorów ze związków chiralnych Produkty reakcji eliminacji bromowodoru z -bromo-,-difenylopropanu zaleŝą od konfiguracji substratu. Ze stereoizomerów (,) i (S,S) otrzymuje się cis-,-difenylopropen, podczas gdy z (S,) i (,S) powstaje trans-,-difenylopropen. (,) (S,S) -bromo-,-difenylopropan cis-,-difenylopropen (S,) (,S) -bromo-,-difenylopropan tras-,-difenylopropen PowyŜsza zaleŝność wynika z preferencji konformacyjnej stanu pośredniego reakcji E. Naładowana ujemnie zasada odrywająca proton moŝe zbliŝyć się do cząsteczki organicznej z przeciwnej strony do grupy odchodzącej, gdyŝ ona ma teŝ ładunek ujemny (cząstkowy). Najdogodniejszą konformacją dla takiego układu będzie konformacja antyperiplanarna, gdyŝ jest to konformacja najbardziej uprzywilejowana ze względu energetycznego, a atom odrywany przez zasadę B - znajduje się w pozycji najbardziej oddalonej od grupy odchodzącej. zasada zasada konformacja antiperiplanarna (naprzemianległa) korzystna energetycznie konformacja synperiplanarna (naprzeciwległa) niekorzystna energetycznie ys. Konformacja substratu w trakcie eliminacji typu E
5 B: B δ + B- + : - zasada atakuje proton stan przejściowy alken ys. chanizm reakcji E PowyŜsze wyjaśnienia ułatwiają zrozumienie dlaczego z (S,)- i (,S)--bromo-,- difenylopropanu powstaje (E)-,-difenylopropen, a z (,)- i (S,S)--bromo-,- difenylopropanu tworzy się (Z)-,-difenylopropen. (S,) (,S) -bromo-,-difenylopropan tras-,-difenylopropen W projekcji perspektywicznej cząsteczki widać wyraźnie, Ŝe eliminacja cząsteczki z (S,)--bromo-,-difenylopropanu prowadzi do izomeru E. Ten sam produkt powstaje w trakcie eliminacji cząsteczki z jego enancjomeru - (,S): :B (S,)--bromo-,-difenylopropan tras-,-difenylopropen Zaś z enancjomerów (,) i (S,S)--bromo-,-difenylopropanu powstaje (Z)-,- difenylopropen: (,) (S,S) -bromo-,-difenylopropan cis-,-difenylopropen :B
6 eakcje eliminacji typu E Z chlorku t-butylu w roztworze wodnym zawierającym etanol (ułatwiający rozpuszczenie) powstaje zarówno t-butanol jak i -metylopropen. Wiadomo, Ŝe alkohol powstaje wg mechanizmu S N, a jak tworzy się alken, kiedy w środowisku nie ma silnej zasady? O/EtO l O + + l 60 o chlorek tert-butylu alkohol tert-butylowy -metylopropen (6%) (-chloro--metylopropan) (-metylopropan--ol) (6%) Dla obu produktów szybkość reakcji zaleŝy jedynie od stęŝenia chlorku t-butylu, a więc i - metylopropen powstaje wg mechanizmu reakcji eliminacji jednocząsteczkowej, określanej typem E. chanizm reakcji: v = k[-] l dysocjacja,etap najwolniejszy l O.. O.. + O: + O O tert-butanol, S N -metylopropen Eliminacji typu E ulegają przede wszystkim halogenki o, wolniej ale równieŝ drugorzędowe w środowisku niezbyt zasadowym. Pod wpływem silnych zasad dochodzi do E nawet dla halogenków o, pod warunkiem, Ŝe będą spełnione warunki stereochemiczne moŝliwość ułoŝenia się atomu wodoru i grupy odchodzącej w konformacji antyperiplanarnej. Taką moŝliwość obserwuje się w trakcie eliminacji l z chlorku mentylu. Grupa izopropylowa tego związku wymusza znaczną przewagę konformeru, w którym izopropyl zajmuje pozycję ekwatorialną. W tej pozycji nie ma moŝliwości antyperiplanarnego ułoŝenia się i l, wobec czego eliminacja l biegnie bardzo wolno. Jest ona moŝliwa tylko dla nielicznie reprezentowanej populacji konformerów, w których izopropyl zajmuje pozycję akcjalną: E
7 ( ) l chlorek mentylu ułoŝenie trans-diekwatorialne 00 o b. wolno ( ) szybko ment--en ( ) ( ) l szybko ułoŝenie trans-diaksjalne (antyperyplanarne) ys. Eliminacja l z chlorku mentylu zachodzi bardzo wolno poniewaŝ biegnie z udziałem niekorzystnej energetycznie konformacji W stereoizomerycznym chlorku neomentylu reakcja eliminacji jest znacznie szybsza, poniewaŝ w uprzywilejowanym konformerze atomy i l znajdują się w ułoŝeniu antyperyplanarnym. Głównym produktem eliminacji jest ment--en, poniewaŝ atom przy jest bardziej kwaśny niŝ ten przy, a przez to bardziej podatny na oderwanie przez zasadę. l ( ) ułoŝenie trans-diaksjalne (antyperyplanarne) chlorek neopentylu szybko ( ) ment--en ( ) ment--en produkt główny ys. Eliminacja cząsteczki l z chlorku neomentylu biegnie szybko mechanizmem E Eliminacja cząsteczki l z chlorku mentylu pod wpływem etanolanu biegnie wg mechanizmu E, do czego potrzebne jest antyperyplanarne ułoŝenie atomów i l. W lekko zasadowym środowisku eliminację l z chlorku mentylu teŝ się obserwuje, biegnie ona jednak mechanizmem E (szybkość reakcji zaleŝy jedynie od stęŝenia chlorku mentylu), jest ona bardzo wolna, a w produktach znajdują się zarówno ment--en, jak i ment--en. eakcja biegnie dwuetapowo, przy czym w pierwszy etapie po dysocjacji l - powstaje karbokation przy, a ten z kolei stabilizuje się przez oderwanie protonu od lub. PoniewaŜ atom przy ( o ) jest bardziej ruchliwy (b. kwaśny) głównym produktem, zgodnie z regułą Zajcewa, jest ment--en.
8 ( ) l, 0,0 M EtO/O + ( ) ( ) + ( ) ment--en (68%) ment--en (%) ys. Eliminacja l z chlorku mentylu w środowisku słabo zasadowym biegnie wg mechanizmu E Eliminacja typu E zaczynająca się dysocjacją l - konformacyjnych. nie ma specjalnych wymagań Porównanie reakcji substytucji nukleofilowej i eliminacji eakcje substytucji nukleofilowej S N i eliminacji E są reakcjami konkurencyjnymi. O kierunku reakcji decyduje budowa związku organicznego (rzędowość atomu w centrum reakcji), właściwości odczynnika reagującego (nukleofilowość/zasadowść), rodzaj rozpuszczalnika i inne warunki reakcji. Pierwszorzędowe halogenki alkilowe reagują głównie wg mechanizmu S N i E poniewaŝ: w ataku odczynnika nie przeszkadzają duŝe podstawniki; trudno ulegają dysocjacji do karbokationu; o kierunku reakcji decyduje nukleofilowość odczynnika, silnie nukleofilowe preferują substytucję, silne zasady wymuszają eliminację: silny nukleofil - bromek n-butylu mocna zasada NaN TF/MPA t-buok -N pentanonitryl (90%) = but--en (85%) ys. omek n-butylu w zaleŝności od reagenta ulega reakcji S N z NaN (silnym nukleofilem) lub E z t-buok (silna zasadą) Drugorzędowe halogenki alkilowe ulegają substytucji nukleofilowej i to zarówno wg mechanizmu S N i S N oraz eliminacji, takŝe wg obu mechanizmów E i E, poniewaŝ mają pośrednie właściwości pomiędzy halogenkami o i o.
9 mocna zasada bromek izopropylu słaba zasada, silny nukleofil EtONa EtO AcONa O- = + propen eter etylowo-izopropylowy (80%) (0%) OAc = + propen octan izopropylu (0%) (00%) ys. omek izopropylu w reakcji z etanolanem sodu (silna zasada, ale słabsza od t-buok) ulega głównie eliminacji, a w mniejszym stopniu substytucji do eteru, natomiast z silnym nukleofilem jakim jest octan sodu zachodzi wyłącznie substytucja Trzeciorzędowe halogenki alkilowe w zaleŝności od reagentów i warunków ulegają substytucji S N lub eliminacji, przy czym moŝe to być eliminacja E lub E. W reakcji eliminacji o halogenków nie przeszkadza zawada przestrzenna przy atomie związanym z halogenem, poniewaŝ zasada odrywa proton z sąsiedniego atomu węgla. Silne zasady w reakcji z o halogenkami alkilowymi wymuszają eliminację, przy czym biegnie ona zarówno wg mechanizmu E, jak i E; im silniejsza zasada tym większy udział eliminacji typu E. mocna zasada bromek t-butylu EtONa EtO EtO O- + eter t-butylowo-etylowy propen (%) (97%) O- + eter t-butylowo-etylowy propen (80%) (0%) ys. Trzeciorzędowy halogenek jakim jest bromek t-butylu pod działaniem etanolanu sodu ulega głównie reakcji eliminacji (E), w samym alkoholu przewaŝa co prawda substytucja S N, której towarzyszy eliminacja E, ale reakcja jest wolna, wymaga ogrzewania w celu zwiększenia jej szybkości Porównanie reaktywności halogenków alkilowych Tabela zędowość Typ reakcji - S N S N E E o - główny proces pod wpływem silnych nukleofili - główny proces pod wpływem silnych zasad o zachodzi podczas solwolizy w polarnym rozpuszczalniku o główny proces pod wpływem silnych nukleofili, będących słabymi zasadami, biegnie w rozpuszczalnikach polarnych główny proces pod wpływem silnych nukleofili, w polarnym aprotycznym rozpuszczalniku zachodzi podczas solwolizy w polarnym rozpuszczalniku - zachodzi podczas solwolizy główny proces pod wpływem silnych główny proces pod wpływem silnych
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
RJC Y R R Y R R R H R H. Slides 1 to 24
 JC eakcje Eliminacji (E1 & E2) B δ B δ B Slides 1 to 24 JC eakcje Eliminacji Dwa mechanizmy są moŝliwe wtedy, kiedy zasada (B - ) atakuje halogenek alkilowy z atomem w pozycji α; ; zachodząca reakcja eliminacji
JC eakcje Eliminacji (E1 & E2) B δ B δ B Slides 1 to 24 JC eakcje Eliminacji Dwa mechanizmy są moŝliwe wtedy, kiedy zasada (B - ) atakuje halogenek alkilowy z atomem w pozycji α; ; zachodząca reakcja eliminacji
R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu. F Br H 3 C
 alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
alogenoalkany (by Aleksandra Kołodziejczyk, UG) R-X X = halogen Nazewnictwo: podstawnik halogenowy w szkielecie alkanu lub halogenek alkilu/arylu 3 I jodometan (jodek metylu) F 3 3 fluorocykloheksan (fluorek
10. Eliminacja halogenków alkili
 10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
20 i 21. Eliminacja halogenków alkili
 20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Halogenki alkilowe RX
 alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
alogenki alkilowe X Nazewnictwo halogenków alkilowych 1. Znajdź i nazwij łańcuch macierzysty. Tak jak przy nazywaniu alkanów, wybierz najdłuższy łańcuch. Jeżeli w cząsteczce obecne jest wiązanie podwójne
Stereochemia Ułożenie atomów w przestrzeni
 Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka
 Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
ALKENY WĘGLOWODORY NIENASYCONE
 Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami
 Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami I. Otrzymywanie halogenowęglowodorów 1. Reakcje halogenacji (substytucji rodnikowej halogenów (Cl, ) na
Materiał powtórzeniowy do sprawdzianu - halogenowęglowodory + przykładowe zadania z rozwiązaniami I. Otrzymywanie halogenowęglowodorów 1. Reakcje halogenacji (substytucji rodnikowej halogenów (Cl, ) na
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
3. Wprowadzenie do nazewnictwa związków organicznych
 3. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową (C
3. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową (C
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Slajd 1. Wstęp do chemii organicznej. Nomenklatura, własności fizyczne, struktura. eter. mapa potencjału elektrostatycznego cząsteczki eteru etylowego
 Slajd 1 Wstęp do chemii organicznej Nomenklatura, własności fizyczne, struktura hybrydyzacja sp 3 eter mapa potencjału elektrostatycznego cząsteczki eteru etylowego Slajd 2 Alkany to węglowodory zawierające
Slajd 1 Wstęp do chemii organicznej Nomenklatura, własności fizyczne, struktura hybrydyzacja sp 3 eter mapa potencjału elektrostatycznego cząsteczki eteru etylowego Slajd 2 Alkany to węglowodory zawierające
Mechanizm dehydratacji alkoholi
 Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Węglowodory poziom rozszerzony
 Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
4-6. Wprowadzenie do nazewnictwa związków organicznych
 4-6. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową
4-6. Wprowadzenie do nazewnictwa związków organicznych 1 3.1. omologia i izomeria konstytucyjna omologi związki z tej samej klasy, każdy związek różni się od swego poprzednika o jedną grupę metylenową
Zarys Chemii Organicznej
 Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
A B C D A B C 4. D A B C D
 1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
1. Kartkówka, 21 października 2015; zestaw Imię i azwisko: Zad. 1. (1 p) Wśród podanych związków,, i D, wszystkie atomy węgla występują w tym samym stanie hybrydyzacji w związkach: i i D 3. i 4. i D Zad.
R 4 R 1 R 4 R 1 R R 2 = R 3 R 1 R 2 R 2 R 1 R 3 R 1 R 3 R 3 R 3 R 1 H R 1 H R 1 R 4. Zakład Chemii Organicznej: kopiowanie zabronione.
 Witam Państwa 1. Poniżej zamieszczam poprawne odpowiedzi zarówno części testowej jak i reakcji z dodatkowymi komentarzami. 2. Proszę nie uczyć się odpowiedzi do testu na pamięć (bo już raczej taki test
Witam Państwa 1. Poniżej zamieszczam poprawne odpowiedzi zarówno części testowej jak i reakcji z dodatkowymi komentarzami. 2. Proszę nie uczyć się odpowiedzi do testu na pamięć (bo już raczej taki test
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Laboratorium. Podstawowe procesy jednostkowe w technologii chemicznej
 Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Wykład 1. Struktura i wiązania w cząsteczkach organicznych
 Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
Zdzisław Głowacki. Zakres podstawowy i rozszerzony. Odpowiedzi i rozwiązania zadań. Rozdział 2. Strona Linia zadanie Jest Powinno być
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 2 Errata do drugiego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 52 Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 2 Errata do drugiego rozdziału ćwiczeń: Strona Linia zadanie Jest Powinno być Str. 52 Zadanie
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
-pinen (składnik terpentyny)
 ALKENY (OLEFINY) WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) WŁAŚIWOŚI FIZYZNE -pinen (składnik terpentyny) cis-trikoz-9-en (hormon płciowy
ALKENY (OLEFINY) WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) WŁAŚIWOŚI FIZYZNE -pinen (składnik terpentyny) cis-trikoz-9-en (hormon płciowy
KOLOKWIUM II - ROZWIĄZANIA Chemia organiczna B,
 KLKWIUM II - RZWIĄZANIA Chemia organiczna B, 0..008 Zad.. (0 p.) Przedstaw mechanizmy następujących reakcji. W punktach a-c należy posłużyć się wzorami przestrzennymi lub krzesłowymi. a) (R)--fenylobutan--ol
KLKWIUM II - RZWIĄZANIA Chemia organiczna B, 0..008 Zad.. (0 p.) Przedstaw mechanizmy następujących reakcji. W punktach a-c należy posłużyć się wzorami przestrzennymi lub krzesłowymi. a) (R)--fenylobutan--ol
Wykład 7. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 7 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Otrzymywanie węglowodorów aromatycznych 1. z katalitycznego reformingu (frakcje C 6 -C 10 ) 2. synteza alkilowych pochodnych
Wykład 7 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Otrzymywanie węglowodorów aromatycznych 1. z katalitycznego reformingu (frakcje C 6 -C 10 ) 2. synteza alkilowych pochodnych
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
Slajd 1. Reakcje alkinów
 Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
10. Alkeny wiadomości wstępne
 0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
węglowodory posiadające wiązanie podwójne (p) C=C a-pinen (składnik terpentyny)
 ALKENY (OLEFINY) węglowodory posiadające wiązanie podwójne (p) = WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) a-pinen (składnik terpentyny)
ALKENY (OLEFINY) węglowodory posiadające wiązanie podwójne (p) = WZÓR SUMARYZNY n 2n - alkeny łańcuchowe; n 2n-2 - alkeny cykliczne (cykloalkeny) etylen (produkcja polietylenu) a-pinen (składnik terpentyny)
+ CHCl 3. Cl + CH 2. + HCl nadmiar
 . REAKJE SUBSTYTUJI A. Kołodziejczyk 007.. W reakcji metanu z chlorem w obecności światła lub w podwyższonej temperaturze tworzą się produkty, w których atom (atomy) wodoru zostają zastąpione przez atom
. REAKJE SUBSTYTUJI A. Kołodziejczyk 007.. W reakcji metanu z chlorem w obecności światła lub w podwyższonej temperaturze tworzą się produkty, w których atom (atomy) wodoru zostają zastąpione przez atom
CH 3 OH C 2 H 5 OH H 3 C CH 2 CH 2 OH H 3 C CH CH 3 OH metanol etanol propan-1-ol propan-2-ol H 2 C CH 2 OH OH H 2 C CH CH 2 OH OH OH
 Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
4. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
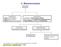 4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
Substytucja nukleofilowa
 Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
Substytucja nukleofilowa Katarzyna strowska eakcja podstawienia nukleofilowego polega na wymianie grupy X związanej z atomem węgla na odczynnik nukleofilowy. Podstawnikiem X jest przeważnie grupa elektronoakceptorowa,
7-9. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
 7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny)
 DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
DIENY węglowodory łańcuchowe lub cykliczne posiadające dwa wiązania podwójne C=C KLASYFIKACJA DIENY SKUMULOWANE alleny (kumuleny) 2 C C C 2 2 C C C C C 3 propa-1,2-dien penta-1,2,3-trien DIENY IZOLOWANE
Konspekt wykładu Chemia Organiczna dla studentów Wydziału Inżynierii Chemicznej i Procesowej
 Konspekt wykładu hemia Organiczna dla studentów Wydziału Inżynierii hemicznej i Procesowej ALKANY 2 godz. 1. Wzór sumaryczny: n 2n+2 (n = liczba naturalna) - węglowodory posiadające tylko wiązania pojedyncze
Konspekt wykładu hemia Organiczna dla studentów Wydziału Inżynierii hemicznej i Procesowej ALKANY 2 godz. 1. Wzór sumaryczny: n 2n+2 (n = liczba naturalna) - węglowodory posiadające tylko wiązania pojedyncze
Wskaż grupy reakcji, do których można zaliczyć proces opisany w informacji wstępnej. A. I i III B. I i IV C. II i III D. II i IV
 Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
17. CH 2 CH CH 2 C CH 18. CH
 1. NAZEWNICTW ZWIĄZKÓW RGANICZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
1. NAZEWNICTW ZWIĄZKÓW RGANICZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Wyznaczanie stałej szybkości reakcji wymiany jonowej
 Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Slajd 1. Etery i epoksydy. Slajd 2. Wprowadzenie. Wzór R-O-R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: CH 3 O CH 3 O CH 3
 Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Narysuj stereoizomery cis i trans dla 1,2-dibromocyklobutanu. Czy ulegają one wzajemnej przemianie, odpowiedź uzasadnij.
 WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Izomerię konstytucyjną można podzielić na podgrupy a) izomeria szkieletowa, która polega na różnej budowie szkieletu węglowego cząsteczek Przykład:
 1 1) Informacje ogólne Izomery są to związki, które maja identyczne wzory sumaryczne ale różnią się sposobem lub kolejnością powiązania atomów lub rozmieszczeniem atomów w przestrzeni. rozróżnia się izomerię
1 1) Informacje ogólne Izomery są to związki, które maja identyczne wzory sumaryczne ale różnią się sposobem lub kolejnością powiązania atomów lub rozmieszczeniem atomów w przestrzeni. rozróżnia się izomerię
Kolokwium z SUBSTYTUCJI NUKLEOFILOWEJI, ELIMINACJI, ADDYCJI Autorzy: A. Białońska, M. Kijewska
 Kolokwium z SUBSTYTUCJI NUKLEFILWEJI, ELIMINACJI, ADDYCJI Autorzy: A. Białońska, M. Kijewska Wersja A czas: 45 minut Imię i nazwisko Kierunek studiów Nazwisko prowadzącego Data Skala ocen: ndst 0 20, dst
Kolokwium z SUBSTYTUCJI NUKLEFILWEJI, ELIMINACJI, ADDYCJI Autorzy: A. Białońska, M. Kijewska Wersja A czas: 45 minut Imię i nazwisko Kierunek studiów Nazwisko prowadzącego Data Skala ocen: ndst 0 20, dst
Alkeny. Wzór ogólny alkenów C n H 2n. (Uwaga identyczny wzór ogólny mają cykloakany!!!)
 Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
Chemia organiczna. Chemia organiczna. Podręczniki
 Chemia organiczna prof. dr hab. Danuta Kalemba, p. 205 konsultacje wt. 12 15-13, 14 15-15 sem. II sem. III sem.iv Wykład: 30 15 Ćwiczenia: 15 15 Laboratorium: 60 Zaliczenie Egzamin Zaliczenie Chemia organiczna
Chemia organiczna prof. dr hab. Danuta Kalemba, p. 205 konsultacje wt. 12 15-13, 14 15-15 sem. II sem. III sem.iv Wykład: 30 15 Ćwiczenia: 15 15 Laboratorium: 60 Zaliczenie Egzamin Zaliczenie Chemia organiczna
Chemia organiczna. prof. dr hab. Danuta Kalemba, p. 205 konsultacje wt , sem. II sem. III sem.iv Wykład: 30 15
 Chemia organiczna prof. dr hab. Danuta Kalemba, p. 205 konsultacje wt. 12 15-13, 14 15-15 sem. II sem. III sem.iv Wykład: 30 15 Ćwiczenia: 15 15 Laboratorium: 60 Zaliczenie Egzamin Zaliczenie 1 Chemia
Chemia organiczna prof. dr hab. Danuta Kalemba, p. 205 konsultacje wt. 12 15-13, 14 15-15 sem. II sem. III sem.iv Wykład: 30 15 Ćwiczenia: 15 15 Laboratorium: 60 Zaliczenie Egzamin Zaliczenie 1 Chemia
EGZAMIN WSTĘPNY NA STUDIUM DOKTORANCKIE W CBMIM PAN W ŁODZI. Zestaw pytań z chemii organicznej
 EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
Budowa przestrzenna alkanów
 Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
 1. NAZEWNITW ZWIĄZKÓW RGANIZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
1. NAZEWNITW ZWIĄZKÓW RGANIZNY węglowodory nasycone: alkany, cykloalkany węglowodory nienasycone: alkeny, alkiny, cykloalkeny Podać nazwy systematyczne następujących węglowodorów, uwzględnić izomerię:
Węglowodory poziom podstawowy
 Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Kartkówka nr 1 Imię i Nazwisko:.. Nr albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1.
 Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
Kartkówka nr 1 Imię i azwisko:.. r albumu 1) Wskaż indywiduum chemiczne, w którym cząstkowy ładunek na atomie tlenu wynosi -1. b) 3 C 3 c) 1 i 3 d) 2 i 2) Wskaż indywiduum chemiczne, w którym suma ładunków
CHEMIA ORGANICZA - węglowodory. Podział węglowodorów
 EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE
 PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
8. Delokalizacja elektronów i reaktywność dienów sprzężonych
 8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
REAKCJE SUBSTYTUCJI. + CHCl 3. Cl + CH 2. + HCl nadmiar
 REAKJE SUBSTYTUJI W reakcji metanu z chlorem w obecno ci wiat a lub w podwy szonej temperaturze tworz si produkty, w których atom (atomy) wodoru zostaj zast pione przez atom (atomy) chloru. Powstaj chloroalkany
REAKJE SUBSTYTUJI W reakcji metanu z chlorem w obecno ci wiat a lub w podwy szonej temperaturze tworz si produkty, w których atom (atomy) wodoru zostaj zast pione przez atom (atomy) chloru. Powstaj chloroalkany
MODEL ODPOWIEDZI I SCHEMAT OCENIANIA ARKUSZA II
 MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
MDEL DPWIEDZI I SEMAT ENIANIA ARKUSZA II. Zdający otrzymuje punkty tylko za całkowicie prawidłową odpowiedź.. Gdy do jednego polecenia są dwie odpowiedzi (jedna prawidłowa, druga nieprawidłowa), to zdający
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
ALKANY (by Aleksandra Kołodziejczyk, UG) Węglowodory: - nasycone = alkany - nienasycone (alkeny, alkiny)
 ALKANY (by Aleksandra Kołodziejczyk, UG) Węglowodory: - nasycone = alkany - nienasycone (alkeny, alkiny) C n n+, brak gr. funkcyjnych. Alkany: - nierozgałęzione; - rozgałęzione; - cykliczne. Związki homologiczne
ALKANY (by Aleksandra Kołodziejczyk, UG) Węglowodory: - nasycone = alkany - nienasycone (alkeny, alkiny) C n n+, brak gr. funkcyjnych. Alkany: - nierozgałęzione; - rozgałęzione; - cykliczne. Związki homologiczne
+ HCl + + CHLOROWCOWANIE
 CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
Zadanie: 2 (4 pkt) Napisz, uzgodnij i opisz równania reakcji, które zaszły w probówkach:
 Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Wykład 1. Struktura i wiązania w cząsteczkach organicznych
 Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
Wykład 19 XII 2018 Żywienie
 Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2
![liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2 liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2](/thumbs/65/54124071.jpg) Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). C. alkiny D. areny
 Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Budowa. Wiązanie C - H C - F C - Cl C - Br C - I. Długość [pm] Energia [kj/mol] X - atom fluorowca
![Budowa. Wiązanie C - H C - F C - Cl C - Br C - I. Długość [pm] Energia [kj/mol] X - atom fluorowca Budowa. Wiązanie C - H C - F C - Cl C - Br C - I. Długość [pm] Energia [kj/mol] X - atom fluorowca](/thumbs/93/112104916.jpg) B I T E N L EMIA G RGANIZNA I A Budowa Fluorowcopochodne zawierające atom fluorowca związany z atomem węgla sp 3 mają budowę przestrzenną zbliżoną do budowy węglowodorów. Wiązanie węgiel - fluorowiec utworzone
B I T E N L EMIA G RGANIZNA I A Budowa Fluorowcopochodne zawierające atom fluorowca związany z atomem węgla sp 3 mają budowę przestrzenną zbliżoną do budowy węglowodorów. Wiązanie węgiel - fluorowiec utworzone
MECHANIZMY FRAGMENTACJI ZWIĄZKÓW ORGANICZNYCH. Copyright 2003 Witold Danikiewicz
 MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
MECANIZMY FAGMENTACJI ZWIĄZKÓW GANICZNYC Copyright 2003 Cechy charakterystyczne zjawiska fragmentacji jonów proces jednocząsteczkowy; szybkość fragmentacji jest mała w porównaniu z szybkością rozpraszania
RJC A-B A + B. Slides 1 to 27
 Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
CHEMIA POZIOM ROZSZERZONY Nowa formuła
 WYDZIAŁ EMII EMIA PZIM RZSZERZNY Nowa formuła RZWIĄZANIA ZADAŃ I SEMAT PUNKTWANIA kwiecień 2016 dpowiedzi: Zadanie 1. (0 1) Poprawna odpowiedź: 32 Ge 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 2 1 p. za poprawny
WYDZIAŁ EMII EMIA PZIM RZSZERZNY Nowa formuła RZWIĄZANIA ZADAŃ I SEMAT PUNKTWANIA kwiecień 2016 dpowiedzi: Zadanie 1. (0 1) Poprawna odpowiedź: 32 Ge 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 10 4p 2 1 p. za poprawny
Chemia ogólna nieorganiczna Wykład XII Kinetyka i statyka chemiczna
 Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
Chemia ogólna nieorganiczna Wykład 10 14 XII 2016 Kinetyka i statyka chemiczna Elementy kinetyki i statyki chemicznej bada drogi przemiany substratów w produkty szybkość(v) reakcji chem. i zależność od
RJC # Defin i i n c i ja
 Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Klasyfikacja i przykłady ETERY
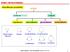 ETERY I EPKSYZWIĄZKI Klasyfikacja i przykłady ETERY acykliczne R--R cykliczne trójczłonowe czteroczłonowe pięcioczłonowe sześcioczłonowe tlenek etylenu (oksiran) oksetan tetrahydrofuran tetrahydropiran
ETERY I EPKSYZWIĄZKI Klasyfikacja i przykłady ETERY acykliczne R--R cykliczne trójczłonowe czteroczłonowe pięcioczłonowe sześcioczłonowe tlenek etylenu (oksiran) oksetan tetrahydrofuran tetrahydropiran
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
KONDUKTOMETRIA. Konduktometria. Przewodnictwo elektrolityczne. Przewodnictwo elektrolityczne zaleŝy od:
 KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze:
 Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze: Mentol w wyniku reakcji utleniania roztworem K 2 Cr 2 O 7 w środowisku kwaśnym daje związek należący do ketonów cyklicznych.
Zadanie 1. (1 pkt) Zapach mięty pochodzi od mentolu, alkoholu o uproszczonym wzorze: Mentol w wyniku reakcji utleniania roztworem K 2 Cr 2 O 7 w środowisku kwaśnym daje związek należący do ketonów cyklicznych.
Alkany i Cykloalkany C n H 2n+2
 Alkany i Cykloalkany C n H 2n+2 C n H 2n Alkany - węglowodory nasycone RH węglowodory ponieważ składają się jedynie z atomów C i H nasycone, bo zawierają jedynie pojedyncze wiązania C C i tym samym mają
Alkany i Cykloalkany C n H 2n+2 C n H 2n Alkany - węglowodory nasycone RH węglowodory ponieważ składają się jedynie z atomów C i H nasycone, bo zawierają jedynie pojedyncze wiązania C C i tym samym mają
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
