Chemia organiczna. Stereochemia. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
|
|
|
- Szymon Bronisław Kurek
- 7 lat temu
- Przeglądów:
Transkrypt
1 Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
2 Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami związków (organicznych). Ta część chemii organicznej, która dotyczy trójwymiarowej struktury cząsteczki nazywa się stereochemią. Izomery (gr. isos równy) związki mające ten sam wzór sumaryczny, ale odmienne właściwości fizyczne i chemiczne. Izomery są różnymi związkami mają odmienną strukturę cząsteczek 2
3 alkohol etylowy eter dimetylowy H H H H H C C O H H C O C H H H H H wzór sumaryczny C 2 H 6 O masa cząsteczkowa 46 alkohol etylowy eter dimetylowy temperatura wrzenia 78 o C - 24 o C stan skupienia ciecz gaz reakcja z HI C 2 H 6 I CH 3 I reakcja z Na met. C 2 H 6 ONa - cis-2-buten temp. wrz. +4 o C trans-2-buten temp. wrz. +1 o C 3
4 IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjna Konformacyjna Konfiguracja absolutna DL Optyczna Ukladów łańcuchowych Geometryczna Układów cyklicznych 4
5 Izomeria konstytucyjna izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjna Konformacyjna Konfiguracja absolutna DL Optyczna Ukladów łańcuchowych Geometryczna Układów cyklicznych 5
6 Izomeria konstytucyjna IZOMERIA Izomeria łańcuchowa izomery tworzą łańcuchy proste i rozgałęzione KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych Łańcuchowa Grup funkcyjnych Położenia STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Konfiguracyjna Optyczna Konformacyjna Ukladów łańcuchowych Konfiguracja absolutna DL Geometryczna Układów cyklicznych 6
7 Izomeria konstytucyjna IZOMERIA Łańcuchowa Izomeria grup funkcyjnych: cząsteczka zawiera różne grupy funkcyjne zbudowane z atomów tych samych pierwiastków KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych Grup funkcyjnych Położenia STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Konfiguracyjna Optyczna Geometryczna Konformayjna Ukladów łańcuchowych Układów cyklicznych Konfiguracja absolutna DL aldehyd glicerynowy dihydroksyaceton 7
8 Izomeria konstytucyjna Izomeria położenia: różne położenia podstawników w łańcuchu lub pierścieniu KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych Łańcuchowa Grup funkcyjnych Położenia IZOMERIA STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Konfiguracyjna Konformacyjna Konfiguracja absolutna DL C1 C6 Optyczna Ukladów łańcuchowych Geometryczna Układów cyklicznych fosfoglukomutaza glukozo-1-fosforan glukozo-6-fosforan bezpośredni produkt odszczepiania cząsteczki glukozy z glikogenu przez glikogenofosforylazę glikogenową 8
9 Stereoizomeria poszczególne stereoizomery różnią się sposobem rozmieszczenia atomów w przestrzeni (przy identycznej kolejności łączenia się tych atomów ze sobą) IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjna Konformacyjna Konfiguracja absolutna DL Optyczna Ukladów łańcuchowych Geometryczna Układów cyklicznych 9
10 Stereoizomeria IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjna Konformacyjna Konfiguracja absolutna DL Stereoizomeria konfiguracyjna: izomery różnią się przestrzennym położeniem wiązań kowalencyjnych. Stereoizomeria konformacyjna izomery różnią się wzajemnym położeniem grup funkcyjnych, w wyniku rotacji podstawników wokół wiązania. Optyczna Geometryczna Ukladów łańcuchowych Układów cyklicznych 10
11 Czynność optyczna substancję określa się jako optycznie czynną, jeżeli wykazuje ona zdolność skręcania płaszczyzny polaryzacji światła. Światło spolaryzowane jest to światło, którego drgania zachodzą tylko w jednej z wielu możliwych płaszczyzn (np. po przejściu przez soczewkę polaryzacyjną lub pryzmat Nicola). Jean Baptiste Biot odkrył zjawisko czynności optycznej (1815 r.) Louis Pasteur roztwory kryształów tego samego związku mogą się różnić skręcalnościa optyczną. Istnieją zatem izomery, które różnią się jedynie tym, że jeden stanowi lustrzane odbicie drugiego. Skręcają one płaszczyznę polaryzacji światła w przeciwnych kierunkach. Polarymetr urządzenie służące do wykrywania oraz pomiaru stopnia skręcalności płaszczyzny światła spolaryzowanego 11
12 Czynność optyczna substancję określa się jako optycznie czynną, jeżeli wykazuje ona zdolność skręcania płaszczyzny polaryzacji światła. fale świetlne drgają we wszystkich kierunkach fale świetlne drgają w jednej płaszczyźnie kierunek przechodzenia światła płaszczyzna światła spolaryzowanego jest skręcona próbka substancji chiralnej 12
13 Izomeria optyczna Substancja prawoskrętna (+) powoduje skręcanie płaszczyzny światła spolaryzowanego w prawo IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Substancja lewoskrętna (-) powoduje skręcanie płaszczyzny światła spolaryzowanego w lewo Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjnaa Optyczna Geometryczna Konformacyjna Ukladów łańcuchowych Układów cyklicznych Konfiguracja absolutna DL 13
14 Izomeria optyczna enancjomery (gr.- enantio przeciwny) izomery będące wzajemnymi odbiciami lustrzanymi, które nie dają się na siebie nałożyć, czyli są chiralne płaszczyzna lustrzana (S)(+) kwas mlekowy (R)(-) kwas mlekowy z tkanki mięśniowej z mleka ]=+13,5 o ]=-13,5 o 14
15 Konfiguracja D i L cząsteczki aldehydu glicerynowego są enancjomerami jeżeli związek (fragment końcowy) można przekształcić do jednego z izomerów aldehydu glicerynowego, to związek ten zaliczamy do szeregu konfiguracyjnego D lub L, w zależności od tego, do którego izomeru przekształcił się przynależność do konfiguracji D lub L nie zależy od kierunku skręcania płaszczyzny światła spolaryzowanego D-mannoza L-mannoza 15
16 ENANCJOMERY właściwości fizykochemiczne. Enancjomery mają identyczne właściwości fizyczne z wyjątkiem kierunku skręcania płaszczyzny swiatła spolaryzowanego. Skręcalność ma taką samą wartość, ale w przeciwnych kierunkach Enancjomery wykazują identyczne właściwości chemiczne i biologiczne z wyjątkiem ich zachowania się w stosunku do optycznie czynnych reagentów 16
17 ENANCJOMERY. Centrum chiralności atom węgla, do którego przyłączone są cztery różne podstawniki. Koniecznym i dostatecznym warunkiem enancjomerii jest chiralność, czyli niemożność nałożenia przedmiotu na jego lustrzane odbicie Chiralność - warunek konieczny (ale nie dostateczny) wystąpienia czynności optycznej. Istnienie lub brak centrum chiralności nie stanowi kryterium chiralności (struktura mezo). 17
18 Struktura mezo jest to związek, którego cząsteczki dają się nakładać na swoje lustrzane odbicia, mimo że zawierają centra chiralności Związek mezo jest optycznie nieczynny. H CH 3 Cl Cl CH 3 H 3 2 CH 3 CH * CH * CH 3 Cl Cl 2,3-dichlorobutan H Cl Cl H CH 3 CH 3 płaszczyzna lustrzana Odmiana racemiczna mieszanina równych ilości enancjomerów. Odmiana racemiczna jest optycznie nieczynna 18
19 Izomeria optyczna w przypadku izomerów optycznych (enancjomerów) określa się w nazwie związku informację o jego budowie przestrzennej przedrostkiem stereochemicznym (R) lub (S) podstawniki związane z asymetrycznym atomem węgla szereguje się w kolejności malejących liczb atomowych (umownie a>b>c>d) np. CHFClBr : Br>Cl>F>H, (R) - rectus - prawy - kierunek podstawników zgodny z ruchem wskazówek zegara (S) - sinister - lewy - kierunek przeciwny do ruchu wskazówek zegara 19
20 Izomeria optyczna w celu przypisania symboli konfiguracyjnych obserwujemy ich modele od strony przeciwnej do podstawnika zaszeregowanego jako ostatni ("d"); następnie śledzimy drogę a b c i określamy kierunek (R)-bromochloro- (R) (S)-bromochloro- (S) fluorometan fluorometan gdy z centrum chiralności związane są dwa, trzy lub cztery identyczne atomy, to porównujemy dalsze atomy z nimi związane np. H 3 C-CHCl-CH 2 OH to: Cl>CH 2 OH>CH 3 >H 20
21 S-talidomid teratogenny R-talidomid uspakajający Talidomid - lek o działaniu przeciwwymiotnym, przeciwbólowym, usypiającym i hipnotycznym. Otrzymywano go jako racemat (zawiera jednakowych ilościach oba enancjomery). R talidomid ma działanie lecznicze, S - talidomid jest silnym teratogenem działającym na DNA płodu oraz wykazującym działanie hamujące angiogenezę hamował tworzenie nowych naczyń krwionośnych w kończynach oraz rozwój już istniejących. (S) -Talidomid obecnie stosowany w leczeniu szpiczaka mnogiego 21
22 DIASTEREOIZOMERY izomery nie będące wzajemnymi odbiciami lustrzanymi 3 2 C 2 H 5 * CH * CH CH 3 Cl Cl H CH 3 Cl Cl CH 3 H 2,3-dichloropentan Cl H Cl H C 2 H 5 C 2 H 5 płaszczyzna lustrzana diastereoizomery (konstytucyjne) - zawierają co najmniej dwa centra stereogeniczne, z których co najmniej jedno ma taką samą konfigurację. 22
23 CH 3 CH 2 CH * CH * CH 3 Cl Cl 2,3-dichloropentan - możliwe stereoizomery H CH 3 Cl Cl CH 3 H H CH 3 Cl Cl CH 3 H Cl H H Cl H Cl Cl H C 2 H 5 C 2 H 5 C 2 H 5 C 2 H 5 płaszczyzna lustrzana płaszczyzna lustrzana nienakładalne enancjomery nienakładalne enancjomery 23
24 Kwas winowy Kwas winowy 2 stereocentra 4 możliwe stereoizomery d i a s t e r e o i z o m e r y kwas (+)-winowy (naturalny) lustro enancjomery kwas (-)-winowy w 175 C tworzą racemat nie są enancjomerami mają takie same elementy budulcowe związki achiralne kwas mezo-winowy d i a s t e r e o i z o m e r y
25 Diastereoizomery Mają podobne właściwości chemiczne, ponieważ należą do tej samej klasy związków. Mają różne właściwości fizyczne: temperaturę wrzenia temperaturę topnienia rozpuszczalność gęstość wartość współczynnika załamania światła różną skręcalność właściwą (jej znak może być ten sam lub przeciwny, a niektóre z nich mogą być optycznie nieczynne) 25
26 Stereoizomery Maksymalna liczba możliwych stereoizomerów (enancjomerów i diastereoizomerów) danego związku jest równa 2 n, gdzie n jest liczbą centrów chiralności 26
27 Izomeria geometryczna IZOMERIA Izomery geometryczne są diastereoizomerami różniącymi się względnym KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych Łańcuchowa Grup funkcyjnych Położenia STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Konfiguracyjna położeniem podstawników połączonych z atomami związnymi wiązaniem podwójnym lub połączonych z płaskim pierścieniem. Mogą tworzyć konfigurację: cis podstawniki są usytuowane po tej samej stronie wiązania podwójnego lub pierścienia Optyczna Geometryczna Konformacyjnaa Ukladów łańcuchowych Układów cyklicznych Konfiguracja absolutna DL trans podstwaniki znajduja się po przeciwnych stronach płaszczyzny wiązania podwójnego lub pierścienia
28 Izomeria geometryczna Cl H Cl H Br H Br H C C C C C C C C Cl H H Cl Br H H Br cis trans cis trans 1,2-dichloroetan 1,2-dibromoetan temp. wrz. 60 o C temp. wrz. 48 o C temp. wrz. 110 o C temp. wrz. 108 o C temp. topn. -80 o C temp. topn. -50 o C temp. topn. -53 o C temp. topn. -6 o C 28
29 Izomeria geometryczna Kwas oleinowy Kwas elaidynowy podwójne wiazanie kwas palmitynowy - nasycony kwas maleinowy cis kwas fumarowy trans 29
30 Właściwości izomerów geometrycznych Izomery geometryczne mają takie same grupy funkcyjne - wykazują podobne właściwości chemiczne. Izomery geometryczne różnią się właściwościami fizycznymi: temperaturą topnienia temperaturą wrzenia wartościami współczynnika załamania światła rozpuszczalnością gęstością cis-2-buten temp. wrz. +4 o C trans-2-buten temp. wrz. +1 o C 30
31 Izomeria konformacyjna IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjna Konformacyjna Konfiguracja absolutna DL Optyczna Ukladów łańcuchowych Stereoizomery konformacyjne różnią się wzajemnym położeniem grup funkcyjnych, które jest wynikiem rotacji podstawników wokół pojedynczego wiązania. Geometryczna Układów cyklicznych 31
32 Izomeria konformacyjna IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjna Konformacyjna Konfiguracja absolutna DL Konformacja układów łańcuchowych: Optyczna Geometryczna Ukladów łańcuchowych Układów cyklicznych naprzeciwległa naprzemianległa 32
33 Izomeria konformacyjna IZOMERIA KONSTUTYCJA Izomery różnią się rodzajem i sekwencją wiązań kowalencyjnych STEREOIZOMERIA Izomery posiadają identyczną konstytucję, ale różnią się przestrzennym rozmieszczeniem atomów Łańcuchowa Grup funkcyjnych Położenia Konfiguracyjna Konformacyjna Konfiguracja absolutna DL Konformacja układów cyklicznych: łódkowa krzesełkowa Optyczna Geometryczna Ukladów łańcuchowych Układów cyklicznych 33
34 Stereochemia układów alicyklicznych Układy alicykliczne mogą tworzyć konfiguracje: cis podstawniki (lub atomy wodoru) przy węglach łączących obydwa pierścienie znajdują się po jednej stronie wiązania kowalencyjnego wspólnego dla obu pierścieni; jeden pierścień ma konformację krzesełkową, a drugi łódkową trans podstawniki (lub atomy wodoru) przy węglach łączących obydwa pierścienie znajdują się po przeciwnych stronach wiązania kowalencyjnego wspólnego dla obu pierścieni; oba pierścienie mają konformacje łódkową cis dekalina trans dekalina 34
35 Stereochemia układów alicyklicznych trans dekalina cis dekalina 35
36 Układ steranu C D A B cyklopentanoperhydrofenantren Budowa trzy pierścienie cykloheksanu jeden pierścień cyklopentanu Składnik cholesterolu hormonów sterydowych kwasów żółciowych Występuje jako pochodne alkoholowe hydroksyketony 36
37 Układ steranu pod płaszczyzną nad płaszczyzną pierścienia Przyłączone grupy metylowe do węgla C13 węgiel C18 do węgla C10 węgiel C19 Znajdują się nad płaszczyzną pierścienia (pozycja ) Pierścienie B i C oraz C i D położenie trans 37
38 Układ steranu --- pod płaszczyzną nad płaszczyzną pierścienia 5- - hydrogen 5- - hydrogen układ trans układ cis Atom wodoru przy węglu C5 decyduje o układzie pierścieni A i B - pierścienie A i B są w konformacji trans - pierścienie A i B są w konformacji cis 38
39 Układ steranu 5- - hydrogen 5- - hydrogen --- pod płaszczyzną nad płaszczyzną pierścienia Atom wodoru przy węglu C5 - pierścienie A i B - pierścienie A i B są w konformacji trans są w konformacji cis 39
40 Cholesterol Brak atomu wodoru przy węglu C5 podwójne wiązanie w pierścieniu B Hydroksylowa pochodna steranu grupa -OH przy węglu C3 --- pod płaszczyzną nad płaszczyzną pierścienia 40
41 Kwasy żółciowe powstają z cholesterolu w wątrobie zawierają od 1 do 3 grup hydroksylowych związanych z pierścieniem zawierają grupę karboksylową w łańcuchu bocznym mają właściwości amfipatyczne obniżają napięcie powierzchniowe wody emulgują tłuszcze pokarmowe 41
42 Kwas cholowy 42
Chemia organiczna. Stereochemia. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
Chemia organiczna Stereochemia Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego Chemia organiczna jest nauką, która zajmuje się poszukiwaniem zależności pomiędzy budową cząsteczki a właściwościami
4. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
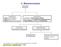 4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
4. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
7-9. Stereoizomeria. izomery. konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych
 7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
7-9. Stereoizomeria izomery konstytucyjne różne szkielety węglowe, różne grupy funkcyjne różne położenia gr. funkcyjnych stereoizomery zbudowane z takich samych atomów atomy połączone w takiej samej sekwencji
Izomerię konstytucyjną można podzielić na podgrupy a) izomeria szkieletowa, która polega na różnej budowie szkieletu węglowego cząsteczek Przykład:
 1 1) Informacje ogólne Izomery są to związki, które maja identyczne wzory sumaryczne ale różnią się sposobem lub kolejnością powiązania atomów lub rozmieszczeniem atomów w przestrzeni. rozróżnia się izomerię
1 1) Informacje ogólne Izomery są to związki, które maja identyczne wzory sumaryczne ale różnią się sposobem lub kolejnością powiązania atomów lub rozmieszczeniem atomów w przestrzeni. rozróżnia się izomerię
RJC # Alk l a k ny n Ster St eoi er zom eoi er zom y er Slides 1 to 30
 Alkany Stereoizomery Slides 1 to 30 Centrum asymetryczne (stereogeniczne) Atom węgla o hybrydyzacji sp 3 połączony z czterema róŝnymi podstawnikami tworzy centrum asymetryczne (stereogeniczne). Chiralność
Alkany Stereoizomery Slides 1 to 30 Centrum asymetryczne (stereogeniczne) Atom węgla o hybrydyzacji sp 3 połączony z czterema róŝnymi podstawnikami tworzy centrum asymetryczne (stereogeniczne). Chiralność
Stereochemia Jak przedstawiamy cząsteczkę z węglem tetraedrycznym:
 Stereochemia Jak przedstawiamy cząsteczkę z węglem tetraedrycznym: 2 wiązania leżą w płaszczyźnie kartki ( linia prosta ) 1 wiązanie wychodzi do przodu, przed kartkę ( linia pogrubiona ) 1 wiązanie wychodzi
Stereochemia Jak przedstawiamy cząsteczkę z węglem tetraedrycznym: 2 wiązania leżą w płaszczyźnie kartki ( linia prosta ) 1 wiązanie wychodzi do przodu, przed kartkę ( linia pogrubiona ) 1 wiązanie wychodzi
Stereochemia Ułożenie atomów w przestrzeni
 Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
IZOMERIA OPTYCZNA. Znaczenie izomerii optycznej.
 IZOMERIA OPTYZNA 1 Znaczenie izomerii optycznej. Izomeria optyczna to zjawisko bardzo rozpowszechnione w przyrodzie. Odgrywa niezwykle ważną rolę np. w biochemii. Można śmiało powiedzieć, że większość
IZOMERIA OPTYZNA 1 Znaczenie izomerii optycznej. Izomeria optyczna to zjawisko bardzo rozpowszechnione w przyrodzie. Odgrywa niezwykle ważną rolę np. w biochemii. Można śmiało powiedzieć, że większość
Węglowodany (Cukry) Część 1. Związki wielofunkcyjne
 Węglowodany (Cukry) Część 1 Związki wielofunkcyjne Węglowodany - wiadomości ogólne - podział Monosacharydy - wiadomości ogólne - budowa strukturalna - izomeria Węglowodany (Cukry) Węglowodany wiadomości
Węglowodany (Cukry) Część 1 Związki wielofunkcyjne Węglowodany - wiadomości ogólne - podział Monosacharydy - wiadomości ogólne - budowa strukturalna - izomeria Węglowodany (Cukry) Węglowodany wiadomości
Materiały do zajęć dokształcających z chemii organicznej
 hemia Warta Poznania - nowa JAKŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
hemia Warta Poznania - nowa JAKŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
STEREOCHEMIA ORGANICZNA
 STEECEMI GNICZN Sławomir Jarosz Wykład 3 B B B B B B B B enancjomery enancjomery enancjomery enancjomery B S S S B S S B S S B S B B S B S B S S S brót o 180 Centrum pseudoasymetrii Konfiguracja względna
STEECEMI GNICZN Sławomir Jarosz Wykład 3 B B B B B B B B enancjomery enancjomery enancjomery enancjomery B S S S B S S B S S B S B B S B S B S S S brót o 180 Centrum pseudoasymetrii Konfiguracja względna
IZOMERIA Izomery - związki o takim samym składzie lecz różniące się budową
 IZMERIA Izomery - związki o takim samym składzie lecz różniące się budową TAK zy atomy są tak samo połączone? NIE izomery konstytucyjne stereoizomery zy odbicie lustrzane daje się nałożyć na cząsteczkę?
IZMERIA Izomery - związki o takim samym składzie lecz różniące się budową TAK zy atomy są tak samo połączone? NIE izomery konstytucyjne stereoizomery zy odbicie lustrzane daje się nałożyć na cząsteczkę?
Izomeria cukrów prostych
 Izomeria cukrów prostych 1. Cele lekcji a) Wiadomości Uczeń zna: podział izomerii. pojęcia: konstytucja, konfiguracja, cząsteczka chiralna, centrum chiralności. b) Umiejętności Uczeń potrafi: wskazać w
Izomeria cukrów prostych 1. Cele lekcji a) Wiadomości Uczeń zna: podział izomerii. pojęcia: konstytucja, konfiguracja, cząsteczka chiralna, centrum chiralności. b) Umiejętności Uczeń potrafi: wskazać w
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
RJC # Konf n ig i ur u ac a ja a a bs b olu l t u na
 Konfiguracja absolutna Konfiguracja absolutna Reguły Cahna-Ingolda Ingolda-Preloga Slides to 2 Reguły Cahna-Ingolda-Preloga Sposób określenia absolutnej konfiguracji (R lub S) centrum asymetrycznego. Reguły
Konfiguracja absolutna Konfiguracja absolutna Reguły Cahna-Ingolda Ingolda-Preloga Slides to 2 Reguły Cahna-Ingolda-Preloga Sposób określenia absolutnej konfiguracji (R lub S) centrum asymetrycznego. Reguły
Spis treści ELEMENTY STEREOCHEMII
 Spis treści 1 ELEMENTY STEREOCHEMII 2 Czynność optyczna 3 IZOMERY 3.1 Izomery konstytucyjne 3.2 Izomery konformacyjne 3.3 Izomery konfiguracyjne (stereoizomery) 3.4 Enancjomery 3.5 Diastereoizomery (diastereomery)
Spis treści 1 ELEMENTY STEREOCHEMII 2 Czynność optyczna 3 IZOMERY 3.1 Izomery konstytucyjne 3.2 Izomery konformacyjne 3.3 Izomery konfiguracyjne (stereoizomery) 3.4 Enancjomery 3.5 Diastereoizomery (diastereomery)
STEREOCHEMIA ORGANICZNA
 STERECEMIA RGANICZNA Sławomir Jarosz Wykład 3 antyperiplanarna synperiplanarna synklinalna antyklinalna Konformacja uprzywilejowana s-trans s-cis s-trans s-cis (C=) = 1674 cm -1 (C=) = 1698 cm -1 (C=C)
STERECEMIA RGANICZNA Sławomir Jarosz Wykład 3 antyperiplanarna synperiplanarna synklinalna antyklinalna Konformacja uprzywilejowana s-trans s-cis s-trans s-cis (C=) = 1674 cm -1 (C=) = 1698 cm -1 (C=C)
Węglowodany. Monosacharydy Oligosacharydy Polisacharydy. Skrobia Celuloza Glikogen. Aldopentozy (ryboza) Disacharydy. Ketopentozy (rybuloza)
 Cz. XXVIII-a Węglowodany - cukry - sacharydy: klasyfikacja, budowa, nazewnictwo i izomeria I. Definicja i klasyfikacja Węglowodany to polihydroksylowe aldehydy i ketony oraz ich pochodne Węglowodany Monosacharydy
Cz. XXVIII-a Węglowodany - cukry - sacharydy: klasyfikacja, budowa, nazewnictwo i izomeria I. Definicja i klasyfikacja Węglowodany to polihydroksylowe aldehydy i ketony oraz ich pochodne Węglowodany Monosacharydy
Politechnika Wrocławska Wydział Chemiczny Zakład Materiałów Polimerowych i Węglowych. Analiza składu enancjomerów
 Politechnika Wrocławska Wydział Chemiczny Zakład Materiałów Polimerowych i Węglowych Analiza składu enancjomerów Wrocław 2005 1. Związki optycznie czynne. Zjawisko skręcania płaszczyzny drgań światła spolaryzowanego
Politechnika Wrocławska Wydział Chemiczny Zakład Materiałów Polimerowych i Węglowych Analiza składu enancjomerów Wrocław 2005 1. Związki optycznie czynne. Zjawisko skręcania płaszczyzny drgań światła spolaryzowanego
Zagadnienia na Konkurs Chemiczny, który w ramach Akademii Ciekawej Chemii odbędzie się 26 maja, godz
 Zagadnienia na Konkurs Chemiczny, który w ramach Akademii Ciekawej Chemii odbędzie się 26 maja, godz. 16.30 Wykład Nr 1 Struktura cząsteczek chemicznych od atomu do makromolekuł. dr Marcin Palusiak 1.
Zagadnienia na Konkurs Chemiczny, który w ramach Akademii Ciekawej Chemii odbędzie się 26 maja, godz. 16.30 Wykład Nr 1 Struktura cząsteczek chemicznych od atomu do makromolekuł. dr Marcin Palusiak 1.
STEREOCHEMIA ORGANICZNA
 STERECEMIA RGANICZNA Sławomir Jarosz Wykład 3 Konfiguracja względna Ułożenie grup (atomów) względem siebie trans cis Konfiguracja absolutna Bezwzględne ułożenie atomów w przestrzeni trans trans cis W jaki
STERECEMIA RGANICZNA Sławomir Jarosz Wykład 3 Konfiguracja względna Ułożenie grup (atomów) względem siebie trans cis Konfiguracja absolutna Bezwzględne ułożenie atomów w przestrzeni trans trans cis W jaki
CO_05_W: Stereochemia
 CO_05_W: Stereochemia UWAGA: W tej części kursu CO_05: Stereochemia zawarto materiały i przykłady rozszerzające zagadnienia zawarte w podręcznikach: 1. H. Hart, L. E. Craine, D. J. Hart, Ch. M. Hadad Chemia
CO_05_W: Stereochemia UWAGA: W tej części kursu CO_05: Stereochemia zawarto materiały i przykłady rozszerzające zagadnienia zawarte w podręcznikach: 1. H. Hart, L. E. Craine, D. J. Hart, Ch. M. Hadad Chemia
RJC # Defin i i n c i ja
 Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
O MATURZE Z CHEMII ANALIZA TRUDNYCH DLA ZDAJĄCYCH PROBLEMÓW
 O MATURZE Z CHEMII ANALIZA TRUDNYCH DLA ZDAJĄCYCH PROBLEMÓW Jolanta Baldy Wrocław, 2 grudnia 2016 r. Matura 2016 z chemii w liczbach Średni wynik procentowy Województwo dolnośląskie 36% (1981) Województwo
O MATURZE Z CHEMII ANALIZA TRUDNYCH DLA ZDAJĄCYCH PROBLEMÓW Jolanta Baldy Wrocław, 2 grudnia 2016 r. Matura 2016 z chemii w liczbach Średni wynik procentowy Województwo dolnośląskie 36% (1981) Województwo
Makrocząsteczki. Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe
 Makrocząsteczki Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe Syntetyczne: -Elastomery bardzo duża elastyczność charakterystyczna dla gumy -Włókna długie,
Makrocząsteczki Przykłady makrocząsteczek naturalnych: -Polisacharydy skrobia, celuloza -Białka -Kwasy nukleinowe Syntetyczne: -Elastomery bardzo duża elastyczność charakterystyczna dla gumy -Włókna długie,
Ćwiczenie 9 Wyznaczanie skręcalności właściwej sacharozy, glukozy i fruktozy (zjawisko inwersji)
 Ćwiczenie 9 Wyznaczanie skręcalności właściwej sacharozy, glukozy i fruktozy (zjawisko inwersji) zęść teoretyczna: Światło to fala elektromagnetyczna, która polega na rozchodzeniu się zmian pola elektrycznego
Ćwiczenie 9 Wyznaczanie skręcalności właściwej sacharozy, glukozy i fruktozy (zjawisko inwersji) zęść teoretyczna: Światło to fala elektromagnetyczna, która polega na rozchodzeniu się zmian pola elektrycznego
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Oznaczenia konfiguracji absolutnej związków konformacyjnie labilnych
 Uniwersytet im. Adama Mickiewicza Wydział Chemii Zakład Stereochemii Organicznej Grunwaldzka 6, 60 780 Poznań Poznań, 20 lutego 2012 r. Dr Marcin Kwit Autoreferat Oznaczenia konfiguracji absolutnej związków
Uniwersytet im. Adama Mickiewicza Wydział Chemii Zakład Stereochemii Organicznej Grunwaldzka 6, 60 780 Poznań Poznań, 20 lutego 2012 r. Dr Marcin Kwit Autoreferat Oznaczenia konfiguracji absolutnej związków
Test kompetencji z chemii do liceum. Grupa A.
 Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Różnorodny świat izomerów powtórzenie wiadomości przed maturą
 Różnorodny świat izomerów powtórzenie wiadomości przed maturą Maria Kluz Klasa III, profil biologiczno-chemiczny i matematyczno-chemiczny 1 godzina lekcyjna, praca w grupie 16-osobowej. Cele edukacyjne:
Różnorodny świat izomerów powtórzenie wiadomości przed maturą Maria Kluz Klasa III, profil biologiczno-chemiczny i matematyczno-chemiczny 1 godzina lekcyjna, praca w grupie 16-osobowej. Cele edukacyjne:
Rozdział 9. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 9 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Cukry Zadanie 9.1. Kolejno:
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 9 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Cukry Zadanie 9.1. Kolejno:
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA
 Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
BIOCHEMIA! Kierunek: Technologia Żywności # i Żywienie Człowieka# semestr III #
 BIOCHEMIA! Kierunek: Technologia Żywności # i Żywienie Człowieka# semestr III # Prof. dr hab. inż. Artur Bartkowiak! (pok. 1.13 ul Janickiego 35)! Wykłady: 15 tyg. x 2 godz. = 30 godz.# Egzamin:# pisemny
BIOCHEMIA! Kierunek: Technologia Żywności # i Żywienie Człowieka# semestr III # Prof. dr hab. inż. Artur Bartkowiak! (pok. 1.13 ul Janickiego 35)! Wykłady: 15 tyg. x 2 godz. = 30 godz.# Egzamin:# pisemny
Podstawy Chemii. Zarys chemii organicznej. Dr inż. Marcin Libera
 Podstawy Chemii Zarys chemii organicznej Dr inż. Marcin Libera Zakres merytoryczny 1. Podstawowe pojęcia i prawa chemii. 2. Budowa atomu i układ okresowy pierwiastków. 3. Budowa cząsteczek (organicznych
Podstawy Chemii Zarys chemii organicznej Dr inż. Marcin Libera Zakres merytoryczny 1. Podstawowe pojęcia i prawa chemii. 2. Budowa atomu i układ okresowy pierwiastków. 3. Budowa cząsteczek (organicznych
Wykład 1. Struktura i wiązania w cząsteczkach organicznych
 Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
Wykład 1. Struktura i wiązania w cząsteczkach organicznych Pierwszy wykład służył przypomnieniu znanych pojęć, zaakcentowaniu które pojęcia są ważne w chemii organicznej. Proszę zwrócić uwagę na zagadnienia
Karty pracy dla uczniów, plansze ze wzorami kwasów, sprzęt i odczynniki niezbędne do wykonania doświadczeń.
 Hydroksykwasy 1. Cele lekcji a) Wiadomości Uczeń zna: wzory kwasów: mlekowego, winowego, cytrynowego, salicylowego, pojęcia: czynność optyczna, odmiana mezo, enancjomer. b) Umiejętności Uczeń potrafi:
Hydroksykwasy 1. Cele lekcji a) Wiadomości Uczeń zna: wzory kwasów: mlekowego, winowego, cytrynowego, salicylowego, pojęcia: czynność optyczna, odmiana mezo, enancjomer. b) Umiejętności Uczeń potrafi:
Cukry. C x H 2y O y lub C x (H 2 O) y
 Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
Cukry Cukry organiczne związki chemiczne składające się z atomów węgla oraz wodoru i tlenu, zazwyczaj w stosunku H:O = 2:1. Zawierają liczne grupy hydroksylowe, karbonylowe a czasami mostki półacetalowe.
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
WĘGLOWODORY. Uczeń: Przykłady wymagań nadobowiązkowych Uczeń:
 WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
C H N O L B I O T E ORGANICZNA I A. Hybrydyzacja. Atom węgla. Hybrydyzacja sp 3. Hybrydyzacja sp 2. Hybrydyzacja sp
 B I O T E N O L EMIA O G ORGANIZNA I A ybrydyzacja Atom węgla ybrydyzacja sp 3 ybrydyzacja sp 2 ybrydyzacja sp B I O T E N O L EMIA O G ORGANIZNA I A Sposób rysowania wzorów 1) Wzory STRUKTURALNE KONSTYTUYJNE
B I O T E N O L EMIA O G ORGANIZNA I A ybrydyzacja Atom węgla ybrydyzacja sp 3 ybrydyzacja sp 2 ybrydyzacja sp B I O T E N O L EMIA O G ORGANIZNA I A Sposób rysowania wzorów 1) Wzory STRUKTURALNE KONSTYTUYJNE
Chemiczne składniki komórek
 Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
Chemiczne składniki komórek Pierwiastki chemiczne w komórkach: - makroelementy (pierwiastki biogenne) H, O, C, N, S, P Ca, Mg, K, Na, Cl >1% suchej masy - mikroelementy Fe, Cu, Mn, Mo, B, Zn, Co, J, F
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Alkeny. Wzór ogólny alkenów C n H 2n. (Uwaga identyczny wzór ogólny mają cykloakany!!!)
 Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
Polarność cząsteczek
 Wykład II Polarność cząsteczek Cz steczka jest polarna gdy rodek ci ko ci adunku ujemnego nie pokrywa si ze rodkiem ci ko ci adunku dodatniego. Cz steczka taka wykazuje moment dipolowy. Jest dipolem. Moment
Wykład II Polarność cząsteczek Cz steczka jest polarna gdy rodek ci ko ci adunku ujemnego nie pokrywa si ze rodkiem ci ko ci adunku dodatniego. Cz steczka taka wykazuje moment dipolowy. Jest dipolem. Moment
Modele: kulkowy i czaszowy: wzór półstrukturalny: H 2 C=CH 2. Obecność wiązania podwójnego sygnalizuje końcówka nazwy "-en" Wzór strukturalny:
 Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Wojewódzki Konkurs Przedmiotowy z chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2010/2011
 Wojewódzki Konkurs Przedmiotowy z chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2010/2011 KOD UCZNIA Etap: Data: Czas pracy: rejonowy 7 lutego 2011r 90 minut Informacje dla ucznia
Wojewódzki Konkurs Przedmiotowy z chemii dla uczniów gimnazjów województwa śląskiego w roku szkolnym 2010/2011 KOD UCZNIA Etap: Data: Czas pracy: rejonowy 7 lutego 2011r 90 minut Informacje dla ucznia
Test diagnostyczny. Dorota Lewandowska, Lidia Wasyłyszyn, Anna Warchoł. Część A (0 5) Standard I
 strona 1/9 Test diagnostyczny Dorota Lewandowska, Lidia Wasyłyszyn, Anna Warchoł Część A (0 5) Standard I 1. Przemianą chemiczną nie jest: A. mętnienie wody wapiennej B. odbarwianie wody bromowej C. dekantacja
strona 1/9 Test diagnostyczny Dorota Lewandowska, Lidia Wasyłyszyn, Anna Warchoł Część A (0 5) Standard I 1. Przemianą chemiczną nie jest: A. mętnienie wody wapiennej B. odbarwianie wody bromowej C. dekantacja
CHIRALNOŚĆ WŁAŚCIWOŚĆ MATERII EGZOTYCZNA CZY WSZECHOBECNA?
 IRALNŚĆ WŁAŚIWŚĆ MATERII EGZTYZNA ZY WSZEBENA? Stanisław Krompiec Uniwersytet Śląski, Katowice, 2017 r. hiralność definicja biekty achiralne i chiralne biekt achiralny biekty achiralne - przykłady hiralność
IRALNŚĆ WŁAŚIWŚĆ MATERII EGZTYZNA ZY WSZEBENA? Stanisław Krompiec Uniwersytet Śląski, Katowice, 2017 r. hiralność definicja biekty achiralne i chiralne biekt achiralny biekty achiralne - przykłady hiralność
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Pomiar kąta skręcenia polaryzacji światła oraz skręcalności właściwej roztworów sacharozy I. Wstęp, zastosowania metody w medycynie
 Pomiar kąta skręcenia polaryzacji światła oraz skręcalności właściwej roztworów sacharozy I. Wstęp, zastosowania metody w medycynie Związki, których cząsteczki ze względu na swoją budowę występują w postaci
Pomiar kąta skręcenia polaryzacji światła oraz skręcalności właściwej roztworów sacharozy I. Wstęp, zastosowania metody w medycynie Związki, których cząsteczki ze względu na swoją budowę występują w postaci
Struktura biomakromolekuł chemia biologiczna III rok
 truktura biomakromolekuł chemia biologiczna III rok jak są zbudowane białka? dlaczego białka są tak zbudowane? co z tego wynika? 508 13 604 liczba struktur dostępnych w Protein Data Bank wynosi aktualnie
truktura biomakromolekuł chemia biologiczna III rok jak są zbudowane białka? dlaczego białka są tak zbudowane? co z tego wynika? 508 13 604 liczba struktur dostępnych w Protein Data Bank wynosi aktualnie
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 2002 BYŁA DZISIAJ CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY ARKUSZ EGZAMINACYJNY I
 MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
I KSZTAŁCENIA PRAKTYCZNEGO. Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
Wymagania programowe na poszczególne oceny. Chemia Kl.1. I. Substancje chemiczne i ich przemiany
 Wymagania programowe na poszczególne oceny Chemia Kl.1 I. Substancje chemiczne i ich przemiany Ocena dopuszczająca [1] zna zasady bhp obowiązujące w pracowni chemicznej nazywa sprzęt i szkło laboratoryjne
Wymagania programowe na poszczególne oceny Chemia Kl.1 I. Substancje chemiczne i ich przemiany Ocena dopuszczająca [1] zna zasady bhp obowiązujące w pracowni chemicznej nazywa sprzęt i szkło laboratoryjne
H H H. Wzór "płaskostrukturalny": Wzór klinowy: H H. Model kulkowy cząsteczki: (obrazuje długosci wiązań, kąty między wiązaniami)
 Autor: Marek Walnik, 04 Alkany - węglowodory nasycone, parafiny. Związki węgla z wodorem, w których cząsteczkach występują wyłącznie wiązania pojedyncze. Szczególną klasę związków tego typu stanowią cykloalkany
Autor: Marek Walnik, 04 Alkany - węglowodory nasycone, parafiny. Związki węgla z wodorem, w których cząsteczkach występują wyłącznie wiązania pojedyncze. Szczególną klasę związków tego typu stanowią cykloalkany
Zdzisław Głowacki. Zakres podstawowy i rozszerzony. Odpowiedzi i rozwiązania zadań. Rozdział 1. Powinno być
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 1 Errata do pierwszego rozdziału ćwiczeń: Strona Linia / zadanie Str. 10. Linia 1. Str. 16.
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 1 Errata do pierwszego rozdziału ćwiczeń: Strona Linia / zadanie Str. 10. Linia 1. Str. 16.
Skala słodkości cukrów Laktoza < maltoza < glukoza < sacharoza < fruktoza najsłodsza
 Źródła cukrów (węglowodanów) w produktach spożywczych: Warzywa i owoce (winogrona cukier gronowy glukoza) Produkty zbożowe: pieczywo, kasze, płatki śniadaniowe Funkcja węglowodanów w organizmie: Energetyczna:
Źródła cukrów (węglowodanów) w produktach spożywczych: Warzywa i owoce (winogrona cukier gronowy glukoza) Produkty zbożowe: pieczywo, kasze, płatki śniadaniowe Funkcja węglowodanów w organizmie: Energetyczna:
SUBSTANCJE CHEMICZNE I ICH PRZEMIANY
 DOPUSZCZAJĄCĄ DZIAŁ SUBSTANCJE CHEMICZNE I ICH PRZEMIANY -zna zasady bhp obowiązujące w pracowni chemicznej -nazywa sprzęt i szkło laboratoryjne używane w pracowni chemicznej -wie, że substancje charakteryzują
DOPUSZCZAJĄCĄ DZIAŁ SUBSTANCJE CHEMICZNE I ICH PRZEMIANY -zna zasady bhp obowiązujące w pracowni chemicznej -nazywa sprzęt i szkło laboratoryjne używane w pracowni chemicznej -wie, że substancje charakteryzują
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wskaż grupy reakcji, do których można zaliczyć proces opisany w informacji wstępnej. A. I i III B. I i IV C. II i III D. II i IV
 Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne. Z CHEMII W KLASIE III gimnazjum
 WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE III gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE III gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie)
 Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie) Kod ucznia Suma punktów Witamy Cię na trzecim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Konkurs przedmiotowy z chemii dla uczniów gimnazjów 6 marca 2015 r. zawody III stopnia (wojewódzkie) Kod ucznia Suma punktów Witamy Cię na trzecim etapie konkursu chemicznego. Podczas konkursu możesz korzystać
Deskryptory molekularne
 Deskryptory molekularne Molekuła - definicje Konstytucja sposób łączenia atomów Stereochemia sposób rozmieszczenia atomów w przestrzeni (konfiguracja) Izomery związki o tym samym wzorze cząsteczkowym różniące
Deskryptory molekularne Molekuła - definicje Konstytucja sposób łączenia atomów Stereochemia sposób rozmieszczenia atomów w przestrzeni (konfiguracja) Izomery związki o tym samym wzorze cząsteczkowym różniące
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE Z CHEMII 2013/2014
 Uczeń klasy I: WYMAGANIA EDUKACYJNE Z CHEMII 2013/2014 -rozróżnia i nazywa podstawowy sprzęt laboratoryjny -wie co to jest pierwiastek, a co to jest związek chemiczny -wyszukuje w układzie okresowym nazwy
Uczeń klasy I: WYMAGANIA EDUKACYJNE Z CHEMII 2013/2014 -rozróżnia i nazywa podstawowy sprzęt laboratoryjny -wie co to jest pierwiastek, a co to jest związek chemiczny -wyszukuje w układzie okresowym nazwy
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna
 Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
CHEMIA KLASA Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
1. Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Woda. Najpospolitsza czy najbardziej niezwykła substancja Świata?
 Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/55/35935976.jpg) KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Szanowne koleżanki i koledzy nauczyciele chemii!
 Szanowne koleżanki i koledzy nauczyciele chemii! Chciałabym podzielić się z Wami moimi spostrzeżeniami dotyczącymi poziomu wiedzy z chemii uczniów rozpoczynających naukę w Liceum Ogólnokształcącym. Co
Szanowne koleżanki i koledzy nauczyciele chemii! Chciałabym podzielić się z Wami moimi spostrzeżeniami dotyczącymi poziomu wiedzy z chemii uczniów rozpoczynających naukę w Liceum Ogólnokształcącym. Co
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Wymagania edukacyjne. niezbędne do uzyskania poszczególnych. śródrocznych i rocznych ocen klasyfikacyjnych. z chemii
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii klasa III,,Program nauczania chemii w gimnazjum. Chemia Nowej Ery Teresa Kulawik, Maria
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z chemii klasa III,,Program nauczania chemii w gimnazjum. Chemia Nowej Ery Teresa Kulawik, Maria
Wymagania programowe na poszczególne oceny chemia kl. I
 I. Substancje i ich przemiany Wymagania programowe na poszczególne oceny chemia kl. I Ocena dopuszczająca [1] zalicza chemię do nauk przyrodniczych stosuje zasady bezpieczeństwa obowiązujące w pracowni
I. Substancje i ich przemiany Wymagania programowe na poszczególne oceny chemia kl. I Ocena dopuszczająca [1] zalicza chemię do nauk przyrodniczych stosuje zasady bezpieczeństwa obowiązujące w pracowni
Opis efektów kształcenia dla modułu zajęć
 Nazwa modułu: Chemia organiczna Rok akademicki: 2012/2013 Kod: JFM-1-208-s Punkty ECTS: 2 Wydział: Fizyki i Informatyki Stosowanej Kierunek: Fizyka Medyczna Specjalność: - Poziom studiów: Studia I stopnia
Nazwa modułu: Chemia organiczna Rok akademicki: 2012/2013 Kod: JFM-1-208-s Punkty ECTS: 2 Wydział: Fizyki i Informatyki Stosowanej Kierunek: Fizyka Medyczna Specjalność: - Poziom studiów: Studia I stopnia
CHEMIA. Wymagania szczegółowe. Wymagania ogólne
 CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA klasa 1 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 1 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Substancje i ich przemiany WYMAGANIA PODSTAWOWE stosuje zasady bezpieczeństwa
CHEMIA klasa 1 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Substancje i ich przemiany WYMAGANIA PODSTAWOWE stosuje zasady bezpieczeństwa
Zadanie 4. Mrówczan metylu ma taki sam wzór sumaryczny jak: A. octan etylu. C. kwas mrówkowy. B. octan metylu. D. kwas octowy.
 Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 3 marca 2011 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 3 marca 2011 r. zawody III stopnia (wojewódzkie) Witamy Cię na trzecim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Wewnętrzna budowa materii
 Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
Ocenę niedostateczną otrzymuje uczeń, który: Ocenę dopuszczającą otrzymuje uczeń, który: Ocenę dostateczną otrzymuje uczeń, który:
 Kryteria oceniania z chemii dla klasy 3A i 3B Gimnazjum w Borui Kościelnej Rok szkolny: 2015/2016 Semestr: pierwszy Opracowała: mgr Krystyna Milkowska, mgr inż. Malwina Beyga Ocenę niedostateczną otrzymuje
Kryteria oceniania z chemii dla klasy 3A i 3B Gimnazjum w Borui Kościelnej Rok szkolny: 2015/2016 Semestr: pierwszy Opracowała: mgr Krystyna Milkowska, mgr inż. Malwina Beyga Ocenę niedostateczną otrzymuje
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem
 Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości.
 Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości. Cel główny: przypomnienie i utrwalenie wiadomości dotyczących węglowodorów i pochodnych
Konspekt lekcji chemii w klasie III gimnazjum. Temat: Węglowodory i pochodne węglowodorów powtórzenie wiadomości. Cel główny: przypomnienie i utrwalenie wiadomości dotyczących węglowodorów i pochodnych
STEREOCHEMIA ORGANICZNA Wykład 6
 STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
Spektroskopia molekularna. Spektroskopia w podczerwieni
 Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
Spektroskopia molekularna Ćwiczenie nr 4 Spektroskopia w podczerwieni Spektroskopia w podczerwieni (IR) jest spektroskopią absorpcyjną, która polega na pomiarach promieniowania elektromagnetycznego pochłanianego
Węglowodany (Cukry) Część 2. Związki wielofunkcyjne
 Węglowodany (Cukry) Część 2 Związki wielofunkcyjne Monosacharydy Glukoza, Fruktoza: - wzory łańcuchowe, wzory Fishera, - właściwości fizyczne i chemiczne (zależności między budową a właściwościami) - funkcje
Węglowodany (Cukry) Część 2 Związki wielofunkcyjne Monosacharydy Glukoza, Fruktoza: - wzory łańcuchowe, wzory Fishera, - właściwości fizyczne i chemiczne (zależności między budową a właściwościami) - funkcje
Węglowodory poziom rozszerzony
 Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Wymagania programowe: Gimnazjum chemia kl. II
 Wymagania programowe: Gimnazjum chemia kl. II Dział: Wewnętrzna budowa materii Ocena dopuszczająca [1] posługuje się symbolami odróżnia wzór sumaryczny od wzoru strukturalnego zapisuje wzory sumaryczne
Wymagania programowe: Gimnazjum chemia kl. II Dział: Wewnętrzna budowa materii Ocena dopuszczająca [1] posługuje się symbolami odróżnia wzór sumaryczny od wzoru strukturalnego zapisuje wzory sumaryczne
Wymagania programowe na poszczególne oceny z chemii w kl.1. I. Substancje i ich przemiany
 Wymagania programowe na poszczególne oceny z chemii w kl.1 I. Substancje i ich przemiany Ocena dopuszczająca [1] Ocena dostateczna [1 + 2] zalicza chemię do nauk przyrodniczych wyjaśnia, dlaczego chemia
Wymagania programowe na poszczególne oceny z chemii w kl.1 I. Substancje i ich przemiany Ocena dopuszczająca [1] Ocena dostateczna [1 + 2] zalicza chemię do nauk przyrodniczych wyjaśnia, dlaczego chemia
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej
 Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
