Absolutna skala temperatur.
|
|
|
- Konrad Kalinowski
- 9 lat temu
- Przeglądów:
Transkrypt
1 Wykład z fizyki, Piotr Posmykiewicz 88 Absolutna skala temperatur. W wykładzie XII skala temperatur dla gazu doskonałego została zdefiniowana za pomocą własności gazów posiadających małą gęstość. PoniewaŜ współczynnik sprawności cyklu Carnota zaleŝy jedynie od temperatur dwóch zbiorników ciepła, to moŝe zostać uŝyty do zdefiniowania stosunku temperatur tych dwu zbiorników ciepła niezaleŝnie od własności jakiejkolwiek substancji. Definiujemy stosunek temperatur absolutnych grzejnicy i chłodnicy jako: = 5-7 gdzie jest energią pobieraną z grzejnicy, a jest energią oddawaną do chłodnicy w silniku Carnota pracującego między tymi dwoma zbiornikami. W rezultacie, aby znaleźć stosunek temperatur dwu zbiorników ciepła, moŝemy zbudować silnik odwracalny działający między tymi temperaturami i mierzyć ciepło pobierane i oddawane przez kaŝdy zbiornik w trakcie jednego cyklu. emperatura absolutna będzie wtedy całkowicie określona równaniem 5-7 i przez wybór jednego określonego punktu. JeŜeli punkt ten zdefiniowany jest jako 73,6K dla punktu potrójnego wody, wtedy absolutna skala temperatur zgadza się ze skalą temperatur dla gazu doskonałego w zakresie temperatur większym niŝ te które, moŝe mierzyć za pomocą termometru gazowego. 5-5 Pompa cieplna. Pompa cieplna jest w zasadzie lodówką, która została uŝyta do pompowania ciepła z zimnego zbiornika (na przykład zimne powietrze na zewnątrz budynku ) do ciepłego zbiornika ( na przykład ciepłe powietrze wewnątrz budynku ). JeŜeli praca W jest wykonana aby usunąć ciepło z chłodnego zbiornika i przekazać ciepło = W + do ciepłego zbiornika, to współczynnik wydajności chłodniczej ( Równanie 5-3 ) jest równy: WWC = W Podstawiając W = powyŝszy współczynnik moŝna zapisać:
2 Wykład z fizyki, Piotr Posmykiewicz 89 WWC = = 5-8 / / Maksymalny współczynnik chłodniczy otrzymamy dla pompy Carnota. Wtedy i są dane związkiem 5-5. Podstawiając / = / do równania 5-8 moŝemy obliczyć maksymalny współczynnik chłodniczy: gdzie / WWCmax = = / = 5-9 jest róŝnicą temperatur między ciepłym, a chłodnym zbiornikiem ciepła. Rzeczywista pompa cieplna lub lodówka mają WWC mniejsze niŝ WWC max z powodu strat energii wywołanej tarciem i innymi nieodwracalnymi procesami. Zwykle interesuje nas praca jaka musi być wykonana, aby doprowadzić określoną ilość ciepła do ciepłego zbiornika, który w przypadku domowej pompy cieplnej, byłby ciepłym powietrzem dostarczanym do domowego wentylatora ciepła. Podstawiając = W, równanie 5-3 moŝemy zapisać w postaci: + lub W WWC = = W W W = WWC Ćwiczenie. Idealna pompa cieplna jest zastosowana do przepompowania powietrza z zewnątrz o temperaturze -5 0 C i do ogrzania wnętrza domu do temperatury 40 0 C. Jaką pracę trzeba wykonać, aby przepompować kj do wnętrza domu? ( Zastosuj równanie 5-9, a potem 5-0 ). Odpowiedź: 0,44kJ. Uwaga : Potrzeba tylko 0,44kJ aby przepompować kj ciepła do zbiornika cieplnego jakim jest dom. Widzimy, Ŝe w zasadzie pompa cieplna pomnaŝa energię potrzebną do pracy tej pompy o + WWC. JeŜeli uŝyjemy kj do pracy pompy o WWC = 5,96, to moŝemy dostarczyć 6,96kJ ciepła do ogrzania domu.
3 Wykład z fizyki, Piotr Posmykiewicz Nieodwracalność, a nieuporządkowanie. Istnieje cały szereg procesów nieodwracalnych, które nie mogą być opisane drugim prawem termodynamiki w sformułowaniach w oparciu o silnik cieplny, czy lodówkę; na przykład, spadająca szklanka na podłogę i rozbijająca się. Jednak wszystkie procesy nieodwracalne mają jedną wspólną cechę: układ i otoczenie przechodzi uporządkowanego. do stanu mniej ZałóŜmy, Ŝe pojemnik zawierający gaz o masie M i temperaturze porusza się bez tarcia po stole z prędkością v śm ( Rysunek 5-9a ). Całkowita energia kinetyczna składa się z dwu części: pierwszej związanej z ruchem środka masy cząsteczek gazu względem środka masy. Energia środka masy Mv śm Mv śm i drugiej - energii ruchu jest uporządkowaną energią mechaniczną, która moŝe być całkowicie zamieniona na pracę. Energia względem środka masy jest wewnętrzną energią cieplną, która jest związana z temperaturą gazu. Jest to przypadkowa, nieuporządkowana energia, która nie moŝe być bezpośrednio zamieniona na pracę. ZałóŜmy teraz, Ŝe pojemnik uderza w nieruchomą ścianę i zatrzymuje się ( Rysunek 5-9b ): o niespręŝyste zderzenie jest, w sposób oczywisty, procesem nieodwracalnym. Uporządkowana energia mechaniczna gazu została przekształcona w przypadkową energię wewnętrzną i temperatura gazu wzrosła. Gaz ciągle posiada tę samą energię całkowitą, ale v śm Rysunek 5-9a Rysunek 5-9b teraz cała energia jest związana z przypadkowym ( chaotycznym ) ruchem jego cząsteczek względem jego środka masy, który znajduje się obecnie w spoczynku. W rezultacie gaz stał się układem mniej uporządkowanym ( lub bardziej nieuporządkowanym ) i stracił zdolność wykonania pracy. Np. jeŝeli jakiś cięŝar byłby przymocowany liną z poruszającym się pojemnikiem, to energia ta mogła by być zamieniona na podniesienie tego cięŝaru.
4 Wykład z fizyki, Piotr Posmykiewicz Entropia. Istnieje funkcja termodynamiczna zwana entropią S, która jest miarą nieuporządkowania układu. Podobnie jak ciśnienie p, objętość, temperatura i energia wewnętrzna, entropia jest funkcją stanu układu. Podobnie jak jest to w przypadku energii potencjalnej, tylko zmiana entropii jest istotna. Zmiana entropii ds układu, gdy ten przechodzi z jednego stanu do drugiego jest zdefiniowana jako: gdzie dodwr dodwr ds = 5- Definicja zmiany entropii. jest ciepłem, które musi być dodane do układu w procesie odwracalnym, które przeprowadza układ ze stanu początkowego do stanu końcowego. JeŜeli to zmiana entropii teŝ jest ujemna. WyraŜenie dodwr jest ujemne, d odwr nie oznacza, Ŝe musi zachodzić odwracalne przekazanie ciepła, aby entropia układu się zmieniła. Rzeczywiście; istnieje cały szereg sytuacji, w których entropia układu zmienia się, ale nie ma Ŝadnego wymiany ciepła. Równanie 5-, po prostu, podaje nam sposób w jaki moŝemy policzyć zmianę entropii dwu stanów układu. PoniewaŜ entropia jest funkcją stanu, to jej zmiana kiedy układ przechodzi z jednego stanu do drugiego, zaleŝy tylko od stanu początkowego i końcowego, a nie od przemiany w trakcie której, ta zmiana zachodzi. Entropia gazu doskonałego. MoŜemy teraz pokazać, Ŝe rzeczywiście, d / jest funkcją stanu, a d nie jest. Weźmy pod uwagę dowolny odwracalny, kwazistatyczny proces, w którym układ składający się z gazu doskonałego pobiera pewną porcję ciepła. Zgodnie z pierwszym prawem termodynamiki, d jest związane ze zmianą wewnętrznej energii du gazu i pracą wykonaną dw = pd poprzez: d = du + dw = du + pd
5 Wykład z fizyki, Piotr Posmykiewicz 9 Dla gazu doskonałego energia wewnętrzna wynosi zamiast p wyraŝenie nr /. Wtedy: du = C d i moŝemy podstawić v d d C d + nr = 5- Równanie to nie moŝe być scałkowane jeŝeli nie wiemy jak zaleŝy od. Jest to jeszcze jeden sposób stwierdzenia, Ŝe d nie jest róŝniczką funkcji stanu. MoŜemy jednak podzielić powyŝsze wyraŝenie przez i otrzymamy: PoniewaŜ d C d + d nr = 5-3 C zaleŝy tylko od temperatury, to pierwsze wyraŝenie po prawej stronie moŝe być scałkowane i teraz równieŝ z drugiego członu moŝemy policzyć całkę. W ten sposób d / jest funkcją róŝniczkowalną, a tym samym funkcja entropia teŝ: d d d ds = C + nr Dla uproszczenia załóŝmy, Ŝe = 5-4 C jest stałe. Całkując wyraŝenie 5-4 otrzymamy: d S = = C ln + nrln 5-5 Równanie 5-5 podaje zmianę entropii dla gazu doskonałego, który podlega odwracalnemu rozprzestrzenianiu się ze stanu o objętości i temperaturze do stanu końcowego o objętości i temperaturze. Zmiana entropii dla róŝnych procesów. S dla izotermicznego rozprzestrzeniania się gazu. Kiedy gaz doskonały przechodzi izotermiczne rozpręŝanie, =, to jego entropia zmienia się
6 Wykład z fizyki, Piotr Posmykiewicz 93 d = = S nrln 5-6 Zmiana entropii jest dodatnia poniewaŝ jest większe od. W procesie tym określona ilość ciepła opuszcza zbiornik ciepła i przechodzi do gazu. a ilość ciepła jest równa jest pracy wykonanej przez gaz: d = W = nr ln 5-7 pd = nr = Entropia gazu zmieniła się o + /. PoniewaŜ taka sama ilość ciepła została odprowadzona ze zbiornika ciepła o temperaturze, to zmiana entropii zbiornika jest równa /. Wypadkowa zmiana entropii gazu i zbiornika ciepła jest, zatem, równa zeru. MoŜemy odnieść rozpatrywany układ wraz z jego otoczeniem do wszechświata. PowyŜszy przykład ilustruje ogólną ideę: W procesach odwracalnych całkowita zmiana entropii wszechświata wynosi zero. S dla swobodnego rozprzestrzeniania się gazu. W przypadku swobodnego rozpręŝania się gazu omawianego w rozdziale 4 poprzedniego wykładu, gaz początkowo jest ograniczony do jednej części zbiornika, która to część jest połączona z drugą, pustą częścią zbiornika za pomocą rurki z zakręconym zaworem. Cały układ ma sztywne ścianki i jest izolowany termicznie od otoczenia, czyli Ŝadna praca nie moŝe być wykonana ani ciepło nie ni moŝe dostarczone lub odprowadzone z układu ( Rysunek 4-3 ). Kiedy zawór zostaje otwarty gaz zaczyna przemieszczać do części próŝniowej. W końcu gaz osiąga stan równowagi termicznej z samym sobą. PoniewaŜ nie jest wykonywana praca i ciepło nie jest przekazywane, to końcowa energia wewnętrzna musi być równa początkowej energii wewnętrznej. ZałóŜmy, Ŝe gaz jest doskonały. Wtedy temperatura końcowa będzie równa temperaturze początkowej. Moglibyśmy przypuszczać, Ŝe entropia gazu nie zmieni się, poniewaŝ ciepło nie było przesyłane. Jednak proces ten nie jest procesem odwracalnym, dlatego nie moŝemy uŝyć wyraŝenia d / dla określenia zmiany entropii tego gazu. Z drugiej strony stan początkowy i końcowy tego gazu podczas swobodnego rozpręŝania jest taki sam jak podczas
7 Wykład z fizyki, Piotr Posmykiewicz 94 odwracalnego procesu izotermicznego omawianego powyŝej. PoniewaŜ zmiana entropii układu dla dowolnego procesu zaleŝy tylko od stanów początkowego i końcowego układu, to entropia gazu ulegającego swobodnemu rozpręŝaniu zmieni się samo, jak w przypadku izotermicznego rozpręŝania. JeŜeli jest początkową objętością gazu, a jest objętością końcową, to zmiana entropii tego gazu będzie taka sama jak ta dana równaniem 5-6: S gaz = nrln W tym przypadku nie ma zmian w otoczeniu, czyli zmiana entropii gazu będzie takŝe zmianą entropii wszechświata: S wszech = nrln 5-8 Zwróćmy uwagę, Ŝe poniewaŝ jest większe niŝ, to zmiana entropii wszechświata dla tego nieodwracalnego procesu będzie dodatnia, a to oznacza, Ŝe entropia wszechświata wzrasta. Jest to jednocześnie uniwersalne stwierdzenie, w myśl którego: Dla nieodwracalnych procesów entropia wszechświata wzrasta. JeŜeli końcowa objętość podczas swobodnego rozpręŝania byłaby mniejsza niŝ początkowa, to entropia wszechświata by zmalała, ale coś takiego nie moŝe się zdarzyć. Gaz pozostawiony swobodnie sam sobie nigdy nie zmniejszy swojej objętości. Prowadzi nas to do jeszcze jednego sformułowania drugiej zasady termodynamiki: W Ŝadnym procesie entropia wszechświata się nie zmniejsza S dla procesów stało-ciśnieniowych. Kiedy substancja jest podgrzewana od temperatury do temperatury przy stałym ciśnieniu, to ciepło pobrane d jest związane ze zmianą jej temperatury w następujący sposób: d = C p d MoŜemy przybliŝyć proces odwracalnego przewodzenia ciepła, poprzez stworzenie duŝej ilości zbiorników cieplnych, których temperatura będzie zmieniać się od do o bardzo
8 Wykład z fizyki, Piotr Posmykiewicz 95 małe przyrosty temperatury. Następnie umieśćmy naszą substancję, której temperatura początkowa wynosi w kontakcie cieplnym z pierwszym zbiornikiem mającym tylko niewiele wyŝszą temperaturę niŝ i pozwólmy substancji pobrać niewielką ilość ciepła. PoniewaŜ dostarczone ciepło jest w przybliŝeniu procesem izotermicznym, to proces będzie w przybliŝeniu odwracalny. Następnie umieśćmy naszą substancję z kolejnym zbiornikiem ciepła o trochę wyŝszej temperaturze i tak dalej, aŝ zostanie osiągnięta końcowa temperatura. JeŜeli ciepłod jest dostarczane w sposób odwracalny, to zmiana entropii substancji wyniesie: ds = d = C p d Całkując od do otrzymamy całkowitą zmianę entropii danej substancji: S = C d p = C p ln 5-9 Wynik ten określa zmianę entropii substancji, która jest podgrzewana od temperatury do dla dowolnego procesu; odwracalnego lub nieodwracalnego, jeŝeli tylko ciśnienie końcowe pozostaje równe ciśnieniu początkowemu. Wzór powyŝszy podaje równieŝ zmianę entropii wtedy, gdy substancja jest ochładzana. W przypadku gdy jest mniejsze od, to ln / jest ujemny co daje równieŝ ujemny przyrost entropii. S w przypadku zderzeń niespręŝystych. PoniewaŜ energia mechaniczna w zderzeniach niespręŝystych jest zamieniana na energię cieplną, to takie procesy, w sposób oczywisty są nieodwracalne. Zatem entropia wszechświata musi wzrastać. Weźmy pod uwagę klocek o masie m spadający z wysokości h i zderzający się niespręŝyście z podłoŝem. Niech klocek, podłoŝe i atmosfera mają tę samą temperaturę, która nie zmienia się istotnie w tym procesie. JeŜeli przyjmiemy klocek, podłoŝe i atmosferę jako układ izolowany, to nie ma przenoszenia ciepła z lub do tego układu. Stan termodynamiczny układu ulega zmianie, poniewaŝ jego energia wewnętrzna zwiększa się o wartość mgh. a zmiana jest taka sama
9 Wykład z fizyki, Piotr Posmykiewicz 96 jakbyśmy dodali ciepło = mgh do układu, który posiada stałą temperaturę. Aby obliczyć zmianę entropii tego układu, po prostu rozpatrujemy odwracalny proces, w którym ciepło odwr = mgh jest dostarczone do układu o stałej temperaturze. Zgodnie z równaniem 5- zmiana entropii w tym wypadku wyniesie: S = = mgh a dodatnia zmiana entropii jest takŝe dodatnią zmianą entropii uniwersum. S w przypadku przewodzenia ciepła z jednego zbiornika ciepła do drugiego. Przewodnictwo cieplne jest równieŝ procesem nieodwracalnym, czyli moŝemy spodziewać się, Ŝe entropia wszechświata wzrośnie. Rozpatrzmy prosty przypadek kiedy ciepło jest przewodzone z ciepłego zbiornika o temperaturze do zbiornika chłodnego o temperaturze. Stan zbiornika ciepła jest określony tylko przez jego temperaturę i energię wewnętrzną. Zmiana entropii zbiornika ciepła z powodu wymiany ciepła jest jednakowa bez względu na to, czy ta wymiana jest odwracalna, czy nie. JeŜeli ciepło jest dostarczone do zbiornika o temperaturze, to entropia zbiornika zwiększy się o /. JeŜeli ciepło jest odprowadzone, to entropia zbiornika zmaleje o /. W przypadku przewodnictwa cieplnego, ciepły zbiornik traci ciepło, czyli jego zmiana entropii wyniesie: S grz = Zbiornik chłodniejszy pobierze ciepło, czyli jego entropia zwiększy się o S ch = Wypadkowa entropia wszechświata będzie, zatem, równa: S wszech = S + S grz ch = Zwróćmy uwagę, Ŝe zawsze kiedy ciepło przepływa ze zbiornika cieplejszego do chłodniejszego, to entropia wszechświata musi wzrosnąć.
10 Wykład z fizyki, Piotr Posmykiewicz 97 S dla cyklu Carnota. PoniewaŜ cykl Carnota z definicji jest odwracalny, to zmiana entropii wszechświata po jednym cyklu musi być równa zero. Zademonstrujemy to poprzez pokazanie, Ŝe zmiana entropii zbiorników jest równa zero. ( PoniewaŜ silnik Carnota pracuje w cyklu, to zmiana jego entropii jest równa zero; zmiana entropii wszechświata jest równa sumie zmian entropii zbiorników ). Zmiana entropii ciepłego zbiornika ( grzejnicy ) wynosi S = /, gdzie jest ciepłem usuwanym z grzejnicy. Zmiana entropii grz chłodnego zbiornika ( chłodnicy ) wynosi S ch + /, gdzie jest ciepłem dostarczonym do chłodnicy. Energie te są związane równaniem 5-7: = = W związku z tym entropia uniwersum wyniesie: ( / ) Swszech = Sgrz + Sch = + = + = 0 Rzeczywiście, zmiana entropii wszechświata, w tym wypadku, wynosi zero, tak jak tego oczekiwaliśmy. 5-8 Entropia, a dostępność energii. JeŜeli zachodzi proces nieodwracalny, to energia jest zachowana, ale część energii jest marnowana, co oznacza, Ŝe nie jest moŝliwe zamienienie jej na pracę. RozwaŜmy klocek spadający na ziemię. Kiedy klocek znajduje się na wysokości h, to jego energia potencjalna mgh moŝe być wykorzystana do wykonania poŝytecznej pracy. Po niespręŝystym zderzeniu klocka z podłoŝem, energia ta juŝ nie jest dostępna, poniewaŝ stała się nieuporządkowaną energią wewnętrzną klocka i otoczenia. a energia, która staje się niewykorzystaną jest równa mgh S wszech =. Stąd ogólna konstatacja: W procesie nieodwracalnym energię równą Swszech nie moŝemy zamienić na pracę, gdzie jest temperaturą najzimniejszego dostępnego zbiornika ciepła.
11 Wykład z fizyki, Piotr Posmykiewicz 98 Dla prostoty, będziemy nazywać tę energią, która staje się nieosiągalna do wykonania pracy jako pracę straconą : W = 5- strac S wszech Podczas swobodnego rozpręŝania, o którym była mowa wcześniej, równieŝ tracona jest zdolność układu do wykonania pracy. W tym przypadku, zmiana entropii wszechświata jest równa nr ln( / ). Jest to praca, którą gaz mógłby wykonać, jeŝeli gaz rozpręŝał by się izotermicznie od objętości do, zgodnie z równaniem 4-3. Kiedy ciepło jest przewodzone z ciepłego zbiornika do chłodnego, to zmiana entropii wszechświata jest dana równaniem 0-0, a stracona praca jest równa: W = strac = Swszech MoŜemy zauwaŝyć, Ŝe jest to właśnie praca, która mogłaby być wykonana przez silnik Carnota działający między tymi zbiornikami, usuwający ciepło z ciepłego zbiornika i wykonujący pracę W = η C, gdzie C = / η. 5-9 Entropia, a prawdopodobieństwo. Entropia, która jest miarą nieuporządkowania układu, ma związek z prawdopodobieństwem. W istocie; stan o duŝym stopniu uporządkowania ma małe prawdopodobieństwo istnienia, podczas gdy stan o niskim stopniu uporządkowania ma duŝe prawdopodobieństwo powstania. W rezultacie, dla procesów nieodwracalnych wszechświat porusza się od stanu o niskim prawdopodobieństwie do stanu o wysokim prawdopodobieństwie. Rozpatrzmy swobodne rozpręŝanie się gazu od początkowej objętości do objętości końcowej 8: =. Zmiana entropii wszechświata dla tego procesu jest dana równaniem 5- S = nrln = nrln 5-
12 Wykład z fizyki, Piotr Posmykiewicz 99 Dlaczego proces ten jest nieodwracalny? Dlaczego gaz nie moŝe ulec samoistnie kompresji do swojej początkowej objętości? PoniewaŜ nie zmienia się energia układu, to pierwsza zasada termodynamiki nie byłaby naruszona przez taką kompresję. Powód jest zaledwie (!) taki, Ŝe taka sytuacja byłaby krańcowo nieprawdopodobna. Aby to sobie uświadomić załóŝmy, Ŝe gaz składa się z tylko 0 cząsteczek, i Ŝe początkowo cząsteczki te zajmują całą objętość pojemnika. Wtedy szansa, Ŝe jedna konkretna cząsteczka będzie znajdować się w lewej połowie pojemnika w dowolnym momencie czasu wynosi. Szansa, Ŝe dowolne dwie wybrane cząsteczki znajdują się w lewej połowie jest równa = 4. Szansa, Ŝe trzy wybrane cząstki znajdą się w lewej połowie wyniesie 3 = =. Prawdopodobieństwo, Ŝe wszystkie 0 cząsteczek znajdzie się w 8 lewej połówce naczynia jest równa 0 = 04. o oznacza, Ŝe jest jedna szansa na 04 moŝliwości, Ŝe wszystkie 0 cząstek będzie znajdować się w lewej części naczynia w określonej chwili. ChociaŜ takie prawdopodobieństwo znalezienia się wszystkich 0 cząstek w jednej połowie zbiornika jest małe, to mimo wszystko, nie bylibyśmy całkowicie zaskoczeni gdyby, rzeczywiście, miało to miejsce. JeŜeli oglądalibyśmy gaz jeden raz przez sekundę, to moglibyśmy oczekiwać, Ŝe taka sytuacja pojawi się po 04s, lub inaczej, raz na 7 minut. JeŜeli początkowo mielibyśmy dziesięć przypadkowo rozłoŝonych cząsteczek w całym naczyniu, a potem znaleźlibyśmy je wszystkie w lewej połowie początkowej objętości naczynia, to entropia wszechświata zmalała by o nr ln. Jednak to zmniejszenie jest ekstremalnie małe poniewaŝ ilość moli odpowiadających dziesięciu cząsteczkom wynosi tylko około 0-3. Jednak w dalszym ciągu naruszało by to drugą zasadę termodynamiki sformułowaną w oparciu o definicję entropii, która mówi, Ŝe dla dowolnego procesu entropia wszechświata nie moŝe zmaleć. JeŜeli chcielibyśmy zastosować drugą zasadę termodynamiki do tak niewielkiej ilości cząsteczek, to powinniśmy ją sformułować w kategoriach prawdopodobieństwa. MoŜemy znaleźć związek między prawdopodobieństwem gazu spręŝającemu się spontanicznie i zmniejszającemu swoją objętość, a zmianą jego entropii. JeŜeli początkowa Jest to taka sama szansa, jak wtedy gdy moneta podrzucona dwa razy upadnie dwa razy orłem do góry.
13 Wykład z fizyki, Piotr Posmykiewicz 00 wartość objętości wynosi, to prawdopodobieństwo p znalezienia N cząsteczek w mniejszej objętości jest równe: p = N Logarytmując powyŝsze równanie stronami otrzymamy: gdzie n jest ilością moli i p = N ln = nn ln ln A 5-3 S = nrln N A jest liczbą Avogadra. Zmiana entropii tego gazu wynosi : 5-4 ( entropia ta jest ujemna, jeŝeli jest mniejsze od, ) Porównując wzory 5-3 i 5-4 widzimy, Ŝe gdzie k jest stałą Boltzmanna. R S = ln p = k ln p 5-5 N A MoŜe być to trochę denerwujące, jeŝeli zdamy sobie sprawę, Ŝe takie zdarzenia jak spontaniczne spręŝanie gazu lub spontaniczne przewodzenie ciepła ze zbiornika chłodniejszego do cieplejszego ( procesy, dla których S < 0 ) są tylko nieprawdopodobne, ale nie niemoŝliwe. Jednak, tak jak widzieliśmy, sensowne prawdopodobieństwo zajścia zjawiska istnieje tylko wtedy, jeŝeli ilość cząstek, z których składa się układ jest bardzo mała. ermodynamika, jako taka, jest jednak stosowana do układów makroskopowych, czyli składających się z ogromnej liczby cząsteczek. Spróbujmy zmierzyć ciśnienie gazu składającego się tylko z dziesięciu cząsteczek. Ciśnienie takie będzie zmieniać się istotnie w zaleŝności od tego czy Ŝadna, dwie, lub dziesięć cząsteczek będzie uderzać w ściankę naczynia w czasie dokonywania pomiaru. Zmiany makroskopowe ciśnienia i temperatury są, po prostu, niestosowalne do układów mikroskopowych składających się tylko z dziesięciu cząsteczek. JeŜeli zwiększymy ilość cząsteczek układu, to szansa pojawienia się zdarzenia, dla którego wszech S < 0 zmaleje w sposób bardzo drastyczny. Na przykład, jeŝeli mamy 50 cząsteczek w naczyniu, to szansa znalezienia ich wszystkich w lewej połowie naczynia wyniesie
14 Wykład z fizyki, Piotr Posmykiewicz Zatem patrząc na gaz raz w ciągu sekundy moŝemy oczekiwać, Ŝe zobaczymy je wszystkie w lewej części naczynia raz na 0 5 s, czyli jeden raz na 36 milionów lat! Dla jednego mola = 6 X 0 3 cząstek szansa, Ŝe wszystkie zbiorą się tylko w lewej połowie naczynia praktycznie nieskończenie małe, w istocie, równe zero. Dla układów makroskopowych prawdopodobieństwo procesu kończącego się zmniejszeniem entropii wszechświata jest tak granicznie małe, Ŝe zanika rozróŝnienie między pojęciami nieprawdopodobny, a niemoŝliwy.
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Wykład FIZYKA I. 14. Termodynamika fenomenologiczna cz.ii. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
Wykład 1 i 2. Termodynamika klasyczna, gaz doskonały
 Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Wykład 7: Przekazywanie energii elementy termodynamiki
 Wykład 7: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ emperatura Fenomenologicznie wielkość informująca o tym jak ciepłe/zimne
Wykład 7: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ emperatura Fenomenologicznie wielkość informująca o tym jak ciepłe/zimne
b) Wybierz wszystkie zdania prawdziwe, które odnoszą się do przemiany 2.
 Sprawdzian 8A. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach. a) Wybierz spośród nich wszystkie zdania
Sprawdzian 8A. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach. a) Wybierz spośród nich wszystkie zdania
= = Budowa materii. Stany skupienia materii. Ilość materii (substancji) n - ilość moli, N liczba molekuł (atomów, cząstek), N A
 Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
TERMODYNAMIKA FENOMENOLOGICZNA
 TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12
 Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
TERMODYNAMIKA. przykłady zastosowań. I.Mańkowski I LO w Lęborku
 TERMODYNAMIKA przykłady zastosowań I.Mańkowski I LO w Lęborku 2016 UKŁAD TERMODYNAMICZNY Dla przykładu układ termodynamiczny stanowią zamknięty cylinder z ruchomym tłokiem, w którym znajduje się gaz tak
TERMODYNAMIKA przykłady zastosowań I.Mańkowski I LO w Lęborku 2016 UKŁAD TERMODYNAMICZNY Dla przykładu układ termodynamiczny stanowią zamknięty cylinder z ruchomym tłokiem, w którym znajduje się gaz tak
Ciepło i pierwsza zasada termodynamiki.
 Wykład z fizyki, Piotr Posmykiewicz 162 W Y K Ł A D XIII Ciepło i pierwsza zasada termodynamiki. Ciepło jest energią, która jest przekazywana z jednego układu do drugiego w wyniku róŝnicy temperatur obu
Wykład z fizyki, Piotr Posmykiewicz 162 W Y K Ł A D XIII Ciepło i pierwsza zasada termodynamiki. Ciepło jest energią, która jest przekazywana z jednego układu do drugiego w wyniku róŝnicy temperatur obu
WYKŁAD 2 TERMODYNAMIKA. Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami
 WYKŁAD 2 TERMODYNAMIKA Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami Zasada zerowa Kiedy obiekt gorący znajduje się w kontakcie cieplnym z obiektem zimnym następuje
WYKŁAD 2 TERMODYNAMIKA Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami Zasada zerowa Kiedy obiekt gorący znajduje się w kontakcie cieplnym z obiektem zimnym następuje
Fizyka 14. Janusz Andrzejewski
 Fizyka 14 Janusz Andrzejewski Egzaminy Egzaminy odbywają się w salach 3 oraz 314 budynek A1 w godzinach od 13.15 do 15.00 I termin 4 luty 013 poniedziałek II termin 1 luty 013 wtorek Na wykład zapisanych
Fizyka 14 Janusz Andrzejewski Egzaminy Egzaminy odbywają się w salach 3 oraz 314 budynek A1 w godzinach od 13.15 do 15.00 I termin 4 luty 013 poniedziałek II termin 1 luty 013 wtorek Na wykład zapisanych
Termodynamika. Część 4. Procesy izoparametryczne Entropia Druga zasada termodynamiki. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Wykład 7 Entalpia: odwracalne izobaryczne rozpręŝanie gazu, adiabatyczne dławienie gazu dla przepływu ustalonego, nieodwracalne napełnianie gazem
 Wykład 7 Entalpia: odwracalne izobaryczne rozpręŝanie gazu, adiabatyczne dławienie gazu dla przepływu ustalonego, nieodwracalne napełnianie gazem pustego zbiornika rzy metody obliczeń entalpii gazu doskonałego
Wykład 7 Entalpia: odwracalne izobaryczne rozpręŝanie gazu, adiabatyczne dławienie gazu dla przepływu ustalonego, nieodwracalne napełnianie gazem pustego zbiornika rzy metody obliczeń entalpii gazu doskonałego
Temperatura jest wspólną własnością dwóch ciał, które pozostają ze sobą w równowadze termicznej.
 1 Ciepło jest sposobem przekazywania energii z jednego ciała do drugiego. Ciepło przepływa pod wpływem różnicy temperatur. Jeżeli ciepło nie przepływa mówimy o stanie równowagi termicznej. Zerowa zasada
1 Ciepło jest sposobem przekazywania energii z jednego ciała do drugiego. Ciepło przepływa pod wpływem różnicy temperatur. Jeżeli ciepło nie przepływa mówimy o stanie równowagi termicznej. Zerowa zasada
Wykład 6: Przekazywanie energii elementy termodynamiki
 Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Wykład 6: Przekazywanie energii elementy termodynamiki
 Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
b) Wybierz wszystkie zdania prawdziwe, które odnoszą się do przemiany 2.
 Fizyka Z fizyką w przyszłość Sprawdzian 8B Sprawdzian 8B. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach.
Fizyka Z fizyką w przyszłość Sprawdzian 8B Sprawdzian 8B. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach.
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Termodynamika. Cel. Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa. William Thomson 1. Baron Kelvin
 Cel Termodynamika Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa Nicolas Léonard Sadi Carnot 1796 1832 Rudolf Clausius 1822 1888 William Thomson 1. Baron Kelvin 1824 1907 i inni...
Cel Termodynamika Opis układu niezależny od jego struktury mikroskopowej Uniwersalne prawa Nicolas Léonard Sadi Carnot 1796 1832 Rudolf Clausius 1822 1888 William Thomson 1. Baron Kelvin 1824 1907 i inni...
Fizyka 1 Wróbel Wojciech. w poprzednim odcinku
 w poprzednim odcinku 1 Kinetyczna teoria gazów AZ DOSKONAŁY Liczba rozważanych cząsteczek gazu jest bardzo duża. Średnia odległość między cząsteczkami jest znacznie większa niż ich rozmiar. Cząsteczki
w poprzednim odcinku 1 Kinetyczna teoria gazów AZ DOSKONAŁY Liczba rozważanych cząsteczek gazu jest bardzo duża. Średnia odległość między cząsteczkami jest znacznie większa niż ich rozmiar. Cząsteczki
T 1 > T 2 U = 0. η = = = - jest to sprawność maszyny cieplnej. ε = 1 q. Sprawność maszyn cieplnych. Z II zasady termodynamiki wynika:
 Sprawność maszyn cieplnych. Z II zasady termodynamiki wynika: Zamiana ciepła na pracę przez cyklicznie działającą maszynę cieplną jest możliwa tylko przy wykorzystaniu dwóch zbiorników ciepła o różnych
Sprawność maszyn cieplnych. Z II zasady termodynamiki wynika: Zamiana ciepła na pracę przez cyklicznie działającą maszynę cieplną jest możliwa tylko przy wykorzystaniu dwóch zbiorników ciepła o różnych
Termodynamika. Energia wewnętrzna ciał
 ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
S ścianki naczynia w jednostce czasu przekazywany
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
Druga zasada termodynamiki.
 Wykład z fizyki, Piotr Posmykiewicz 79 W Y K Ł A D XIV Druga zasada termodynamiki. Często naszym zadaniem jest zastosowanie zasady zachowania energii. Jednak, zgodnie z pierwszą zasadą termodynamiki, energia
Wykład z fizyki, Piotr Posmykiewicz 79 W Y K Ł A D XIV Druga zasada termodynamiki. Często naszym zadaniem jest zastosowanie zasady zachowania energii. Jednak, zgodnie z pierwszą zasadą termodynamiki, energia
Termodynamika. Część 5. Procesy cykliczne Maszyny cieplne. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 5 Procesy cykliczne Maszyny cieplne Janusz Brzychczyk, Instytut Fizyki UJ Z pierwszej zasady termodynamiki: Procesy cykliczne du = Q el W el =0 W cyklu odwracalnym (złożonym z procesów
Termodynamika Część 5 Procesy cykliczne Maszyny cieplne Janusz Brzychczyk, Instytut Fizyki UJ Z pierwszej zasady termodynamiki: Procesy cykliczne du = Q el W el =0 W cyklu odwracalnym (złożonym z procesów
Obiegi gazowe w maszynach cieplnych
 OBIEGI GAZOWE Obieg cykl przemian, po przejściu których stan końcowy czynnika jest identyczny ze stanem początkowym. Obrazem geometrycznym obiegu jest linia zamknięta. Dla obiegu termodynamicznego: przyrost
OBIEGI GAZOWE Obieg cykl przemian, po przejściu których stan końcowy czynnika jest identyczny ze stanem początkowym. Obrazem geometrycznym obiegu jest linia zamknięta. Dla obiegu termodynamicznego: przyrost
TERMODYNAMIKA Zajęcia wyrównawcze, Częstochowa, 2009/2010 Ewa Mandowska
 1. Bilans cieplny 2. Przejścia fazowe 3. Równanie stanu gazu doskonałego 4. I zasada termodynamiki 5. Przemiany gazu doskonałego 6. Silnik cieplny 7. II zasada termodynamiki TERMODYNAMIKA Zajęcia wyrównawcze,
1. Bilans cieplny 2. Przejścia fazowe 3. Równanie stanu gazu doskonałego 4. I zasada termodynamiki 5. Przemiany gazu doskonałego 6. Silnik cieplny 7. II zasada termodynamiki TERMODYNAMIKA Zajęcia wyrównawcze,
Pierwsza i druga zasada termodynamiki.
 Pierwsza i druga zasada termodynamiki. Jaki jest sens fizyczny tego równania? E= W Zmiana energii ciała równa jest pracy wykonanej nad tym ciałem przez siły zewnętrzne lub przez to ciało. Kiedy praca jest
Pierwsza i druga zasada termodynamiki. Jaki jest sens fizyczny tego równania? E= W Zmiana energii ciała równa jest pracy wykonanej nad tym ciałem przez siły zewnętrzne lub przez to ciało. Kiedy praca jest
FIZYKA STATYSTYCZNA. d dp. jest sumaryczną zmianą pędu cząsteczek zachodzącą na powierzchni S w
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
Wykład Temperatura termodynamiczna 6.4 Nierówno
 ykład 8 6.3 emperatura termodynamiczna 6.4 Nierówność Clausiusa 6.5 Makroskopowa definicja entropii oraz zasada wzrostu entropii 6.6 Entropia dla czystej substancji 6.8 Cykl Carnota 6.7 Entropia dla gazu
ykład 8 6.3 emperatura termodynamiczna 6.4 Nierówność Clausiusa 6.5 Makroskopowa definicja entropii oraz zasada wzrostu entropii 6.6 Entropia dla czystej substancji 6.8 Cykl Carnota 6.7 Entropia dla gazu
Podstawy termodynamiki
 Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
100 29,538 21,223 38,112 29, ,118 24,803 49,392 41,077
 . Jak określa się ilość substancji? Ile kilogramów substancji zawiera mol wody?. Zbiornik zawiera 5 kmoli CO. Ile kilogramów CO znajduje się w zbiorniku? 3. Jaka jest definicja I zasady termodynamiki dla
. Jak określa się ilość substancji? Ile kilogramów substancji zawiera mol wody?. Zbiornik zawiera 5 kmoli CO. Ile kilogramów CO znajduje się w zbiorniku? 3. Jaka jest definicja I zasady termodynamiki dla
Przemiany gazowe. 4. Który z poniższych wykresów reprezentuje przemianę izobaryczną: 5. Który z poniższych wykresów obrazuje przemianę izochoryczną:
 Przemiany gazowe 1. Czy możliwa jest przemiana gazowa, w której temperatura i objętość pozostają stałe, a ciśnienie rośnie: a. nie b. jest możliwa dla par c. jest możliwa dla gazów doskonałych 2. W dwóch
Przemiany gazowe 1. Czy możliwa jest przemiana gazowa, w której temperatura i objętość pozostają stałe, a ciśnienie rośnie: a. nie b. jest możliwa dla par c. jest możliwa dla gazów doskonałych 2. W dwóch
Termodynamika cz.1. Ziarnista budowa materii. Jak wielka jest liczba Avogadro? Podstawowe definicje. Notes. Notes. Notes. Notes
 Termodynamika cz.1 dr inż. Ireneusz Owczarek CNMiF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 1 dr inż. Ireneusz Owczarek Termodynamika cz.1 Ziarnista budowa materii Ziarnista budowa
Termodynamika cz.1 dr inż. Ireneusz Owczarek CNMiF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 1 dr inż. Ireneusz Owczarek Termodynamika cz.1 Ziarnista budowa materii Ziarnista budowa
3. Przyrost temperatury gazu wynosi 20 C. Ile jest równy ten przyrost w kelwinach?
 1. Która z podanych niżej par wielkości fizycznych ma takie same jednostki? a) energia i entropia b) ciśnienie i entalpia c) praca i entalpia d) ciepło i temperatura 2. 1 kj nie jest jednostką a) entropii
1. Która z podanych niżej par wielkości fizycznych ma takie same jednostki? a) energia i entropia b) ciśnienie i entalpia c) praca i entalpia d) ciepło i temperatura 2. 1 kj nie jest jednostką a) entropii
Jednostki podstawowe. Tuż po Wielkim Wybuchu temperatura K Teraz ok. 3K. Długość metr m
 TERMODYNAMIKA Jednostki podstawowe Wielkość Nazwa Symbol Długość metr m Masa kilogramkg Czas sekunda s Natężenieprąduelektrycznego amper A Temperaturatermodynamicznakelwin K Ilość materii mol mol Światłość
TERMODYNAMIKA Jednostki podstawowe Wielkość Nazwa Symbol Długość metr m Masa kilogramkg Czas sekunda s Natężenieprąduelektrycznego amper A Temperaturatermodynamicznakelwin K Ilość materii mol mol Światłość
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Wykład Praca (1.1) c Całka liniowa definiuje pracę wykonaną w kierunku działania siły. Reinhard Kulessa 1
 1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
Termodynamiczny opis przejść fazowych pierwszego rodzaju
 Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
Maszyny cieplne substancja robocza
 Maszyny cieplne cel: zamiana ciepła na pracę (i odwrotnie) pracują cyklicznie pracę wykonuje substancja robocza (np.gaz, mieszanka paliwa i powietrza) która: pochłania ciepło dostarczane ze źródła ciepła
Maszyny cieplne cel: zamiana ciepła na pracę (i odwrotnie) pracują cyklicznie pracę wykonuje substancja robocza (np.gaz, mieszanka paliwa i powietrza) która: pochłania ciepło dostarczane ze źródła ciepła
Obieg Ackeret Kellera i lewobieżny obieg Philipsa (Stirlinga) podstawy teoretyczne i techniczne możliwości realizacji
 Obieg Ackeret Kellera i lewobieżny obieg Philipsa (Stirlinga) podstawy teoretyczne i techniczne możliwości realizacji Monika Litwińska Inżynieria Mechaniczno-Medyczna GDAŃSKA 2012 1. Obieg termodynamiczny
Obieg Ackeret Kellera i lewobieżny obieg Philipsa (Stirlinga) podstawy teoretyczne i techniczne możliwości realizacji Monika Litwińska Inżynieria Mechaniczno-Medyczna GDAŃSKA 2012 1. Obieg termodynamiczny
Wykład 3. Entropia i potencjały termodynamiczne
 Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Podstawy fizyki sezon 1 X. Elementy termodynamiki
 Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
Krótki przegląd termodynamiki
 Wykład I Przejścia fazowe 1 Krótki przegląd termodynamiki Termodynamika fenomenologiczna oferuje makroskopowy opis układów statystycznych w stanie równowagi termodynamicznej bądź w stanach jemu bliskich.
Wykład I Przejścia fazowe 1 Krótki przegląd termodynamiki Termodynamika fenomenologiczna oferuje makroskopowy opis układów statystycznych w stanie równowagi termodynamicznej bądź w stanach jemu bliskich.
Przegląd termodynamiki II
 Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
ZADANIA Z FIZYKI - TERMODYNAMIKA
 ZADANIA Z FIZYKI - TERMODYNAMIKA Zad 1.(RH par 22-8 zad 36) Cylinder jest zamknięty dobrze dopasowanym metalowym tłokiem o masie 2 kg i polu powierzchni 2.0 cm 2. Cylinder zawiera wodę i parę o temperaturze
ZADANIA Z FIZYKI - TERMODYNAMIKA Zad 1.(RH par 22-8 zad 36) Cylinder jest zamknięty dobrze dopasowanym metalowym tłokiem o masie 2 kg i polu powierzchni 2.0 cm 2. Cylinder zawiera wodę i parę o temperaturze
C V dla róŝnych gazów. Widzimy C C dla wszystkich gazów jest, zgodnie z przewidywaniami równa w
 Wykład z fizyki, Piotr Posmykiewicz 7 P dt dt + nrdt i w rezultacie: nr 4-7 P + Dla gazu doskonałego pojemność cieplna przy stałym ciśnieniu jest większa od pojemności cieplnej przy stałej objętości o
Wykład z fizyki, Piotr Posmykiewicz 7 P dt dt + nrdt i w rezultacie: nr 4-7 P + Dla gazu doskonałego pojemność cieplna przy stałym ciśnieniu jest większa od pojemności cieplnej przy stałej objętości o
Układ termodynamiczny Parametry układu termodynamicznego Proces termodynamiczny Układ izolowany Układ zamknięty Stan równowagi termodynamicznej
 termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
Wykład 12 Silnik Carnota z gazem doskonałym Sprawność silnika Carnota z gazem doskonałym Współczynnik wydajności chłodziarki i pompy cieplnej Carnota
 Wykła Silnik Carnota z azem oskonałym Sprawność silnika Carnota z azem oskonałym Współczynnik wyajności chłoziarki i pompy cieplnej Carnota z azem oskonałym RównowaŜność skali temperatury termoynamicznej
Wykła Silnik Carnota z azem oskonałym Sprawność silnika Carnota z azem oskonałym Współczynnik wyajności chłoziarki i pompy cieplnej Carnota z azem oskonałym RównowaŜność skali temperatury termoynamicznej
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Drgania. W Y K Ł A D X Ruch harmoniczny prosty. k m
 Wykład z fizyki Piotr Posmykiewicz 119 W Y K Ł A D X Drgania. Drgania pojawiają się wtedy, gdy układ zostanie wytrącony ze stanu równowagi stabilnej. MoŜna przytoczyć szereg znanych przykładów: kołysząca
Wykład z fizyki Piotr Posmykiewicz 119 W Y K Ł A D X Drgania. Drgania pojawiają się wtedy, gdy układ zostanie wytrącony ze stanu równowagi stabilnej. MoŜna przytoczyć szereg znanych przykładów: kołysząca
Podstawowe pojęcia 1
 Tomasz Lubera Podstawowe pojęcia 1 Układ część przestrzeni wyodrębniona myślowo lub fizycznie z otoczenia Układ izolowany niewymieniający masy i energii z otoczeniem Układ zamknięty wymieniający tylko
Tomasz Lubera Podstawowe pojęcia 1 Układ część przestrzeni wyodrębniona myślowo lub fizycznie z otoczenia Układ izolowany niewymieniający masy i energii z otoczeniem Układ zamknięty wymieniający tylko
K raków 26 ma rca 2011 r.
 K raków 26 ma rca 2011 r. Zadania do ćwiczeń z Podstaw Fizyki na dzień 1 kwietnia 2011 r. r. dla Grupy II Zadanie 1. 1 kg/s pary wo dne j o ciśnieniu 150 atm i temperaturze 342 0 C wpada do t urbiny z
K raków 26 ma rca 2011 r. Zadania do ćwiczeń z Podstaw Fizyki na dzień 1 kwietnia 2011 r. r. dla Grupy II Zadanie 1. 1 kg/s pary wo dne j o ciśnieniu 150 atm i temperaturze 342 0 C wpada do t urbiny z
Plan wykładu. Termodynamika cz.1. Jak wielka jest liczba Avogadro? Ziarnista budowa materii
 Plan wykładu Termodynamika cz1 dr inż Ireneusz Owczarek CMF PŁ ireneuszowczarek@plodzpl http://cmfplodzpl/iowczarek 2012/13 1 Ziarnista budowa materii Liczba Avogadro 2 Temperatura termodynamiczna 3 Sposoby
Plan wykładu Termodynamika cz1 dr inż Ireneusz Owczarek CMF PŁ ireneuszowczarek@plodzpl http://cmfplodzpl/iowczarek 2012/13 1 Ziarnista budowa materii Liczba Avogadro 2 Temperatura termodynamiczna 3 Sposoby
Gaz rzeczywisty zachowuje się jak modelowy gaz doskonały, gdy ma małą gęstość i umiarkowaną
 F-Gaz doskonaly/ GAZY DOSKONAŁE i PÓŁDOSKONAŁE Gaz doskonały cząsteczki są bardzo małe w porównaniu z objętością naczynia, które wypełnia gaz cząsteczki poruszają się chaotycznie ruchem postępowym i zderzają
F-Gaz doskonaly/ GAZY DOSKONAŁE i PÓŁDOSKONAŁE Gaz doskonały cząsteczki są bardzo małe w porównaniu z objętością naczynia, które wypełnia gaz cząsteczki poruszają się chaotycznie ruchem postępowym i zderzają
Termodynamika Techniczna dla MWT, wykład 7. AJ Wojtowicz IF UMK
 Wykład 7. Entalpia układu termodynamicznego.. Entalpia; odwracalne izobaryczne rozpręŝanie gazu.2. Entalpia; adiabatyczne dławienie gazu dla przepływu ustalonego.3. Entalpia; nieodwracalne napełnianie
Wykład 7. Entalpia układu termodynamicznego.. Entalpia; odwracalne izobaryczne rozpręŝanie gazu.2. Entalpia; adiabatyczne dławienie gazu dla przepływu ustalonego.3. Entalpia; nieodwracalne napełnianie
Plan wykładu. Termodynamika cz.1. Jak wielka jest liczba Avogadro? Ziarnista budowa materii
 Plan wykładu Termodynamika cz1 dr inż Ireneusz Owczarek CMF PŁ ireneuszowczarek@plodzpl http://cmfplodzpl/iowczarek 2013/14 1 Ziarnista budowa materii Liczba Avogadro 2 Pomiary temperatury Temperatura
Plan wykładu Termodynamika cz1 dr inż Ireneusz Owczarek CMF PŁ ireneuszowczarek@plodzpl http://cmfplodzpl/iowczarek 2013/14 1 Ziarnista budowa materii Liczba Avogadro 2 Pomiary temperatury Temperatura
GAZ DOSKONAŁY. Brak oddziaływań między cząsteczkami z wyjątkiem zderzeń idealnie sprężystych.
 TERMODYNAMIKA GAZ DOSKONAŁY Gaz doskonały to abstrakcyjny, matematyczny model gazu, chociaż wiele gazów (azot, tlen) w warunkach normalnych zachowuje się w przybliżeniu jak gaz doskonały. Model ten zakłada:
TERMODYNAMIKA GAZ DOSKONAŁY Gaz doskonały to abstrakcyjny, matematyczny model gazu, chociaż wiele gazów (azot, tlen) w warunkach normalnych zachowuje się w przybliżeniu jak gaz doskonały. Model ten zakłada:
Ciepła tworzenia i spalania (3)
 Ciepła tworzenia i spalania (3) Standardowa entalpia tworzenia jest standardową entalpią związku 0 0 H = H Dla pierwiastków: Dla związków: H H 98 tw,98 0 tw, = C p ( ) d 98 0 0 tw, = Htw,98 + C p ( ) 98
Ciepła tworzenia i spalania (3) Standardowa entalpia tworzenia jest standardową entalpią związku 0 0 H = H Dla pierwiastków: Dla związków: H H 98 tw,98 0 tw, = C p ( ) d 98 0 0 tw, = Htw,98 + C p ( ) 98
Maszyny cieplne i II zasada termodynamiki
 Maszyny cieplne i II zasada termodynamiki Maszyny cieplne, chłodnie i pompy tlenowe II zasada termodynamiki Cykl Carnot a Entropia termodynamiczna definicja II zasada termodynamiki i entropia Cykle termodynamiczne.
Maszyny cieplne i II zasada termodynamiki Maszyny cieplne, chłodnie i pompy tlenowe II zasada termodynamiki Cykl Carnot a Entropia termodynamiczna definicja II zasada termodynamiki i entropia Cykle termodynamiczne.
Rozwiązanie: Rozwiązanie najlepiej rozpocząć od sporządzenia szkicu, który jest pierwszym stopniem zrozumienia opisywanego procesu (serii przemian).
 Nowe zadania z termodynamiki. 06.0.00. Zadanie. 0/8, moli gazu azotu (traktować jako gaz doskonały), znajdującego się początkowo (stan ) w warunkach T =00K, =0 a, przechodzi następującą serię przemian
Nowe zadania z termodynamiki. 06.0.00. Zadanie. 0/8, moli gazu azotu (traktować jako gaz doskonały), znajdującego się początkowo (stan ) w warunkach T =00K, =0 a, przechodzi następującą serię przemian
Kinetyczna teoria gazów Termodynamika. dr Mikołaj Szopa Wykład
 Kinetyczna teoria gazów Termodynamika dr Mikołaj Szopa Wykład 7.11.015 Kinetyczna teoria gazów Kinetyczna teoria gazów. Termodynamika Termodynamika klasyczna opisuje tylko wielkości makroskopowe takie
Kinetyczna teoria gazów Termodynamika dr Mikołaj Szopa Wykład 7.11.015 Kinetyczna teoria gazów Kinetyczna teoria gazów. Termodynamika Termodynamika klasyczna opisuje tylko wielkości makroskopowe takie
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Stany skupienia materii
 Stany skupienia materii Ciała stałe Ciecze Płyny Gazy Plazma 1 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -
Stany skupienia materii Ciała stałe Ciecze Płyny Gazy Plazma 1 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -
Fizyka Termodynamika Chemia reakcje chemiczne
 Termodynamika zajmuje się badaniem efektów energetycznych towarzyszących procesom fizykochemicznym i chemicznym. Termodynamika umożliwia: 1. Sporządzanie bilansów energetycznych dla reakcji chemicznych
Termodynamika zajmuje się badaniem efektów energetycznych towarzyszących procesom fizykochemicznym i chemicznym. Termodynamika umożliwia: 1. Sporządzanie bilansów energetycznych dla reakcji chemicznych
Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }
![Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] } Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }](/thumbs/64/51033976.jpg) Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
Kontakt,informacja i konsultacje
 Kontakt,informacja i konsultacje Chemia A ; pokój 307 elefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl tablica ogłoszeń Katedry Chemii Fizycznej http://www.pg.gda.pl/chem/dydaktyka/ lub http://www.pg.gda.pl/chem/katedry/fizyczna
Kontakt,informacja i konsultacje Chemia A ; pokój 307 elefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl tablica ogłoszeń Katedry Chemii Fizycznej http://www.pg.gda.pl/chem/dydaktyka/ lub http://www.pg.gda.pl/chem/katedry/fizyczna
10. FALE, ELEMENTY TERMODYNAMIKI I HYDRODY- NAMIKI.
 0. FALE, ELEMENY ERMODYNAMIKI I HYDRODY- NAMIKI. 0.9. Podstawy termodynamiki i raw gazowych. Podstawowe ojęcia Gaz doskonały: - cząsteczki są unktami materialnymi, - nie oddziałują ze sobą siłami międzycząsteczkowymi,
0. FALE, ELEMENY ERMODYNAMIKI I HYDRODY- NAMIKI. 0.9. Podstawy termodynamiki i raw gazowych. Podstawowe ojęcia Gaz doskonały: - cząsteczki są unktami materialnymi, - nie oddziałują ze sobą siłami międzycząsteczkowymi,
ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa
 Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii
 Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Wykład 1. Anna Ptaszek. 5 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 1. Anna Ptaszek 1 / 36
 Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
1. PIERWSZA I DRUGA ZASADA TERMODYNAMIKI TERMOCHEMIA
 . PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
. PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
Techniki niskotemperaturowe w medycynie
 INŻYNIERIA MECHANICZNO-MEDYCZNA WYDZIAŁ MECHANICZNY POLITECHNIKA GDAŃSKA Techniki niskotemperaturowe w medycynie Temat: Lewobieżny obieg gazowy Joule a a obieg parowy Lindego Prowadzący: dr inż. Zenon
INŻYNIERIA MECHANICZNO-MEDYCZNA WYDZIAŁ MECHANICZNY POLITECHNIKA GDAŃSKA Techniki niskotemperaturowe w medycynie Temat: Lewobieżny obieg gazowy Joule a a obieg parowy Lindego Prowadzący: dr inż. Zenon
Zmiana energii wewnętrznej ciała lub układu ciał jest równa sumie dostarczonego ciepła i pracy wykonanej nad ciałem lub układem ciał.
 Temat : Pierwsza zasada termodynamiki. Wyobraźmy sobie następującą sytuację : Jest zima. Temperatura poniżej zera. W wyniku długotrwałego wystawiania dłoni na działanie lodowatego powietrza, odczuwamy,
Temat : Pierwsza zasada termodynamiki. Wyobraźmy sobie następującą sytuację : Jest zima. Temperatura poniżej zera. W wyniku długotrwałego wystawiania dłoni na działanie lodowatego powietrza, odczuwamy,
Zasady termodynamiki
 Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Elementy fizyki statystycznej
 5-- lementy fizyki statystycznej ermodynamika Gęstości stanów Funkcje rozkładu Gaz elektronów ermodynamika [K] 9 wszechświat tuż po powstaniu ermodynamika to dział fizyki zajmujący się energią termiczną
5-- lementy fizyki statystycznej ermodynamika Gęstości stanów Funkcje rozkładu Gaz elektronów ermodynamika [K] 9 wszechświat tuż po powstaniu ermodynamika to dział fizyki zajmujący się energią termiczną
Teoria kinetyczna gazów
 Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
Termodynamika program wykładu
 Termodynamika program wykładu Wiadomości wstępne: fizyka statystyczna a termodynamika masa i rozmiary cząstek stan układu, przemiany energia wewnętrzna pierwsza zasada termodynamiki praca wykonana przez
Termodynamika program wykładu Wiadomości wstępne: fizyka statystyczna a termodynamika masa i rozmiary cząstek stan układu, przemiany energia wewnętrzna pierwsza zasada termodynamiki praca wykonana przez
1. 1 J/(kg K) nie jest jednostką a) entropii właściwej b) indywidualnej stałej gazowej c) ciepła właściwego d) pracy jednostkowej
 1. 1 J/(kg K) nie jest jednostką a) entropii właściwej b) indywidualnej stałej gazowej c) ciepła właściwego d) pracy jednostkowej 2. 1 kmol każdej substancji charakteryzuje się taką samą a) masą b) objętością
1. 1 J/(kg K) nie jest jednostką a) entropii właściwej b) indywidualnej stałej gazowej c) ciepła właściwego d) pracy jednostkowej 2. 1 kmol każdej substancji charakteryzuje się taką samą a) masą b) objętością
TERMODYNAMIKA I TERMOCHEMIA
 TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów
 Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny
 Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Spis treści. PRZEDMOWA. 11 WYKAZ WAśNIEJSZYCH OZNACZEŃ. 13 I. POJĘCIA PODSTAWOWE W TERMODYNAMICE. 19
 Spis treści PRZEDMOWA. 11 WYKAZ WAśNIEJSZYCH OZNACZEŃ. 13 I. POJĘCIA PODSTAWOWE W TERMODYNAMICE. 19 Wykład 1: WPROWADZENIE DO PRZEDMIOTU 19 1.1. Wstęp... 19 1.2. Metody badawcze termodynamiki... 21 1.3.
Spis treści PRZEDMOWA. 11 WYKAZ WAśNIEJSZYCH OZNACZEŃ. 13 I. POJĘCIA PODSTAWOWE W TERMODYNAMICE. 19 Wykład 1: WPROWADZENIE DO PRZEDMIOTU 19 1.1. Wstęp... 19 1.2. Metody badawcze termodynamiki... 21 1.3.
Ciśnienie i temperatura model mikroskopowy
 Ciśnienie i temperatura model mikroskopowy Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy
Ciśnienie i temperatura model mikroskopowy Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy
00516 Termodynamika D Część 1
 1 00516 Termodynamika D Dane osobowe właściciela arkusza 00516 Termodynamika D Część 1 Energia wewnętrzna. I zasada termodynamiki Ciepło właściwe i przemiany fazowej Model gazów doskonałych Aktualizacja
1 00516 Termodynamika D Dane osobowe właściciela arkusza 00516 Termodynamika D Część 1 Energia wewnętrzna. I zasada termodynamiki Ciepło właściwe i przemiany fazowej Model gazów doskonałych Aktualizacja
Przemiany termodynamiczne
 Przemiany termodynamiczne.:: Przemiana adiabatyczna ::. Przemiana adiabatyczna (Proces adiabatyczny) - proces termodynamiczny, podczas którego wyizolowany układ nie nawiązuje wymiany ciepła, lecz całość
Przemiany termodynamiczne.:: Przemiana adiabatyczna ::. Przemiana adiabatyczna (Proces adiabatyczny) - proces termodynamiczny, podczas którego wyizolowany układ nie nawiązuje wymiany ciepła, lecz całość
4. 1 bar jest dokładnie równy a) Pa b) 100 Tr c) 1 at d) 1 Atm e) 1000 niutonów na metr kwadratowy f) 0,1 MPa
 1. Adiatermiczny wymiennik ciepła to wymiennik, w którym a) ciepło płynie od czynnika o niższej temperaturze do czynnika o wyższej temperaturze b) nie ma strat ciepła na rzecz otoczenia c) czynniki wymieniające
1. Adiatermiczny wymiennik ciepła to wymiennik, w którym a) ciepło płynie od czynnika o niższej temperaturze do czynnika o wyższej temperaturze b) nie ma strat ciepła na rzecz otoczenia c) czynniki wymieniające
Rodzaje pracy mechanicznej
 Rodzaje pracy mechanicznej. Praca bezwzględna Jest to praca przekazana przez czynnik termodynamiczny na wewnętrzną stronę denka tłoka. Podczas beztarciowej przemiany kwazystatycznej praca przekazana oczeniu
Rodzaje pracy mechanicznej. Praca bezwzględna Jest to praca przekazana przez czynnik termodynamiczny na wewnętrzną stronę denka tłoka. Podczas beztarciowej przemiany kwazystatycznej praca przekazana oczeniu
3. Przejścia fazowe pomiędzy trzema stanami skupienia materii:
 Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
Równanie gazu doskonałego
 Równanie gazu doskonałego Gaz doskonały to abstrakcyjny model gazu, który zakłada, że gaz jest zbiorem sprężyście zderzających się kulek. Wiele gazów w warunkach normalnych zachowuje się jak gaz doskonały.
Równanie gazu doskonałego Gaz doskonały to abstrakcyjny model gazu, który zakłada, że gaz jest zbiorem sprężyście zderzających się kulek. Wiele gazów w warunkach normalnych zachowuje się jak gaz doskonały.
Termochemia elementy termodynamiki
 Termochemia elementy termodynamiki Termochemia nauka zajmująca się badaniem efektów cieplnych reakcji chemicznych Zasada zachowania energii Energia całkowita jest sumą energii kinetycznej i potencjalnej.
Termochemia elementy termodynamiki Termochemia nauka zajmująca się badaniem efektów cieplnych reakcji chemicznych Zasada zachowania energii Energia całkowita jest sumą energii kinetycznej i potencjalnej.
Temodynamika Roztwór N 2 i Ar (gazów doskonałych) ma wykładnik adiabaty κ = 1.5. Określić molowe udziały składników. 1.7
 Temodynamika Zadania 2016 0 Oblicz: 1 1.1 10 cm na stopy, 60 stóp na metry, 50 ft 2 na metry. 45 m 2 na ft 2 g 40 cm na uncję na stopę sześcienną, na uncję na cal sześcienny 3 60 g cm na funt na stopę
Temodynamika Zadania 2016 0 Oblicz: 1 1.1 10 cm na stopy, 60 stóp na metry, 50 ft 2 na metry. 45 m 2 na ft 2 g 40 cm na uncję na stopę sześcienną, na uncję na cal sześcienny 3 60 g cm na funt na stopę
Podstawy Procesów i Konstrukcji Inżynierskich. Praca, moc, energia INZYNIERIAMATERIALOWAPL. Kierunek Wyróżniony przez PKA
 Podstawy Procesów i Konstrukcji Inżynierskich Praca, moc, energia Energia Energia jest to wielkość skalarna, charakteryzująca stan, w jakim znajduje się jedno lub wiele ciał. Energia jest miarą różnych
Podstawy Procesów i Konstrukcji Inżynierskich Praca, moc, energia Energia Energia jest to wielkość skalarna, charakteryzująca stan, w jakim znajduje się jedno lub wiele ciał. Energia jest miarą różnych
Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne
 Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne W3. Zjawiska transportu Zjawiska transportu zachodzą gdy układ dąży do stanu równowagi. W zjawiskach
Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne W3. Zjawiska transportu Zjawiska transportu zachodzą gdy układ dąży do stanu równowagi. W zjawiskach
(równanie Bernoulliego) (15.29)
 Lekcja 5 Temat: Równanie ernoulliego. Równanie ernoulliego. Statyczne konsekwencje równania ernoulliego a) nieruchomy płyn w zbiorniku b) manometr c) pomiar ciśnienia krwi za pomocą kaniuli Zagadnienia
Lekcja 5 Temat: Równanie ernoulliego. Równanie ernoulliego. Statyczne konsekwencje równania ernoulliego a) nieruchomy płyn w zbiorniku b) manometr c) pomiar ciśnienia krwi za pomocą kaniuli Zagadnienia
będzie momentem Twierdzenie Steinera
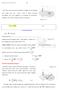 Wykład z fizyki, Piotr Posmykiewicz. Niech 90 oznacza moment bezwładności względem osi przechodzącej przez środek masy ciała o masie i niech będzie momentem bezwładności tego ciała względem osi równoległej
Wykład z fizyki, Piotr Posmykiewicz. Niech 90 oznacza moment bezwładności względem osi przechodzącej przez środek masy ciała o masie i niech będzie momentem bezwładności tego ciała względem osi równoległej
Zasady Termodynamiki
 Zasady Termodynamiki I-sza zasada termodynamiki: - bilans energii w procesie przejścia układu ze stanu A do stanu B - identyfikacja kanałów przekazu B A W oparciu o I-szą zasadę wiemy, Ŝe Przekaz moŝe
Zasady Termodynamiki I-sza zasada termodynamiki: - bilans energii w procesie przejścia układu ze stanu A do stanu B - identyfikacja kanałów przekazu B A W oparciu o I-szą zasadę wiemy, Ŝe Przekaz moŝe
