Fizyka 2 Wyk»ad W6 1 Moment pedu w mechanice kwantowej Z zasady odpowiednioñci: r h. We wspó»rz dnych kartezja½skich: We wspó»rz dnych sferycznych
|
|
|
- Judyta Nawrocka
- 5 lat temu
- Przeglądów:
Transkrypt
1 Fizyka Wyk»ad W6 1 Moment pedu w mechanice kwantowej Z zasady odpowiednioñci: We wspó»rz dnych kartezja½skich: y x - x y = i L x z - z x = i L z y - y z = i L z y x h h h ˆ ˆ ˆ We wspó»rz dnych sferycznych φ φ φ θ θ θ φ φ θ θ θ i = - L + ctg - = i L + ctg = i L z y x h h h ˆ sin cos ˆ cos sin ˆ r =-i p L=r r h r r r ˆ ˆ
2 Fizyka Wyk»ad W6 Jak widać: jedna składowa (z-towa) jest wyróŝniona. Ma to znaczenie wtedy gdy symetria sferyczna rozwaŝanego problemu zostanie złamana przez wprowadzenie wyróŝnionego kierunku w przestrzeni. Przykład: Zewnętrzne pole magnetyczne wyznacza taki wyróŝniony kierunek. Zamiast modu»u (długości) wektora momentu p du wprowadza si operator kwadratu momentu p du: L we współrzędnych sferycznych ^ = -h 1 sin ^ L = Lˆ x + Lˆ y + Lˆ 1 sinθ + θ θ sin θ φ θ Operatory momentu p du posiadaj nast pujce w»asnoñci: Operator kwadratu momentu pedu i operator jednej składowej momentu pędu komutują ^ [L, Lˆ z ] = 0 z
3 Fizyka Wyk»ad W6 3 a pozosta»e operatory nie komutuj ze sob: [ Lˆ [ Lˆ x y, Lˆ, Lˆ y z ] = Lˆ ] = Lˆ [ Lˆ z, Lˆ x ] = Lˆ y Wniosek: modu» (a raczej jego kwadrat) wektora momentu p du oraz jedn jego sk»adow moóna mierzyƒ jednoczeñnie. Uwaga: wyróŝniona składowa z-towa to ta, która odpowiada wyróŝnionemu kierunkowi w przestrzeni. Taki kierunek powstaje na skutek złamania symetrii sferycznej np. gdy przyłoŝymy zewnętrzne pole magnetyczne do badanego układu. Wypadkowe wewnętrzne pola sił w kryształach teŝ wyróŝniają kierunek w przestrzeni. operator kwadratu momentu p du oraz operator z-towej sk»adowej posiadaj wspólne funkcje w»asne (bo operatory te komutują) Lˆ z Y l,m ( θ, φ )= h m Y l,m ( θ, φ ) ^ L Y l,m ( θ, φ )= h l (l +1) Y l,m ( θ, φ ) gdzie Y m ( θ, ) s funkcjami kulistymi (są to funkcje nie elementarne). l, φ z x
4 Fizyka Wyk»ad W6 4 Przykład: Kilka pierwszych takich funkcji ma nast pujc postaƒ m (w notacji równowaŝnej Y ( θ, φ ) Y ( θ, φ )): l lm
5 Fizyka Wyk»ad W6 5 Przykład: Gęstość prawdopodobieństwa związana z kilkoma przykładowymi funkcjami sferycznymi:
6 Fizyka Wyk»ad W6 6 DoÑwiadczenie Zeemana: Przykładając pole magnetyczne do atomów gazu, Zeeman zbadał własności orbitalnego momentu magnetycznego związanego z elektronem na orbicie atomowej. Eksperyment znajdziecie odtworzony na stronie: qm/index.html {hyperlink: za pomocą programu Zeeman Spectroscopy { W eksperymencie tym, Zeman powoli zwiększał działające na atomy pole magnetyczne (elektromagnes po lewej strony obrazu) i obserwował widma optyczne (górny rysunek widm). Bez zewnętrznego pola magnetycznego otrzymano jedynie pojedynczy prąŝek (pojedyncza zielona linia)
7 Fizyka Wyk»ad W6 7 W symulacji załoŝono, Ŝe w atomie moŝe zajść tylko przejście kwantowe pomiędzy dwoma poziomami atomowymi: orbital d z 6-tej powłoki atomowej (6d) oraz orbital p z 7-mej powłoki (7p) (znaczenie tych symboli zostanie wyjaśnione poniŝej). Uwaga: na stronie internetowej jest błąd: oznaczenia orbitalu d pomylono z orbitalem p a oznaczenia orbitalu s z orbitalem d PrzyłoŜenie zewnętrznego pola magnetycznego powoduje rozszczepienie poziomów atomowych na kilka i zwielokrotnienie przejñƒ kwantowych. Orbital d rozszczepia się na 5 a orbital p na 3. Powoduje to zwielokrotnienie liczby linii widmowych jak na rysunku obok.
8 Fizyka Wyk»ad W6 8 Dzieje się tak dlatego, Ŝe: Wiadomo z doświadcze½ z przep»ywem prądu w zwojach drutu w polu magnetycznym: moment p du prądu elektrycznego w zwoju wiąŝe si z dipolowym momentem magnetycznym r e r µ r L = - L me Elektron krąŝąc po zamkniętej orbicie elektronowej teŝ posiada moment pędu zupełnie jak elektron poruszający się w zwoju drutu. W przypadku elektronu na powłoce atomowej rzut momentu pędu na kierunek wyróóniony (kierunek pola magnetycznego w tych doñwiadczeniach) jest skwantowany: e h µ - m= µ m Lz = B me gdzie m e masa elektronu µ B jest sta» fizyczn (magneton Bohra). m = - l, -l+1,..,0,..., l-1, l Skwantowanie rzutu momentu pędu (dyskretne wartości liczby kwantowej m) oznacza, Ŝe moment pędu w 3-wymiarowej przestrzeni nie moŝe się ustawić dowolnie a jedynie pod ściśle określonym kątem do kierunku wyróŝnionego przez pole magnetyczne (kwantyzacja przestrzenna momentu pędu).
9 Fizyka Wyk»ad W6 9 Jak wynika z kwantowego modelu atomu (patrz rozdział poniŝej): orbitalom oznaczanym literą p odpowiada liczba kwantowa l = 1. Zatem magnetyczna liczba kwantowa m moŝe być równa -1,0 lub 1. Daje to 3 orbitale, które są zdegenerowane bez zewnętrznego pola magnetycznego ich energia jest jednakowa => zachowują się jak 1 poziom energetyczny dopóki nie włączymy zewnętrznego pola magnetycznego. Gdy włączymy pole magnetyczne kaŝdy moment pędu uzyskuje energię dodatkową: r r E = µ B = µ B = mb dod L µ z B Prowadzi to do rozszczepienia poziomu atomego na 3 orbitale o róŝnej energii. Stopień rozszczepienia jest więc zaleŝny od pola magnetycznego B Podobnie orbitalom oznaczonym literą d odpowiada liczba kwantowa l = a zatem i m = -,-1,0,1, (w programie na stronie Visual Quantum Mechanics jest błąd! W rzeczywistości sa tam pokazane orbitale to 6d oraz 7p; widać to po tym jak się one rozszczepiają w polu magnetycznym). Struktura subtelna widma optycznego: Okazuje się, Ŝe kaŝda z linii widocznych w spektrogramie, po przyłoŝeniu jeszcze silniejszego pola magnetycznego niŝ na rysunkach powyŝej ulega dalszemu rozszczepieniu, tym razem na linie. Jest to skutek wewnętrznego momentu pędu elektronu tzw. spinu.
10 Fizyka Wyk»ad W6 10 Spinowy moment p du Jest to wewn trzny moment p du czstek elementarnych. Nie ma nic wspólnego z rzeczywistym obrotem czstki wokó» w»asnej osi. W»asnoÑci spinu czstki moŝna wyprowadziƒ na gruncie relatywistycznej mechaniki kwantowej. Wynik doñwiadczenia Zeemana w silnych polach magnetycznych wskazuje, óe elektrony posiadaj w»asny magnetyczny moment dipolowy, którego rzut moóe mieƒ tylko wartoñci: tzn. S z = ± ½. Spin posiadają nie tylko pojedyncze cząstki takie jak elektrony, protony czy neutrony. DoÑwiadczenie Sterna Gerlacha: Wizka atomów srebra przechodzc przez niejednorodne pole magnetyczne uleg»a rozsczepieniu na wiazki.
11 Fizyka Wyk»ad W6 11 WyjaÑnienie: atomy srebra występują w postaci dwóch izotopów jednego o parzystej liczbie nukleonów w jądrze atomowym i drugiego o nieparzystej ich liczbie. Jdra atomowe posiadajce nieparzystą liczbę nukleonów maj spin, którego rzut ma długość n /, gdzie n = 3,5,7,... Jdra atomowe o parzystej liczbie nukleonów posiadaj jdrowy moment spinowy, którego rzut ma długość n gdzie n = 1,,3,... Podsumowujc wyniki doñwiadcze½: Czstki dziel si na fermiony obdarzone spinowym momentem p du n+1 h gdzie n = 0,1,,3,... Przykład: elektrony, protony, neutrony oraz bozony gdy ich ca»kowity spin jest n, gdzie n = 1,,3... Przykład: foton, wiele cząstek złoŝonych jak fonony, magnony, pary Coopera (tj. nośniki prądu w stanie nadprzewodnictwa) Zobaczymy później, Ŝe ten podział cząstek ma nie tylko znaczenie formalne: mają one istotnie róŝne własności statystyczne. Wpływa to na wiele zjawisk fizycznych takuch jak struktura elektronowa ciał stałych i zjawisko nadprzewodnictwa.
12 Fizyka Wyk»ad W6 1 Ze spinem czstki zwizany jest magnetyczny moment dipolowy a jego rzut moŝe przyjąć tylko wartości: e h µ = - ms = µ B ms ; ms = me r r r Oznacza to, óe ca»kowity moment p du atomu wynosi J = L + S S z ± ale ca»kowity dipolowy moment magnetyczny atomu r r µ r J = - µ B ( L + S ) dlatego, óe magneton spinowy jest razy wi kszy od magnetonu Bohra. A wi c moment magnetyczny ca»ego atomu nie jest równoleg»y do ca»kowitego momentu p du atomu. Komplikuje to w»asnoñci magnetyczne jonów, czstek i cia» stalych, gdzie liczba cząstek jest duŝa a ich orbitalne momenty pędu i spinowe orbitalne momenty pędu dodają się w złoŝony sposób. 1 r r S µ = - e m e r S
13 Fizyka Wyk»ad W6 13 Budowa atomu model atomu wodoropodobnego Cel: wyznaczyƒ poziomy energetyczne i funkcje falowe elektronu poruszajcego si w potencjale jdra atomowego o»adunku Z e gdzie Z liczba porzdkowa atomu. Przyblióenie: zak»adamy, óe jadro atomu jest nieruchome Potencja»: 1 Ze V ( r, θ, φ )= - 4π ε 0 r Problem ma symetri sferyczn => naleóy rozwizaƒ równanie Schrödingera we wspó»rz dnych sferycznych pˆ r +V(r) (r, θ, φ )= Eψ (r, θ, φ ) m ψ Okazuje si, óe po zapisaniu laplasjanu we wspó»rz dnych sferycznych ^ p + L ˆ r r +V(r) ψ (r, θ, φ )= Eψ (r, θ, ) m mr φ
14 Fizyka Wyk»ad W6 14 Operator kwadratu momentu p du jest zaleŝny jedynie of katów θ oraz φ. Sugeruje to postaƒ rozwizania: ψ (r, θ, φ )= R(r) Y lm( θ, φ ) i prowadzi do separacji zmiennych w zwyk»y sposób: ^ Y( θ, φ )= β Y( θ, φ ) prl ˆ r +V ef (r) R(r)= β R(r) m gdzie potencja» efektywny dzia»ający na elektron h l (l +1) V ef ( r )=V(r)+ m r a liczba kwantowa l jest zwizana z operatorem kwadratu momentu p du poprzez ^ L Y l,m ( θ, φ )= h β Y l, m ( θ, φ ) Widaƒ, óe kwantowe w»asnoñci momentu p du wp»ywaj silnie na w»asnoñci elektronu w atomie.
15 Fizyka Wyk»ad W6 15 Rozwizanie obu równa½ daje gdzie ρ l - ψ n l m ( r, θ, φ )= ρ e Lnl ( ρ ) Ylm ( θ, φ ) ρ h m E r a Y lm ( θ, φ ) s funkcjami sferycznymi natomiast L nl (ρ) s to wielomianami Laguerre. n = 1,,3... g»ówna liczba kwantowa - okreñla pow»ok atomow energia elektronu E ~ 1/ n l = 0,1,,3,..., n-1 orbitalna liczba kwantowa Przyjęto oznaczać orbitale literami s,p,d,f w zaleŝności od wartości liczby kwantowej l m = -l, -l+1,...,0,...,l-1,l magnetyczna liczba kwantowa Degeneracja orbitali atomowych: jednej wartoñci energii (zadanej przez wartoñƒ n) moóe odpowiadaƒ wiele orbitali okreñlonych przez liczb kwantow l. Dodatkowo trzeba uwzgl dniƒ jeszcze spin elektronu - dochodzi jeszcze czwarta liczba kwantowa (magnetyczna liczba kwantowa) m s = ± 1/.
16 Fizyka Wyk»ad W6 16 Przyk»ad: funkcja falowa elektronu w atomie wodoropodobnym dla n = 1 oraz l = m = Zr = 100 e me 0 1 Z ψ π a 4π ε 0 _ gdzie a0 = jest to tzw. promie½ orbity Bohra. me Prawdopodobie½stwo znalezienia elektronu wewntrz warstwy sferycznej o promieniu r i gruboñci dr wynosi: P(r)dr = ψ (r) 4 r dr 100 π
17 Fizyka Wyk»ad W6 17 Funkcja falowa elektronu w atomie wodoru dla n = 1 i l=0 oraz m = 0 n = oraz l = m =0
18 Fizyka Wyk»ad W6 18 n = 3 oraz l = m =0 n = 4 oraz l = m =0
19 Fizyka Wyk»ad W6 19 n = oraz l =1 i m =0 n = oraz l =1 i m= ±1
20 Fizyka Wyk»ad W6 0 n = 3 l =, m = 0 n = 3 l = oraz m =±1 n = 5
21 Fizyka Wyk»ad W6 1 l = 3 m = ±1 n = 5 l = 4 m = ±1
22 Fizyka Wyk»ad W6 Wewnątrz jądra atomowego znajdują się nukleony protony oraz neutrony. Protony mają ładunek dodatni więc odpychają się nawzajem siłą Coulomba. To, Ŝe jądra atomowe są stabilne wynika z oddziaływań jądrowych. MoŜna ich działanie przybliŝyć za pomocą studni potencjału oddziałującej na nukleony. Stąd juŝ prosta droga do modelu powłokowego jądra atomu. Schemat poziomów energetycznych nukleonów w jądrze pokazuje poniŝszy obok: Na lewo podane są liczby kwantowe l a w środku liczby kwantowe j. Liczby w kółkach pokazują liczbę nukleonów, które wypełniają wszystkie poziomy o mniejszej energii. Model ten wyjaśnia wiele cech pierwiastków w układzie tablicy Mendelejewa. M. in. moŝna wykazać, jakie pierwiastki izotopy są stabilne (wyspy stabilności) a jakie będą niestabilne (promieniotwórcze). Wyjaśnia teŝ zachowanie izotopów pod wpływem napromieniowania tego izotopu promieniowaniem przenikliwym.
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków).
 Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Stara i nowa teoria kwantowa
 Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym
 II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym Jan Królikowski Fizyka IVBC 1 II.4.1 Ogólne własności wektora kwantowego momentu pędu Podane poniżej własności kwantowych wektorów
II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym Jan Królikowski Fizyka IVBC 1 II.4.1 Ogólne własności wektora kwantowego momentu pędu Podane poniżej własności kwantowych wektorów
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Mechanika kwantowa. Erwin Schrödinger ( ) Werner Heisenberg
 Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
Atomy mają moment pędu
 Atomy mają moment pędu Model na rysunku jest modelem tylko klasycznym i jak wiemy z mechaniki kwantowej, nie odpowiada dokładnie rzeczywistości Jednakże w mechanice kwantowej elektron nadal ma orbitalny
Atomy mają moment pędu Model na rysunku jest modelem tylko klasycznym i jak wiemy z mechaniki kwantowej, nie odpowiada dokładnie rzeczywistości Jednakże w mechanice kwantowej elektron nadal ma orbitalny
Atom wodoru i jony wodoropodobne
 Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Atom wodoru w mechanice kwantowej. Równanie Schrödingera
 Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Liczby kwantowe elektronu w atomie wodoru
 Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Spektroskopia magnetyczna
 Spektroskopia magnetyczna Literatura Zbigniew Kęcki, Podstawy spektroskopii molekularnej, PWN W- wa 1992 lub nowsze wydanie Przypomnienie 1) Mechanika ruchu obrotowego - moment bezwładności, moment pędu,
Spektroskopia magnetyczna Literatura Zbigniew Kęcki, Podstawy spektroskopii molekularnej, PWN W- wa 1992 lub nowsze wydanie Przypomnienie 1) Mechanika ruchu obrotowego - moment bezwładności, moment pędu,
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Równanie Schrödingera dla elektronu w atomie wodoru Równanie niezależne od czasu w trzech wymiarach współrzędne prostokątne
 Równanie Schrödingera dla elektronu w atomie wodoru Równanie nieależne od casu w trech wymiarach współrędne prostokątne ψ ψ ψ h V m + + x y + ( x, y, ) ψ = E ψ funkcja falowa ψ( x, y, ) Energia potencjalna
Równanie Schrödingera dla elektronu w atomie wodoru Równanie nieależne od casu w trech wymiarach współrędne prostokątne ψ ψ ψ h V m + + x y + ( x, y, ) ψ = E ψ funkcja falowa ψ( x, y, ) Energia potencjalna
Fizyka 2. Janusz Andrzejewski
 Fizyka 2 wykład 14 Janusz Andrzejewski Atom wodoru Wczesne modele atomu -W czasach Newtona atom uważany była za małą twardą kulkę co dość dobrze sprawdzało się w rozważaniach dotyczących kinetycznej teorii
Fizyka 2 wykład 14 Janusz Andrzejewski Atom wodoru Wczesne modele atomu -W czasach Newtona atom uważany była za małą twardą kulkę co dość dobrze sprawdzało się w rozważaniach dotyczących kinetycznej teorii
Atomy w zewnętrznym polu magnetycznym i elektrycznym
 Atomy w zewnętrznym polu magnetycznym i elektrycznym 1. Kwantowanie przestrzenne momentów magnetycznych i rezonans spinowy 2. Efekt Zeemana (normalny i anomalny) oraz zjawisko Paschena-Backa 3. Efekt Starka
Atomy w zewnętrznym polu magnetycznym i elektrycznym 1. Kwantowanie przestrzenne momentów magnetycznych i rezonans spinowy 2. Efekt Zeemana (normalny i anomalny) oraz zjawisko Paschena-Backa 3. Efekt Starka
Spin jądra atomowego. Podstawy fizyki jądrowej - B.Kamys 1
 Spin jądra atomowego Nukleony mają spin ½: Całkowity kręt nukleonu to: Spin jądra to suma krętów nukleonów: Dla jąder parzysto parzystych, tj. Z i N parzyste ( ee = even-even ) I=0 Dla jąder nieparzystych,
Spin jądra atomowego Nukleony mają spin ½: Całkowity kręt nukleonu to: Spin jądra to suma krętów nukleonów: Dla jąder parzysto parzystych, tj. Z i N parzyste ( ee = even-even ) I=0 Dla jąder nieparzystych,
JEDNOSTKI ATOMOWE =1, m e =1, e=1, ; 1 E 2 h = 4, J. Energia atomu wodoru lub jonu wodoropodobnego w jednostkach atomowych:
 do wyk ladu z 1.10.13 Atom wodoru i jon wodoropodobny Ze - ladunek jadra, e - ladunek elektronu, µ - masa zredukowana µ = mem j m e+m j ( µ m e ) M j - masa jadra, m e - masa elektronu, ε 0 - przenikalność
do wyk ladu z 1.10.13 Atom wodoru i jon wodoropodobny Ze - ladunek jadra, e - ladunek elektronu, µ - masa zredukowana µ = mem j m e+m j ( µ m e ) M j - masa jadra, m e - masa elektronu, ε 0 - przenikalność
Podstawy fizyki kwantowej i budowy materii
 Podstawy fizyki kwantowej i budowy materii prof. dr hab. Aleksander Filip Żarnecki Zakład Cząstek i Oddziaływań Fundamentalnych Instytut Fizyki Doświadczalnej Wykład 13 8 stycznia 2018 A.F.Żarnecki Podstawy
Podstawy fizyki kwantowej i budowy materii prof. dr hab. Aleksander Filip Żarnecki Zakład Cząstek i Oddziaływań Fundamentalnych Instytut Fizyki Doświadczalnej Wykład 13 8 stycznia 2018 A.F.Żarnecki Podstawy
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Wykład Atom o wielu elektronach Laser Rezonans magnetyczny
 Wykład 21. 12.2016 Atom o wielu elektronach Laser Rezonans magnetyczny Jeszcze o atomach Przypomnienie: liczby kwantowe elektronu w atomie wodoru, zakaz Pauliego, powłoki, podpowłoki, orbitale, Atomy wieloelektronowe
Wykład 21. 12.2016 Atom o wielu elektronach Laser Rezonans magnetyczny Jeszcze o atomach Przypomnienie: liczby kwantowe elektronu w atomie wodoru, zakaz Pauliego, powłoki, podpowłoki, orbitale, Atomy wieloelektronowe
Własności jąder w stanie podstawowym
 Własności jąder w stanie podstawowym Najważniejsze liczby kwantowe charakteryzujące jądro: A liczba masowa = liczbie nukleonów (l. barionów) Z liczba atomowa = liczbie protonów (ładunek) N liczba neutronów
Własności jąder w stanie podstawowym Najważniejsze liczby kwantowe charakteryzujące jądro: A liczba masowa = liczbie nukleonów (l. barionów) Z liczba atomowa = liczbie protonów (ładunek) N liczba neutronów
VIII. VIII.1. ORBITALNY MOMENT MAGNETYCZNY ELEKTRONU, L= r p (VIII.1.1) p=m v (VIII.1.2) L= L =mvr (VIII.1.1a) r v. r=v (VIII.1.3)
 VIII. VIII.1. ORBITALNY MOMENT MAGNETYCZNY ELEKTRONU, L= r p (VIII.1.1) p=m v (VIII.1.2) Z (VIII.1.1) i (VIII.1.2) wynika (VIII.1.1a): L= L =mvr (VIII.1.1a) r v r=v (VIII.1.3) Z zależności (VIII.1.1a)
VIII. VIII.1. ORBITALNY MOMENT MAGNETYCZNY ELEKTRONU, L= r p (VIII.1.1) p=m v (VIII.1.2) Z (VIII.1.1) i (VIII.1.2) wynika (VIII.1.1a): L= L =mvr (VIII.1.1a) r v r=v (VIII.1.3) Z zależności (VIII.1.1a)
Atomowa budowa materii
 Atomowa budowa materii Wszystkie obiekty materialne zbudowane są z tych samych elementów cząstek elementarnych Cząstki elementarne oddziałują tylko kilkoma sposobami oddziaływania wymieniając kwanty pól
Atomowa budowa materii Wszystkie obiekty materialne zbudowane są z tych samych elementów cząstek elementarnych Cząstki elementarne oddziałują tylko kilkoma sposobami oddziaływania wymieniając kwanty pól
Cząstki elementarne. Składnikami materii są leptony, mezony i bariony. Leptony są niepodzielne. Mezony i bariony składają się z kwarków.
 Cząstki elementarne Składnikami materii są leptony, mezony i bariony. Leptony są niepodzielne. Mezony i bariony składają się z kwarków. Cząstki elementarne Leptony i kwarki są fermionami mają spin połówkowy
Cząstki elementarne Składnikami materii są leptony, mezony i bariony. Leptony są niepodzielne. Mezony i bariony składają się z kwarków. Cząstki elementarne Leptony i kwarki są fermionami mają spin połówkowy
Statystyka nieoddziaływujących gazów Bosego i Fermiego
 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bozony: fotony (kwanty pola elektromagnetycznego, których liczba nie jest zachowana mogą być pojedynczo pochłaniane lub tworzone. W konsekwencji,
Statystyka nieoddziaływujących gazów Bosego i Fermiego Bozony: fotony (kwanty pola elektromagnetycznego, których liczba nie jest zachowana mogą być pojedynczo pochłaniane lub tworzone. W konsekwencji,
W6. Model atomu Thomsona
 W6. Model atomu Thomsona Na początku XX w. znano wiele wyników eksperymentalnych, które wskazywały na to, że atomy zawierają elektrony. Z faktu, że atomy są elektrycznie obojętne wnioskowano, że mają one
W6. Model atomu Thomsona Na początku XX w. znano wiele wyników eksperymentalnych, które wskazywały na to, że atomy zawierają elektrony. Z faktu, że atomy są elektrycznie obojętne wnioskowano, że mają one
Fizyka 3.3 WYKŁAD II
 Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Atom wodoru. Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu:
 ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
Układy wieloelektronowe
 Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Rysunek 1: Schemat doświadczenia Sterna-Gerlacha. Rysunek 2: Schemat doświadczenia Sterna-Gerlacha w różnych rzutach przestrzennych.
 VII. SPIN 1 Rysunek 1: Schemat doświadczenia Sterna-Gerlacha. Rysunek 2: Schemat doświadczenia Sterna-Gerlacha w różnych rzutach przestrzennych. 1 Wstęp Spin jest wielkością fizyczną charakteryzującą cząstki
VII. SPIN 1 Rysunek 1: Schemat doświadczenia Sterna-Gerlacha. Rysunek 2: Schemat doświadczenia Sterna-Gerlacha w różnych rzutach przestrzennych. 1 Wstęp Spin jest wielkością fizyczną charakteryzującą cząstki
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 4 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2013/14
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 4 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2013/14
Liczby kwantowe n, l, m l = 0 l =1 l = 2 l = 3
 Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Wykład 27. Elementy współczesnej fizyki atomów i cząsteczek.
 1 Wykład 7 Elementy współczesnej fizyki atomów i cząsteczek. 1.1 Atom wodoru w mechanice kwantowej. Znalezienie poziomów energetycznych elektronu w atomie wodoru (a także układów wodoropodobnych: jonu
1 Wykład 7 Elementy współczesnej fizyki atomów i cząsteczek. 1.1 Atom wodoru w mechanice kwantowej. Znalezienie poziomów energetycznych elektronu w atomie wodoru (a także układów wodoropodobnych: jonu
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Podstawy fizyki kwantowej i budowy materii
 Podstawy fizyki kwantowej i budowy materii prof. dr hab. Aleksander Filip Żarnecki Zakład Cząstek i Oddziaływań Fundamentalnych Instytut Fizyki Doświadczalnej Wykład 12 9 stycznia 2017 A.F.Żarnecki Podstawy
Podstawy fizyki kwantowej i budowy materii prof. dr hab. Aleksander Filip Żarnecki Zakład Cząstek i Oddziaływań Fundamentalnych Instytut Fizyki Doświadczalnej Wykład 12 9 stycznia 2017 A.F.Żarnecki Podstawy
Wykład FIZYKA II. 13. Fizyka atomowa. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA II 13. Fizyka atomowa Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/ ZASADA PAULIEGO Układ okresowy pierwiastków lub jakiekolwiek
Wykład FIZYKA II 13. Fizyka atomowa Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/ ZASADA PAULIEGO Układ okresowy pierwiastków lub jakiekolwiek
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
cz. 1. dr inż. Zbigniew Szklarski
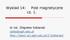 Wykład 14: Pole magnetyczne cz. 1. dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Wektor indukcji pola magnetycznego, siła Lorentza v F L Jeżeli na dodatni ładunek
Wykład 14: Pole magnetyczne cz. 1. dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Wektor indukcji pola magnetycznego, siła Lorentza v F L Jeżeli na dodatni ładunek
II.6 Atomy w zewnętrznym polu magnetycznym
 II.6 Atomy w zewnętrznym polu magnetycznym 1. Kwantowanie przestrzenne w zewnętrznym polu magnetycznym. Model wektorowy raz jeszcze 2. Zjawisko Zeemana Normalne zjawisko Zeemana i jego wyjaśnienie w modelu
II.6 Atomy w zewnętrznym polu magnetycznym 1. Kwantowanie przestrzenne w zewnętrznym polu magnetycznym. Model wektorowy raz jeszcze 2. Zjawisko Zeemana Normalne zjawisko Zeemana i jego wyjaśnienie w modelu
Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały
 WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
Spis treści. Przedmowa redaktora do wydania czwartego 11
 Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki
 OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
h 2 h p Mechanika falowa podstawy pˆ 2
 Mechanika falowa podstawy Hipoteza de Broglie a Zarówno promieniowanie jak i cząstki materialne posiadają naturę dwoistą korpuskularno-falową. Z każdą mikrocząstką można związać pewien proces falowy pierwotnie
Mechanika falowa podstawy Hipoteza de Broglie a Zarówno promieniowanie jak i cząstki materialne posiadają naturę dwoistą korpuskularno-falową. Z każdą mikrocząstką można związać pewien proces falowy pierwotnie
Widmo sodu, serie. p główna s- ostra d rozmyta f -podstawowa
 Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
gdzie λ - długość fali, h - stała Plancka, p - pęd cząstki.
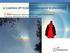 3.7. Model współczesny Louis Victor Pierre Raymond de Broglie (189-1987) (Rysunek 3-35) w swojej pracy doktorskiej z 194 roku, wysunął przypuszczenie, że skoro fale elektromagnetyczne mogą przejawiać naturę
3.7. Model współczesny Louis Victor Pierre Raymond de Broglie (189-1987) (Rysunek 3-35) w swojej pracy doktorskiej z 194 roku, wysunął przypuszczenie, że skoro fale elektromagnetyczne mogą przejawiać naturę
Atom wodoropodobny. Biegunowy układ współrzędnych. współrzędne w układzie. kartezjańskim. współrzędne w układzie. (x,y,z) biegunowym.
 Atom wodoropodobny z współrzędne w układzie kartezjańskim r sinθ cosφ x r cosθ φ θ r r sinθ (x,y,z) r sinθ sinφ Biegunowy układ współrzędnych y funkcja faowa współrzędne w układzie biegunowym ( ) r,θ,φ
Atom wodoropodobny z współrzędne w układzie kartezjańskim r sinθ cosφ x r cosθ φ θ r r sinθ (x,y,z) r sinθ sinφ Biegunowy układ współrzędnych y funkcja faowa współrzędne w układzie biegunowym ( ) r,θ,φ
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
Metody rezonansowe. Magnetyczny rezonans jądrowy Magnetometr protonowy
 Metody rezonansowe Magnetyczny rezonans jądrowy Magnetometr protonowy Co należy wiedzieć Efekt Zeemana, precesja Larmora Wektor magnetyzacji w podstawowym eksperymencie NMR Transformacja Fouriera Procesy
Metody rezonansowe Magnetyczny rezonans jądrowy Magnetometr protonowy Co należy wiedzieć Efekt Zeemana, precesja Larmora Wektor magnetyzacji w podstawowym eksperymencie NMR Transformacja Fouriera Procesy
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
ANALITYKA W KONTROLI JAKOŚCI
 ANALITYKA W KONTROLI JAKOŚCI ANALIZA ŚLADÓW METODA ICP-OES Optyczna spektroskopia emisyjna ze wzbudzeniem w indukcyjnie sprzężonej plazmie WYKŁAD 4 Rodzaje widm i mechanizm ich powstania PODSTAWY SPEKTROSKOPII
ANALITYKA W KONTROLI JAKOŚCI ANALIZA ŚLADÓW METODA ICP-OES Optyczna spektroskopia emisyjna ze wzbudzeniem w indukcyjnie sprzężonej plazmie WYKŁAD 4 Rodzaje widm i mechanizm ich powstania PODSTAWY SPEKTROSKOPII
WYKŁAD 15. Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego
 WYKŁAD 15 Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego 1 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bosony
WYKŁAD 15 Gęstość stanów Zastosowanie: oscylatory kwantowe (ª bosony bezmasowe) Formalizm dla nieoddziaływujących cząstek Bosego lub Fermiego 1 Statystyka nieoddziaływujących gazów Bosego i Fermiego Bosony
24 Spin i efekty relatywistyczne
 4 Spin i efekty relatywistyczne 4. Doświadczenie Sterna Gerlacha Zauważmy, że klasycznie na moment magnetyczny µ w stałym polu magnetycznym B działa moment siły N = µ B. (4.) Efektem tego oddziaływania
4 Spin i efekty relatywistyczne 4. Doświadczenie Sterna Gerlacha Zauważmy, że klasycznie na moment magnetyczny µ w stałym polu magnetycznym B działa moment siły N = µ B. (4.) Efektem tego oddziaływania
Uklady modelowe III - rotator, atom wodoru
 Wyk lad 5 Uklady modelowe III - rotator, atom wodoru Model Separacja ruchu środka masy R = m 1r 1 + m 2 r 2 m 1 + m 2 Ĥ = Ĥ tr (R) + Ĥ rot (r) Ĥ tr 2 (R) = 2(m 1 + m 2 ) R [ Ψ E tr (R; t) = exp i (k R
Wyk lad 5 Uklady modelowe III - rotator, atom wodoru Model Separacja ruchu środka masy R = m 1r 1 + m 2 r 2 m 1 + m 2 Ĥ = Ĥ tr (R) + Ĥ rot (r) Ĥ tr 2 (R) = 2(m 1 + m 2 ) R [ Ψ E tr (R; t) = exp i (k R
Podstawy Fizyki Jądrowej
 Podstawy Fizyki Jądrowej III rok Fizyki Kurs WFAIS.IF-D008.0 Składnik egzaminu licencjackiego (sesja letnia)! OPCJA: Po uzyskaniu zaliczenia z ćwiczeń możliwość zorganizowania ustnego egzaminu (raczej
Podstawy Fizyki Jądrowej III rok Fizyki Kurs WFAIS.IF-D008.0 Składnik egzaminu licencjackiego (sesja letnia)! OPCJA: Po uzyskaniu zaliczenia z ćwiczeń możliwość zorganizowania ustnego egzaminu (raczej
NMR (MAGNETYCZNY REZONANS JĄDROWY) dr Marcin Lipowczan
 NMR (MAGNETYCZNY REZONANS JĄDROWY) dr Marcin Lipowczan Spis zagadnień Fizyczne podstawy zjawiska NMR Parametry widma NMR Procesy relaksacji jądrowej Metody obrazowania Fizyczne podstawy NMR Proton, neutron,
NMR (MAGNETYCZNY REZONANS JĄDROWY) dr Marcin Lipowczan Spis zagadnień Fizyczne podstawy zjawiska NMR Parametry widma NMR Procesy relaksacji jądrowej Metody obrazowania Fizyczne podstawy NMR Proton, neutron,
Podstawowe własności jąder atomowych
 Podstawowe własności jąder atomowych 1. Ilość protonów i neutronów Z, N 2. Masa jądra M j = M p + M n - B 2 2 Q ( M c ) ( M c ) 3. Energia rozpadu p 0 k 0 Rozpad zachodzi jeżeli Q > 0, ta nadwyżka energii
Podstawowe własności jąder atomowych 1. Ilość protonów i neutronów Z, N 2. Masa jądra M j = M p + M n - B 2 2 Q ( M c ) ( M c ) 3. Energia rozpadu p 0 k 0 Rozpad zachodzi jeżeli Q > 0, ta nadwyżka energii
TEORIA PASMOWA CIAŁ STAŁYCH
 TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
Chemia Ogólna wykład 1
 Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Modele atomu wodoru. Modele atomu wodoru Thomson'a Rutherford'a Bohr'a
 Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki
 OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Równania optyki półklasycznej Posłużymy się teraz równaniem (2.4), i Ψ t = ĤΨ ażeby wyprowadzić
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Równania optyki półklasycznej Posłużymy się teraz równaniem (2.4), i Ψ t = ĤΨ ażeby wyprowadzić
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU
 X. RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU Równanie Schrődingera niezależne od czasu to równanie postaci: ħ 2 2m d 2 x dx 2 V xx = E x (X.1) Warunki regularności na x i a) skończone b) ciągłe c) jednoznaczne
X. RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU Równanie Schrődingera niezależne od czasu to równanie postaci: ħ 2 2m d 2 x dx 2 V xx = E x (X.1) Warunki regularności na x i a) skończone b) ciągłe c) jednoznaczne
WYKŁAD 5. Maria Krawczyk, Wydział Fizyki UW. Fermiony i bozony. Oddziaływanie słabe i rodziny cząstek fundamentalnych. Spin - historia odkrycia
 Wszechświat cząstek elementarnych WYKŁAD 5 Maria Krawczyk, Wydział Fizyki UW Spin - historia odkrycia Fermiony i bozony Oddziaływanie słabe i rodziny cząstek fundamentalnych sem letni 2013/14 Spin - jeszcze
Wszechświat cząstek elementarnych WYKŁAD 5 Maria Krawczyk, Wydział Fizyki UW Spin - historia odkrycia Fermiony i bozony Oddziaływanie słabe i rodziny cząstek fundamentalnych sem letni 2013/14 Spin - jeszcze
CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna. Model atomu Bohra
 CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna Model atomu Bohra SPIS TREŚCI: 1. Modele budowy atomu Thomsona, Rutherforda i Bohra 2. Budowa atomu 3. Liczba atomowa a liczba
CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna Model atomu Bohra SPIS TREŚCI: 1. Modele budowy atomu Thomsona, Rutherforda i Bohra 2. Budowa atomu 3. Liczba atomowa a liczba
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Fizyka 3. Konsultacje: p. 329, Mechatronika
 Fizyka 3 Konsultacje: p. 39, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 1 sprawdzian 30 pkt 15.1 18 3.0 18.1 1 3.5 1.1 4 4.0 4.1 7 4.5 7.1 30 5.0 http:\\adam.mech.pw.edu.pl\~marzan Program: - elementy
Fizyka 3 Konsultacje: p. 39, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 1 sprawdzian 30 pkt 15.1 18 3.0 18.1 1 3.5 1.1 4 4.0 4.1 7 4.5 7.1 30 5.0 http:\\adam.mech.pw.edu.pl\~marzan Program: - elementy
r. akad. 2012/2013 Atom wodoru wykład V-VI Podstawy Procesów i Konstrukcji Inżynierskich Atom wodoru Zakład Biofizyki 1
 r. akad. 01/013 wykład V-VI Podstawy Procesów i Konstrukcji Inżynierskic Atom wodoru Zakład Biofizyki 1 Model atomu Tompsona Model atomu typu ciastka z rodzynkami w 1903 J.J. Tompson zaproponował model
r. akad. 01/013 wykład V-VI Podstawy Procesów i Konstrukcji Inżynierskic Atom wodoru Zakład Biofizyki 1 Model atomu Tompsona Model atomu typu ciastka z rodzynkami w 1903 J.J. Tompson zaproponował model
Fizyka współczesna Co zazwyczaj obejmuje fizyka współczesna (modern physics)
 Fizyka współczesna Co zazwyczaj obejmuje fizyka współczesna (modern physics) Koniec XIX / początek XX wieku Lata 90-te XIX w.: odkrycie elektronu (J. J. Thomson, promienie katodowe), promieniowania Roentgena
Fizyka współczesna Co zazwyczaj obejmuje fizyka współczesna (modern physics) Koniec XIX / początek XX wieku Lata 90-te XIX w.: odkrycie elektronu (J. J. Thomson, promienie katodowe), promieniowania Roentgena
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu
 Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
Wykład FIZYKA II. 5. Magnetyzm. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA II 5. Magnetyzm Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka2.html MAGNESY Pierwszymi poznanym magnesem był magnetyt
Wykład FIZYKA II 5. Magnetyzm Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka2.html MAGNESY Pierwszymi poznanym magnesem był magnetyt
Budowa atomu. Izotopy
 Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Informacje ogólne. 45 min. test na podstawie wykładu Zaliczenie ćwiczeń na podstawie prezentacji Punkty: test: 60 %, prezentacja: 40 %.
 Informacje ogólne Wykład 28 h Ćwiczenia 14 Charakter seminaryjny zespołu dwuosobowe ~20 min. prezentacje Lista tematów na stronie Materiały do wykładu na stronie: http://urbaniak.fizyka.pw.edu.pl Zaliczenie:
Informacje ogólne Wykład 28 h Ćwiczenia 14 Charakter seminaryjny zespołu dwuosobowe ~20 min. prezentacje Lista tematów na stronie Materiały do wykładu na stronie: http://urbaniak.fizyka.pw.edu.pl Zaliczenie:
FIZYKA III MEL Fizyka jądrowa i cząstek elementarnych
 FIZYKA III MEL Fizyka jądrowa i cząstek elementarnych Wykład 1 własności jąder atomowych Odkrycie jądra atomowego Rutherford (1911) Ernest Rutherford (1871-1937) R 10 fm 1908 Skala przestrzenna jądro
FIZYKA III MEL Fizyka jądrowa i cząstek elementarnych Wykład 1 własności jąder atomowych Odkrycie jądra atomowego Rutherford (1911) Ernest Rutherford (1871-1937) R 10 fm 1908 Skala przestrzenna jądro
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Wykład 16: Atomy wieloelektronowe
 Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład V Wiązanie kowalencyjne. Półprzewodniki
 Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
2008/2009. Seweryn Kowalski IVp IF pok.424
 2008/2009 seweryn.kowalski@us.edu.pl Seweryn Kowalski IVp IF pok.424 Model powłokowy Moment kwadrupolowy w jednocząstkowym modelu powłokowym: Dla pojedynczego protonu znajdującego się na orbicie j (m j
2008/2009 seweryn.kowalski@us.edu.pl Seweryn Kowalski IVp IF pok.424 Model powłokowy Moment kwadrupolowy w jednocząstkowym modelu powłokowym: Dla pojedynczego protonu znajdującego się na orbicie j (m j
Wykład 27 Wersja robocza. Elementy współczesnej fizyki atomów i cząsteczek.
 Wykłady z fizyki Piotr Posmykiewicz 1 Wykład 7 Wersja robocza. Elementy współczesnej fizyki atomów i cząsteczek. 7.1 Atom wodoru w mechanice kwantowej. Znalezienie poziomów energetycznych elektronu w atomie
Wykłady z fizyki Piotr Posmykiewicz 1 Wykład 7 Wersja robocza. Elementy współczesnej fizyki atomów i cząsteczek. 7.1 Atom wodoru w mechanice kwantowej. Znalezienie poziomów energetycznych elektronu w atomie
W dotychczasowych rozważaniach dotyczących różnych układów fizycznych (w tym i atomu wodoropodobnego)
 3.1.4 17. Teoria spinu 1/ 196 Rozdział 17 Teoria spinu 1/ 17.1 Wprowadzenie braki dotychczasowej teorii W dotychczasowych rozważaniach dotyczących różnych układów fizycznych w tym i atomu wodoropodobnego
3.1.4 17. Teoria spinu 1/ 196 Rozdział 17 Teoria spinu 1/ 17.1 Wprowadzenie braki dotychczasowej teorii W dotychczasowych rozważaniach dotyczących różnych układów fizycznych w tym i atomu wodoropodobnego
Dwie lub więcej cząstek poza zamkniętą powłoką
 Dwie lub więcej cząstek poza zamkniętą powłoką Rozważmy dwa (takie same) nukleony (lub dwie dziury) na orbitalu j poza zamkniętymi powłokami. Te dwie cząstki mogą sprzęgać się do momentu pędu J = j + j,
Dwie lub więcej cząstek poza zamkniętą powłoką Rozważmy dwa (takie same) nukleony (lub dwie dziury) na orbitalu j poza zamkniętymi powłokami. Te dwie cząstki mogą sprzęgać się do momentu pędu J = j + j,
Rezonanse magnetyczne oraz wybrane techniki pomiarowe fizyki ciała stałego
 Paweł Szroeder Rezonanse magnetyczne oraz wybrane techniki pomiarowe fizyki ciała stałego Wykład I Moment magnetyczny a moment pędu czynnik g. Precesja Larmora. Zjawisko rezonansu magnetycznego. Fenomenologiczny
Paweł Szroeder Rezonanse magnetyczne oraz wybrane techniki pomiarowe fizyki ciała stałego Wykład I Moment magnetyczny a moment pędu czynnik g. Precesja Larmora. Zjawisko rezonansu magnetycznego. Fenomenologiczny
Własności magnetyczne materii
 Własności magnetyczne materii Dipole magnetyczne Najprostszą strukturą magnetyczną są magnetyczne dipole. Fe 3 O 4 Kompas, Chiny 220 p.n.e Kołowy obwód z prądem dipol magnetyczny! Wartość B w środku kołowego
Własności magnetyczne materii Dipole magnetyczne Najprostszą strukturą magnetyczną są magnetyczne dipole. Fe 3 O 4 Kompas, Chiny 220 p.n.e Kołowy obwód z prądem dipol magnetyczny! Wartość B w środku kołowego
r. akad. 2012/2013 Atom wodoru wykład 5-6 Podstawy Procesów i Konstrukcji Inżynierskich Atom wodoru Zakład Biofizyki 1
 r. akad. 01/013 wykład 5-6 Podstawy Procesów i Konstrukcji Inżynierskich Atom wodoru Zakład Biofizyki 1 Model atomu Thompsona Model atomu typu ciastka z rodzynkami w 1903 J.J. Thompson zaproponował model
r. akad. 01/013 wykład 5-6 Podstawy Procesów i Konstrukcji Inżynierskich Atom wodoru Zakład Biofizyki 1 Model atomu Thompsona Model atomu typu ciastka z rodzynkami w 1903 J.J. Thompson zaproponował model
FIZYKA-egzamin opracowanie pozostałych pytań
 FIZYKA-egzamin opracowanie pozostałych pytań Andrzej Przybyszewski Michał Witczak Marcin Talarek. Definicja pracy na odcinku A-B 2. Zdefiniować różnicę energii potencjalnych gdy ciało przenosimy z do B
FIZYKA-egzamin opracowanie pozostałych pytań Andrzej Przybyszewski Michał Witczak Marcin Talarek. Definicja pracy na odcinku A-B 2. Zdefiniować różnicę energii potencjalnych gdy ciało przenosimy z do B
Słowniczek pojęć fizyki jądrowej
 Słowniczek pojęć fizyki jądrowej atom - najmniejsza ilość pierwiastka jaka może istnieć. Atomy składają się z małego, gęstego jądra, zbudowanego z protonów i neutronów (nazywanych inaczej nukleonami),
Słowniczek pojęć fizyki jądrowej atom - najmniejsza ilość pierwiastka jaka może istnieć. Atomy składają się z małego, gęstego jądra, zbudowanego z protonów i neutronów (nazywanych inaczej nukleonami),
II.1 Serie widmowe wodoru
 II.1 Serie widmowe wodoru Jan Królikowski Fizyka IVBC 1 II.1 Serie widmowe wodoru W obszarze widzialnym wystepują 3 silne linie wodoru: H α (656.3 nm), H β (486.1 nm) i H γ (434.0 nm) oraz szereg linii
II.1 Serie widmowe wodoru Jan Królikowski Fizyka IVBC 1 II.1 Serie widmowe wodoru W obszarze widzialnym wystepują 3 silne linie wodoru: H α (656.3 nm), H β (486.1 nm) i H γ (434.0 nm) oraz szereg linii
II.5 Sprzężenie spin-orbita - oddziaływanie orbitalnych i spinowych momentów magnetycznych
 r. akad. 004/005 II.5 Sprzężenie spin-orbita - oddziaływanie orbitalnych i spinowych momentów magnetycznych Sprzężenie spin - orbita jest drugim, po efektach relatywistycznych, źródłem rozszczepienia subtelnego
r. akad. 004/005 II.5 Sprzężenie spin-orbita - oddziaływanie orbitalnych i spinowych momentów magnetycznych Sprzężenie spin - orbita jest drugim, po efektach relatywistycznych, źródłem rozszczepienia subtelnego
Jądrowy model atomu. 2. Budowa atomu. Model jądra atomowego Helu
 0--6. Budowa atomu.. Jądrowy model atomu.. Sfera elektronowa w atomach.. Liczby kwantowe i orbitale.. Konfiguracje elektronowe neutron proton Model jądra atomowego Helu nukleony... Jądrowy model atomu
0--6. Budowa atomu.. Jądrowy model atomu.. Sfera elektronowa w atomach.. Liczby kwantowe i orbitale.. Konfiguracje elektronowe neutron proton Model jądra atomowego Helu nukleony... Jądrowy model atomu
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Wartość n 1 2 3 4 5 6 Symbol literowy K L M N O P
 3.4 Liczby kwantowe Funkcja falowa jest wyrażeniem matematycznym, które opisuje elektron jako cząstkę o właściwościach falowych a to oznacza, że każdemu z elektronów w atomie możemy przyporządkować jedną
3.4 Liczby kwantowe Funkcja falowa jest wyrażeniem matematycznym, które opisuje elektron jako cząstkę o właściwościach falowych a to oznacza, że każdemu z elektronów w atomie możemy przyporządkować jedną
NMR Nuclear Magnetic Resonance. Co to jest?
 1 NMR Nuclear Magnetic Resonance Co to jest? Spektroskopia NMR ang. Nuclear Magnetic Resonance Spektroskopia Magnetycznego Rezonansu Jądrowego (MRJ) Wykorzystuje własności magnetyczne jąder atomowych Spektroskopia
1 NMR Nuclear Magnetic Resonance Co to jest? Spektroskopia NMR ang. Nuclear Magnetic Resonance Spektroskopia Magnetycznego Rezonansu Jądrowego (MRJ) Wykorzystuje własności magnetyczne jąder atomowych Spektroskopia
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
REZONANSY : IDENTYFIKACJA WŁAŚCIWOŚCI PRZEZ ANALIZĘ FAL PARCJALNYCH, WYKRESY ARGANDA
 REZONANSY : IDENTYFIKACJA WŁAŚCIWOŚCI PRZEZ ANALIZĘ FAL PARCJALNYCH, WYKRESY ARGANDA Opis układu cząsteczek w mechanice kwantowej: 1. Funkcja falowa, 2. Wektora stanu ψ. TRANSFORMACJE UKŁADU CZĄSTEK: 1.
REZONANSY : IDENTYFIKACJA WŁAŚCIWOŚCI PRZEZ ANALIZĘ FAL PARCJALNYCH, WYKRESY ARGANDA Opis układu cząsteczek w mechanice kwantowej: 1. Funkcja falowa, 2. Wektora stanu ψ. TRANSFORMACJE UKŁADU CZĄSTEK: 1.
Fizyka 3. Konsultacje: p. 329, Mechatronika
 Fizyka 3 Konsultacje: p. 329, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 2 sprawdziany (10 pkt każdy) lub egzamin (2 części po 10 punktów) 10.1 12 3.0 12.1 14 3.5 14.1 16 4.0 16.1 18 4.5 18.1 20 5.0
Fizyka 3 Konsultacje: p. 329, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 2 sprawdziany (10 pkt każdy) lub egzamin (2 części po 10 punktów) 10.1 12 3.0 12.1 14 3.5 14.1 16 4.0 16.1 18 4.5 18.1 20 5.0
Wczesne modele atomu
 Wczesne modele atomu Wczesne modele atomu Demokryt (400 p.n.e.) Grecki filozof Demokryt rozpoczął poszukiwania opisu materii około 2400 lat temu. Postawił pytanie: Czy materia może być podzielona na mniejsze
Wczesne modele atomu Wczesne modele atomu Demokryt (400 p.n.e.) Grecki filozof Demokryt rozpoczął poszukiwania opisu materii około 2400 lat temu. Postawił pytanie: Czy materia może być podzielona na mniejsze
Metody analizy pierwiastków z zastosowaniem wtórnego promieniowania rentgenowskiego. XRF, SRIXE, PIXE, SEM (EPMA)
 Metody analizy pierwiastków z zastosowaniem wtórnego promieniowania rentgenowskiego. XRF, SRIXE, PIXE, SEM (EPMA) Promieniowaniem X nazywa się promieniowanie elektromagnetyczne o długości fali od około
Metody analizy pierwiastków z zastosowaniem wtórnego promieniowania rentgenowskiego. XRF, SRIXE, PIXE, SEM (EPMA) Promieniowaniem X nazywa się promieniowanie elektromagnetyczne o długości fali od około
