Jak leczę chorego z rozpoznanym de novo chłoniakiem grudkowym?
|
|
|
- Dagmara Stachowiak
- 8 lat temu
- Przeglądów:
Transkrypt
1 PRACA POGLĄDOWA Hematologia 2010, tom 1, nr 4, Copyright 2010 Via Medica ISSN Jak leczę chorego z rozpoznanym de novo chłoniakiem grudkowym? How I treat a patient with newly diagnosed follicular lymphoma? Andrzej Deptała Zakład Profilaktyki Onkologicznej, Warszawski Uniwersytet Medyczny Klinika Onkologii i Hematologii, Centralny Szpital Kliniczny Ministerstwa Spraw Wewnętrznych i Administracji, Warszawa Streszczenie Leczenie de novo chłoniaka grudkowego (FL) jest skomplikowane z uwagi na brak powszechnie akceptowanych standardów terapeutycznych. Pierwszym krokiem przy podejmowaniu decyzji o sposobie postępowania jest określenie, czy dany chory na FL rzeczywiście wymaga niezwłocznego leczenia, czy też może być poddany jedynie uważnej obserwacji (strategia watch and wait). Decyzja leczyć od razu lub uważnie obserwować powinna być podjęta na podstawie obiektywnych i zweryfikowanych naukowo kryteriów, jakimi są indeksy prognostyczne (FLIPI/FLIPI2) i algorytmy kliniczne (GELF/BNLI). Leczenie podtrzymujące za pomocą rytuksymabu wydaje się standardową strategią terapeutyczną dla pacjentów, którzy uzyskali odpowiedź kliniczną po leczeniu I linii. Alternatywnym postępowaniem jest konsolidacja pierwszej remisji za pomocą radioimmunoterapii (RIT). Konsolidacja pierwszej remisji przy użyciu procedury autologicznego przeszczepienia macierzystych komórek krwiotwórczych (auto-hsct) powinna być zalecana jedynie w ramach dobrze zaplanowanych badań klinicznych. W niniejszej pracy przedstawiono syntetyczne podejście do terapii chorych na nieleczonego FL. Słowa kluczowe: chłoniak grudkowy, rytuksymab, immunochemioterapia, radioimmunoterapia, autologiczne przeszczepianie macierzystych komórek krwiotwórczych Hematologia 2010; 1, 4: Abstract Treatment of de novo follicular lymphoma (FL) is difficult due to lack of generally accepted standards for therapy. During the first attempt to the patient with FL is mandatory to determine whether the treatment should be applied to the patient without delay or supposed to be postponed (watch and wait stategy). Such decision to defer treatment or to watch and wait must be based on the objective and scientific proven criteria as they are prognostic indices (FLIPI/FLIPI2) and clinical algorithms (GELF/BNLI). Rituximab maintenance is considered to be a standard therapeutic strategy for patients achieving clinical response with first- -line therapy. Consolidation of the first remission using radioimmunotherapy (RIT) serves as alternative approach. First remission consolidation with autologous hematopoietic stem cell Adres do korespondencji: Andrzej Deptała, Klinika Onkologii i Hematologii CSK MSWiA, ul. Wołoska 137, Warszawa, tel.: , faks: , andrzej.deptala@cskmswia.pl 320
2 Andrzej Deptała, Jak leczę chorego z rozpoznanym de novo chłoniakiem grudkowym? transplantation (auto-hsct) is recommended only in well designed clinical trials. In this manuscript a comprehensive approach to the therapy of untreated FL is provided. Key words: follicular lymphoma, rituximab, immunochemotherapy, radioimmunotherapy, autologous hematopoietic stem cell transplantation Hematologia 2010; 1, 4: Wprowadzenie Chłoniak grudkowy (FL, follicular lymphoma) należy do najczęstszych rozrostów limfoidalnych o niskim stopniu złośliwości; w Stanach Zjednoczonych, na przykład, stanowi 20 25% wszystkich de novo rozpoznań chłoniaków [1]. W Polsce FL jest rozpoznawany rzadziej, u 4 5% chorych według Centralnego Rejestru Patologów z 2007 roku, tym niemniej należy do najczęstszych z rodziny chłoniaków indolentnych wywodzących się z dojrzałych limfocytów B [2]. Przebieg FL jest wyjątkowo zmienny, a w obraz kliniczny choroby wpisane są częste nawroty. Niektórzy pacjenci żyją z tym chłoniakiem ponad 20 lat, ale są i tacy, którzy umierają na FL w ciągu 1 2 lat. Znikoma wyleczalność oraz wysoka nawrotowość FL spowodowały, że dla hematoonkologów zajmujących się leczeniem tego chłoniaka, zasadnicze problemy to: 1) właściwe rozróżnienie, którzy chorzy wymagają jedynie obserwacji, a którzy są kandydatami do niezwłocznego leczenia; 2) jeśli leczyć, to w jaki sposób uzyskać i utrzymać remisję chłoniaka. W ciągu wielu lat badań nad FL opracowano tak wiele różnych sposobów postępowania, że trudno jest podać jednoznaczne zalecenia w wyborze terapii. Dlatego w tym artykule, wykorzystując swoje 25-letnie doświadczenie w pracy hematologa oraz na podstawie dostępnego i aktualnego piśmiennictwa naukowego, przedstawiłem poglądy na leczenie de novo FL u dorosłych. Cechy kliniczno-patologiczne FL Chłoniak grudkowy występuje z reguły u dorosłych, najczęściej w 6. dekadzie życia [1], a mediana wieku w momencie rozpoznania FL wynosi 59 lat [3]. Kobiety chorują na FL tylko nieznacznie częściej niż mężczyźni (1,7:1) [1, 3]. Typowo FL zajmuje węzły chłonne zarówno te, które można zbadać palpacyjnie, jak i te, które wymagają nowoczesnych technik obrazowania jamy brzusznej i miednicy małej oraz klatki piersiowej. Spośród innych narządów limfatycznych relatywnie często są zajęte śledziona oraz pierścień Waldeyera. Naciek szpiku kostnego stwierdza się w 60 70% przypadków [4]. Narządy pozalimfatyczne, takie jak wątroba, przewód pokarmowy, skóra, przydatki oka, piersi, jądra, ośrodkowy układ nerwowy (OUN), rzadko są miejscem nacieku FL. Nieczęsto występują objawy B lub zmiany o typie bulky. W zdecydowanej większości przypadków przebieg choroby jest skąpoobjawowy, choć FL z reguły rozpoznaje się w III lub IV stadium zaawansowania klinicznego (CS III lub CS IV wg Ann Arbor). Jedynie u 26 33% chorych rozpoznanie FL następuje w stadium CS I lub CS II. W piśmiennictwie są opisywane samoistne, przejściowe regresje FL, które występują z różną częstością, od kilku do nawet 20% przypadków [3, 4]. Historyczne opracowania podają medianę przeżycia całkowitego (OS, overall survival) wahającą się w granicach 6 10 lat. W patomorfologicznej definicji określa się FL jako nowotwór składający się z komórek linii B, czyli centrocytów i centroblastów/dużych transformowanych komórek, których naciek przypomina swym układem grudki chłonne [1]. W zależności od wzajemnej odsetkowej proporcji centrocytów i centroblastów oraz od typu nacieku, który zawiera centrocyty/centroblasty, można stopniować FL patomorfologicznie (tab. 1) [1]. Obecnie uważa się, że FL powstaje w wyniku transformacji nowotworowej limfocytów B pochodzących z ośrodków rozmnażania grudek chłonnych. Immunofenotypowo charakteryzuje się ekspresją powierzchniowych immunoglobulin (IgM+/, IgD, IgG lub rzadko IgA) i wykazuje dodatnie barwienia dla antygenów: CD19, CD20, CD22, CD79a, CD10 oraz BCL2 (w 85 90%) i BCL6. Barwienia w kierunku CD5, CD43 i IRF4/MUM1 są z reguły ujemne [1]. Chłoniak grudkowy w stopniu 3. (zwłaszcza 3B) może być CD10-ujemny i BCL2-ujemny, przy zachowanej ekspresji BCL6. Przypadki CD10- i BCL2- -ujemne są z reguły IRF4/MUM1-dodatnie [1]. Klasyczną anomalią kariotypu FL jest t(14;18) (q32;q21), którą stwierdza się w 80 90% przypadków, oraz rearanżacja genu BCL2 (ok. 80% przypadków). W wyniku tej klasycznej translokacji gen (BCL2 18q21.3) kodujący białko BCL2 ulega fuzji z genem kodującym łańcuch ciężki immunoglobulin (IGH 14q32.33). Deregulacja powstałego 321
3 Hematologia 2010, tom 1, nr 4 Tabela 1. Stopniowanie patomorfologiczne chłoniaka grudkowego (FL) (źródło [1]) Table 1. Pathological grading of follicular lymphoma (FL) (source [1]) Architektonika nacieku chłoniakowego Grudkowy Układ grudkowy stanowi > 75% Grudkowy i rozlany Układ grudkowy stanowi 25 75% Grudkowy ogniskowo Układ grudkowy stanowi < 25% *Rozlany Układ grudkowy stanowi 0% Stopień 1 2 (niski) Stopień 1 Stopień 2 Stopień 3 (wysoki) Stopień 3A Stopień 3B Stopniowanie i definicja 0 15 centroblastów w dużym polu widzenia 0 5 centroblastów w dużym polu widzenia 6 15 centroblastów w dużym polu widzenia > 15 centroblastów w dużym polu widzenia Centrocyty obecne Obecne wyłącznie centroblasty *Układ nacieku rozlany musi zawierać centrocyty, a komórki nowotworowe muszą wykazywać typowy immunofenotyp dla FL lub t(14;18); pola z naciekiem rozlanym zawierające > 15% centroblastów należy rozpoznać jako chłoniaka rozlanego z dużych komórek B z obecnością FL (FL w stopniu 1 2, 3A lub 3B) genu fuzyjnego prowadzi do transkrypcji i translacji bardzo dużych ilości BCL2 białka hamującego apoptozę. Znacznie rzadziej dochodzi do translokacji BCL2 i genów kodujących łańcuchy lekkie immunoglobulin t(2;18)(p11;q21) lub t(18;22)(q21;q11). W przebiegu FL mogą występować również inne aberracje kariotypu (+7, +18, 3q27-28/BCL6), wśród których 6q23-26 i 17p wydają się mieć niekorzystne znaczenie prognostyczne. Transformacja FL, zwykle w chłoniaka rozlanego z dużych komórek B (DLBCL, diffuse large B-cell lymphoma), występuje w 25 35% i jest związana z inaktywacją TP53, CDKN2A (p16ink4a) i aktywacją MYC [1]. Kryteria wyboru postępowania z chorym na de novo FL Każdego chorego z rozpoznanym de novo FL należy dokładnie zbadać i wykonać u niego tomografię komputerową klatki piersiowej, jamy brzusznej i miednicy małej oraz trepanobiopsję szpiku kostnego. Pierwszym krokiem przy podejmowaniu decyzji o sposobie postępowania jest określenie, czy dany chory na FL rzeczywiście wymaga niezwłocznego leczenia, czy też może być poddany jedynie uważnej obserwacji (strategia watch and wait). Decyzja, czy leczyć od razu, czy uważnie obserwować, powinna być podjęta na podstawie obiektywnych i zweryfikowanych naukowo kryteriów: 1) indeksów prognostycznych FL i 2) algorytmów klinicznych opisujących progresywną postać FL. Pierwszym kryterium jest ocena rokowania za pomocą indeksu prognostycznego. Według mnie indeks FLIPI2 (Follicular Lymphoma International Prognostic Index 2), którego pierwszym punktem końcowym jest przeżycie wolne od progresji (PFS, progression free survival), pozwala lepiej przewidzieć postęp FL niż klasyczny indeks FLIPI, w którym punktem końcowym było OS. Wiadomo, że PFS dokładniej niż OS odwzorowuje dynamikę choroby, a okres PFS nie zależy od kolejnych linii chemioterapii. Ponadto zawarte we FLIPI2 parametry, w tym stężenie b 2 -mikroglobuliny i wielkość węzłów chłonnych (> 6 cm), precyzyjniej określają masę nowotworu niż aktywność dehydrogenazy mleczanowej (LDH, lactate dehydrogenase) czy liczba zajętych okolic węzłowych we FLIPI. Indeks FLIPI2 został opracowany na podstawie danych zbieranych prospektywnie (FLIPI na podstawie danych zbieranych retrospektywnie) oraz z uwzględnieniem wyników leczenia FL rytuksymabem (FLIPI nie obejmował badań z zastosowaniem rytuksymabu). Wysokie ryzyko FLIPI2 będzie więc wskazaniem do rozpoczęcia leczenia. Tabela 2 zawiera porównanie indeksów FLIPI i FLIPI2 [5, 6]. Oprócz FLIPI2, drugim zasadniczym kryterium w wyborze postępowania (watch and wait v. leczenie) są algorytmy kliniczne opisujące progresywną postać FL. Algorytmy takie, pomagające w wyborze wymienianych strategii, zaproponowali w 1997 roku Brice i wsp. (GELF, Groupe d Etude Lymphome Folliculaires) i w 2003 roku Ardeshna i wsp. (BNLI, British National Lymphoma Investigation) (tab. 3) [7]. Kryteria GELF i BNLI o odroczonym leczeniu FL powinno się traktować jako uzupełniające w stosunku do FLIPI2/FLIPI. Oprócz oceny za pomocą wymienionych indeksów i algorytmów klinicznych, wskazań, które przeważą szalę na korzyść rozpoczęcia leczenia, może dostarczyć opis badania histopatologicznego. Znalezienie w preparacie ognisk o układzie rozlanym z obecnością powyżej 15 centroblastów (współistnienie DLBCL i FL) stanowi wskazanie do natychmiastowej terapii, gdyż przemawia za transformacją FL w chłoniaka rozlanego [1] i wiąże się ze skróconym przeżyciem [8]. Również rozpoznanie FL 3B, 322
4 Andrzej Deptała, Jak leczę chorego z rozpoznanym de novo chłoniakiem grudkowym? Tabela 2. Porównanie indeksów rokowniczych FLIPI i FLIPI2 (źródło [5, 6]) Table 2. Comparison of FLIPI and FLIPI2 prognostic indices (source [5, 6]) FLIPI Wiek > 60 lat Stadium III IV Hb < 12,0 g/dl Liczba zajętych okolic węzłowych > 4 LDH > górnej granicy normy FLIPI2 Wiek > 60 lat Zajęcie szpiku kostnego Hb < 12,0 g/dl Węzły chłonne > 6 cm b 2 -mikroglobulina > górnej granicy normy Ryzyko Niskie (0 1czynników), 5-letni OS = 91% Niskie (0 czynników), 5-letni OS = 98%, 5-letni PFS = 79% Pośrednie (2 czynniki), 5-letni OS = 77% Pośrednie (1 2 czynniki), 5-letni OS = 88%, 5-letni PFS = 51% Wysokie ( 3 czynników), 5-letni OS = 53% Wysokie (3 5 czynników), 5-letni OS = 77%, 5-letni PFS = 19% Hb (haemoglobin) hemoglobina; LDH (lactate dehydrogenase) dehydrogenaza mleczanowa; PFS (progression free survival) czas do progresji choroby; OS (overall survival) całkowity czas przeżycia Tabela 3. Kryteria przemawiające za strategią uważnej obserwacji (źródło [7]) Table 3. Criteria for wait and watch strategy (source [7]) GELF (Groupe d Etude Lymphome Folliculaires) BNLI (British National Lymphoma Investigation) Wszystkie poniższe spełnione: Nieobecne żadne z poniższych: 1. Maksymalny wymiar zmiany < 7 cm 1. Objawy B lub świąd skóry 2. Zajęcie < 3 grup węzłów 2. Szybka, uogólniona progresja chłoniaka 3. Wielkość śledziony < 16 cm 3. Zagrażające życiu zajęcie narządów 4. Brak objawów naciekania/ucisku miejscowego 4. Nacieki nerek przez guz nowotworowy 5. Zmiany w kościach 5. Brak objawów ogólnych 6. Hb < 10,0 g/dl 6. Brak komórek chłoniaka we krwi obwodowej 7. WBC < 3, /l 7. Nieobecność: 8. PLT < 100, /l Hb < 10,0g/dl WBC < 1, /l PLT < 100, /l Hb (haemoglobin) hemoglobina; WBC (white blood cells) liczba krwinek białych; PLT (platelets) liczba płytek w mojej opinii, jest wskazaniem do rozpoczęcia terapii, ponieważ biologia i postęp tego typu chłoniaka wykazują znaczące podobieństwo do de novo DLBCL [3]. Co prawda, wyniki niektórych badań [8, 9] wykazywały, że OS i czas do niepomyślnego zdarzenia (EFS, event free survival) dla FL 3A i FL 3B nie różnią się istotnie statystycznie, lecz były to badania retrospektywne, a więc nie w pełni wiarygodne. Podstawami bardziej nowoczesnych prób ustalenia rokowania chorego na FL de novo są immunofenotypowanie i analizy molekularne. Stwierdzane tymi metodami różne nieprawidłowości komórek chłoniakowych i/lub komórek prawidłowych mikrośrodowiska z reguły są niedostępne na co dzień i tym samym mało użyteczne w praktyce klinicznej, na przykład wykrycie za pomocą CGH (comparative genomic hybridization) utraty materiału genetycznego 1p36.22-p36.33 i 6q21-q24.3, świadczącej o szybkiej transformacji FL i krótszym przeżyciu [3]). Niejednokrotnie nowe markery tracą swoją znamienność statystyczną w analizach wielowymiarowych z uwzględnieniem indeksów prognostycznych na przykład markery immunofenotypowe CD10, BCL6, PU.1, p53, BCLX L [3] lub ich status staje się niejednoznaczny, ponieważ pochodzą z danych retrospektywnych i sprzed ery leczenia rytuksymabem (np. markery cytogenetyczne: 6q, +7, +X, +12, +21, 17p lub molekularne LOH 6q25-27 [3]). Odrębnym zagadnieniem są braki w walidacji większości markerów immunofenotypo- 323
5 Hematologia 2010, tom 1, nr 4 wych i molekularnych w prospektywnych randomizowanych badaniach klinicznych III fazy. Dlatego, według mnie, immunofenotypowe i molekularne markery prognostyczne nie mają obecnie znaczenia w podejmowaniu decyzji o rozpoczęciu leczenia FL. Wybór terapii I linii Chory na FL znajdujący się w grupie wysokiego ryzyka FLIPI2 kwalifikuje się do bezzwłocznego rozpoczęcia leczenia. W przypadku grupy pośredniego lub niskiego ryzyka FLIPI2 pomocne w podjęciu decyzji leczyć, czy obserwować są algorytmy BNLI lub GELF. Dla chorego od razu zakwalifikowanego do leczenia pozostaje wybór rodzaju terapii teleradioterapia, immunoterapia lub immunochemioterapia. Teleradioterapia Tradycyjnie teleradioterapię, jako samodzielną metodę leczenia, stosuje się we wczesnych stadiach zaawansowania FL CS I i CS II zwykle bez objawów ogólnych (wg MacManusa tylko 3% chorych miało objawy B [10]). Takie postępowanie skutkuje uzyskaniem długotrwałych remisji FL na poziomie 30 50%, z medianą przeżycia 13,8 roku. Po 5, 10, 15 i 20 latach w stanie wolnym od nawrotu pozostaje odpowiednio 55%, 44%, 40% i 37% pacjentów, a żyjących odpowiednio: 82%, 64%, 44% i 37% chorych [10]. Krzywe przeżycia wolnego od choroby (DFS, disease free survival) osiągają plateau po 15 latach [3], co może sugerować, że za pomocą teleradioterapii możliwe jest wyleczenie FL w stadiach zaawansowania CS IA IIA. Do pełnej oceny roli teleradioterapii we wczesnych stadiach FL brakuje prospektywnych, randomizowanych badań III fazy, porównujących tę metodę z leczeniem opartym na rytuksymabie, na przykład: teleradioterapia z rytuksymabem versus teleradioterapia oraz teleradioterapia z rytuksymabem versus chemioterapia z rytuksymabem. Rytuksymab w monoterapii Wprowadzenie do praktyki klinicznej, w latach 90. XX wieku, rytuksymabu spowodowało przełom w terapii chłoniaków B-komórkowych, a FL w szczególności. Rytuksymab, chimeryczne przeciwciało monoklonalne anty-cd20 zabijające komórki w wyniku aktywacji mechanizmu cytotoksyczności zależnej od dopełniacza (CDC, complement dependent cytotoxicity) i przeciwciał (ADCC, antibody dependent cell cytotoxicity), okazał się skuteczny w monoterapii, a także w skojarzeniu z chemioterapią. Wyniki badań z zastosowaniem rytuksymabu w FL są powszechnie znane polskim hematoonkologom, były też publikowane w polskim piśmiennictwie [2, 11] i dlatego zrezygnowałem z systematycznego omawiania poszczególnych badań. Omówiłem jedynie ważniejsze prace i dokonałem syntezy pozostałych. Leczenie de novo FL za pomocą rytuksymabu w monoterapii, podawanego w sposób klasyczny (indukcyjny: mg/m 2 co 7 dni), pozwoliło na uzyskanie całkowitej odpowiedzi klinicznej (ORR, overall response rate) u około 70% chorych, w tym całkowitych remisji (CR, complete remission) u 20 35%, i mediany PFS wynoszącej około 23 miesiące [12]; w jednym z badań po 7 latach żyło 91% chorych [12]. W 2004 roku Ghielmini i wsp. [13] opublikowali wyniki randomizowanego badania, w którym porównano klasyczny schemat podawania rytuksymabu (faza indukcyjna + obserwacja grupa A) z przedłużonym stosowaniem tego leku (faza indukcyjna + dodatkowo w tej samej dawce, 4 co 2 miesiące grupa B), u pacjentów nieleczonych (32%) i z nawrotowym FL wrażliwym na poprzednie terapie (64%). Okazało się, że w grupie B chorych nieleczonych uzyskano znamienne wydłużenie EFS do 36 miesięcy (19 miesięcy w grupie A; p = 0,009); odsetek ORR wyniósł 67% [13]. Czas trwania odpowiedzi nie różnił się statystycznie istotnie między grupami B i A (mediana nieosiągnięta, w porównaniu z 20,4 miesiąca; p = 0,079). Czynnikiem predykcyjnym EFS było uzyskanie odpowiedzi klinicznej na fazę indukcyjną. Niezależnymi czynnikami predykcyjnymi uzyskania odpowiedzi klinicznej okazały się: brak wcześniejszej chemioterapii i nieobecność zmian typu bulky. W tym badaniu większość chorych była w stadium CS III IV (85%) i w stopniu histologicznym 1 2 (79%). Podsumowując wyniki badań z zastosowaniem rytuksymabu w monoterapii, uważam, że z tego typu leczenia mogą skorzystać pacjenci z nieleczonym objawowym FL i postacią lepiej rokującą, czyli cechujący się niskim ryzykiem według FLIPI2, stopniem histologicznym 1 2 i brakiem bulky disease lub klinicznych zespołów uciskowych. Preferowanym schematem byłby ten zaproponowany przez Ghielmini i wsp. [13]. Duża skuteczność i dobra tolerancja rytuksymabu w monoterapii stawiają pod znakiem zapytania przydatność strategii uważnej obserwacji w postępowaniu z chorym na de novo FL. Publikacja w niedalekiej przyszłości wyników badania Watch and Wait, którego rekrutacja została niedawno zakończona, powinna wyjaśnić rolę uważnej obserwacji w strategii postępowania z chorymi na de novo FL i zweryfikować schemat podawania rytuksymabu w monoterapii. 324
6 Andrzej Deptała, Jak leczę chorego z rozpoznanym de novo chłoniakiem grudkowym? Rytuksymab w skojarzeniu z chemioterapią W badaniach II i III fazy udowodniono, że skojarzenie rytuksymabu z różnymi schematami chemioterapii powoduje znamienne wydłużenie PFS i OS, zwiększenie odsetka CR oraz wydłużenie okresu ich trwania. Dlatego uważam, że rytuksymab powinien być składnikiem każdego rodzaju terapii rozpoznanego de novo FL. Potwierdzeniem tego faktu jest opublikowana w 2009 roku analiza Cochrane, w której wykazano, że immunochemioterapia, oprócz poprawy ORR i PFS, statystycznie znamiennie poprawia OS chorych na FL (współczynnik ryzyka [HR, hazard ratio] dla umieralności 0,63; 95-proc. przedział ufności [CI, confidence interval] 0,51 0,79) w porównaniu z samą chemioterapią [14]. Rytuksymab był kojarzony z różnymi schematami chemioterapii, w tym z CHOP (cyklofosfamid, doksorubicyna, winkrystyna, prednizon), CVP (cyklofosfamid, winkrystyna, prednizon), CHVP (cyklofosfamid, doksorubicyna, winblastyna, prednizon), MCP (mitoksantron, cyklofosfamid, prednizon), FCM (fludarabina, cyklofosfamid, prednizon) i bendamustyną (B). Na podstawie opublikowanych i dostępnych wyników badań nie można jednoznacznie stwierdzić, który z tych schematów jest lepszy do kojarzenia z rytuksymabem. Także na podstawie wyników badania PRIMA (Primary Rituximab and Maintenance) [15], zaprezentowanych na tegorocznym zjeździe ASCO (American Society of Clincal Oncology), nie można rozstrzygnąć tego dylematu. W pierwotnych założeniach tego badania analiza pierwszej randomizacji miała umożliwić ocenę skuteczności poszczególnych schematów, a okazało się, że 75% chorych otrzymało rytuksymab w połączeniu z CHOP (R-CHOP), 22% z CVP (R-CVP), a 3% z FCM (R-FCM) [15]. Z piśmiennictwa wynika, że do tej pory najczęściej stosowano 2 schematy immunochemioterapii, R-CHOP i R-CVP, które choć dotychczas nieporównane bezpośrednio pełnią rolę referencyjnych. Pomijając szczególne przypadki, jestem zwolennikiem stosowania w I linii terapii FL schematu R-CVP, a pogląd ten wynika z następujących przesłanek: 1) schemat R-CVP jest tak samo skuteczny, a pozbawiony kardiotoksyczności i znacznie mniej mielotoksyczny w porównaniu z R-CHOP; 2) w przypadku niepowodzenia po R-CVP w I linii istnieją szanse na efekt R-CHOP w II linii odwrotna kolejność terapii tej szansy nie daje; 3) FL z reguły ma przebieg indolentny i bardzo rzadko wymaga intensywnego postępowania w I linii. Na potwierdzenie tej subiektywnej opinii można przytoczyć metaanalizę, w której porównano wyniki badań z R-CVP i R-CHOP w leczeniu FL [16]. We wnioskach autorzy podają, że choć obydwa schematy zapewniają uzyskanie znakomitych wskaźników odpowiedzi klinicznej, to R-CVP jest korzystniejszą opcją dla osób z dodatnim wywiadem w kierunku chorób serca oraz dla osób młodych, u których jedną z opcji w przyszłości może być autologiczne przeszczepienie macierzystych komórek krwiotwórczych (auto-hsct, autologous hematopoietic stem cell transplantation), z uwagi na skumulowanie efektów kardiotoksycznych w długotrwałym przebiegu FL [16]. Rozstrzygnięcie, który z tych dwóch schematów jest bardziej skuteczny w indukcji remisji FL, powinno przynieść prowadzone właśnie badanie kliniczne Polskiej Grupy Badawczej Chłoniaków (PLRG, Polish Lymphoma Research Group) PLRG4. Do szczególnych przypadków, w których w I linii zastosowałbym R-CHOP zamiast R-CVP, należą FL 3B niezależnie od indeksu FLIPI2 oraz FL3A i wysokie ryzyko według FLIPI2. To stanowisko jest zgodne z doniesieniami innych autorów [12]. W grudniu 2009 roku na kongresie ASH (American Society of Hematology) przedstawiono wyniki prospektywnego, randomizowanego badania III fazy porównującego skuteczność i bezpieczeństwo schematu R-CHOP w stosunku do stosowania rytuksymabu w połączeniu z B (BR) w leczeniu I linii 513 chorych na chłoniaki indolentne (w tym 285 chorych na FL) i chłoniaka z komórek płaszcza [17]. Okazało się, że w grupie 513 chorych schemat BR w porównaniu z R-CHOP pozwolił na osiągnięcie statystycznie znamiennie wyższego odsetka CR (40,1% v. 30,8%; p = 0,032), co przełożyło się na istotne wydłużenie mediany PFS (54,8 mies. v. 34,8 mies.; p = 0,0002) oraz mediany czasu do zastosowania kolejnego leczenia (nie osiągnięto v. 40,7 mies.; p = 0,0002); mediany OS nie różniły się istotnie. Schemat BR okazał się też znacznie mniej toksyczny niż R-CHOP, w tym odnotowano znamiennie mniej neutropenii, zakażeń, łysienia i zapaleń jamy ustnej [17]. Do zaakceptowania schematu BR, jako nowego standardu w I linii leczenia FL, konieczne są wyniki kolejnych badań randomizowanych. Leczenie FL po uzyskaniu odpowiedzi klinicznej za pomocą terapii I linii Po uzyskaniu odpowiedzi klinicznej, w tym CR lub częściowej remisji (PR, partial remission), za pomocą terapii I linii hematolog lub onkolog opiekujący się chorym na FL powinien dołożyć starań, aby jak najdłużej utrzymać remisję chłoniaka, gdyż takie postępowanie zapewnia lepszy komfort życia pacjenta. Istnieją naukowe przesłanki, że takie po- 325
7 Hematologia 2010, tom 1, nr 4 stępowanie z chorym na FL powoduje, że żyje on dłużej niż pacjent leczony od progresji do progresji [11, 18]. Według mnie, obecnie, tylko dwie koncepcje, których zadaniem jest utrzymanie remisji FL, zasługują na uwagę, a mianowicie leczenie podtrzymujące za pomocą rytuksymabu i konsolidacja remisji z wykorzystaniem radioimmunoterapii (RIT). Nie jestem zwolennikiem przeprowadzania auto-hsct w pierwszej remisji FL, z uwagi na brak rzetelnych naukowych podstaw do stosowania tego typu procedury. Badania randomizowane z zastosowaniem auto-hsct pochodzą sprzed ery rytuksymabu i uzyskano w nich niespójne wyniki końcowe, przy czym w żadnym nie udowodniono wpływu transplantacji na wydłużenie OS [4, 11, 12]. W badaniu niemieckiej grupy GSLG (German Study Lymphoma Group) [19] w indukcji remisji FL u połowy pacjentów zastosowano R-CHOP, jednak w leczeniu podtrzymującym nie podawano rytuksymabu tylko interferon a (IFNa), a procedurze auto-hsct poddano zaledwie 44 osoby (w wieku < 60 lat). W leczeniu podtrzymującym zastosowano IFNa u 132 chorych poniżej 60. roku życia (indukowanych za pomocą R-CHOP) i u wszystkich chorych po 60. roku życia (niepoddanych przeszczepieniu). Słabością tego badania jest brak analizy statystycznej porównującej przeżycie chorych, którzy otrzymali w indukcji R-CHOP i po uzyskaniu remisji zostali poddani konsolidacji auto-hsct, z grupą, która otrzymała R-CHOP, nie była poddana przeszczepieniu i otrzymała leczenia podtrzymujące IFNa. Zamieszczone w pracy krzywe przeżycia obrazują tylko czas trwania remisji, a nie OS i wykazują jedynie tendencję na korzyść procedury przeszczepowej. Do czasu opublikowania twardych dowodów, że strategia oparta na indukcji remisji za pomocą immunochemioterapii, uzupełniona konsolidacją pierwszej remisji w oparciu o auto-hsct i następowym leczeniem podtrzymującym z użyciem rytuksymabu (a nie IFNa) wydłuża przeżycie bardziej niż strategia z pominięciem procedury przeszczepowej, nie należy stosować procedury auto-hsct w pierwszej remisji FL w standardowej praktyce klinicznej, a wyłącznie w ramach dobrze zaplanowanych badań klinicznych. Leczenie podtrzymujące w chłoniakach indolentnych, a szczególnie w FL, zostało dokładnie omówione w mojej poprzedniej publikacji [11]. Dlatego w tej pracy, oprócz podsumowania terapii podtrzymującej, przedstawiam wyniki prac, które ukazały się w 2010 roku. Terapia podtrzymująca za pomocą IFNa nie sprawdziła się w leczeniu podtrzymującym FL. Metaanaliza opublikowana przez Rohatiner i wsp. [20] wykazała, że IFNa w większych dawkach ( 5 MU/ /d. i 36 MU/mies.) dodany do chemioterapii statystycznie znamiennie wydłuża OS, ale w leczeniu indukującym remisję, a nie w leczeniu podtrzymującym. Uporczywe i dość licznie występujące działania niepożądane w czasie leczenia IFNa zmusiły 15 33% chorych do zaprzestania terapii. Te dwa fakty czynią IFNa nieprzydatnym w leczeniu podtrzymującym [11]. Leczenie podtrzymujące z użyciem rytuksymabu Rytuksymab, jak dotąd, pozostaje jedynym lekiem, w stosunku do którego udowodniono wydłużenie PFS/EFS i/lub OS w nawrotowych/opornych FL, po indukcji remisji za pomocą chemioterapii, chemioimmunoterapii lub monoterapii rytuksymabem [2, 11, 13, 21]. Metaanaliza 5 randomizowanych badań potwierdziła, że chorzy otrzymujący leczenie podtrzymujące rytuksymabem żyją statystycznie znamiennie dłużej w porównaniu z pacjentami poddanymi obserwacji lub leczonymi rytuksymabem dopiero podczas nawrotu chłoniaka, ale dotyczy to wyłącznie FL nawrotowego/opornego (HR dla zgonu 0,58; 95% CI 0,42 0,79). Autorzy metaanalizy konkludują, że rytuksymab powinien być podawany w postaci 4 cotygodniowych iniekcji co 6 miesięcy lub pojedynczej iniekcji co 2 3 miesiące. Zazwyczaj terapia podtrzymująca nie trwała dłużej niż 2 lata [22]. Profil toksyczności rytuksymabu jest znany i przewidywalny. Wczesne działania niepożądane są łagodne i zwykle ograniczają się do niezbyt nasilonych reakcji poprzetoczeniowych w postaci gorączki i dreszczy, najczęściej podczas pierwszego podania [11]. Toksyczność hematologiczna w stopniu występuje pod postacią limfopenii u 40%, neutropenii u 6%, niedokrwistości u 3% i małopłytkowości u 2% leczonych [11]. Obniżenie stężenia immunoglobulin i limfopenia po zastosowaniu rytuksymabu mogą predysponować do rozwoju infekcji, zwłaszcza gdy podaje się ten lek dłużej niż rok [11]. Zgodnie z tematem tej pracy pozostaje mi udowodnić korzyści z terapii podtrzymującej rytuksymabem dla przeżycia chorych nieleczonych. Publikacja wyników toczących się badań dotyczących de novo FL powinna wyjaśnić kwestię leczenia podtrzymującego rytuksymabem po indukcji remisji za pomocą tego leku w monoterapii (RESORT i Rituximab versus Watch and Wait Trial) i po indukcji za pomocą immunochemioterapii (PRIMA, OSHO/ /GLSG i PLRG4). Obecnie istnieją jedynie wyniki badania PRI- MA bez analizy OS [15]. Do tego badania włączono 326
8 Andrzej Deptała, Jak leczę chorego z rozpoznanym de novo chłoniakiem grudkowym? 1202 chorych z nieleczonym FL w stopniu histologicznym 1 3A, którzy spełnili co najmniej jedno z następujących kryteriów: stan sprawności ECOG poniżej 2, choroba typu bulky, obecne objawy B, wartości LDH lub b 2 -mikroglobuliny powyżej górnej granicy normy, zajęcie co najmniej 3 grup węzłowych (każda > 3 cm wielkości), objawowe powiększenie śledziony, zespoły uciskowe, hydrothorax/ascites. Do badania nie kwalifikowano FL 3B. Terapia indukcyjna składała się z 8 cykli immunochemioterapii; schematy do wyboru: R-CHOP, R-CVP lub R-FCM. Po uzyskaniu CR, niepotwierdzonej CR (CRu, CR unconfirmed) lub PR chorych przydzielono w stosunku 1:1 do 2 grup: 505 pacjentów do grupy leczonej rytuksymabem (1 375 mg/m 2 co 8 tygodni przez 2 lata) i 513 do grupy poddanej jedynie obserwacji. Po 24 miesiącach od randomizacji pierwszorzędowy punkt, jakim było PFS, został spełniony i w grupie leczonej rytuksymabem 2 lata przeżyło 82% pacjentów, a w grupie obserwacyjnej 66% bez progresji chłoniaka (HR 0,50; 95% CI 0,39 0,64; p < 0,0001). Statystycznie znamiennie na korzyść podtrzymywania za pomocą rytuksymabu wypadły również niektóre drugorzędowe punkty końcowe: TTNLT (time to next anti-lymphoma treatment) i TTNCT (time to next chemotherapy), odpowiednio: HR 0,61 (p = 0,0003) i HR 0,60 (p = 0,0011). Po 2 latach stosowania rytuksymabu w CR/ /CRu pozostawało 66,8% w grupie podtrzymującej i 47,7% w grupie obserwacyjnej [15]. Objawy niepożądane częściej występowały w grupie podtrzymującej leczonej rytuksymabem w porównaniu z grupą obserwacyjną i dotyczyły zwłaszcza całkowitego odsetka zakażeń (37% v. 22%) oraz w stopniach (4% v. 1%), a także neutropenii w stopniach (4% v. < 1%) [15]. Od chwili przedstawienia wyników badania PRIMA strategia leczenia de novo FL oparta na indukcji za pomocą immunochemioterapii i leczenia podtrzymującego CR lub PR przez 2 lata za pomocą rytuksymabu stały się platformą odniesienia do konstruowania przyszłych badań nad leczeniem podtrzymującym i można tę strategię zalecać w rutynowej praktyce klinicznej. Po udowodnieniu korzyści dla OS i opublikowaniu w pełnej formie pracy strategia ta będzie nowym standardem postępowania w nieleczonym objawowym FL 1 3A. Doprecyzowania wymaga jedynie rodzaj immunochemioterapii indukcyjnej, bowiem w badaniu PRIMA, decyzją badaczy, 75% chorych otrzymało R-CHOP. Wyniki randomizowanego badania III fazy PLRG4, porównującego R-CHOP z R-CVP w indukcji remisji oraz leczenie podtrzymujące rytuksymabem przez 2 lata w stosunku do obserwacji, ma szansę przyczynić się do ustalenia nowego standardu postępowania nie tylko w nieleczonym FL, ale w innych de novo chłoniakach indolentnych. Leczenie konsolidujące z wykorzystaniem RIT Lek 131 I-tositumomab nie jest stosowany w Polsce i w Europie jako RIT, dlatego nie będzie omawiany w dalszej części tej pracy. W Polsce i w Europie w RIT podaje się 90 Y-ibritumomab tiuksetanu ( 90 Y-IT) i z tego względu określenia RIT i 90 Y-IT będą używane zamiennie. Gotowy do iniekcji preparat RIT składa się z 2 aktywnych terapeutycznie podjednostek, czyli radioizotopu itru ( 90 Y) i przeciwciała monoklonalnego anty-cd20 (ibritumomabu tiuksetanu), połączonego z czynnikiem chelatującym MX-DTPA. Radioizotop 90 Y jest emiterem cząstek b (elektronów), które mają maksymalną energię 2,2 MeV i zdolność do promieniowania na głębokość do około 5 mm. Fizyczny okres półtrwania izotopu wynosi 64 godziny. Ibritumomab tiuksetanu jest rekombinowanym mysim przeciwciałem monoklonalnym IgG1k, rozpoznającym swoiście antygen CD20. Aby zwiększyć stopień wiązania ibritumomabu tiuksetanu z komórkami chłoniaka, konieczna jest premedykacja małymi dawkami rytuksymabu w celu usunięcia krążących limfocytów B. Ta premedykacja pozwala na bardziej precyzyjne niszczenie nowotworu w mechanizmie ADCC oraz w wyniku działania promieniowania b emitowanego przez 90 Y. Mediana skutecznego klinicznie okresu półtrwania w surowicy krwi gotowego leku wynosi 28 godzin. Na leczenie 90 Y-IT najlepiej odpowiadają guzy o rozmiarach nie większych niż 5 cm średnicy ze względu na skąpe unaczynienie chłoniaka. Warunkiem sine qua non zastosowania tego leku jest brak zajęcia szpiku kostnego przez chłoniaka lub nacieczenie nieprzekraczające 25% utkania komórkowego [18, 23, 24]. W opublikowanych wynikach kilku badań II fazy autorzy donosili, że po konsolidacji pierwszej remisji za pomocą 90 Y-IT znacząco zwiększył się odsetek CR (z 28%, 44% i 70% do odpowiednio 67%, 89% i 96%), a ponad 75% chorych przeżyło 2 lata bez progresji FL [24]. Jednak dopiero w randomizowanym badaniu III fazy Morschhauser i wsp. [25] udowodnili wartość konsolidacji pierwszej remisji za pomocą RIT w nieleczonym FL. W opublikowanej w 2008 roku pracy (414 pacjentów) wykazano, że po leczeniu indukcyjnym za pomocą różnych rodzajów chemioterapii (tylko 15% chorych było leczonych na bazie rytuksymabu) konsolidacja 90 Y-IT (208 pacjentów) w porównaniu z obserwacją (206 pacjentów) poskutkowała wydłużeniem mediany 327
9 Hematologia 2010, tom 1, nr 4 PFS do 36,5 miesiąca w porównaniu z 13,5 miesiącem (HR 0,465; p < 0,0001). Ta statystycznie znamienna poprawa nie zależała od stanu remisji uzyskanej po indukcji i dotyczyła zarówno PR (mediana PFS = 29,7 v. 6,3 mies.; HR 0,304; p < 0,0001), jak i CR (mediana PFS 54,6 v. 29,9 mies.; HR 0,613; p = 0,0154). Leczenie RIT było dość dobrze tolerowane, ale często po 90 Y-IT obserwowano limfopenię, neutropenię i małopłytkowość w stopniach 3. i 4. (odpowiednio u 60%, 67% i 61% chorych). Zakażenia wystąpiły u 7% chorych. W innym badaniu Goff i wsp. [26] zaobserwowali, że obecna po chemioterapii indukcyjnej minimalna choroba resztkowa (MRD, minimal residual disease) stała się niewykrywalna u 90% pacjentów w okresie 3 miesięcy po konsolidacji 90 Y-IT (w grupie bez RIT jedynie u 36%). To zniknięcie MRD przełożyło się na dłuższe PFS w grupie chorych poddanych konsolidacji RIT (40,8 mies. v. 24 mies.; HR 0,339; p < 0,01) [26]. Podsumowanie Właściwe postępowanie z chorym z rozpoznanym de novo FL nie jest łatwe. Jak wskazują dane ze Stanów Zjednoczonych (National LymphoCare Study), w codziennej praktyce amerykańskiego hematoonkologa przewijają się różne opcje terapeutyczne uważnej obserwacji podlegało 17,7% chorych, rytuksymab w monoterapii otrzymało 13,9%, tylko radioterapię 5,6%, tylko chemioterapię 3,2%, rytuksymab z chemioterapią zastosowano u 51,9% pacjentów, a do badań klinicznych włączono jedynie 6,1% chorych [27]. Rozpoczęcie leczenia de novo FL we właściwym czasie, czyli niezwłocznie po rozpoznaniu lub po okresie uważnej obserwacji, wymaga określenia rokowania za pomocą indeksu FLIPI2 oraz dokonania analizy, czy pacjent cierpi na progresywną chorobę, czy też nie (algorytmy kliniczne GELF/BNLI). Nie bez znaczenia jest wybór optymalnej pierwszej terapii. Dla FL w stadium zaawansowania IA IIA według klasyfikacji Ann Arbor tym pierwszym krokiem będzie radioterapia. Z kolei chory na FL z objawami ogólnymi lub w III IV stadium zaawansowania według Ann Arbor albo z innymi cechami progresji chłoniaka będzie kandydatem do terapii na bazie rytuksymabu. W przypadku niskiego ryzyka według FLIPI2, bez obecności bulky disease lub innych niepokojących sytuacji klinicznych (np. zespołów uciskowych) oraz w stopniu histologicznym można rozpocząć leczenie od monoterapii rytuksymabem. W pozostałych przypadkach de novo FL należy zastosować immunochemioterapię (R-CVP lub R-CHOP). Po uzyskaniu odpowiedzi klinicznej (CR lub PR) lekarz ma do wyboru dwie opcje, w tym terapię podtrzymującą za pomocą rytuksymabu lub konsolidację przy użyciu 90 Y-IT. Nie opublikowano wyników bezpośredniego porównania tych dwóch metod, dlatego należy dokonać wyboru w sposób pośredni, kierując się innymi wskazaniami i przeciwwskazaniami klinicznymi oraz preferencjami pacjenta. Za leczeniem podtrzymującym rytuksymabem przemawiają wyniki dobrze udokumentowanych badań III fazy, łatwość zastosowania i niewiele działań niepożądanych o niskim stopniu toksyczności. Przeciwko terapii podtrzymującej rytuksymabem przemawia niewielka szansa na eradykację MRD oraz konieczność powtarzających się hospitalizacji przez 2 lata. Z kolei za konsolidacją 90 Y-IT świadczą eradykacja MRD u zdecydowanej większości pacjentów (wyleczenie?) i możliwość uwolnienia chorego na 2 lata od hospitalizacji z powodu progresji chłoniaka (ok. 3/4 pacjentów). Przeciwko RIT przemawiają jej nieznana skuteczność po indukcji remisji FL na bazie immunochemioterapii z zastosowaniem rytuksymabu, skomplikowana procedura aplikacji oraz występowanie częstych i nasilonych objawów toksycznych. Wysoka skuteczność ofatumumabu (O), w pełni ludzkiego przeciwciała monoklonalnego IgG1 o nieco innym mechanizmie działania niż rytuksymab (łączy się z małą i dużą pętlą antygenu CD20 i silniej aktywuje CDC), z chemioterapią CHOP (O-CHOP) w postaci 76% CR/CRu w grupie de novo FL wysokiego ryzyka (FLIPI 3-5), dowodzi, że w niedługim czasie będzie do dyspozycji nowy lek w terapii tego chłoniaka [28]. Trwają badania kliniczne I III fazy obejmujące chorych na chłoniaki B-komórkowe nad kilkoma innymi przeciwciałami monoklonalnymi anty-cd20 nowej generacji, w tym GA101 (w pełni ludzkie IgG1, wielokrotnie silniej aktywujące ADCC i bezpośrednią cytotoksyczność niż rytuksymab), weltuzumabem (humanizowane IgG1, silniej aktywujące CDC niż rytuksymab), okrelizumabem (humanizowane IgG1, słabiej aktywujące CDC niż rytuksymab), AME-133v (w pełni ludzkie IgG1, ze zmodyfikowanym fragmentem Fc, silniej aktywujące ADCC niż rytuksymab) i PRO (humanizowane IgG1, o podobnej do rytuksymabu zdolności aktywującej ADCC i CDC i silniej bezpośrednio niszczące komórki nowotworowe). Jeśli do tego armamentarium dodać inne przeciwciała monoklonalne (galiksimab, anty-cd80 i epratuzumab, anty-cd22), szczepionki antyidiotypowe oraz substancje celowane molekularnie (bortezomib, niskocząsteczkowe inhibitory BCL2, inhibitory pętli p53-mdm, akty- 328
10 Andrzej Deptała, Jak leczę chorego z rozpoznanym de novo chłoniakiem grudkowym? watory receptorów śmierci TRAIL), to można dostrzec zupełnie nowe kierunki rozwoju leczenia FL w przyszłości [29]. Podziękowanie Dziękuję Prof. dr. hab. n. med. Krzysztofowi Warzocha za zachętę do napisania tej pracy. Piśmiennictwo 1. Harris N.L., Swerdlow S.H., Jaffe E.S. i wsp. Follicular lymphoma. W: Swerdlow S.H., Campo E., Harris N.L. i wsp. (red.). WHO classification of tumours of haematopoietic and lymphoid tissues. IARC Press, Lyon 2008: Jurczak W., Walewski J. Rola rytuksymabu w leczeniu chorych na chłoniaki grudkowe. Onkol. Klin. Prakt. 2006; 2: Relander T., Johnson N.A., Farinha P., Connors J.M., Sehn L.H., Gascoyne R.D. Prognostic factors in follicular lymphoma. J. Clin. Oncol. 2010; 28: Tan D., Horning S.J. Follicular lymphoma: clinical features and treatment. Hematol. Oncol. Clin. North Am. 2008; 22: Solal-Celigny P., Roy P., Colombat P. i wsp. Follicular Lymphoma International Prognostic Index. Blood 2004; 104: Federico M., Bellei M., Marcheselli L. i wsp. Follicular Lymphoma International Prognostic Index 2: a new prognostic index for follicular lymphoma developed by the International Follicular Lymphoma Prognostic Factor Project. J. Clin. Oncol. 2009; 27: Gribben J.G. How I treat indolent lymphoma. Blood 2007; 109: Hans C.P., Weisenburger D.D., Vose J.M. i wsp. A significant diffuse component predicts for inferior survival in grade 3 follicular lymphoma, but cytologic subtypes do not predict survival. Blood 2003; 101: Chau I., Jones R., Cunningham D. i wsp. Outcome of follicular lymphoma 3: is antracycline necessary as front-line therapy? Br. J. Cancer 2003; 89: MacManus M.P., Hoppe R.T. Is radiotherapy curative for stage I and II low-grade follicular lymphoma? Results of a long-term follow-up study of patients treated at Stanford University. J. Clin. Oncol. 1996; 14: Deptała A., Pałynyczko G. Leczenie podtrzymujące w przewlekłych chłoniakach niehodgkinowskich. Acta Haematol. Pol. 2009; 40: Seiler T., Hiddemann W., Dreyling M. Optimal application of antibodies in the treatment of follicular lymphoma: current standards and future strategies. Immunotherapy 2009; 1: Ghielmini M., Schmitz S-F.H., Cogliatti S.B. i wsp. Prolonged treatment with rytuksymab in patients with follicular lymphoma significantly increases event-free survival and response duration compared with the standard weekly 4 schedule. Blood 2004; 103: Schulz H., Bohlius J., Skoetz N. i wsp. Chemotherapy plus rituximab versus chemotherapy alone for B-cell non-hodgkin s lymphoma (review). Cochrane Database Systematic Review, The Cochrane Library 2009, Issue Salles G.A., Seymour J.F., Feugier P. i wsp. Rituximab maintenance for 2 years in patients with untreated high tumor burden follicular lymphoma after response to immunochemotherapy. J. Clin. Oncol. 2010; 28: abstrakt Siddhartha G., Vijay P. R-CHOP versus R-CVP in the treatment of follicular lymphoma: a meta-analysis and critical appraisal of current literature. J. Hematol. Oncol. 2009; 2: Rummel M.J., Niederle N., Maschmeyer G. i wsp. Bendamustine plus rituximab is superior in respect of progression free survival and CR rate when compared to CHOP plus rituximab as first-line treatment of patients with advanced follicular, indolent, and mantle cell lymphomas: final results of a randomized phase III study of the StiL (Study Group Indolent Lymphomas, Germany). Blood 2009; 114: 405a. 18. Morschhauser F., Dreyling M., Rohatiner A., Hagemeister F., Bischof Delaloye A. Rationale for consolidation to improve progression-free survival in patients with non-hodgkin s lymphoma: A review of the evidence. Oncologist 2009; 14 (supl. 2): Hiddemann W., Kneba M., Dreyling M. i wsp. Frontline therapy with rituximab added to the combination of cyclophosphamide, doxorubicin, vincristine, and prednisone (CHOP) significantly improves the outcome for patients with advanced-stage follicular lymphoma compared with therapy with CHOP alone: results of a prospective randomized study of the German Low-Grade Lymphoma Study Group. Blood 2005; 106: Rohatiner A.Z.S., Gregory W.M., Peterson B. i wsp. Meta-analysis to evaluate the role of interferon in follicular lymphoma. J. Clin. Oncol. 2005; 23: Van Oers M.H.J., Van Glabbeke M., Giurgea L. i wsp. Rituximab maintenance of relapsed/resistant follicular non-hodgkin lymphoma: a long term outcome of the EORTC phase III randomized intergroup study. Blood 2010; 28: Vidal L., Gafter-Gvili A., Leibovici L. i wsp. Rituximab maintenance for the treatment of patients with follicular lymphoma: systematic review and meta-analysis of randomized trials. J. Natl. Cancer Inst. 2009; 101: Dawidowska A., Deptała A. Radioimmunoterapia w leczeniu konsolidującym wybranych postaci chłoniaków niehodgkinowskich. Bayer Schering Pharma 2010; 1: Lehnert M., Ludwig H., Zojer N. Update on the rational use of 90Y-ibrytumomab tiuxetan in the treatment of follicular lymphoma. Onco. Targets Ther. 2009; 2: Morschhauser F., Radford J., Van Hoof A. i wsp. Phase III trial of consolidation therapy with yttrium-90-ibrytumomab tiuxetan compared with no additional therapy after first remission in advanced follicular lymphoma. J. Clin. Oncol. 2008; 26: Goff L., Summers K., Iqbal S. i wsp. Quantitative PCR analysis for Bcl-2/IgH in phase II Study of 90Y ibrytumomab tiuxetan as consolidation of first remission in patient with follicular lymphoma. J. Clin. Oncol. 2009; 27: Friedberg J.W., Taylor M.D., Cerhan J.R i wsp. Follicular lymphoma in the United States: first report of the National Lympho- -Care Study. J. Clin. Oncol. 2009; 27: Czuczman S., Viardot A., Hess G. i wsp. Ofatumumab in combination with CHOP (O-CHOP) achieves high response rate in previously untreated follicular lymphoma (FL) patients with high-risk score Tageja N., Padheye S., Dandawate P. i wsp. New targets for the treatment of follicular lymphoma. J. Hematol. Oncol. 2009; 2:
MabThera. w leczeniu podtrzymującym chorych na chłoniaka grudkowego. Dr hab. med. Maciej Machaczka, Prof. UR
 MabThera w leczeniu podtrzymującym chorych na chłoniaka grudkowego Dr hab. med. Maciej Machaczka, Prof. UR Senior Consultant and Research Scientist Hematology Center Karolinska and Karolinska Institutet
MabThera w leczeniu podtrzymującym chorych na chłoniaka grudkowego Dr hab. med. Maciej Machaczka, Prof. UR Senior Consultant and Research Scientist Hematology Center Karolinska and Karolinska Institutet
NON-HODGKIN S LYMPHOMA
 NON-HODGKIN S LYMPHOMA Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku We Wrocławiu Aleksandra Bogucka-Fedorczuk DEFINICJA Chłoniaki Non-Hodgkin (NHL) to heterogeniczna grupa nowotworów charakteryzująca
NON-HODGKIN S LYMPHOMA Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku We Wrocławiu Aleksandra Bogucka-Fedorczuk DEFINICJA Chłoniaki Non-Hodgkin (NHL) to heterogeniczna grupa nowotworów charakteryzująca
Chłoniak grudkowy. Definicja. Epidemiologia. Etiopatogeneza. Ewa Lech-Marańda
 Ewa Lech-Marańda Definicja Zgodnie z klasyfikacją Światowej Organizacji Zdrowia (WHO, World Health Organization) z 2008 roku chłoniak grudkowy (FL, follicular lymphoma) jest nowotworem wywodzącym się z
Ewa Lech-Marańda Definicja Zgodnie z klasyfikacją Światowej Organizacji Zdrowia (WHO, World Health Organization) z 2008 roku chłoniak grudkowy (FL, follicular lymphoma) jest nowotworem wywodzącym się z
Rak piersi. Doniesienia roku Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie
 Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Ocena immunologiczna i genetyczna białaczkowych komórek macierzystych
 Karolina Klara Radomska Ocena immunologiczna i genetyczna białaczkowych komórek macierzystych Streszczenie Wstęp Ostre białaczki szpikowe (Acute Myeloid Leukemia, AML) to grupa nowotworów mieloidalnych,
Karolina Klara Radomska Ocena immunologiczna i genetyczna białaczkowych komórek macierzystych Streszczenie Wstęp Ostre białaczki szpikowe (Acute Myeloid Leukemia, AML) to grupa nowotworów mieloidalnych,
Warszawa, 16-17.03.201217.03.2012 PLRG / PALG 16-17.03.2012
 Przegląd badań klinicznych PLRG Konferencja PLRG i PALG Warszawa, 16-17.03.201217.03.2012 Janusz Szczepanik CRO Quantum Satis 1 Badania kliniczne PLRG PLRG R-CVP/CHOP (PLRG4) HOVON 68 CLL Watch and Wait
Przegląd badań klinicznych PLRG Konferencja PLRG i PALG Warszawa, 16-17.03.201217.03.2012 Janusz Szczepanik CRO Quantum Satis 1 Badania kliniczne PLRG PLRG R-CVP/CHOP (PLRG4) HOVON 68 CLL Watch and Wait
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 171/2014 z dnia 7 lipca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego obejmującego
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 171/2014 z dnia 7 lipca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego obejmującego
Piotr Potemski. Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi
 Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
Piotr Potemski Uniwersytet Medyczny w Łodzi, Szpital im. M. Kopernika w Łodzi VI Letnia Akademia Onkologiczna dla Dziennikarzy, Warszawa, 10-12.08.2016 1 Obserwowane są samoistne regresje zmian przerzutowych
Leczenie podtrzymujące u chorych na chłoniaka grudkowego
 PRACA PRZEGLĄDOWA Piotr Smolewski 1, Tadeusz Robak 2 1 Zakład Hematologii Doświadczalnej Uniwersytetu Medycznego w Łodzi 2 Klinika Hematologii Uniwersytetu Medycznego w Łodzi Leczenie podtrzymujące u chorych
PRACA PRZEGLĄDOWA Piotr Smolewski 1, Tadeusz Robak 2 1 Zakład Hematologii Doświadczalnej Uniwersytetu Medycznego w Łodzi 2 Klinika Hematologii Uniwersytetu Medycznego w Łodzi Leczenie podtrzymujące u chorych
S T R E S Z C Z E N I E
 STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
Leczenie podtrzymujące rytuksymabem u chorych na chłoniaka grudkowego w pierwszej i kolejnych remisjach choroby
 PRACA POGLĄDOWA Hematologia 2012, tom 3, nr 4, 343 354 Copyright 2012 Via Medica ISSN 2081 0768 Leczenie podtrzymujące rytuksymabem u chorych na chłoniaka grudkowego w pierwszej i kolejnych remisjach choroby
PRACA POGLĄDOWA Hematologia 2012, tom 3, nr 4, 343 354 Copyright 2012 Via Medica ISSN 2081 0768 Leczenie podtrzymujące rytuksymabem u chorych na chłoniaka grudkowego w pierwszej i kolejnych remisjach choroby
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym?
 Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
Wydłużenie życia chorych z rakiem płuca - nowe możliwości
 Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Wydłużenie życia chorych z rakiem płuca - nowe możliwości Pulmonologia 2015, PAP, Warszawa, 26 maja 2015 1 Epidemiologia raka płuca w Polsce Pierwszy nowotwór w Polsce pod względem umieralności. Tendencja
Rola rituksymabu w leczeniu chorych na chłoniaki grudkowe
 P R A C A P R Z E G L Ą D O W A Wojciech Jurczak 1, Jan Walewski 2 1 Collegium Medicum Uniwersytetu Jagiellońskiego w Krakowie 2 Centrum Onkologii Instytut im. Marii Skłodowskiej-Curie w Warszawie Rola
P R A C A P R Z E G L Ą D O W A Wojciech Jurczak 1, Jan Walewski 2 1 Collegium Medicum Uniwersytetu Jagiellońskiego w Krakowie 2 Centrum Onkologii Instytut im. Marii Skłodowskiej-Curie w Warszawie Rola
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego. Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa
 Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Personalizacja leczenia w hematoonkologii dziecięcej
 MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
c) poprawa jakości życia chorych z nieziarniczym chłoniakiem typu grudkowego w III i IV stopniu
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 9 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011r. LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 9 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011r. LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
c) poprawa jakości życia chorych z nieziarniczym chłoniakiem typu grudkowego w III i IV stopniu
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2009 Załącznik nr 10 do zarządzenia Nr 98/2008/DGL Prezesa NFZ z dnia 27 października 2008 roku LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Nazwa programu: Terapeutyczne Programy Zdrowotne 2009 Załącznik nr 10 do zarządzenia Nr 98/2008/DGL Prezesa NFZ z dnia 27 października 2008 roku LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Międzynarodowe standardy leczenia szpiczaka plazmocytowego w roku 2014
 Międzynarodowe standardy leczenia szpiczaka plazmocytowego w roku 2014 Wiesław Wiktor Jędrzejczak, Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawskiego Uniwersytetu Medycznego Tak
Międzynarodowe standardy leczenia szpiczaka plazmocytowego w roku 2014 Wiesław Wiktor Jędrzejczak, Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawskiego Uniwersytetu Medycznego Tak
c) poprawa jakości życia chorych z nieziarniczym chłoniakiem typu grudkowego w III i IV stopniu
 załącznik nr 10 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chloniak grudkowy C 83 chłoniaki nieziarniczy rozlane Dziedzina
załącznik nr 10 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chloniak grudkowy C 83 chłoniaki nieziarniczy rozlane Dziedzina
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 9/2012 z dnia 27 lutego 2012 w zakresie zmiany sposobu finansowania świadczenia gwarantowanego Leczenie chłoniaków
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 9/2012 z dnia 27 lutego 2012 w zakresie zmiany sposobu finansowania świadczenia gwarantowanego Leczenie chłoniaków
POSTĘPY W LECZENIU PBL
 POSTĘPY W LECZENIU PBL Klinika Chorób Wewnętrznych i Hematologii Wojskowy Instytut Medyczny Prof. dr hab. med. Piotr Rzepecki Terapia przełomowa Pojęcie terapii przełomowych w hematoonkologii zostało wprowadzone
POSTĘPY W LECZENIU PBL Klinika Chorób Wewnętrznych i Hematologii Wojskowy Instytut Medyczny Prof. dr hab. med. Piotr Rzepecki Terapia przełomowa Pojęcie terapii przełomowych w hematoonkologii zostało wprowadzone
Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych
 Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych Jadwiga Dwilewicz-Trojaczek Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa
Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych Jadwiga Dwilewicz-Trojaczek Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa
Nowe możliwości leczenia ostrej białaczki limfoblastycznej
 Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Przykłady opóźnień w rozpoznaniu chorób nowotworowych u dzieci i młodzieży Analiza przyczyn i konsekwencji
 PROGRAM POPRAWY WCZESNEGO WYKRYWANIA I DIAGNOZOWANIA NOWOTWORÓW U DZIECI W PIĘCIU WOJEWÓDZTWACH POLSKI Przykłady opóźnień w rozpoznaniu chorób nowotworowych u dzieci i młodzieży Analiza przyczyn i konsekwencji
PROGRAM POPRAWY WCZESNEGO WYKRYWANIA I DIAGNOZOWANIA NOWOTWORÓW U DZIECI W PIĘCIU WOJEWÓDZTWACH POLSKI Przykłady opóźnień w rozpoznaniu chorób nowotworowych u dzieci i młodzieży Analiza przyczyn i konsekwencji
CHŁONIAKI ZŁOŚLIWE U DZIECI
 Prof. dr hab.med. Jacek Wachowiak CHŁONIAKI ZŁOŚLIWE PODZIAŁ CHŁONIAKI ZŁOŚLIWE 1. CHŁONIAKI NIEZIARNICZE 2. CHOROBA HODGKINA (ZIARNICA ZŁOŚLIWA) EPIDEMIOLOGIA - OK. 10% NOWOTWORÓW Klinika Onkologii, Hematologii
Prof. dr hab.med. Jacek Wachowiak CHŁONIAKI ZŁOŚLIWE PODZIAŁ CHŁONIAKI ZŁOŚLIWE 1. CHŁONIAKI NIEZIARNICZE 2. CHOROBA HODGKINA (ZIARNICA ZŁOŚLIWA) EPIDEMIOLOGIA - OK. 10% NOWOTWORÓW Klinika Onkologii, Hematologii
Przewlekła białaczka limfocytowa
 Przewlekła białaczka limfocytowa Ewa Lech-Marańda Klinika Hematologii Instytutu Hematologii i Transfuzjologii Klinika Hematologii i Transfuzjologii CMKP Przewlekła białaczka limfocytowa (CLL) Początek
Przewlekła białaczka limfocytowa Ewa Lech-Marańda Klinika Hematologii Instytutu Hematologii i Transfuzjologii Klinika Hematologii i Transfuzjologii CMKP Przewlekła białaczka limfocytowa (CLL) Początek
Typ histopatologiczny
 Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Typ histopatologiczny Wiek Stopieo zróżnicowania nowotworu Typ I (hormonozależny) Adenocarcinoma Adenoacanthoma Naciekanie przestrzeni naczyniowych Wielkośd guza Typ II (hormononiezależny) Serous papillary
Białaczka limfatyczna
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
Polskie doświadczenia kliniczne z bendamustyną
 Polskie doświadczenia kliniczne z bendamustyną Iwona Hus Klinika Hematoonkologii i Transplantacji Szpiku UM w Lublinie XXIII Zjazd PTHiT Wrocław 2009 Bendamustyna w leczeniu PBL monoterapia Efficacy of
Polskie doświadczenia kliniczne z bendamustyną Iwona Hus Klinika Hematoonkologii i Transplantacji Szpiku UM w Lublinie XXIII Zjazd PTHiT Wrocław 2009 Bendamustyna w leczeniu PBL monoterapia Efficacy of
LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0)
 Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
Ocena czynników rokowniczych w raku płaskonabłonkowym przełyku w materiale Kliniki Chirurgii Onkologicznej AM w Gdańsku doniesienie wstępne
 Ocena czynników rokowniczych w raku płaskonabłonkowym przełyku w materiale Kliniki Chirurgii Onkologicznej AM w Gdańsku doniesienie wstępne Świerblewski M. 1, Kopacz A. 1, Jastrzębski T. 1 1 Katedra i
Ocena czynników rokowniczych w raku płaskonabłonkowym przełyku w materiale Kliniki Chirurgii Onkologicznej AM w Gdańsku doniesienie wstępne Świerblewski M. 1, Kopacz A. 1, Jastrzębski T. 1 1 Katedra i
Raport etapowy 28.02.2007 20.05.2008. Protokół w. 3.5; 17/05/2007
 Immunochemioterapia R-CVP lub R-CHOP w indukcji remisji chłoniaków przewlekłych oraz rituximab w leczeniu podtrzymującym Wieloośrodkowe, randomizowane badanie kliniczne Polskiej Grupy Badawczej Chłoniaków
Immunochemioterapia R-CVP lub R-CHOP w indukcji remisji chłoniaków przewlekłych oraz rituximab w leczeniu podtrzymującym Wieloośrodkowe, randomizowane badanie kliniczne Polskiej Grupy Badawczej Chłoniaków
Efektywna kontrola chorych po leczeniu nowotworów jąder
 Efektywna kontrola chorych po leczeniu nowotworów jąder Marzena Wełnicka-Jaśkiewicz Klinika Onkologii i Radioterapii Gdańskiego Uniwersytetu Medycznego Efektywna kontrola ścisła obserwacja po leczeniu
Efektywna kontrola chorych po leczeniu nowotworów jąder Marzena Wełnicka-Jaśkiewicz Klinika Onkologii i Radioterapii Gdańskiego Uniwersytetu Medycznego Efektywna kontrola ścisła obserwacja po leczeniu
Zespoły mielodysplastyczne
 Zespoły mielodysplastyczne J A D W I G A D W I L E W I C Z - T R O J A C Z E K K L I N I K A H E M ATO LO G I I, O N KO LO G I I I C H O R Ó B W E W N Ę T R Z N YC H WA R S Z AW S K I U N I W E R S Y T
Zespoły mielodysplastyczne J A D W I G A D W I L E W I C Z - T R O J A C Z E K K L I N I K A H E M ATO LO G I I, O N KO LO G I I I C H O R Ó B W E W N Ę T R Z N YC H WA R S Z AW S K I U N I W E R S Y T
Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną. Klinika Onkologii i Radioterapii
 Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną chemioterapię z udziałem cisplatyny? Jacek Jassem Klinika Onkologii i Radioterapii Gdańskiego ń Uniwersytetu t Medycznego Jaka jest siła
Czy chore na raka piersi z mutacją BRCA powinny otrzymywać wstępną chemioterapię z udziałem cisplatyny? Jacek Jassem Klinika Onkologii i Radioterapii Gdańskiego ń Uniwersytetu t Medycznego Jaka jest siła
Profilaktyka i leczenie czerniaka. Dr n. med. Jacek Calik
 Profilaktyka i leczenie czerniaka Dr n. med. Jacek Calik Czerniaki Czerniaki są grupą nowotworów o bardzo zróżnicowanej biologii, przebiegu i rokowaniu. Nowotwory wywodzące się z melanocytów. Pochodzenie
Profilaktyka i leczenie czerniaka Dr n. med. Jacek Calik Czerniaki Czerniaki są grupą nowotworów o bardzo zróżnicowanej biologii, przebiegu i rokowaniu. Nowotwory wywodzące się z melanocytów. Pochodzenie
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Rak pęcherza moczowego - chemioterapia jako element leczenia skojarzonego
 Rak pęcherza moczowego - chemioterapia jako element leczenia skojarzonego Elżbieta Senkus-Konefka Klinika Onkologii i Radioterapii Gdański Uniwersytet Medyczny Kliknij ikonę, aby dodać obraz 888 cystektomii
Rak pęcherza moczowego - chemioterapia jako element leczenia skojarzonego Elżbieta Senkus-Konefka Klinika Onkologii i Radioterapii Gdański Uniwersytet Medyczny Kliknij ikonę, aby dodać obraz 888 cystektomii
Leczenie podtrzymujące w przewlekłych chłoniakach niehodgkinowskich
 PRACA POGLĄDOWA Review Article Acta Haematologica Polonica 2009, 40, Nr 2, str. 159 167 ANDRZEJ DEPTAŁA 1,2, GRAśYNA PAŁYNYCZKO 1 Leczenie podtrzymujące w przewlekłych chłoniakach niehodgkinowskich Maintenance
PRACA POGLĄDOWA Review Article Acta Haematologica Polonica 2009, 40, Nr 2, str. 159 167 ANDRZEJ DEPTAŁA 1,2, GRAśYNA PAŁYNYCZKO 1 Leczenie podtrzymujące w przewlekłych chłoniakach niehodgkinowskich Maintenance
Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008.
 załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
Chłoniak z komórek płaszcza optymalne podejście do leczenia w świetle wyników badań klinicznych
 P R A C A P R Z E G L Ą D O W A Wojciech Jurczak 1, Jan Walewski 2 1 Collegium Medicum Uniwersytet Jagielloński w Krakowie 2 Centrum Onkologii Instytut im. Marii Skłodowskiej-Curie w Warszawie Chłoniak
P R A C A P R Z E G L Ą D O W A Wojciech Jurczak 1, Jan Walewski 2 1 Collegium Medicum Uniwersytet Jagielloński w Krakowie 2 Centrum Onkologii Instytut im. Marii Skłodowskiej-Curie w Warszawie Chłoniak
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20)
 Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
Dziennik Urzędowy Ministra Zdrowia 511 Poz. 42 Załącznik B.4. LECZENIE ZAAWANSOWANEGO RAKA JELITA GRUBEGO (ICD-10 C 18 C 20) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie zaawansowanego
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 20/2014 z dnia 20 stycznia 2014 r. w sprawie usunięcia świadczenia obejmującego podawanie winorelbiny w rozpoznaniach
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 20/2014 z dnia 20 stycznia 2014 r. w sprawie usunięcia świadczenia obejmującego podawanie winorelbiny w rozpoznaniach
Leczenie systemowe raka nie-jasnokomórkowego
 Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Bendamustyna w leczeniu opornych postaci szpiczaka mnogiego
 Bendamustyna w leczeniu opornych postaci szpiczaka mnogiego Iwona Hus, Joanna Mańko Klinika Hematonkologii i Transplantacji Szpiku Uniwersytetu Medycznego w Lublinie Nałęczów 22 listopada 2008 Bendamustyna
Bendamustyna w leczeniu opornych postaci szpiczaka mnogiego Iwona Hus, Joanna Mańko Klinika Hematonkologii i Transplantacji Szpiku Uniwersytetu Medycznego w Lublinie Nałęczów 22 listopada 2008 Bendamustyna
Cel programu: 1. wydłużenie czasu przeżycia chorych na szpiczaka mnogiego ( plazmocytowego), 2. uzyskanie remisji choroby, 3. poprawa jakości życia.
 Nazwa programu LECZENIE OPORNYCH POSTACI SZPICZAKA MNOGIEGO (PLAZMOCYTOWEGO) ICD 10 C 90.0 szpiczak mnogi Dziedzina medycyny: hematologia. Cel programu: 1. wydłużenie czasu przeżycia chorych na szpiczaka
Nazwa programu LECZENIE OPORNYCH POSTACI SZPICZAKA MNOGIEGO (PLAZMOCYTOWEGO) ICD 10 C 90.0 szpiczak mnogi Dziedzina medycyny: hematologia. Cel programu: 1. wydłużenie czasu przeżycia chorych na szpiczaka
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Konsultacyjna Stanowisko Rady Konsultacyjnej nr 40/2011 z dnia 23 maja 2011 r. w zakresie usunięcia z wykazu świadczeo gwarantowanych świadczenia opieki zdrowotnej
Agencja Oceny Technologii Medycznych Rada Konsultacyjna Stanowisko Rady Konsultacyjnej nr 40/2011 z dnia 23 maja 2011 r. w zakresie usunięcia z wykazu świadczeo gwarantowanych świadczenia opieki zdrowotnej
Znaczenie PFS oraz OS w analizach klinicznych w onkologii
 Znaczenie PFS oraz OS w analizach klinicznych w onkologii experience makes the difference Magdalena Władysiuk, lek. med., MBA Cel terapii w onkologii/hematologii Kontrola rozwoju choroby Kontrola objawów
Znaczenie PFS oraz OS w analizach klinicznych w onkologii experience makes the difference Magdalena Władysiuk, lek. med., MBA Cel terapii w onkologii/hematologii Kontrola rozwoju choroby Kontrola objawów
Rysunek. Układ limfatyczny.
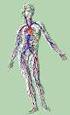 Informacja dotyczy chłoniaka grudkowego, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu odpornościowego
Informacja dotyczy chłoniaka grudkowego, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu odpornościowego
ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH
 ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH 1 Państwo Członkowskie UE/EOG Austria Belgia Dania Finlandia Francja Irlandia
ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH 1 Państwo Członkowskie UE/EOG Austria Belgia Dania Finlandia Francja Irlandia
Wnioski o objęcie refundacją leków MabThera (rytuksymab)
 Agencja Oceny Technologii Medycznych Wydział Oceny Technologii Medycznych Wnioski o objęcie refundacją leków MabThera (rytuksymab) Analiza weryfikacyjna Nr: AOTM-OT-4351-2/2014 Data ukończenia: 10 kwietnia
Agencja Oceny Technologii Medycznych Wydział Oceny Technologii Medycznych Wnioski o objęcie refundacją leków MabThera (rytuksymab) Analiza weryfikacyjna Nr: AOTM-OT-4351-2/2014 Data ukończenia: 10 kwietnia
EBM w farmakoterapii
 EBM w farmakoterapii Dr Przemysław Niewiński Katedra i Zakład Farmakologii Klinicznej AM we Wrocławiu Katedra i Zakład Farmakologii Klinicznej AM Wrocław EBM Evidence Based Medicine (EBM) "praktyka medyczna
EBM w farmakoterapii Dr Przemysław Niewiński Katedra i Zakład Farmakologii Klinicznej AM we Wrocławiu Katedra i Zakład Farmakologii Klinicznej AM Wrocław EBM Evidence Based Medicine (EBM) "praktyka medyczna
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 33/2012 z dnia 18 czerwca 2012 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych albo zmiany jego poziomu
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 33/2012 z dnia 18 czerwca 2012 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych albo zmiany jego poziomu
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Załącznik nr 11 do Zarządzenia Nr 41/2009 Prezesa NFZ z dnia 15 września 2009 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4, D80.5,
Chłoniak z komórek płaszcza
 Chłoniak z komórek płaszcza Jan Walewski Definicja Aktualna klasyfikacja Światowej Organizacji Zdrowia (WHO, World Health Organization) z 2008 roku definiuje chłoniaka z komórek płaszcza (MCL, mantle cell
Chłoniak z komórek płaszcza Jan Walewski Definicja Aktualna klasyfikacja Światowej Organizacji Zdrowia (WHO, World Health Organization) z 2008 roku definiuje chłoniaka z komórek płaszcza (MCL, mantle cell
Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI
 Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
Załącznik nr 12 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku Nazwa programu: LECZENIE PIERWOTNYCH NIEDOBORÓW ODPORNOŚCI U DZIECI ICD 10 D80 w tym D80.0, D80.1, D80.3, D80.4,
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Rysunek. Układ limfatyczny.
 Poniższa informacja dotyczy rodzaju chłoniaka nieziarniczego, zwanego chłoniakiem anaplastycznym z dużych komórek. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest
Poniższa informacja dotyczy rodzaju chłoniaka nieziarniczego, zwanego chłoniakiem anaplastycznym z dużych komórek. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest
Terapeutyczne Programy Zdrowotne 2012 Leczenie glejaków mózgu Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r.
 Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
Dr n. med. Norbert Grząśko w imieniu Polskiej Grupy Szpiczakowej Lublin, 12.04.2008
 Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI. Maria Litwiniuk Warszawa 28 maja 2019
 LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI Maria Litwiniuk Warszawa 28 maja 2019 Konflikt interesów Wykłady sponsorowane dla firm: Teva, AstraZeneca, Pfizer, Roche Sponorowanie
LECZENIE KOBIET Z ROZSIANYM, HORMONOZALEŻNYM, HER2 UJEMNYM RAKIEM PIERSI Maria Litwiniuk Warszawa 28 maja 2019 Konflikt interesów Wykłady sponsorowane dla firm: Teva, AstraZeneca, Pfizer, Roche Sponorowanie
Radioterapia w leczeniu raka pęcherza moczowego - zalecenia
 Radioterapia w leczeniu raka pęcherza moczowego - zalecenia Radioterapia w leczeniu raka pęcherza moczowego może być stosowana łącznie z leczeniem operacyjnym chemioterapią. Na podstawie literatury anglojęzycznej
Radioterapia w leczeniu raka pęcherza moczowego - zalecenia Radioterapia w leczeniu raka pęcherza moczowego może być stosowana łącznie z leczeniem operacyjnym chemioterapią. Na podstawie literatury anglojęzycznej
Radioterapia stereotaktyczna. Rafal Dziadziuszko Gdański Uniwersytet Medyczny
 Radioterapia stereotaktyczna przerzutów do OUN Rafal Dziadziuszko Gdański Uniwersytet Medyczny Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do
Radioterapia stereotaktyczna przerzutów do OUN Rafal Dziadziuszko Gdański Uniwersytet Medyczny Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do RT stereotaktycznej - nóż gamma Urządzenia do
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r.
 Dziennik Ustaw Nr 269 15678 Poz. 1593 1593 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie
Dziennik Ustaw Nr 269 15678 Poz. 1593 1593 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 grudnia 2011 r. zmieniające rozporządzenie w sprawie świadczeń gwarantowanych z zakresu programów zdrowotnych Na podstawie
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Rak jajnika. Prof. Mariusz Bidziński. Klinika Ginekologii Onkologicznej
 Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
Rak jajnika Prof. Mariusz Bidziński Klinika Ginekologii Onkologicznej Współpraca z firmami: Roche, Astra Zeneca, MSD, Olympus Mutacje w genach BRCA1 i BRCA2 Materiały edukacyjne Astra Zeneca Mutacje w
Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego.
 Chłoniak z komórek płaszcza Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego,
Chłoniak z komórek płaszcza Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego,
Lublin, 26 maja, 2015 roku
 Lublin, 26 maja, 2015 roku Recenzja pracy doktorskiej lek. Iwony Kubickiej- Mendak pt. Ocena przyczyn niepowodzenia leczenia i ryzyka późnych powikłań brachyterapii LDR i HDR chorych na raka szyjki macicy
Lublin, 26 maja, 2015 roku Recenzja pracy doktorskiej lek. Iwony Kubickiej- Mendak pt. Ocena przyczyn niepowodzenia leczenia i ryzyka późnych powikłań brachyterapii LDR i HDR chorych na raka szyjki macicy
Jarosław B. Ćwikła. Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie
 Nowe algorytmy oceny odpowiedzi na leczenie w badaniach strukturalnych, dużo dalej niż klasyczne kryteria RECIST Jarosław B. Ćwikła Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie Radiologiczna
Nowe algorytmy oceny odpowiedzi na leczenie w badaniach strukturalnych, dużo dalej niż klasyczne kryteria RECIST Jarosław B. Ćwikła Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie Radiologiczna
LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48)
 Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Dziennik Urzędowy Ministra Zdrowia 492 Poz. 66 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48)
 Dziennik Urzędowy Ministra Zdrowia 546 Poz. 71 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Dziennik Urzędowy Ministra Zdrowia 546 Poz. 71 Załącznik B.3. LECZENIE NOWOTWORÓW PODŚCIELISKA PRZEWODU POKARMOWEGO (GIST) (ICD-10 C 15, C 16, C 17, C 18, C 20, C 48) ŚWIADCZENIOBIORCY 1. Leczenie adjuwantowe
Nowotwór złośliwy oskrzela i płuca
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy oskrzela i płuca Bevacizumab Bewacyzumab w skojarzeniu z chemioterapią opartą na pochodnych platyny jest wskazany w leczeniu pierwszego
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Nowotwór złośliwy oskrzela i płuca Bevacizumab Bewacyzumab w skojarzeniu z chemioterapią opartą na pochodnych platyny jest wskazany w leczeniu pierwszego
ALLOPRZESZCZEPIENIE KRWIOTWÓRCZYCH KOMÓREK MACIERZYSTYCH w PRZEWLEKŁEJ BIAŁACZCE LIMFOCYTOWEJ w POLSCE ANKIETA WIELOOŚRODKOWA
 ALLOPRZESZCZEPIENIE KRWIOTWÓRCZYCH KOMÓREK MACIERZYSTYCH w PRZEWLEKŁEJ BIAŁACZCE LIMFOCYTOWEJ w POLSCE ANKIETA WIELOOŚRODKOWA Ośrodek koordynujący: Śląskiego Uniwersytetu Medycznego w Katowicach Kierownik
ALLOPRZESZCZEPIENIE KRWIOTWÓRCZYCH KOMÓREK MACIERZYSTYCH w PRZEWLEKŁEJ BIAŁACZCE LIMFOCYTOWEJ w POLSCE ANKIETA WIELOOŚRODKOWA Ośrodek koordynujący: Śląskiego Uniwersytetu Medycznego w Katowicach Kierownik
Komunikat prasowy. Dodatkowe informacje
 Dane na temat czasu przeżycia całkowitego uzyskane w badaniu LUX-Lung 7 bezpośrednio porównującym leki afatynib i gefitynib, przedstawione na ESMO 2016 W badaniu LUX-Lung 7 zaobserwowano mniejsze ryzyko
Dane na temat czasu przeżycia całkowitego uzyskane w badaniu LUX-Lung 7 bezpośrednio porównującym leki afatynib i gefitynib, przedstawione na ESMO 2016 W badaniu LUX-Lung 7 zaobserwowano mniejsze ryzyko
Rysunek. Układ Limfatyczny.
 Informacja dotyczy chłoniaka rozlanego z dużych komórek B, będącego odmianą chłoniaka nieziarniczego. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest częścią systemu
Informacja dotyczy chłoniaka rozlanego z dużych komórek B, będącego odmianą chłoniaka nieziarniczego. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest częścią systemu
Terapeutyczne Programy Zdrowotne 2009 Leczenie opornych postaci szpiczaka mnogiego (plazmocytowego)
 Załącznik nr 28 do zarządzenia Nr 98/2008/DGL Prezesa NFZ z dnia 27 października 2008 roku Nazwa programu: LECZENIE OPORNYCH POSTACI SZPICZAKA MNOGIEGO (PLAZMOCYTOWEGO) ICD-10 C 90.0 szpiczak mnogi Dziedzina
Załącznik nr 28 do zarządzenia Nr 98/2008/DGL Prezesa NFZ z dnia 27 października 2008 roku Nazwa programu: LECZENIE OPORNYCH POSTACI SZPICZAKA MNOGIEGO (PLAZMOCYTOWEGO) ICD-10 C 90.0 szpiczak mnogi Dziedzina
Szpiczak plazmocytowy. Grzegorz Helbig Klinika Hematologii i Transplantacji Szpiku Śląski Uniwersytet Medyczny w Katowicach
 Szpiczak plazmocytowy Grzegorz Helbig Klinika Hematologii i Transplantacji Szpiku Śląski Uniwersytet Medyczny w Katowicach MM - epidemiologia 90% przypadków rozpoznaje się powyżej 50 r.ż., Mediana wieku
Szpiczak plazmocytowy Grzegorz Helbig Klinika Hematologii i Transplantacji Szpiku Śląski Uniwersytet Medyczny w Katowicach MM - epidemiologia 90% przypadków rozpoznaje się powyżej 50 r.ż., Mediana wieku
ostrym reumatoidalnym zapaleniem stawów (choroba powodująca stan zapalny stawów), gdzie produkt MabThera podaje się dożylnie z metotreksatem;
 EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/614203/2010 EMEA/H/C/000165 Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
ZBYT PÓŹNE WYKRYWANIE RAKA NERKI ROLA LEKARZA PIERWSZEGO KONTAKTU
 ZBYT PÓŹNE WYKRYWANIE RAKA NERKI ROLA LEKARZA PIERWSZEGO KONTAKTU 14 czerwca 2012 r dr n. med. Piotr Tomczak Klinika Onkologii U.M. Poznań Epidemiologia raka nerki RCC stanowi 2 3% nowotworów złośliwych
ZBYT PÓŹNE WYKRYWANIE RAKA NERKI ROLA LEKARZA PIERWSZEGO KONTAKTU 14 czerwca 2012 r dr n. med. Piotr Tomczak Klinika Onkologii U.M. Poznań Epidemiologia raka nerki RCC stanowi 2 3% nowotworów złośliwych
WCZESNE OBJAWY CHOROBY NOWOTWOROWEJ U DZIECI
 WCZESNE OBJAWY CHOROBY NOWOTWOROWEJ U DZIECI Elżbieta Adamkiewicz-Drożyńska Katedra i Klinika Pediatrii, Hematologii i Onkologii Początki choroby nowotworowej u dzieci Kumulacja wielu zmian genetycznych
WCZESNE OBJAWY CHOROBY NOWOTWOROWEJ U DZIECI Elżbieta Adamkiewicz-Drożyńska Katedra i Klinika Pediatrii, Hematologii i Onkologii Początki choroby nowotworowej u dzieci Kumulacja wielu zmian genetycznych
Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce
 Warszawa, 27.01.2016 Seminarium naukowe: Terapie przełomowe w onkologii i hematoonkologii a dostępność do leczenia w Polsce na tle Europy Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce Dr n.
Warszawa, 27.01.2016 Seminarium naukowe: Terapie przełomowe w onkologii i hematoonkologii a dostępność do leczenia w Polsce na tle Europy Terapie dla kobiet z zaawansowanym rakiem piersi w Polsce Dr n.
chorych na ITP Krzysztof Chojnowski Warszawa, 27 listopada 2009 r.
 Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Terapeutyczne Programy Zdrowotne 2010 Leczenie raka nerki Załącznik nr 42 do zarządzenia Nr 8/2010/DGL Prezesa NFZ z dnia 20 stycznia 2010 roku
 Załącznik nr 42 do zarządzenia Nr 8/2010/DGL Prezesa NFZ z dnia 20 stycznia 2010 roku Nazwa programu: LECZENIE RAKA NERKI ICD-10 C 64 Dziedzina medycyny: Nowotwór złośliwy nerki za wyjątkiem miedniczki
Załącznik nr 42 do zarządzenia Nr 8/2010/DGL Prezesa NFZ z dnia 20 stycznia 2010 roku Nazwa programu: LECZENIE RAKA NERKI ICD-10 C 64 Dziedzina medycyny: Nowotwór złośliwy nerki za wyjątkiem miedniczki
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
Rysunek. Układ limfatyczny.
 Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
Ulotka dołączona do opakowania: informacja dla użytkownika. Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Aneks. Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków
 Aneks Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Produkt leczniczy Folotyn roztwór
Aneks Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Produkt leczniczy Folotyn roztwór
Skuteczność schematu bendamustyna i rytuksymab w leczeniu nawrotowej postaci przewlekłej białaczki limfocytowej
 OPIS PRZYPADKU Hematologia 2010, tom 1, nr 4, 359 363 Copyright 2010 Via Medica ISSN 2081 0768 Skuteczność schematu bendamustyna i rytuksymab w leczeniu nawrotowej postaci przewlekłej białaczki limfocytowej
OPIS PRZYPADKU Hematologia 2010, tom 1, nr 4, 359 363 Copyright 2010 Via Medica ISSN 2081 0768 Skuteczność schematu bendamustyna i rytuksymab w leczeniu nawrotowej postaci przewlekłej białaczki limfocytowej
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
Raport Biała Księga PBL
 Raport Biała Księga PBL 01 agenda 01 Informacje o raporcie 02 Fakty o chorobie 03 Sylwetka pacjenta 04 Standardy leczenia i diagnostyka 05 Wyzwania w opiece nad chorymi w Polsce 06 Wnioski 02 Informacje
Raport Biała Księga PBL 01 agenda 01 Informacje o raporcie 02 Fakty o chorobie 03 Sylwetka pacjenta 04 Standardy leczenia i diagnostyka 05 Wyzwania w opiece nad chorymi w Polsce 06 Wnioski 02 Informacje
Terapeutyczne Programy Zdrowotne 2012 Leczenie opornych postaci szpiczaka mnogiego (plazmocytowego)
 Załącznik nr 25 do zarządzenia 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE OPORNYCH POSTACI SZPICZAKA MNOGIEGO (PLAZMOCYTOWEGO) ICD-10 C 90.0 szpiczak mnogi Dziedzina
Załącznik nr 25 do zarządzenia 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE OPORNYCH POSTACI SZPICZAKA MNOGIEGO (PLAZMOCYTOWEGO) ICD-10 C 90.0 szpiczak mnogi Dziedzina
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków
 Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Aneks I Wnioski naukowe i podstawy zawieszenia pozwolenia na dopuszczenie do obrotu przedstawione przez Europejską Agencję Leków 1 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej kwasu nikotynowego/laropiprantu
Rola wysokodawkowanej chemioterapii w połączeniu z autologicznym przeszczepieniem macierzystych komórek krwiotwórczych w chłoniaku Hodgkina
 Rola wysokodawkowanej chemioterapii w połączeniu z autologicznym przeszczepieniem macierzystych komórek krwiotwórczych w chłoniaku Hodgkina Role of high dose chemotherapy and autologous hematopoietic stem
Rola wysokodawkowanej chemioterapii w połączeniu z autologicznym przeszczepieniem macierzystych komórek krwiotwórczych w chłoniaku Hodgkina Role of high dose chemotherapy and autologous hematopoietic stem
Lek. Dominika Kulej. Przebieg kliniczny a wyjściowy status białek oporności wielolekowej w leczeniu ostrej białaczki limfoblastycznej u dzieci
 Lek. Dominika Kulej Katedra i Hematologii Dziecięcej Uniwersytetu Medycznego im. Piastów Śląskich we Wrocławiu Przebieg kliniczny a wyjściowy status białek oporności wielolekowej w leczeniu ostrej białaczki
Lek. Dominika Kulej Katedra i Hematologii Dziecięcej Uniwersytetu Medycznego im. Piastów Śląskich we Wrocławiu Przebieg kliniczny a wyjściowy status białek oporności wielolekowej w leczeniu ostrej białaczki
LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4)
 Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Załącznik B.53. LECZENIE WYSOKO ZRÓŻNICOWANEGO NOWOTWORU NEUROENDOKRYNNEGO TRZUSTKI (ICD-10 C25.4) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY 1. Leczenie wysoko zróżnicowanego nowotworu neuroendokrynnego
Postępy w diagnostyce i leczeniu chorych na chłoniaki nie-hodgkina
 PRACA POGLĄDOWA Hematologia 2015, tom 6, nr 1, 31 43 DOI: 10.5603/Hem.2015.0013 Copyright 2015 Via Medica ISSN 2081 0768 Postępy w diagnostyce i leczeniu chorych na chłoniaki nie-hodgkina Advances in the
PRACA POGLĄDOWA Hematologia 2015, tom 6, nr 1, 31 43 DOI: 10.5603/Hem.2015.0013 Copyright 2015 Via Medica ISSN 2081 0768 Postępy w diagnostyce i leczeniu chorych na chłoniaki nie-hodgkina Advances in the
Pułapki z pozycji radioterapeuty GLEJAKI. dr n. med. Milena Szacht Centrum Radioterapii CSK MSWiA w Warszawie
 Pułapki z pozycji radioterapeuty GLEJAKI dr n. med. Milena Szacht Centrum Radioterapii CSK MSWiA w Warszawie Pułapka 1 błędne przekonanie o dobrej skuteczności medycyny w leczeniu glejaków Jestem dobrym
Pułapki z pozycji radioterapeuty GLEJAKI dr n. med. Milena Szacht Centrum Radioterapii CSK MSWiA w Warszawie Pułapka 1 błędne przekonanie o dobrej skuteczności medycyny w leczeniu glejaków Jestem dobrym
