Warszawa, PLRG / PALG
|
|
|
- Sabina Majewska
- 9 lat temu
- Przeglądów:
Transkrypt
1 Przegląd badań klinicznych PLRG Konferencja PLRG i PALG Warszawa, Janusz Szczepanik CRO Quantum Satis 1
2 Badania kliniczne PLRG PLRG R-CVP/CHOP (PLRG4) HOVON 68 CLL Watch and Wait ACT 1 PLRG8/OMB PALG REMARC 2
3 R-CVP/CHOP (PLRG4 PLRG4) Immunochemioterapia R-CVP lub R-CHOP w indukcji remisji u chorych na chłoniaki przewlekłe oraz rytuksymab (rituximab, MabThera ) w leczeniu podtrzymującym. Wieloośrodkowe, randomizowane badanie kliniczne Polskiej Grupy Badawczej Chłoniaków 3
4 Schematbadania R-CVP/CHOP PLRG4 R-CVP L E CZ L E CZ Rozpoznanie FL, MZL, SLL, LP. Wskazania do leczenia R A N D O M IZ A C JA R-CHOP E N IE I N DU K C Y J N E E N IE P O DT R ZY M UJ Ą C E O BS E R W A C JA 4
5 R-CVP/CHOP - PLRG4 Liczba ośrodków 14. Planowana/osiągnięta rekrutacja 250 pacjentów Pierwsza Wizyta Pierwszego Pacjenta Pierwsza Wizyta Ostatniego Pacjenta Ostatnia Wizyta Ostatniego Pacjenta grudzień 2013 (zakończenie leczenia podtrzymującego) Punkty końcowe: EFS, ORR, TBR, PFS, TNLT, DFS, DR, OS Planowane analizy: przejściowe po 37, 74, 111 oraz ostateczna po 147 zdarzeniach 5
6 PLRG4 -Analiza przejściowa po 77 zdarzeniach Razem A B p Zdarzenia (33%) 37 (29%) 0,562 EFS 67% 71% 0,562 Czas do zdarzenia(dni) Wznowy/ Nawroty (13%) 13 (10%) 0,494 Zgony 13 5 (4%) 8 (6%) 0,426 CR 74/178 40% 43% PR 95/178 56% 51% NC/PD 9/178 3% 6% 6
7 HOVON 68 CLL Fludarabina i Cyklofosfamid vs Fludarabina i Cyklofosfamid skojarzone z niskimi dawkami alemtuzumabu u chorych z przewlekłą białaczką limfatyczną o wysokim stopniu ryzyka. Randomizowane badanie kliniczne III fazy. 7
8 HOVON 68 CLL Liczba ośrodków: 4 aktywne Liczba chorych włączonych do badania w Polsce: 22 Zakończenie rekrutacji chorych Zakończenie badania
9 Watch and Wait Międzynarodowe, randomizowane badanie kliniczne porównujące skuteczność podawania rytuksymabu i postępowania obserwuj i czekaj u pacjentów z zaawansowanym, bez masywnych zmian węzłowych, bezobjawowym chłoniakiem grudkowym Liczba ośrodków: 2 aktywne Liczba chorych włączonych do badania: 3 Rekrutacja zakończona w
10 ACT 1 (younger 60 years) ALEMTUZUMAB AND CHOP IN T-CELL LYMPHOMA Randomizowane badanie kliniczne III fazy oceniające skuteczność chemioimmunoterapii dwutygodniowym programem CHOP pojedynczo lub w skojarzeniu z przeciwciałem monoklonalnym Campath-1H (alemtuzumab) u młodych pacjentów z uprzednio nieleczonymi ogólnoustrojowymi chłoniakami T- komórkowymi wywodzącymi się z limfocytów obwodowych 10
11 ACT 1 (younger patients) ALEMTUZUMAB AND CHOP IN T-CELL LYMPHOMA Wskazanie: uogólniony chłoniak z obwodowych komórek T, uprzednio nieleczony Leczenie: 6xCHOP14 vs 6xCHOP14 + alemtuzumab 30 mg s.c. (1 dnia cyklów 1-4) Konsolidacja - autologiczny przeszczep komórek macierzystych jeśli CR, CRu, PR Faza: III 11
12 ACT1 - Status quo Włączono w CO-I - 2 pacjentów 12
13 PLRG 8 / OMB Badanie II fazy dotyczące zastosowania ofatumumabu w skojarzeniu z programem chemioterapii IVAC (O-IVAC) w leczeniu chorych na chłoniaki rozlane z dużych komórek B w fazie oporności lub nawrotu po uprzednim leczeniu zawierającym R-CHOP, niekwalifikujących się do autotransplantacji komórek krwiotwórczych 13
14 PLRG 8 / OMB Sponsor: PLRG Współpraca: GSK Koordynator: Prof. Jan Walewski EudraCT Nr Zgoda Prezesa Urzędu Rejestracji PLWMPB Pozytywna opinia Komisji Bioetycznej Planowana liczba chorych: 77 Liczba ośrodków: 4 Początek badania: Planowany okres rekrutacji chorych (2 chorych/mies.) = 3 lata 3 miesiące 14
15 PLRG 8 / OMB Projekt badania: Wyjściowa ocena choroby Ocena odpowiedzi po 2 cyklach O-IVAC (Cheson 1999/2007) Kontynuacja leczenia O-IVAC do maksymalnej odpowiedzi + 2 cykle (maks. 6 cyklów). Ofatumumab 1000 mg i.v. w 1 d cyklu. Dawki IVAC dostosowane zależnie od wieku (> lub < 60 r.ż) Punkty końcowe: I RR, II PFS, EFS, OS Po zakończeniu leczenia 12-miesięczna obserwacja z oceną co 3 mies. (w tym CT po 6 i 12 mies., PET jeśli trzeba) 15
16 Główni Badacze, Ośrodki Główny Badacz 1 Prof. J. Walewski Ośrodek Klinika Nowotworów Układu Chłonnego Centrum Onkologii Instytut im. Marii Skłodowskiej-Curie. W-wa Liczba pacjentów 3 2 Prof. K.Warzocha Klinika Hematologii. Instytut Hematologii i Transfuzjologii. W-wa 0 3 Prof. A.Hellmann Klinika Hematologii i Transplantologii, Akademickie Centrum Kliniczne Szpital AMG. Gdańsk 0 4 Prof. A.Pluta Oddział Hematoonkologii Podkarpackiego Ośrodka Onkologicznego. Brzozów 0 16
17 PLRG8 - Kryteria włączenia Potwierdzone histopatologicznie rozpoznanie chłoniaka rozlanego z dużych limfocytów B (diffuse large B-cell lymphoma DLBCL) CD20+ Progresja lub nawrót po uprzednim leczeniu zawierającym, lecz nie ograniczonym do schematu rytuksymab-chop Niekwalifikujący się do leczenia z autologicznym przeszczepieniem komórek pnia (ASCT) (wiek > 60 lat, PS 2, przebyte ASCT, jako część uprzedniego leczenia z powodu DLBCL, i/lub inne powody medyczne, które uniemożliwiają choremu poddanie się procedurze ASCT, np. NYHA II, klirens kreatyniny < 50 ml/min) Wiek 18 lat Stan sprawności wg ECOG/ WHO 0-3 Ustąpienie toksyczności uprzedniego leczenia do stopnia 1 Podpisany formularz świadomej zgody chorego. 17
18 REMARC Wieloośrodkowe, randomizowane, prowadzone metodą podwójnie ślepej próby badanie kliniczne III fazy u chorych na chłoniaka rozlanego z dużych komórek B, oceniające korzyści z zastosowania terapii podtrzymującej lenalidomidem (Revlimid ) w porównaniu z placebo, po uzyskaniu odpowiedzi terapeutycznej po chemioterapii pierwszej linii R- CHOP 18
19 REMARC Sponsor: GELARC Koordynator PL: Prof. Krzysztof Warzocha EudraCT Nr Zgoda Ministra Zdrowia Pozytywna opinia Komisji Bioetycznej Liczba ośrodków: 4 Planowana rekrutacja chorych: ok. 30 / 621 Początek badania:
20 REMARC - Projekt badania 6 do 8 cyklów leczenia pierwszej linii R-CHOP u pacjentów z DBLCL CD20+ powtarzanymi co 14 lub 21 dni zgodnie z preferencją ośrodka; następnie ocena (w okresie do 8 tygodni od 1 dnia ostatniego cyklu) czy uzyskano PR lub CR (Cheson 2007) RANDOMIZACJA do leczenia podtrzymującego (do 12 tyg. od 1 dnia ostatniego cyklu leczenia) POCZĄTEK BADANIA W POLSCE Lenalidomid 25 mg/d vs placebo przez 3 / 4 tyg. przez 24 miesiące 26 cyklów Obserwacja 12 miesięcy Stratyfikacja: CR lub PR w danym kraju 20
21 REMARC - Cel badania Punkty końcowe: I-rzędowe PFS II-rzędowe % pacjentów konwertujących od PR do CR ocena skuteczności w zależności od odpowiedzi na R-CHOP OS Ocena bezpieczeństwa 21
22 REMARC Ośrodki, Rekrutacja Główny badacz Ośrodek Pacjenci włączeni Prof. Krzysztof Warzocha Klinika Hematologii, IHiT Warszawa 1 Prof. Jan Walewski KlinikaNowotworów Układu Chłonnego, CO-I, Warszawa 0 Dr Sebastian Grosicki Specjalistyczna Praktyka Lekarska, Katowice 5 Dr Ewa Kalinka-Warzocha Oddział Chorób Rozrostowych, Regionalny Ośrodek Onkologiczny, Łódź 1 22
23 23
24 REMARC Kryteria włączenia Pacjent z potwierdzonym histologicznie CD20 + rozlanym chłoniakiem dużych limfocytów typu B (DLBCL) wg klasyfikacji WHO 2008 włącznie z podtypami klinicznymi (pierwotny śródpiersiowy, wewnątrznaczyniowy itd.) Pacjenci z transformacją de novo DLBCL z chłoniaków o niższym stopniu złośliwości (grudkowy i inne) Mogą również być włączeni Pacjenci z: DLBCL z drobnokomórkowym naciekaniem szpiku lub chłoniakiem z komórek B CD20 + z pośrednimi cechami pomiędzy DLBCL i chłoniakiem Burkitta lub pośrednimi cechami pomiędzy DLBCL a klasycznym chłoniakiem Hodgkina lub chłoniakiem grudkowym CD20+ stopień 3B lub agresywnym chłoniakiem CD20+ z limfocytów B niesklasyfikowanym Pacjenci, którzy uzyskali całkowita lub częściową remisję (Cheson 2007) po leczeniu pierwszego rzutu co najmniej 6 do 8 cyklów R-CHOP-14 lub R- CHOP-21 Bez uprzedniego leczenia (radioterapia) 24
25 REMARC Kryteria włączenia Wiek od 60 do 80 lat Okres zaawansowania klinicznego 2-4 wg Ann Arbor w okresie postawienia rozpoznania aaipi 1 w okresie postawienia rozpoznania Stan sprawności (ECOG) od 0 2 Minimalny okres oczekiwanego przeżycia - 3 miesiące Podpisana dobrowolna zgoda na udział w badaniu przed wykonaniem jakiejkolwiek procedury badania nie będącej częścią właściwej procedury medycznej z zastrzeżeniem, że zgoda może być wycofana przez pacjenta w każdym czasie bez wpływu na późniejszą opiekę zdrowotną. 25
26 Ustawa o URPL Badanie kliniczne niekomercyjne - badanie kliniczne spełniające łącznie następujące wymagania: - właścicielem danych uzyskanych w trakcie badania jest sponsor, będący uczelnią lub inną placówką naukową posiadającą prawo nadawania stopni naukowych, zakładem opieki zdrowotnej, głównym badaczem, organizacją pacjentów, organizacją głównych badaczy albo inną osobą fizyczną lub prawną, której celem działalności nie jest osiąganie zysku w zakresie prowadzenia i organizacji badań klinicznych bądź wytwarzania lub obrotu produktami leczniczymi, - dane uzyskane w trakcie badania nie mogą być wykorzystane w celu uzyskania pozwolenia na dopuszczenie do obrotu produktu leczniczego, dokonania zmian w istniejącym pozwoleniu lub w celach marketingowych, 26
27 Ustawa o URPL - Wykorzystanie w badaniu klinicznym niekomercyjnym badanych produktów leczniczych uzyskanych od wytwórcy lub podmiotu odpowiedzialnego bezpłatnie lub po obniżonych kosztach, wsparcie merytoryczne lub techniczne wytwórcy lub podmiotu odpowiedzialnego wymaga niezwłocznego poinformowania właściwej komisji bioetycznej i Prezesa Urzędu. - sponsor składając wniosek o rozpoczęcie badania oświadcza, że nie zostały zawarte i nie będą zawarte podczas prowadzenia badania klinicznego jakiekolwiek porozumienia umożliwiające wykorzystanie danych uzyskanych w trakcie badania klinicznego w celu uzyskania pozwolenia na dopuszczenie do obrotu produktu leczniczego, dokonania zmian w istniejącym pozwoleniu lub w celach marketingowych, - planowanie, przeprowadzanie, dokumentowanie oraz raportowanie badania klinicznego jest wykonywane pod nadzorem sponsora; 27
28 Ustawa o URPL Sponsor będzie finansować świadczenia opieki zdrowotnej związane z badaniem klinicznym objęte protokołem badania klinicznego, które nie mieszczą się w zakresie świadczeń gwarantowanych na podstawie przepisów ustawy z dnia 27 sierpnia 2004 r. o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych (Dz. U. z 2008 r. Nr 164, poz. w tym w szczególności będzie dostarczać bezpłatnie uczestnikom badania klinicznego badane produkty lecznicze, komparatory oraz urządzenia stosowane do ich podawania. 28
29 Ustawa o URPL Sponsor będzie również finansować świadczenia opieki zdrowotnej w zakresie pojawiających się powikłań zdrowotnych oraz świadczenia opieki zdrowotnej, których konieczność zastosowania wyniknie z zastosowania badanego produktu leczniczego. [Roszczenie regresowe roszczenia, które wynikają z faktu spełnienia świadczenia przez NFZ i mające za przedmiot dokonanie podziału ciężaru długu lub korzyści wynikających ze spełnienia świadczenia.] Sponsor będzie zobowiązany do finansowania świadczeń opieki zdrowotnej niezbędnych do zakwalifikowania pacjenta do udziału w badaniu klinicznym. Koszty świadczeń opieki zdrowotnej, które będą świadczeniami gwarantowanymi na podstawie przepisów ustawy z dnia 27 sierpnia 2004 r. o świadczeniach opieki zdrowotnej finansowanych ze środków publicznych w ramach leczenia danej jednostki chorobowej, pokrywał będzie Narodowy Fundusz Zdrowia. 29
30 Projekt Ustawy o badaniach klinicznych produktów leczniczych Minister właściwy do spraw zdrowia może określić, w drodze rozporządzenia, szczegółowe wymagania dotyczące przeprowadzania badań klinicznych niekomercyjnych,, mając na względzie charakter badania klinicznego niekomercyjnego, sposób wykorzystania danych do celów naukowych, wytyczne Unii Europejskiej w zakresie badań klinicznych niekomercyjnych oraz zapewnienie bezpieczeństwa uczestnikom badania klinicznego niekomercyjnego. 30
31 Projekt Ustawy o badaniach klinicznych produktów leczniczych W przypadku ośrodków badawczych, które posiadają umowę o udzielanie świadczeń opieki zdrowotnej zawartą z Narodowym Funduszem Zdrowia albo ministrem właściwym do spraw zdrowia w zakresie świadczeń wysokospecjalistycznych, na kierownika ośrodka badawczego będzie nałożony obowiązek złożenia Narodowemu Funduszowi Zdrowia albo ministrowi właściwemu do spraw zdrowia oświadczenia, iż realizacja umowy o prowadzenie badania klinicznego nie zakłóci działalności ośrodka związanej z realizacją umowy o udzielanie świadczeń opieki zdrowotnej. 31
32 Projekt Ustawy o badaniach klinicznych produktów leczniczych Umowa o prowadzenie badania klinicznego będzie musiała zawierać: 1) określenie ogólnej kwoty przeznaczonej na prowadzenie badania klinicznego w danym ośrodku badawczym (przewidywany przez sponsora budżet badania); 2) określenie wysokości wynagrodzenia dla głównego badacza za prowadzenie badania klinicznego; 3) określenie kwoty wynagrodzenia dla ośrodka badawczego; 4) wycenę świadczeń opieki zdrowotnej, które będą wykonywane w ramach tego badania klinicznego. 32
Raport etapowy 28.02.2007 20.05.2008. Protokół w. 3.5; 17/05/2007
 Immunochemioterapia R-CVP lub R-CHOP w indukcji remisji chłoniaków przewlekłych oraz rituximab w leczeniu podtrzymującym Wieloośrodkowe, randomizowane badanie kliniczne Polskiej Grupy Badawczej Chłoniaków
Immunochemioterapia R-CVP lub R-CHOP w indukcji remisji chłoniaków przewlekłych oraz rituximab w leczeniu podtrzymującym Wieloośrodkowe, randomizowane badanie kliniczne Polskiej Grupy Badawczej Chłoniaków
Wsparcie merytoryczne i logistyczne niekomercyjnych badań klinicznych
 Wsparcie merytoryczne i logistyczne niekomercyjnych badań klinicznych Badanie kliniczne definicje badaniem klinicznym jest każde badanie prowadzone z udziałem ludzi w celu odkrycia lub potwierdzenia klinicznych,
Wsparcie merytoryczne i logistyczne niekomercyjnych badań klinicznych Badanie kliniczne definicje badaniem klinicznym jest każde badanie prowadzone z udziałem ludzi w celu odkrycia lub potwierdzenia klinicznych,
Wykaz badań aktualnie prowadzonych w Klinice Hematoonkologii i Transplantacji Szpiku
 Aktualizacja data: 24-04-2012 1. Kod badania i tytuł: CAMN 107 EIC01 Wieloośrodkowe, otwarte badanie fazy IIIb oceniajace skuteczność nilotynibu u dorosłych pacjentów z noworozpoznaną przewlekła białaczka
Aktualizacja data: 24-04-2012 1. Kod badania i tytuł: CAMN 107 EIC01 Wieloośrodkowe, otwarte badanie fazy IIIb oceniajace skuteczność nilotynibu u dorosłych pacjentów z noworozpoznaną przewlekła białaczka
Badanie kliniczne a eksperyment medyczny 23 października 2014 r.
 1 2 Badanie kliniczne a eksperyment medyczny 23 października 2014 r. Olga Zielińska Specjalista w Wydziale Organizacyjno-Prawnym Departamentu Polityki Lekowej i Farmacji Pierwsze badanie kliniczne na świecie
1 2 Badanie kliniczne a eksperyment medyczny 23 października 2014 r. Olga Zielińska Specjalista w Wydziale Organizacyjno-Prawnym Departamentu Polityki Lekowej i Farmacji Pierwsze badanie kliniczne na świecie
Białaczka limfatyczna
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
Niekomercyjne badania kliniczne z perspektywy badacza. Dr n.med. Maciej Siński
 Niekomercyjne badania kliniczne z perspektywy badacza Dr n.med. Maciej Siński Plan prezentacji Definicja niekomercyjnego badania klinicznego Podstawowe problemy praktyczne Wiedza Finansowanie Przygotowanie
Niekomercyjne badania kliniczne z perspektywy badacza Dr n.med. Maciej Siński Plan prezentacji Definicja niekomercyjnego badania klinicznego Podstawowe problemy praktyczne Wiedza Finansowanie Przygotowanie
c) poprawa jakości życia chorych z nieziarniczym chłoniakiem typu grudkowego w III i IV stopniu
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 9 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011r. LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 9 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011r. LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
c) poprawa jakości życia chorych z nieziarniczym chłoniakiem typu grudkowego w III i IV stopniu
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2009 Załącznik nr 10 do zarządzenia Nr 98/2008/DGL Prezesa NFZ z dnia 27 października 2008 roku LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Nazwa programu: Terapeutyczne Programy Zdrowotne 2009 Załącznik nr 10 do zarządzenia Nr 98/2008/DGL Prezesa NFZ z dnia 27 października 2008 roku LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 33/2012 z dnia 18 czerwca 2012 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych albo zmiany jego poziomu
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 33/2012 z dnia 18 czerwca 2012 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych albo zmiany jego poziomu
MabThera. w leczeniu podtrzymującym chorych na chłoniaka grudkowego. Dr hab. med. Maciej Machaczka, Prof. UR
 MabThera w leczeniu podtrzymującym chorych na chłoniaka grudkowego Dr hab. med. Maciej Machaczka, Prof. UR Senior Consultant and Research Scientist Hematology Center Karolinska and Karolinska Institutet
MabThera w leczeniu podtrzymującym chorych na chłoniaka grudkowego Dr hab. med. Maciej Machaczka, Prof. UR Senior Consultant and Research Scientist Hematology Center Karolinska and Karolinska Institutet
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 9/2012 z dnia 27 lutego 2012 w zakresie zmiany sposobu finansowania świadczenia gwarantowanego Leczenie chłoniaków
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 9/2012 z dnia 27 lutego 2012 w zakresie zmiany sposobu finansowania świadczenia gwarantowanego Leczenie chłoniaków
c) poprawa jakości życia chorych z nieziarniczym chłoniakiem typu grudkowego w III i IV stopniu
 załącznik nr 10 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chloniak grudkowy C 83 chłoniaki nieziarniczy rozlane Dziedzina
załącznik nr 10 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu: LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chloniak grudkowy C 83 chłoniaki nieziarniczy rozlane Dziedzina
Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie?
 Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie? lek. med. Marek Dudziński Oddział Hematologii Wojewódzki Szpital Specjalistyczny
Rozwiązania systemowe dla leków hematoonkologicznych dla małych populacji pacjentów - czy program lekowy to optymalne rozwiązanie? lek. med. Marek Dudziński Oddział Hematologii Wojewódzki Szpital Specjalistyczny
INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII SKŁODOWSKIEJ-CURIE, ODDZIALE W GLIWICACH
 KLINIKA TRANSPLANTACJI SZPIKU /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII SKŁODOWSKIEJ-CURIE,
KLINIKA TRANSPLANTACJI SZPIKU /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII SKŁODOWSKIEJ-CURIE,
H11 advanced stage HL trial
 H11 advanced stage HL trial Baseline PET/CT + tumortarc and plasmatarc Experimental Arm Standard Arm 1 x ABVD 1 x BEAesc PET/CT + plasmatarc PET+ PET- PET+/- 3 x BEAesc 3 x ABVD 3 x BEAesc CT + plasmatarc
H11 advanced stage HL trial Baseline PET/CT + tumortarc and plasmatarc Experimental Arm Standard Arm 1 x ABVD 1 x BEAesc PET/CT + plasmatarc PET+ PET- PET+/- 3 x BEAesc 3 x ABVD 3 x BEAesc CT + plasmatarc
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Nowe możliwości leczenia ostrej białaczki limfoblastycznej
 Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
23 Zebranie PLRG / PALG. Sprawozdanie z XXIII Zebrania PLRG/PALG 12-13.03.2010 r.
 23 Zebranie PLRG / PALG Sprawozdanie z XXIII Zebrania PLRG/PALG 12-13.03.2010 r. Miejsce zebrania Uczestnicy: Program zebrania Stan badań PLRG raport CRO Centrum Onkologii - Instytut, Aula im. T. Koszarowskiego,
23 Zebranie PLRG / PALG Sprawozdanie z XXIII Zebrania PLRG/PALG 12-13.03.2010 r. Miejsce zebrania Uczestnicy: Program zebrania Stan badań PLRG raport CRO Centrum Onkologii - Instytut, Aula im. T. Koszarowskiego,
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 20/2014 z dnia 20 stycznia 2014 r. w sprawie usunięcia świadczenia obejmującego podawanie winorelbiny w rozpoznaniach
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 20/2014 z dnia 20 stycznia 2014 r. w sprawie usunięcia świadczenia obejmującego podawanie winorelbiny w rozpoznaniach
Przewlekła białaczka limfocytowa
 Przewlekła białaczka limfocytowa Ewa Lech-Marańda Klinika Hematologii Instytutu Hematologii i Transfuzjologii Klinika Hematologii i Transfuzjologii CMKP Przewlekła białaczka limfocytowa (CLL) Początek
Przewlekła białaczka limfocytowa Ewa Lech-Marańda Klinika Hematologii Instytutu Hematologii i Transfuzjologii Klinika Hematologii i Transfuzjologii CMKP Przewlekła białaczka limfocytowa (CLL) Początek
21 Zebranie Polskiej Grupy Badawczej Chłoniaków
 Sprawozdanie z 21 Zebrania PLRG 24-25.04.2009 Miejsce zebrania: Hotel Szkoleniowy Ursynów, Warszawa, ul. Roentgena 5 Uczestnicy W zebraniu uczestniczyło 47 osób, w tym 36 członków zwyczajnych PGBCh. Sprawy
Sprawozdanie z 21 Zebrania PLRG 24-25.04.2009 Miejsce zebrania: Hotel Szkoleniowy Ursynów, Warszawa, ul. Roentgena 5 Uczestnicy W zebraniu uczestniczyło 47 osób, w tym 36 członków zwyczajnych PGBCh. Sprawy
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Polskie doświadczenia kliniczne z bendamustyną
 Polskie doświadczenia kliniczne z bendamustyną Iwona Hus Klinika Hematoonkologii i Transplantacji Szpiku UM w Lublinie XXIII Zjazd PTHiT Wrocław 2009 Bendamustyna w leczeniu PBL monoterapia Efficacy of
Polskie doświadczenia kliniczne z bendamustyną Iwona Hus Klinika Hematoonkologii i Transplantacji Szpiku UM w Lublinie XXIII Zjazd PTHiT Wrocław 2009 Bendamustyna w leczeniu PBL monoterapia Efficacy of
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Rysunek. Układ limfatyczny.
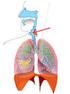 Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
NON-HODGKIN S LYMPHOMA
 NON-HODGKIN S LYMPHOMA Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku We Wrocławiu Aleksandra Bogucka-Fedorczuk DEFINICJA Chłoniaki Non-Hodgkin (NHL) to heterogeniczna grupa nowotworów charakteryzująca
NON-HODGKIN S LYMPHOMA Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku We Wrocławiu Aleksandra Bogucka-Fedorczuk DEFINICJA Chłoniaki Non-Hodgkin (NHL) to heterogeniczna grupa nowotworów charakteryzująca
Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych
 Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych Jadwiga Dwilewicz-Trojaczek Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa
Leki immunomodulujące-przełom w leczeniu nowotworów hematologicznych Jadwiga Dwilewicz-Trojaczek Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa
OSTRA BIALACZKA SZPIKOWA
 KLINIKA TYTUL BADANIA NUMER BADANIA OSOBA KONTAKTOWA Badanie kliniczne fazy III, podwójnie zaslepione, kontrolowane za pomoca placebo, z losowym doborem azacytydyny podawanej lacznie z najlepsza terapia
KLINIKA TYTUL BADANIA NUMER BADANIA OSOBA KONTAKTOWA Badanie kliniczne fazy III, podwójnie zaslepione, kontrolowane za pomoca placebo, z losowym doborem azacytydyny podawanej lacznie z najlepsza terapia
OSTRA BIALACZKA SZPIKOWA
 KLINIKA TYTUL BADANIA NUMER BADANIA OSTRA BIALACZKA SZPIKOWA Badanie fazy 1B / 2 sluzace ocenie bezpieczenstwa i skutecznosci leku PF- 04449913, doustnego inhibitora szlaku Hedgehog, podawanego w polaczeniu
KLINIKA TYTUL BADANIA NUMER BADANIA OSTRA BIALACZKA SZPIKOWA Badanie fazy 1B / 2 sluzace ocenie bezpieczenstwa i skutecznosci leku PF- 04449913, doustnego inhibitora szlaku Hedgehog, podawanego w polaczeniu
Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008.
 załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
załącznik nr 7 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Program dotyczy wyłącznie kontynuacji leczenia pacjentów włączonych do programu do dnia 30.03.2008. 1. Nazwa programu:
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej u dorosłych imatinibem 1.1 Kryteria kwalifikacji Świadczeniobiorcy
INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII SKŁODOWSKIEJ-CURIE, ODDZIALE W GLIWICACH
 KLINIKA TRANSPLANTACJI SZPIKU I ONKOHEMATOLOGII /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE
KLINIKA TRANSPLANTACJI SZPIKU I ONKOHEMATOLOGII /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE
HEMATOLOGIA ONKOLOGICZNA ASPEKTY KLINICZNE, EKONOMICZNE I SYSTEMOWE
 HEMATOLOGIA ONKOLOGICZNA ASPEKTY KLINICZNE, EKONOMICZNE I SYSTEMOWE Raport Instytutu Zarządzania w Ochronie Zdrowia Uczelni Łazarskiego we współpracy z Instytutem Hematologii i Transfuzjologii (Prof. Krzysztof
HEMATOLOGIA ONKOLOGICZNA ASPEKTY KLINICZNE, EKONOMICZNE I SYSTEMOWE Raport Instytutu Zarządzania w Ochronie Zdrowia Uczelni Łazarskiego we współpracy z Instytutem Hematologii i Transfuzjologii (Prof. Krzysztof
OSTRA BIALACZKA SZPIKOWA
 INSTYTUT HEMATOLOGII I TRANSFUZJOLOGII KLINIKA TYTUL BADANIA NUMER BADANIA OSTRA BIALACZKA SZPIKOWA Badanie kliniczne fazy III, podwójnie zaslepione, kontrolowane za pomoca placebo, z losowym doborem azacytydyny
INSTYTUT HEMATOLOGII I TRANSFUZJOLOGII KLINIKA TYTUL BADANIA NUMER BADANIA OSTRA BIALACZKA SZPIKOWA Badanie kliniczne fazy III, podwójnie zaslepione, kontrolowane za pomoca placebo, z losowym doborem azacytydyny
chorych na ITP Krzysztof Chojnowski Warszawa, 27 listopada 2009 r.
 Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
PROGRAM KONFERENCJI PALG - PLRG - PSH
 Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl tel.: +48 32 278-8523, -8529, fax: +48 32 278-8524 PROGRAM KONFERENCJI PALG - PLRG - PSH 8-9 listopada 2013 Stowarzyszenie Polska
Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl tel.: +48 32 278-8523, -8529, fax: +48 32 278-8524 PROGRAM KONFERENCJI PALG - PLRG - PSH 8-9 listopada 2013 Stowarzyszenie Polska
LECZENIE CHORYCH NA OPORNEGO LUB NAWROTOWEGO SZPICZAKA PLAZMOCYTOWEGO (ICD10 C90.0)
 Załącznik B.54. LECZENIE CHORYCH NA OPORNEGO LUB NAWROTOWEGO SZPICZAKA PLAZMOCYTOWEGO (ICD10 C90.0) ŚWIADCZENIOBIORCY 1. Leczenie lenalidomidem chorych na opornego lub nawrotowego szpiczaka plazmocytowego.
Załącznik B.54. LECZENIE CHORYCH NA OPORNEGO LUB NAWROTOWEGO SZPICZAKA PLAZMOCYTOWEGO (ICD10 C90.0) ŚWIADCZENIOBIORCY 1. Leczenie lenalidomidem chorych na opornego lub nawrotowego szpiczaka plazmocytowego.
Konferencja Naukowa TRANSPLANTACJA KOMÓREK KRWIOTWÓRCZYCH U CHORYCH NA NOWOTWORY LIMFOIDALNE
 Konferencja Naukowa TRANSPLANTACJA KOMÓREK KRWIOTWÓRCZYCH U CHORYCH NA NOWOTWORY LIMFOIDALNE Jubileusz 20-lecia transplantacji komórek krwiotwórczych w Klinice Hematoonkologii i Transplantacji Szpiku w
Konferencja Naukowa TRANSPLANTACJA KOMÓREK KRWIOTWÓRCZYCH U CHORYCH NA NOWOTWORY LIMFOIDALNE Jubileusz 20-lecia transplantacji komórek krwiotwórczych w Klinice Hematoonkologii i Transplantacji Szpiku w
Program konferencji PALG / PLRG (XXIV) 1-2 Października 2010
 Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl, jholowiecki@io.gliwice.pl, tel.: +48 32 278 8523, lub +48 32 278 8529, fax: +48 32 2788524 Stowarzyszenie Polska Grupa Badawcza
Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl, jholowiecki@io.gliwice.pl, tel.: +48 32 278 8523, lub +48 32 278 8529, fax: +48 32 2788524 Stowarzyszenie Polska Grupa Badawcza
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzić Skład zespołu badawczego rozpoczęcia
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 618 Poz. 51 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ I OSTRĄ BIAŁACZKĘ SZPIKOWĄ
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka szpikowa OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ I OSTRĄ BIAŁACZKĘ SZPIKOWĄ Dasatinib Dasatinib jest wskazany do leczenia dorosłych pacjentów z:
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka szpikowa OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ I OSTRĄ BIAŁACZKĘ SZPIKOWĄ Dasatinib Dasatinib jest wskazany do leczenia dorosłych pacjentów z:
ALLOPRZESZCZEPIENIE KRWIOTWÓRCZYCH KOMÓREK MACIERZYSTYCH w PRZEWLEKŁEJ BIAŁACZCE LIMFOCYTOWEJ w POLSCE ANKIETA WIELOOŚRODKOWA
 ALLOPRZESZCZEPIENIE KRWIOTWÓRCZYCH KOMÓREK MACIERZYSTYCH w PRZEWLEKŁEJ BIAŁACZCE LIMFOCYTOWEJ w POLSCE ANKIETA WIELOOŚRODKOWA Ośrodek koordynujący: Śląskiego Uniwersytetu Medycznego w Katowicach Kierownik
ALLOPRZESZCZEPIENIE KRWIOTWÓRCZYCH KOMÓREK MACIERZYSTYCH w PRZEWLEKŁEJ BIAŁACZCE LIMFOCYTOWEJ w POLSCE ANKIETA WIELOOŚRODKOWA Ośrodek koordynujący: Śląskiego Uniwersytetu Medycznego w Katowicach Kierownik
Narodowy Instytut Onkologii i Hematologii. prof. dr hab. n. med. Krzysztof Warzocha
 Narodowy Instytut Onkologii i Hematologii IHiT CO-I NZOZ M. Warszawa mln zł zmian % mln zł zmian % mln zł zmian % 2008 70,03 100,00% 381,81 100,00% 11,94 100,00% 2009 79,13 112,99% 383,94 100,56% 27,97
Narodowy Instytut Onkologii i Hematologii IHiT CO-I NZOZ M. Warszawa mln zł zmian % mln zł zmian % mln zł zmian % 2008 70,03 100,00% 381,81 100,00% 11,94 100,00% 2009 79,13 112,99% 383,94 100,56% 27,97
ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH
 ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH 1 Państwo Członkowskie UE/EOG Austria Belgia Dania Finlandia Francja Irlandia
ANEKS I WYKAZ NAZW, POSTACI)FARMACEUTYCZNYCH, MOCY PRODUKTÓW LECZNICZYCH, DRÓG PODANIA, WNIOSKODAWCA W PAŃSTWACH CZŁONKOWSKICH 1 Państwo Członkowskie UE/EOG Austria Belgia Dania Finlandia Francja Irlandia
Rysunek. Układ limfatyczny.
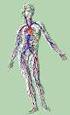 Informacja dotyczy chłoniaka grudkowego, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu odpornościowego
Informacja dotyczy chłoniaka grudkowego, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu odpornościowego
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 38/2014 z dnia 28 stycznia 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia opieki zdrowotnej obejmującego
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 38/2014 z dnia 28 stycznia 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia opieki zdrowotnej obejmującego
Rak piersi. Doniesienia roku Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie
 Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
Rak piersi Doniesienia roku 2014 Renata Duchnowska Klinika Onkologii Wojskowy Instytut Medyczny w Warszawie Miejscowe leczenie Skrócone napromienianie części piersi (accelerated partial breast irradiation;
CO TO SĄ NIEKOMERCYJNE BADANIA KLINICZNE?
 CO TO SĄ NIEKOMERCYJNE BADANIA KLINICZNE? Celem niekomercyjnych badań klinicznych jest poszerzanie wiedzy i rozwój praktyki klinicznej Nie służą one osiąganiu zysku w zakresie prowadzenia i organizacji
CO TO SĄ NIEKOMERCYJNE BADANIA KLINICZNE? Celem niekomercyjnych badań klinicznych jest poszerzanie wiedzy i rozwój praktyki klinicznej Nie służą one osiąganiu zysku w zakresie prowadzenia i organizacji
Badania kliniczne doświadczenie Polski
 URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH, WYROBÓW MEDYCZNYCH I PRODUKTÓW BIOBÓJCZYCH Badania kliniczne doświadczenie Polski Michał Gryz Dyrektor Departamentu Inspekcji Produktów Leczniczych i Wyrobów Medycznych
URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH, WYROBÓW MEDYCZNYCH I PRODUKTÓW BIOBÓJCZYCH Badania kliniczne doświadczenie Polski Michał Gryz Dyrektor Departamentu Inspekcji Produktów Leczniczych i Wyrobów Medycznych
Wykaz badań aktualnie prowadzonych w Klinice Hematoonkologii i Transplantacji Szpiku
 Wykaz badań aktualnie prowadzonych Aktualizacja data: 31.05.2012. l. Kod badania i tytuł: NN1731-3S62 (ADEPT 2) "Skuteczność i bezpieczeństwo NNC 0078-0000-0007 w leczeniu epizodów ostrych krwawień u pacjentów
Wykaz badań aktualnie prowadzonych Aktualizacja data: 31.05.2012. l. Kod badania i tytuł: NN1731-3S62 (ADEPT 2) "Skuteczność i bezpieczeństwo NNC 0078-0000-0007 w leczeniu epizodów ostrych krwawień u pacjentów
Dr n. med. Norbert Grząśko w imieniu Polskiej Grupy Szpiczakowej Lublin, 12.04.2008
 Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
Ocena skuteczności i bezpieczeństwa leczenia układem CTD (cyklofosfamid, talidomid, deksametazon) u chorych na szpiczaka plazmocytowego aktualizacja danych Dr n. med. Norbert Grząśko w imieniu Polskiej
Badania laboratoryjne (i inne) są wykonywane w jednych z najlepszych na świecie laboratoriów.
 {jcomments off} BADANIA KLINICZNE 1. W badaniach klinicznych testuje się nowe leki. 2. Badania kliniczne są często jedyną okazją do podjęcia leczenia w przypadku nieskuteczności lub niskiej sktutecznosći
{jcomments off} BADANIA KLINICZNE 1. W badaniach klinicznych testuje się nowe leki. 2. Badania kliniczne są często jedyną okazją do podjęcia leczenia w przypadku nieskuteczności lub niskiej sktutecznosći
Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego.
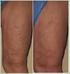 Chłoniak z komórek płaszcza Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego,
Chłoniak z komórek płaszcza Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego,
LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0)
 Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
Załącznik B.65. LECZENIE CHORYCH NA OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ICD-10 C91.0) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji do leczenia dazatynibem ostrej białaczki limfoblastycznej z obecnością chromosomu
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym?
 Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
Czy wiemy jak u chorych na raka gruczołu krokowego optymalnie stosować leczenie systemowe w skojarzeniu z leczeniem miejscowym? Piotr Potemski Klinika Chemioterapii Nowotworów Katedry Onkologii Uniwersytet
WSPIERAMY I ORGANIZUJEMY NIEKOMERCYJNE BADANIA KLINICZNE
 WSPIERAMY I ORGANIZUJEMY NIEKOMERCYJNE BADANIA KLINICZNE CO TO SĄ NIEKOMERCYJNE BADANIA KLINICZNE? Celem niekomercyjnych badań klinicznych jest poszerzanie wiedzy i rozwój praktyki klinicznej Nie służą
WSPIERAMY I ORGANIZUJEMY NIEKOMERCYJNE BADANIA KLINICZNE CO TO SĄ NIEKOMERCYJNE BADANIA KLINICZNE? Celem niekomercyjnych badań klinicznych jest poszerzanie wiedzy i rozwój praktyki klinicznej Nie służą
Terapeutyczne Programy Zdrowotne 2012 Leczenie glejaków mózgu Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r.
 Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
Załącznik nr 6 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: LECZENIE GLEJAKÓW MÓZGU ICD-10 C71 nowotwór złośliwy mózgu Dziedzina medycyny: Onkologia kliniczna,
LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2)
 Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
Załącznik B.71. LECZENIE PRZEWLEKŁEGO WIRUSOWEGO ZAPALENIA WĄTROBY TYPU C TERAPIĄ BEZINTERFERONOWĄ (ICD-10 B 18.2) ŚWIADCZENIOBIORCY 1. Kryteria kwalifikacji: 1) Do programu kwalifikowani są dorośli świadczeniobiorcy
BENDAMUSTINUM HYDROCHLORIDUM
 Dziennik Urzędowy Ministra Zdrowia 1499 Poz. 71 Załącznik C.67. BENDAMUSTINUM HYDROCHLORIDUM 1. BENDAMUSTINUM HYDROCHLORIDUM C81 2. BENDAMUSTINUM HYDROCHLORIDUM C81.0 3. BENDAMUSTINUM HYDROCHLORIDUM C81.1
Dziennik Urzędowy Ministra Zdrowia 1499 Poz. 71 Załącznik C.67. BENDAMUSTINUM HYDROCHLORIDUM 1. BENDAMUSTINUM HYDROCHLORIDUM C81 2. BENDAMUSTINUM HYDROCHLORIDUM C81.0 3. BENDAMUSTINUM HYDROCHLORIDUM C81.1
Nowotwory układu chłonnego
 Nowotwory układu chłonnego Redakcja: Krzysztof Warzocha, Monika Prochorec-Sobieszek, Ewa Lech-Marańda Zespół autorski: Sebastian Giebel, Krzysztof Jamroziak, Przemysław Juszczyński, Ewa Kalinka-Warzocha,
Nowotwory układu chłonnego Redakcja: Krzysztof Warzocha, Monika Prochorec-Sobieszek, Ewa Lech-Marańda Zespół autorski: Sebastian Giebel, Krzysztof Jamroziak, Przemysław Juszczyński, Ewa Kalinka-Warzocha,
Wykaz badań aktualnie prowadzonych w Klinice Hematoonkologii i Transplantacji Szpiku
 Wykaz badań aktualnie prowadzonych Aktualizacja data: 04-05-2012r.. 1. Kod badania i tytuł: BO B020603 "Wieloośrodkowe, randomizowane, podwójnie zaślepione badanie fazy III kontrolowane przy pomocy placebo,
Wykaz badań aktualnie prowadzonych Aktualizacja data: 04-05-2012r.. 1. Kod badania i tytuł: BO B020603 "Wieloośrodkowe, randomizowane, podwójnie zaślepione badanie fazy III kontrolowane przy pomocy placebo,
Leczenie systemowe raka nie-jasnokomórkowego
 Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Leczenie systemowe raka nie-jasnokomórkowego Piotr Tomczak Uniwersytet Medyczny w Poznaniu Klinika Onkologii Jastrzębia Góra Nie-jasnokomórkowy rak nerki (ncc RCC) niejednorodna grupa o zróżnicowanej histologii
Limfocyty powstają w szpiku kostnym, czyli tam gdzie powstają wszystkie komórki krwi. Występują
 Informacja dotyczy chłoniaka śródpiersia z dużych komórek B, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu
Informacja dotyczy chłoniaka śródpiersia z dużych komórek B, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu
Międzynarodowe standardy leczenia szpiczaka plazmocytowego w roku 2014
 Międzynarodowe standardy leczenia szpiczaka plazmocytowego w roku 2014 Wiesław Wiktor Jędrzejczak, Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawskiego Uniwersytetu Medycznego Tak
Międzynarodowe standardy leczenia szpiczaka plazmocytowego w roku 2014 Wiesław Wiktor Jędrzejczak, Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawskiego Uniwersytetu Medycznego Tak
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 268/2013 z dnia 30 grudnia 2013 r. w sprawie usunięcia świadczenia obejmującego podawanie nelarabiny w rozpoznaniach
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 268/2013 z dnia 30 grudnia 2013 r. w sprawie usunięcia świadczenia obejmującego podawanie nelarabiny w rozpoznaniach
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 73/2012 z dnia 24 września 2012 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia z wykazu świadczeń gwarantowanych
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 73/2012 z dnia 24 września 2012 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia z wykazu świadczeń gwarantowanych
LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
Załącznik B.14. LECZENIE CHORYCH NA PRZEWLEKŁĄ BIAŁACZKĘ SZPIKOWĄ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 90/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 19 grudnia 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 90/2011 Prezesa Agencji Oceny Technologii Medycznych z dnia 19 grudnia 2011 r. w sprawie usunięcia z wykazu świadczeń gwarantowanych
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego. Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa
 Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Rak trzustki - chemioterapia i inne metody leczenia nieoperacyjnego Piotr Wysocki Klinika Onkologiczna Centrum Onkologii Instytut Warszawa RAK TRZUSTKI U 50% chorych w momencie rozpoznania stwierdza się
Nazwa programu: PROGRAM LECZENIA W RAMACH ŚWIADCZENIA CHEMIOTERAPII NIESTANDARDOWEJ
 Załącznik nr 38 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: PROGRAM LECZENIA W RAMACH ŚWIADCZENIA CHEMIOTERAPII NIESTANDARDOWEJ ZAKRES ŚWIADCZENIA GWARANTOWANEGO
Załącznik nr 38 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 r. Nazwa programu: PROGRAM LECZENIA W RAMACH ŚWIADCZENIA CHEMIOTERAPII NIESTANDARDOWEJ ZAKRES ŚWIADCZENIA GWARANTOWANEGO
CZWARTEK 7 listopada 2013 Zespół ds. Transplantacji Szpiku narada robocza godz. 19.00 Miejsce: Salka Szkoleniowa, Hotel Ursynów
 Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl tel.: +48 32 278-8523, -8529, fax: +48 32 278-8524 PROGRAM KONFERENCJI PALG - PLRG - PSH 8-9 listopada 2013 Stowarzyszenie Polska
Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl tel.: +48 32 278-8523, -8529, fax: +48 32 278-8524 PROGRAM KONFERENCJI PALG - PLRG - PSH 8-9 listopada 2013 Stowarzyszenie Polska
Wykaz badań aktualnie prowadzonych
 Wykaz badań aktualnie prowadzonych w Kliniec Hematoonkologii i Transplantacji Szpiku Aktualizacja data: 06-07-2012. ;--._-_._----_...---...-. l. Kod badania i tytul: _. ------._---_._-_.._------, CA204004:
Wykaz badań aktualnie prowadzonych w Kliniec Hematoonkologii i Transplantacji Szpiku Aktualizacja data: 06-07-2012. ;--._-_._----_...---...-. l. Kod badania i tytul: _. ------._---_._-_.._------, CA204004:
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 234/2014 z dnia 3 listopada 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego MabThera
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 234/2014 z dnia 3 listopada 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie objęcia refundacją produktu leczniczego MabThera
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 143/2013 z dnia 21 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia opieki zdrowotnej
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 143/2013 z dnia 21 października 2013 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia opieki zdrowotnej
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia.2018 r. w sprawie Krajowego Rejestru Nowotworów
 ROZPORZĄDZENIE Projekt z dnia 20.02.2018 r. MINISTRA ZDROWIA 1) z dnia.2018 r. w sprawie Krajowego Rejestru Nowotworów Na podstawie art. 20 ust. 1 ustawy z dnia 28 kwietnia 2011 r. o systemie informacji
ROZPORZĄDZENIE Projekt z dnia 20.02.2018 r. MINISTRA ZDROWIA 1) z dnia.2018 r. w sprawie Krajowego Rejestru Nowotworów Na podstawie art. 20 ust. 1 ustawy z dnia 28 kwietnia 2011 r. o systemie informacji
Ocena potrzeb i warunków reorganizacji Centrum Onkologii Instytutu im. Marii Skłodowskiej-Curie w Warszawie. prof. dr hab. n. med.
 Ocena potrzeb i warunków reorganizacji Centrum Onkologii Instytutu im. Marii Skłodowskiej-Curie w Warszawie CZAS OCZEKIWANIA KILKA TYGODNI CZAS OCZEKIWANIA MIESIĄCE, LATA Obraz stanu faktycznego oraz budowa
Ocena potrzeb i warunków reorganizacji Centrum Onkologii Instytutu im. Marii Skłodowskiej-Curie w Warszawie CZAS OCZEKIWANIA KILKA TYGODNI CZAS OCZEKIWANIA MIESIĄCE, LATA Obraz stanu faktycznego oraz budowa
Raport Biała Księga PBL
 Raport Biała Księga PBL 01 agenda 01 Informacje o raporcie 02 Fakty o chorobie 03 Sylwetka pacjenta 04 Standardy leczenia i diagnostyka 05 Wyzwania w opiece nad chorymi w Polsce 06 Wnioski 02 Informacje
Raport Biała Księga PBL 01 agenda 01 Informacje o raporcie 02 Fakty o chorobie 03 Sylwetka pacjenta 04 Standardy leczenia i diagnostyka 05 Wyzwania w opiece nad chorymi w Polsce 06 Wnioski 02 Informacje
Specjalności. Warunki GINEKOLOGIA ONKOLOGICZNA HEMATO-ONKOLOGIA DZIECIĘCA TRYB AMBULATORYJNY ENDOKRYNOLOGIA HOSPITALIZACJA
 Katalog chemioterapii nie stanowi źródła wiedzy medycznej, a jest jedynie narzędziem sprawozdawczo-rozliczeniowym NFZ. W każdym przypadku za wdrożenie odpowiedniej terapii zgodnie z aktualną wiedzą medyczną
Katalog chemioterapii nie stanowi źródła wiedzy medycznej, a jest jedynie narzędziem sprawozdawczo-rozliczeniowym NFZ. W każdym przypadku za wdrożenie odpowiedniej terapii zgodnie z aktualną wiedzą medyczną
Praktyczne stosowanie terapii celowanej w hematologii aktualne problemy
 Prof. Andrzej Hellmann Katedra i Klinika Hematologii i Transplantologii Gdański Uniwersytet Medyczny Praktyczne stosowanie terapii celowanej w hematologii aktualne problemy Seminarium Edukacyjne Innowacje
Prof. Andrzej Hellmann Katedra i Klinika Hematologii i Transplantologii Gdański Uniwersytet Medyczny Praktyczne stosowanie terapii celowanej w hematologii aktualne problemy Seminarium Edukacyjne Innowacje
Data rozpoczęcia badania klinicznego i przewidywan y czas jego trwania. Przewidywana liczba uczestników badania klinicznego i kryteria ich rekrutacji
 Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzid Skład zespołu badawczego rozpoczęcia
Lp. Tytuł Nazwa sponsora lub przedstawiciela sponsora Dane identyfikujące koordynatora /lub badacza, w tym czy prowadzi on równolegle inne kliniczne lub zamierza je prowadzid Skład zespołu badawczego rozpoczęcia
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 171/2014 z dnia 7 lipca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego obejmującego
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 171/2014 z dnia 7 lipca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia świadczenia gwarantowanego obejmującego
Rysunek. Układ limfatyczny.
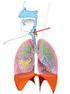 Poniższa informacja dotyczy rodzaju chłoniaka nieziarniczego, zwanego chłoniakiem anaplastycznym z dużych komórek. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest
Poniższa informacja dotyczy rodzaju chłoniaka nieziarniczego, zwanego chłoniakiem anaplastycznym z dużych komórek. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest
Zastosowanie badania wczesnego PET w ocenie wyników leczenia chłoniaka DLBCL w świetle najnowszych publikacji. Edyta Subocz
 Zastosowanie badania wczesnego PET w ocenie wyników leczenia chłoniaka DLBCL w świetle najnowszych publikacji Edyta Subocz - posi-pet nie jest czynnikiem prognostycznym gorszego rokowania u pacjentów z
Zastosowanie badania wczesnego PET w ocenie wyników leczenia chłoniaka DLBCL w świetle najnowszych publikacji Edyta Subocz - posi-pet nie jest czynnikiem prognostycznym gorszego rokowania u pacjentów z
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria kwalifikacji 1) przewlekła białaczka szpikowa
OSTRA BIAŁACZKA SZPIKOWA
 KLINIKA TYTUŁ BADANIA NUMER BADANIA NAZWA BADANEJ SUBSTANCJI (SPONSOR) Badanie fazy III prowadzone metodą podwójnie ślepej próby z grupą kontrolną otrzymującą placebo oceniające stosowanie quizartinibu
KLINIKA TYTUŁ BADANIA NUMER BADANIA NAZWA BADANEJ SUBSTANCJI (SPONSOR) Badanie fazy III prowadzone metodą podwójnie ślepej próby z grupą kontrolną otrzymującą placebo oceniające stosowanie quizartinibu
Jarosław B. Ćwikła. Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie
 Nowe algorytmy oceny odpowiedzi na leczenie w badaniach strukturalnych, dużo dalej niż klasyczne kryteria RECIST Jarosław B. Ćwikła Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie Radiologiczna
Nowe algorytmy oceny odpowiedzi na leczenie w badaniach strukturalnych, dużo dalej niż klasyczne kryteria RECIST Jarosław B. Ćwikła Wydział Nauk Medycznych Uniwersytet Warmińsko-Mazurski w Olsztynie Radiologiczna
LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1)
 Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Dziennik Urzędowy Ministra Zdrowia 624 Poz. 71 Załącznik B.14. LECZENIE PRZEWLEKŁEJ BIAŁACZKI SZPIKOWEJ (ICD-10 C 92.1) ŚWIADCZENIOBIORCY 1. Leczenie przewlekłej białaczki szpikowej dazatynibem 1.1. Kryteria
Etyka finansowania leczenia chorób rzadkich onkologicznych
 Etyka finansowania leczenia chorób rzadkich onkologicznych Piotr Fiedor VI Letnia Akademia Onkologiczna dla Dziennikarzy Opracowano na podstawie źródeł udostępnionych w systemie informacji publicznej 11.08.2016
Etyka finansowania leczenia chorób rzadkich onkologicznych Piotr Fiedor VI Letnia Akademia Onkologiczna dla Dziennikarzy Opracowano na podstawie źródeł udostępnionych w systemie informacji publicznej 11.08.2016
PROGRAM KONFERENCJI PALG - PLRG - PSH
 Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl tel.: +48 32 278-8523, -8529, fax: +48 32 278-8524 PROGRAM KONFERENCJI PALG - PLRG - PSH 8-9 listopada 2013 Stowarzyszenie Polska
Stowarzyszenie Polska Grupa Białaczkowa Dorosłych email: palg@io.gliwice.pl tel.: +48 32 278-8523, -8529, fax: +48 32 278-8524 PROGRAM KONFERENCJI PALG - PLRG - PSH 8-9 listopada 2013 Stowarzyszenie Polska
INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII SKŁODOWSKIEJ-CURIE, ODDZIALE W GLIWICACH
 KLINIKA TRANSPLANTACJI SZPIKU I ONKOHEMATOLOGII /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE
KLINIKA TRANSPLANTACJI SZPIKU I ONKOHEMATOLOGII /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE
Leczenie chłoniaków nieziarniczych zakwalifikowanych do kodu ICD-10 C84 przy wykorzystaniu produktu leczniczego MabThera (rytuksymab)
 Agencja Oceny Technologii Medycznych Wydział Oceny Technologii Medycznych Leczenie chłoniaków nieziarniczych zakwalifikowanych do kodu ICD-10 C84 przy wykorzystaniu produktu leczniczego MabThera (rytuksymab)
Agencja Oceny Technologii Medycznych Wydział Oceny Technologii Medycznych Leczenie chłoniaków nieziarniczych zakwalifikowanych do kodu ICD-10 C84 przy wykorzystaniu produktu leczniczego MabThera (rytuksymab)
INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII SKŁODOWSKIEJ-CURIE, ODDZIALE W GLIWICACH
 I KLINIKA RADIOTERAPII I CHEMIOTERAPII /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII
I KLINIKA RADIOTERAPII I CHEMIOTERAPII /komórka organizacyjna/ Załącznik do Zarządzenia Nr 25/2014 z dnia 20.06.2014 INFORMACJA O BADANIACH KLINICZNYCH PROWADZONYCH W CENTRUM ONKOLOGII INSTYTUCIE IM. MARII
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 162/2014 z dnia 30 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia z wykazu świadczeń gwarantowanych
Agencja Oceny Technologii Medycznych www.aotm.gov.pl Rekomendacja nr 162/2014 z dnia 30 czerwca 2014 r. Prezesa Agencji Oceny Technologii Medycznych w sprawie usunięcia z wykazu świadczeń gwarantowanych
Aneks. Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków
 Aneks Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Produkt leczniczy Folotyn roztwór
Aneks Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję Leków Produkt leczniczy Folotyn roztwór
S T R E S Z C Z E N I E
 STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
STRESZCZENIE Cel pracy: Celem pracy jest ocena wyników leczenia napromienianiem chorych z rozpoznaniem raka szyjki macicy w Świętokrzyskim Centrum Onkologii, porównanie wyników leczenia chorych napromienianych
Rysunek. Układ Limfatyczny.
 Informacja dotyczy chłoniaka rozlanego z dużych komórek B, będącego odmianą chłoniaka nieziarniczego. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest częścią systemu
Informacja dotyczy chłoniaka rozlanego z dużych komórek B, będącego odmianą chłoniaka nieziarniczego. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest częścią systemu
Personalizacja leczenia w hematoonkologii dziecięcej
 MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
MedTrends 2016 Europejskie Forum Nowoczesnej Ochrony Zdrowia Zabrze, 18-19 marca 2016 r. Personalizacja leczenia w hematoonkologii dziecięcej Prof. dr hab. n. med. Tomasz Szczepański Katedra i Klinika
