ostrym reumatoidalnym zapaleniem stawów (choroba powodująca stan zapalny stawów), gdzie produkt MabThera podaje się dożylnie z metotreksatem;
|
|
|
- Jan Lis
- 9 lat temu
- Przeglądów:
Transkrypt
1 EMA/614203/2010 EMEA/H/C/ Streszczenie EPAR dla ogółu społeczeństwa rytuksymab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia, jak Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) ocenił lek w celu ustalenia opinii, na podstawie której przyznano pozwolenie na dopuszczenie produktu do obrotu, oraz zaleceń w sprawie stosowania leku. Co to jest lek? Produkt jest lekiem zawierającym substancję czynną rytuksymab. Lek jest dostępny w postaci koncentratu do sporządzania roztworu do wlewu dożylnego oraz w postaci roztworu do podawania podskórnego. W jakim celu stosuje się lek? Produkt stosuje się w leczeniu osób dorosłych z: dwiema postaciami chłoniaka nieziarniczego (nowotwór tkanki limfatycznej) zwanego chłoniakiem grudkowym i rozproszoną postacią grudkowego B-komórkowego chłoniaka nieziarniczego. Produkt można stosować w monoterapii lub w skojarzeniu z chemioterapią (leki przeciwnowotworowe). Lek można podawać w postaci zastrzyku dożylnego lub podskórnego; przewlekłą białaczką limfatyczną (PBL nowotwór limfocytów B: rodzaj krwinek białych), gdzie produkt stosuje się w skojarzeniu z chemioterapią; ostrym reumatoidalnym zapaleniem stawów (choroba powodująca stan zapalny stawów), gdzie produkt podaje się dożylnie z metotreksatem; dwiema postaciami ostrego zapalenia naczyń (zapalenie małej lub średniej wielkości naczyń krwionośnych) zwane ziarniniakowatością z zapaleniem naczyń (inaczej GPA lub ziarniniakiem Wegenera) oraz mikroskopowym zapaleniem naczyń (MPA). Produkt podaje się dożylnie z lekami zwanymi kortykosteroidami. 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom Telephone +44 (0) Facsimile +44 (0) info@ema.europa.eu Website An agency of the European Union European Medicines Agency, Reproduction is authorised provided the source is acknowledged.
2 Lek wydaje się wyłącznie z przepisu lekarza. Jak stosować produkt? Produkt należy podawać pod ścisłym nadzorem doświadczonego personelu medycznego. Produkt zawsze podaje się w otoczeniu wyposażonym w urządzenia umożliwiające natychmiastową reanimację pacjenta. W przypadku stosowania w skojarzeniu z chemioterapią lek podaje się pierwszego dnia każdego cyklu chemioterapii. Przed każdym wlewem dożylnym pacjentom należy podać zapobiegający wystąpieniu reakcji alergicznych lek przeciwhistaminowy (zapobiegający reakcjom alergicznym) oraz przeciwgorączkowy. W ramach leczenia pacjenci mogą także wymagać podania kortykosteroidu. W leczeniu chłoniaka nieziarniczego typowa dawka leku podawana dożylnie wynosi 375 mg na metr kwadratowy powierzchni ciała (obliczona na podstawie wzrostu i masy ciała pacjenta). Liczba i częstość wlewów dożylnych zależy od typu leczonego chłoniaka. Niektórzy pacjenci, którzy otrzymali jedną pełną dawkę we wlewie dożylnym mogą otrzymać kolejne dawki w postaci zastrzyku podskórnego. Zalecana dawka zastrzyku podskórnego wynosi mg, niezależnie od powierzchni ciała pacjenta. W PBL produkt podaje się w sześciokrotnie podskórnie: pierwsza dawka wynosi 375 mg/m 2, a pozostałe dawki 500 mg/m 2. Aby zapobiec wystąpieniu działań niepożądanych związanych z rozpadem nowotworowych limfocytów, przed rozpoczęciem leczenia pacjentów należy dobrze nawodnić i podawać im leki pomagające w stabilizacji poziomu kwasu moczowego. W reumatoidalnym zapaleniu stawów produkt podaje się w dwóch wlewach dożylnych po 1000 mg wykonywanych w odstępie dwutygodniowym. U większości pacjentów na odpowiedź trzeba czekać od 16 do 24 tygodni od leczenia wstępnego. Po upływie 24 tygodni leczenie można powtórzyć, w zależności od odpowiedzi obserwowanej u danego pacjenta. Pacjentom, którzy otrzymują lek w leczeniu reumatoidalnego zapalenia stawów oraz GPA/MPA, należy przekazać specjalną kartę, która zawiera wyjaśnienie objawów niektórych rodzajów zakażeń mogących wystąpić jako działania niepożądane związane ze stosowaniem leku, oraz instrukcje dla pacjentów dotyczące konieczności natychmiastowego zgłoszenia się do lekarza w przypadku wystąpienia tych objawów. Szczegółowe informacje znajdują się w charakterystyce produktu leczniczego (także część EPAR). W przypadku GPA i MPA produkt podaje się we wlewie dożylnym w dawce 375 mg/m 2 raz na tydzień przez 4 tygodnie. Jak działa produkt? Substancja czynna leku, rytuksymab, jest przeciwciałem monoklonalnym. Przeciwciało monoklonalne to przeciwciało (typ białka), które zostało zaprojektowane w taki sposób, aby rozpoznawało określone struktury (zwane antygenami), występujące na określonych komórkach organizmu, oraz wiązało się z tymi strukturami. Rytuksymab został opracowany w taki sposób, aby wiązał się z występującym na powierzchni limfocytów B antygenem CD20. Gdy rytuksymab wiąże się z antygenem, powoduje to śmierć komórki. Jest to korzystne w przypadku chłoniaka i PBL, gdyż niszczone są nowotworowe limfocyty B. W reumatoidalnym zapaleniu stawów limfocyty B są niszczone w stawach, co pomaga złagodzić stan zapalny. W przypadku GPA i MPA zniszczenie limfocytów B zmniejsza wytwarzanie przeciwciał przeciw cytoplazmie neutrofilów (ANCA), które uważa się za przeciwciała odgrywające ważną rolę w atakowaniu naczyń krwionośnych, oraz zmniejsza stan zapalny. EMA/76051/2014 Strona 2/5
3 Jak badano produkt? Lek badano w obu typach chłoniaka nieziarniczego: w chłoniaku grudkowym lek oceniano w jednym badaniu głównym z udziałem 322 pacjentów, u których chłoniak grudkowy nie był wcześniej leczony. W badaniu tym oceniano skuteczność dołączenia leku do standardowej chemioterapii (CVP: cyklofosfamid, winkrystyna i prednizolon), mierząc czas przeżycia pacjentów bez nawrotu choroby. W trzech kolejnych badaniach z opublikowanej literatury naukowej oceniano wpływ dołączenia leku do innych typów chemioterapii. W trzech badaniach oceniano także lek przyjmowany w monoterapii: w jednym badaniu oceniano ogólną częstość odpowiedzi na lek u 203 pacjentów po niepowodzeniu wcześniejszego leczenia, natomiast dwa kolejne badania stanowiły leczenie podtrzymujące obejmujące łącznie 1353 pacjentów (334 pacjentów, u których wystąpił nawrót choroby po wcześniejszym leczeniu oraz 1019 pacjentów uprzednio nieleczonych), w których mierzono czas przeżycia pacjentów do ponownego nasilenia choroby. Ponadto lek podawany podskórnie porównywano z produktem podawanym dożylnie w badaniu z udziałem 127 pacjentów z chłoniakiem grudkowym. Produkt podano przed zastosowaniem leczenia określanego jako CHOP (cyklofosfamid, doksorubicyna, winkrystyna i prednizolon) albo chemioterapią CVP. W przypadku podawania podskórnego i dożylnego główne kryterium oceny skuteczności oparto na stężeniu rytuksymabu we krwi w celu wykazania, że osiągnięto odpowiednie stężenia. W badaniu pod uwagę brano również odsetek pacjentów z całkowitą lub częściową odpowiedzią na leczenie. Odpowiedź na leczenie oceniono za pomocą obrazowania ciała i danych klinicznych pacjentów. w rozsianym chłoniaku z limfocytów B skuteczność dołączenia leku do chemioterapii CHOP oceniano w badaniu z udziałem 399 pacjentów w wieku powyżej 60. roku życia. Głównym kryterium oceny skuteczności był czas przeżycia pacjentów bez wystąpienia nasilenia choroby lub bez konieczności zmiany leczenia. W PBL skuteczność dołączenia leku do chemioterapii FC (fludarabina i cyklofosfamid) oceniano w badaniu z udziałem 817 pacjentów, którzy nie otrzymywali wcześniej leczenia, i u 552 pacjentów, u których wystąpił nawrót choroby po wcześniejszym leczeniu. Głównym kryterium oceny skuteczności był czas przeżycia pacjentów bez nasilenia choroby. W dodatkowych badaniach z opublikowanej literatury naukowej oceniano wpływ dołączenia leku do innych typów chemioterapii. W reumatoidalnym zapaleniu stawów lek oceniano u 517 pacjentów. Skuteczność dołączenia produktu do metotreksatu porównywano ze skutecznością zaobserwowaną po dołączeniu placebo. W badaniu tym określano, u jakiej liczby pacjentów po 24 tygodniach wystąpiła poprawa o 20% pod kątem głównych objawów reumatoidalnego zapalenia stawów. W przypadku GPA i MPA lek porównywano do cyklofosfamidu innego leku stosowanego w leczeniu zapalenia naczyń krwionośnych, w pojedynczym badaniu trwającym 18 miesięcy z udziałem 198 dotychczas nieleczonych lub wcześniej leczonych pacjentów (spośród których ok. trzy czwarte cierpiało na GPA). Głównym kryterium oceny skuteczności leku była liczba pacjentów niewykazujących żadnych objawów choroby (remisja całkowita), którzy nie wymagali dalszego leczenia z użyciem kortykosteroidów, w ciągu 6 miesięcy od rozpoczęcia badania. Jakie korzyści ze stosowania produktu zaobserwowano w badaniach? W chłoniaku nieziarniczym pacjenci przyjmujący lek uzyskiwali lepsze wyniki leczenia niż pacjenci nieleczeni tym produktem: EMA/76051/2014 Strona 3/5
4 w chłoniaku grudkowym u pacjentów przyjmujących lek w skojarzeniu z chemioterapią CVP czas przeżycia bez wystąpienia nawrotu choroby wynosił średnio 25,9 miesiąca w porównaniu z 6,7 miesiąca u pacjentów otrzymujących jedynie chemioterapię CVP. Trzy dodatkowe badania także wykazały, że dołączenie leku do innych typów chemioterapii poprawia wyniki leczenia pacjentów. W badaniach nad lekiem stosowanym w monoterapii odpowiedź na lek zaobserwowano u 48% pacjentów po niepowodzeniu wcześniejszego leczenia. Badanie leczenia podtrzymującego wykazało, że u pacjentów otrzymujących lek czas przeżycia bez nasilenia choroby wynosił średnio 42,2 miesiąca w porównaniu z 14,3 miesiąca u pacjentów, którzy nie otrzymywali tego leku. Badanie leczenia podtrzymującego u uprzednio nieleczonych pacjentów wykazało zaś, że prawdopodobieństwo nasilenia choroby udało się zmniejszyć o 50% u pacjentów leczonych z użyciem leku ; W przypadku podskórnego podawania leku stężenie substancji czynnej porównywano ze stężeniem produktu podawanego dożylnie. Odsetek odpowiedzi pacjentów, którzy otrzymywali produkt podskórnie był podobny do odsetka pacjentów, którzy otrzymywali produkt dożylnie. w rozproszonej postaci grudkowego B-komórkowego chłoniaka nieziarniczego u pacjentów, u których dołączono lek do chemioterapii CHOP czas przeżycia bez nasilenia choroby lub bez konieczności zmiany leczenia wynosił średnio 35 miesięcy wobec przeciętnej 13 miesięcy u pacjentów, którzy otrzymywali jedynie chemioterapię CHOP. W przypadku PBL pacjenci także uzyskiwali lepsze wyniki leczenia podczas przyjmowania leku. U pacjentów, którzy nie byli wcześniej leczeni, czas przeżycia bez wystąpienia nasilenia choroby wynosił średnio 39,8 miesiąca podczas przyjmowania leku dołączonego do chemioterapii FC w porównaniu z 32,2 miesiąca u pacjentów otrzymujących jedynie chemioterapię FC. U pacjentów z nawrotem choroby po wcześniejszym leczeniu czas przeżycia bez wystąpienia nasilenia choroby wynosił 30,6 miesiąca podczas przyjmowania dodatkowo leku w porównaniu z 20,6 miesiąca u pacjentów otrzymujących jedynie chemioterapię FC. Dodatkowe badania również wykazały, że dołączenie leku do innych typów chemioterapii także prowadziło do poprawy wyników leczenia u pacjentów z PBL. W reumatoidalnym zapaleniu stawów lek był skuteczniejszy niż placebo: poprawa objawów wystąpiła u 51% pacjentów otrzymujących lek, w porównaniu z 18% pacjentów otrzymujących placebo. W przypadku GPA i MPA 64% pacjentów przyjmujących lek (63 z 98) doznało całkowitej remisji po 6 miesiącach, w porównaniu z 55% pacjentów przyjmujących cyklofosfamid (52 z 95). Jakie ryzyko wiąże się ze stosowaniem produktu? W przypadku leczenia chłoniaka nieziarniczego lub PBL najczęstsze działania niepożądane związane ze stosowaniem leku (obserwowane u więcej niż 1 na 10 pacjentów) to: zakażenia bakteryjne i wirusowe, zapalenie oskrzeli (zapalenie dróg oddechowych w płucach), neutropenia (niski poziom krwinek białych obojętnochłonnych rodzaj białych krwinek), leukopenia (niski poziom białych krwinek), neutropenia z gorączką, trombocytopenia (niski poziom płytek krwi), reakcje na wlew (głównie gorączka, dreszcze i uczucie zimna), obrzęk naczynioworuchowy (spuchnięcie pod skórą), nudności (mdłości), świąd, wysypka, łysienie, gorączka, dreszcze, astenia (osłabienie), ból głowy i obniżony poziom IgG (rodzaj przeciwciała). Z kolei najczęstsze działanie niepożądane przy stosowaniu do leczenia reumatoidalnego zapalenia stawów (obserwowane u więcej niż 1 na 10 pacjentów) obejmowało: bóle głowy, zakażenia górnych dróg oddechowych (przeziębienia), zakażenia układu moczowego, tj. infekcje przewodów moczowych i reakcje towarzyszące wlewom dożylnym. EMA/76051/2014 Strona 4/5
5 W przypadku stosowania z GPA lub MPA najczęstsze działania niepożądane (obserwowane u więcej niż 1 na 10 pacjentów) to: biegunka, obrzęk obwodowy (obrzęk kostek i nóg), skurcze mięśni, bóle stawów i pleców, zawroty głowy, drżenia, duszności, krwawienie z nosa oraz nadciśnienie. Niektóre z tych objawów mogą mieć związek z wlewem. W badaniu porównującym produkt podawany podskórnie lub dożylnie działania niepożądane były porównywalne z wyjątkiem reakcji wokół miejsca wstrzyknięcia (ból, swędzenie, wysypka), które występowały częściej w przypadku podawania podskórnego. Pełny wykaz działań niepożądanych związanych ze stosowaniem leku znajduje się w ulotce dla pacjenta. Leku nie wolno stosować u osób, u których występuje nadwrażliwość (alergia) na rytuksymab, białka myszy lub którykolwiek składnik leku. Leku do stosowania podskórnego nie wolno również stosować u pacjentów z alergią na substancję o nazwie hialuronidaza. Leku nie wolno stosować u pacjentów z czynnym ostrym zakażeniem lub poważnie osłabionym systemem odpornościowym. Ponadto produktu nie wolno podawać pacjentom z reumatoidalnym zapaleniem stawów, GPA lub MPA, jeżeli występuje u nich ciężka niewydolność serca (kiedy serce nie jest w stanie pompować odpowiedniej ilości krwi w organizmie) lub poważna choroba serca. Na jakiej podstawie zatwierdzono produkt? Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) uznał, że korzyści ze stosowania produktu przewyższają związane z tym ryzyko, i zalecił przyznanie pozwolenia na dopuszczenie leku do obrotu. Inne informacje dotyczące produktu : W dniu 2 czerwca 1998 r. Komisja Europejska przyznała pozwolenie na dopuszczenie produktu do obrotu ważne w całej Unii Europejskiej. Pełne sprawozdanie EPAR dotyczące leku znajduje się na stronie internetowej Agencji pod adresem: ema.europa.eu/find medicine/human medicines/european Public Assessment Reports. W celu uzyskania dodatkowych informacji dotyczących leczenia produktem należy zapoznać się z ulotką dla pacjenta (także część EPAR) bądź skontaktować się z lekarzem lub farmaceutą. Data ostatniej aktualizacji: EMA/76051/2014 Strona 5/5
Simponi jest lekiem o działaniu przeciwzapalnym. Preparat stosuje się w leczeniu następujących chorób u osób dorosłych:
 EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
EMA/411054/2015 EMEA/H/C/000992 Streszczenie EPAR dla ogółu społeczeństwa golimumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
czerniak (nowotwór skóry), który rozprzestrzenił się lub którego nie można usunąć chirurgicznie;
 EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/524789/2017 EMEA/H/C/003820 Streszczenie EPAR dla ogółu społeczeństwa pembrolizumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
EMA/115257/2019 EMEA/H/C/000992 Przegląd wiedzy na temat leku Simponi i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Simponi i w jakim celu się go stosuje Simponi jest
zaawansowanym rakiem nerkowokomórkowym, rodzajem raka nerki, u pacjentów, którzy byli wcześniej leczeni lekami przeciwnowotworowymi;
 EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/303208/2017 EMEA/H/C/003985 Streszczenie EPAR dla ogółu społeczeństwa niwolumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
W szpiczaku mnogim, nowotworze pewnego typu białych krwinek zwanych komórkami plazmatycznymi, Revlimid stosuje się:
 EMA/113870/2017 EMEA/H/C/000717 Streszczenie EPAR dla ogółu społeczeństwa lenalidomid Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/113870/2017 EMEA/H/C/000717 Streszczenie EPAR dla ogółu społeczeństwa lenalidomid Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Keytruda (pembrolizumab)
 EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
EMA/235911/2019 EMEA/H/C/003820 Przegląd wiedzy na temat leku Keytruda i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Keytruda i w jakim celu się go stosuje Keytruda
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
EMA/489091/2018 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest
Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
EMA/55246/2019 EMEA/H/C/003985 Przegląd wiedzy na temat leku Opdivo i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Opdivo i w jakim celu się go stosuje Opdivo jest lekiem
Lek Avastin stosuje się u osób dorosłych w leczeniu następujących rodzajów nowotworów w skojarzeniu z innymi lekami przeciwnowotworowymi:
 EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/175824/2015 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
zaawansowany rak nerki lub rak nerki z przerzutami, w skojarzeniu z interferonem alfa-2a;
 EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/302947/2017 EMEA/H/C/000582 Streszczenie EPAR dla ogółu społeczeństwa bewacyzumab Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Revolade. eltrombopag. Co to jest Revolade? W jakim celu stosuje się produkt Revolade? Streszczenie EPAR dla ogółu społeczeństwa
 EMA/33466/2016 EMEA/H/C/001110 Streszczenie EPAR dla ogółu społeczeństwa eltrombopag Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
EMA/33466/2016 EMEA/H/C/001110 Streszczenie EPAR dla ogółu społeczeństwa eltrombopag Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku. Wyjaśnia,
Pradaxa jest lekiem zawierającym substancję czynną eteksylan dabigatranu. Lek jest dostępny w postaci kapsułek (75, 110 i 150 mg).
 EMA/47517/2015 EMEA/H/C/000829 Streszczenie EPAR dla ogółu społeczeństwa eteksylan dabigatranu Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego
EMA/47517/2015 EMEA/H/C/000829 Streszczenie EPAR dla ogółu społeczeństwa eteksylan dabigatranu Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego
szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana)
 EMA/90006/2015 EMEA/H/C/001104 Streszczenie EPAR dla ogółu społeczeństwa szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana) Niniejszy dokument jest streszczeniem
EMA/90006/2015 EMEA/H/C/001104 Streszczenie EPAR dla ogółu społeczeństwa szczepionka przeciw pneumokokom polisacharydowa, skoniugowana (13- walentna, adsorbowana) Niniejszy dokument jest streszczeniem
zaburzeniem widzenia spowodowanym obrzękiem plamki wywołanym cukrzycą;
 EMA/677928/2015 EMEA/H/C/002392 Streszczenie EPAR dla ogółu społeczeństwa aflibercept Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
EMA/677928/2015 EMEA/H/C/002392 Streszczenie EPAR dla ogółu społeczeństwa aflibercept Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego leku.
Ulotka dołączona do opakowania: informacja dla użytkownika. Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
EMA/481361/2018 EMEA/H/C/002392 Przegląd wiedzy na temat leku Eylea i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Eylea i w jakim celu się go stosuje Eylea jest lekiem
Leki, zarejestrowane i stosowane aktualnie w krajach UE do leczenia onkologicznego i Stwardnienia Guzowatego.
 Leki, zarejestrowane i stosowane aktualnie w krajach UE do leczenia onkologicznego i Stwardnienia Guzowatego. Afinitor Ewerolumis Streszczenie EPAR dla ogółu społeczeństwa Niniejszy dokument stanowi streszczenie
Leki, zarejestrowane i stosowane aktualnie w krajach UE do leczenia onkologicznego i Stwardnienia Guzowatego. Afinitor Ewerolumis Streszczenie EPAR dla ogółu społeczeństwa Niniejszy dokument stanowi streszczenie
Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek przeciwcukrzycowy Suliqua
 19 stycznia 2017 r. EMA/747766/2016 Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek Środki mające na celu zmniejszenie ryzyka pomylenia dwóch wstrzykiwaczy o różnej mocy
19 stycznia 2017 r. EMA/747766/2016 Materiały edukacyjne dla pracowników służby zdrowia i pacjentów stosujących lek Środki mające na celu zmniejszenie ryzyka pomylenia dwóch wstrzykiwaczy o różnej mocy
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 25 January 2018 EMA/PRAC/35597/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
25 January 2018 EMA/PRAC/35597/2018 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Wyniki procedur na mocy art. 20 rozporządzenia (WE) nr 726/2004 oraz art. 31 dyrektywy 2001/83/WE
 28 lutego 2013 r. EMA/136606/2013 wer.1 EMEA/H/A-31/1333 EMEA/H/C/000604/A20/45 EMEA/H/C/000622/A20/60 EMEA/H/C/000674/A20/52 Pytania i odpowiedzi dotyczące ponownej oceny monowalentnych i poliwalentnych
28 lutego 2013 r. EMA/136606/2013 wer.1 EMEA/H/A-31/1333 EMEA/H/C/000604/A20/45 EMEA/H/C/000622/A20/60 EMEA/H/C/000674/A20/52 Pytania i odpowiedzi dotyczące ponownej oceny monowalentnych i poliwalentnych
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 764 Poz. 86 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.
 Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 765 Poz. 42 Załącznik B.75. LECZENIE AKTYWNEJ POSTACI ZIARNINIAKOWATOŚCI Z ZAPALENIEM NACZYŃ (GPA) LUB MIKROSKOPOWEGO ZAPALENIA NACZYŃ (MPA) (ICD-10 M31.3, M 31.8) ŚWIADCZENIOBIORCY
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 10 November 2016 EMA/PRAC/730052/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
10 November 2016 EMA/PRAC/730052/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri
 25/04/2016 EMA/266665/2016 EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri U pacjentów z grupy zwiększonego
25/04/2016 EMA/266665/2016 EMA potwierdza zalecenia mające na celu jak największe ograniczenie ryzyka wystąpienia zakażenia mózgu PML w trakcie stosowania leku Tysabri U pacjentów z grupy zwiększonego
Aneks II Zmiany w drukach informacyjnych produktów leczniczych zarejestrowanych w procedurze narodowej
 Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Aktualizacja ChPL i ulotki dla produktów leczniczych zawierających jako substancję czynną immunoglobulinę anty-t limfocytarną pochodzenia króliczego stosowaną u ludzi [rabbit anti-human thymocyte] (proszek
Rysunek. Układ limfatyczny.
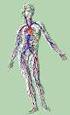 Informacja dotyczy chłoniaka grudkowego, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu odpornościowego
Informacja dotyczy chłoniaka grudkowego, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu odpornościowego
Aneks IV. Wnioski naukowe
 Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Aneks IV Wnioski naukowe 1 Wnioski naukowe W dniu 10 marca 2016 r. Komisja Europejska została poinformowana, że niezależna grupa monitorowania danych dotyczących bezpieczeństwa zaobserwowała w trzech badaniach
Nowe możliwości leczenia ostrej białaczki limfoblastycznej
 Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Nowe możliwości leczenia ostrej białaczki limfoblastycznej Dr hab. med. Grzegorz W. Basak Katedra i Klinika Hematologii, Onkologii i Chorób Wewnętrznych Warszawski Uniwersytet Medyczny Warszawa, 17.12.15
Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu
 Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu Zmiany mają przede wszystkim na celu zmniejszenie ryzyka neurologicznych działań niepożądanych Komitet ds. Produktów Leczniczych Stosowanych
Europejska Agencja Leków potwierdza zmiany w stosowaniu metoklopramidu Zmiany mają przede wszystkim na celu zmniejszenie ryzyka neurologicznych działań niepożądanych Komitet ds. Produktów Leczniczych Stosowanych
Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie
 brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
brygatynib Informacje dla pacjenta i fachowych pracowników ochrony zdrowia zaangażowanych w opiekę medyczną lub leczenie Imię i nazwisko pacjenta: Dane lekarza (który przepisał lek Alunbrig ): Numer telefonu
Przewodnik użytkownika raportu internetowego
 Ochrona zdrowia pacjentów zawiera informacje dotyczące elementów składowych danych, układu, interpretacji i funkcji w raporcie internetowym. 1. Elementy składowe danych... 2 2. Dodatkowe informacje dotyczące
Ochrona zdrowia pacjentów zawiera informacje dotyczące elementów składowych danych, układu, interpretacji i funkcji w raporcie internetowym. 1. Elementy składowe danych... 2 2. Dodatkowe informacje dotyczące
KEYTRUDA (pembrolizumab)
 Poradnik dotyczący leku KEYTRUDA (pembrolizumab) Informacja dla Pacjentów Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie.
Poradnik dotyczący leku KEYTRUDA (pembrolizumab) Informacja dla Pacjentów Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie.
Ograniczenia stosowania leków zawierających domperidon
 1 września 2014 r. EMA/465179/2014 W dniu 23 kwietnia 2014 r. grupa koordynacyjna ds. procedur wzajemnego uznania i zdecentralizowanej produkty stosowane u ludzi (CMDh) zatwierdziła nowe zalecenia o ograniczeniu
1 września 2014 r. EMA/465179/2014 W dniu 23 kwietnia 2014 r. grupa koordynacyjna ds. procedur wzajemnego uznania i zdecentralizowanej produkty stosowane u ludzi (CMDh) zatwierdziła nowe zalecenia o ograniczeniu
Lek BI w porównaniu z lekiem Humira u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą
 Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Lek w porównaniu z lekiem u pacjentów z umiarkowaną lub ciężką łuszczycą plackowatą Jest to podsumowanie badania klinicznego dotyczącego łuszczycy plackowatej. Podsumowanie sporządzono dla ogółu społeczeństwa.
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Białaczka limfatyczna
 www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
www.oncoindex.org SUBSTANCJE CZYNNE W LECZENIU: Białaczka limfatyczna OBEJMUJE PRZEWLEKŁĄ BIAŁACZKĘ LIMFOCYTOWĄ (PBL) I OSTRĄ BIAŁACZKĘ LIMFOBLASTYCZNĄ (ALL) Clofarabine Leczenie ostrej białaczki limfoblastycznej
Rysunek. Układ limfatyczny.
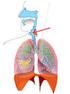 Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
Informacja dotyczy rodzaju chłoniaka nieziarniczego zwanego chłoniakiem z małych limfocytów B. Warto również przeczytać informacje na temat przewlekłej białaczki limfocytowej (CLL), która jest podobnym
chorych na ITP Krzysztof Chojnowski Warszawa, 27 listopada 2009 r.
 Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Współczesne leczenie chorych na ITP Krzysztof Chojnowski Klinika Hematologii UM w Łodzi Warszawa, 27 listopada 2009 r. Dlaczego wybór postępowania u chorych na ITP może być trudny? Choroba heterogenna,
Aneks III. Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Aneks III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja zmian w charakterystyce produktu leczniczego i ulotce
Ulotka dołączona do opakowania: informacja dla użytkownika. MabThera 100 mg koncentrat do sporządzania roztworu do infuzji rytuksymab
 Ulotka dołączona do opakowania: informacja dla użytkownika MabThera 100 mg koncentrat do sporządzania roztworu do infuzji rytuksymab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
Ulotka dołączona do opakowania: informacja dla użytkownika MabThera 100 mg koncentrat do sporządzania roztworu do infuzji rytuksymab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
Ulotka dołączona do opakowania: informacja dla użytkownika. Truxima 500 mg koncentrat do sporządzania roztworu do infuzji rytuksymab
 Ulotka dołączona do opakowania: informacja dla użytkownika Truxima 500 mg koncentrat do sporządzania roztworu do infuzji rytuksymab ^^Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi
Ulotka dołączona do opakowania: informacja dla użytkownika Truxima 500 mg koncentrat do sporządzania roztworu do infuzji rytuksymab ^^Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 9/2012 z dnia 27 lutego 2012 w zakresie zmiany sposobu finansowania świadczenia gwarantowanego Leczenie chłoniaków
Agencja Oceny Technologii Medycznych Rada Przejrzystości Stanowisko Rady Przejrzystości nr 9/2012 z dnia 27 lutego 2012 w zakresie zmiany sposobu finansowania świadczenia gwarantowanego Leczenie chłoniaków
Lek Riximyo spowalnia powodowane przez proces zapalny uszkodzenie stawów i poprawia zdolność codziennej aktywności.
 Ulotka dołączona do opakowania: informacja dla użytkownika Riximyo 100 mg koncentrat do sporządzania roztworu do infuzji Riximyo 500 mg koncentrat do sporządzania roztworu do infuzji rytuksymab Niniejszy
Ulotka dołączona do opakowania: informacja dla użytkownika Riximyo 100 mg koncentrat do sporządzania roztworu do infuzji Riximyo 500 mg koncentrat do sporządzania roztworu do infuzji rytuksymab Niniejszy
Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie
 23 April 2015 EMA/PRAC/273915/2015 Pharmacovigilance Risk Assessment Committee Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte na posiedzeniu PRAC w dniach 7 10 kwietnia
23 April 2015 EMA/PRAC/273915/2015 Pharmacovigilance Risk Assessment Committee Zalecenia PRAC dotyczące przesłanek do aktualizacji informacji o produkcie Przyjęte na posiedzeniu PRAC w dniach 7 10 kwietnia
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
KEYTRUDA (pembrolizumab)
 Poradnik dotyczący leku KEYTRUDA (pembrolizumab) Informacja dla Pacjentów Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie.
Poradnik dotyczący leku KEYTRUDA (pembrolizumab) Informacja dla Pacjentów Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi to szybkie zidentyfikowanie nowych informacji o bezpieczeństwie.
Przegląd wiedzy na temat leku Metacam i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Przegląd wiedzy na temat leku Metacam i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Metacam i w jakim celu się go stosuje? Metacam
EMA/CVMP/259397/2006 EMEA/V/C/000033 Przegląd wiedzy na temat leku Metacam i uzasadnienie udzielenia Pozwolenia na dopuszczenie do obrotu w UE Co to jest lek Metacam i w jakim celu się go stosuje? Metacam
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta
 ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
ANEKS III Zmiany w odpowiednich punktach charakterystyki produktu leczniczego i ulotki dla pacjenta Uwaga: Konieczna może być późniejsza aktualizacja charakterystyki produktu leczniczego i ulotki dla pacjenta
Metacam. meloksykam. Co to jest produkt Metacam i w jakim celu się go stosuje? Streszczenie EPAR dla ogółu społeczeństwa
 EMA/CVMP/259397/2006 EMEA/V/C/000033 Streszczenie EPAR dla ogółu społeczeństwa meloksykam Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
EMA/CVMP/259397/2006 EMEA/V/C/000033 Streszczenie EPAR dla ogółu społeczeństwa meloksykam Niniejszy dokument jest streszczeniem Europejskiego Publicznego Sprawozdania Oceniającego (EPAR) dotyczącego produktu.
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL
 PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO Szanowny Farmaceuto, Należy
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY A. Leczenie infliksymabem 1. Leczenie choroby Leśniowskiego-Crohna (chlc)
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Neupogen 300 µg/ml (30 mln j.m./ml) roztwór do wstrzykiwań Neupogen 300 µg/ml (48 mln j.m./1,6 ml) roztwór do wstrzykiwań (Filgrastimum) Należy zapoznać
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Neupogen 300 µg/ml (30 mln j.m./ml) roztwór do wstrzykiwań Neupogen 300 µg/ml (48 mln j.m./1,6 ml) roztwór do wstrzykiwań (Filgrastimum) Należy zapoznać
VI.2 Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego Bendamustine Actavis przeznaczone do publicznej wiadomości
 VI.2 Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego Bendamustine Actavis przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Przewlekła białaczka
VI.2 Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego Bendamustine Actavis przeznaczone do publicznej wiadomości VI.2.1 Omówienie rozpowszechnienia choroby Przewlekła białaczka
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Rysunek. Układ limfatyczny.
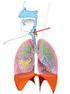 Poniższa informacja dotyczy rodzaju chłoniaka nieziarniczego, zwanego chłoniakiem anaplastycznym z dużych komórek. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest
Poniższa informacja dotyczy rodzaju chłoniaka nieziarniczego, zwanego chłoniakiem anaplastycznym z dużych komórek. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest
Poradnik dotyczący interpretacji spontanicznych zgłoszeń przypadków podejrzewanych działań niepożądanych leków
 30 styczeń 2017 r. Wydział ds. inspekcji, nadzoru nad bezpieczeństwem stosowania produktów leczniczych u ludzi i komisji EMA/749446/2016 Zmiana nr 1* Poradnik dotyczący interpretacji spontanicznych zgłoszeń
30 styczeń 2017 r. Wydział ds. inspekcji, nadzoru nad bezpieczeństwem stosowania produktów leczniczych u ludzi i komisji EMA/749446/2016 Zmiana nr 1* Poradnik dotyczący interpretacji spontanicznych zgłoszeń
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 15 September 2016 EMA/PRAC/603539/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
15 September 2016 EMA/PRAC/603539/2016 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęte na posiedzeniu PRAC w dniach
Notyfikacja nr EMA/CHMP/188871/2015 z dnia 27.03.2015 zmiana EMEA/H/C/002221/IB/0019/G Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Dacogen 50 mg proszek do sporządzania koncentratu roztworu do infuzji Decytabina Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi
Ulotka dołączona do opakowania: informacja dla użytkownika Dacogen 50 mg proszek do sporządzania koncentratu roztworu do infuzji Decytabina Niniejszy produkt leczniczy będzie dodatkowo monitorowany. Umożliwi
Annex I. Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia
 Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
Annex I Podsumowanie naukowe i uzasadnienie dla wprowadzenia zmiany w warunkach pozwolenia Podsumowanie naukowe Biorąc pod uwagę Raport oceniający komitetu PRAC dotyczący Okresowego Raportu o Bezpieczeństwie
Podsumowanie u zarządzania rzyzkiem dla produktu leczniczego Cartexan przeznaczone do publicznej wiadomości
 Podsumowanie u zarządzania rzyzkiem dla produktu leczniczego Cartexan przeznaczone do publicznej wiadomości Omówienie rozpowszechnienia choroby Rosnąca oczekiwana długość życia i starzejące się społeczeństwo
Podsumowanie u zarządzania rzyzkiem dla produktu leczniczego Cartexan przeznaczone do publicznej wiadomości Omówienie rozpowszechnienia choroby Rosnąca oczekiwana długość życia i starzejące się społeczeństwo
Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń
 17 December 2015 EMA/PRAC/835763/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęto w dniach od 30 listopada
17 December 2015 EMA/PRAC/835763/2015 Pharmacovigilance Risk Assessment Committee (PRAC) Nowa treść informacji o produkcie fragmenty zaleceń PRAC dotyczących zgłoszeń Przyjęto w dniach od 30 listopada
LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50)
 Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Załącznik B.32. LECZENIE CHOROBY LEŚNIOWSKIEGO - CROHNA (chlc) (ICD-10 K 50) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY SCHEMAT DAWKOWANIA LEKÓW W PROGRAMIE BADANIA DIAGNOSTYCZNE WYKONYWANE W
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta Miacalcic, 50 j.m./ml, roztwór do wstrzykiwań Miacalcic, 100 j.m./ml, roztwór do wstrzykiwań Calcitoninum salmonis Należy zapoznać się z treścią
Ulotka dołączona do opakowania: informacja dla pacjenta Miacalcic, 50 j.m./ml, roztwór do wstrzykiwań Miacalcic, 100 j.m./ml, roztwór do wstrzykiwań Calcitoninum salmonis Należy zapoznać się z treścią
Często zadawane pytania (FAQ)
 4 listopada 2011 r. EMA/527628/2011 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków Jeśli nie znajdą tu Państwo odpowiedzi
4 listopada 2011 r. EMA/527628/2011 Dyrekcja W niniejszym dokumencie znajdują się odpowiedzi na najczęściej zadawane pytania otrzymane przez Europejską Agencję Leków Jeśli nie znajdą tu Państwo odpowiedzi
ULOTKA DLA PACJENTA 1
 ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta PENTASA, 1 g, czopki Mesalazinum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla pacjenta PENTASA, 1 g, czopki Mesalazinum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta. BIODRIBIN, 1 mg/ml, roztwór do infuzji. Cladribinum
 Ulotka dołączona do opakowania: informacja dla pacjenta BIODRIBIN, 1 mg/ml, roztwór do infuzji Cladribinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta BIODRIBIN, 1 mg/ml, roztwór do infuzji Cladribinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa.
 Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa. Niniejszy dokument stanowi streszczenie Europejskiego Publicznego Sprawozdania Oceniajc ego (EPAR). Wyja nia, jak Komitet ds. Produktów Leczniczych
Simponi/golimumab Streszczenie EPAR dla ogółu społeczeństwa. Niniejszy dokument stanowi streszczenie Europejskiego Publicznego Sprawozdania Oceniajc ego (EPAR). Wyja nia, jak Komitet ds. Produktów Leczniczych
Zaobserwowano częstsze przypadki stosowania produktu leczniczego Vistide w niezatwierdzonych wskazaniach i (lub) drogach podawania.
 Komunikat skierowany do fachowych pracowników ochrony zdrowia dotyczący występowania ciężkich działań niepożądanych związanych z stosowaniem produktu leczniczego Vistide (cydofowir) niezgodnie z zapisami
Komunikat skierowany do fachowych pracowników ochrony zdrowia dotyczący występowania ciężkich działań niepożądanych związanych z stosowaniem produktu leczniczego Vistide (cydofowir) niezgodnie z zapisami
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Karbis, 4 mg, tabletki Karbis, 8 mg, tabletki Karbis, 16 mg, tabletki Karbis, 32 mg, tabletki Candesartanum cilexetilum Należy zapoznać się z treścią ulotki
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Karbis, 4 mg, tabletki Karbis, 8 mg, tabletki Karbis, 16 mg, tabletki Karbis, 32 mg, tabletki Candesartanum cilexetilum Należy zapoznać się z treścią ulotki
B. ULOTKA DLA PACJENTA
 B. ULOTKA DLA PACJENTA 1 ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA UŻYTKOWNIKA Zevalin 1,6 mg/ml zestaw do sporządzania produktu radiofarmaceutycznego do infuzji Ibrytumomab tiuksetan [ 90 Y] Należy
B. ULOTKA DLA PACJENTA 1 ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA UŻYTKOWNIKA Zevalin 1,6 mg/ml zestaw do sporządzania produktu radiofarmaceutycznego do infuzji Ibrytumomab tiuksetan [ 90 Y] Należy
20 września 2013 r. EMA/564255/2013. 7 Westferry Circus Canary Wharf London E14 4HB United Kingdom
 20 września 2013 r. EMA/564255/2013 Zawieszenie pozwolenia na dopuszczenie do obrotu produktu leczniczego Numeta G13%E i wprowadzenie nowych działań służących zminimalizowaniu ryzyka stosowania produktu
20 września 2013 r. EMA/564255/2013 Zawieszenie pozwolenia na dopuszczenie do obrotu produktu leczniczego Numeta G13%E i wprowadzenie nowych działań służących zminimalizowaniu ryzyka stosowania produktu
Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego.
 Chłoniak z komórek płaszcza Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego,
Chłoniak z komórek płaszcza Poniższa informacja dotyczy chłoniaka z komórek płaszcza, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego,
Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO
 Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1. Pacjent jest kwalifikowany
Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY 1. Pacjent jest kwalifikowany
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika. Perjeta 420 mg koncentrat do sporządzania roztworu do infuzji pertuzumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Perjeta 420 mg koncentrat do sporządzania roztworu do infuzji pertuzumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
Ulotka dołączona do opakowania: informacja dla użytkownika Perjeta 420 mg koncentrat do sporządzania roztworu do infuzji pertuzumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M 45)
 Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Dziennik Urzędowy Ministra Zdrowia 615 Poz. 27 Załącznik B.36. LECZENIE INHIBITORAMI TNF ALFA ŚWIADCZENIOBIORCÓW Z CIĘŻKĄ, AKTYWNĄ POSTACIĄ ZESZTYWNIAJĄCEGO ZAPALENIA STAWÓW KRĘGOSŁUPA (ZZSK) (ICD-10 M
Ulotka dołączona do opakowania: informacja dla użytkownika. MabThera 1400 mg roztwór do wstrzykiwań podskórnych rytuksymab
 Ulotka dołączona do opakowania: informacja dla użytkownika MabThera 1400 mg roztwór do wstrzykiwań podskórnych rytuksymab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika MabThera 1400 mg roztwór do wstrzykiwań podskórnych rytuksymab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Pełny wykaz substancji pomocniczych, patrz punkt 6.1 Charakterystyki Produktu Leczniczego (ChPL).
 Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
Limfocyty powstają w szpiku kostnym, czyli tam gdzie powstają wszystkie komórki krwi. Występują
 Informacja dotyczy chłoniaka śródpiersia z dużych komórek B, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu
Informacja dotyczy chłoniaka śródpiersia z dużych komórek B, stanowiącego odmianę chłoniaka nieziarniczego. Chłoniak nieziarniczy Jest to choroba rozrostowa układu limfatycznego, który stanowi część systemu
LOPERAMID WZF 2 mg, tabletki Loperamidi hydrochloridum
 Ulotka dołączona do opakowania: informacja dla pacjenta LOPERAMID WZF 2 mg, tabletki Loperamidi hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla pacjenta LOPERAMID WZF 2 mg, tabletki Loperamidi hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06)
 Dziennik Urzędowy Ministra Zdrowia 614 Poz. 56 Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY
Dziennik Urzędowy Ministra Zdrowia 614 Poz. 56 Załącznik B.45. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10: M 05, M 06) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY
Ból uważany jest za jeden z potencjalnie istotnych czynników ryzyka dotyczących śmiertelności (Sokka).
 VI. 2 Elementy do podsumowania podawanego do publicznej wiadomości. VI. 2.1 Przegląd epidemiologii choroby Odczuwanie bólu jest powszechnym zjawiskiem wśród dzieci. Szacuje się, że ta dolegliwość może
VI. 2 Elementy do podsumowania podawanego do publicznej wiadomości. VI. 2.1 Przegląd epidemiologii choroby Odczuwanie bólu jest powszechnym zjawiskiem wśród dzieci. Szacuje się, że ta dolegliwość może
Ulotka dołączona do opakowania: informacja dla użytkownika. Dacogen 50 mg proszek do sporządzania koncentratu roztworu do infuzji decytabina
 Ulotka dołączona do opakowania: informacja dla użytkownika Dacogen 50 mg proszek do sporządzania koncentratu roztworu do infuzji decytabina Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika Dacogen 50 mg proszek do sporządzania koncentratu roztworu do infuzji decytabina Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Rysunek. Układ Limfatyczny.
 Informacja dotyczy chłoniaka rozlanego z dużych komórek B, będącego odmianą chłoniaka nieziarniczego. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest częścią systemu
Informacja dotyczy chłoniaka rozlanego z dużych komórek B, będącego odmianą chłoniaka nieziarniczego. Chłoniak nieziarniczy Chłoniak nieziarniczy jest nowotworem układu chłonnego, który jest częścią systemu
Przednia część okładki PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL
 Przednia część okładki PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO
Przednia część okładki PRZEWODNIK DLA FARMACEUTY JAK WYDAWAĆ LEK INSTANYL WAŻNE INFORMACJE DOTYCZĄCE BEZPIECZEŃSTWA: INSTANYL, AEROZOL DO NOSA LEK STOSOWANY W LECZENIU PRZEBIJAJĄCEGO BÓLU NOWOTWOROWEGO
Ulotka dołączona do opakowania: informacja dla pacjenta. LORATADYNA GALENA, 10 mg, tabletki Loratadinum
 Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA GALENA, 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA GALENA, 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Ulotka dołączona do opakowania: informacja dla użytkownika. SALOFALK 250, 250 mg, czopki Mesalazinum
 Ulotka dołączona do opakowania: informacja dla użytkownika SALOFALK 250, 250 mg, czopki Mesalazinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla użytkownika SALOFALK 250, 250 mg, czopki Mesalazinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08)
 Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY
Załącznik B.33. LECZENIE REUMATOIDALNEGO ZAPALENIA STAWÓW I MŁODZIEŃCZEGO IDIOPATYCZNEGO ZAPALENIA STAWÓW O PRZEBIEGU AGRESYWNYM (ICD-10 M 05, M 06, M 08) I. LEKI BIOLOGICZNE A. Kryteria kwalifikacji ŚWIADCZENIOBIORCY
Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
 18 października 2012 EMA/653433/2012 EMEA/H/A-5(3)/1319 Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
18 października 2012 EMA/653433/2012 EMEA/H/A-5(3)/1319 Pytania i dopowiedzi na temat analizy nie-selektywnych niesteroidowych leków przeciwzapalnych (NLPZ) oraz ryzyka chorób układu sercowo-naczyniowego.
Ulotka dołączona do opakowania: informacja dla pacjenta. PENTASA, 1 g, granulat o przedłużonym uwalnianiu. Mesalazinum
 Ulotka dołączona do opakowania: informacja dla pacjenta PENTASA, 1 g, granulat o przedłużonym uwalnianiu Mesalazinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta PENTASA, 1 g, granulat o przedłużonym uwalnianiu Mesalazinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika. MabThera 100 mg koncentrat do sporządzania roztworu do infuzji rytuksymab
 Ulotka dołączona do opakowania: informacja dla użytkownika MabThera 100 mg koncentrat do sporządzania roztworu do infuzji rytuksymab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
Ulotka dołączona do opakowania: informacja dla użytkownika MabThera 100 mg koncentrat do sporządzania roztworu do infuzji rytuksymab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
c) poprawa jakości życia chorych z nieziarniczym chłoniakiem typu grudkowego w III i IV stopniu
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 9 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011r. LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 9 do zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011r. LECZENIE CHŁONIAKÓW ZŁOŚLIWYCH ICD-10 C 82 chłoniak grudkowy
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Biorąc pod uwagę sprawozdanie komitetu PRAC do raportu PSUR dla dexamethasonu (za wyjątkiem
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Biorąc pod uwagę sprawozdanie komitetu PRAC do raportu PSUR dla dexamethasonu (za wyjątkiem
