C V dla róŝnych gazów. Widzimy C C dla wszystkich gazów jest, zgodnie z przewidywaniami równa w
|
|
|
- Przybysław Czarnecki
- 7 lat temu
- Przeglądów:
Transkrypt
1 Wykład z fizyki, Piotr Posmykiewicz 7 P dt dt + nrdt i w rezultacie: nr 4-7 P + Dla gazu doskonałego pojemność cieplna przy stałym ciśnieniu jest większa od pojemności cieplnej przy stałej objętości o nr. Dla jednego mola gazu mamy: CP C + R TABELA Molowa pojemność cieplna( J/mol K ) dla róŝnych gazów w 5 0 C Gaz C P C C /R C P - C (C P - C )/R Jednoatomowy He 0,79,5,5 8,7 0,99 Ne 0,79,68,5 8, 0,98 Ar 0,79,45,50 8,34,00 Kr 0,79,45,50 8,34,00 Xe 0,79,5,5 8,7 0,99 Dwuatomowy N 9, 0,80,50 8,3,00 H 8,8 0,44,46 8,38,0 O 9,37 0,98,5 8,39,0 CO 9,04 0,74,49 8,30,00 Wieloatomowe CO 36,6 8,7 3,39 8,45,0 N O 36,90 8,39 3,4 8,5,0 H S 36, 7,36 3,9 8,76,05 PowyŜsza tabela przedstawia listę ciepła molowego równieŝ, Ŝe C P i C dla róŝnych gazów. Widzimy C C dla wszystkich gazów jest, zgodnie z przewidywaniami równa w przybliŝeniu R. Z tabeli widać równieŝ, Ŝe dla gazów jednoatomowych dla wszystkich gazów wynosi składających się z cząsteczek wieloatomowych,5 R, dla gazów dwuatomowych,5 R C jest większe od C w przybliŝeniu, a dla gazów,5 R. PowyŜsze wyniki moŝna wyjaśnić w oparciu o model gazu przedstawiony w poprzednim wykładzie. Całkowita energia kinetyczna ruchu postępowego n moli gazu jest równa K 3 / nrt ( Równanie 3- ). W rezultacie, jeŝeli energia wewnętrzna gazu składa się tylko z energii kinetycznej ruchu postępowego, to otrzymamy: 3 U nrt 4-8
2 Wykład z fizyki, Piotr Posmykiewicz 7 Pojemności cieplne wyniosą zatem: du 3 nr 4-9 dt C dla gazu jednoatomowego. 5 + nr nr 4-0 P C P dla gazu jednoatomowego. Wyniki z powyŝszej tabeli dobrze zgadzają się z przewidywaniami dla gazów jednoatomowych, jednak dla innych gazów pojemności cieplne są większe niŝ to wynika z równań 4-9 i 4-0. Dla innych gazów energia wewnętrzna jest wyraźnie większa niŝ 3 / nrt. Powodem tego jest fakt, Ŝe cząsteczki gazów wieloatomowych posiadają inne formy energii oprócz energii kinetycznej ruchu postępowego.; energię ruchu obrotowego i ruchu drgającego. Pojemność cieplna, a zasada ekwipartycji energii. Zgodnie z zasadą ekwipartycji energii ( patrz poprzedni wykład ) energia wewnętrzna n moli gazu przypadająca na kaŝdy stopień swobody cząsteczki gazu powinna być równa Pojemność cieplna gazu w stałej objętości powinna zatem być równa swobody cząsteczki. Z powyŝszej tabeli widać, Ŝe cząsteczki azotu, tlenu, wodoru i tlenku węgla mają ciepło molowe w stałej objętości w przybliŝeniu równe 5 R. Czyli cząsteczki te mają pięć stopni swobody ( Rysunek 4-6 ). Około roku 880 Clausjus wysunął nrt. nr razy ilość stopni hipotezę, Ŝe cząsteczki te mogą obracać się wokół dwu osi, co daje dwa dodatkowe stopnie swobody. Dlatego energia kinetyczna cząsteczki dwuatomowej jest równa: K mvx + mvy + mvz + I x' ω x' + Zatem całkowita energia wewnętrzna n moli takiego gazu wynosi: I y' v y' Rysunek 4-6 Środek
3 Wykład z fizyki, Piotr Posmykiewicz 73 5 U 5 nrt nrt 4- a pojemność cieplna w stałej objętości jest równa 5 nr Pojemność cieplna ciał stałych. Ciepło molowe większości ciał stałych jest w przybliŝeniu jednakowe i w przybliŝeniu równe 3 R : Rysunek 4-7 C 3R 4,9J / mol K 4-3 Ten eksperymentalny rezultat znany jest jako prawo Dulonga-Petit. MoŜna to wytłumaczyć teoretycznie stosując zasadę ekwipartycji energii do prostego modelu ciała stałego przedstawionego na rysunku 4-7. Zgodnie z tym modelem, ciało stałe składa się z przestrzennej siatki krystalicznej, w której atomy mają stałe połoŝenie równowagi i są połączone spręŝynkami z sąsiadami. KaŜdy atom moŝe drgać w kierunkach x, y, z. Całkowita energia takiego atomu w ciele stałym jest, w związku z tym, równa: E mvx + mvy + mvz + kef x + kef y + k ef z gdzie kef jest skutecznym współczynnikiem spręŝystości tych hipotetycznych spręŝynek. W takim razie kaŝdy atom ma sześć niezaleŝnych stopni swobody. Zasada ekwipartycji energii mówi, Ŝe w jeŝeli substancja znajduje się w stanie równowagi, to na jeden mol i na jeden stopień swobody przypada średnia energia równa jednego mola ciała stałego będzie równa: RT. W rezultacie energia wewnętrzna U m 6 RT 3RT 4-4 a to oznacza, Ŝe ciepło molowe jest równe 3 R.
4 Wykład z fizyki, Piotr Posmykiewicz Niepowodzenie zasady ekwipartycji energii. Pomimo tego, iŝ zasada ekwipartycji energii odniosła spektakularny sukces w wyjaśnieniu pojemności cieplnej gazów i ciał stałych, to równieŝ odniosła spektakularną poraŝkę. Na przykład, jeŝeli cząsteczka gazu dwuatomowego, taka jak ta na rysunku 4-6, obraca się wokół linii łączącej oba atomy, to powinien istnieć dodatkowy stopień swobody. Podobnie jeŝeli cząsteczka dwuatomowa nie jest sztywna, to dwa atomy powinny wykonywać drgania wzdłuŝ łączącej je linii. Powinniśmy, zatem otrzymać dwa dodatkowe stopnie swobody związane z energią kinetyczną i potencjalną drgań. Jednak zmierzone wartości ciepła molowego gazów dwuatomowych, przedstawione w tabeli, wskazują wyraźnie, Ŝe cząsteczki ani nie obracają się wokół linii łączącej je, ani nie wykonują drgań. Teoria ekwipartycji energii nie wyjaśnia tego faktu, ani faktu, Ŝe cząsteczki jednoatomowe nie obracają się wokół ani jednej z trzech prostopadłych osi. Poza tym stwierdzono, Ŝe pojemność cieplna zaleŝy od temperatury, w przeciwieństwie do wniosków wypływających z zasady ekwipartycji energii. Jaskrawym przejawem zaleŝności pojemności cieplnej od temperatury jest pojemność cieplna H pokazana na rysunku 4-8. W niskich temperaturach H zachowuje się jak pojedynczy atom niewykonujący Ŝadnych obrotów. W bardzo wysokich temperaturach H zaczyna wykonywać drgania, ale cząsteczki ulegają dysocjacji zanim ciepło molowe osiągnie wartość 7 R. W końcu, zasada ekwipartycji energii przewiduje, Ŝe ciepło molowe wszystkich ciał stałych powinno wynosić Rysunek 4-8 posiadających wysoką temperaturę, jednak w bardzo niskich temperaturach nie otrzymujemy takich wartości ciepła molowego. Zasada ekwipartycji energii zawodzi, poniewaŝ energia jest skwantowana: Cząsteczki mogą posiadać tylko określone wartości energii, jak jest to przedstawione schematycznie na wykresie poziomów energetycznych na rysunku 4-9. Cząsteczki mogą tylko wtedy osiągnąć lub stracić energię, jeŝeli pozwoli im 3 R. Wynik ten otrzymano dla wielu ciał stałych Rysunek 4-9
5 Wykład z fizyki, Piotr Posmykiewicz 75 to na przejście na inny dozwolony poziom energetyczny. Na przykład energia, która moŝe być przekazana między cząsteczkami w wyniku zderzeń między nimi jest rzędu kt, co jest typową energią cieplną cząsteczki. Zakres stosowalności zasady ekwipartycji energii zaleŝy od stosunku wartości kt do wartości energii między dozwolonymi poziomami energetycznymi. JeŜeli odległość między poziomami jest duŝa w porównaniu z wartością kt, to energia nie moŝe być przekazywana w wyniku zderzeń i klasyczna zasada ekwipartycji energii zawodzi. JeŜeli odległość między poziomami jest znacznie mniejsza od kt, to skwantowanie energii nie będzie odgrywało roli i zasada ekwipartycji energii będzie spełniona. Warunek stosowalności zasady ekwipartycji energii. Weźmy pod uwagę obracającą się cząsteczkę. Energia obrotowa jest równa: E I ( Iω) I L I ω 4-5 gdzie I jest momentem bezwładności cząsteczki,ω jest jej prędkością kątową i L Iω jest momentem pędu. Okazuje się, Ŝe moment pędu jest wielkością skwantowaną, tzn. moŝe przybierać tylko określone wartości dane wzorem: L l( l + )h gdzie l,,3, gdzie h h / π, h jest stałą Plancka. Dlatego energia obracającej się cząsteczki jest równieŝ skwantowana i moŝe przybierać następujące wartości: gdzie ( l + ) L l h E l + I I ( l ) E0 R 4-7 E 0R h I 4-8 jest charakterystyczną przerwą energetyczną między poziomami. JeŜeli energia ta jest znacznie mniejsza od kt, to moŝemy oczekiwać, Ŝe jesteśmy w obszarze fizyki klasycznej i zasada ekwipartycji energii jest spełniona. Zdefiniujmy temperaturę krytyczną
6 Wykład z fizyki, Piotr Posmykiewicz 76 kt c h E0R 4-8 I JeŜeli T jest duŝo większe niŝ T c, to kt będzie znacznie większe od odległości między poziomami energetycznymi i zasada ekwipartycji będzie obowiązywać. JeŜeli T jest mniejsze lub rzędu T c, to kt nie będzie duŝo większa od odległości między poziomami energetycznymi i moŝemy oczekiwać, Ŝe zasada ekwipartycji nie będzie obowiązywać. Oszacujemy T c dla paru charakterystycznych przypadków.. Obrót H wokół osi prostopadłej do linii łączącej atomy H i przechodzącej przez środek masy. ( patrz Rysunek 4-6 ) Moment bezwładności H jest równy rs I H M H M H rs gdzie M jest masą atomu wodoru, a r s jest odległością między atomami. Dla H wodoru M H krytyczna będzie równa : T c h ki H 7,67 0 kg i r 8 0 m. W rezultacie temperatura h km H rs 34 (,05 0 J s) 3 7 (,38 0 J / K )(,67 0 kg)( 8 0 m) s 75K Jak widać z rysunku 4-8 jest to w przybliŝeniu temperatura poniŝej której, energia ruchu obrotowego nie wnosi wkładu do pojemności cieplnej.. O : PoniewaŜ masa O jest około 6 razy większa od masy H, a odległości między atomami są w przybliŝeniu takie same, to temperatura krytyczna O powinna wynosić około 75/6 4,7K. Dla wszystkich temperatur, dla których O istnieje jako gaz T >> Tc, a zatem kt jest znacznie większe niŝ odległość między poziomami energetycznymi i naleŝy się spodziewać, Ŝe zasada ekwipartycji fizyki klasycznej będzie spełniona. 3. Obroty gazu jednoatomowego. Rozpatrzmy atom He. Masa elektronu jest około 000 razy mniejsza niŝ jego jądra. Ale promień jądra jest około razy
7 Wykład z fizyki, Piotr Posmykiewicz 77 mniejszy niŝ odległość od elektronów He. Tak więc moment bezwładności tego atomu powstaje praktycznie dzięki jego elektronom. Odległość między jądrem helu, a jego dwoma elektronami jest równa około połowy odległości między atomami wodoru w cząsteczce H. W rezultacie podstawiając m e M H /000 i r r s / otrzymamy moment bezwładności dla dwu elektronów He w przybliŝeniu: I He mr M H rs 000 I H 000 Temperatura krytyczna helu jest więc około 000 razy wyŝsza niŝ dla H tzn K. Jest to oczywiście znacznie więcej niŝ temperatura dysocjacji ( temperatura, przy której elektrony są oderwane od jądra ) helu. W rezultacie przerwa między dozwolonymi poziomami energetycznymi jest zawsze znacznie większa niŝ kt i atomy He nigdy nie mogą być wprowadzone w ruch obrotowy w wyniku zderzeń występujących w gazach. Inne jednoatomowe gazy posiadają nieco większe momenty bezwładności, poniewaŝ posiadają więcej elektronów, ale ich temperatura krytyczna jest ciągle rzędu dziesiątków tysięcy kelwinów, czyli równieŝ nie mogą być wprawione w ruch obrotowy w wyniku zderzeń występujących w gazie. 4. Obroty gazu dwuatomowego w wokół osi łączącej atomy. Z dyskusji o gazach jednoatomowych wynika, Ŝe moment bezwładności w przypadku dwuatomowym będzie takŝe związany z elektronami i będzie tego samego rzędu jak w przypadku gazów jednoatomowych. RównieŜ w tym wypadku, temperatura krytyczna niezbędna, aby wywołać ruch obrotowy z powodu zderzeń między cząsteczkami przekracza temperaturę dysocjacji, a zatem i w tym wypadku ruch obrotowy jest niemoŝliwy. T c Warto odnotować, Ŝe zasada ekwipartycji energii przyczyniła się w dziewiętnastym wieku do zrozumienia cząsteczkowej budowy materii, a niezgodności zasady ekwipartycji z danymi doświadczalnymi w dwudziestym wieku odegrały duŝą rolę do rozwoju mechaniki kwantowej. 4-9 Kwazistatyczne, adiabatyczne rozpręŝanie gazu.
8 Wykład z fizyki, Piotr Posmykiewicz 78 Przemiana, w której nie ma przepływu ciepła do, lub z układu nazywa się przemianą adiabatyczną. Weźmy pod uwagę kwazistatyczne adiabatyczne rozpręŝanie gazu, w którym gaz znajduje się w naczyniu izolowanym cieplnie i rozpręŝa się wolno przesuwając tłok i wykonując pracę nad tym tłokiem. PoniewaŜ ciepło nie wpływa ani nie wypływa z gazu, to praca wykonana przez gaz zmniejsza energię wewnętrzną gazu i temperatura gazu maleje. Na rysunku 4-0 pokazana jest ta krzywa na wykresie p. MoŜemy Izoterma T Przejście adiabatyczne Rysunek 4-0 Izoterma T znaleźć równanie krzywej adiabatycznej ( adiabaty ) dla gazu doskonałego, jeŝeli zastosujemy równanie stanu i pierwszą zasadę termodynamiki. W rezultacie otrzymamy: gdzie dq du + dw dt + pd du dt z równania 4-5. Stosując p nrt / d dt + nrt 0 Przekształcenie powyŝszego daje: dt T nr d Równanie 4-30 moŝna uprościć podstawiając nr C P P κ C nr : P gdzie κ (kappa ) jest stosunkiem pojemności cieplnych zwanym wykładnikiem adiabaty C ' C κ P P 4-3 C W rezultacie otrzymujemy: dt T d ( ) 0 + κ Całkując powyŝsze równanie: ( ) ln comstans ln T + κ Korzystając z własności logarytmów:
9 Wykład z fizyki, Piotr Posmykiewicz 79 lub ln κ ( T ) const κ T const 4-3 Kwazistatyczna przemiana adiabatyczna Gdzie stałe w poprzednich dwu równaniach nie są jednakowe. MoŜemy wyeliminować T z równania 4-3 stosując p nrt. Otrzymamy wtedy : lub p κ constans nr κ p const 4-33 Kwazistatyczna przemiana adiabatyczna Równanie 4-33 podaje związek między p i dla rozpręŝania i spręŝania adiabatycznego. Praca wykonana przez gaz podczas adiabatycznego rozpręŝania moŝe być policzona z pierwszej zasady termodynamiki: dq du + dw du + PoniewaŜ dq 0 otrzymamy: Wtedy: dw du gdzie przyjmujemy, Ŝe dt pd dw dt Wadiabatyczna T 4-34 Praca w procesie adiabatycznym C ' jest stałe. Zwróćmy uwagę, Ŝe praca wykonana przez gaz zaleŝy tylko od zmiany temperatury bezwzględnej. Podczas rozpręŝania adiabatycznego gaz wykonuje pracę, a jego energia wewnętrzna i temperatura bezwzględna maleją. Podczas adiabatycznego spręŝania praca zostaje wykonana nad gazem i energia wewnętrzna i temperatura wzrastają. MoŜemy zastosować równanie stanu gazu doskonałego, aby zapisać równanie 4-34 za pomocą wartości początkowych i końcowych objętości i ciśnienia. JeŜeli T jest temperaturą Dla gazu doskonałego U jest proporcjonalne do temperatury bezwzględnej i dlatego C du/dt jest stałe.
10 Wykład z fizyki, Piotr Posmykiewicz 80 początkową, a T temperaturą końcową, to otrzymamy pracę wykonaną w przemianie adiabatycznej w postaci: W Korzystając z adiabatyczna p nrt : T ( T T ) ( T T ) W adiabatyczna gdzie zastosowaliśmy podstawienie p nr nr p nr i podstawiając κ zamiast C / C otrzymamy: P P ( p p ) P. Dzieląc licznik i mianownik przez C ' p p κ Wadiabatyczna 4-35 Praca adiabatyczna Prędkość fali dźwiękowej. Zastosujmy równanie 4.33 do obliczenia adiabatycznego modułu ściśliwości, który jest związany z prędkością rozchodzenia się dźwięku w powietrzu. W tym celu zróŝniczkujmy równanie 4 33: lub wtedy κ κ pd( ) + dp 0 pκ κ d + κpd dp κ dp 0 Porównując to z równaniem -6 moŝemy policzyć adiabatyczny moduł ściśliwości : B adiab dp κp d / Prędkość dźwięku dana jest wzorem: 4-36 v B adib ρ Izotermiczny moduł ściśliwości, który opisuje zmiany zachodzące przy stałej temperaturze róŝni się od adiabatycznego modułu ściśliwości opisującego zmiany, gdy nie ma wymiany ciepła z otoczeniem. Jednak dla fal dźwiękowych zmiany zachodzą zbyt gwałtownie, aby zdąŝył nastąpić przepływ ciepła. Dlatego naleŝy zastosować adiabatyczny moduł ściśliwości.
11 Wykład z fizyki, Piotr Posmykiewicz 8 gdzie ρ jest związane z ilością moli n i masą molową µ równaniem ρ m / nµ /. Korzystając z równania Clapeyrona moŝemy wyeliminować z gęstości: n µ nµ µ p ρ RT / p RT Wykorzystując powyŝszy wynik i równanie 4-36 otrzymamy Badiab κp v ρ µ p/ RT κrt µ
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Ciepło właściwe. Autorzy: Zbigniew Kąkol Bartek Wiendlocha
 Ciepło właściwe Autorzy: Zbigniew Kąkol Bartek Wiendlocha 01 Ciepło właściwe Autorzy: Zbigniew Kąkol, Bartek Wiendlocha W module zapoznamy się z jednym z kluczowych pojęć termodynamiki - ciepłem właściwym.
Ciepło właściwe Autorzy: Zbigniew Kąkol Bartek Wiendlocha 01 Ciepło właściwe Autorzy: Zbigniew Kąkol, Bartek Wiendlocha W module zapoznamy się z jednym z kluczowych pojęć termodynamiki - ciepłem właściwym.
Ciśnienie i temperatura model mikroskopowy
 Ciśnienie i temperatura model mikroskopowy Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy
Ciśnienie i temperatura model mikroskopowy Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12
 Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
= = Budowa materii. Stany skupienia materii. Ilość materii (substancji) n - ilość moli, N liczba molekuł (atomów, cząstek), N A
 Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
Budowa materii Stany skupienia materii Ciało stałe Ciecz Ciała lotne (gazy i pary) Ilość materii (substancji) n N = = N A m M N A = 6,023 10 mol 23 1 n - ilość moli, N liczba molekuł (atomów, cząstek),
TERMODYNAMIKA FENOMENOLOGICZNA
 TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
TERMODYNAMIKA FENOMENOLOGICZNA Przedmiotem badań są własności układów makroskopowych w zaleŝności od temperatury. Układ makroskopowy Np. 1 mol substancji - tyle składników ile w 12 gramach węgla C 12 N
Termodynamika Część 3
 Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
WYKŁAD 2 TERMODYNAMIKA. Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami
 WYKŁAD 2 TERMODYNAMIKA Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami Zasada zerowa Kiedy obiekt gorący znajduje się w kontakcie cieplnym z obiektem zimnym następuje
WYKŁAD 2 TERMODYNAMIKA Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami Zasada zerowa Kiedy obiekt gorący znajduje się w kontakcie cieplnym z obiektem zimnym następuje
Kinetyczna teoria gazów Termodynamika. dr Mikołaj Szopa Wykład
 Kinetyczna teoria gazów Termodynamika dr Mikołaj Szopa Wykład 7.11.015 Kinetyczna teoria gazów Kinetyczna teoria gazów. Termodynamika Termodynamika klasyczna opisuje tylko wielkości makroskopowe takie
Kinetyczna teoria gazów Termodynamika dr Mikołaj Szopa Wykład 7.11.015 Kinetyczna teoria gazów Kinetyczna teoria gazów. Termodynamika Termodynamika klasyczna opisuje tylko wielkości makroskopowe takie
Wykład FIZYKA I. 15. Termodynamika statystyczna. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 15. Termodynamika statystyczna Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html TERMODYNAMIKA KLASYCZNA I TEORIA
Wykład FIZYKA I 15. Termodynamika statystyczna Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html TERMODYNAMIKA KLASYCZNA I TEORIA
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów
 Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
Temperatura, ciepło, oraz elementy kinetycznej teorii gazów opis makroskopowy równowaga termodynamiczna temperatura opis mikroskopowy średnia energia kinetyczna molekuł Równowaga termodynamiczna A B A
S ścianki naczynia w jednostce czasu przekazywany
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA. d dp. jest sumaryczną zmianą pędu cząsteczek zachodzącą na powierzchni S w
 FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
FIZYKA STATYSTYCZNA W ramach fizyki statystycznej przyjmuje się, że każde ciało składa się z dużej liczby bardzo małych cząstek, nazywanych cząsteczkami. Cząsteczki te znajdują się w ciągłym chaotycznym
10. FALE, ELEMENTY TERMODYNAMIKI I HYDRODY- NAMIKI.
 0. FALE, ELEMENY ERMODYNAMIKI I HYDRODY- NAMIKI. 0.9. Podstawy termodynamiki i raw gazowych. Podstawowe ojęcia Gaz doskonały: - cząsteczki są unktami materialnymi, - nie oddziałują ze sobą siłami międzycząsteczkowymi,
0. FALE, ELEMENY ERMODYNAMIKI I HYDRODY- NAMIKI. 0.9. Podstawy termodynamiki i raw gazowych. Podstawowe ojęcia Gaz doskonały: - cząsteczki są unktami materialnymi, - nie oddziałują ze sobą siłami międzycząsteczkowymi,
Wykład 7: Przekazywanie energii elementy termodynamiki
 Wykład 7: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ emperatura Fenomenologicznie wielkość informująca o tym jak ciepłe/zimne
Wykład 7: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ emperatura Fenomenologicznie wielkość informująca o tym jak ciepłe/zimne
Wykład 6 Ciepło właściwe substancji prostych Ciepło właściwe gazów doskonałych Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C )
 Wykład 6 Ciepło właściwe substancji prostych Ciepło właściwe gazów doskonałych Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C ) ZaleŜność stosunku R od temperatury dla gazu doskonałego
Wykład 6 Ciepło właściwe substancji prostych Ciepło właściwe gazów doskonałych Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C ) ZaleŜność stosunku R od temperatury dla gazu doskonałego
Przemiany termodynamiczne
 Przemiany termodynamiczne.:: Przemiana adiabatyczna ::. Przemiana adiabatyczna (Proces adiabatyczny) - proces termodynamiczny, podczas którego wyizolowany układ nie nawiązuje wymiany ciepła, lecz całość
Przemiany termodynamiczne.:: Przemiana adiabatyczna ::. Przemiana adiabatyczna (Proces adiabatyczny) - proces termodynamiczny, podczas którego wyizolowany układ nie nawiązuje wymiany ciepła, lecz całość
Ciepło i pierwsza zasada termodynamiki.
 Wykład z fizyki, Piotr Posmykiewicz 162 W Y K Ł A D XIII Ciepło i pierwsza zasada termodynamiki. Ciepło jest energią, która jest przekazywana z jednego układu do drugiego w wyniku róŝnicy temperatur obu
Wykład z fizyki, Piotr Posmykiewicz 162 W Y K Ł A D XIII Ciepło i pierwsza zasada termodynamiki. Ciepło jest energią, która jest przekazywana z jednego układu do drugiego w wyniku róŝnicy temperatur obu
Podstawy termodynamiki
 Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Podstawy termodynamiki Temperatura i ciepło Praca jaką wykonuje gaz I zasada termodynamiki Przemiany gazowe izotermiczna izobaryczna izochoryczna adiabatyczna Co to jest temperatura? 40 39 38 Temperatura
Termodynamika Techniczna dla MWT, wykład 5. AJ Wojtowicz IF UMK
 Wykład 5 Gaz doskonały w ujęciu teorii kinetycznej Ciśnienie i temperatura gazu doskonałego Prędkość średnia kwadratowa cząsteczek gazu doskonałego Rozkład awella prędkości cząsteczek gazu doskonałego
Wykład 5 Gaz doskonały w ujęciu teorii kinetycznej Ciśnienie i temperatura gazu doskonałego Prędkość średnia kwadratowa cząsteczek gazu doskonałego Rozkład awella prędkości cząsteczek gazu doskonałego
Podstawy Procesów i Konstrukcji Inżynierskich. Teoria kinetyczna INZYNIERIAMATERIALOWAPL. Kierunek Wyróżniony przez PKA
 Podstawy Procesów i Konstrukcji Inżynierskich Teoria kinetyczna Kierunek Wyróżniony rzez PKA 1 Termodynamika klasyczna Pierwsza zasada termodynamiki to rosta zasada zachowania energii, czyli ogólna reguła
Podstawy Procesów i Konstrukcji Inżynierskich Teoria kinetyczna Kierunek Wyróżniony rzez PKA 1 Termodynamika klasyczna Pierwsza zasada termodynamiki to rosta zasada zachowania energii, czyli ogólna reguła
GAZ DOSKONAŁY W TERMODYNAMICE TO POJĘCIE RÓŻNE OD GAZU DOSKONAŁEGO W HYDROMECHANICE (ten jest nielepki)
 Właściwości gazów GAZ DOSKONAŁY Równanie stanu to zależność funkcji stanu od jednoczesnych wartości parametrów koniecznych do określenia stanów równowagi trwałej. Jest to zwykle jednowartościowa i ciągła
Właściwości gazów GAZ DOSKONAŁY Równanie stanu to zależność funkcji stanu od jednoczesnych wartości parametrów koniecznych do określenia stanów równowagi trwałej. Jest to zwykle jednowartościowa i ciągła
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii
 Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Drgania. W Y K Ł A D X Ruch harmoniczny prosty. k m
 Wykład z fizyki Piotr Posmykiewicz 119 W Y K Ł A D X Drgania. Drgania pojawiają się wtedy, gdy układ zostanie wytrącony ze stanu równowagi stabilnej. MoŜna przytoczyć szereg znanych przykładów: kołysząca
Wykład z fizyki Piotr Posmykiewicz 119 W Y K Ł A D X Drgania. Drgania pojawiają się wtedy, gdy układ zostanie wytrącony ze stanu równowagi stabilnej. MoŜna przytoczyć szereg znanych przykładów: kołysząca
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego
 Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
TERMODYNAMIKA Zajęcia wyrównawcze, Częstochowa, 2009/2010 Ewa Mandowska
 1. Bilans cieplny 2. Przejścia fazowe 3. Równanie stanu gazu doskonałego 4. I zasada termodynamiki 5. Przemiany gazu doskonałego 6. Silnik cieplny 7. II zasada termodynamiki TERMODYNAMIKA Zajęcia wyrównawcze,
1. Bilans cieplny 2. Przejścia fazowe 3. Równanie stanu gazu doskonałego 4. I zasada termodynamiki 5. Przemiany gazu doskonałego 6. Silnik cieplny 7. II zasada termodynamiki TERMODYNAMIKA Zajęcia wyrównawcze,
Jednostki podstawowe. Tuż po Wielkim Wybuchu temperatura K Teraz ok. 3K. Długość metr m
 TERMODYNAMIKA Jednostki podstawowe Wielkość Nazwa Symbol Długość metr m Masa kilogramkg Czas sekunda s Natężenieprąduelektrycznego amper A Temperaturatermodynamicznakelwin K Ilość materii mol mol Światłość
TERMODYNAMIKA Jednostki podstawowe Wielkość Nazwa Symbol Długość metr m Masa kilogramkg Czas sekunda s Natężenieprąduelektrycznego amper A Temperaturatermodynamicznakelwin K Ilość materii mol mol Światłość
Teoria kinetyczna gazów
 Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
Teoria kinetyczna gazów Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy ciepło właściwe przy
Gaz rzeczywisty zachowuje się jak modelowy gaz doskonały, gdy ma małą gęstość i umiarkowaną
 F-Gaz doskonaly/ GAZY DOSKONAŁE i PÓŁDOSKONAŁE Gaz doskonały cząsteczki są bardzo małe w porównaniu z objętością naczynia, które wypełnia gaz cząsteczki poruszają się chaotycznie ruchem postępowym i zderzają
F-Gaz doskonaly/ GAZY DOSKONAŁE i PÓŁDOSKONAŁE Gaz doskonały cząsteczki są bardzo małe w porównaniu z objętością naczynia, które wypełnia gaz cząsteczki poruszają się chaotycznie ruchem postępowym i zderzają
Wykład 6: Przekazywanie energii elementy termodynamiki
 Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
Termodynamika Techniczna dla MWT, wykład 6. AJ Wojtowicz IF UMK
 Wykład 6. Ciepło właściwe substancji prostych. Ciepło właściwe gazów doskonałych.. Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C )... ZaleŜność ciepła właściwego C od temperatury.. Molowe
Wykład 6. Ciepło właściwe substancji prostych. Ciepło właściwe gazów doskonałych.. Molowe ciepło właściwe gazu doskonałego przy stałej objętości (C )... ZaleŜność ciepła właściwego C od temperatury.. Molowe
Podstawy fizyki sezon 1 X. Elementy termodynamiki
 Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
Podstawy fizyki sezon 1 X. Elementy termodynamiki Agnieszka Obłąkowska-Mucha AGH, WFIiS, Katedra Oddziaływań i Detekcji Cząstek, D11, pok. 111 amucha@agh.edu.pl http://home.agh.edu.pl/~amucha Temodynamika
FIZYKA STATYSTYCZNA. Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych
 FIZYKA STATYSTYCZA Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych elementów takich jak atomy czy cząsteczki. Badanie ruchów pojedynczych cząstek byłoby bardzo trudnym
FIZYKA STATYSTYCZA Liczne eksperymenty dowodzą, że ciała składają się z wielkiej liczby podstawowych elementów takich jak atomy czy cząsteczki. Badanie ruchów pojedynczych cząstek byłoby bardzo trudnym
GAZ DOSKONAŁY. Brak oddziaływań między cząsteczkami z wyjątkiem zderzeń idealnie sprężystych.
 TERMODYNAMIKA GAZ DOSKONAŁY Gaz doskonały to abstrakcyjny, matematyczny model gazu, chociaż wiele gazów (azot, tlen) w warunkach normalnych zachowuje się w przybliżeniu jak gaz doskonały. Model ten zakłada:
TERMODYNAMIKA GAZ DOSKONAŁY Gaz doskonały to abstrakcyjny, matematyczny model gazu, chociaż wiele gazów (azot, tlen) w warunkach normalnych zachowuje się w przybliżeniu jak gaz doskonały. Model ten zakłada:
Wykład FIZYKA I. 14. Termodynamika fenomenologiczna cz.ii. Dr hab. inż. Władysław Artur Woźniak
 Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
Wykład FIZYKA I 14. Termodynamika fenomenologiczna cz.ii Dr hab. inż. Władysław Artur Woźniak Instytut Fizyki Politechniki Wrocławskiej http://www.if.pwr.wroc.pl/~wozniak/fizyka1.html GAZY DOSKONAŁE Przez
Wykład 6: Przekazywanie energii elementy termodynamiki
 Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
Wykład 6: Przekazywanie energii elementy termodynamiki dr inż. Zbigniew Szklarski szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Temperatura Fenomenologicznie wielkość informująca o tym jak
Układ termodynamiczny Parametry układu termodynamicznego Proces termodynamiczny Układ izolowany Układ zamknięty Stan równowagi termodynamicznej
 termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
Termodynamika. Część 12. Procesy transportu. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 12 Procesy transportu Janusz Brzychczyk, Instytut Fizyki UJ Zjawiska transportu Zjawiska transportu są typowymi procesami nieodwracalnymi zachodzącymi w przyrodzie. Zjawiska te polegają
Termodynamika Część 12 Procesy transportu Janusz Brzychczyk, Instytut Fizyki UJ Zjawiska transportu Zjawiska transportu są typowymi procesami nieodwracalnymi zachodzącymi w przyrodzie. Zjawiska te polegają
Stany materii. Masa i rozmiary cząstek. Masa i rozmiary cząstek. m n mol. n = Gaz doskonały. N A = 6.022x10 23
 Stany materii Masa i rozmiary cząstek Masą atomową ierwiastka chemicznego nazywamy stosunek masy atomu tego ierwiastka do masy / atomu węgla C ( C - izoto węgla o liczbie masowej ). Masą cząsteczkową nazywamy
Stany materii Masa i rozmiary cząstek Masą atomową ierwiastka chemicznego nazywamy stosunek masy atomu tego ierwiastka do masy / atomu węgla C ( C - izoto węgla o liczbie masowej ). Masą cząsteczkową nazywamy
WSTĘP DO ĆWICZEŃ DOTYCZĄCYCH CIEPŁA WŁAŚCIWEGO
 W3 WSTĘP DO ĆWICZEŃ DOTYCZĄCYCH CIEPŁA WŁAŚCIWEGO Ciepło właściwe jest jedną z podstawowych cech termodynamicznych ciał, mającą duże znaczenie praktyczne. Zależność ciepła właściwego różnych ciał od temperatury
W3 WSTĘP DO ĆWICZEŃ DOTYCZĄCYCH CIEPŁA WŁAŚCIWEGO Ciepło właściwe jest jedną z podstawowych cech termodynamicznych ciał, mającą duże znaczenie praktyczne. Zależność ciepła właściwego różnych ciał od temperatury
Wykład 4. Przypomnienie z poprzedniego wykładu
 Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Rozwiązanie: Rozwiązanie najlepiej rozpocząć od sporządzenia szkicu, który jest pierwszym stopniem zrozumienia opisywanego procesu (serii przemian).
 Nowe zadania z termodynamiki. 06.0.00. Zadanie. 0/8, moli gazu azotu (traktować jako gaz doskonały), znajdującego się początkowo (stan ) w warunkach T =00K, =0 a, przechodzi następującą serię przemian
Nowe zadania z termodynamiki. 06.0.00. Zadanie. 0/8, moli gazu azotu (traktować jako gaz doskonały), znajdującego się początkowo (stan ) w warunkach T =00K, =0 a, przechodzi następującą serię przemian
Wykład 1 i 2. Termodynamika klasyczna, gaz doskonały
 Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
TERMODYNAMIKA. przykłady zastosowań. I.Mańkowski I LO w Lęborku
 TERMODYNAMIKA przykłady zastosowań I.Mańkowski I LO w Lęborku 2016 UKŁAD TERMODYNAMICZNY Dla przykładu układ termodynamiczny stanowią zamknięty cylinder z ruchomym tłokiem, w którym znajduje się gaz tak
TERMODYNAMIKA przykłady zastosowań I.Mańkowski I LO w Lęborku 2016 UKŁAD TERMODYNAMICZNY Dla przykładu układ termodynamiczny stanowią zamknięty cylinder z ruchomym tłokiem, w którym znajduje się gaz tak
Przegląd termodynamiki II
 Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
Wykład II Mechanika statystyczna 1 Przegląd termodynamiki II W poprzednim wykładzie po wprowadzeniu podstawowych pojęć i wielkości, omówione zostały pierwsza i druga zasada termodynamiki. Tutaj wykorzystamy
Wykład 7 Entalpia: odwracalne izobaryczne rozpręŝanie gazu, adiabatyczne dławienie gazu dla przepływu ustalonego, nieodwracalne napełnianie gazem
 Wykład 7 Entalpia: odwracalne izobaryczne rozpręŝanie gazu, adiabatyczne dławienie gazu dla przepływu ustalonego, nieodwracalne napełnianie gazem pustego zbiornika rzy metody obliczeń entalpii gazu doskonałego
Wykład 7 Entalpia: odwracalne izobaryczne rozpręŝanie gazu, adiabatyczne dławienie gazu dla przepływu ustalonego, nieodwracalne napełnianie gazem pustego zbiornika rzy metody obliczeń entalpii gazu doskonałego
Temperatura jest wspólną własnością dwóch ciał, które pozostają ze sobą w równowadze termicznej.
 1 Ciepło jest sposobem przekazywania energii z jednego ciała do drugiego. Ciepło przepływa pod wpływem różnicy temperatur. Jeżeli ciepło nie przepływa mówimy o stanie równowagi termicznej. Zerowa zasada
1 Ciepło jest sposobem przekazywania energii z jednego ciała do drugiego. Ciepło przepływa pod wpływem różnicy temperatur. Jeżeli ciepło nie przepływa mówimy o stanie równowagi termicznej. Zerowa zasada
Wyznaczanie momentów bezwładności brył sztywnych metodą zawieszenia trójnitkowego
 POLTECHNKA ŚLĄSKA WYDZAŁ CHEMCZNY KATEDRA FZYKOCHEM TECHNOLOG POLMERÓW LABORATORUM Z FZYK Wyznaczanie momentów bezwładności brył sztywnych metodą zawieszenia trójnitkowego WYZNACZANE MOMENTÓW BEZWŁADNOŚC
POLTECHNKA ŚLĄSKA WYDZAŁ CHEMCZNY KATEDRA FZYKOCHEM TECHNOLOG POLMERÓW LABORATORUM Z FZYK Wyznaczanie momentów bezwładności brył sztywnych metodą zawieszenia trójnitkowego WYZNACZANE MOMENTÓW BEZWŁADNOŚC
Zasady oceniania karta pracy
 Zadanie 1.1. 5) stosuje zasadę zachowania energii oraz zasadę zachowania pędu do opisu zderzeń sprężystych i niesprężystych. Zderzenie, podczas którego wózki łączą się ze sobą, jest zderzeniem niesprężystym.
Zadanie 1.1. 5) stosuje zasadę zachowania energii oraz zasadę zachowania pędu do opisu zderzeń sprężystych i niesprężystych. Zderzenie, podczas którego wózki łączą się ze sobą, jest zderzeniem niesprężystym.
Termodynamika. Część 4. Procesy izoparametryczne Entropia Druga zasada termodynamiki. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
1 I zasada termodynamiki
 1 I zasada termodynamiki 1.1 Pojęcie podstawowe W chemii fizycznej wszechświat dzielimy na dwie części : układ i otoczenie. Układ jest interesującą nas częścią rzeczywistości (przyrody, wszechświata) może
1 I zasada termodynamiki 1.1 Pojęcie podstawowe W chemii fizycznej wszechświat dzielimy na dwie części : układ i otoczenie. Układ jest interesującą nas częścią rzeczywistości (przyrody, wszechświata) może
Gaz doskonały w ujęciu teorii kinetycznej; ciśnienie gazu
 Wykład 5 Gaz doskonały w ujęciu teorii kinetycznej; ciśnienie gazu Prędkość średnia kwadratowa cząsteczek gazu doskonałego Rozkład Maxwella prędkości cząsteczek gazu doskonałego Średnia energia kinetyczna
Wykład 5 Gaz doskonały w ujęciu teorii kinetycznej; ciśnienie gazu Prędkość średnia kwadratowa cząsteczek gazu doskonałego Rozkład Maxwella prędkości cząsteczek gazu doskonałego Średnia energia kinetyczna
b) Wybierz wszystkie zdania prawdziwe, które odnoszą się do przemiany 2.
 Sprawdzian 8A. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach. a) Wybierz spośród nich wszystkie zdania
Sprawdzian 8A. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach. a) Wybierz spośród nich wszystkie zdania
b) Wybierz wszystkie zdania prawdziwe, które odnoszą się do przemiany 2.
 Fizyka Z fizyką w przyszłość Sprawdzian 8B Sprawdzian 8B. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach.
Fizyka Z fizyką w przyszłość Sprawdzian 8B Sprawdzian 8B. Gaz doskonały przeprowadzono ze stanu P do stanu K dwoma sposobami: i, tak jak pokazano na rysunku. Poniżej napisano kilka zdań o tych przemianach.
Materiały pomocnicze do laboratorium z przedmiotu Metody i Narzędzia Symulacji Komputerowej
 Materiały pomocnicze do laboratorium z przedmiotu Metody i Narzędzia Symulacji Komputerowej w Systemach Technicznych Symulacja prosta dyszy pomiarowej Bendemanna Opracował: dr inż. Andrzej J. Zmysłowski
Materiały pomocnicze do laboratorium z przedmiotu Metody i Narzędzia Symulacji Komputerowej w Systemach Technicznych Symulacja prosta dyszy pomiarowej Bendemanna Opracował: dr inż. Andrzej J. Zmysłowski
Fizyka 14. Janusz Andrzejewski
 Fizyka 14 Janusz Andrzejewski Egzaminy Egzaminy odbywają się w salach 3 oraz 314 budynek A1 w godzinach od 13.15 do 15.00 I termin 4 luty 013 poniedziałek II termin 1 luty 013 wtorek Na wykład zapisanych
Fizyka 14 Janusz Andrzejewski Egzaminy Egzaminy odbywają się w salach 3 oraz 314 budynek A1 w godzinach od 13.15 do 15.00 I termin 4 luty 013 poniedziałek II termin 1 luty 013 wtorek Na wykład zapisanych
00516 Termodynamika D Część 1
 1 00516 Termodynamika D Dane osobowe właściciela arkusza 00516 Termodynamika D Część 1 Energia wewnętrzna. I zasada termodynamiki Ciepło właściwe i przemiany fazowej Model gazów doskonałych Aktualizacja
1 00516 Termodynamika D Dane osobowe właściciela arkusza 00516 Termodynamika D Część 1 Energia wewnętrzna. I zasada termodynamiki Ciepło właściwe i przemiany fazowej Model gazów doskonałych Aktualizacja
Kontakt,informacja i konsultacje
 Kontakt,informacja i konsultacje Chemia A ; pokój 307 elefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl tablica ogłoszeń Katedry Chemii Fizycznej http://www.pg.gda.pl/chem/dydaktyka/ lub http://www.pg.gda.pl/chem/katedry/fizyczna
Kontakt,informacja i konsultacje Chemia A ; pokój 307 elefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl tablica ogłoszeń Katedry Chemii Fizycznej http://www.pg.gda.pl/chem/dydaktyka/ lub http://www.pg.gda.pl/chem/katedry/fizyczna
będzie momentem Twierdzenie Steinera
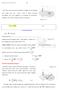 Wykład z fizyki, Piotr Posmykiewicz. Niech 90 oznacza moment bezwładności względem osi przechodzącej przez środek masy ciała o masie i niech będzie momentem bezwładności tego ciała względem osi równoległej
Wykład z fizyki, Piotr Posmykiewicz. Niech 90 oznacza moment bezwładności względem osi przechodzącej przez środek masy ciała o masie i niech będzie momentem bezwładności tego ciała względem osi równoległej
Temperatura i energia kinetyczna gazów.
 Wykład z fizyki, Piotr Posmykiewicz 49 W Y K Ł A D XII Temperatura i energia kinetyczna gazów. Temperatura jest nam wszystkim znana jako miara tego czy ciało jest ciepłe, czy zimne. W wykładzie tym pokaŝemy,
Wykład z fizyki, Piotr Posmykiewicz 49 W Y K Ł A D XII Temperatura i energia kinetyczna gazów. Temperatura jest nam wszystkim znana jako miara tego czy ciało jest ciepłe, czy zimne. W wykładzie tym pokaŝemy,
FIZYKA CZĄSTECZKOWA I TERMODYNAMIKA
 FIZYKA CZĄSTECZKOWA I TERMODYNAMIKA Fizyka - cząsteczkowa Dział fizyki badający budowę i własności aterii przy założeniu, że każde ciało składa się z dużej liczby bardzo ałych cząsteczek. Cząsteczki te
FIZYKA CZĄSTECZKOWA I TERMODYNAMIKA Fizyka - cząsteczkowa Dział fizyki badający budowę i własności aterii przy założeniu, że każde ciało składa się z dużej liczby bardzo ałych cząsteczek. Cząsteczki te
Wykład Praca (1.1) c Całka liniowa definiuje pracę wykonaną w kierunku działania siły. Reinhard Kulessa 1
 1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
3. Przyrost temperatury gazu wynosi 20 C. Ile jest równy ten przyrost w kelwinach?
 1. Która z podanych niżej par wielkości fizycznych ma takie same jednostki? a) energia i entropia b) ciśnienie i entalpia c) praca i entalpia d) ciepło i temperatura 2. 1 kj nie jest jednostką a) entropii
1. Która z podanych niżej par wielkości fizycznych ma takie same jednostki? a) energia i entropia b) ciśnienie i entalpia c) praca i entalpia d) ciepło i temperatura 2. 1 kj nie jest jednostką a) entropii
Termodynamika cz. 2. Gaz doskonały. Gaz doskonały... Gaz doskonały... Notes. Notes. Notes. Notes. dr inż. Ireneusz Owczarek
 Termodynamika cz. 2 dr inż. Ireneusz Owczarek CNMiF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 1 dr inż. Ireneusz Owczarek Termodynamika cz. 2 Gaz doskonały Definicja makroskopowa (termodynamiczna)
Termodynamika cz. 2 dr inż. Ireneusz Owczarek CNMiF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 1 dr inż. Ireneusz Owczarek Termodynamika cz. 2 Gaz doskonały Definicja makroskopowa (termodynamiczna)
1. PIERWSZA I DRUGA ZASADA TERMODYNAMIKI TERMOCHEMIA
 . PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
. PIERWSZA I DRUGA ZASADA ERMODYNAMIKI ERMOCHEMIA Zadania przykładowe.. Jeden mol jednoatomowego gazu doskonałego znajduje się początkowo w warunkach P = 0 Pa i = 300 K. Zmiana ciśnienia do P = 0 Pa nastąpiła:
ZADANIA Z FIZYKI - TERMODYNAMIKA
 ZADANIA Z FIZYKI - TERMODYNAMIKA Zad 1.(RH par 22-8 zad 36) Cylinder jest zamknięty dobrze dopasowanym metalowym tłokiem o masie 2 kg i polu powierzchni 2.0 cm 2. Cylinder zawiera wodę i parę o temperaturze
ZADANIA Z FIZYKI - TERMODYNAMIKA Zad 1.(RH par 22-8 zad 36) Cylinder jest zamknięty dobrze dopasowanym metalowym tłokiem o masie 2 kg i polu powierzchni 2.0 cm 2. Cylinder zawiera wodę i parę o temperaturze
Stany skupienia materii
 Stany skupienia materii Ciała stałe Ciecze Płyny Gazy Plazma 1 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -
Stany skupienia materii Ciała stałe Ciecze Płyny Gazy Plazma 1 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -
Termodynamika. Energia wewnętrzna ciał
 ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
ermodynamika Energia wewnętrzna ciał Cząsteczki ciał stałych, cieczy i gazów znajdują się w nieustannym ruchu oddziałując ze sobą. Sumę energii kinetycznej oraz potencjalnej oddziałujących cząsteczek nazywamy
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
ĆWICZENIE 3 REZONANS AKUSTYCZNY
 ĆWICZENIE 3 REZONANS AKUSTYCZNY W trakcie doświadczenia przeprowadzono sześć pomiarów rezonansu akustycznego: dla dwóch różnych gazów (powietrza i CO), pięć pomiarów dla powietrza oraz jeden pomiar dla
ĆWICZENIE 3 REZONANS AKUSTYCZNY W trakcie doświadczenia przeprowadzono sześć pomiarów rezonansu akustycznego: dla dwóch różnych gazów (powietrza i CO), pięć pomiarów dla powietrza oraz jeden pomiar dla
Wykład 3. Entropia i potencjały termodynamiczne
 Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Termodynamika program wykładu
 Termodynamika program wykładu Wiadomości wstępne: fizyka statystyczna a termodynamika masa i rozmiary cząstek stan układu, przemiany energia wewnętrzna pierwsza zasada termodynamiki praca wykonana przez
Termodynamika program wykładu Wiadomości wstępne: fizyka statystyczna a termodynamika masa i rozmiary cząstek stan układu, przemiany energia wewnętrzna pierwsza zasada termodynamiki praca wykonana przez
Absolutna skala temperatur.
 Wykład z fizyki, Piotr Posmykiewicz 88 Absolutna skala temperatur. W wykładzie XII skala temperatur dla gazu doskonałego została zdefiniowana za pomocą własności gazów posiadających małą gęstość. PoniewaŜ
Wykład z fizyki, Piotr Posmykiewicz 88 Absolutna skala temperatur. W wykładzie XII skala temperatur dla gazu doskonałego została zdefiniowana za pomocą własności gazów posiadających małą gęstość. PoniewaŜ
Wykład 1. Anna Ptaszek. 5 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 1. Anna Ptaszek 1 / 36
 Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
100 29,538 21,223 38,112 29, ,118 24,803 49,392 41,077
 . Jak określa się ilość substancji? Ile kilogramów substancji zawiera mol wody?. Zbiornik zawiera 5 kmoli CO. Ile kilogramów CO znajduje się w zbiorniku? 3. Jaka jest definicja I zasady termodynamiki dla
. Jak określa się ilość substancji? Ile kilogramów substancji zawiera mol wody?. Zbiornik zawiera 5 kmoli CO. Ile kilogramów CO znajduje się w zbiorniku? 3. Jaka jest definicja I zasady termodynamiki dla
VII.1 Pojęcia podstawowe.
 II.1 Pojęcia podstawowe. Jan Królikowski Fizyka IBC 1 Model matematyczny ciała sztywnego Zbiór punktów materialnych takich, że r r = const; i, j= 1,... N i j Ciało sztywne nie ulega odkształceniom w wyniku
II.1 Pojęcia podstawowe. Jan Królikowski Fizyka IBC 1 Model matematyczny ciała sztywnego Zbiór punktów materialnych takich, że r r = const; i, j= 1,... N i j Ciało sztywne nie ulega odkształceniom w wyniku
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny
 Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 7 Trzecia zasada termodynamiki Metody otrzymywania niskich temperatur Zjawisko Joule'a Thomsona Chłodzenie magnetyczne
 Termodynamika Część 7 Trzecia zasada termodynamiki Metody otrzymywania niskich temperatur Zjawisko Joule'a Thomsona Chłodzenie magnetyczne Janusz Brzychczyk, Instytut Fizyki UJ Postulat Nernsta (1906):
Termodynamika Część 7 Trzecia zasada termodynamiki Metody otrzymywania niskich temperatur Zjawisko Joule'a Thomsona Chłodzenie magnetyczne Janusz Brzychczyk, Instytut Fizyki UJ Postulat Nernsta (1906):
podać przykład wielkości fizycznej, która jest iloczynem wektorowym dwóch wektorów.
 PLAN WYNIKOWY FIZYKA - KLASA TRZECIA TECHNIKUM 1. Ruch postępowy i obrotowy bryły sztywnej Lp. Temat lekcji Treści podstawowe 1 Iloczyn wektorowy dwóch wektorów podać przykład wielkości fizycznej, która
PLAN WYNIKOWY FIZYKA - KLASA TRZECIA TECHNIKUM 1. Ruch postępowy i obrotowy bryły sztywnej Lp. Temat lekcji Treści podstawowe 1 Iloczyn wektorowy dwóch wektorów podać przykład wielkości fizycznej, która
Podstawy fizyki wykład 4
 Podstawy fizyki wykład 4 Dr Piotr Sitarek Instytut Fizyki, Politechnika Wrocławska Dynamika Obroty wielkości liniowe a kątowe energia kinetyczna w ruchu obrotowym moment bezwładności moment siły II zasada
Podstawy fizyki wykład 4 Dr Piotr Sitarek Instytut Fizyki, Politechnika Wrocławska Dynamika Obroty wielkości liniowe a kątowe energia kinetyczna w ruchu obrotowym moment bezwładności moment siły II zasada
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
1. 1 J/(kg K) nie jest jednostką a) entropii właściwej b) indywidualnej stałej gazowej c) ciepła właściwego d) pracy jednostkowej
 1. 1 J/(kg K) nie jest jednostką a) entropii właściwej b) indywidualnej stałej gazowej c) ciepła właściwego d) pracy jednostkowej 2. 1 kmol każdej substancji charakteryzuje się taką samą a) masą b) objętością
1. 1 J/(kg K) nie jest jednostką a) entropii właściwej b) indywidualnej stałej gazowej c) ciepła właściwego d) pracy jednostkowej 2. 1 kmol każdej substancji charakteryzuje się taką samą a) masą b) objętością
Nazwisko i imię: Zespół: Data: Ćwiczenie nr 1: Wahadło fizyczne. opis ruchu drgającego a w szczególności drgań wahadła fizycznego
 Nazwisko i imię: Zespół: Data: Cel ćwiczenia: Ćwiczenie nr 1: Wahadło fizyczne opis ruchu drgającego a w szczególności drgań wahadła fizycznego wyznaczenie momentów bezwładności brył sztywnych Literatura
Nazwisko i imię: Zespół: Data: Cel ćwiczenia: Ćwiczenie nr 1: Wahadło fizyczne opis ruchu drgającego a w szczególności drgań wahadła fizycznego wyznaczenie momentów bezwładności brył sztywnych Literatura
WYZNACZANIE STOSUNKU c p /c v
 Uniwersytet Wrocławski, Instytut Fizyki Doświadczalnej, I Pracownia Ćwiczenie nr 33 WYZNACZANIE STOSUNKU c p /c v I WSTĘP Układ termodynamiczny Rozważania dotyczące przekazywania energii poprzez wykonywanie
Uniwersytet Wrocławski, Instytut Fizyki Doświadczalnej, I Pracownia Ćwiczenie nr 33 WYZNACZANIE STOSUNKU c p /c v I WSTĘP Układ termodynamiczny Rozważania dotyczące przekazywania energii poprzez wykonywanie
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY
 WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
TERMODYNAMIKA. Termodynamika jest to dział nauk przyrodniczych zajmujący się własnościami
 TERMODYNAMIKA Termodynamika jest to dział nauk rzyrodniczych zajmujący się własnościami energetycznymi ciał. Przy badaniu i objaśnianiu własności układów fizycznych termodynamika osługuje się ojęciami
TERMODYNAMIKA Termodynamika jest to dział nauk rzyrodniczych zajmujący się własnościami energetycznymi ciał. Przy badaniu i objaśnianiu własności układów fizycznych termodynamika osługuje się ojęciami
Termodynamika Termodynamika
 Termodynamika 1. Wiśniewski S.: Termodynamika techniczna, WNT, Warszawa 1980, 1987, 1993. 2. Jarosiński J., Wiejacki Z., Wiśniewski S.: Termodynamika, skrypt PŁ. Łódź 1993. 3. Zbiór zadań z termodynamiki
Termodynamika 1. Wiśniewski S.: Termodynamika techniczna, WNT, Warszawa 1980, 1987, 1993. 2. Jarosiński J., Wiejacki Z., Wiśniewski S.: Termodynamika, skrypt PŁ. Łódź 1993. 3. Zbiór zadań z termodynamiki
Prędkośd rozchodzenia się sprężystych fal podłużnych w ciałach stałych, cieczach i
 1 S t r o n a 6. Prędkośd rozchodzenia się sprężystych fal podłużnych w ciałach stałych, cieczach i gazach. Prawo Hooke a: Siła sprężystości: F Xsp = k. 0) Co do wartości bezwzględnej jest ona równa (lub
1 S t r o n a 6. Prędkośd rozchodzenia się sprężystych fal podłużnych w ciałach stałych, cieczach i gazach. Prawo Hooke a: Siła sprężystości: F Xsp = k. 0) Co do wartości bezwzględnej jest ona równa (lub
Rozważmy nieustalony, adiabatyczny, jednowymiarowy ruch gazu nielepkiego i nieprzewodzącego ciepła. Mamy następujące równania rządzące tym ruchem:
 WYKŁAD 13 DYNAMIKA MAŁYCH (AKUSTYCZNYCH) ZABURZEŃ W GAZIE Rozważmy nieustalony, adiabatyczny, jednowymiarowy ruch gazu nielepkiego i nieprzewodzącego ciepła. Mamy następujące równania rządzące tym ruchem:
WYKŁAD 13 DYNAMIKA MAŁYCH (AKUSTYCZNYCH) ZABURZEŃ W GAZIE Rozważmy nieustalony, adiabatyczny, jednowymiarowy ruch gazu nielepkiego i nieprzewodzącego ciepła. Mamy następujące równania rządzące tym ruchem:
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab.
 WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa
 Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Plan wynikowy fizyka rozszerzona klasa 3a
 Plan wynikowy fizyka rozszerzona klasa 3a 1. Hydrostatyka Temat lekcji dostateczną uczeń Ciśnienie hydrostatyczne. Prawo Pascala zdefiniować ciśnienie, objaśnić pojęcie ciśnienia hydrostatycznego, objaśnić
Plan wynikowy fizyka rozszerzona klasa 3a 1. Hydrostatyka Temat lekcji dostateczną uczeń Ciśnienie hydrostatyczne. Prawo Pascala zdefiniować ciśnienie, objaśnić pojęcie ciśnienia hydrostatycznego, objaśnić
PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ
 LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ . Cel ćwiczenia Doświadczalne i teoretyczne wyznaczenie profilu prędkości w rurze prostoosiowej 2. Podstawy teoretyczne:
LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ . Cel ćwiczenia Doświadczalne i teoretyczne wyznaczenie profilu prędkości w rurze prostoosiowej 2. Podstawy teoretyczne:
Testy Która kombinacja jednostek odpowiada paskalowi? N/m, N/m s 2, kg/m s 2,N/s, kg m/s 2
 Testy 3 40. Która kombinacja jednostek odpowiada paskalowi? N/m, N/m s 2, kg/m s 2,N/s, kg m/s 2 41. Balonik o masie 10 g spada ze stałą prędkością w powietrzu. Jaka jest siła wyporu? Jaka jest średnica
Testy 3 40. Która kombinacja jednostek odpowiada paskalowi? N/m, N/m s 2, kg/m s 2,N/s, kg m/s 2 41. Balonik o masie 10 g spada ze stałą prędkością w powietrzu. Jaka jest siła wyporu? Jaka jest średnica
15 Kinetyczna teoria gazów i termodynamika I
 MODUŁ Moduł Kinetyczna teoria gazów i termodynamika I 5 Kinetyczna teoria gazów i termodynamika I ermodynamika zajmuje się właściwościami cieplnymi układów makroskopowych, zaniedbując w odróżnieniu od
MODUŁ Moduł Kinetyczna teoria gazów i termodynamika I 5 Kinetyczna teoria gazów i termodynamika I ermodynamika zajmuje się właściwościami cieplnymi układów makroskopowych, zaniedbując w odróżnieniu od
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1. Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski
 Chemia Fizyczna Technologia Chemiczna II rok Wykład 1 Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski Kontakt,informacja i konsultacje Chemia A ; pokój 307 Telefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl
Chemia Fizyczna Technologia Chemiczna II rok Wykład 1 Kierownik przedmiotu: Dr hab. inż. Wojciech Chrzanowski Kontakt,informacja i konsultacje Chemia A ; pokój 307 Telefon: 347-2769 E-mail: wojtek@chem.pg.gda.pl
Podstawy fizyki wykład 4
 Podstawy fizyki wykład 4 Dr Piotr Sitarek Katedra Fizyki Doświadczalnej, W11, PWr Dynamika Obroty wielkości liniowe a kątowe energia kinetyczna w ruchu obrotowym moment bezwładności moment siły II zasada
Podstawy fizyki wykład 4 Dr Piotr Sitarek Katedra Fizyki Doświadczalnej, W11, PWr Dynamika Obroty wielkości liniowe a kątowe energia kinetyczna w ruchu obrotowym moment bezwładności moment siły II zasada
Wyznaczanie stałej szybkości reakcji wymiany jonowej
 Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
K raków 26 ma rca 2011 r.
 K raków 26 ma rca 2011 r. Zadania do ćwiczeń z Podstaw Fizyki na dzień 1 kwietnia 2011 r. r. dla Grupy II Zadanie 1. 1 kg/s pary wo dne j o ciśnieniu 150 atm i temperaturze 342 0 C wpada do t urbiny z
K raków 26 ma rca 2011 r. Zadania do ćwiczeń z Podstaw Fizyki na dzień 1 kwietnia 2011 r. r. dla Grupy II Zadanie 1. 1 kg/s pary wo dne j o ciśnieniu 150 atm i temperaturze 342 0 C wpada do t urbiny z
