(U.13) Atom wodoropodobny
|
|
|
- Konrad Antczak
- 7 lat temu
- Przeglądów:
Transkrypt
1 U.13 Atom wodoropodobny 122 Rozdział 3 U.13 Atom wodoropodobny 3.1 Model Bohra przypomnienie Zaznaczmy na wstępie o czym już wspominaliśmy w kontekście zasady nieoznaczoności, że model Bohra jest niezgodny z przewidywaniami mechaniki kwantowej. Jest on jednak znaczący ze względów historycznych, a ponadto daje pewne intuicyjne pojęcie o budowie atomu. Rzeczą zdumiewającą jest natomiast, że mimo swej błędności, niektóre wyniki otrzymane w ramach modelu Bohra są identyczne ze ścisłymi wynikami mechaniki kwantowej Postulaty Bohra Model Bohra opisuje atom wodoropodobny, to jest atom złożony z jądra o ładunku Ze wokół którego krąży pojedynczy elektron. Model ten bazuje na dwóch następujących założeniach. Elektron porusza się po orbicie kołowej wokół jądra pojęcie trajektorii!!!. Siła Coulomba jest siłą dośrodkową ruch w układzie środka masy v 2 r = 1 πε 0 Ze 2 r 2 = β r Energia elektronu jest sumą energii kinetycznej i potencjalnej E = 1 2 v2 β r. 3.2 Postulat Bohra: moment pędu elektronu na orbicie kołowej jest wielokrotnością stałej Plancka L = vr = n gdzie n = 1, 2, 3, Podkreślmy, że pierwsze założenie jest czysto klasyczne. Drugie postulat Bohra, określa procedurę kwantowania. Jednakże postulat ten znikąd nie wynika, jest postulatem typu ad hoc. Warto także zauważyć, że możemy postulat 3.3 zapisać 2πr = n h mv = nh p = nλ, 3. gdzie skorzystaliśmy z kolei z hipotezy de Broglie a. Warunek ten oznacza, że obwód orbity jest pełną wielokrotnością długości fali związanej z elektronem. Innymi słowy, na orbicie kołowej tworzy się fala stojąca. Tego stwierdzenia Bohr jednak nie mógł podać, bowiem hipoteza de Broglie a jest historycznie późniejsza. S.Kryszewski MECHANIKA KWANTOWA 122
2 U.13 Atom wodoropodobny Obliczenia E n i r n W ramach modelu Bohra chcemy teraz obliczyć następujące wielkości: E n dozwolone energie elektronu w atomie, r n dozwolone promienie orbit, bowiem z wprowadzonych założeń wynika, że wielkości te nie mogą przyjmować dowolnych wartości. Równania stanowią układ trzech równań z niewiadomymi v, r i E. Z równania 3.3 od razu mamy v = n r. 3.5 Zatem możemy wyeliminować prędkość w dwóch pozostałych równaniach, otrzymując w ten sposób n 2 2 r = β oraz E = n2 2 2r 2 β r. 3.6 Pierwsze z powyższych równań daje więc r = n2 2 β, 3.7 co wyznacza dozwolone wartości promienia w zależności od liczby kwantowej n. Wynik ten pozwala wyznaczyć energie z drugiego równania 3.6 E = n β 2 n β β n 2 2 = β2 2 n Promień orbity już mamy w 3.7. Zatem z 3.5 wyliczamy prędkość i dostajemy v = n r = n β n 2 2 = β n. 3.9 Zbierając wyniki i numerując je całkowitą liczbą dodatnią n mamy E n = 1 n 2 β = 1 n 2 Z 2 e 2 πε 0 2, 3.10a r n = n 2 2 β = n2 πε 0 2 Ze 2, v n = 1 n β = 1 n Ze 2 πε b 3.10c A zatem poszukiwane wielkości są skwantowane, zarówno energia elektronu jak i promień jego orbity przyjmują tylko ściśle określone wartości. Dla atomu wodoru Z = 1 najmniejsza orbita n = 1 ma promień r 1 a 0 = 2 πε 0 e który, nieprzypadkowo, nazywamy promieniem Bohra. Na orbicie o najmniejszym promieniu n = 1 elektron ma najmniejszą energię równą E 1 = β2 2 2 = Z 2 e 2 πε S.Kryszewski MECHANIKA KWANTOWA 123
3 U.13 Atom wodoropodobny 12 Aby atom zjonizować, trzeba elektronowi dostarczyć energię dodatnią o wartości równej E 1. Dlatego też energię E IB = β2 2 2 = Z 2 e 2 πε 0 2, 3.13 nazywamy energią jonizacji atomu wodoropodobnego. Zapiszmy, za pomocą wprowadzonej notacji, uzyskane wyżej wyniki E n = E IB n 2 = E I n 2 Z 2, 3.1a r n = n 2 a B = n 2 a 0 Z. 3.1b Warto także zadać sobie trud obliczenia wartości liczbowych promienia Bohra i energii jonizacji atomu wodoru. Wyniki są następujące a 0 = 2 πε 0 e Å, 3.15a E I = e 2 πε ev. 3.15b W obliczeniach tych przyjęliśmy masę zredukowaną elektronu m e. 3.2 Pęd radialny w atomie wodoropodobnym Uwagi wstępne Atom wodoropodobny jest to układ dwóch ciał elektronu i jądra atomowego, które są związane oddziaływaniem coulombowskim vr = β Ze2, gdzie β =, 3.16 r πε 0 gdzie r jest względną odległością pomiędzy cząstkami, mierzoną w układzie środka masy. Hamiltonian ruchu względnego wynikający z 1.15 ma postać Ĥ = 2 1 r 2 r 2 r r + L 2 2r 2 β r Lemat 3.1 Dla operatorów różniczkowania względem zmiennej radialnej zachodzi następująca relacja 1 r 2 r 2 r r = i 1 r r r Dowód. Niech fr będzie dowolną funkcją zmiennej radialnej. Z jednej strony mamy 1 r 2 r 2 fr = 1 r r r 2 2r fr + r 2 2 fr r r 2 = 2 r fr r 2 fr r S.Kryszewski MECHANIKA KWANTOWA 12
4 U.13 Atom wodoropodobny 125 Zaś z drugiej strony otrzymujemy i 1 r r r 2 fr = 1 r 1 r r r = 1 r r = 2 fr r r r r fr f + r f r co, na mocy dowolności funkcji fr, kończy dowód Pęd radialny Wprowadzany teraz operator pędu radialnego 2 fr r 2, 3.20 p r = 1 r r r, za pomocą którego hamiltonian 3.17 możemy zapisać w postaci 3.21 Ĥ = p2 r 2 + L 2 2r 2 β r, 3.22 gdzie oczywiście wykorzystaliśmy lemat Aby przekonać się, czy p r możemy rzeczywiście nazwać operatorem pędu radialnego, zbadamy odpowiednie relacje komutacyjne. Lemat 3.2 Niech fr będzie dowolną funkcją odległości r która, w reprezentacji położeniowej ma także sens operatorowy. Zachodzi następująca relacja komutacyjna pr, fr = fr r Dowód. Niech gr będzie inną dowolną funkcją r. Wówczas pr, fr gr = 1 r, fr gr r r = 1 r r rfrgr + fr 1 r r rgr = fg + r f g gr + rfr + r r r r fr g + r g. 3.2 r Składniki pierwszy i czwarty oraz trzeci i piąty znoszą się parami. A zatem pr, fr fr gr = gr 3.25 r i z dowolności funkcji gr wynika teza. Z wykazanej relacji 3.23 natychmiast wynika, że pr, r =, 3.26 więc pęd i zmienna radialne spełniają kanoniczną relację komutacyjną, a zatem ich interpretacja fizyczna jest poprawna. S.Kryszewski MECHANIKA KWANTOWA 125
5 U.13 Atom wodoropodobny Równania ruchu dla wielkości radialnych Rozważymy podstawowe równania ruchu dla obserwabli r i p r. Pokażemy, że dla atomu wodoropodobnego ṙ = d dt r = p r, 3.27a ṗ r = d dt p r = L 2 r 3 β r b Istotnie, z równań Heisenberga dla operatora r otrzymujemy ṙ = 1 r, Ĥ = 1 p 2 r, r 2 + L 2 2r 2 β r, Całkowity moment pędu zależy tylko od zmiennych kątowych, więc widzimy, że r komutuje z dwoma ostatnimi składnikami. Wyliczenie pozostałego komutatora jest proste, korzystając z 3.26 otrzymujemy ṙ = 1 r, p r = 2 2p r = p r, 3.29 a więc 3.27a jest udowodnione. Analogicznie dowodzimy wzoru 3.27b ṗ r = 1 pr, Ĥ = 1 pr, = 1 L 2 1 pr, pr 2r 2, p 2 r 2 + L 2 2r 2 β r, β r Operatory L 2 i p r komutują, bo zależą od różnych zmiennych kątowych i radialnych, zatem L ṗ r = 2 pr, 2 = L r 2 2 r 3 β 1 pr, r β 1 r 2 = L 2 r 3 β r 2, 3.31 co było do wykazania. Relacje dotyczące pochodnych czasowych operatorów radialnych okażą się być pożyteczne w dalszych zastosowaniach. 3.3 Wzór rekurencyjny Kramersa dla r s nl Celem naszych rozważań jest wyprowadzenie, podanego w części głównej wykładu bez dowodu, wzoru rekurencyjnego Kramersa 0 = s + 1 n 2 r s nl 2s + 1 a 0 Z rs 1 nl + s 2l s 2 a 2 0 Z 2 rs 2 nl, 3.32 gdzie r s nl jest wartością oczekiwaną s-tej potęgi odległości pomiędzy elektronem a jądrem atomu wodoropodobnego, obliczaną w stanach własnych energii atomu r s nl = ψ nlm r s ψ nlm = 0 dr r s+2 Rnl 2 r Obliczanie całek 3.33, gdzie funkcje radialne dane są wzorem jest za wyjątkiem kilku przypadków bardzo żmudne. Zaprezentujemy tu metodę wyprowadzenia relacji 3.32 pozwalającą uniknąć jakiegokolwiek całkowania. S.Kryszewski MECHANIKA KWANTOWA 126
6 U.13 Atom wodoropodobny Zastosowanie twierdzenia o wiriale Przystępujemy do wyprowadzenia relacji rekurencyjnej Wszelkie występujące tu średnie obliczamy w stanach własnych hamiltonianu atomu wodoropodobnego. Możemy więc skorzystać z tzw. uogólnionego twierdzenia o wiriale 25.27, które orzeka, że wartość oczekiwana pochodnej czasowej dowolnej obserwabli obliczana w stanie własnym hamiltonianu jest równa zeru. A zatem, w szczególności, dla atomu wodoropodobnego możemy napisać d p r r s+1 = ψ nlm d p r r s+1 ψ nlm = dt nl dt Powyższe stwierdzenie jest naszym punktem wyjścia, który teraz musimy odpowiednio przekształcić. Obliczmy pochodną czasową występującą po lewej stronie, pamiętając, że ṙ jest proporcjonalne do p r, więc nie komutuje z r. Zgodnie z regułami różniczkowania, z 3.3 otrzymujemy 0 = ṗ r r s+1 nl + p r r k ṙ r s k nl Stosujemy teraz pochodne = 1 L 2 r s 2 nl β r s 1 nl + 1 p r r k p r r s k nl Stany ψ nlm w których obliczamy występujące tu średnie są stanami własnymi nie tylko hamiltonianu Ĥ, ale także momentu pędu L 2 i L 3. Wobec tego 0 = 2 ll + 1 r s 2 nl β r s 1 nl + 1 p r r k p r r s k nl 3.37 i cały problem sprowadza się do umiejętnego przekształcenia ostatniego członu Wykorzystanie równań ruchu dla wielkości radialnych Na mocy relacji 3.23 możemy napisać pr, r k = k r k 1, 3.38 lub równoważnie p r r k + k r k 1 = r k p r A zatem ostatni człon w 3.37 to P s = 1 p r r k p r r s k nl = 1 = 1 p r pr r k + k r k 1 r s k nl p 2 r r s nl + k p r r s 1 nl. 3.0 Pierwszy człon nie zależy od indeksu sumowania. Występuję on w każdym składniku, a więc pojawia się s+1-krotnie. W drugim członie sumowaniu podlega jedynie czynnik k. W rezultacie mamy P s = s + 1 p2 r r s nl + p r r s 1 nl s + 1 = p 2 r rs nl + 2 ss + 1 p r r s 1 nl, 3.1 bowiem suma w pierwszej linii jest dobrze znana. Pozostały nam więc do obliczenia dwie wartości oczekiwane. k S.Kryszewski MECHANIKA KWANTOWA 127
7 U.13 Atom wodoropodobny Pomocnicze wartości oczekiwane Wartość oczekiwaną p 2 r r s nl obliczymy eliminując p 2 r za pomocą hamiltonianu, bowiem p 2 r = 2 Ĥ L 2 2r 2 + β r. 3.2 Wobec tego p 2 L r rs nl = 2 Ĥ 2 2r 2 + β r r s nl = 2 Ĥ rs nl L 2 r s 2 nl + 2β r s 1 nl = 2E n r s nl 2 ll + 1 r s 2 nl + 2β r s 1 nl, 3.3 bowiem stany ψ nlm są stanami własnymi hamiltonianu i całkowitego momentu pędu. Jedna z potrzebnych nam w 3.1 wartości oczekiwanych jest więc gotowa. Drugą wartość średnią, tj. p r r s 1 nl, obliczymy ponownie odwołując się do twierdzenia o wiriale, z którego wynika, że d dt rs nl = ψ nlm d dt rs+1 ψ nlm = Obliczamy teraz lewą stronę, posługując się tym samym sposobem, co poprzednio. Otrzymujemy więc 0 = s 1 = 1 = 1 r k ṙ r s k 1 nl = 1 s 1 s 1 s 1 p r r k + k r k 1 r s k 1 nl pr r s 1 nl + k r s 2 nl = s p r r s 1 nl + s 1 rs 2 nl = s p r r s 1 nl + Stąd oczywiście wynika, że ss 1 2 r k p r r s k 1 nl k r s 2 nl. 3.5 p r r s 1 nl = 2 s 1 rs 2 nl. 3.6 Druga z wartości oczekiwanych obecnych w 3.1 jest więc także obliczona. S.Kryszewski MECHANIKA KWANTOWA 128
8 U.13 Atom wodoropodobny Ostatni etap obliczeń Mamy już wszystkie niezbędne elementy wzoru Najpierw uporządkujemy ostatni człon dany w 3.1, do którego podstawiamy wyrażenia 3.3 i 3.6. Otrzymujemy więc P s = s + 1 2E n r s nl 2 ll + 1 r s 2 nl + 2β r s 1 nl + ss + 1 s 1 r s 2 nl 2 2 = 2 s + 1 E n r s nl + 2 β s + 1 r s 1 nl s + 1 ss 1 ll + 1 r s 2 nl 3.7 Wyrażenie to podstawiamy teraz zamiast ostatniego członu w 3.37 i mamy 0 = 2 ll + 1 rs 2 nl β r s 1 nl + 2 s + 1 E n r s nl + 2 β s + 1 r s 1 nl s + 1 ll + 1 ss 1 Zbieramy wyrazy zawierające te same wartości oczekiwane r s 2 nl = 2 s + 1 E n r s nl + β 2s + 1 r s 1 nl rs 2 nl ll + 1s + 1 ll + 1 ss Dalej porządkując otrzymujemy 0 = 2 s + 1 E n r s nl + β 2s + 1 r s 1 nl s rs 2 nl ll + 1 s I wreszcie zmieniamy znaki co jest wygodne dostając w końcu 0 = 2 E n s + 1 r s nl β 2s + 1 r s 1 nl + 2 s 2l s 2 r s 2 nl Formuła ta to już prawie to co chcieliśmy uzyskać. Różni się ona od wzoru 3.32 jedynie kształtem współczynników. Energie stanów własnych atomu wodoropodobnego to patrz i E n = E IB n 2 = 1 n 2 β Podstawiamy to wyrażenie do 3.51 i mnożymy stronami przez 2 /β 2. W rezultacie dostajemy 0 = s + 1 n 2 r s nl β 2s + 1 rs 1 nl + 2 β 2 s 2l s 2 r s 2 nl S.Kryszewski MECHANIKA KWANTOWA 129
9 U.13 Atom wodoropodobny 130 Przypominamy teraz, że promień Bohra to a 0 /Z = 2 /β. Wobec tego, otrzymujemy 0 = s + 1 n 2 r s nl 2s + 1 a 0 Z + s a 2 0 Z 2 rs 1 nl 2l s 2 r s 2 nl. 3.5 co jest już dokładnie związkiem rekurencyjnym Kramersa. Przykłady pewnych jego zastosowań podane są w głównej części wykładu. * * * * * * * * * * * * * * * * * * * * * * * * * * * * * * S.Kryszewski MECHANIKA KWANTOWA 130
Mechanika kwantowa Schrödingera
 Fizyka 2 Wykład 2 1 Mechanika kwantowa Schrödingera Hipoteza de Broglie a wydawała się nie zgadzać z dynamiką Newtona. Mechanika kwantowa Schrödingera zawiera mechanikę kwantową jako przypadek graniczny
Fizyka 2 Wykład 2 1 Mechanika kwantowa Schrödingera Hipoteza de Broglie a wydawała się nie zgadzać z dynamiką Newtona. Mechanika kwantowa Schrödingera zawiera mechanikę kwantową jako przypadek graniczny
Model Bohra budowy atomu wodoru - opis matematyczny
 Model Bohra budowy atomu wodoru - opis matematyczny Uwzględniając postulaty kwantowe Bohra, można obliczyć promienie orbit dozwolonych, energie elektronu na tych orbitach, wartość prędkości elektronu na
Model Bohra budowy atomu wodoru - opis matematyczny Uwzględniając postulaty kwantowe Bohra, można obliczyć promienie orbit dozwolonych, energie elektronu na tych orbitach, wartość prędkości elektronu na
Modele atomu wodoru. Modele atomu wodoru Thomson'a Rutherford'a Bohr'a
 Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
(U.14) Oddziaływanie z polem elektromagnetycznym
 3.10.2004 35. U.14 Oddziaływanie z polem elektromagnetycznym 131 Rozdział 35 U.14 Oddziaływanie z polem elektromagnetycznym 35.1 Niezmienniczość ze względu na W rozdziale 16 wspominaliśmy jedynie o podstawowych
3.10.2004 35. U.14 Oddziaływanie z polem elektromagnetycznym 131 Rozdział 35 U.14 Oddziaływanie z polem elektromagnetycznym 35.1 Niezmienniczość ze względu na W rozdziale 16 wspominaliśmy jedynie o podstawowych
Stara i nowa teoria kwantowa
 Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Atom wodoru i jony wodoropodobne
 Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
VII. CZĄSTKI I FALE VII.1. POSTULAT DE BROGLIE'A (1924) De Broglie wysunął postulat fal materii tzn. małym cząstkom przypisał fale.
 VII. CZĄSTKI I FALE VII.1. POSTULAT DE BROGLIE'A (1924) De Broglie wysunął postulat fal materii tzn. małym cząstkom przypisał fale. Światło wykazuje zjawisko dyfrakcyjne. Rys.VII.1.Światło padające na
VII. CZĄSTKI I FALE VII.1. POSTULAT DE BROGLIE'A (1924) De Broglie wysunął postulat fal materii tzn. małym cząstkom przypisał fale. Światło wykazuje zjawisko dyfrakcyjne. Rys.VII.1.Światło padające na
Atom wodoru. Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu:
 ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki
 OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Rezonansowe oddziaływanie układu atomowego z promieniowaniem "! "!! # $%&'()*+,-./-(01+'2'34'*5%.25%&+)*-(6
Zasada nieoznaczoności
 3.10.2004 5. Zasada nieoznaczoności 63 Rozdział 5 Zasada nieoznaczoności 5.1 Formalna zasada nieoznaczoności 5.1.1 Średnie i dyspersje. Pojęcia wstępne Niech Â, ˆB oraz Ĉ będą operatorami hermitowskimi
3.10.2004 5. Zasada nieoznaczoności 63 Rozdział 5 Zasada nieoznaczoności 5.1 Formalna zasada nieoznaczoności 5.1.1 Średnie i dyspersje. Pojęcia wstępne Niech Â, ˆB oraz Ĉ będą operatorami hermitowskimi
IX. MECHANIKA (FIZYKA) KWANTOWA
 IX. MECHANIKA (FIZYKA) KWANTOWA IX.1. OPERACJE OBSERWACJI. a) klasycznie nie ważna kolejność, w jakiej wykonujemy pomiary. AB = BA A pomiar wielkości A B pomiar wielkości B b) kwantowo wartość obserwacji
IX. MECHANIKA (FIZYKA) KWANTOWA IX.1. OPERACJE OBSERWACJI. a) klasycznie nie ważna kolejność, w jakiej wykonujemy pomiary. AB = BA A pomiar wielkości A B pomiar wielkości B b) kwantowo wartość obserwacji
Wczesne modele atomu
 Wczesne modele atomu Wczesne modele atomu Demokryt (400 p.n.e.) Grecki filozof Demokryt rozpoczął poszukiwania opisu materii około 2400 lat temu. Postawił pytanie: Czy materia może być podzielona na mniejsze
Wczesne modele atomu Wczesne modele atomu Demokryt (400 p.n.e.) Grecki filozof Demokryt rozpoczął poszukiwania opisu materii około 2400 lat temu. Postawił pytanie: Czy materia może być podzielona na mniejsze
Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały
 WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
Mechanika kwantowa. Erwin Schrödinger ( ) Werner Heisenberg
 Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
Modele atomu wodoru. Modele atomu wodoru Thomson'a Rutherford'a Bohr'a
 Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
Modele atomu wodoru Modele atomu wodoru Thomson'a Rutherford'a Bohr'a Demokryt: V w. p.n.e najmniejszy, niepodzielny metodami chemicznymi składnik materii. atomos - niepodzielny Co to jest atom? trochę
Fizyka 3.3 WYKŁAD II
 Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
FIZYKA-egzamin opracowanie pozostałych pytań
 FIZYKA-egzamin opracowanie pozostałych pytań Andrzej Przybyszewski Michał Witczak Marcin Talarek. Definicja pracy na odcinku A-B 2. Zdefiniować różnicę energii potencjalnych gdy ciało przenosimy z do B
FIZYKA-egzamin opracowanie pozostałych pytań Andrzej Przybyszewski Michał Witczak Marcin Talarek. Definicja pracy na odcinku A-B 2. Zdefiniować różnicę energii potencjalnych gdy ciało przenosimy z do B
Znaleźć wzór ogólny i zbadać istnienie granicy ciągu określonego rekurencyjnie:
 Ciągi rekurencyjne Zadanie 1 Znaleźć wzór ogólny i zbadać istnienie granicy ciągu określonego rekurencyjnie: w dwóch przypadkach: dla i, oraz dla i. Wskazówka Należy poszukiwać rozwiązania w postaci, gdzie
Ciągi rekurencyjne Zadanie 1 Znaleźć wzór ogólny i zbadać istnienie granicy ciągu określonego rekurencyjnie: w dwóch przypadkach: dla i, oraz dla i. Wskazówka Należy poszukiwać rozwiązania w postaci, gdzie
Prawo Biota-Savarta. Autorzy: Zbigniew Kąkol Piotr Morawski
 Prawo Biota-Savarta Autorzy: Zbigniew Kąkol Piotr Morawski 2018 Prawo Biota-Savarta Autorzy: Zbigniew Kąkol, Piotr Morawski Istnieje równanie, zwane prawem Biota-Savarta, które pozwala obliczyć pole B
Prawo Biota-Savarta Autorzy: Zbigniew Kąkol Piotr Morawski 2018 Prawo Biota-Savarta Autorzy: Zbigniew Kąkol, Piotr Morawski Istnieje równanie, zwane prawem Biota-Savarta, które pozwala obliczyć pole B
Wykład Budowa atomu 2
 Wykład 7.12.2016 Budowa atomu 2 O atomach cd Model Bohra podsumowanie Serie widmowe O czym nie mówi model Bohra Wzbudzenie, emisja, absorpcja O liniach widmowych Kwantowomechaniczny model atomu sformułowanie
Wykład 7.12.2016 Budowa atomu 2 O atomach cd Model Bohra podsumowanie Serie widmowe O czym nie mówi model Bohra Wzbudzenie, emisja, absorpcja O liniach widmowych Kwantowomechaniczny model atomu sformułowanie
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków).
 Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Rysunek 3-23 Hipotetyczne widmo ciągłe atomu Ernesta Rutherforda oraz rzeczywiste widmo emisyjne wodoru w zakresie światła widzialnego
 3.5. Model Bohra-Sommerfelda Przeciw modelowi atomu zaproponowanego przez Ernesta Rutherforda przemawiały także wyniki badań spektroskopowych pierwiastków. Jeśli elektrony, jak wynika z teorii Maxwella,
3.5. Model Bohra-Sommerfelda Przeciw modelowi atomu zaproponowanego przez Ernesta Rutherforda przemawiały także wyniki badań spektroskopowych pierwiastków. Jeśli elektrony, jak wynika z teorii Maxwella,
Energetyka Jądrowa. Wykład 28 lutego Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów
 Energetyka Jądrowa Wykład 8 lutego 07 Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Model atomu. Promieniowanie atomów 8.II.07 EJ - Wykład / r
Energetyka Jądrowa Wykład 8 lutego 07 Zygmunt Szefliński Środowiskowe Laboratorium Ciężkich Jonów szef@fuw.edu.pl http://www.fuw.edu.pl/~szef/ Model atomu. Promieniowanie atomów 8.II.07 EJ - Wykład / r
Fizyka 3. Konsultacje: p. 329, Mechatronika
 Fizyka 3 Konsultacje: p. 39, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 1 sprawdzian 30 pkt 15.1 18 3.0 18.1 1 3.5 1.1 4 4.0 4.1 7 4.5 7.1 30 5.0 http:\\adam.mech.pw.edu.pl\~marzan Program: - elementy
Fizyka 3 Konsultacje: p. 39, Mechatronika marzan@mech.pw.edu.pl Zaliczenie: 1 sprawdzian 30 pkt 15.1 18 3.0 18.1 1 3.5 1.1 4 4.0 4.1 7 4.5 7.1 30 5.0 http:\\adam.mech.pw.edu.pl\~marzan Program: - elementy
gęstością prawdopodobieństwa
 Funkcja falowa Zgodnie z hipotezą de Broglie'a, cząstki takie jak elektron czy proton, mają własności falowe. Własności falowe cząstki (lub innego obiektu) w mechanice kwantowej opisuje tzw. funkcja falowa(,t)
Funkcja falowa Zgodnie z hipotezą de Broglie'a, cząstki takie jak elektron czy proton, mają własności falowe. Własności falowe cząstki (lub innego obiektu) w mechanice kwantowej opisuje tzw. funkcja falowa(,t)
17 Naturalne jednostki w fizyce atomowej
 7 Naturalne jednostki w fizyce atomowej W systemie CGS wszystkie wielkości fizyczne wyrażane są jako potęgi trzech fundamentalnych jednostek:. długości (l) cm,. masy (m) g, 3. czasu (t) s. Wymiary innych
7 Naturalne jednostki w fizyce atomowej W systemie CGS wszystkie wielkości fizyczne wyrażane są jako potęgi trzech fundamentalnych jednostek:. długości (l) cm,. masy (m) g, 3. czasu (t) s. Wymiary innych
Definicja i własności wartości bezwzględnej.
 Równania i nierówności z wartością bezwzględną. Rozwiązywanie układów dwóch (trzech) równań z dwiema (trzema) niewiadomymi. Układy równań liniowych z parametrem, analiza rozwiązań. Definicja i własności
Równania i nierówności z wartością bezwzględną. Rozwiązywanie układów dwóch (trzech) równań z dwiema (trzema) niewiadomymi. Układy równań liniowych z parametrem, analiza rozwiązań. Definicja i własności
Fizyka 2. Janusz Andrzejewski
 Fizyka 2 wykład 14 Janusz Andrzejewski Atom wodoru Wczesne modele atomu -W czasach Newtona atom uważany była za małą twardą kulkę co dość dobrze sprawdzało się w rozważaniach dotyczących kinetycznej teorii
Fizyka 2 wykład 14 Janusz Andrzejewski Atom wodoru Wczesne modele atomu -W czasach Newtona atom uważany była za małą twardą kulkę co dość dobrze sprawdzało się w rozważaniach dotyczących kinetycznej teorii
Wykład z równań różnicowych
 Wykład z równań różnicowych 1 Wiadomości wstępne Umówmy się, że na czas tego wykładu zrezygnujemy z oznaczania n-tego wyrazu ciągu symbolem typu x n, y n itp. Zamiast tego pisać będziemy x (n), y (n) itp.
Wykład z równań różnicowych 1 Wiadomości wstępne Umówmy się, że na czas tego wykładu zrezygnujemy z oznaczania n-tego wyrazu ciągu symbolem typu x n, y n itp. Zamiast tego pisać będziemy x (n), y (n) itp.
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Nieskończona jednowymiarowa studnia potencjału
 Nieskończona jednowymiarowa studnia potencjału Zagadnienie dane jest następująco: znaleźć funkcje własne i wartości własne operatora energii dla cząstki umieszczonej w nieskończonej studni potencjału,
Nieskończona jednowymiarowa studnia potencjału Zagadnienie dane jest następująco: znaleźć funkcje własne i wartości własne operatora energii dla cząstki umieszczonej w nieskończonej studni potencjału,
Wykład 9 Podstawy teorii kwantów fale materii, dualizm falowo-korpuskularny, funkcja falowa, równanie Schrödingera, stacjonarne równanie
 Wykład 9 Podstawy teorii kwantów fale materii, dualizm falowo-korpuskularny, funkcja falowa, równanie Schrödingera, stacjonarne równanie Schrödingera, zasada nieoznaczoności Heisenberga, ruch cząstki swobodnej,
Wykład 9 Podstawy teorii kwantów fale materii, dualizm falowo-korpuskularny, funkcja falowa, równanie Schrödingera, stacjonarne równanie Schrödingera, zasada nieoznaczoności Heisenberga, ruch cząstki swobodnej,
Przykładowe zadania z teorii liczb
 Przykładowe zadania z teorii liczb I. Podzielność liczb całkowitych. Liczba a = 346 przy dzieleniu przez pewną liczbę dodatnią całkowitą b daje iloraz k = 85 i resztę r. Znaleźć dzielnik b oraz resztę
Przykładowe zadania z teorii liczb I. Podzielność liczb całkowitych. Liczba a = 346 przy dzieleniu przez pewną liczbę dodatnią całkowitą b daje iloraz k = 85 i resztę r. Znaleźć dzielnik b oraz resztę
Wykład 2 - zagadnienie dwóch ciał (od praw Keplera do prawa powszechnego ciążenia i z powrotem..)
 Wykład 2 - zagadnienie dwóch ciał (od praw Keplera do prawa powszechnego ciążenia i z powrotem..) 24.02.2014 Prawa Keplera Na podstawie obserwacji zgromadzonych przez Tycho Brahe (głównie obserwacji Marsa)
Wykład 2 - zagadnienie dwóch ciał (od praw Keplera do prawa powszechnego ciążenia i z powrotem..) 24.02.2014 Prawa Keplera Na podstawie obserwacji zgromadzonych przez Tycho Brahe (głównie obserwacji Marsa)
Dystrybucje, wiadomości wstępne (I)
 Temat 8 Dystrybucje, wiadomości wstępne (I) Wielkości fizyczne opisujemy najczęściej przyporządkowując im funkcje (np. zależne od czasu). Inną drogą opisu tych wielkości jest przyporządkowanie im funkcjonałów
Temat 8 Dystrybucje, wiadomości wstępne (I) Wielkości fizyczne opisujemy najczęściej przyporządkowując im funkcje (np. zależne od czasu). Inną drogą opisu tych wielkości jest przyporządkowanie im funkcjonałów
Temat: Promieniowanie atomu wodoru (teoria)
 Temat: Promieniowanie atomu wodoru (teoria) Zgodnie z drugim postulatem Bohra elektron poruszając się po dozwolonej orbicie nie wypromieniowuje energii. Promieniowanie zostaje wyemitowane, gdy elektron
Temat: Promieniowanie atomu wodoru (teoria) Zgodnie z drugim postulatem Bohra elektron poruszając się po dozwolonej orbicie nie wypromieniowuje energii. Promieniowanie zostaje wyemitowane, gdy elektron
(U.6) Oscylator harmoniczny
 3.0.004 7. U.6 Oscylator harmoniczny 47 Rozdział 7 U.6 Oscylator harmoniczny 7. Rozwiązanie przez rozwinięcie w szereg W głównej części wykładu rozwiązanie zagadnienia własnego dla hamiltonianu kwantowo-mechanicznego
3.0.004 7. U.6 Oscylator harmoniczny 47 Rozdział 7 U.6 Oscylator harmoniczny 7. Rozwiązanie przez rozwinięcie w szereg W głównej części wykładu rozwiązanie zagadnienia własnego dla hamiltonianu kwantowo-mechanicznego
Postulaty mechaniki kwantowej
 3.10.2004 11. Postulaty mechaniki kwantowej 120 Rozdział 11 Postulaty mechaniki kwantowej Mechanika kwantowa, jak zresztą każda teoria fizyczna, bazuje na kilku postulatach, które przyjmujemy "na wiarę".
3.10.2004 11. Postulaty mechaniki kwantowej 120 Rozdział 11 Postulaty mechaniki kwantowej Mechanika kwantowa, jak zresztą każda teoria fizyczna, bazuje na kilku postulatach, które przyjmujemy "na wiarę".
FALE MATERII. De Broglie, na podstawie analogii optycznych, w roku 1924 wysunął hipotezę, że
 FAL MATRII De Broglie, na podstawie analogii optycznych, w roku 194 wysunął hipotezę, że cząstki materialne także charakteryzują się dualizmem korpuskularno-falowym. Hipoteza de Broglie a Cząstce materialnej
FAL MATRII De Broglie, na podstawie analogii optycznych, w roku 194 wysunął hipotezę, że cząstki materialne także charakteryzują się dualizmem korpuskularno-falowym. Hipoteza de Broglie a Cząstce materialnej
Stany stacjonarne w potencjale centralnym
 6.03.2010 14. Stany stacjonarne w potencjale centralnym 155 Rozdział 14 Stany stacjonarne w potencjale centralnym 14.1 Postawienie problemu Jednym z najważniejszych problemów mechaniki kwantowej jest wyjaśnienie
6.03.2010 14. Stany stacjonarne w potencjale centralnym 155 Rozdział 14 Stany stacjonarne w potencjale centralnym 14.1 Postawienie problemu Jednym z najważniejszych problemów mechaniki kwantowej jest wyjaśnienie
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
OLIMPIADA MATEMATYCZNA
 OLIMPIADA MATEMATYCZNA Na stronie internetowej wwwomgedupl Olimpiady Matematycznej Gimnazjalistów (OMG) ukazały się ciekawe broszury zawierające interesujące zadania wraz z pomysłowymi rozwiązaniami z
OLIMPIADA MATEMATYCZNA Na stronie internetowej wwwomgedupl Olimpiady Matematycznej Gimnazjalistów (OMG) ukazały się ciekawe broszury zawierające interesujące zadania wraz z pomysłowymi rozwiązaniami z
Funkcje wymierne. Funkcja homograficzna. Równania i nierówności wymierne.
 Funkcje wymierne. Funkcja homograficzna. Równania i nierówności wymierne. Funkcja homograficzna. Definicja. Funkcja homograficzna jest to funkcja określona wzorem f() = a + b c + d, () gdzie współczynniki
Funkcje wymierne. Funkcja homograficzna. Równania i nierówności wymierne. Funkcja homograficzna. Definicja. Funkcja homograficzna jest to funkcja określona wzorem f() = a + b c + d, () gdzie współczynniki
Matematyka dyskretna. Andrzej Łachwa, UJ, /10
 Matematyka dyskretna Andrzej Łachwa, UJ, 2018 andrzej.lachwa@uj.edu.pl 10/10 Podziały i liczby Stirlinga Liczba Stirlinga dla cykli (często nazywana liczbą Stirlinga pierwszego rodzaju) to liczba permutacji
Matematyka dyskretna Andrzej Łachwa, UJ, 2018 andrzej.lachwa@uj.edu.pl 10/10 Podziały i liczby Stirlinga Liczba Stirlinga dla cykli (często nazywana liczbą Stirlinga pierwszego rodzaju) to liczba permutacji
Wykład 17: Dr inż. Zbigniew Szklarski. Katedra Elektroniki, paw. C-1, pok
 Wykład 17: Atom Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.31 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ 1 Wczesne modele atomu Grecki filozof Demokryt rozpoczął poszukiwania
Wykład 17: Atom Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.31 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ 1 Wczesne modele atomu Grecki filozof Demokryt rozpoczął poszukiwania
Wykład 5 - całki ruchu zagadnienia n ciał i perturbacje ruchu keplerowskiego
 Wykład 5 - całki ruchu zagadnienia n ciał i perturbacje ruchu keplerowskiego 20.03.2013 Układ n ciał przyciągających się siłami grawitacji Mamy n ciał przyciągających się siłami grawitacji. Masy ciał oznaczamy
Wykład 5 - całki ruchu zagadnienia n ciał i perturbacje ruchu keplerowskiego 20.03.2013 Układ n ciał przyciągających się siłami grawitacji Mamy n ciał przyciągających się siłami grawitacji. Masy ciał oznaczamy
ZASADY DYNAMIKI. Przedmiotem dynamiki jest badanie przyczyn i sposobów zmiany ruchu ciał.
 ZASADY DYNAMIKI Przedmiotem dynamiki jest badanie przyczyn i sposobów zmiany ruchu ciał Dynamika klasyczna zbudowana jest na trzech zasadach podanych przez Newtona w 1687 roku I zasada dynamiki Istnieją
ZASADY DYNAMIKI Przedmiotem dynamiki jest badanie przyczyn i sposobów zmiany ruchu ciał Dynamika klasyczna zbudowana jest na trzech zasadach podanych przez Newtona w 1687 roku I zasada dynamiki Istnieją
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki
 OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Równania optyki półklasycznej Posłużymy się teraz równaniem (2.4), i Ψ t = ĤΨ ażeby wyprowadzić
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Równania optyki półklasycznej Posłużymy się teraz równaniem (2.4), i Ψ t = ĤΨ ażeby wyprowadzić
Rozdział 22 METODA FUNKCJONAŁÓW GĘSTOŚCI Wstęp. Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 22 METODA FUNKCJONAŁÓW GĘSTOŚCI 22.1 Wstęp Definiujemy dla gazu elektronowego operatory anihilacji ψ σ (r) i kreacji ψ σ(r) pola fermionowego ψ σ
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 22 METODA FUNKCJONAŁÓW GĘSTOŚCI 22.1 Wstęp Definiujemy dla gazu elektronowego operatory anihilacji ψ σ (r) i kreacji ψ σ(r) pola fermionowego ψ σ
h 2 h p Mechanika falowa podstawy pˆ 2
 Mechanika falowa podstawy Hipoteza de Broglie a Zarówno promieniowanie jak i cząstki materialne posiadają naturę dwoistą korpuskularno-falową. Z każdą mikrocząstką można związać pewien proces falowy pierwotnie
Mechanika falowa podstawy Hipoteza de Broglie a Zarówno promieniowanie jak i cząstki materialne posiadają naturę dwoistą korpuskularno-falową. Z każdą mikrocząstką można związać pewien proces falowy pierwotnie
RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU
 X. RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU Równanie Schrődingera niezależne od czasu to równanie postaci: ħ 2 2m d 2 x dx 2 V xx = E x (X.1) Warunki regularności na x i a) skończone b) ciągłe c) jednoznaczne
X. RÓWNANIE SCHRÖDINGERA NIEZALEŻNE OD CZASU Równanie Schrődingera niezależne od czasu to równanie postaci: ħ 2 2m d 2 x dx 2 V xx = E x (X.1) Warunki regularności na x i a) skończone b) ciągłe c) jednoznaczne
IV. TEORIA (MODEL) BOHRA ATOMU (1913)
 IV. TEORIA (MODEL) BOHRA ATOMU (1913) Bohr zastanawiał się, jak wyjaśnić strukturę widm liniowych. Elektron musi krążyć, aby zrównoważyć siłę Coulomba (przyciągającą). Skoro krąży to doznaje przyspieszenia
IV. TEORIA (MODEL) BOHRA ATOMU (1913) Bohr zastanawiał się, jak wyjaśnić strukturę widm liniowych. Elektron musi krążyć, aby zrównoważyć siłę Coulomba (przyciągającą). Skoro krąży to doznaje przyspieszenia
n=0 (n + r)a n x n+r 1 (n + r)(n + r 1)a n x n+r 2. Wykorzystując te obliczenia otrzymujemy, że lewa strona równania (1) jest równa
 Równanie Bessela Będziemy rozważać następujące równanie Bessela x y xy x ν )y 0 ) gdzie ν 0 jest pewnym parametrem Rozwiązania równania ) nazywamy funkcjami Bessela rzędu ν Sprawdzamy, że x 0 jest regularnym
Równanie Bessela Będziemy rozważać następujące równanie Bessela x y xy x ν )y 0 ) gdzie ν 0 jest pewnym parametrem Rozwiązania równania ) nazywamy funkcjami Bessela rzędu ν Sprawdzamy, że x 0 jest regularnym
Równanie Schrödingera
 Fizyka 2 Wykład 3 1 Równanie Schrödingera Chcemy znaleźć dopuszczalne wartości energii układu fizycznego, dla którego znamy energię potencjalną. Z zasady odpowiedniości znamy postać hamiltonianu. Wybieramy
Fizyka 2 Wykład 3 1 Równanie Schrödingera Chcemy znaleźć dopuszczalne wartości energii układu fizycznego, dla którego znamy energię potencjalną. Z zasady odpowiedniości znamy postać hamiltonianu. Wybieramy
Jednowymiarowa mechanika kwantowa Rozpraszanie na potencjale Na początek rozważmy najprostszy przypadek: próg potencjału
 Fizyka 2 Wykład 4 1 Jednowymiarowa mechanika kwantowa Rozpraszanie na potencjale Na początek rozważmy najprostszy przypadek: próg potencjału Niezależne od czasu równanie Schödingera ma postać: 2 d ( x)
Fizyka 2 Wykład 4 1 Jednowymiarowa mechanika kwantowa Rozpraszanie na potencjale Na początek rozważmy najprostszy przypadek: próg potencjału Niezależne od czasu równanie Schödingera ma postać: 2 d ( x)
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu
 Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
II.1 Serie widmowe wodoru
 II.1 Serie widmowe wodoru Jan Królikowski Fizyka IVBC 1 II.1 Serie widmowe wodoru W obszarze widzialnym wystepują 3 silne linie wodoru: H α (656.3 nm), H β (486.1 nm) i H γ (434.0 nm) oraz szereg linii
II.1 Serie widmowe wodoru Jan Królikowski Fizyka IVBC 1 II.1 Serie widmowe wodoru W obszarze widzialnym wystepują 3 silne linie wodoru: H α (656.3 nm), H β (486.1 nm) i H γ (434.0 nm) oraz szereg linii
Pochodna i różniczka funkcji oraz jej zastosowanie do obliczania niepewności pomiarowych
 Pochodna i różniczka unkcji oraz jej zastosowanie do obliczania niepewności pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją
Pochodna i różniczka unkcji oraz jej zastosowanie do obliczania niepewności pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją
17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 17 KLASYCZNA DYNAMIKA MOLEKULARNA 17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek Rozważamy układ N punktowych cząstek
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 17 KLASYCZNA DYNAMIKA MOLEKULARNA 17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek Rozważamy układ N punktowych cząstek
Zagadnienie dwóch ciał
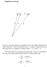 Zagadnienie dwóch ciał Rysunek : Rysunek ilustrujący zagadnienie dwóch ciał. Wektor R określa położenie środka masy, wektor x położenie masy m, a wektor x 2 położenie masy m 2. Położenie masy m 2 względem
Zagadnienie dwóch ciał Rysunek : Rysunek ilustrujący zagadnienie dwóch ciał. Wektor R określa położenie środka masy, wektor x położenie masy m, a wektor x 2 położenie masy m 2. Położenie masy m 2 względem
Geometria analityczna
 Geometria analityczna Paweł Mleczko Teoria Informacja (o prostej). postać ogólna prostej: Ax + By + C = 0, A + B 0, postać kanoniczna (kierunkowa) prostej: y = ax + b. Współczynnik a nazywamy współczynnikiem
Geometria analityczna Paweł Mleczko Teoria Informacja (o prostej). postać ogólna prostej: Ax + By + C = 0, A + B 0, postać kanoniczna (kierunkowa) prostej: y = ax + b. Współczynnik a nazywamy współczynnikiem
Indukcja matematyczna
 Indukcja matematyczna Zadanie 1 Wykazać, że dla dowolnego prawdziwa jest równość: Do obu stron założenia indukcyjnego należy dodać brakujący wyraz. Sprawdzamy prawdziwość równości (1) dla. Prawa strona:.
Indukcja matematyczna Zadanie 1 Wykazać, że dla dowolnego prawdziwa jest równość: Do obu stron założenia indukcyjnego należy dodać brakujący wyraz. Sprawdzamy prawdziwość równości (1) dla. Prawa strona:.
PODSTAWY MECHANIKI KWANTOWEJ
 PODSTAWY MECHANIKI KWANTOWEJ De Broglie, na podstawie analogii optycznych, w roku 194 wysunął hipotezę, że cząstki materialne także charakteryzują się dualizmem korpuskularno-falowym. Hipoteza de Broglie
PODSTAWY MECHANIKI KWANTOWEJ De Broglie, na podstawie analogii optycznych, w roku 194 wysunął hipotezę, że cząstki materialne także charakteryzują się dualizmem korpuskularno-falowym. Hipoteza de Broglie
Reprezentacje położeniowa i pędowa
 3.10.2004 9. Reprezentacje położeniowa i pędowa 103 Rozdział 9 Reprezentacje położeniowa i pędowa 9.1 Reprezentacja położeniowa Reprezentacja położeniowa jest szczególnie uprzywilejowana i najczęściej
3.10.2004 9. Reprezentacje położeniowa i pędowa 103 Rozdział 9 Reprezentacje położeniowa i pędowa 9.1 Reprezentacja położeniowa Reprezentacja położeniowa jest szczególnie uprzywilejowana i najczęściej
4. Postęp arytmetyczny i geometryczny. Wartość bezwzględna, potęgowanie i pierwiastkowanie liczb rzeczywistych.
 Jarosław Wróblewski Matematyka dla Myślących, 008/09. Postęp arytmetyczny i geometryczny. Wartość bezwzględna, potęgowanie i pierwiastkowanie liczb rzeczywistych. 15 listopada 008 r. Uwaga: Przyjmujemy,
Jarosław Wróblewski Matematyka dla Myślących, 008/09. Postęp arytmetyczny i geometryczny. Wartość bezwzględna, potęgowanie i pierwiastkowanie liczb rzeczywistych. 15 listopada 008 r. Uwaga: Przyjmujemy,
II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym
 II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym Jan Królikowski Fizyka IVBC 1 II.4.1 Ogólne własności wektora kwantowego momentu pędu Podane poniżej własności kwantowych wektorów
II.4 Kwantowy moment pędu i kwantowy moment magnetyczny w modelu wektorowym Jan Królikowski Fizyka IVBC 1 II.4.1 Ogólne własności wektora kwantowego momentu pędu Podane poniżej własności kwantowych wektorów
Logarytmy. Funkcje logarytmiczna i wykładnicza. Równania i nierówności wykładnicze i logarytmiczne.
 Logarytmy. Funkcje logarytmiczna i wykładnicza. Równania i nierówności wykładnicze i logarytmiczne. Definicja. Niech a i b będą dodatnimi liczbami rzeczywistymi i niech a. Logarytmem liczby b przy podstawie
Logarytmy. Funkcje logarytmiczna i wykładnicza. Równania i nierówności wykładnicze i logarytmiczne. Definicja. Niech a i b będą dodatnimi liczbami rzeczywistymi i niech a. Logarytmem liczby b przy podstawie
Wykład Budowa atomu 1
 Wykład 30. 11. 2016 Budowa atomu 1 O atomach Trochę historii i wprowadzenie w temat Promieniowanie i widma Doświadczenie Rutherforda i odkrycie jądra atomowego Model atomu wodoru Bohra sukcesy i ograniczenia
Wykład 30. 11. 2016 Budowa atomu 1 O atomach Trochę historii i wprowadzenie w temat Promieniowanie i widma Doświadczenie Rutherforda i odkrycie jądra atomowego Model atomu wodoru Bohra sukcesy i ograniczenia
Oddziaływanie z polem elektromagnetycznym
 3.10.2004 16. Oddziaływanie z polem elektromagnetycznym 180 Rozdział 16 Oddziaływanie z polem elektromagnetycznym 16.1 Przypomnienie fizyki klasycznej 16.1.1 Równania Lagrange a Równania Lagrange a drugiego
3.10.2004 16. Oddziaływanie z polem elektromagnetycznym 180 Rozdział 16 Oddziaływanie z polem elektromagnetycznym 16.1 Przypomnienie fizyki klasycznej 16.1.1 Równania Lagrange a Równania Lagrange a drugiego
(U.16) Dodawanie momentów pędu
 .0.004 7. (U.6) Dodawanie momentów pędu 5 Rozdział 7 (U.6) Dodawanie momentów pędu 7. Złożenie orbitalnego momentu pędu i spinu / 7.. Przejście do bazy sprzężonej W praktycznych zastosowaniach potrzebujemy
.0.004 7. (U.6) Dodawanie momentów pędu 5 Rozdział 7 (U.6) Dodawanie momentów pędu 7. Złożenie orbitalnego momentu pędu i spinu / 7.. Przejście do bazy sprzężonej W praktycznych zastosowaniach potrzebujemy
1 Równania różniczkowe zwyczajne o rozdzielonych zmiennych
 Równania różniczkowe zwyczajne o rozdzielonych zmiennych Definicja. Równaniem różniczkowym o rozdzielonych zmiennych nazywamy równanie postaci p(y) = q() (.) rozwiązanie równania sprowadza się do postaci
Równania różniczkowe zwyczajne o rozdzielonych zmiennych Definicja. Równaniem różniczkowym o rozdzielonych zmiennych nazywamy równanie postaci p(y) = q() (.) rozwiązanie równania sprowadza się do postaci
UKŁADY RÓWNAŃ LINIOWYCH
 Projekt dofinansowała Fundacja mbanku UKŁADY RÓWNAŃ LINIOWYCH CZĘŚĆ I Układ równań to przynajmniej dwa równania spięte z lewej strony klamrą, np.: x + 0 Każde z równań musi zawierać przynajmniej jedną
Projekt dofinansowała Fundacja mbanku UKŁADY RÓWNAŃ LINIOWYCH CZĘŚĆ I Układ równań to przynajmniej dwa równania spięte z lewej strony klamrą, np.: x + 0 Każde z równań musi zawierać przynajmniej jedną
3. FUNKCJA LINIOWA. gdzie ; ół,.
 1 WYKŁAD 3 3. FUNKCJA LINIOWA FUNKCJĄ LINIOWĄ nazywamy funkcję typu : dla, gdzie ; ół,. Załóżmy na początek, że wyraz wolny. Wtedy mamy do czynienia z funkcją typu :.. Wykresem tej funkcji jest prosta
1 WYKŁAD 3 3. FUNKCJA LINIOWA FUNKCJĄ LINIOWĄ nazywamy funkcję typu : dla, gdzie ; ół,. Załóżmy na początek, że wyraz wolny. Wtedy mamy do czynienia z funkcją typu :.. Wykresem tej funkcji jest prosta
F t+ := s>t. F s = F t.
 M. Beśka, Całka Stochastyczna, wykład 1 1 1 Wiadomości wstępne 1.1 Przestrzeń probabilistyczna z filtracją Niech (Ω, F, P ) będzie ustaloną przestrzenią probabilistyczną i niech F = {F t } t 0 będzie rodziną
M. Beśka, Całka Stochastyczna, wykład 1 1 1 Wiadomości wstępne 1.1 Przestrzeń probabilistyczna z filtracją Niech (Ω, F, P ) będzie ustaloną przestrzenią probabilistyczną i niech F = {F t } t 0 będzie rodziną
Rozwiązania zadań z podstaw fizyki kwantowej
 Rozwiązania zadań z podstaw fizyki kwantowej Jacek Izdebski 5 stycznia roku Zadanie 1 Funkcja falowa Ψ(x) = A n sin( πn x) jest zdefiniowana jedynie w obszarze
Rozwiązania zadań z podstaw fizyki kwantowej Jacek Izdebski 5 stycznia roku Zadanie 1 Funkcja falowa Ψ(x) = A n sin( πn x) jest zdefiniowana jedynie w obszarze
Atom wodoru w mechanice kwantowej. Równanie Schrödingera
 Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
gdzie λ - długość fali, h - stała Plancka, p - pęd cząstki.
 3.7. Model współczesny Louis Victor Pierre Raymond de Broglie (189-1987) (Rysunek 3-35) w swojej pracy doktorskiej z 194 roku, wysunął przypuszczenie, że skoro fale elektromagnetyczne mogą przejawiać naturę
3.7. Model współczesny Louis Victor Pierre Raymond de Broglie (189-1987) (Rysunek 3-35) w swojej pracy doktorskiej z 194 roku, wysunął przypuszczenie, że skoro fale elektromagnetyczne mogą przejawiać naturę
INFORMATYKA MÓJ SPOSÓB NA POZNANIE I OPISANIE ŚWIATA.
 SCENARIUSZ LEKCJI OPRACOWANY W RAMACH PROJEKTU: INFORMATYKA MÓJ SPOSÓB NA POZNANIE I OPISANIE ŚWIATA. PROGRAM NAUCZANIA INFORMATYKI Z ELEMENTAMI PRZEDMIOTÓW MATEMATYCZNO-PRZYRODNICZYCH Autorzy scenariusza:
SCENARIUSZ LEKCJI OPRACOWANY W RAMACH PROJEKTU: INFORMATYKA MÓJ SPOSÓB NA POZNANIE I OPISANIE ŚWIATA. PROGRAM NAUCZANIA INFORMATYKI Z ELEMENTAMI PRZEDMIOTÓW MATEMATYCZNO-PRZYRODNICZYCH Autorzy scenariusza:
Pochodna i różniczka funkcji oraz jej zastosowanie do rachunku błędów pomiarowych
 Pochodna i różniczka unkcji oraz jej zastosowanie do rachunku błędów pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją symbolami:
Pochodna i różniczka unkcji oraz jej zastosowanie do rachunku błędów pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją symbolami:
Układy równań i nierówności liniowych
 Układy równań i nierówności liniowych Wiesław Krakowiak 1 grudnia 2010 1 Układy równań liniowych DEFINICJA 11 Układem równań m liniowych o n niewiadomych X 1,, X n, nazywamy układ postaci: a 11 X 1 + +
Układy równań i nierówności liniowych Wiesław Krakowiak 1 grudnia 2010 1 Układy równań liniowych DEFINICJA 11 Układem równań m liniowych o n niewiadomych X 1,, X n, nazywamy układ postaci: a 11 X 1 + +
Dwa równania kwadratowe z częścią całkowitą
 Dwa równania kwadratowe z częścią całkowitą Andrzej Nowicki Wydział Matematyki i Informatyki Uniwersytet M. Kopernika w Toruniu anow @ mat.uni.torun.pl 4 sierpnia 00 Jeśli r jest liczbą rzeczywistą, to
Dwa równania kwadratowe z częścią całkowitą Andrzej Nowicki Wydział Matematyki i Informatyki Uniwersytet M. Kopernika w Toruniu anow @ mat.uni.torun.pl 4 sierpnia 00 Jeśli r jest liczbą rzeczywistą, to
POSTULATY MECHANIKI KWANTOWEJ cd i formalizm matematyczny
 POSTULATY MECHANIKI KWANTOWEJ cd i formalizm matematyczny Funkcja Falowa Postulat 1 Dla każdego układu istnieje funkcja falowa (funkcja współrzędnych i czasu), która jest ciągła, całkowalna w kwadracie,
POSTULATY MECHANIKI KWANTOWEJ cd i formalizm matematyczny Funkcja Falowa Postulat 1 Dla każdego układu istnieje funkcja falowa (funkcja współrzędnych i czasu), która jest ciągła, całkowalna w kwadracie,
Całka nieoznaczona, podstawowe wiadomości
 Całka nieoznaczona, podstawowe wiadomości Funkcją pierwotną funkcji w przedziale nazywamy funkcję taką, że dla każdego punktu z tego przedziału zachodzi Różnica dwóch funkcji pierwotnych w przedziale danej
Całka nieoznaczona, podstawowe wiadomości Funkcją pierwotną funkcji w przedziale nazywamy funkcję taką, że dla każdego punktu z tego przedziału zachodzi Różnica dwóch funkcji pierwotnych w przedziale danej
Funkcje wymierne. Jerzy Rutkowski. Działania dodawania i mnożenia funkcji wymiernych określa się wzorami: g h + k l g h k.
 Funkcje wymierne Jerzy Rutkowski Teoria Przypomnijmy, że przez R[x] oznaczamy zbiór wszystkich wielomianów zmiennej x i o współczynnikach rzeczywistych Definicja Funkcją wymierną jednej zmiennej nazywamy
Funkcje wymierne Jerzy Rutkowski Teoria Przypomnijmy, że przez R[x] oznaczamy zbiór wszystkich wielomianów zmiennej x i o współczynnikach rzeczywistych Definicja Funkcją wymierną jednej zmiennej nazywamy
Spis treści. Przedmowa redaktora do wydania czwartego 11
 Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
Mechanika kwantowa : teoria nierelatywistyczna / Lew D. Landau, Jewgienij M. Lifszyc ; z jęz. ros. tł. Ludwik Dobrzyński, Andrzej Pindor. - Wyd. 3. Warszawa, 2012 Spis treści Przedmowa redaktora do wydania
1 Działania na zbiorach
 M. Beśka, Wstęp do teorii miary, rozdz. 1 1 1 Działania na zbiorach W rozdziale tym przypomnimy podstawowe działania na zbiorach koncentrując się na własnościach tych działań, które będą przydatne w dalszej
M. Beśka, Wstęp do teorii miary, rozdz. 1 1 1 Działania na zbiorach W rozdziale tym przypomnimy podstawowe działania na zbiorach koncentrując się na własnościach tych działań, które będą przydatne w dalszej
Stałe : h=6, Js h= 4, eVs 1eV= J nie zależy
 T_atom-All 1 Nazwisko i imię klasa Stałe : h=6,626 10 34 Js h= 4,14 10 15 evs 1eV=1.60217657 10-19 J Zaznacz zjawiska świadczące o falowej naturze światła a) zjawisko fotoelektryczne b) interferencja c)
T_atom-All 1 Nazwisko i imię klasa Stałe : h=6,626 10 34 Js h= 4,14 10 15 evs 1eV=1.60217657 10-19 J Zaznacz zjawiska świadczące o falowej naturze światła a) zjawisko fotoelektryczne b) interferencja c)
Wstęp. Ruch po okręgu w kartezjańskim układzie współrzędnych
 Wstęp Ruch po okręgu jest najprostszym przypadkiem płaskich ruchów krzywoliniowych. W ogólnym przypadku ruch po okręgu opisujemy równaniami: gdzie: dowolna funkcja czasu. Ruch odbywa się po okręgu o środku
Wstęp Ruch po okręgu jest najprostszym przypadkiem płaskich ruchów krzywoliniowych. W ogólnym przypadku ruch po okręgu opisujemy równaniami: gdzie: dowolna funkcja czasu. Ruch odbywa się po okręgu o środku
Całki nieoznaczone. 1 Własności. 2 Wzory podstawowe. Adam Gregosiewicz 27 maja a) Jeżeli F (x) = f(x), to f(x)dx = F (x) + C,
 Całki nieoznaczone Adam Gregosiewicz 7 maja 00 Własności a) Jeżeli F () = f(), to f()d = F () + C, dla dowolnej stałej C R. b) Jeżeli a R, to af()d = a f()d. c) Jeżeli f i g są funkcjami całkowalnymi,
Całki nieoznaczone Adam Gregosiewicz 7 maja 00 Własności a) Jeżeli F () = f(), to f()d = F () + C, dla dowolnej stałej C R. b) Jeżeli a R, to af()d = a f()d. c) Jeżeli f i g są funkcjami całkowalnymi,
EGZAMIN MATURALNY 2013 FIZYKA I ASTRONOMIA
 Centralna Komisja Egzaminacyjna EGZAMIN MATURALNY 2013 FIZYKA I ASTRONOMIA POZIOM PODSTAWOWY Kryteria oceniania odpowiedzi MAJ 2013 2 Egzamin maturalny z fizyki i astronomii Zadanie 1. (0 1) Obszar standardów
Centralna Komisja Egzaminacyjna EGZAMIN MATURALNY 2013 FIZYKA I ASTRONOMIA POZIOM PODSTAWOWY Kryteria oceniania odpowiedzi MAJ 2013 2 Egzamin maturalny z fizyki i astronomii Zadanie 1. (0 1) Obszar standardów
Wielomiany Legendre a, itp.
 3.0.2004 Dod. mat. D. Wieomiany Legendre a, itp. 25 Dodatek D Wieomiany Legendre a, itp. Wieomiany Legendre a i stowarzyszone z nimi funkcje są szeroko omawiane w wieu podręcznikach fizyki matematycznej.
3.0.2004 Dod. mat. D. Wieomiany Legendre a, itp. 25 Dodatek D Wieomiany Legendre a, itp. Wieomiany Legendre a i stowarzyszone z nimi funkcje są szeroko omawiane w wieu podręcznikach fizyki matematycznej.
(U.10) Ewolucja układów kwantowych w czasie
 3.10.2004 31. (U.10) Ewolucja układów kwantowych w czasie 81 Rozdział 31 (U.10) Ewolucja układów kwantowych w czasie 31.1 Równanie Schrödingera i operator ewolucji 31.1.1 Podstawowe definicje Gdy układ
3.10.2004 31. (U.10) Ewolucja układów kwantowych w czasie 81 Rozdział 31 (U.10) Ewolucja układów kwantowych w czasie 31.1 Równanie Schrödingera i operator ewolucji 31.1.1 Podstawowe definicje Gdy układ
Elementy mechaniki kwantowej. Mechanika kwantowa co to jest? Fale materii hipoteza de Broglie'a Funkcja falowa Równanie Schrödingera
 lementy mechaniki kwantowej Mechanika kwantowa co to jest? Fale materii hipoteza de Broglie'a Funkcja falowa Równanie Schrödingera Fale materii de Broglie a (rok 193) De Broglie zaproponował, że każdy
lementy mechaniki kwantowej Mechanika kwantowa co to jest? Fale materii hipoteza de Broglie'a Funkcja falowa Równanie Schrödingera Fale materii de Broglie a (rok 193) De Broglie zaproponował, że każdy
WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE.
 1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
Rozdział 2. Liczby zespolone
 Rozdział Liczby zespolone Zbiór C = R z działaniami + oraz określonymi poniżej: x 1, y 1 ) + x, y ) := x 1 + x, y 1 + y ), 1) x 1, y 1 ) x, y ) := x 1 x y 1 y, x 1 y + x y 1 ) ) jest ciałem zob rozdział
Rozdział Liczby zespolone Zbiór C = R z działaniami + oraz określonymi poniżej: x 1, y 1 ) + x, y ) := x 1 + x, y 1 + y ), 1) x 1, y 1 ) x, y ) := x 1 x y 1 y, x 1 y + x y 1 ) ) jest ciałem zob rozdział
Rok akademicki: 2012/2013 Kod: JFM s Punkty ECTS: 6. Poziom studiów: Studia I stopnia Forma i tryb studiów: Stacjonarne
 Nazwa modułu: Wstęp do fizyki atomowej i kwantowej Rok akademicki: 2012/2013 Kod: JFM-1-302-s Punkty ECTS: 6 Wydział: Fizyki i Informatyki Stosowanej Kierunek: Fizyka Medyczna Specjalność: Poziom studiów:
Nazwa modułu: Wstęp do fizyki atomowej i kwantowej Rok akademicki: 2012/2013 Kod: JFM-1-302-s Punkty ECTS: 6 Wydział: Fizyki i Informatyki Stosowanej Kierunek: Fizyka Medyczna Specjalność: Poziom studiów:
WYMAGANIE EDUKACYJNE Z MATEMATYKI W KLASIE II GIMNAZJUM. dopuszczającą dostateczną dobrą bardzo dobrą celującą
 1. Statystyka odczytać informacje z tabeli odczytać informacje z diagramu 2. Mnożenie i dzielenie potęg o tych samych podstawach 3. Mnożenie i dzielenie potęg o tych samych wykładnikach 4. Potęga o wykładniku
1. Statystyka odczytać informacje z tabeli odczytać informacje z diagramu 2. Mnożenie i dzielenie potęg o tych samych podstawach 3. Mnożenie i dzielenie potęg o tych samych wykładnikach 4. Potęga o wykładniku
