Chemia organiczna. Związki zawierające azot. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
|
|
|
- Włodzimierz Żurek
- 7 lat temu
- Przeglądów:
Transkrypt
1 Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
2 Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2 nitrometan -ONO 2 azotanowa CH3ONO2 azotan metylu -NO nitrozowa C6H5NO nitrozobenzen -ONO azotynowa CH3ONO azotyn metylu -NH 2 aminowa CH3NH2 metyloamina =NH iminowa CH3CH=NH etanoimina -CN cyjanowa CH3CN etanonitryl -NC izocyjanowa CH3NC izocyjanek metylu -NCO izocyjanianowa CH3NCO izocyjanian metylu -NCS izotiocyjanianowa CH3CNCS izotiocyjanian metylu
3 Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa =NOH hydroksyiminowa CH 3 CH=NOH oksym etanalu -NHNH 2 hydrazynowa CH 3 NHNH 2 metylohydrazyna -CONH 2 amidowa CH 3 CONH 2 amid kwasu octowego NH -C amidynowa CH 3 C acetamidyna NH NH 2 NH 2 -CONHOH hydroksamowa CH 3 CONHOH kwas acetohydroksamowy -N 3 azydowa CH 3 N 3 azydek metylu -NHCNH 2 CH 3 NHCNH 2 guanidynowa NH NH metyloguanidyna
4 Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -N=N- CH 3 N=NCH 3 azoksy O O azoksymetan -N 2 diazowa CH 2 N 2 diazometan -N 2 + diazoniowa C 6 H 5 N 2 + kation fenylodiazoniowy
5 Związki nitrowe - nitrozwiązki związki nitrowe zbudowane są z grupy nitrowej i połączonym z nią rodnikiem alifatycznym lub aromatycznym atom azotu występuje w hybrydyzacji sp 2 tworzy trzy wiązania grupa nitrowa występuje w dwóch strukturach rezonansowych oba atomy tlenu są równocenne związki nitrowe są dipolami oddziaływania między nimi są przyczyną wysokiej temperatury wrzenia
6 Tautomeria i kwasowe właściwości nitrozwiązków Tautomeria izomeria (konstytucyjna), w której izomery mogą przekształacać się w siebie w reakcjach odwracalnych i istnieją w równowadze ze sobą Tautomeria zmiana położenia atomów wodoru Nitrozwiązki w formie tautomerycznej aci-nitropochodne. W środowisku obojętnym równowaga jest przesunięta w stronę formy nitrowej W środowisku zasadowym nitrozwiązki tworzą rozpuszczalne w wodzie formy aci. Zakwaszenie przesuwa równowagę w stronę formy nitro. H + forma nitro forma aci
7 Tautomeria i kwasowe właściwości nitrozwiązków Aci-nitropochodne są silniejszymi kwasami niż kwas węglowy rozpuszczają się w w roztworach węglanu sodu z chlorkiem żelaza (III) reagują tak, jak fenole i alkohole nitrozwiązki w formie nitro nie rozpuszczają się w roztworach węglanów warunkiem powstawania form aci jest obecność atomu wodoru w położeniu względem grupy nitrowej (przeniesienie atomu wodoru z atomu węgla do atomu tlenu) forma nitro forma aci
8 Tautomeria i kwasowe właściwości nitrozwiązków Aci-nitrozwiązki samorzutnie przechodzą w formę nitro. Trwałość form aci uniemożliwia ich wyodrębnienie Wyjątek, m.in.: fenylonitrometan; trwały przez kilka godzin bardzo wolno NaOH wolno H + szybko NaOH szybko fenylonitrometan forma nitro ciecz t.wrz. 226 o C fenylonitrometan forma aci ciało stałe t.top. 84 o C
9 Nitrozwiązki - redukacja redukcji ulegają nitroalkany i związki aromatyczne reakcja katalityczna wodór na katalizatorach metale: żelazo, cynk, cyna przebiega w trzech reakcjach następczych końcowym produktem są aminy 2e, 2H + 2e, 2H + 2e, 2H + C 6 H 5 NO 2 C 6 H 5 NO C 6 H 5 NHOH C 6 H 5 NH 2 -H 2 O -H 2 O nitrobenzen nitrozobenzen fenylohydro- anilina ksyloamina
10 Nitrozwiązki - synteza nitrowanie reakcje substratów organicznych z kwasem azotowym, prowadzące do zastąpienia atomów wodoru z wiązań C-H przez grupy nitrowe nitrowanie pierścieni aromatycznych reakcja podstawienia elektrofilowego, w której elektrofilem jest jon nitroniowy NO + 2 HNO H 2 SO 4 NO H 3 O HSO HNO 3 H 2 SO 4 -H 2 O NO 2 HNO 3 NO 2 H 2 SO 4 +H 2 O otrzymywanie z halogenoalkanów NO 2 R-X + O=N-O - R-O-NO + X - reakcja przy atomie tlenu estry kwasu azotowego (azotany) R-X + O=N-O - R-NO 2 + X - reakcja przy atomie azotu - nitroalkany
11 Aminy Aminy - organiczne pochodne amoniaku, w którym jeden lub więcej atomów wodoru został zastąpiony resztami organicznymi atom azotu w aminach ma hybrydyzację sp 3, trzy orbitale tworzą trzy wiązania σ z atomami wodoru lub/i atomami węgla grup R na czwartym orbitalu znajduje się wolna para elektronowa. W trimetyloaminie kąt między wiązaniami C-N-C wynosi 108 o, jest więc zbliżony do kąta tetraedrycznego bardziej niż w amoniaku. Długość wiązania C N osiąga 1,47 Å amoniak trimetyloamina
12 Aminy Konsekwencją tetraedrycznej budowy amin 3 o jest ich chiralność: trzy różne podstawniki związane z atomem azotu czwartym podstawnikiem jest wolna para elektronowa niska bariera energetyczna (25 kj/mol) przejścia jednego enancjomeru w drugi uniemożliwia ich rozdzielenie. stanem pośrednim pomiędzy jedną, a drugą formą enancjomeryczną jest płaski atom azotu o hybrydyzacji sp 2 trwałe są enancjomery 4 o soli amoniowych
13 Aminy - nomenklatura 1-aminobutan 1-metyloaminopropan 2-amino-2-metylopropan dimetyloaminoetan butanoamina N-metylopropanoamian 2-metylo-2-propanoamina N,N-dimetyloetanoamina n-butyloamina tert-butyloamina metylopropyloamina etylodietyloamina IUPAC grupa aminowa jest przyłączona do grupy alkilowej CA aminy I o przyrostek amina; wyższe rzędy prefiks N- przed przyłączonymi do grupy aminowej podstawnikami nomenklatura zwyczajowa podstawniki alkilowa (w kolejności alfabetycznej) + sufix amina
14 Aminy - występowanie Aminy biogenne powstają w wyniku dekarboksylacji aminokwasów. bardzo toksyczne substancje o silnym działaniu fizjologicznym (na ogół) nieprzyjemny zapach powstają w procesie rozkładu mięsa ornityna putrescyna kadaweryna (z ornityny) (z lizyny) tyramina histamina tryptamina (z tyrozyny) (z histydyny) (z tryptofanu)
15 Alkaloidy kilkunaście tysięcy związków: pochodzenia głównie roślinnego rzadziej zwierzęcego alkaloidy syntetyczne zawierają zasadowy atom azotu, najczęściej w postaci pierścienia heterocyklicznego alkaloidy z alifatyczną grupą aminową - protoalkaloidy (pseudoalkaloidy) w produktach naturalnych alkaloidy i większość innych amin występują w postaci soli wykazują silnie działanie fizjologiczne stymulujące narkotyczne silnie toksyczne do alkaloidów nie są zaliczane aminokwasy, peptydy, białka i proste aminy alifatyczne nawet, jeżeli posiadają ich właściwości
16 Alkaloidy efedryna meskalina koniina rycynina nikotyna kokaina chinina morfina johimbina strychnina kofeina teofilina teobromina
17 Aminy cykliczne aminy naturalne piperydyna indol pirolidyna imidazol pirydyna koniina serotonina kofeina nikotyna muskaryna trucizna neuroprzekaźnik pirolidyna pirymidyna piperydyna piperydyna chinolina pirydyna atropina tiamina morfina chinina witamina B1
18 Aminy - otrzymywanie reakcje alkilowania podstawienia nukleofilowego halogenków alkilowych amoniakiem wzrost nukleofilowości amin w wyniku dołączania kolejnych grup alkilowych - efekt +I. reakcja nie zatrzymuje się na aminach 1 o, ale biegnie dalej do amin 2 o, 3 o i 4 o sole amoniowe. powstaje trudna do rozdzielenia mieszanina produktów
19 reakcje alkilowania podstawienia nukleofilowego halogenków alkilowych amoniakiem wzrost nukleofilowości amin w wyniku dołączania kolejnych grup alkilowych - efekt +I. reakcja nie zatrzymuje się na aminach 1 o, ale biegnie dalej do amin 2 o, 3 o i 4 o sole amoniowe. powstaje trudna do rozdzielenia mieszanina produktów amoniak chlorek metylu chlorek metyloamina metyloamoniowy (amina 1 o ) chlorek metylu chlorek dimetyloamina dimetyloamoniowy (amina 2 o ) dietyloamina chlorek metylu chlorek trimetyloamina trimetyloamoniowy (amina 3 o ) trimetyloamina chlorek metylu chlorek tetrametyloamoniowy (4 o sól amoniowa)
20 Aminy - otrzymywanie synteza Gabriela - alkilowanie ftalimidku potasu ftalimid otrzymuje się w reakcji bezwodnika ftalowego i amoniaku zawiera jeden atom wodoru przy atomie azotu - znacznie kwaśniejszy niż w aminach, a więc bardziej podatny na alkilowanie hydroliza lub hydrazynoliza N-alkiloftalimidu prowadzi do czystej aminy 1 o ftalazyna bezwodnik ftalimid ftalimidek N-(2-fenyloetylo)ftalimid fenyloetyloamina ftalowy potasu
21 Aminy - otrzymywanie redukcyjne aminowanie aldehydy i ketony redukowane katalitycznie wodorem w obecności amoniaku, amin 1 o lub 2 o ulegają przekształceniu w odpowiednie aminy. pośrednio tworzą się iminy, które znacznie łatwiej ulegają redukcji katalitycznej niż związki karbonylowe. związek imina amina I o karboksylowy użycie w reakcji amin 1 o lub amin 2 o prowadzi odpowiednio do amin 2 o lub amin 3 o w redukcyjnym aminowaniu otrzymuje się aminy o jeden rząd wyższe w porównaniu do rzędowości aminy użytej w reakcji związek amina 1 o karbonylowy imina amina 2 o
22 Aminy otrzymywanie przez redukcyjne aminowanie w redukcyjnym aminowaniu otrzymuje się aminy o jeden rząd wyższe w porównaniu do rzędowości aminy użytej w reakcji amina I o amina II o amina III o
23 Aminy otrzymywanie przez redukcyjne aminowanie benzaldehyd benzyloamina 1-fenylopropan-2-on amfetamina cyklo- dietyloamina N,N-dimetyloheksanon cykloheksyloamina
24 Aminy - otrzymywanie redukcyjne aminowanie z alkoholi, w zależności od wybranej metody, można otrzymać różne aminy: o takiej samej długości łańcucha węglowego, skróconym wydłużonym łańcuchu
25 Aminy - otrzymywanie W przegrupowaniu Hofmanna amidy są przeprowadzane w aminy 1 o, zawierające jeden atom węgla mniej niż związki wyjściowe. Amidy przekształcenie w izocyjaniny - pod wpływem bromu w zasadowym środowisku hydroliza do amin z wydzieleniem CO 2 amid amina I o ftalimid monoamid kwas ftalowy kwasu ftalowego
26 Aminy - otrzymywanie W przegrupowaniu Curtiusa azydki są przeprowadzane w aminy I o, zawierające jeden atom węgla mniej niż związki wyjściowe otrzymanie azydków acylowych z chlorków kwasowych pod działaniem azydku sodu w podwyższonej temperaturze reszta organiczna -R w azydkach acylowych przegrupowuje się z C N powstają izocyjaniany alkilowe rozkładają się do amin I o wydzielając CO 2 chlorek acylu azydek acylu izocyjanian alkilu amina 1 o
27 Właściwości amin Aminy są zasadami aminy alifatyczne - silniejsze zasady niż amoniak aminy aromatyczne słabsze zasady niż amoniaku przy atomie azotu obecna jest protonoakceptorowa wolna para elektronowa reakcja amin z kwasami: przyłączenie protonu do wolnej pary elektronów powstają sole amoniowe zasada kwas sól Lewisa amoniowa zasada kwas kation Lewisa (woda) amoniowy amina
28 Zasadowość amin aminy alifatyczne są kilkanaście razy silniejszymi zasadami niż amoniak efekt indukcyjny +I reszt alifatycznych przyczyna wzrostu zasadowości amin alifatycznych w stosunku do NH 3 zwiększenie liczby reszt alifatycznych w aminach 2 o i 3 o ma niewielki wpływ na moc amin. wrasta efekt indukcyjny zwiększa się hydrofobowość cząsteczki, przez co tworzący się kation amoniowy jest trudniej solwatowany przez cząsteczki wody.
29 Zasadowość amin aminy aromatyczne efekty mezomeryczny -M i indukcyjny -I pierścienia fenylowego 1. zmniejszają ładunek ujemny przy atomie azotu, 2. zmniejsza się jego powinowactwo do protonu 3. aminy stają się mniej zasadowe
30 Zasadowość amin aromatycznych podstawniki zwiększające efekt elektronoakceptorowy obniżają zasadowość podstawniki elektronodonowe zwiększają zasadowość
31 Nukleofilowość amin konsekwencja obecności wolnej pary elektronów przy atomie azotu Alkilowanie (m.in. metoda otrzymywania amin z amoniaku) aminy pod wpływem odczynników alkilujących zwiększają rzędowość aminy 1 o przechodzą w aminy 2 o aminy 2 o w aminy 3 o aminy 3 o w 4 o sole amoniowe. praktyczne znaczenie ma alkilowanie amin aromatycznych do 3 o N,N-dialkiloaryloamin i otrzymywanie 4 o soli amoniowych
32 Nukleofilowość amin konsekwencja obecności wolnej pary elektronów przy atomie azotu Arylowanie czynnik arylujący: fluoroareny uaktywnione podstawnikami elektronoakceptorowymi (:B), związanymi z pierścieniem aromatycznym w pozycjach orto- lub/i para- 2,4-dinitrofluorobenzen - odczynnikiem do arylowania amin, w tym aminokwasów (także białkowych) amina 2,4-dinitro- 2,4-dinitrofluorobenzen fenyloamina
33 Nukleofilowość amin konsekwencja obecności wolnej pary elektronów przy atomie azotu Acylowanie aminy pod wpływem: halogenków acylowych bezwodników kwasowych aktywnych estrów ulegają acylowaniu; powstają amidy, pochodne amin pozbawione właściwości zasadowych i nukleofilowych odczynnik amina acylujący amid Y: -F, -Cl, -Br i -I w halogenkach kwasowych; -OCOR w bezwodnikach kwasowych -OR i -OAr w estrach aktywnych
34 Reaktywność amin Grupy -NH 2, -NHR i -NR 2, (podobnie jak -OR i OH) należą do grup trudnoodchodzących aminy 1 o, 2 o i 3 o są związkami trwałymi. nie ulegają termicznemu rozkładowi do alkenów 4 o wodorotlenki amoniowe są nietrwałe w podwyższonej temperaturze, rozkładają się do alkenu i z wydzieleniem 3 o aminy reakcja Hofmana
35 Reakcja eliminacji Hoffmana oderwanie przez zasadę protonu z atomu węgla sąsiadującego z grupą aminową odszczepienie kationu trialkiloamoniowego. reakcja zachodzi jedynie w środowisku zasadowym do eliminacji Hofmanna dochodzi dopiero po przekształceniu 4 o soli amoniowej w 4 o wodorotlenek amoniowy 4 o sól amoniowa 4 o wodorotlenek amoniowy alken heksyloamina jodek N,N,N trimetyloheksyloamoniowy trimetyloamina heks-1-en
36 Reakcje amin z kwasem azotowym (III) Aminy alifatyczne 1 o pod wpływem kwasu azotawego ulegają przemianie, powstaje mieszanina związków składająca się z: alkenu, alkoholu innych produktów podstawienia; wszystkie zawierają ten sam szkielet węglowy co amina
37 Reakcje amin z kwasem azotowym (III) utworzenie kationu nitrozoniowego: + NO kation nitrozoniowy w reakcji z aminą tworzy sól diazoniową alifatyczne soli diazoniowe są nietrwałe, szybko ulegają rozkładowi do karbokationu.
38 Reakcje amin z kwasem azotowym (III) karbokation stabilizując się odszczepia proton i powstaje alken: lub przyłącza nukleofil znajdujący się w środowisku reakcji, np. cząsteczkę wody, anion Cl-,. tworząc odpowiednią pochodną:
39 Aminy aromatyczne słabsze zasady i nukleofile niż aminy alifatyczne reszta arylowa poprzez efekt -M i -I osłabia właściwości zasadowe i nukleofilowe (efekt obecności wolnej pary elektronów na atomie azotu) grupa aminowa modyfikuje właściwości pierścienia aromatycznego czyniąc go bardziej aktywnym w reakcjach SE reakcja bromowania aniliny równoczesne podstawienie wszystkich możliwych miejsc - powstaje tribromoanilina (100%)
40 Aminy aromatyczne wpływ grupy aminowej na reakcje SE w pierścieniu obniżamy blokując acylowaniem grupę NH 2
41 Aminy aromatyczne - acylowanie w reakcji Friedela-Craftsa aminy aromatyczne można acylować w reakcji Friedela- Craftsa po uprzednim zacylowaniu grupy aminowej
42 Aminy aromatyczne - acylowanie w reakcji Friedela-Craftsa Otrzymywanie sulfonamidów leków przeciwbakteryjnych zamiast halogengów acylowych - kwas chlorosulfonowy amonoliza
Chemia organiczna. Związki zawierające azot. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
Chemia organiczna Związki zawierające azot Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Grupy funkcyjne zawierające azot Grupa funkcyjna Przykład związku Wzór Nazwa Wzór Nazwa -NO 2 nitrowa CH3NO2
AMINY. nikotyna. tytoń szlachetny. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
AMINY nikotyna H 3 C NH tytoń szlachetny OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN 2 NUKLEOFILOWOŚĆ i ZASADOWOŚĆ AMIN 3 REAKCJA AMIN Z KWASAMI MINERALNYMI I KARBOKSYLOWYMI
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Slajd 1. Slajd 2. Aminy. trietyloamina. amoniak. chlorofil
 Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Slajd 1 Aminy chlorofil Slajd 2 amoniak trietyloamina Slajd 3 Wypadkowy moment dipolowy 1 lub 2 aminy: donory lub akceptory wiązania wodorowego 3 aminy: mogą być wyłącznie akceptorami wiązania wodorowego
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
AMINY. tytoń szlachetny. nikotyna. pseudoefedryna (SUDAFED) atropina. muskaryna H 3 C CH 3 O
 AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
AMINY tytoń szlachetny H 3 C NH nikotyna OH CH 3 O OH pseudoefedryna (SUDAFED) O N atropina muskaryna 1 KLASYFIKACJA AMIN amoniak amina 1 amina 2 amina 3 HYBRYDYZACJA ATOMU AZOTU I TETRAEDRYCZNA BUDOWA
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Aminy - budowa. R alkil Alkiloamina Amina alifatyczna. Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA III - RZĘDOWA AMINA II - RZĘDOWA
 Aminy Aminy - budowa R alkil Alkiloamina Amina alifatyczna Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA II - RZĘDOWA AMINA III - RZĘDOWA Aminy - budowa ALKILOAMINY PIRAMIDA TRYGONALNA ARYLOAMINY
Aminy Aminy - budowa R alkil Alkiloamina Amina alifatyczna Ar aryl Aryloamina Amina aromatyczna AMINA I - RZĘDOWA AMINA II - RZĘDOWA AMINA III - RZĘDOWA Aminy - budowa ALKILOAMINY PIRAMIDA TRYGONALNA ARYLOAMINY
amoniak amina 1 amina 2 amina 3
 AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
AMINY 1. Klasyfikacja 5 godz. amoniak amina 1 amina 2 amina 3 1.1. 1 (pierwszorzędowe), np. izopropyloamina. 1.2. 2 (drugorzędowe), np. pirolidyna. 1.3. 3 (trzeciorzędowe), np. N,N-dimetyloanilina. 2.
1 Marek Żylewski. Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii Organicznej. NO 2 Zn, HCl HNO 3 N H 2. NH 2 Na 2. S x CHO.
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki azotowe Związki nitrowe 1. Redukcja związków nitrowych. Grupa nitrowa jest bardzo podatna na działanie
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Chemia organiczna. Mechanizmy reakcji chemicznych. Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego
 Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Chemia organiczna Mechanizmy reakcji chemicznych Zakład Chemii Medycznej Pomorskiego Uniwersytetu Medycznego 1 homoliza - homolityczny rozpad wiązania w jednym z reagentów; powstają produkty zawierające
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
WĘGLOWODORY AROMATYCZNE
 WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli
 11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
11. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas 1 11.1. Reakcja
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Aminy pochodne amoniaku, w których
 A M I N Y Aminy pochodne amoniaku, w których jeden (aminy 1 o ), dwa (aminy 2 o ) lub trzy (aminy 3 o ) atomy wodoru zostały zastąpione resztami organicznymi (alifatycznymi bądź aromatycznymi). Przykłady
A M I N Y Aminy pochodne amoniaku, w których jeden (aminy 1 o ), dwa (aminy 2 o ) lub trzy (aminy 3 o ) atomy wodoru zostały zastąpione resztami organicznymi (alifatycznymi bądź aromatycznymi). Przykłady
Aminy. Aminy 1 0 RNH 2 NH. Aminy 3 0 R 3
 Aminy Aminy 1 0 R 2 Aminy 2 0 R 2 Aminy 3 0 R 3 C 3 C 3 C C 3 C 3 C 3 C 2 C 3 C 3 C 3 C 3 alkohol 3 o amina 1 o amina 3 o Czwartorzędowa sól amoniowa: R R R R X 1 Aminy alifatyczne ( wszystkie podstawniki
Aminy Aminy 1 0 R 2 Aminy 2 0 R 2 Aminy 3 0 R 3 C 3 C 3 C C 3 C 3 C 3 C 2 C 3 C 3 C 3 C 3 alkohol 3 o amina 1 o amina 3 o Czwartorzędowa sól amoniowa: R R R R X 1 Aminy alifatyczne ( wszystkie podstawniki
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania
 Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Podstawy chemii organicznej. T. 2 / Aleksander Kołodzieczyk, Krystyna Dzierzbicka. Gdańsk, 2013 Spis treści 14. ZWIĄZKI KARBONYLOWE 11 14.1. Budowa grupy karbonylowej 11 14.2. Reaktywność związków karbonylowych
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
AMINY I ICH POCHODNE
 AMIY I I PDE rganiczne pochodne amoniaku. 4/5 powietrza azot. W naturze: aminokwasy, peptydy, białka, alkaloidy (kokaina, nikotyna, morfina, meskalina ), neurotransmitery, stymulanty, kwasy nukleinowe
AMIY I I PDE rganiczne pochodne amoniaku. 4/5 powietrza azot. W naturze: aminokwasy, peptydy, białka, alkaloidy (kokaina, nikotyna, morfina, meskalina ), neurotransmitery, stymulanty, kwasy nukleinowe
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 2
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 2 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Wykład 6. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
Widma UV charakterystyczne cechy ułatwiające określanie struktury pirydyny i pochodnych
 Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
Laboratorium. Podstawowe procesy jednostkowe w technologii chemicznej
 Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
 Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Temat: Białka Aminy Pochodne węglowodorów zawierające grupę NH 2 Wzór ogólny amin: R NH 2 Przykład: CH 3 -CH 2 -NH 2 etyloamina Aminy mają właściwości zasadowe i w roztworach kwaśnych tworzą jon alkinowy
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego. ĆWICZENIE 6 i 7. Aminy i amidy kwasowe
 ĆWICZENIE 6 i 7 Aminy i amidy kwasowe Do amin zaliczamy związki organiczne, których wzór można wyprowadzić ze wzoru amoniaku przez podstawienie w nim atomu lub atomów wodoru grupą lub grupami alkilowymi
ĆWICZENIE 6 i 7 Aminy i amidy kwasowe Do amin zaliczamy związki organiczne, których wzór można wyprowadzić ze wzoru amoniaku przez podstawienie w nim atomu lub atomów wodoru grupą lub grupami alkilowymi
Azotowe związki organiczne
 strona 1/1 Azotowe związki organiczne Krystyna Bogdanowicz-Szwed Procesy zachodzące w żywych organizmach są ściśle związane z chemią wielofunkcyjnych związków organicznych zawierających w swoich cząsteczkach
strona 1/1 Azotowe związki organiczne Krystyna Bogdanowicz-Szwed Procesy zachodzące w żywych organizmach są ściśle związane z chemią wielofunkcyjnych związków organicznych zawierających w swoich cząsteczkach
Podział związków organicznych
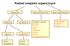 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Ćwiczenie 6 Aminokwasy
 Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
Ćwiczenie 6 Aminokwasy Aminokwasy są to związki dwufunkcyjne, których cząsteczki zawierają grupy karboksylowe i aminowe: grupa aminowa:nh 2 grupa karboksylowa COOH Nomenklatura aminokwasów: Naturalne aminokwasy
Reakcje chemiczne. Typ reakcji Schemat Przykłady Reakcja syntezy
 Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
Reakcje chemiczne Literatura: L. Jones, P. Atkins Chemia ogólna. Cząsteczki, materia, reakcje. Lesław Huppenthal, Alicja Kościelecka, Zbigniew Wojtczak Chemia ogólna i analityczna dla studentów biologii.
C H N O L B I O T E ORGANICZNA I A. Nomenklatura
 B T E L EMA G GAZA A omenklatura B T E L EMA G GAZA A Synteza AMY -rzędowe ' 2 2 2 ' 2 0 0 0 1 2 3 Typy amin -rzędowych w zależności od rzędowości atomu węgla związanego z grupą aminową METDY EDUKYJE
B T E L EMA G GAZA A omenklatura B T E L EMA G GAZA A Synteza AMY -rzędowe ' 2 2 2 ' 2 0 0 0 1 2 3 Typy amin -rzędowych w zależności od rzędowości atomu węgla związanego z grupą aminową METDY EDUKYJE
R 2 III-rzędowe R 1 N R 3
 ZWIĄZKI ZAWIERAJĄE AZT W GRUPA FUKYJY I. Wprowadzenie teoretyczne Ważniejsze związki organiczne zawierające azot w grupie funkcyjnej to aminy, aminokwasy, związki nitrowe oraz hydrazyna i jej pochodne.
ZWIĄZKI ZAWIERAJĄE AZT W GRUPA FUKYJY I. Wprowadzenie teoretyczne Ważniejsze związki organiczne zawierające azot w grupie funkcyjnej to aminy, aminokwasy, związki nitrowe oraz hydrazyna i jej pochodne.
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Analiza jakościowa wybranych aminokwasów
 Ćwiczenie 14 Analiza jakościowa wybranych aminokwasów I. Aminokwasy Aminokwasy są jednostkami strukturalnymi peptydów i białek. W swojej cząsteczce mają co najmniej 2 grupy funkcyjne: grupę aminową NH
Ćwiczenie 14 Analiza jakościowa wybranych aminokwasów I. Aminokwasy Aminokwasy są jednostkami strukturalnymi peptydów i białek. W swojej cząsteczce mają co najmniej 2 grupy funkcyjne: grupę aminową NH
MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA
 MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA Zadanie Odpowiedzi Uwagi a) za uzupełnienie tabeli: Symbol pierwiastka Konfiguracja elektronowa w stanie podstawowym Liczba elektronów walencyjnych S b) za uzupełnienie
MODEL ODPOWIEDZI I SCHEMAT PUNKTOWANIA Zadanie Odpowiedzi Uwagi a) za uzupełnienie tabeli: Symbol pierwiastka Konfiguracja elektronowa w stanie podstawowym Liczba elektronów walencyjnych S b) za uzupełnienie
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 2002 BYŁA DZISIAJ CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY ARKUSZ EGZAMINACYJNY I
 MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
CHARAKTERYSTYKA KARBOKSYLANÓW
 AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego ĆWICZENIE 5. Związki aromatyczne
 ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
Zarys Chemii Organicznej
 Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych:
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych: - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych reakcji; konstrukcja
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
WARSZTATY olimpijskie. Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna Kinetyka
 WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
WARSZTATY olimpijskie Co już było: Atomy i elektrony Cząsteczki i wiązania Stechiometria Gazy, termochemia Równowaga chemiczna inetyka WARSZTATY olimpijskie Co będzie: Data Co robimy 1 XII 2016 wasy i
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
Spis treści. Nazewnictwo kwasów karboksylowych.
 Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
CHEMIA. Treści nauczania- wymagania szczegółowe. Substancje i ich właściwości. Uczeń: Wewnętrzna budowa materii. Uczeń:
 CHEMIA Treści nauczania- wymagania szczegółowe Substancje i ich właściwości. Uczeń: Podaje przykłady zastosować chemii w życiu codziennym Nazywa wybrane szkło i sprzęt laboratoryjny oraz określa jego przeznaczenie
CHEMIA Treści nauczania- wymagania szczegółowe Substancje i ich właściwości. Uczeń: Podaje przykłady zastosować chemii w życiu codziennym Nazywa wybrane szkło i sprzęt laboratoryjny oraz określa jego przeznaczenie
fenol ninhydryna difenyloamina kwas octowy Określ ph amin: n-butyloamina dietyloamina difenyloamina anilina N,N-dimetyloanilina
 REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
REAKCJE PROBÓWKOWE 5. Aminy, aminokwasy, białka imię i nazwisko data nr str. Rubryki oznaczone po prawej stronie ciemnym prostokątem należy wypełniać przed zajęciami. W reakcjach obowiązują wzory strukturalne
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Organiczne związki azotu
 Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Organiczne związki azotu 1. arysuj wzory: a. acetylocholina b. adrenalina c. putrescyna d. dopamina e. kolamina 2. azwij poniższe związki: H 2 CH H C CH 2 A. B. C. D. OH H 2 2 2 E. F. G. H. H 2 I. 2 J.
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
PROGRAM ĆWICZEŃ Program ćwiczeń z chemii organicznej obejmuje wykonanie jedenastu zadań praktycznych i zdanie czterech kolokwiów.
 Wrocław 2019-10-01 REGULAMIN PRZEDMIOTU CHEMIA ORGANICZNA DLA STUDENTÓW II ROKU WYDZIAŁU FARMACEUTYCZNEGO UMW WE WROCŁAWIU (150 godzin ćwiczeń, 60 godzin wykładów) w roku akademickim 2019/ 2020 PROGRAM
Wrocław 2019-10-01 REGULAMIN PRZEDMIOTU CHEMIA ORGANICZNA DLA STUDENTÓW II ROKU WYDZIAŁU FARMACEUTYCZNEGO UMW WE WROCŁAWIU (150 godzin ćwiczeń, 60 godzin wykładów) w roku akademickim 2019/ 2020 PROGRAM
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
1. Substytucja nukleofilowa we fluorowcopochodnych
 B T E L EMA G GAZA A Synteza 1. Substytucja nukleofilowa we fluorowcopochodnych 1a) Etery dialkilowe można otrzymywać w reakcji pierwszorzędowych fluorowcopochodnych z ALKLAAM. Jest to reakcja Williamsona.
B T E L EMA G GAZA A Synteza 1. Substytucja nukleofilowa we fluorowcopochodnych 1a) Etery dialkilowe można otrzymywać w reakcji pierwszorzędowych fluorowcopochodnych z ALKLAAM. Jest to reakcja Williamsona.
δ + δ - δ + R O H RJC R δ + δ - δ - δ + R O R Grupy Funkcyjne δ + O NH 2 R N H H R N Slides 1 to 41
 1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
1 δ + δ + δ + R R X Grupy Funkcyjne δ + δ + R R R δ + R δ + X δ + R N R δ + R δ + R R δ + R δ + N 2 R δ + R N δ + δ + Slides 1 to 41 2 Grupy Funkcyjne Zawierające eteroatomy Grupy funkcyjne mają często
Program wykładu Chemia Organiczna I
 Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
Program wykładu Chemia Organiczna I Semestr III - 2016/2017 r. poziom A i B Wtorek 17:30-18:15 (B, sala 338), czwartek 14:30 15:15 (A i B, aula) oraz piątek 11:30 13:00 (A i B, aula), prof. dr hab. R.
MIKROANALIZY WĘGLOWODORY. W1 Utlenianie węglowodorów nadmanganianem potasu w środowisku kwaśnym (w temp. pokojowej) RÓWNANIA REAKCJI: OBSERWACJE:
 MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka
 Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Ćwiczenie 4. Reakcja aminokwasów z ninhydryną. Opisz typy reakcji przebiegających w tym procesie i zaznacz ich miejsca przebiegu.
 azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
azwisko i imię grupa data Protokół z ćwiczenia: eakcje chemiczne związków biologicznych: aminokwasy i peptydy. Definicja punktu izoelektrycznego pi. Formy jonowe aminokwasów w różnym ph. ph < pi ph = pi
Narysuj stereoizomery cis i trans dla 1,2-dibromocyklobutanu. Czy ulegają one wzajemnej przemianie, odpowiedź uzasadnij.
 WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
WERSJA A EGZAMIN z hemii rganicznej I. IZMERIA ZWIĄZKÓW RGANIZNY 1. Narysuj wzory w projekcji konikowej i w projekcji Newmana 1,2-dibromoetanu 1,1-dibromoetanu w konformacji synklinalnej (gauche) w najbardziej
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14):
 Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Zagadnienia obowiązujące przy każdym kolokwium z ćwiczeń syntetycznych (rok akademicki 2013/14): - znajomość instrukcji (kolejność i cel poszczególnych operacji; umiejętność zapisu równań wszystkich przeprowadzanych
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Chemia węgla. Chemia Wydział SiMR, kierunek IPEiH I rok I stopnia studiów, semestr I. Chemia organiczna - podstawy
 hemia Wydział SiMR, kierunek IPEi I rok I stopnia studiów, semestr I dr inż. Leszek iedzicki hemia organiczna - podstawy hemia węgla hemia organiczna to chemia związków węgla. Inne pierwiastki, które zwykle
hemia Wydział SiMR, kierunek IPEi I rok I stopnia studiów, semestr I dr inż. Leszek iedzicki hemia organiczna - podstawy hemia węgla hemia organiczna to chemia związków węgla. Inne pierwiastki, które zwykle
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Mechanizm dehydratacji alkoholi
 Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Benzen 2C 6 H 6 + 3O 2 12C + 6H 2 O
 Benzen Najprostszym arenem, jest benzen o wzorze sumarycznym C 6 H 6. To bezbarwna, lotna ciecz, topniejąca w temperaturze 5,533 C, a wrząca w temperaturze 80,09 C. Gęstość benzenu w temperaturze 20 C,
Benzen Najprostszym arenem, jest benzen o wzorze sumarycznym C 6 H 6. To bezbarwna, lotna ciecz, topniejąca w temperaturze 5,533 C, a wrząca w temperaturze 80,09 C. Gęstość benzenu w temperaturze 20 C,
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
