WPŁYW SIŁY JONOWEJ ROZTWORU NA SZYBKOŚĆ REAKCJI CHEMICZNEJ EFEKT SOLNY BRÖNSTEDA
|
|
|
- Dominik Karpiński
- 6 lat temu
- Przeglądów:
Transkrypt
1 Ćwzene nr B6 WPŁYW SIŁY JONOWEJ ROZTWORU NA SZYBKOŚĆ REAKCJI CHEMICZNEJ EFEKT SOLNY BRÖNSTEDA I. Cel ćwzena Wyznazają stałą szybkoś reakj hemznej elem ćwzena jest zbadane zy obeność jonów ne borąyh udzału w reakj wpływa na jej szybkość. II. Zagadnena wprowadzająe 1. Defnja szybkoś reakj hemznej. 2. Stała szybkoś reakj metody wyznazana. 3. Czynnk wpływająe na szybkość reakj hemznej: - stężene reagentów, - temperatura, - katalzator, - obeność jonów w roztworze - efekt solny Brönsteda. 4. Prawo Lamberta-Beera. 5. Sła jonowa roztworu (granzne prawo Debye a-hükela). Lteratura obowązująa: 1. R. Brdčka, Podstawy hem fzyznej, PWN, Warszawa, Praa zborowa, Chema fzyzna, PWN, Warszawa, roznk, wydane dowolne. 3. E. Szyszko, Instrumentalne metody analtyzne, PZWL, W. Szzepanak, Metody nstrumentalne w analze hemznej, PWN, Warszawa, 1985, str P.W. Atkns, Podstawy hem fzyznej, PWN, Warszawa, P.W. Atkns, Chema fzyzna, PWN, Warszawa, 2001.
2 III. Część teoretyzna III. 1. Szybkość reakj Szybkość reakj ν to welkość harakteryzująa stosunek zmany stężeń produktów (substratów) do zasu trwana reakj hemznej. d v = ± (1) dt gdze: stężene reagenta (produktu znak plus lub substratu znak mnus), t zas trwana reakj. Na przykład, szybkość reakj rozpadu amonaku: 2NH N +3H dla substratów można zlustrować równanem: a dla produktów następująą zależnośą: dnnh v = 3 (2) dt dnn dn 2 H2 v = lub v = (3) dt dt Dla rozważanej reakj szybkość tworzena sę poszzególnyh produktów jest różna. W wynku rozpadu dwóh mol amonaku powstaje ne tylko mol azotu, ale w tym samym zase powstają równeż trzy mole wodoru. Szybkość reakj wyrażona równanem (1) jest zależna od rodzaju rozważanego reagenta. Aby tę zależność wyelmnować, w równanu określająym szybkość reakj wprowadza sę współzynnk stehometryzne reakj (dodatne dla produktów a ujemne dla substratów). Dla rozważanej reakj można napsać: dnnh dnn2 = ( 2) dt dt 3 = dn H 2 3dt (4) Tak wę szybkoś reakj podzelone przez współzynnk stehometryzne są sobe równe, tak jak zmany lzby mol reagentów w danym zase do h współzynnków stehometryznyh: 2
3 dnnh dn 3 N dn 2 H 2 d ξ = = = (5) gdze: ξ oznaza postęp reakj wyrażony ogólnym wzorem: dn d = v ξ (6) a ν to współzynnk stehometryzny -tego reagenta (dodatn dla produktów, ujemny dla substratów reakj). Dlatego też zgodne z zaleenem Mędzynarodowej Un Chem Czystej Stosowanej (IUPAC) szybkość reakj defnuje sę ostatezne jako: d dn v = ξ = (7) dt v dt Powyższe równane (7) unezależna szybkość reakj od rodzaju reagenta, którego użyto do pomaru szybkoś reakj. III. 2. Rząd reakj Szybkość reakj można powązać ze stężenem reagująyh reagentów. Taka forma wyrażana szybkoś reakj nos nazwę równana knetyznego reakj. Ogólne równane knetyzne reakj ma postać: = (8) gdze:,, stężene reagentów A, B, C..., k stała szybkoś reakj. Wykładnk potęgowe α, β, χ noszą nazwę rzędu reakj a h suma to ałkowty rząd reakj (n): n = α + β + χ +... (9) Wartość k lzbowo równa jest szybkoś reakj, gdy stężena wszystkh reagująyh produktów są równe jednoś. Współzynnk k jest harakterystyzny dla danej reakj jest nezależny od stężeń reagentów. Jego wartość może zmenać sę wraz z temperaturą, dodatkem katalzatora, słą jonową roztworu dla substanj reagująyh jonowo. 3
4 III. 3. Wyznazane stałej szybkoś reakj Wyznazene stałej szybkoś reakj wymaga znalezena zależnoś pomędzy zasem reakj a stężenem reagentów. Można ją wyprowadzć poprzez połązene równana (1) oraz równana (8) otrzymuje sę wtedy tzw. ałkowe równane knetyzne reakj. Dla reakj I rzędu otrzymujemy zależność: d = k1 (10) dt Całkują lewą stronę równana w granah od = do a prawą od = do t otrzymujemy: = 0 d a po sałkowanu otrzymuje sę zależność: t t 0 k1 dt (11) ln = k1t ln = ln 0 kt (12) 0 Przykładem takej reakj może być rozpad pęotlenku dazotu: N O 2NO+ O Z równana (12) wynka, że logarytm stężena substratu w reakj perwszego rzędu maleje lnowo wraz z zasem trwana reakj. Z równana knetyznego można wyznazyć także zas połówkowy reakj, tj. zas, w którym stężene substratu zmnejszy sę o połowę: ln 2 t 1 = (13) 2 k Dla reakj II rzędu, przy założenu, że stężena substratów są sobe równe otrzymujemy zależność: d dt 1 k 2 = 2 (14) 4
5 a po jej przekształenu sałkowanu równane: = t t d k dt 2 2 (15) = k2t = k2t (16) 0 Z powyższego wyrażena wynka, że dla reakj II rzędu odwrotność stężena substratu rośne lnowo z zasem. Czas połówkowy reakj II rzędu opsuje wzór: Przykładem tego typu reakj może być: t = 1 1/ 2 k (17) I +ClO IO +Cl III. 4. Teora absolutnyh szybkoś reakj Eyrnga teora kompleksu aktywnego Jedną z bardzo stotnyh eh reakj hemznyh jest h zułość na zmany temperatury. Zmana temperatury może wpłynąć na wartość stałej równowag reakj, o może zmenć jej szybkość, zyl stałą szybkoś reakj. Wpływ temperatury na wartość stałej równowag reakj określa efekt energetyzny reakj ( H), natomast wpływ temperatury na szybkość reakj określa wartość energ aktywaj reakj. Wyjaśnene tego zjawska dla reakj przebegająyh w ekłyh roztworah opraował Eyrng na grune termodynamk. Podstawowym założenem teor Eyrnga jest to, że etapem przejśowym w reakj hemznej pomędzy substratam a produktam jest kompleks aktywny. W tym przypadku shematyzne drogę reakj hemznej można przedstawć następująym wyrażenem: "+# ("#) &+' (18) gdze: (AB)* oznaza przejśowy kompleks aktywny utworzony na skutek zderzena sę ząstezek reagentów. Kompleks aktywny jest układem netrwałym, którego ne można wyzolować ze środowska reakj. Ma on bardzo krótk zas żya rozpada sę z utworzenem produktów (C D) bądź z odtworzenem substratów A B. 5
6 Teora absolutnej szybkoś reakj Eyrnga pozwolła na wyjaśnene sensu fzyznego parametrów równana Arrhenusa, oraz na wpływu sły jonowej roztworu na szybkość reakj hemznej. III. 5. Wpływ sły jonowej roztworu na szybkość reakj hemznej Zaobserwowano, że na szybkość nektóryh reakj hemznyh ma wpływ obeność monyh elektroltów w roztworah reakyjnyh. Należy zaznazyć, że żaden z jonów elektroltu ne jest katalzatorem badanej reakj. Tak efekt nazwano perwotnym efektem solnym lub efektem solnym Brönsteda. Rozważmy reakję pomędzy jonam A B o ładunkah ( (. Shematyzne, z uwzględnenem powstawana kompleksu aktywnego, można przedstawć ją w następująy sposób: z A 1 z z z k' + B 2 AB * C + (19) 2 gdze: z 1 (AB)* + z oznaza aktywny kompleks. ( ) D Stała równowag tworzena tego kompleksu wyrażona jest ogólnym wzorem: a K* = a a (AB)* (AB)* (AB)* = (20) A B A B A B gdze: a aktywność danej substanj, współzynnk aktywnoś, stężene molowe. Szybkość reakj (19) jest określona przez szybkość rozpadu kompleksu aktywnego, przy zym według teor kompleksu aktywnego jest to reakja perwszego rzędu, tak wę: v = k' (AB)* (21) Z równana (20) można oblzyć stężene kompleksu aktywnego: A B (AB)* = K*AB (22) (AB)* Tak wę równane (21) na szybkość reakj ma postać: A B A B v = k'k* AB = k0 AB (23) (AB)* (AB)* gdze: k 0 = k K*. 6
7 Jeśl reakja A+B jest reakją drugego rzędu, to równane knetyzne na szybkość reakj (19) można napsać w następująej posta: Porównują równane (23) (24) otrzymamy: v = k A B (24) k k0 A B = (25) (AB)* Współzynnk aktywnoś reagująyh jonów oraz kompleksu aktywnego można określć przy pomoy teor Debye a Hükela z 1924 roku, która po raz perwszy uwzględnła oddzaływana mędzy jonam w roztworze. Zakłada ona stnene sł kulombowskh mędzy rozpatrywanym jonem a pozostałym jonam w roztworze. Energa potenjalna tyh oddzaływań jest wększa dla jonów blskh mnejsza dla odległyh, poneważ jest odwrotne proporjonalna do odległoś. Poneważ lzba jonów rośne proporjonalne wraz z drugą potęgą odległoś ne wolno zanedbywać oddzaływana jonów znajdująyh sę w pewnej odległoś od danego jonu. Dla roztworów rozeńzonyh współzynnk aktywnoś można określć zależnośą zwaną granznym prawem Debye a-hükela: log 2 = Az I (26) gdze: z ładunek -tego jonu, A stała, zależna od temperatury rodzaju rozpuszzalnka (dla roztworów wodnyh w temperaturze pokojowej A = 0,509), I sła jonowa roztworu. 1 2 I = z (27) 2 Na podstawe równań (25) (27) można zapsać: A log B (AB)* ( z + z z ) = A I (28) A B (AB)* Poneważ ładunek kompleksu aktywnego jest równy sume ładunków tworząyh go jonów: z = z + z (29) (AB)* A B równane (28) przyjme postać: AB log = 2Az AzB I (30) (AB)* 7
8 a po podstawenu równana (30) do równana (25) otrzymujemy: log k = log k + 0 2Az z I (31) Jak wynka z równana (31) wartość stałej szybkoś reakj zmena sę wraz ze wzrostem sły jonowej roztworu. Charakter tyh zman zależy od znaku reagująyh jonów. Jeśl h znak są take same to wzrost sły jonowej roztworu powoduje wzrost wartoś stałej szybkoś reakj, o oznaza, że zwększene stężena elektroltu, którego jony ne borą udzału w reakj wpływa na jej szybkość. W przypadku, kedy reagująe jony są przewnyh znaków, wtedy wzrost sły jonowej roztworu powoduje zmnejszene stałej szybkoś reakj tak wę szybkość reakj maleje wraz ze wzrostem stężena elektroltu ne borąego udzału w rozważanej reakj hemznej. A B III. 6. Absorpja promenowana elektromagnetyznego Prawa Lamberta-Beera Promenowane elektromagnetyzne może być pohłanane przez materę. Pohłonęe kwantu promenowana powoduje wzbudzene elektronowe atomów lub ząstezek. Energa potrzebna do takego wzbudzena w zależnoś od ząstk wzbudzonej mater waha sę od klku do klkuset elektronowoltów. Dlatego też absorbowane fotony leżą w granah śwatła wdzalnego lub promenowana nadfoletowego. Pohłanane promenowana przez materę nos nazwę absorpj promenowana. Jedną z konsekwenj pohłanana promenowana elektromagnetyznego jest barwa otazająyh nas przedmotów. Śwatło wdzalne (bałe) składa sę z promenowana elektromagnetyznego o różnej długoś fal odpowadająej barwom wszystkh kolorów od zerwonego poprzez pomarańzowy, żółty, zelony, nebesk do foletowego. Usunęe z wdzalnej zęś promenowana elektromagnetyznego którejś z barw na skutek pohłanana (absorpj) promenowana powoduje, że otrzymujemy barwę komplementarną. Na przykład, absorpja przez substanję promenowana elektromagnetyznego odpowadająego barwe zerwonej będze powodowała, że dany obekt będze mał kolor zelony, barwy foletowej kolor żółty td.). Postrzegane przez nas barw jest zjawskem bardzo złożonym subektywnym. Substanje whodząe w skład danego obektu mogą absorbować promenowane elektromagnetyzne o różnej długoś fal. W skrajnym przypadku (ała doskonale zarnego) ałe spektrum promenowana z zakresu wdzalnego, padająego na tak obekt, jest absorbowana. Ponadto oko każdego złoweka harakteryzuje sę neo nną wrażlwośą postrzegana kolorów. Nemnej jednak w głównej merze barwa otazająyh nas przedmotów jest 8
9 konsekwenją oddzaływana promenowana elektromagnetyznego (śwatła) z materą. Absorpja promenowana przez daną substanję zależy od: rodzaju substanj, energ promenowana (zęstoś, długoś fal promenowana), długoś drog promen elektromagnetyznyh w próbe (gruboś warstwy absorpyjnej), molowego stężena substanj w próbe. Absorpję promenowana można wyrazć przy pomoy transmtanj T lub absorbanj A. Transmtanja T jest to stosunek natężena promenowana przehodząego przez próbkę I do natężena promenowana padająego na próbkę I 0 : I T = (32) I 0 Absorbanja A nazywana także ekstynkją lub gęstośą optyzną jest zdefnowana jako: " = *+,- =*+,. = *+,/ 0 / (33) Absorpja promenowana określona jest przez dwa prawa: III Prawo Lamberta Względne zmnejszene natężena śwatła przehodząego przez układ jest nezależne od natężena śwatła padająego: I = I 0 onst (34) Natężene promenowana zmena sę o ten sam ułamek w każdej warstwe o tej samej gruboś układu absorbująego: I~ l gdze: l grubość warstwy absorbująej. III Prawo Beera Natężene promenowana przehodząego przez ośrodek absorbująy jest proporjonalne do lzby entrów absorbująyh: 9
10 I~ gdze: stężene molowe substanj absorbująej promenowane. Prawa te są spełnone jeżel: promenowane padająe na układ stanow wązkę równoległą monohromatyzną, warstwa substanj absorbująej jest jednolta (homogenzna), układ absorbująy ma entra absorpyjne dzałająe nezależne od sebe, można zanedbać następująe proesy towarzysząe absorbj promenowana take jak: rozproszene śwatła, reakje fotohemzne, obsadzane stanów wzbudzonyh, proesy welofotonowe. Często te dwa prawa są stosowane razem znane pod nazwą prawa Lamberta- Beera. Absorbanja promenowana elektromagnetyznego jest proporjonalna do drog optyznej l stężena molowego (dla fazy gazowej do śnena) substanj absorbująej. Matematyzne prawo to można wyrazć w posta: di = εl (35) dl gdze: ε stała proporjonalnoś. Po sałkowanu równana (35) otrzymujemy: *1 / 0 =2* / *+,/ 0 = " =2* (36) / Jeżel stężene absorbująej substanj jest wyrażone w mol dm 3 a droga optyzna lw m to ε nos nazwę molowego współzynnka absorpj. Przyrządy rejestrująe welkość absorbanj lub transmtanj nazywamy spektrofotometram. Wększość spektrofotometrów rejestruje zmany welkoś A lub T w zależnoś od długoś fal lub jej zęstoś. Ze względu na to, że absorbanja jest lnowo zależna od drog optyznej oraz stężena molowego absorbująej substanj znajduje wększe zastosowane w praktye. W przypadku, gdy w badanym układze znajduje sę klka substanj absorbująyh promenowane o danej długoś fal, absorbanja układu jest równa sume absorbanj poszzególnyh składnków układu jest to tzw. prawo addytywnoś absorbanj: A = A = εl (37) Przy pomoy wyżej omówonyh praw można z dużą dokładnośą określć stężene substanj absorbująej promenowane dla roztworów rozeńzonyh 10
11 ( < 10 2 mol/dm 3 ). Tylko w takh roztworah współzynnk ε ne zależy od współzynnka załamana śwatła (w przeweństwe do roztworów stężonyh). III Odhylena od prawa Lamberta Beera Odhylena od prawa Lamberta-Beera mogą występować z przyzyn aparaturowyh lub wynkać z właśwoś badanyh układów. Instrumentalne przyzyny odhylena od prawa Lamberta-Beera są następująe: nehomogenzna wązka promenowana brak monohromatyznoś promenowana wązk może powodować zarówno odhylena dodatne jak ujemne, poneważ molowy współzynnk absorbanj zależy od długoś fal; występowane promenowana rozproszonego; zjawsko to jest wdozne szzególne w przyrządah nskej klasy, takh, w któryh detektor rejestruje zarówno promenowane przehodząe przez roztwór jak rozproszone). w przyrządah o dobryh parametrah tehnznyh ten problem ne stneje. Fzykohemzne przyzyny odhyleń od prawa Lamberta-Beera: fluoresenja składnków układu, zmany stężena spowodowane oddzaływanem absorbująyh substanj asojają, kompleksowanem, zmany absorbanj spowodowane przejśem w stan jonowy badanej substanj np. dysojają, zależność wartoś ε od polaryzaj promenowana. Szzegółowo zagadnenam dotyząym oddzaływana wdzalnego promenowana elektromagnetyznego z materą zajmuje sę dzał fzyk o nazwe optyka. 11
12 IV. Część dośwadzalna A. Aparatura odzynnk 1. Aparatura: Spektrofotometr Cel CE Sprzęt laboratoryjny: kolbka marowa o poj. 25 m 3 4 szt. ppeta marowa o poj. 0,5 lub 1 m 3 1 szt. ppeta marowa o poj. 2 m 3 2 szt. ppeta marowa o poj. 10 m 3 1 szt. 3. Odzynnk: 1, mol/dm 3 wodny roztwór foletu krystalznego 0,5 mol/dm 3 wodny roztwór Na 2 SO 4 0,5 mol/dm 3 wodny roztwór NaOH B. Wykonane ćwzena 1. Określene długoś fal odpowadająej maksymalnej absorbanj (λ max ). W tym elu należy roztwór wyjśowy foletu krystalznego rozeńzyć dzesęokrotne przy pomoy wody destylowanej tak, aby uzyskać o najmnej 3 m 3 roztworu. Następne dla tak sporządzonego roztworu należy zmerzyć absorbanję A względem wody (nstrukja obsług spektrofotometru Cel CE1011, znajduje sę na praown, przy aparae). Pomary należy przeprowadzć dla długoś fal od 560 do 630 nm (o 10 nm). Przy wykonywanu pomarów należy pamętać, że dla każdej długoś fal należy ustawć wartość absorbanj równą 0 dla wody destylowanej. 2. Wykonane 4 ser pomarowyh przy długoś fal, dla której absorbanja jest najwększa. W kolbkah o pojemnoś 25 m 3 sporządzamy roztwory zgodne z ponższą tabelą: Numer ser 1, mol/dm 3 foletu krystalznego Objętość roztworu (m 3 ) 0,5 mol/dm 3 H 2 O destylowanej Na 2 SO 4 0,5 mol/dm 3 NaOH* I 1,5 0 0,2 II 1,5 1 Uzupełnć wodą 0,2 III 1,5 3 do kresk 0,2 IV 1,5 6 0,2 *dodajmy tuż przed rozpozęem pomaru (t=0). 12
13 Do sporządzonyh roztworów foletu z sarzanem VI sodu (do każdej ser) dodajemy bezpośredno przed rozpozęem pomaru 0,2 m 3 0,5 mol/dm 3 roztworu NaOH (t=0). Roztwór należy dokładne wymeszać przelać do przygotowanej kuwety. Merzymy zapsujemy wartoś absorbanj o 1 mn (dla ser IV o 2 mn) w zase mn. C. Opraowane wynków Folet krystalzny (hlorowodorek heksametylo-p-rozanlny) jest jednym z ważnejszyh zasadowyh barwnków trfenylometanolowyh. Stosuje sę go do barwena wyrobów z włókna polakrylontrylowego (anlany), wyrobów papernzyh farb drukarskh oraz jako środek dezynfekyjny (tzw. folet genjanowy) wskaźnk w analze. Folet używany jest także w proesah barwena drobnoustrojów, przede wszystkm w barwenu metodą Grama podstawowej próbe różnująej baktere. W środowsku zasadowym folet krystalzny przehodz w formę bezbarwną. Reakja ta jest na tyle powolna, że można ją śledzć spektrofotometryzne. Jeśl w roztworze jest tak duży nadmar jonów hydroksylowyh, że podzas przebegu reakj h stężene można uważać za stałe, wówzas do opsu przemany foletu krystalznego z formy barwnej w bezbarwną, można użyć równana knetyznego perwszego rzędu. Właśne z taką sytuają mamy do zynena w przypadku badanej przez nas reakj (stężene NaOH jest około 450 razy wyższe nż stężene foletu krystalznego). Zgodne z prawem Lamberta-Beera merzona absorbanja jest proporjonalna do stężena foletu krystalznego, zyl / 0 = A/A 0. Stałą szybkoś reakj znajdujemy grafzne. 13
14 1. Wynk pomarów należy przedstawć w tabel: t [s] Objętość roztworu Na 2 SO 4 (m 3 ) A lna A lna A lna A lna 2. Dla każdego z badanyh roztworów wykreślć zależność lna=f(t). 3. Ze sporządzonyh wykresów znaleźć grafzne stałą szybkoś reakj (k). 4. Dla każdego roztworu oblzyć wartość sły jonowej roztworu (I), uwzględnają stężene jonów pohodząyh z dysojaj Na 2 SO 4 oraz NaOH (stężene jonów pohodząyh z dysojaj barwnka jest tak małe, że możemy je zanedbać). 5. Zebrać w tabel wartoś sły jonowej roztworu oraz odpowadająe m stałe szybkoś reakj. Nr ser I I 1/2 k log k 6. Narysować wykres zależnoś k = f ( I ) log. 7. We wnoskah należy określć: Wpływ obenoś sol na szybkość reakj hemznej. Jak typ efektu Brönsteda występuje (dodatn zy ujemny)? odpowedź uzasadnć. Porównać wartość współzynnka kerunkowego otrzymanego z wykresu ( I ) log k = f z wartośą teoretyzną otrzymaną z równana (31). 14
Wyznaczenie współczynnika podziału kwasu octowego pomiędzy fazą organiczną a wodną
 Ćwzene 13 Wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną a wodną Cel ćwzena Celem ćwzena jest wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną (butanolem) a wodną w oparu
Ćwzene 13 Wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną a wodną Cel ćwzena Celem ćwzena jest wyznazene współzynnka podzału kwasu otowego pomędzy fazą anzną (butanolem) a wodną w oparu
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
WPŁYW SIŁY JONOWEJ ROZTWORU N STŁĄ SZYKOŚI REKJI WSTĘP Rozpatrzmy reakcję przebegającą w roztworze mędzy jonam oraz : k + D (1) Gdy reakcja ta zachodz przez równowagę wstępną, w układze występuje produkt
I PRACOWNIA FIZYCZNA, UMK TORUŃ WYZNACZANIE MOMENTU BEZWŁADNOŚCI BRYŁY SZTYWNEJ ZA POMOCĄ WAHADŁA TORSYJNEGO
 PACOWNA FZYCZNA, UMK TOUŃ nstrukja do ćwzena nr 9 * WYZNACZANE MOMENTU BEZWŁANOŚC BYŁY SZTYWNEJ ZA POMOCĄ WAHAŁA TOSYJNEGO. Cel ćwzena Wyznazene momentu bezwładnoś za pomoą wahadła torsyjnego (metoda dynamzna).
PACOWNA FZYCZNA, UMK TOUŃ nstrukja do ćwzena nr 9 * WYZNACZANE MOMENTU BEZWŁANOŚC BYŁY SZTYWNEJ ZA POMOCĄ WAHAŁA TOSYJNEGO. Cel ćwzena Wyznazene momentu bezwładnoś za pomoą wahadła torsyjnego (metoda dynamzna).
SPEKTROSKOPIA MOLEKULARNA
 SPEKTROSKOPIA MOLEKULARNA Ćwzene 1 Badane wązana wodorowego za pomoą spektroskop absorpyjnej w podzerwen. A. BADANIE AUTOASOCJACJI ALKOHOLU OKTYLOWEGO ODCZYNNIKI Substanja badana: oktanol (d=0.83 g/m 3
SPEKTROSKOPIA MOLEKULARNA Ćwzene 1 Badane wązana wodorowego za pomoą spektroskop absorpyjnej w podzerwen. A. BADANIE AUTOASOCJACJI ALKOHOLU OKTYLOWEGO ODCZYNNIKI Substanja badana: oktanol (d=0.83 g/m 3
Kwantowa natura promieniowania elektromagnetycznego
 Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
Efekt Comptona. Kwantowa natura promenowana elektromagnetycznego Zadane 1. Foton jest rozpraszany na swobodnym elektrone. Wyznaczyć zmanę długośc fal fotonu w wynku rozproszena. Poneważ układ foton swobodny
Współczynniki aktywności w roztworach elektrolitów. W.a. w roztworach elektrolitów (2) W.a. w roztworach elektrolitów (3) 1 r. Przypomnienie!
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ (s) Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H H H r Przypomnene! tw, Ag ( aq) tw, ( aq) Jest ona merzalna ma sens fzyczny.
WYSYCHANIE ZABYTKOWYCH MURÓW Z CEGŁY *
 ROCZNIKI INŻYNIERII BUDOWLANEJ ZESZYT 7/007 Komsja Inżyner Budowlanej Oddzał Polskej Akadem Nauk w Katowah WYSYCHANIE ZABYTKOWYCH MURÓW Z CEGŁY * Andrzej KUCHARCZYK Poltehnka Opolska, Opole. Wprowadzene
ROCZNIKI INŻYNIERII BUDOWLANEJ ZESZYT 7/007 Komsja Inżyner Budowlanej Oddzał Polskej Akadem Nauk w Katowah WYSYCHANIE ZABYTKOWYCH MURÓW Z CEGŁY * Andrzej KUCHARCZYK Poltehnka Opolska, Opole. Wprowadzene
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Współczynnk aktywnośc w roztworach elektroltów Ag(s) + ½ 2 (s) = Ag + (aq) + (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag + + ( aq) Jest ona merzalna ma sens
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda aceton chloroform metodą refraktometryczną opracowała dr hab. Małgorzata Jóźwak ćwczene nr 0 Zakres zagadneń
1 Kinetyka reakcji chemicznych
 Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
EFEKT SOLNY BRÖNSTEDA
 EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
Współczynniki aktywności w roztworach elektrolitów
 Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Współczynnk aktywnośc w roztworach elektroltów Ag(s) ½ 2 (s) = Ag (aq) (aq) Standardowa molowa entalpa takej reakcj jest dana wzorem: H r Przypomnene! = H tw, Ag ( aq) Jest ona merzalna ma sens fzyczny.
Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych
 CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
SPRAWDZANIE PRAWA MALUSA
 INSTYTUT ELEKTRONIKI I SYSTEMÓW STEROWANIA WYDZIAŁ ELEKTRYCZNY POLITECHNIKA CZĘSTOCHOWSKA LABORATORIUM FIZYKI ĆWICZENIE NR O- SPRAWDZANIE PRAWA MALUSA I. Zagadnena do przestudowana 1. Fala elektromagnetyczna,
INSTYTUT ELEKTRONIKI I SYSTEMÓW STEROWANIA WYDZIAŁ ELEKTRYCZNY POLITECHNIKA CZĘSTOCHOWSKA LABORATORIUM FIZYKI ĆWICZENIE NR O- SPRAWDZANIE PRAWA MALUSA I. Zagadnena do przestudowana 1. Fala elektromagnetyczna,
Refraktometria. sin β sin β
 efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
efraktometra Prędkość rozchodzena sę promen śwetlnych zależy od gęstośc optycznej ośrodka oraz od długośc fal promenena. Promene śwetlne padając pod pewnym kątem na płaszczyznę granczących ze sobą dwóch
Definicja szybkości reakcji
 Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
13. Termodynamika - równania Gibbsa, Gibbsa-Duhema i wstęp do diagramów fazowych.
 13. Termodynamka - równana Gbbsa, Gbbsa-Duhema wstęp do dagramów fazowyh. 13.1. Potenjały termodynamzne: Energa wewnętrzna U reprezentuje ałkowtą energę układu, będąą sumą energ knetyznyh potenjalnyh zarówno
13. Termodynamka - równana Gbbsa, Gbbsa-Duhema wstęp do dagramów fazowyh. 13.1. Potenjały termodynamzne: Energa wewnętrzna U reprezentuje ałkowtą energę układu, będąą sumą energ knetyznyh potenjalnyh zarówno
SZYBKOŚĆ REAKCJI JONOWYCH W ZALEŻNOŚCI OD SIŁY JONOWEJ ROZTWORU
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW SZYBKOŚĆ REAKCI ONOWYCH W ZALEŻNOŚCI OD SIŁY ONOWE ROZTWORU Opiekun: Krzysztof Kozieł Miejsce ćwiczenia: Czerwona Chemia,
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW SZYBKOŚĆ REAKCI ONOWYCH W ZALEŻNOŚCI OD SIŁY ONOWE ROZTWORU Opiekun: Krzysztof Kozieł Miejsce ćwiczenia: Czerwona Chemia,
Sieć kątowa metoda spostrzeżeń pośredniczących. Układ równań obserwacyjnych
 Seć kątowa etoda spostrzeżeń pośrednząyh Układ równań obserwayjnyh rzyrosty współrzędnyh X = X X X X = X X Y = Y Y X Y = Y Y Długość odnka X ' ' ' ' x y Współzynnk kerunkowe x y * B * x y x y gdze - odpowedn
Seć kątowa etoda spostrzeżeń pośrednząyh Układ równań obserwayjnyh rzyrosty współrzędnyh X = X X X X = X X Y = Y Y X Y = Y Y Długość odnka X ' ' ' ' x y Współzynnk kerunkowe x y * B * x y x y gdze - odpowedn
FUGATYWNOŚCI I AKTYWNOŚCI
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część VI TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene G n de,t, n j G na odstawe tego, że otenjał
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część VI TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene G n de,t, n j G na odstawe tego, że otenjał
Definicja szybkości reakcji
 Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany. v zas zmiana stężenia potrzebny do zajśia
Definicja szybkości reakcji. Szybkości reakcji. Równanie kinetyczne reakcji ...
 Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany v zmiana stężenia zas potrzebny do zajśia dx
Definija szybkośi reakji Szybkość reakji definiuje się jako stosunek zmiany stężenia substratów lub produktów reakji do zasu potrzebnego do zajśia tej zmiany v zmiana stężenia zas potrzebny do zajśia dx
Chemia fizyczna. Notatki z wykładów dr hab. Szczepana Zapotocznego
 Anna Krzykawska Chema fzyzna Notatk z wykładów dr hab. Szzepana Zapotoznego Zwększene lzby absolwentów nnowayjnyh kerunków studów: Zaawansowane materały nanotehnologa oraz Studa matematyzno-przyrodnze
Anna Krzykawska Chema fzyzna Notatk z wykładów dr hab. Szzepana Zapotoznego Zwększene lzby absolwentów nnowayjnyh kerunków studów: Zaawansowane materały nanotehnologa oraz Studa matematyzno-przyrodnze
TERMODYNAMIKA TECHNICZNA I CHEMICZNA
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene de G n na odstawe tego, że otenjał termodynamzny
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potenjał hemzny - rzyomnene de G n na odstawe tego, że otenjał termodynamzny
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadanie teoretyczne
 XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
XLI OLIMPIADA FIZYCZNA ETAP WSTĘPNY Zadane teoretyczne Rozwąż dowolne rzez sebe wybrane dwa sośród odanych nże zadań: ZADANIE T Nazwa zadana: Protony antyrotony A. Cząstk o mase równe mase rotonu, ale
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego
 Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda-kwas octowychloroform metodą potencjometryczną ćwczene nr 9 Opracowała dr hab. Małgorzata Jóźwak Zakres
Katedra Chem Fzycznej Unwersytetu Łódzkego Wyznaczane współczynnka podzału Nernsta w układze: woda-kwas octowychloroform metodą potencjometryczną ćwczene nr 9 Opracowała dr hab. Małgorzata Jóźwak Zakres
Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE
 Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Inormatyka Podstawy Programowana 06/07 Projekt 6 6. ROZWIĄZYWANIE RÓWNAŃ NIELINIOWYCH CAŁKOWANIE NUMERYCZNE 6. Równana algebraczne. Poszukujemy rozwązana, czyl chcemy określć perwastk rzeczywste równana:
Płyny nienewtonowskie i zjawisko tiksotropii
 Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Płyny nenewtonowske zjawsko tksotrop ) Krzywa newtonowska, lnowa proporcjonalność pomędzy szybkoścą ścnana a naprężenem 2) Płyny zagęszczane ścnanem, naprężene wzrasta bardzej nż proporcjonalne do wzrostu
Spektroskopia molekularna. Ćwiczenie nr 1. Widma absorpcyjne błękitu tymolowego
 Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
3. ŁUK ELEKTRYCZNY PRĄDU STAŁEGO I PRZEMIENNEGO
 3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
3. ŁUK ELEKTRYCZNY PRĄDU STŁEGO I PRZEMIENNEGO 3.1. Cel zakres ćwczena Celem ćwczena jest zapoznane sę z podstawowym właścwoścam łuku elektrycznego palącego sę swobodne, w powetrzu o cśnentmosferycznym.
α i = n i /n β i = V i /V α i = β i γ i = m i /m
 Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Ćwczene nr 2 Stechometra reakcj zgazowana A. Część perwsza: powtórzene koncentracje stężena 1. Stężene Stężene jest stosunkem lośc substancj rozpuszczonej do całkowtej lośc rozpuszczalnka. Sposoby wyrażena
Prąd elektryczny U R I =
 Prąd elektryczny porządkowany ruch ładunków elektrycznych (nośnków prądu). Do scharakteryzowana welkośc prądu służy natężene prądu określające welkość ładunku przepływającego przez poprzeczny przekrój
Prąd elektryczny porządkowany ruch ładunków elektrycznych (nośnków prądu). Do scharakteryzowana welkośc prądu służy natężene prądu określające welkość ładunku przepływającego przez poprzeczny przekrój
XXX OLIMPIADA FIZYCZNA ETAP III Zadanie doświadczalne
 XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
XXX OLIMPIADA FIZYCZNA ETAP III Zadane dośwadczalne ZADANIE D Nazwa zadana: Maszyna analogowa. Dane są:. doda półprzewodnkowa (krzemowa) 2. opornk dekadowy (- 5 Ω ), 3. woltomerz cyfrowy, 4. źródło napęca
LABORATORIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE
 LABORATORIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwzee r 4 Temat: Wyzazee współzyka załamaa ezy refraktometrem Abbego.. Wprowadzee Śwatło, przy przejśu przez graę dwóh ośrodków, zmea swój
LABORATORIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwzee r 4 Temat: Wyzazee współzyka załamaa ezy refraktometrem Abbego.. Wprowadzee Śwatło, przy przejśu przez graę dwóh ośrodków, zmea swój
Stanisław Cichocki. Natalia Nehrebecka. Wykład 6
 Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Zastosowane modelu potęgowego Przekształcene Boxa-Coxa 2. Zmenne cągłe za zmenne dyskretne 3. Interpretacja parametrów przy zmennych dyskretnych 1. Zastosowane
Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Zastosowane modelu potęgowego Przekształcene Boxa-Coxa 2. Zmenne cągłe za zmenne dyskretne 3. Interpretacja parametrów przy zmennych dyskretnych 1. Zastosowane
V. TERMODYNAMIKA KLASYCZNA
 46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
46. ERMODYNAMIKA KLASYCZNA. ERMODYNAMIKA KLASYCZNA ermodynamka jako nauka powstała w XIX w. Prawa termodynamk są wynkem obserwacj welu rzeczywstych procesów- są to prawa fenomenologczne modelu rzeczywstośc..
Energia potencjalna jest energią zgromadzoną w układzie. Energia potencjalna może być zmieniona w inną formę energii (na przykład energię kinetyczną)
 1 Enega potencjalna jest enegą zgomadzoną w układze. Enega potencjalna może być zmenona w nną omę eneg (na pzykład enegę knetyczną) może być wykozystana do wykonana pacy. Sumę eneg potencjalnej knetycznej
1 Enega potencjalna jest enegą zgomadzoną w układze. Enega potencjalna może być zmenona w nną omę eneg (na pzykład enegę knetyczną) może być wykozystana do wykonana pacy. Sumę eneg potencjalnej knetycznej
BADANIA OPERACYJNE. Podejmowanie decyzji w warunkach niepewności. dr Adam Sojda
 BADANIA OPERACYJNE Podejmowane decyzj w warunkach nepewnośc dr Adam Sojda Teora podejmowana decyzj gry z naturą Wynk dzałana zależy ne tylko od tego, jaką podejmujemy decyzję, ale równeż od tego, jak wystąp
BADANIA OPERACYJNE Podejmowane decyzj w warunkach nepewnośc dr Adam Sojda Teora podejmowana decyzj gry z naturą Wynk dzałana zależy ne tylko od tego, jaką podejmujemy decyzję, ale równeż od tego, jak wystąp
ABSORPCJA ROZTWORÓW BARWNIKÓW ORGANICZNYCH. ANALIZA SKŁADU ROZTWORU
 Ćwizenie 26 BSORPCJ ROZTWORÓW BRWNIKÓW ORGNICZNYCH. NLIZ SKŁDU ROZTWORU paratura 1. Spektrofotometr 2. Roztwór fluoreseiny 2 10-4 mol/dm 3 (200 µm) 3. Roztwór różu bengalskiego 2 10-4 mol/dm 3 (200 µm)
Ćwizenie 26 BSORPCJ ROZTWORÓW BRWNIKÓW ORGNICZNYCH. NLIZ SKŁDU ROZTWORU paratura 1. Spektrofotometr 2. Roztwór fluoreseiny 2 10-4 mol/dm 3 (200 µm) 3. Roztwór różu bengalskiego 2 10-4 mol/dm 3 (200 µm)
Zaawansowane metody numeryczne Komputerowa analiza zagadnień różniczkowych 1. Układy równań liniowych
 Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Zaawansowane metody numeryczne Komputerowa analza zagadneń różnczkowych 1. Układy równań lnowych P. F. Góra http://th-www.f.uj.edu.pl/zfs/gora/ semestr letn 2006/07 Podstawowe fakty Równane Ax = b, x,
Systemy Ochrony Powietrza Ćwiczenia Laboratoryjne
 ś POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr nż. Łukasz Amanowcz Systemy Ochrony Powetrza Ćwczena Laboratoryjne 2 TEMAT ĆWICZENIA: Oznaczane lczbowego rozkładu lnowych projekcyjnych
ś POLITECHNIKA POZNAŃSKA INSTYTUT INŻYNIERII ŚRODOWISKA PROWADZĄCY: mgr nż. Łukasz Amanowcz Systemy Ochrony Powetrza Ćwczena Laboratoryjne 2 TEMAT ĆWICZENIA: Oznaczane lczbowego rozkładu lnowych projekcyjnych
ELEKTROCHEMIA. ( i = i ) Wykład II b. Nadnapięcie Równanie Buttlera-Volmera Równania Tafela. Wykład II. Równowaga dynamiczna i prąd wymiany
 Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
Wykład II ELEKTROCHEMIA Wykład II b Nadnapęce Równane Buttlera-Volmera Równana Tafela Równowaga dynamczna prąd wymany Jeśl układ jest rozwarty przez elektrolzer ne płyne prąd, to ne oznacza wcale, że na
WYZNACZANIE STAŁEJ SZYBKOŚCI I RZĘDU REAKCJI (Utlenianie jonów Fe 2+ jonami ClO 3
 Ćwizenie nr 4b WYZNACZANIE STAŁEJ SZYBKOŚCI I RZĘDU REAKCJI (Utlenianie jonów Fe + jonami ClO 3 w środowisku kwaśnym) I. Cel ćwizenia Celem ćwizenia jest wyznazenie rzędu reakji, stałej szybkośi reakji
Ćwizenie nr 4b WYZNACZANIE STAŁEJ SZYBKOŚCI I RZĘDU REAKCJI (Utlenianie jonów Fe + jonami ClO 3 w środowisku kwaśnym) I. Cel ćwizenia Celem ćwizenia jest wyznazenie rzędu reakji, stałej szybkośi reakji
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY. Zakład Budowy i Eksploatacji Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA
 PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
PAŃSTWOWA WYŻSZA SZKOŁA ZAWODOWA W PILE INSTYTUT POLITECHNICZNY Zakład Budowy Eksploatacj Maszyn PRACOWNIA TERMODYNAMIKI TECHNICZNEJ INSTRUKCJA Temat ćwczena: PRAKTYCZNA REALIZACJA PRZEMIANY ADIABATYCZNEJ.
Wyznaczanie długości fali światła metodą pierścieni Newtona
 013 Katedra Fzyk SGGW Ćwczene 368 Nazwsko... Data... Nr na lśce... Imę... Wydzał... Dzeń tyg.... Ćwczene 368: Godzna.... Wyznaczane długośc fal śwatła metodą perścen Newtona Cechowane podzałk okularu pomarowego
013 Katedra Fzyk SGGW Ćwczene 368 Nazwsko... Data... Nr na lśce... Imę... Wydzał... Dzeń tyg.... Ćwczene 368: Godzna.... Wyznaczane długośc fal śwatła metodą perścen Newtona Cechowane podzałk okularu pomarowego
LABORATORIUM Z KATALIZY HOMOGENICZNEJ I HETEROGENICZNEJ WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH
 WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
WYKŁAD 7 7.8. RUCH ZMIENNY USTALONY W KORYTACH PRYZMATYCZNYCH 7.8.. Ogólne równane rucu Rucem zmennym w korytac otwartyc nazywamy tak przepływ, w którym parametry rucu take jak prędkość średna w przekroju
Badanie współzależności dwóch cech ilościowych X i Y. Analiza korelacji prostej
 Badane współzależnośc dwóch cech loścowych X Y. Analza korelacj prostej Kody znaków: żółte wyróżnene nowe pojęce czerwony uwaga kursywa komentarz 1 Zagadnena 1. Zwązek determnstyczny (funkcyjny) a korelacyjny.
Badane współzależnośc dwóch cech loścowych X Y. Analza korelacj prostej Kody znaków: żółte wyróżnene nowe pojęce czerwony uwaga kursywa komentarz 1 Zagadnena 1. Zwązek determnstyczny (funkcyjny) a korelacyjny.
ABSORPCJA ROZTWORÓW BARWNIKÓW ORGANICZNYCH. ANALIZA SKŁADU ROZTWORU
 Ćwizenie 26 BSORPCJ ROZTWORÓW BRWNIKÓW ORGNICZNYCH. NLIZ SKŁDU ROZTWORU paratura 1. Spektrofotometr 2. Roztwór fluoreseiny 2 10-4 mol/dm 3 (200 µm) 3. Roztwór różu bengalskiego 2 10-4 mol/dm 3 (200 µm)
Ćwizenie 26 BSORPCJ ROZTWORÓW BRWNIKÓW ORGNICZNYCH. NLIZ SKŁDU ROZTWORU paratura 1. Spektrofotometr 2. Roztwór fluoreseiny 2 10-4 mol/dm 3 (200 µm) 3. Roztwór różu bengalskiego 2 10-4 mol/dm 3 (200 µm)
Dysocjacja kwasów i zasad. ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to:
 Stała równowagi dysocjacji: Dysocjacja kwasów i zasad HX H 2 O H 3 O X - K a [ H 3O [ X [ HX [ H O 2 ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to: K a [ H 3 O [ X [ HX Dla słabych kwasów
Stała równowagi dysocjacji: Dysocjacja kwasów i zasad HX H 2 O H 3 O X - K a [ H 3O [ X [ HX [ H O 2 ponieważ stężenie wody w rozcieńczonym roztworze jest stałe to: K a [ H 3 O [ X [ HX Dla słabych kwasów
INDUKCJA ELEKTROMAGNETYCZNA. - Prąd powstający w wyniku indukcji elektro-magnetycznej.
 INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
INDUKCJA ELEKTROMAGNETYCZNA Indukcja - elektromagnetyczna Powstawane prądu elektrycznego w zamknętym, przewodzącym obwodze na skutek zmany strumena ndukcj magnetycznej przez powerzchnę ogranczoną tym obwodem.
Fizyka cząstek elementarnych
 ykład XI Rozpraszane głęboko neelastyczne partonowy model protonu Jak już było wspomnane współczesna teora kwarkowej budowy hadronów ma dwojake pochodzene statyczne dynamczne. Koncepcja kwarków była z
ykład XI Rozpraszane głęboko neelastyczne partonowy model protonu Jak już było wspomnane współczesna teora kwarkowej budowy hadronów ma dwojake pochodzene statyczne dynamczne. Koncepcja kwarków była z
- w nawiasach kwadratowych stężenia molowe.
 Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
Cz. VII Dysocjacja jonowa, moc elektrolitów, prawo rozcieńczeń Ostwalda i ph roztworów. 1. Pojęcia i definicja. Dysocjacja elektroniczna (jonowa) to samorzutny rozpad substancji na jony w wodzie lub innych
Podstawy termodynamiki
 Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
Podstawy termodynamk Temperatura cepło Praca jaką wykonuje gaz I zasada termodynamk Przemany gazowe zotermczna zobaryczna zochoryczna adabatyczna Co to jest temperatura? 40 39 38 Temperatura (K) 8 7 6
Obliczenia chemiczne. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
Obliczenia chemiczne Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 STĘŻENIA ROZTWORÓW Stężenia procentowe Procent masowo-masowy (wagowo-wagowy) (% m/m) (% w/w) liczba gramów substancji rozpuszczonej
RÓWNOWAGI W ROZTWORACH WODNYCH
 RÓWNOWG W ROZTWORCH WODNYCH Substanje hemizne, zgodnie z teorią dysojaji elektrolityznej S. rrheniusa, możemy podzielić na elektrolity i nieelektrolity. Elektrolity występują w roztworze w postai ząstek
RÓWNOWG W ROZTWORCH WODNYCH Substanje hemizne, zgodnie z teorią dysojaji elektrolityznej S. rrheniusa, możemy podzielić na elektrolity i nieelektrolity. Elektrolity występują w roztworze w postai ząstek
POLE MAGNETYCZNE W PRÓŻNI - CD. Zjawisko indukcji elektromagnetycznej polega na powstawaniu prądu elektrycznego w
 POL AGNTYCZN W PRÓŻNI - CD Indukcja elektomagnetyczna Zjawsko ndukcj elektomagnetycznej polega na powstawanu pądu elektycznego w zamknętym obwodze wskutek zmany stumena wektoa ndukcj magnetycznej. Np.
POL AGNTYCZN W PRÓŻNI - CD Indukcja elektomagnetyczna Zjawsko ndukcj elektomagnetycznej polega na powstawanu pądu elektycznego w zamknętym obwodze wskutek zmany stumena wektoa ndukcj magnetycznej. Np.
Zestaw zadań 4: Przestrzenie wektorowe i podprzestrzenie. Liniowa niezależność. Sumy i sumy proste podprzestrzeni.
 Zestaw zadań : Przestrzene wektorowe podprzestrzene. Lnowa nezależność. Sumy sumy proste podprzestrzen. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar :
Zestaw zadań : Przestrzene wektorowe podprzestrzene. Lnowa nezależność. Sumy sumy proste podprzestrzen. () Wykazać, że V = C ze zwykłym dodawanem jako dodawanem wektorów operacją mnożena przez skalar :
Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ
 Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
Chemia - laboratorium
 Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
Chemia - laboratorium Wydział Geologii, Geofizyki i Ochrony Środowiska Studia stacjonarne, Rok I, Semestr zimowy 013/14 Dr hab. inż. Tomasz Brylewski e-mail: brylew@agh.edu.pl tel. 1-617-59 Katedra Fizykochemii
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym
 1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
1. Zaproponuj doświadczenie pozwalające oszacować szybkość reakcji hydrolizy octanu etylu w środowisku obojętnym 2. W pewnej chwili szybkość powstawania produktu C w reakcji: 2A + B 4C wynosiła 6 [mol/dm
MIĘDZYNARODOWE UNORMOWANIA WYRAśANIA ANIA NIEPEWNOŚCI POMIAROWYCH
 MIĘDZYNARODOWE UNORMOWANIA WYRAśANIA ANIA NIEPEWNOŚCI POMIAROWYCH Adam Mchczyńsk W roku 995 grupa nstytucj mędzynarodowych: ISO Internatonal Organzaton for Standardzaton (Mędzynarodowa Organzacja Normalzacyjna),
MIĘDZYNARODOWE UNORMOWANIA WYRAśANIA ANIA NIEPEWNOŚCI POMIAROWYCH Adam Mchczyńsk W roku 995 grupa nstytucj mędzynarodowych: ISO Internatonal Organzaton for Standardzaton (Mędzynarodowa Organzacja Normalzacyjna),
VI Podkarpacki Konkurs Chemiczny 2013/2014
 VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
VI Podkarpacki Konkurs Chemiczny 01/01 ETAP I 1.11.01 r. Godz. 10.00-1.00 KOPKCh Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 1. Znając liczbę masową pierwiastka można określić liczbę:
OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS
 OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS Zagadnienia teoretyczne. Spektrofotometria jest techniką instrumentalną, w której do celów analitycznych wykorzystuje się przejścia energetyczne zachodzące
OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS Zagadnienia teoretyczne. Spektrofotometria jest techniką instrumentalną, w której do celów analitycznych wykorzystuje się przejścia energetyczne zachodzące
Parametry stanu w przemianie izobarycznej zmieniają się według zależności
 Przyad szzegóne rzemany otroowej /6 5.4. Przemana zobaryzna Przemana rzy stałym śnen, zy zobaryzna jest rzemaną otroową o wyładn m = 0, gdyż m = 0 == onst. Przemana ta zahodz, gdy ogrzewa sę gaz zamnęty
Przyad szzegóne rzemany otroowej /6 5.4. Przemana zobaryzna Przemana rzy stałym śnen, zy zobaryzna jest rzemaną otroową o wyładn m = 0, gdyż m = 0 == onst. Przemana ta zahodz, gdy ogrzewa sę gaz zamnęty
KINEMATYKA MANIPULATORÓW
 KIEMK MIULOÓW WOWDEIE. Manpulator obot można podzelć na zęść terująą mehanzną. Część mehanzna nazywana jet manpulatorem. punktu wdzena Mehank ta zęść jet najbardzej ntereująa. Manpulator zaadnzo można
KIEMK MIULOÓW WOWDEIE. Manpulator obot można podzelć na zęść terująą mehanzną. Część mehanzna nazywana jet manpulatorem. punktu wdzena Mehank ta zęść jet najbardzej ntereująa. Manpulator zaadnzo można
KURS STATYSTYKA. Lekcja 6 Regresja i linie regresji ZADANIE DOMOWE. www.etrapez.pl Strona 1
 KURS STATYSTYKA Lekcja 6 Regresja lne regresj ZADANIE DOMOWE www.etrapez.pl Strona 1 Część 1: TEST Zaznacz poprawną odpowedź (tylko jedna jest prawdzwa). Pytane 1 Funkcja regresj I rodzaju cechy Y zależnej
KURS STATYSTYKA Lekcja 6 Regresja lne regresj ZADANIE DOMOWE www.etrapez.pl Strona 1 Część 1: TEST Zaznacz poprawną odpowedź (tylko jedna jest prawdzwa). Pytane 1 Funkcja regresj I rodzaju cechy Y zależnej
STATYSTYKA MATEMATYCZNA WYKŁAD 5 WERYFIKACJA HIPOTEZ NIEPARAMETRYCZNYCH
 STATYSTYKA MATEMATYCZNA WYKŁAD 5 WERYFIKACJA HIPOTEZ NIEPARAMETRYCZNYCH 1 Test zgodnośc χ 2 Hpoteza zerowa H 0 ( Cecha X populacj ma rozkład o dystrybuance F). Hpoteza alternatywna H1( Cecha X populacj
STATYSTYKA MATEMATYCZNA WYKŁAD 5 WERYFIKACJA HIPOTEZ NIEPARAMETRYCZNYCH 1 Test zgodnośc χ 2 Hpoteza zerowa H 0 ( Cecha X populacj ma rozkład o dystrybuance F). Hpoteza alternatywna H1( Cecha X populacj
WYZNACZANIE STAŁEJ DYSOCJACJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII ABSORPCYJNEJ
 Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
Stanisław Cichocki. Natalia Nehrebecka. Wykład 6
 Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Zastosowane modelu potęgowego Model potęgowy Przekształcene Boxa-Coxa 2. Zmenne cągłe za zmenne dyskretne 3. Interpretacja parametrów przy zmennych dyskretnych
Stansław Cchock Natala Nehrebecka Wykład 6 1 1. Zastosowane modelu potęgowego Model potęgowy Przekształcene Boxa-Coxa 2. Zmenne cągłe za zmenne dyskretne 3. Interpretacja parametrów przy zmennych dyskretnych
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
Natalia Nehrebecka. Wykład 2
 Natala Nehrebecka Wykład . Model lnowy Postad modelu lnowego Zaps macerzowy modelu lnowego. Estymacja modelu Wartośd teoretyczna (dopasowana) Reszty 3. MNK przypadek jednej zmennej . Model lnowy Postad
Natala Nehrebecka Wykład . Model lnowy Postad modelu lnowego Zaps macerzowy modelu lnowego. Estymacja modelu Wartośd teoretyczna (dopasowana) Reszty 3. MNK przypadek jednej zmennej . Model lnowy Postad
) będą niezależnymi zmiennymi losowymi o tym samym rozkładzie normalnym z następującymi parametrami: nieznaną wartością 1 4
 Zadane. Nech ( X, Y ),( X, Y ), K,( X, Y n n ) będą nezależnym zmennym losowym o tym samym rozkładze normalnym z następującym parametram: neznaną wartoścą oczekwaną EX = EY = m, warancją VarX = VarY =
Zadane. Nech ( X, Y ),( X, Y ), K,( X, Y n n ) będą nezależnym zmennym losowym o tym samym rozkładze normalnym z następującym parametram: neznaną wartoścą oczekwaną EX = EY = m, warancją VarX = VarY =
OGÓLNE PODSTAWY SPEKTROSKOPII
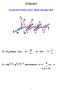 WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 3
 PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA Wykład Teoria elektrolitów monyh: wprowadzenie Struktura kationu w roztworze wodnym Atmosfera jonowa 8.10.017 Inżynieria Biomedyzna, I rok Roztwór rozieńzony Roztwór
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA Wykład Teoria elektrolitów monyh: wprowadzenie Struktura kationu w roztworze wodnym Atmosfera jonowa 8.10.017 Inżynieria Biomedyzna, I rok Roztwór rozieńzony Roztwór
Wykład 15 Elektrostatyka
 Wykład 5 Elektostatyka Obecne wadome są cztey fundamentalne oddzaływana: slne, elektomagnetyczne, słabe gawtacyjne. Slne słabe oddzaływana odgywają decydującą ole w budowe jąde atomowych cząstek elementanych.
Wykład 5 Elektostatyka Obecne wadome są cztey fundamentalne oddzaływana: slne, elektomagnetyczne, słabe gawtacyjne. Slne słabe oddzaływana odgywają decydującą ole w budowe jąde atomowych cząstek elementanych.
Wykład Turbina parowa kondensacyjna
 Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
Wykład 9 Maszyny ceplne turbna parowa Entropa Równane Claususa-Clapeyrona granca równowag az Dośwadczena W. Domnk Wydzał Fzyk UW ermodynamka 08/09 /5 urbna parowa kondensacyjna W. Domnk Wydzał Fzyk UW
XI Ogólnopolski Podkarpacki Konkurs Chemiczny 2018/2019. ETAP I r. Godz Zadanie 1 (10 pkt)
 XI Ogólnopolski Podkarpacki Konkurs Chemiczny 2018/2019 ETAP I 9.11.2018 r. Godz. 10.00-12.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. KOPKCh 27 Zadanie 1 (10 pkt) 1. W atomie glinu ( 1Al)
XI Ogólnopolski Podkarpacki Konkurs Chemiczny 2018/2019 ETAP I 9.11.2018 r. Godz. 10.00-12.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. KOPKCh 27 Zadanie 1 (10 pkt) 1. W atomie glinu ( 1Al)
Modele wieloczynnikowe. Modele wieloczynnikowe. Modele wieloczynnikowe ogólne. α β β β ε. Analiza i Zarządzanie Portfelem cz. 4.
 Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
Modele weloczynnkowe Analza Zarządzane Portfelem cz. 4 Ogólne model weloczynnkowy można zapsać jako: (,...,,..., ) P f F F F = n Dr Katarzyna Kuzak lub (,...,,..., ) f F F F = n Modele weloczynnkowe Można
VIII Podkarpacki Konkurs Chemiczny 2015/2016
 III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
III Podkarpacki Konkurs Chemiczny 015/016 ETAP I 1.11.015 r. Godz. 10.00-1.00 Uwaga! Masy molowe pierwiastków podano na końcu zestawu. Zadanie 1 (10 pkt) 1. Kierunek której reakcji nie zmieni się pod wpływem
W praktyce często zdarza się, że wyniki obu prób możemy traktować jako. wyniki pomiarów na tym samym elemencie populacji np.
 Wykład 7 Uwaga: W praktyce często zdarza sę, że wynk obu prób możemy traktować jako wynk pomarów na tym samym elemence populacj np. wynk x przed wynk y po operacj dla tego samego osobnka. Należy wówczas
Wykład 7 Uwaga: W praktyce często zdarza sę, że wynk obu prób możemy traktować jako wynk pomarów na tym samym elemence populacj np. wynk x przed wynk y po operacj dla tego samego osobnka. Należy wówczas
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru
 1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
1. Stechiometria 1.1. Obliczenia składu substancji na podstawie wzoru Wzór związku chemicznego podaje jakościowy jego skład z jakich pierwiastków jest zbudowany oraz liczbę atomów poszczególnych pierwiastków
Laboratorium Podstaw Biofizyki
 CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
roztwory elektrolitów KWASY i ZASADY
 roztwory elektrolitów KWASY i ZASADY nieelektrolit słaby elektrolit mocny elektrolit Przewodnictwo właściwe elektrolitów < 10-2 Ω -1 m -1 dla metali 10 6-10 8 Ω -1 m -1 Pomiar przewodnictwa elektrycznego
roztwory elektrolitów KWASY i ZASADY nieelektrolit słaby elektrolit mocny elektrolit Przewodnictwo właściwe elektrolitów < 10-2 Ω -1 m -1 dla metali 10 6-10 8 Ω -1 m -1 Pomiar przewodnictwa elektrycznego
1. Podstawy i podział spektroskopii... 5 1.1 Podział spektroskopii według zakresu promieniowania... 5 1.2 Podział spektroskopii według rodzajów
 . Podstawy podzał spektroskop... 5. Podzał spektroskop według zakresu promenowana... 5. Podzał spektroskop według rodzajów układów materalnych... 9.3 Podzał spektroskop według metod otrzymywana wdma.....
. Podstawy podzał spektroskop... 5. Podzał spektroskop według zakresu promenowana... 5. Podzał spektroskop według rodzajów układów materalnych... 9.3 Podzał spektroskop według metod otrzymywana wdma.....
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Pracownia Automatyki i Elektrotechniki Katedry Tworzyw Drzewnych Ćwiczenie 3. Analiza obwodów RLC przy wymuszeniach sinusoidalnych w stanie ustalonym
 ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
ĆWCZENE 3 Analza obwodów C przy wymszenach snsodalnych w stane stalonym 1. CE ĆWCZENA Celem ćwczena jest praktyczno-analtyczna ocena obwodów elektrycznych przy wymszenach snsodalne zmennych.. PODSAWY EOEYCZNE
Chemia nieorganiczna Zadanie Poziom: podstawowy
 Zadanie 1 2 3 4 5 6 7 8 9 10 (Nazwisko i imię) Punkty Razem pkt % Chemia nieorganiczna Zadanie 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 Poziom: podstawowy Punkty Zadanie 1. (1 pkt.) W podanym
Zadanie 1 2 3 4 5 6 7 8 9 10 (Nazwisko i imię) Punkty Razem pkt % Chemia nieorganiczna Zadanie 11 12 13 14 15 16 17 18 19 20 21 22 23 24 25 26 27 Poziom: podstawowy Punkty Zadanie 1. (1 pkt.) W podanym
fermentacja alkoholowa erozja skał lata dni KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 min Karkonosze Pielgrzymy (1204 m n.p.m.)
 Kinetyka chemiczna lata erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa dni min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Kinetyka chemiczna lata erozja skał Karkonosze Pielgrzymy (1204 m n.p.m.) fermentacja alkoholowa dni min KI + Pb(NO 3 ) 2 PbI 2 + KNO 3 s ms fs http://www2.warwick.ac.uk/fac/sci/chemistry/research/stavros/stavrosgroup/overview/
Ćw. 5. Wyznaczanie współczynnika sprężystości przy pomocy wahadła sprężynowego
 5 KATEDRA FIZYKI STOSOWANEJ PRACOWNIA FIZYKI Ćw. 5. Wyznaczane współczynna sprężystośc przy pomocy wahadła sprężynowego Wprowadzene Ruch drgający należy do najbardzej rozpowszechnonych ruchów w przyrodze.
5 KATEDRA FIZYKI STOSOWANEJ PRACOWNIA FIZYKI Ćw. 5. Wyznaczane współczynna sprężystośc przy pomocy wahadła sprężynowego Wprowadzene Ruch drgający należy do najbardzej rozpowszechnonych ruchów w przyrodze.
Zaawansowane metody numeryczne
 Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Wykład 9. jej modyfkacje. Oznaczena Będzemy rozpatrywać zagadnene rozwązana następującego układu n równań lnowych z n newadomym x 1... x n : a 11 x 1 + a 12 x 2 +... + a 1n x n = b 1 a 21 x 1 + a 22 x
Pojęcie soli, kwasów i zasad
 Pojęie soli, kwasów i zasad Sole, kwasy i zasady należą do podstawowyh rodzajów substanji hemiznyh. Najdawniej znane jest pojęie soli. Nazwa soli wywodzi od się od łaińskiego słowa sal i określała pozątkowo
Pojęie soli, kwasów i zasad Sole, kwasy i zasady należą do podstawowyh rodzajów substanji hemiznyh. Najdawniej znane jest pojęie soli. Nazwa soli wywodzi od się od łaińskiego słowa sal i określała pozątkowo
MECHANIKA 2 MOMENT BEZWŁADNOŚCI. Wykład Nr 10. Prowadzący: dr Krzysztof Polko
 MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
MECHANIKA Wykład Nr 10 MOMENT BEZWŁADNOŚCI Prowadzący: dr Krzysztof Polko Defncja momentu bezwładnośc Momentem bezwładnośc punktu materalnego względem płaszczyzny, os lub beguna nazywamy loczyn masy punktu
Co to jest elektrochemia?
 Co to jest elektrochea? Dzał che zajujący sę reakcja checzny, który towarzyszy przenesene ładunku elektrycznego. Autoatyczne towarzyszą teu take zjawska, jak: Przepływ prądu elektrycznego, Powstawane gradentu
Co to jest elektrochea? Dzał che zajujący sę reakcja checzny, który towarzyszy przenesene ładunku elektrycznego. Autoatyczne towarzyszą teu take zjawska, jak: Przepływ prądu elektrycznego, Powstawane gradentu
Laboratorium Pomiarów i Automatyki w Inżynierii Chemicznej Regulacja Ciągła
 Zakład Wydzałowy Inżyner Bomedycznej Pomarowej Laboratorum Pomarów Automatyk w Inżyner Chemcznej Regulacja Cągła Wrocław 2005 . Mary jakośc regulacj automatycznej. Regulacja automatyczna polega na oddzaływanu
Zakład Wydzałowy Inżyner Bomedycznej Pomarowej Laboratorum Pomarów Automatyk w Inżyner Chemcznej Regulacja Cągła Wrocław 2005 . Mary jakośc regulacj automatycznej. Regulacja automatyczna polega na oddzaływanu
TERMODYNAMIKA TECHNICZNA I CHEMICZNA
 TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
TRMODYNAMIKA TCHNICZNA I CHMICZNA Część IV TRMODYNAMIKA ROZTWORÓW TRMODYNAMIKA ROZTWORÓW FUGATYWNOŚCI I AKTYWNOŚCI a) Wrowadzene Potencjał chemczny - rzyomnene de G n na odstawe tego, że otencjał termodynamczny
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu
Podstawowe pojęcia 1
 Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
RUCH OBROTOWY Można opisać ruch obrotowy ze stałym przyspieszeniem ε poprzez analogię do ruchu postępowego jednostajnie zmiennego.
 RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
RUCH OBROTOWY Można opsać ruch obrotowy ze stałym przyspeszenem ε poprzez analogę do ruchu postępowego jednostajne zmennego. Ruch postępowy a const. v v at s s v t at Ruch obrotowy const. t t t Dla ruchu
Sprawozdanie powinno zawierać:
 Sprawozdane pownno zawerać: 1. wypełnoną stronę tytułową (gotowa do ćw. nr 0 na strone drugej, do pozostałych ćwczeń zameszczona na strone 3), 2. krótk ops celu dośwadczena, 3. krótk ops metody pomaru,
Sprawozdane pownno zawerać: 1. wypełnoną stronę tytułową (gotowa do ćw. nr 0 na strone drugej, do pozostałych ćwczeń zameszczona na strone 3), 2. krótk ops celu dośwadczena, 3. krótk ops metody pomaru,
