Orientacyjny plan zajęć (semestr VI)
|
|
|
- Wacław Karpiński
- 8 lat temu
- Przeglądów:
Transkrypt
1 Orientacyjny plan zajęć (semestr VI) 1. Wprowadzenie 2. Wiadomości wstępne Struktura, defekty, wiązania a właściwości; Podstawy termodynamiczne; Dyfuzja; Reakcje w fazie stałej. Orientacyjny plan zajęć (semestr VI) 3. Wybrane materiały funkcjonalne i technologie stosowane w elektronice i elektrotechnice: Materiały elektroniczne i elektrotechniczne: metale; Materiały elektroniczne i elektrotechniczne: półprzewodniki; Wytwarzanie monokryształów; Cienkie warstwy; Litografia, trawienie i inne technologie półprzewodnikowe; Układ scalony, połączenia między różnymi materiałami;
2 Orientacyjny plan zajęć (semestr VI) 4. Inne materiały funkcjonalne Szkło i aerożele; Nadprzewodniki; Kompozyty; Materiały twarde; Orientacyjny plan zajęć (semestr IX) 1. Materiały ceramiczne Izolatory; Przewodniki jonów; Materiały magnetyczne; Ceramiki o szczególnych właściwościach mechanicznych; 2. Materiały a energia Magazynowanie i oszczędzanie energii Ogniwa fotowoltaiczne; Diody elektroluminescencyjne i lasery; Ogniwa paliwowe; 3. Materiały naturalne
3 Świat materiałów Metale Ceramika, szkło Kompozyty Polimery, elastomery Pianki Materiały naturalne Unit 1, Frame 1.4 Znaczenie różnych materiałów
4 Funkcja materiału... SKŁAD, STRUKTURA, WIĄZANIA PROCESY TECHNOLO- GICZNE FUNKCJA WŁAŚCI- WOŚCI I KSZTAŁT Na czym polega wybór odpowiedniego materiału? PROJEKTOWANIE
5 Projektowanie Stworzyć produkt efektywnie i bezpiecznie spełniający swoją funkcję przy rozsądnych kosztach Gromadzenie danych analiza statystycz na Wybór materiałów i procesów Analiza Ekonomiczna Mechanical Properties Bulk Modulus GPa Compressive MPa Strength Ductility Elastic Limit MPa Endurance Limit MPa Fracture Toughness MPa.m 1/2 Hardness MPa Loss Coefficient Modulus of Rupture MPa Poisson's Ratio Shear Modulus GPa Tensile Strength MPa Young's Modulus GPa $ Test Wyniki testu Wszystkie dane Potencjalne zastosowania Produkt końcowy Badania Wybór i wdrożenie Przykład: ABS Acrylonitrile-butadiene-styrene (ABS) - (CH 2 -CH-C 6 H 4 ) n Ogólne: gęstość g/cm 3 cena około 8 zł/kg Własności mechaniczne: Moduł Younga GPa Granica sprężystości MPa Wytrzymałość MPa Wydłużenie 6-8 % Twardość - Vickers 6-15 HV Odporność na uderzenia duża
6 Przykład: ABS Acrylonitrile-butadiene-styrene (ABS) - (CH 2 -CH-C 6 H 4 ) n Własności termiczne Maksymalna temperatura pracy K Rozszerzalność termiczna x10-6 1/K Ciepło właściwe J/kg.K Przewodność cieplna W/m.K Własności elektryczne Dobry izolator Własności optyczne Nieprzezroczysty Przykład: ABS Acrylonitrile-butadiene-styrene (ABS) - (CH 2 -CH-C 6 H 4 ) n Procesy technologiczne ABS może być wyciągane, kształtowane w formach pod ciśnieniem lub wytwarzane w postaci arkuszy, które są później ostatecznie formowane w próżni w podwyższonej temperaturze. Fragmenty można ze sobą łączyć za pomocą ultradźwięków, zgrzewania, lub można je sklejać żywicami poliestrowymi, epoksydowymi itd.
7 Przykład: ABS Acrylonitrile-butadiene-styrene (ABS) - (CH 2 -CH-C 6 H 4 ) n Mając to wszystko na uwadze: Z ABS wytwarza się: kaski, rury hydrauliczne, wewnętrzne części wyposażenia samochodów, pokłady łodzi, walizki, tace,obudowy komputerów, zabawki,.. 1. Wiadomości wstępne 1. Wiązania chemiczne. 2. Struktura krystaliczna. 3. Defekty strukturalne. 4. Co z tego wszystkiego wynika: niektóre właściwości fizyczne i chemiczne.
8 Pierwotnym źródłem wszelkich właściwości materiału a zatem i potencjalnych funkcji pełnionych przez materiał są wiązania chemiczne, a zatem konfiguracjia elektronowa składników materiału. Wiązania: uwagi ogólne F A F R r F = F + F N A R 1. Gdzie F N : Wypadkowa siła działająca między atomami 2. F A : Siła przyciągająca 3. F R : Siła odpychająca
9 Obliczanie energii wiązania: 1. Zależność między siłą i energią: de 2. Gdy dr wiązania E = E N = = = Fdr r F r E N F dr + A dr A = 0, E E N N = + E 0 R r F R dr Energia Siła i energia
10 Wiązanie jonowe Wiązanie kowalencyjne 1. Nie jest to zwykłe nałożenie chmur elektronowych; 2. Zmiana rozkładu gęstości elektronowej i energii;
11 Wiązanie metaliczne Wiązania pomiędzy cząsteczkami: Przyciąganie między dipolami (mogą to być też tylko chwilowe dipole),
12 Wiązanie wodorowe Rodzaje ciał stałych Krystaliczne i amorficzne
13 Można sobie kryształ wyobrazić jako: Powtarzające się w przestrzeni, identyczne bryły geometryczne KOMÓRKI ELEMENTARNE lub PRYMITYWNE Aby jednoznacznie opisać budowę ciała krystalicznego: Należy podać: KSZTAŁT ROZMIAR ZAWARTOŚĆ Komórki elementarnej lub prymitywnej
14 Kształty możliwych komórek elementarnych Istotne pojęcia: Stosowane oznaczenia: wskaźniki kierunków i płaszczyzn; Liczba atomów w komórce elementarnej; Liczba koordynacyjna; Gęstość upakowania; Kierunki i płaszczyzny gęsto upakowane; Luki tetraedryczne, oktaedryczne, sześcienne;
15 Wskaźniki kierunków, płaszczyzn,.. (c) 2003 Brooks/Cole Publishing / Thomson Learning Gęstość upakowania, liczba koordynacyjna,... Ilość atomów w komórce: 4 Liczba koordynacyjna: 12 Gęstość upakowania: 0.74 Płaszczyzny najgęściej upakowane: (001) i (111)
16 Gęstość upakowania na płaszczyźnie: (c) 2003 Brooks/Cole Publishing / Thomson Learning Kierunki gęsto upakowane. Znajdowanie kierunku gęsto upakowanego. (c) 2003 Brooks/Cole Publishing / Thomson Learning
17 Położenia międzywęzłowe Położenia międzywęzłowe (luka międzywęzłowa) Położenia pomiędzy normalnymi atomami i jonami w krysztale w których inny atom lub jon może się znajdować. Zazwyczaj, rozmiar położenia międzywęzłowego jest mniejszy niż jon lub atom zajmujący takie położenie. Położenia międzywęzłowe są ważne m in dlatego, że są one często zajęte przez mniejsze atomy (w kryształach związków chemicznych). Położenia międzywęzłowe Położenia międzywęzłowe mogą być różne: Luka sześcienna Atom międzywęzłowy ma liczbę koordynacyjną osiem. Luka oktaedryczna - Atom międzywęzłowy ma liczbę koordynacyjną sześć. Luka tetraedryczna - Atom międzywęzłowy ma liczbę koordynacyjną cztery.
18 Położenia międzywęzłowe w regularnych komórkach elementarnych. (c) 2003 Brooks/Cole Publishing / Thomson Learning Przykład: luki oktaedryczne w komórce fcc (c) 2003 Brooks/Cole Publishing / Thomson Learning
19 Przykład: luki oktaedryczne w komórce fcc 12 oktaedrycznych położeń międzywęzłowych na środkach krawędzi sześcianu: 1,0, ,, ,0, 2 1,1, ,, ,0, 2 1,0, ,, ,1, 2 1,1, , 2 1 0,1, 2,1 Oraz jedna w środku: 1/2, 1/2, 1/2. Każde z położeń na krawędziach komórki należy do czterech sąsiednich komórek, zatem tylko 1/4 każdego położenia należy do komórki. Zatem, liczba oktaedrycznych położeń międzywęzłowych w jednej komórce elementarnej fcc: (12 krawędzi) (1/4 na komórkę) + 1 w środku = 4
20 Materiały amorficzne O tym, czy dane ciało będzie krystaliczne, czy amorficzne decydują różne czynniki, z których najważniejszym jest szybkość chłodzenia.
21 Materiały amorficzne 1. Uporządowanie atomów w materiale amorfcznym nie jest całowicie przypadowe: 1) Koordynacja atomów jest podobna. 2) Kąty między wązaniami i ich długość też są zbliżone do tych w krysztale. Uporządowanie jest reprezentowane przez radialną funckję rozkładu, g(r) g(r) jest prawdopodobieństwem znalezienia atomu w odległości między r a r+δr od środka atomu odniesienia. Radialna funkcja rozkładu 1. Wybieramy atom odniesienia o promieniu a; Wtedy: 2. g(r) = 0 dla r<a 3. g(r) 1 dla dużych r 4.W odległościach pośrednich, g(r) oscyluje wokół jedności - uporządkowanie bliskiego zasięgu. Najbliżsi sąsiedzi dowolnego atomu wykazują pewne uporządkowanie - jednak nie takie jak w krysztale. SiO 4 -kąty są około 120º ale nie są dokładnie równe 120 º
22 Radialna funkcja rozkładu 1.Wynik pomiaru i obliczone na jego podstawie odległości między atomami w szkle kwarcowym: Radialna funkcja rozkładu Nie ma dużej różnicy między amorficznym ciałem stałym a cieczą.
23 Defekty punktowe. (c) 2003 Brooks/Cole Publishing / Thomson Learning Dyslokacje. (c) 2003 Brooks/Cole Publishing / Thomson Learning
24 Mikrostruktura 1. Granice międzyziarnowe występują we wszystkich materiałach polikrystalicznych. Jak wszystko to się ze sobą wiąże, zależy jedno od drugiego i wpływa na właściwości materiału
25 1. Jak wiązanie chemiczne wpływa na strukturę materiału Wiązanie jonowe. Wiadomo, że kryształy jonowe krystalizują tylko w niektórych strukturach. Wynika to z silnego elektrostatycznego odpychania między jonami tego samego znaku.
26 Promienie jonowe Promienie jonowe, r k /r a r kation r anion LK ZnS < NaCl CsCl 4
27 Przykład: CsCl r Cs + = 0.17 nm i r Cl - = nm, zatem: r Cs +/ r Cl - = 0.17/0.181 = Ponieważ < < 1.000, więc liczba koordynacyjna powinna być 8. Taka właśnie jest. (c) 2003 Brooks/Cole Publising / Thomson Learning Struktura fluorytu.
28 Inne struktury jonowe ZnS (c) 2003 Brooks/Cole Publishing / Thomson Learning (c) 2003 Brooks/Cole Publishing / Thomson Learning α-ai 2 0 3
29 Wiązanie kowalencyjne. Również kryształy kowalencyjne krystalizują tylko w niektórych strukturach. Wynika to z kierunkowości wiązania. W rezultacie:
30 Przykłady struktur krystalicznych o dominującym wiązaniu kowalencyjnym Wiązanie metaliczne 1. Wiązanie jest bezkierunkowe. Im więcej elektronów uczestniczy w tworzeniu wiązania, tym lepiej. +ve ion cores -ve electron sea
31 Kryształy metaliczne są gęsto upakowane
32 2. Jak wiązanie chemiczne wpływa na defekty Wiązanie jonowe. Podstawowym warunkiem, który musi być spełniony aby utworzyć defekt jest warunek obojętności elektrycznej: kryształ jako całość musi pozostać obojętny.
33 Wakanse Defekt Schottky ego = para wakansów: kationowego i anionowego Defekt Frenkla = Para wakans atom międzywęzłowy Domieszki 1. Sprawa jest prosta, gdy mają taki sam ładunek: Gdy podstawnik ma inny ładunek: wakans
34 Dyslokacje w kryształach jonowych. Dyslokacja w krysztale MgO Wiązanie kowalencyjne. Wiązanie kowalencyjne jest zazwyczaj silne. W związku z tym utworzenie wakansu wymaga dużej energii. Domieszki, natomiast, można wytworzyć łatwo i mają one bardzo duże znaczenie technologiczne. Dyslokacje powstają, ale są mało ruchliwe.
35 Wiązanie metaliczne. W kryształach metalicznych występują wszystkie możliwe defekty. Podsumowanie: jaki to wszystko ma wpływ na właściwości materiału (w wielkim skrócie)
36 F F Właściwości fizyczne 1. Temperatura topnienia; 2. Moduły sprężystości moduł Younga (E). 3. Wytrzymałość - naprężenie, powyżej którego materiał się trwale odkształca. 4. Współczynnik rozszerzalności cieplnej miara zmiany rozmiarów materiału wskutek zmiany temperatury. 5. Właściwości elektryczne. T M Długość wiązania, r r Temperatura topnienia, Tm Energia (r) Energia wiązania, Eo Energia (r) r o mniejsza T m r Długość równowagowa r o r Eo= energia wiązania większa T m Tm jest wyższa gdy Eo większa. 15
37 d( Energia) sila = = d( odleglosc) de da 2003 Brooks/Cole Publishing / Thomson Learning E Prawo Hooke a length, Lo niezdeformowane L rozciągnięte Przekrój poprzeczny A 0 F Moduł Younga F L = E A o Lo A naprężenie odkształcenie Zatem: F = 0 E( L ) siła jest liniową funkcją zmiany Lo długości, a współczynnik proporcjonalności zależy od E.
38 E 2003 Brooks/Cole Publishing / Thomson Learning Zatem moduł Younga zależy od nachylenia dflda w pobliżu odległości równowagowej. Oznacza to, że: E Moduł Younga jest większy gdy Eo jest większe Energia r o Długość równowagowa r Mniejszy moduł Younga Większy moduł Younga 16
39 α Współczynnik rozszerzalności cieplej, α długość Lo T 1 < T 2 T 1 L T 2 L = α (T 2 -T 1 ) Lo α 2003 Brooks/Cole Publishing / Thomson Learning Materiały o silnym wiązaniu: duże E 0, co oznacza głębokie i wąskie minimum energii, mają mały współczynnik rozszerzalności cieplnej.
40 Wytrzymałość Wytrzymałość i granica plastyczności zależy od rodzaju wiązań chemicznych, od struktury krystalicznej i od defektów struktury Naprężenie Stal Aluminium Alumina Glass Odkształcenie Przewodnictwo elektryczne
41 Metale Tylko w metalach są prawie swobodne elektrony, które przewodza prąd. Pasmo przewodzenia Pasmo walencyjne Półprzewodniki i izolatory Pasmo przewodzenia (puste) Duża przerwa energetyczna Pasmo walencyjne (całkowicie zapełnione) Pasmo przewodzenia (puste) Mała przerwa Pasmo walencyjne (całkowicie zapełnione) Izolator Półprzewodnik
42 Wpływ defektów na właściwości elektryczne: P N Pasmo przewodnictwa Pasmo przewodnictwa Poziomy domieszek Pasmo walencyjne Pasmo walencyjne
INŻYNIERIA NOWYCH MATERIAŁÓW
 INŻYNIERIA NOWYCH MATERIAŁÓW Wykład: 15 h Seminarium 15 h Laboratorium 45 h Świat materiałów Metale Ceramika, szkło Kompozyty Polimery, elastomery Pianki Materiały naturalne Znaczenie różnych materiałów
INŻYNIERIA NOWYCH MATERIAŁÓW Wykład: 15 h Seminarium 15 h Laboratorium 45 h Świat materiałów Metale Ceramika, szkło Kompozyty Polimery, elastomery Pianki Materiały naturalne Znaczenie różnych materiałów
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Właściwości kryształów
 Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Laboratorium inżynierii materiałowej LIM
 Laboratorium inżynierii materiałowej LIM wybrane zagadnienia fizyki ciała stałego czyli skrót skróconego skrótu dr hab. inż.. Ryszard Pawlak, P prof. PŁP Fizyka Ciała Stałego I. Wstęp Związki Fizyki Ciała
Laboratorium inżynierii materiałowej LIM wybrane zagadnienia fizyki ciała stałego czyli skrót skróconego skrótu dr hab. inż.. Ryszard Pawlak, P prof. PŁP Fizyka Ciała Stałego I. Wstęp Związki Fizyki Ciała
Transport jonów: kryształy jonowe
 Transport jonów: kryształy jonowe JONIKA I FOTONIKA MICHAŁ MARZANTOWICZ Jodek srebra AgI W 42 K strukturalne przejście fazowe I rodzaju do fazy α stopiona podsieć kationowa. Fluorek ołowiu PbF 2 zdefektowanie
Transport jonów: kryształy jonowe JONIKA I FOTONIKA MICHAŁ MARZANTOWICZ Jodek srebra AgI W 42 K strukturalne przejście fazowe I rodzaju do fazy α stopiona podsieć kationowa. Fluorek ołowiu PbF 2 zdefektowanie
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Wstęp. Krystalografia geometryczna
 Wstęp Przedmiot badań krystalografii. Wprowadzenie do opisu struktury kryształów. Definicja sieci Bravais go i bazy atomowej, komórki prymitywnej i elementarnej. Podstawowe typy komórek elementarnych.
Wstęp Przedmiot badań krystalografii. Wprowadzenie do opisu struktury kryształów. Definicja sieci Bravais go i bazy atomowej, komórki prymitywnej i elementarnej. Podstawowe typy komórek elementarnych.
Chemia nieorganiczna. Copyright 2000 by Harcourt, Inc. All rights reserved.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
S. Baran - Podstawy fizyki materii skondensowanej Wiązania chemiczne w ciałach stałych. Wiązania chemiczne w ciałach stałych
 Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Pasmowa teoria przewodnictwa. Anna Pietnoczka
 Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
INŻYNIERIA MATERIAŁOWA w elektronice
 Wydział Elektroniki Mikrosystemów i Fotoniki Politechniki Wrocławskiej... INŻYNIERIA MATERIAŁOWA w elektronice... Dr hab. inż. JAN FELBA Profesor nadzwyczajny PWr 1 PROGRAM WYKŁADU Struktura materiałów
Wydział Elektroniki Mikrosystemów i Fotoniki Politechniki Wrocławskiej... INŻYNIERIA MATERIAŁOWA w elektronice... Dr hab. inż. JAN FELBA Profesor nadzwyczajny PWr 1 PROGRAM WYKŁADU Struktura materiałów
Nauka o Materiałach Wykład II Monokryształy Jerzy Lis
 Wykład II Monokryształy Jerzy Lis Treść wykładu: 1. Wstęp stan krystaliczny 2. Budowa kryształów - krystalografia 3. Budowa kryształów rzeczywistych defekty WPROWADZENIE Stan krystaliczny jest podstawową
Wykład II Monokryształy Jerzy Lis Treść wykładu: 1. Wstęp stan krystaliczny 2. Budowa kryształów - krystalografia 3. Budowa kryształów rzeczywistych defekty WPROWADZENIE Stan krystaliczny jest podstawową
Chemia nieorganiczna. Pierwiastki. niemetale Be. 27 Co. 28 Ni. 26 Fe. 29 Cu. 45 Rh. 44 Ru. 47 Ag. 46 Pd. 78 Pt. 76 Os.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
Elektrolity wykazują przewodnictwo jonowe Elektrolity ciekłe substancje rozpadające się w roztworze na jony
 Elektrolity wykazują przewodnictwo jonowe Elektrolity ciekłe substancje rozpadające się w roztworze na jony Przewodniki jonowe elektrolity stałe duża przewodność jonowa w stanie stałym; mały wkład elektronów
Elektrolity wykazują przewodnictwo jonowe Elektrolity ciekłe substancje rozpadające się w roztworze na jony Przewodniki jonowe elektrolity stałe duża przewodność jonowa w stanie stałym; mały wkład elektronów
Funkcja rozkładu Fermiego-Diraca w różnych temperaturach
 Funkcja rozkładu Fermiego-Diraca w różnych temperaturach 1 f FD ( E) = E E F exp + 1 kbt Styczna do krzywej w punkcie f FD (E F )=0,5 przecina oś energii i prostą f FD (E)=1 w punktach odległych o k B
Funkcja rozkładu Fermiego-Diraca w różnych temperaturach 1 f FD ( E) = E E F exp + 1 kbt Styczna do krzywej w punkcie f FD (E F )=0,5 przecina oś energii i prostą f FD (E)=1 w punktach odległych o k B
Fizyka Ciała Stałego
 Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
Zjawiska zachodzące w półprzewodnikach Przewodniki samoistne i niesamoistne
 Zjawiska zachodzące w półprzewodnikach Przewodniki samoistne i niesamoistne Materiały dydaktyczne dla kierunku Technik Optyk (W12) Kwalifikacyjnego kursu zawodowego. Zadania elektroniki: Urządzenia elektroniczne
Zjawiska zachodzące w półprzewodnikach Przewodniki samoistne i niesamoistne Materiały dydaktyczne dla kierunku Technik Optyk (W12) Kwalifikacyjnego kursu zawodowego. Zadania elektroniki: Urządzenia elektroniczne
Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową
 Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową Kryształy Atomy w krysztale ułożone są w pewien powtarzający się regularny wzór zwany siecią krystaliczną. Struktura kryształu NaCl Polikryształy
Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową Kryształy Atomy w krysztale ułożone są w pewien powtarzający się regularny wzór zwany siecią krystaliczną. Struktura kryształu NaCl Polikryształy
7. Defekty samoistne Typy defektów Zdefektowanie samoistne w związkach stechiometrycznych
 7. Defekty samoistne 7.1. Typy defektów Zgodnie z trzecią zasadą termodynamiki, tylko w temperaturze 0[K] kryształ może mieć zerową entropię. Oznacza to, że jeśli temperatura jest wyższa niż 0[K] to w
7. Defekty samoistne 7.1. Typy defektów Zgodnie z trzecią zasadą termodynamiki, tylko w temperaturze 0[K] kryształ może mieć zerową entropię. Oznacza to, że jeśli temperatura jest wyższa niż 0[K] to w
Teoria pasmowa ciał stałych
 Teoria pasmowa ciał stałych Poziomy elektronowe atomów w cząsteczkach ulegają rozszczepieniu. W kryształach zjawisko to prowadzi do wytworzenia się pasm. Klasyfikacja ciał stałych na podstawie struktury
Teoria pasmowa ciał stałych Poziomy elektronowe atomów w cząsteczkach ulegają rozszczepieniu. W kryształach zjawisko to prowadzi do wytworzenia się pasm. Klasyfikacja ciał stałych na podstawie struktury
Wiązania chemiczne. Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych. 5 typów wiązań
 Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
Ciała stałe. Literatura: Halliday, Resnick, Walker, t. 5, rozdz. 42 Orear, t. 2, rozdz. 28 Young, Friedman, rozdz
 Ciała stałe Podstawowe własności ciał stałych Struktura ciał stałych Przewodnictwo elektryczne teoria Drudego Poziomy energetyczne w krysztale: struktura pasmowa Metale: poziom Fermiego, potencjał kontaktowy
Ciała stałe Podstawowe własności ciał stałych Struktura ciał stałych Przewodnictwo elektryczne teoria Drudego Poziomy energetyczne w krysztale: struktura pasmowa Metale: poziom Fermiego, potencjał kontaktowy
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
Defekty. Defekty strukturalne. Kryształ idealny nie istnieje
 Defekty Kryształ idealny nie istnieje Defekty strukturalne Każde zaburzenie periodycznego uporządkowania atomów w krysztale jest defektem. Może to być zaburzenie: Położenia atomów Typu atomów Typ i rodzaj
Defekty Kryształ idealny nie istnieje Defekty strukturalne Każde zaburzenie periodycznego uporządkowania atomów w krysztale jest defektem. Może to być zaburzenie: Położenia atomów Typu atomów Typ i rodzaj
Opis efektów kształcenia dla modułu zajęć
 Nazwa modułu: Fizyka metali Rok akademicki: 2013/2014 Kod: OM-2-101-OA-s Punkty ECTS: 3 Wydział: Odlewnictwa Kierunek: Metalurgia Specjalność: Odlewnictwo artystyczne i precyzyjne Poziom studiów: Studia
Nazwa modułu: Fizyka metali Rok akademicki: 2013/2014 Kod: OM-2-101-OA-s Punkty ECTS: 3 Wydział: Odlewnictwa Kierunek: Metalurgia Specjalność: Odlewnictwo artystyczne i precyzyjne Poziom studiów: Studia
Dobór materiałów konstrukcyjnych cz. 2
 Dobór materiałów konstrukcyjnych cz. 2 dr inż. Hanna Smoleńska Katedra Inżynierii Materiałowej i Spajania Wydział Mechaniczny, Politechnika Gdańska Materiały edukacyjne Własności materiałów brane pod uwagę
Dobór materiałów konstrukcyjnych cz. 2 dr inż. Hanna Smoleńska Katedra Inżynierii Materiałowej i Spajania Wydział Mechaniczny, Politechnika Gdańska Materiały edukacyjne Własności materiałów brane pod uwagę
Zaburzenia periodyczności sieci krystalicznej
 Zaburzenia periodyczności sieci krystalicznej Defekty liniowe dyslokacja krawędziowa dyslokacja śrubowa dyslokacja mieszana Defekty punktowe obcy atom w węźle luka w sieci (defekt Schottky ego) obcy atom
Zaburzenia periodyczności sieci krystalicznej Defekty liniowe dyslokacja krawędziowa dyslokacja śrubowa dyslokacja mieszana Defekty punktowe obcy atom w węźle luka w sieci (defekt Schottky ego) obcy atom
Fizyka 2. Janusz Andrzejewski
 Fizyka 2 wykład 13 Janusz Andrzejewski Scaledlugości Janusz Andrzejewski 2 Scaledługości Simple molecules
Fizyka 2 wykład 13 Janusz Andrzejewski Scaledlugości Janusz Andrzejewski 2 Scaledługości Simple molecules
STRUKTURA CIAŁA STAŁEGO
 STRUKTURA CIAŁA STAŁEGO Podział ciał stałych Ciała - bezpostaciowe (amorficzne) Szkła, żywice, tłuszcze, niektóre proszki. Nie wykazują żadnych regularnych płaszczyzn ograniczających, nie można w nich
STRUKTURA CIAŁA STAŁEGO Podział ciał stałych Ciała - bezpostaciowe (amorficzne) Szkła, żywice, tłuszcze, niektóre proszki. Nie wykazują żadnych regularnych płaszczyzn ograniczających, nie można w nich
Budowa ciał stałych. sieć krystaliczna układy krystalograficzne sieć realna defekty wiązania w ciałach stałych
 Budowa ciał stałych sieć krystaliczna układy krystalograficzne sieć realna defekty wiązania w ciałach stałych Ciała stałe to substancje o regularnej, przestrzennej budowie krystalicznej, czyli regularnym
Budowa ciał stałych sieć krystaliczna układy krystalograficzne sieć realna defekty wiązania w ciałach stałych Ciała stałe to substancje o regularnej, przestrzennej budowie krystalicznej, czyli regularnym
Przewodność elektryczna ciał stałych. Elektryczne własności ciał stałych Izolatory, metale i półprzewodniki
 Przewodność elektryczna ciał stałych Elektryczne własności ciał stałych Izolatory, metale i półprzewodniki Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności
Przewodność elektryczna ciał stałych Elektryczne własności ciał stałych Izolatory, metale i półprzewodniki Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Materiały i technologie w elektrotechnice i elektronice wykład I
 Materiały i technologie w elektrotechnice i elektronice wykład I Instytut Systemów Inżynierii Elektrycznej Zakład Inżynierii Materiałowej i Systemów Pomiarowych, ul Stefanowskiego 18/22 IV p. pok. 412
Materiały i technologie w elektrotechnice i elektronice wykład I Instytut Systemów Inżynierii Elektrycznej Zakład Inżynierii Materiałowej i Systemów Pomiarowych, ul Stefanowskiego 18/22 IV p. pok. 412
Absorpcja związana z defektami kryształu
 W rzeczywistych materiałach sieć krystaliczna nie jest idealna występują różnego rodzaju defekty. Podział najważniejszych defektów ze względu na właściwości optyczne: - inny atom w węźle sieci: C A atom
W rzeczywistych materiałach sieć krystaliczna nie jest idealna występują różnego rodzaju defekty. Podział najważniejszych defektów ze względu na właściwości optyczne: - inny atom w węźle sieci: C A atom
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Materiałoznawstwo optyczne CERAMIKA OPTYCZNA
 Materiałoznawstwo optyczne CERAMIKA OPTYCZNA Szkło optyczne i fotoniczne, A. Szwedowski, R. Romaniuk, WNT, 2009 POLIKRYSZTAŁY - ciała stałe o drobnoziarnistej strukturze, które są złożone z wielkiej liczby
Materiałoznawstwo optyczne CERAMIKA OPTYCZNA Szkło optyczne i fotoniczne, A. Szwedowski, R. Romaniuk, WNT, 2009 POLIKRYSZTAŁY - ciała stałe o drobnoziarnistej strukturze, które są złożone z wielkiej liczby
Elektryczne własności ciał stałych
 Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności elektryczne trzeba zdefiniować kilka wielkości Oporność właściwa (albo przewodność) ładunek [C] = 1/
Elektryczne własności ciał stałych Do sklasyfikowania różnych materiałów ze względu na ich własności elektryczne trzeba zdefiniować kilka wielkości Oporność właściwa (albo przewodność) ładunek [C] = 1/
Nauka o Materiałach. Wykład XI. Właściwości cieplne. Jerzy Lis
 Nauka o Materiałach Wykład XI Właściwości cieplne Jerzy Lis Nauka o Materiałach Treść wykładu: 1. Stabilność termiczna materiałów 2. Pełzanie wysokotemperaturowe 3. Przewodnictwo cieplne 4. Rozszerzalność
Nauka o Materiałach Wykład XI Właściwości cieplne Jerzy Lis Nauka o Materiałach Treść wykładu: 1. Stabilność termiczna materiałów 2. Pełzanie wysokotemperaturowe 3. Przewodnictwo cieplne 4. Rozszerzalność
Defekty punktowe II. M. Danielewski
 Defekty punktowe II 2008 M. Danielewski Defekty, niestechiometria, roztwory stałe i przewodnictwo jonowe w ciałach stałych Atkins, Shriver, Mrowec i inni Defekty w kryształach: nie można wytworzyć kryształu
Defekty punktowe II 2008 M. Danielewski Defekty, niestechiometria, roztwory stałe i przewodnictwo jonowe w ciałach stałych Atkins, Shriver, Mrowec i inni Defekty w kryształach: nie można wytworzyć kryształu
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Struktura pasmowa ciał stałych
 Struktura pasmowa ciał stałych dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści 1. Pasmowa teoria ciała stałego 2 1.1. Wstęp do teorii..............................................
Struktura pasmowa ciał stałych dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści 1. Pasmowa teoria ciała stałego 2 1.1. Wstęp do teorii..............................................
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
WŁAŚCIWOŚCI MECHANICZNE PLASTYCZNOŚĆ. Zmiany makroskopowe. Zmiany makroskopowe
 WŁAŚCIWOŚCI MECHANICZNE PLASTYCZNOŚĆ Zmiany makroskopowe Zmiany makroskopowe R e = R 0.2 - umowna granica plastyczności (0.2% odkształcenia trwałego); R m - wytrzymałość na rozciąganie (plastyczne); 1
WŁAŚCIWOŚCI MECHANICZNE PLASTYCZNOŚĆ Zmiany makroskopowe Zmiany makroskopowe R e = R 0.2 - umowna granica plastyczności (0.2% odkształcenia trwałego); R m - wytrzymałość na rozciąganie (plastyczne); 1
Struktura materiałów. Zakres tematyczny. Politechnika Rzeszowska - Materiały lotnicze - I LD / dr inż. Maciej Motyka.
 STRUKTURA, KLASYFIKACJA I OGÓLNA CHARAKTERYSTYKA MATERIAŁÓW INŻYNIERSKICH Zakres tematyczny y 1 Struktura materiałów MATERIAŁAMI (inżynierskimi) nazywa się skondensowane (stałe) substancje, których właściwości
STRUKTURA, KLASYFIKACJA I OGÓLNA CHARAKTERYSTYKA MATERIAŁÓW INŻYNIERSKICH Zakres tematyczny y 1 Struktura materiałów MATERIAŁAMI (inżynierskimi) nazywa się skondensowane (stałe) substancje, których właściwości
Materiały Reaktorowe. Właściwości mechaniczne
 Materiały Reaktorowe Właściwości mechaniczne Naprężenie i odkształcenie F A 0 l i l 0 l 0 l l 0 a. naprężenie rozciągające b. naprężenie ściskające c. naprężenie ścinające d. Naprężenie torsyjne Naprężenie
Materiały Reaktorowe Właściwości mechaniczne Naprężenie i odkształcenie F A 0 l i l 0 l 0 l l 0 a. naprężenie rozciągające b. naprężenie ściskające c. naprężenie ścinające d. Naprężenie torsyjne Naprężenie
Krystalografia. Typowe struktury pierwiastków i związków chemicznych
 Krystalografia Typowe struktury pierwiastków i związków chemicznych Wiązania w kryształach jonowe silne, bezkierunkowe kowalencyjne silne, kierunkowe metaliczne słabe lub silne, bezkierunkowe van der Waalsa
Krystalografia Typowe struktury pierwiastków i związków chemicznych Wiązania w kryształach jonowe silne, bezkierunkowe kowalencyjne silne, kierunkowe metaliczne słabe lub silne, bezkierunkowe van der Waalsa
Transport jonów: kryształy jonowe
 Transport jonów: kryształy jonowe Jodek srebra AgI W 420 K strukturalne przejście fazowe I rodzaju do fazy α stopiona podsieć kationowa. Fluorek ołowiu PbF 2 zdefektowanie Frenkla podsieci anionowej, klastry
Transport jonów: kryształy jonowe Jodek srebra AgI W 420 K strukturalne przejście fazowe I rodzaju do fazy α stopiona podsieć kationowa. Fluorek ołowiu PbF 2 zdefektowanie Frenkla podsieci anionowej, klastry
TEORIA PASMOWA CIAŁ STAŁYCH
 TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Wykład VI. Teoria pasmowa ciał stałych
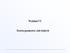 Wykład VI Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Wykład VI Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
DEFEKTY STRUKTURY KRYSTALICZNEJ. Publikacja współfinansowana ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 DEFEKTY STRUKTURY KRYSTALICZNEJ Publikacja współfinansowana ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego Defekty struktury krystalicznej są to każdego rodzaju odchylenia od
DEFEKTY STRUKTURY KRYSTALICZNEJ Publikacja współfinansowana ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego Defekty struktury krystalicznej są to każdego rodzaju odchylenia od
Wykład III. Teoria pasmowa ciał stałych
 Wykład III Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Wykład III Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO KRYSZTAŁY RZECZYWISTE.
 NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO KRYSZTAŁY RZECZYWISTE http://home.agh.edu.pl/~grzesik KRYSZTAŁY IDEALNE Kryształ idealny ciało stałe, w którym atomy, jony lub cząsteczki wykazują idealne uporządkowanie
NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO KRYSZTAŁY RZECZYWISTE http://home.agh.edu.pl/~grzesik KRYSZTAŁY IDEALNE Kryształ idealny ciało stałe, w którym atomy, jony lub cząsteczki wykazują idealne uporządkowanie
Podstawy fizyki wykład 4
 D. Halliday, R. Resnick, J.Walker: Podstawy Fizyki, tom 5, PWN, Warszawa 2003. H. D. Young, R. A. Freedman, Sear s & Zemansky s University Physics with Modern Physics, Addison-Wesley Publishing Company,
D. Halliday, R. Resnick, J.Walker: Podstawy Fizyki, tom 5, PWN, Warszawa 2003. H. D. Young, R. A. Freedman, Sear s & Zemansky s University Physics with Modern Physics, Addison-Wesley Publishing Company,
2. Półprzewodniki. Istnieje duża jakościowa różnica między właściwościami elektrofizycznymi półprzewodników, przewodników i dielektryków.
 2. Półprzewodniki 1 Półprzewodniki to materiały, których rezystywność jest większa niż rezystywność przewodników (metali) oraz mniejsza niż rezystywność izolatorów (dielektryków). Przykłady: miedź - doskonały
2. Półprzewodniki 1 Półprzewodniki to materiały, których rezystywność jest większa niż rezystywność przewodników (metali) oraz mniejsza niż rezystywność izolatorów (dielektryków). Przykłady: miedź - doskonały
Wykład V Wiązanie kowalencyjne. Półprzewodniki
 Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Rozszczepienie poziomów atomowych
 Rozszczepienie poziomów atomowych Poziomy energetyczne w pojedynczym atomie Gdy zbliżamy atomy chmury elektronowe nachodzą na siebie (inaczej: funkcje falowe elektronów zaczynają się przekrywać) Na skutek
Rozszczepienie poziomów atomowych Poziomy energetyczne w pojedynczym atomie Gdy zbliżamy atomy chmury elektronowe nachodzą na siebie (inaczej: funkcje falowe elektronów zaczynają się przekrywać) Na skutek
Transport jonów: kryształy jonowe
 Transport jonów: kryształy jonowe Jodek srebra AgI W 420 K strukturalne przejście fazowe I rodzaju do fazy α stopiona podsieć kationowa. Fluorek ołowiu PbF 2 zdefektowanie Frenkla podsieci anionowej, klastry
Transport jonów: kryształy jonowe Jodek srebra AgI W 420 K strukturalne przejście fazowe I rodzaju do fazy α stopiona podsieć kationowa. Fluorek ołowiu PbF 2 zdefektowanie Frenkla podsieci anionowej, klastry
Dyslokacje w kryształach. ach. Keshra Sangwal, Politechnika Lubelska. Literatura
 Dyslokacje w kryształach ach Keshra Sangwal, Politechnika Lubelska I. Wprowadzenie do defektów II. Dyslokacje: podstawowe pojęcie III. Własności mechaniczne kryształów IV. Źródła i rozmnażanie się dyslokacji
Dyslokacje w kryształach ach Keshra Sangwal, Politechnika Lubelska I. Wprowadzenie do defektów II. Dyslokacje: podstawowe pojęcie III. Własności mechaniczne kryształów IV. Źródła i rozmnażanie się dyslokacji
Dyslokacje w kryształach. ach. Keshra Sangwal Zakład Fizyki Stosowanej, Instytut Fizyki Politechnika Lubelska
 Dyslokacje w kryształach ach Keshra Sangwal Zakład Fizyki Stosowanej, Instytut Fizyki Politechnika Lubelska I. Wprowadzenie do defektów II. Dyslokacje: Podstawowe pojęcie III. Własności mechaniczne kryształów
Dyslokacje w kryształach ach Keshra Sangwal Zakład Fizyki Stosowanej, Instytut Fizyki Politechnika Lubelska I. Wprowadzenie do defektów II. Dyslokacje: Podstawowe pojęcie III. Własności mechaniczne kryształów
Elementy teorii powierzchni metali
 Prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład dla studentów fizyki Rok akademicki 2017/18 (30 godz.) Wykład 1 Plan wykładu Struktura periodyczna kryształów, sieć odwrotna Struktura
Prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład dla studentów fizyki Rok akademicki 2017/18 (30 godz.) Wykład 1 Plan wykładu Struktura periodyczna kryształów, sieć odwrotna Struktura
S. Baran - Podstawy fizyki materii skondensowanej Półprzewodniki. Półprzewodniki
 Półprzewodniki Definicja i własności Półprzewodnik materiał, którego przewodnictwo rośnie z temperaturą (opór maleje) i w temperaturze pokojowej wykazuje wartości pośrednie między przewodnictwem metali,
Półprzewodniki Definicja i własności Półprzewodnik materiał, którego przewodnictwo rośnie z temperaturą (opór maleje) i w temperaturze pokojowej wykazuje wartości pośrednie między przewodnictwem metali,
Jon w otoczeniu dipoli cząsteczkowych rozpuszczalnika utrzymywanych siłami elektrycznymi solwatacja (hydratacja)
 Jon w otoczeniu dipoli cząsteczkowych rozpuszczalnika utrzymywanych siłami elektrycznymi solwatacja (hydratacja) Jon w otoczeniu chmury dipoli i chmury jonowej. W otoczeniu jonu dodatniego (kationu) przewaga
Jon w otoczeniu dipoli cząsteczkowych rozpuszczalnika utrzymywanych siłami elektrycznymi solwatacja (hydratacja) Jon w otoczeniu chmury dipoli i chmury jonowej. W otoczeniu jonu dodatniego (kationu) przewaga
Właściwości optyczne. Oddziaływanie światła z materiałem. Widmo światła widzialnego MATERIAŁ
 Właściwości optyczne Oddziaływanie światła z materiałem hν MATERIAŁ Transmisja Odbicie Adsorpcja Załamanie Efekt fotoelektryczny Tradycyjnie właściwości optyczne wiążą się z zachowaniem się materiałów
Właściwości optyczne Oddziaływanie światła z materiałem hν MATERIAŁ Transmisja Odbicie Adsorpcja Załamanie Efekt fotoelektryczny Tradycyjnie właściwości optyczne wiążą się z zachowaniem się materiałów
Elektrolity wykazują przewodnictwo jonowe Elektrolity ciekłe substancje rozpadające się w roztworze na jony
 Elektrolity wykazują przewodnictwo jonowe Elektrolity ciekłe substancje rozpadające się w roztworze na jony Jony dodatnie - kationy: atomy pozbawione elektronów walencyjnych, np. Li +, Na +, Ag +, Ca 2+,
Elektrolity wykazują przewodnictwo jonowe Elektrolity ciekłe substancje rozpadające się w roztworze na jony Jony dodatnie - kationy: atomy pozbawione elektronów walencyjnych, np. Li +, Na +, Ag +, Ca 2+,
Półprzewodniki samoistne. Struktura krystaliczna
 Półprzewodniki samoistne Struktura krystaliczna Si a5.43 A GaAs a5.63 A ajczęściej: struktura diamentu i blendy cynkowej (ZnS) 1 Wiązania chemiczne Wiązania kowalencyjne i kowalencyjno-jonowe 0K wszystkie
Półprzewodniki samoistne Struktura krystaliczna Si a5.43 A GaAs a5.63 A ajczęściej: struktura diamentu i blendy cynkowej (ZnS) 1 Wiązania chemiczne Wiązania kowalencyjne i kowalencyjno-jonowe 0K wszystkie
Szkło kuloodporne: składa się z wielu warstw różnych materiałów, połączonych ze sobą w wysokiej temperaturze. Wzmacnianie szkła
 Wzmacnianie szkła Laminowanie szkła. Są dwa sposoby wytwarzania szkła laminowanego: 1. Jak na zdjęciach, czyli umieszczenie polimeru pomiędzy warstwy szkła i sprasowanie całego układu; polimer (PVB ma
Wzmacnianie szkła Laminowanie szkła. Są dwa sposoby wytwarzania szkła laminowanego: 1. Jak na zdjęciach, czyli umieszczenie polimeru pomiędzy warstwy szkła i sprasowanie całego układu; polimer (PVB ma
MATERIAŁOZNAWSTWO. Prof. dr hab. inż. Andrzej Zieliński Katedra Inżynierii Materiałowej Pok. 204
 MATERIAŁOZNAWSTWO Prof. dr hab. inż. Andrzej Zieliński Katedra Inżynierii Materiałowej Pok. 204 PODRĘCZNIKI Leszek A. Dobrzański: Podstawy nauki o materiałach i metaloznawstwo K. Prowans: Materiałoznawstwo
MATERIAŁOZNAWSTWO Prof. dr hab. inż. Andrzej Zieliński Katedra Inżynierii Materiałowej Pok. 204 PODRĘCZNIKI Leszek A. Dobrzański: Podstawy nauki o materiałach i metaloznawstwo K. Prowans: Materiałoznawstwo
Defekty. Każde zaburzenie periodyczności kryształu jest defektem.
 Defekty Każde zaburzenie periodyczności kryształu jest defektem. Może to być zaburzenie geometryczne, lub fizyczne: Położenia atomów Typu atomów Uporządkowania spinów, koncentracji elektronów itd. Zaburzenie
Defekty Każde zaburzenie periodyczności kryształu jest defektem. Może to być zaburzenie geometryczne, lub fizyczne: Położenia atomów Typu atomów Uporządkowania spinów, koncentracji elektronów itd. Zaburzenie
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ
 CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
STRUKTURA IDEALNYCH KRYSZTAŁÓW
 BUDOWA WEWNĘTRZNA MATERIAŁÓW METALICZNYCH Zakres tematyczny y 1 STRUKTURA IDEALNYCH KRYSZTAŁÓW 2 1 Sieć przestrzenna kryształu TRANSLACJA WĘZŁA TRANSLACJA PROSTEJ SIECIOWEJ TRANSLACJA PŁASZCZYZNY SIECIOWEJ
BUDOWA WEWNĘTRZNA MATERIAŁÓW METALICZNYCH Zakres tematyczny y 1 STRUKTURA IDEALNYCH KRYSZTAŁÓW 2 1 Sieć przestrzenna kryształu TRANSLACJA WĘZŁA TRANSLACJA PROSTEJ SIECIOWEJ TRANSLACJA PŁASZCZYZNY SIECIOWEJ
Szkło. T g szkła używanego w oknach katedr wynosi ok. 600 C, a czas relaksacji sięga lat. FIZYKA 3 MICHAŁ MARZANTOWICZ
 Szkło Przechłodzona ciecz, w której ruchy uległy zamrożeniu Tzw. przejście szkliste: czas potrzebny na zmianę konfiguracji cząsteczek (czas relaksacji) jest rzędu minut lub dłuższy T g szkła używanego
Szkło Przechłodzona ciecz, w której ruchy uległy zamrożeniu Tzw. przejście szkliste: czas potrzebny na zmianę konfiguracji cząsteczek (czas relaksacji) jest rzędu minut lub dłuższy T g szkła używanego
Podstawowe właściwości fizyczne półprzewodników WYKŁAD 1 SMK J. Hennel: Podstawy elektroniki półprzewodnikowej, WNT, W-wa 2003
 Podstawowe właściwości fizyczne półprzewodników WYKŁAD 1 SMK J. Hennel: Podstawy elektroniki półprzewodnikowej, WNT, W-wa 003 1. Wiązania atomów w krysztale Siły wiążące atomy w kryształ mają charakter
Podstawowe właściwości fizyczne półprzewodników WYKŁAD 1 SMK J. Hennel: Podstawy elektroniki półprzewodnikowej, WNT, W-wa 003 1. Wiązania atomów w krysztale Siły wiążące atomy w kryształ mają charakter
Wykład XIV: Właściwości optyczne. JERZY LIS Wydział Inżynierii Materiałowej i Ceramiki Katedra Technologii Ceramiki i Materiałów Ogniotrwałych
 Wykład XIV: Właściwości optyczne JERZY LIS Wydział Inżynierii Materiałowej i Ceramiki Katedra Technologii Ceramiki i Materiałów Ogniotrwałych Treść wykładu: Treść wykładu: 1. Wiadomości wstępne: a) Załamanie
Wykład XIV: Właściwości optyczne JERZY LIS Wydział Inżynierii Materiałowej i Ceramiki Katedra Technologii Ceramiki i Materiałów Ogniotrwałych Treść wykładu: Treść wykładu: 1. Wiadomości wstępne: a) Załamanie
Wykład IX: Odkształcenie materiałów - właściwości plastyczne
 Wykład IX: Odkształcenie materiałów - właściwości plastyczne JERZY LIS Wydział Inżynierii Materiałowej i Ceramiki Katedra Technologii Ceramiki i Materiałów Ogniotrwałych Treść wykładu: 1. Odkształcenie
Wykład IX: Odkształcenie materiałów - właściwości plastyczne JERZY LIS Wydział Inżynierii Materiałowej i Ceramiki Katedra Technologii Ceramiki i Materiałów Ogniotrwałych Treść wykładu: 1. Odkształcenie
!!!DEL są źródłami światła niespójnego.
 Dioda elektroluminescencyjna DEL Element czynny DEL to złącze p-n. Gdy zostanie ono spolaryzowane w kierunku przewodzenia, to w obszarze typu p, w warstwie o grubości rzędu 1µm, wytwarza się stan inwersji
Dioda elektroluminescencyjna DEL Element czynny DEL to złącze p-n. Gdy zostanie ono spolaryzowane w kierunku przewodzenia, to w obszarze typu p, w warstwie o grubości rzędu 1µm, wytwarza się stan inwersji
Nauka o Materiałach. Wykład IX. Odkształcenie materiałów właściwości plastyczne. Jerzy Lis
 Nauka o Materiałach Wykład IX Odkształcenie materiałów właściwości plastyczne Jerzy Lis Nauka o Materiałach Treść wykładu: 1. Odkształcenie plastyczne 2. Parametry makroskopowe 3. Granica plastyczności
Nauka o Materiałach Wykład IX Odkształcenie materiałów właściwości plastyczne Jerzy Lis Nauka o Materiałach Treść wykładu: 1. Odkształcenie plastyczne 2. Parametry makroskopowe 3. Granica plastyczności
ELEMENTY ELEKTRONICZNE
 AKADEMIA GÓRNICZO-HUTNICZA IM. STANISŁAWA STASZICA W KRAKOWIE Wydział Elektrotechniki, Automatyki, Informatyki i Elektroniki Katedra Elektroniki ELEMENTY ELEKTRONICZNE dr inż. Piotr Dziurdzia paw. C-3,
AKADEMIA GÓRNICZO-HUTNICZA IM. STANISŁAWA STASZICA W KRAKOWIE Wydział Elektrotechniki, Automatyki, Informatyki i Elektroniki Katedra Elektroniki ELEMENTY ELEKTRONICZNE dr inż. Piotr Dziurdzia paw. C-3,
Materiały Reaktorowe. - Struktura pasmowa - Defekty sieci
 Materiały Reaktorowe - Struktura pasmowa - Defekty sieci Struktura pasmowa Właściwości elektronów w ciałach stałych wynikają z ich oddziaływania między sobą i oddziaływania z atomami (jonami) sieci. Jednakże
Materiały Reaktorowe - Struktura pasmowa - Defekty sieci Struktura pasmowa Właściwości elektronów w ciałach stałych wynikają z ich oddziaływania między sobą i oddziaływania z atomami (jonami) sieci. Jednakże
Nauka o Materiałach dr hab. inż. Mirosław Bućko, prof. AGH B-8, p. 1.13, tel
 Nauka o Materiałach dr hab. inż. Mirosław Bućko, prof. AGH B-8, p. 1.13, tel. 12 617 3572 www.kcimo.pl, bucko@agh.edu.pl Plan wykładów Monokryształy, Materiały amorficzne i szkła, Polikryształy budowa,
Nauka o Materiałach dr hab. inż. Mirosław Bućko, prof. AGH B-8, p. 1.13, tel. 12 617 3572 www.kcimo.pl, bucko@agh.edu.pl Plan wykładów Monokryształy, Materiały amorficzne i szkła, Polikryształy budowa,
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Nauka o Materiałach. Wykład VI. Odkształcenie materiałów właściwości sprężyste i plastyczne. Jerzy Lis
 Nauka o Materiałach Wykład VI Odkształcenie materiałów właściwości sprężyste i plastyczne Jerzy Lis Nauka o Materiałach Treść wykładu: 1. Właściwości materiałów -wprowadzenie 2. Statyczna próba rozciągania.
Nauka o Materiałach Wykład VI Odkształcenie materiałów właściwości sprężyste i plastyczne Jerzy Lis Nauka o Materiałach Treść wykładu: 1. Właściwości materiałów -wprowadzenie 2. Statyczna próba rozciągania.
E e l kt k r t o r n o ow o a w a s t s r t u r kt k u t ra r a at a o t m o u
 Elektronowa struktura atomu Anna Pietnoczka BUDOWA ATOMU CZĄSTKA SYMBOL WYSTĘPOWANIE MASA ŁADUNEK ELEKTRYCZNY PROTON p + jądroatomowe około 1 u + 1 NEUTRON n 0 jądroatomowe około 1u Brak ELEKTRON e - powłoki
Elektronowa struktura atomu Anna Pietnoczka BUDOWA ATOMU CZĄSTKA SYMBOL WYSTĘPOWANIE MASA ŁADUNEK ELEKTRYCZNY PROTON p + jądroatomowe około 1 u + 1 NEUTRON n 0 jądroatomowe około 1u Brak ELEKTRON e - powłoki
Elektrolit: przewodność jonowa określa opór wewnętrzny ogniwa. Niska przewodność = duże straty wewnątrz ogniwa
 Przewodność jonowa Elektrolit: przewodność jonowa określa opór wewnętrzny ogniwa. Niska przewodność = duże straty wewnątrz ogniwa Elektrody: przewodność jonowa określa opór wewnętrzny ogniwa. Wartość przewodności
Przewodność jonowa Elektrolit: przewodność jonowa określa opór wewnętrzny ogniwa. Niska przewodność = duże straty wewnątrz ogniwa Elektrody: przewodność jonowa określa opór wewnętrzny ogniwa. Wartość przewodności
Czym się różni ciecz od ciała stałego?
 Szkła Czym się różni ciecz od ciała stałego? gęstość Czy szkło to ciecz czy ciało stałe? Szkło powstaje w procesie chłodzenia cieczy. Czy szkło to ciecz przechłodzona? kryształ szkło ciecz przechłodzona
Szkła Czym się różni ciecz od ciała stałego? gęstość Czy szkło to ciecz czy ciało stałe? Szkło powstaje w procesie chłodzenia cieczy. Czy szkło to ciecz przechłodzona? kryształ szkło ciecz przechłodzona
STRUKTURA PASM ENERGETYCZNYCH
 PODSTAWY TEORII PASMOWEJ Struktura pasm energetycznych Teoria wa Struktura wa stałych Półprzewodniki i ich rodzaje Półprzewodniki domieszkowane Rozkład Fermiego - Diraca Złącze p-n (dioda) Politechnika
PODSTAWY TEORII PASMOWEJ Struktura pasm energetycznych Teoria wa Struktura wa stałych Półprzewodniki i ich rodzaje Półprzewodniki domieszkowane Rozkład Fermiego - Diraca Złącze p-n (dioda) Politechnika
Wykład IV. Półprzewodniki samoistne i domieszkowe
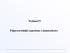 Wykład IV Półprzewodniki samoistne i domieszkowe Półprzewodniki (Si, Ge, GaAs) Konfiguracja elektronowa Si : 1s 2 2s 2 2p 6 3s 2 3p 2 = [Ne] 3s 2 3p 2 4 elektrony walencyjne Półprzewodnik samoistny Talent
Wykład IV Półprzewodniki samoistne i domieszkowe Półprzewodniki (Si, Ge, GaAs) Konfiguracja elektronowa Si : 1s 2 2s 2 2p 6 3s 2 3p 2 = [Ne] 3s 2 3p 2 4 elektrony walencyjne Półprzewodnik samoistny Talent
S. Baran - Podstawy fizyki materii skondensowanej Pasma energetyczne. Pasma energetyczne
 Pasma energetyczne Niedostatki modelu gazu Fermiego elektronów swobodnych Pomimo wielu sukcesów model nie jest w stanie wyjaśnić następujących zagadnień: 1. różnica między metalami, półmetalami, półprzewodnikami
Pasma energetyczne Niedostatki modelu gazu Fermiego elektronów swobodnych Pomimo wielu sukcesów model nie jest w stanie wyjaśnić następujących zagadnień: 1. różnica między metalami, półmetalami, półprzewodnikami
Przyrządy i układy półprzewodnikowe
 Przyrządy i układy półprzewodnikowe Prof. dr hab. Ewa Popko ewa.popko@pwr.edu.pl www.if.pwr.wroc.pl/~popko p.231a A-1 Zawartość wykładu Wy1, Wy2 Wy3 Wy4 Wy5 Wy6 Wy7 Wy8 Wy9 Wy10 Wy11 Wy12 Wy13 Wy14 Wy15
Przyrządy i układy półprzewodnikowe Prof. dr hab. Ewa Popko ewa.popko@pwr.edu.pl www.if.pwr.wroc.pl/~popko p.231a A-1 Zawartość wykładu Wy1, Wy2 Wy3 Wy4 Wy5 Wy6 Wy7 Wy8 Wy9 Wy10 Wy11 Wy12 Wy13 Wy14 Wy15
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY
 WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
Różne dziwne przewodniki
 Różne dziwne przewodniki czyli trzy po trzy o mechanizmach przewodzenia prądu elektrycznego Przewodniki elektronowe Metale Metale (zwane również przewodnikami) charakteryzują się tym, że elektrony ich
Różne dziwne przewodniki czyli trzy po trzy o mechanizmach przewodzenia prądu elektrycznego Przewodniki elektronowe Metale Metale (zwane również przewodnikami) charakteryzują się tym, że elektrony ich
CHEMIA DEFEKTÓW PUNKTOWYCH, CZ. I NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO
 CHEMIA DEFEKTÓW PUNKTOWYCH, CZ. I NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO KRYSZTAŁY RZECZYWISTE - NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO źródła defektów w ciałach stałych i ich klasyfikacja, trwałość termodynamiczna
CHEMIA DEFEKTÓW PUNKTOWYCH, CZ. I NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO KRYSZTAŁY RZECZYWISTE - NIEDOSKONAŁOŚCI BUDOWY CIAŁA STAŁEGO źródła defektów w ciałach stałych i ich klasyfikacja, trwałość termodynamiczna
MATERIAŁOZNAWSTWO Wydział Mechaniczny, Mechatronika, sem. I. dr inż. Hanna Smoleńska
 MATERIAŁOZNAWSTWO Wydział Mechaniczny, Mechatronika, sem. I dr inż. Hanna Smoleńska Defekty struktury Defekty struktury krystalicznej są to każdego rodzaju odchylenia od idealnej struktury. Najczęściej
MATERIAŁOZNAWSTWO Wydział Mechaniczny, Mechatronika, sem. I dr inż. Hanna Smoleńska Defekty struktury Defekty struktury krystalicznej są to każdego rodzaju odchylenia od idealnej struktury. Najczęściej
Wpływ defektów punktowych i liniowych na własności węglika krzemu SiC
 Wpływ defektów punktowych i liniowych na własności węglika krzemu SiC J. Łażewski, M. Sternik, P.T. Jochym, P. Piekarz politypy węglika krzemu SiC >250 politypów, najbardziej stabilne: 3C, 2H, 4H i 6H
Wpływ defektów punktowych i liniowych na własności węglika krzemu SiC J. Łażewski, M. Sternik, P.T. Jochym, P. Piekarz politypy węglika krzemu SiC >250 politypów, najbardziej stabilne: 3C, 2H, 4H i 6H
Podstawy krystalografii
 Podstawy krystalografii Kryształy Pojęcie kryształu znane było już w starożytności. Nazywano tak ciała o regularnych kształtach i gładkich ścianach. Już wtedy podejrzewano, że te cechy związane są ze szczególną
Podstawy krystalografii Kryształy Pojęcie kryształu znane było już w starożytności. Nazywano tak ciała o regularnych kształtach i gładkich ścianach. Już wtedy podejrzewano, że te cechy związane są ze szczególną
Dobór materiałów konstrukcyjnych cz. 9
 Dobór materiałów konstrukcyjnych cz. 9 dr inż. Hanna Smoleńska Katedra Inżynierii Materiałowej i Spajania Wydział Mechaniczny, Politechnika Gdańska Materiały edukacyjne Materiały na uszczelki Ashby M.F.:
Dobór materiałów konstrukcyjnych cz. 9 dr inż. Hanna Smoleńska Katedra Inżynierii Materiałowej i Spajania Wydział Mechaniczny, Politechnika Gdańska Materiały edukacyjne Materiały na uszczelki Ashby M.F.:
