CZĄSTECZKA (VB) Metoda (teoria) wiązań walencyjnych (VB)
|
|
|
- Wanda Włodarczyk
- 8 lat temu
- Przeglądów:
Transkrypt
1 CZĄSTECZKA (VB) Metoda (teoria) wiąań walencjnch (VB) teoria VSEPR (ang. Valence Shell Electron Pair Repulsion), tj. odpchanie się par elektronów powłoki walencjnej teoria Sidgwicka i Powella (1940 r.) teoria Gilleiego i Nholma kstałt cąstecki wiąan jest licbą par elektronów na powłoce walencjnej atomu centralnego, obsadone pre par elektronów orbitale odpchają się, można prewidieć romiescenie orbitali wokół atomu centralnego a tm samm możliwe jest określenie kstałtu cąstecki i kątów międ wiąaniami, Dogodną i użtecną metodę prewidwania kstałtu cąstecki stanowi koncepcja hbrdacji. dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
2 YBRYDYZACJA - wmiesanie funkcji falowch, tworenie orbitali miesanch orbitali atomowch mającch najcęściej tę samą główną licbę kwantową lec różne wartości pobocnej licb kwantowej. brdacja nie jest recwistm jawiskiem ficnm wstępującm w cąstecce, lec jednie formalnm abiegiem matematcnm umożliwiającm wgodn opis wiąań chemicnch i struktur elektronowej cąstecek. Nowe orbitale, którch charakterstki są kombinacją orbitali atomowch (pocątkowch) nawane są orbitalami hbrdowanmi lub hbrdami. Licba hbrd, tn. orbitali hbrdowanch jest awse równa licbie orbitali użtch do hbrdacji. dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii brdacja - dlacego???... np. cąstecka gaowego Be 2 Be - stan podstawow elektron walencjne 2s 2p 2p 2p Be* - stan wbudon 2s 2p 2p 2p I wiąanie 2s + 2p II wiąanie 2p + 2p Wniosek (?) wiąania utworone są różnch orbitali, a więc są: nierównocenne, o różnej długości, różnicowanej energii. dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
3 Recwistość! oba wiąania są jednakowo silne (o tej samej długości i energii) cąstecka ma budowę liniową. rowiąanie hbrdacja + + s p (dwa orbitale atomowe) (dwa orbitale hbrdowane) s + p + p 3 orbitale hbrdowane tpu: 2 s + p + p + p 4 orbitale hbrdowane tpu: kstałt orbitali na dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii Orbitale.url Orbitale hbrdpwane 2 Orbitale hbrdpwane Co bło pierwse, cąstecka c hbrdacja? dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
4 dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii 4Be 1s 2 2s 2 Cąstecka Be 2 2s 2p 2s 2p stan podstawow Be stan wbudon Be* stan wbudon + hbrdacja Be hbrdacja tpu to hbrdacja digonalna każda hbrda awiera jeden elektron 180o Be Be dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
5 5B 1s 2 2s 2 2p 1 Cąstecka B 3 2s 2p 3s 3p stan podstawow B stan wbudon B* stan wbudon + hbrdacja B hbrdacja tpu 2 to hbrdacja trgonalna każda hbrda 2 awiera jeden elektron B B 120o dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii 6C 1s 2 2s 2 2p 2 Cąstecka C 4 2s 2p stan podstawow C stan wbudon C* stan wbudon + hbrdacja C hbrdacja tpu to hbrdacja tetraedrcna każda hbrda awiera jeden elektron 109o28' dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
6 7N 1s 2 2s 2 2p 3 Cąstecka N 3 2s 2p N i N* stan wbudon + hbrdacja N hbrdacja tpu kąt 106 o 45 dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii Cąstecka 2 O 8O 1s 2 2s 2 2p 4 O i O* 2s 2p stan wbudon + hbrdacja O hbrdacja tpu kąt 104 o 30 dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
7 Be 2 CO 2 N 2 O Be 2 CS 2 C B 3 C 2 4 NO 2 O 3 B 3 CO 2 3 NO 2 SO 2 NO 3 SO 3 B 4 C 4 N 3 2 O C 3 N + 4 SO 2 4 C 4 SO 2 3 d P 5 S 4 I 3 d 2 S 6 I 5 d 2, d 2 i inne w wiąkach kompleksowch, np. Pt(N 3 ) 2 2, [e(cn) 6 ] 3 hbrd. kombinacja orbitali kąt geometria cąstecki s + p 180 o liniowa 2 s + p + p 120 o trgonalna (płaski Δ) s + p + p + p 109 o 28 tetraedrcna d s + p + p + p + d 90 o, 120 o bipiramida trgonalna d 2 s + p + p + p + d + d 90 o oktaedrcna dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii Orbitale hbrdpwane d Orbitale hbrdpwane d 2 Orbitale.url dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
8 Cąstecka P 5 15P 1s 2 2s 2 2p 6 3s 2 3p 3 3s 3p 3d stan podstawow P stan wbudon P* stan wbudon + hbrdacja P P hbrdacja tpu d bipiramida trgonalna dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii Cąstecka S 4 16S 1s 2 2s 2 2p 6 3s 2 3p 4 3s 3p 3d stan podstawow S stan wbudon S* stan wbudon + hbrdacja S S hbrdacja tpu d bipiramida trgonalna dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
9 Jon I 3 53I powłoka walencjna 5s 2 5p 5 5s 5p 5d stan podstawow I stan wbudon + hbrdacja I I hbrdacja tpu d bipiramida trgonalna kąt 180 o I I dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii Cąstecka S 6 16S 1s 2 2s 2 2p 6 3s 2 3p 4 3s 3p 3d stan podstawow S stan wbudon S* stan wbudon + hbrdacja S hbrdacja tpu d 2 oktaedr kąt 90 o S dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
10 wiąania tpu + s s s-s + s p s-p + p p p-p wiąania tpu π + p p p-p dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii Cąstecka C 2 6 (etan) 6C 1s 2 2s 2 2p 2 2s 2p stan podstawow C stan wbudon C* stan wbudon + hbrdacja C C C wiąania tpu dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
11 Cąstecka C 2 4 6C 1s 2 2s 2 2p 2 stan podstawow C (eten, etlen) 2s 2p stan wbudon C* p stan wbudon + hbrdacja C. dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii... C π C dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
12 Cąstecka C 2 2 6C 1s 2 2s 2 2p 2 stan podstawow C (etn, acetlen) 2s 2p stan wbudon C* p p stan wbudon + hbrdacja C. dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii... C π,π C dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
13 6C 1s 2 2s 2 2p 2 Cąstecka CO 2 2s stan podstawow C 2p 8O 1s 2 2s 2 2p 4 2s O (2 atom) 2p stan wbudon C* stan wb. + hbrd. C. p p atom O atom C dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii atom O. atom O atom C atom O. O π C π O atom O atom C atom O dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
14 Cąstecka SO 2 16S 1s 2 2s 2 2p 6 3s 2 3p 4 3s 3p 3d stan podstawow S stan wbudon S* stan wbudon + hbrdacja S p d hbrdacja tpu 2 budowa płaska trójkątna kąt 119,5 o O S O dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii MEZOMERIA REZONANS (wor meomercne struktur reonansowe) /osób predstawienia budow elektronowej pewnch wiąków chemicnch (tch w którch nie można rokładu elektronów w cąstecce opisać prawidłowo jednm strukturalnm worem chemicnm) a pomocą struktur granicnch/ benen poprawne wor strukturalne tlenków, kwasów tlenowch i ich anionów: NO NO 2 SO 2 O 3 SO 3 2 CO 3 CO 2 3 NO 3 NO 3 NO 2 NO 2 3 PO 4 2 SO 4 SO SO 3 SO 3 2 S 2 O 3 2 COO COO C 3 COO C 3 COO dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
15 Struktura prestrenna cąstecek i jonów (dla pierwiastków grup głównch) AX n m A atom centraln X inne atom (jednakowe lub różne) atom wodoru bepośrednio wiąan atomem A np. w C 3 n = 3 a m = 1 Licbę orbitali hbrdowanch (licbę hbrd L h ) oblica się wg worów: L pe = ½ L ew 4 n m L h = L pe + n + m L pe L pe L h - licba wolnch par elektronów na atomie centralnm - licba elektronów walencjnch w cąstecce (jonie) - licba hbrd Jeżeli L h wnosi: 2 digonalna 5 bipiramida trgonalna 3 trgonalna 6 oktaedrcna 4 tetraedrcna dr enrk Mska - Uniwerstet Gdański - Wdiał Chemii
TEORIA WIĄZAŃ WALENCYJNYCH (VB) dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 TEORIA WIĄZAŃ WALENCYJNYC (VB) Metoda (teoria) wiąań walencjnch (VB) Dogodną i użtecną metodę prewidwania kstałtu cąstecki stanowi koncepcja hbrdacji. YBRYDYZACJA - wmiesanie funkcji falowch, tworenie
TEORIA WIĄZAŃ WALENCYJNYC (VB) Metoda (teoria) wiąań walencjnch (VB) Dogodną i użtecną metodę prewidwania kstałtu cąstecki stanowi koncepcja hbrdacji. YBRYDYZACJA - wmiesanie funkcji falowch, tworenie
CZĄSTECZKA (VB) Dogodną i użyteczną metodę przewidywania kształtu cząsteczki stanowi koncepcja hybrydyzacji.
 ZĄSTEZKA (VB) Dogodną i użtecną metodę prewidwania kstałtu cąstecki stanowi koncepcja hbrdacji YBRYDYZAJA - wmiesanie funkcji falowch, tworenie orbitali miesanch orbitali atomowch mającch najcęściej tę
ZĄSTEZKA (VB) Dogodną i użtecną metodę prewidwania kstałtu cąstecki stanowi koncepcja hbrdacji YBRYDYZAJA - wmiesanie funkcji falowch, tworenie orbitali miesanch orbitali atomowch mającch najcęściej tę
Cząsteczki wieloatomowe - hybrydyzacja
 ątecki wieloatomowe - hbrdacja w oarciu o koncecję orbitali molekularnch można wtłumacć budowę cątecek? Koncecja OA OA O delokaliowane OA hb OA O lokaliowane OA hb OA hb OA orbitale atomowe OA hb orbitale
ątecki wieloatomowe - hbrdacja w oarciu o koncecję orbitali molekularnch można wtłumacć budowę cątecek? Koncecja OA OA O delokaliowane OA hb OA O lokaliowane OA hb OA hb OA orbitale atomowe OA hb orbitale
BUDOWA ATOMU cd. MECHANIKA KWANTOWA
 BUDOWA ATOMU cd. ajmuje się opisem ruchu cąstek elementarnch, układ można opiswać posługując się współrędnmi określającmi położenie bądź pęd, współrędne określa się pewnm prbliżeniem, np. współrędną dokładnością
BUDOWA ATOMU cd. ajmuje się opisem ruchu cąstek elementarnch, układ można opiswać posługując się współrędnmi określającmi położenie bądź pęd, współrędne określa się pewnm prbliżeniem, np. współrędną dokładnością
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
BUDOWA ATOMU cd. MECHANIKA KWANTOWA
 BUDOWA ATOMU cd. ajmuje się opisem ruchu cąstek elementarnch, układ można opiswać posługując się współrędnmi określającmi położenie bądź pęd, współrędne określa się pewnm prbliżeniem, np. współrędną dokładnością
BUDOWA ATOMU cd. ajmuje się opisem ruchu cąstek elementarnch, układ można opiswać posługując się współrędnmi określającmi położenie bądź pęd, współrędne określa się pewnm prbliżeniem, np. współrędną dokładnością
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Ligand to cząsteczka albo jon, który związany jest z jonem albo atomem centralnym.
 138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
zaprezentowana w 1940 roku (Sidgwick i Powell). O budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu
 Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
H H 2.5 < H H CH 3 N O O H C N ŁADUNEK FORMALNY. 2.5 dla atomu węgla C C 2.5 H 2.1. Li 1.0. liczba e - walencyjnych w atomie wolnym C 2.5 H 2.
 .5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
.5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
RJC. Wiązania Chemiczne & Slides 1 to 39
 Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Budowa atomów. Atomy wieloelektronowe Zakaz Pauliego Układ okresowy pierwiastków
 Novosibirsk Russia September 00 W-6 (Jarosewic) slajdy Na podstawie preentacji prof. J. Rutkowskiego Budowa atomów Atomy wieloelektronowe Zaka Pauliego Układ okresowy pierwiastków Atomy wieloelektronowe
Novosibirsk Russia September 00 W-6 (Jarosewic) slajdy Na podstawie preentacji prof. J. Rutkowskiego Budowa atomów Atomy wieloelektronowe Zaka Pauliego Układ okresowy pierwiastków Atomy wieloelektronowe
Wiązania kowalencyjne
 Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
KSZTAŁTY CZĄSTECZEK I JONÓW. METODA VSEPR
 KSZTAŁTY CZĄSTECZEK I JNÓW METDA VSEPR Teoria VSEPR (ang Valence Shell Electron Pair Repulsion odpychanie się elektronów powłoki walencyjnej) jest uproszczonym sposobem przewidywania kształtu kowalencyjnych
KSZTAŁTY CZĄSTECZEK I JNÓW METDA VSEPR Teoria VSEPR (ang Valence Shell Electron Pair Repulsion odpychanie się elektronów powłoki walencyjnej) jest uproszczonym sposobem przewidywania kształtu kowalencyjnych
b) Pierwiastek E tworzy tlenek o wzorze EO 2 i wodorek typu EH 4, a elektrony w jego atomie rozmieszczone są na dwóch powłokach elektronowych
 1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
TEORIA ORBITALI MOLEKULARNYCH (MO) dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Teoria VSEPR. Jak przewidywac strukturę cząsteczki?
 Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej jedną z dwóch metod (teorii): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
d dz d dy e r d dx ψ = ψ(r, Θ, ϕ) = R n (r) Y l,m (Θ,ϕ) = ψ n,l,m E n 2 n NAJPROSTSZA CZĄSTECZKA - MOLEKUŁA H 2 Przypomnienie: atom wodoru
 NAJPROSTSZA CZĄSTECZKA - MOLEKUŁA H Przomnienie: atom wodoru m d d d d d dz e r Ψ r EΨ r rz rzejściu do wółrzędnch fercznch r, Θ, ϕ ψ ψr, Θ, ϕ R n r Y l,m Θ,ϕ ψ n,l,m liczb kwantowe: n, l, m... l 0,...,n-,
NAJPROSTSZA CZĄSTECZKA - MOLEKUŁA H Przomnienie: atom wodoru m d d d d d dz e r Ψ r EΨ r rz rzejściu do wółrzędnch fercznch r, Θ, ϕ ψ ψr, Θ, ϕ R n r Y l,m Θ,ϕ ψ n,l,m liczb kwantowe: n, l, m... l 0,...,n-,
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
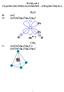 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
2
 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 ZADANIA I PROBLEMY 1). Chlor naturalny jest mieszaniną dwóch izotopów o liczbach masowych 35 i 37, a eksperymentalnie wyznaczona masa atomowa chloru wynosi
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 ZADANIA I PROBLEMY 1). Chlor naturalny jest mieszaniną dwóch izotopów o liczbach masowych 35 i 37, a eksperymentalnie wyznaczona masa atomowa chloru wynosi
Równanie Schrödingera dla elektronu w atomie wodoru Równanie niezależne od czasu w trzech wymiarach współrzędne prostokątne
 Równanie Schrödingera dla elektronu w atomie wodoru Równanie nieależne od casu w trech wymiarach współrędne prostokątne ψ ψ ψ h V m + + x y + ( x, y, ) ψ = E ψ funkcja falowa ψ( x, y, ) Energia potencjalna
Równanie Schrödingera dla elektronu w atomie wodoru Równanie nieależne od casu w trech wymiarach współrędne prostokątne ψ ψ ψ h V m + + x y + ( x, y, ) ψ = E ψ funkcja falowa ψ( x, y, ) Energia potencjalna
Inżynieria Biomedyczna. Wykład XII
 Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oarciu o koncecję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncecja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oarciu o koncecję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncecja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
CHEMIA WARTA POZNANIA
 Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Chemia I Semestr I (1 )
 1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
III Podkarpacki Konkurs Chemiczny 2010/2011. ETAP I r. Godz Zadanie 1
 III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
Wiązania. w świetle teorii kwantów fenomenologicznie
 Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Budowa atomu. Izotopy
 Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Wykład 16: Atomy wieloelektronowe
 Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Zaliczenie przedmiotu: 17.12.2010 21.01.2011. - ocena pozytywna z ćwiczeń jest warunkiem koniecznym przystąpienia do egzaminu
 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. R. M.Silverstein,. X. Webster,
1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. R. M.Silverstein,. X. Webster,
Zaliczenie przedmiotu: ocena pozytywna z ćwiczeń jest warunkiem koniecznym przystąpienia do egzaminu
 Zaliczenie przedmiotu: 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 KLKWIUM
Zaliczenie przedmiotu: 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 KLKWIUM
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Przestrzeń liniowa R n.
 MATEMATYKA IIb - Lcjan Kowalski Prestreń liniowa R n. Element (wektor) prestreni R n będiem onacać [,,, ] Element erow [,, L, ]. Diałania. a) ilocn element pre licbę: b) sma elementów [ c, c, ] c L, c
MATEMATYKA IIb - Lcjan Kowalski Prestreń liniowa R n. Element (wektor) prestreni R n będiem onacać [,,, ] Element erow [,, L, ]. Diałania. a) ilocn element pre licbę: b) sma elementów [ c, c, ] c L, c
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych
 1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Zaliczenie przedmiotu:
 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. J. March, hemia rganiczna:
1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. J. March, hemia rganiczna:
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]
![3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u] 3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]](/thumbs/58/41892324.jpg) 1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
MARATON WIEDZY CHEMIA CZ. II
 MARATON WIEDZY CHEMIA CZ. II 1. Podaj liczbę elektronów, nukleonów, protonów i neuronów zawartych w następujących atomach: a), b) 2. Podaj liczbę elektronów, nukleonów, protonów i neutronów zawartych w
MARATON WIEDZY CHEMIA CZ. II 1. Podaj liczbę elektronów, nukleonów, protonów i neuronów zawartych w następujących atomach: a), b) 2. Podaj liczbę elektronów, nukleonów, protonów i neutronów zawartych w
Nowa Tablica Układu Okresowego Pierwiastków Chemicznych
 Strona 1 z 5 Nowa Tablica Układu Okresowego Pierwiastków Chemicznych Tablica Klasyczna D. Mendelejew Układ Okresowy a budowa atomu NOWA TABLICA 1-168 zgłoś uwagi str. główna Nowy układ okresowy pierwiastków
Strona 1 z 5 Nowa Tablica Układu Okresowego Pierwiastków Chemicznych Tablica Klasyczna D. Mendelejew Układ Okresowy a budowa atomu NOWA TABLICA 1-168 zgłoś uwagi str. główna Nowy układ okresowy pierwiastków
Liczby kwantowe n, l, m l = 0 l =1 l = 2 l = 3
 Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Zad: 1 Spośród poniższych jonów wybierz te, które mają identyczną konfigurację elektronową:
 Zad: 1 Spośród poniższych jonów wybierz te, które mają identyczną konfigurację elektronową: Zad: 2 Zapis 1s 2 2s 2 2p 6 3s 2 3p 2 (K 2 L 8 M 4 ) przedstawia konfigurację elektronową atomu A. argonu. B.
Zad: 1 Spośród poniższych jonów wybierz te, które mają identyczną konfigurację elektronową: Zad: 2 Zapis 1s 2 2s 2 2p 6 3s 2 3p 2 (K 2 L 8 M 4 ) przedstawia konfigurację elektronową atomu A. argonu. B.
TEORIA GRUP - ZASTOSOWANIA
 TOIA GUP - ZASTOSOWANIA Problem oblicania całek Ψdτ Aby ta całka była różna od era to Ψ msi się transformować jak rereentacja ełnosymetrycna lb msi awierać składową ełnosymetrycną. Ψ * Ψ d τ Aby ta całka
TOIA GUP - ZASTOSOWANIA Problem oblicania całek Ψdτ Aby ta całka była różna od era to Ψ msi się transformować jak rereentacja ełnosymetrycna lb msi awierać składową ełnosymetrycną. Ψ * Ψ d τ Aby ta całka
Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne
 Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały
 WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
WYKŁAD 1 Teorie wiązania chemicznego i podstawowe zasady mechaniki kwantowej Zjawiska, które zapowiadały nadejście nowej ery w fizyce i przybliżały sformułowanie praw fizyki kwantowej: promieniowanie katodowe
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
1. Budowa atomu. Układ okresowy pierwiastków chemicznych
 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej (załącznik nr 1 do rozporządzenia, Dz.U. z 2018 r., poz. 467), programie nauczania oraz w części
Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej (załącznik nr 1 do rozporządzenia, Dz.U. z 2018 r., poz. 467), programie nauczania oraz w części
Na rysunku przedstawiono fragment układu okresowego pierwiastków.
 Na rysunku przedstawiono fragment układu okresowego pierwiastków. Zadanie 1 (0 1) W poniższych zdaniach podano informacje o pierwiastkach i ich tlenkach. Które to tlenki? Wybierz je spośród podanych A
Na rysunku przedstawiono fragment układu okresowego pierwiastków. Zadanie 1 (0 1) W poniższych zdaniach podano informacje o pierwiastkach i ich tlenkach. Które to tlenki? Wybierz je spośród podanych A
1. Budowa atomu. Układ okresowy pierwiastków chemicznych
 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej (załącznik nr 1 do rozporządzenia, Dz.U. z 2018 r., poz. 467), programie nauczania oraz w części
Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej (załącznik nr 1 do rozporządzenia, Dz.U. z 2018 r., poz. 467), programie nauczania oraz w części
Postać Jordana macierzy
 Rodiał 8 Postać Jordana macier 8.1. Macier Jordana Niech F = R lub F = C. Macier J r () F r r postaci 1. 1... J r () =..........,.... 1 gdie F, nawam klatką Jordana stopnia r. Ocwiście J 1 () = [. Definicja
Rodiał 8 Postać Jordana macier 8.1. Macier Jordana Niech F = R lub F = C. Macier J r () F r r postaci 1. 1... J r () =..........,.... 1 gdie F, nawam klatką Jordana stopnia r. Ocwiście J 1 () = [. Definicja
Wszystkie arkusze maturalne znajdziesz na stronie: arkuszematuralne.pl
 Egzamin maturalny z chemii - model odpowiedzi poziom rozszerzony Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne
Egzamin maturalny z chemii - model odpowiedzi poziom rozszerzony Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne
Więcej arkuszy znajdziesz na stronie: arkusze.pl
 Egzamin maturalny z chemii - model odpowiedzi poziom rozszerzony Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne
Egzamin maturalny z chemii - model odpowiedzi poziom rozszerzony Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Odpowiedzi niezgodne
Wymagania edukacyjne z chemii Zakres rozszerzony
 Wymagania edukacyjne z chemii Zakres rozszerzony Klasy: 1c, 1d Rok szkolny 2019/2020 Nauczyciel: Aneta Patrzałek Szczegółowe wymagania edukacyjne z chemii na poszczególne stopnie: Wymagania na każdy stopień
Wymagania edukacyjne z chemii Zakres rozszerzony Klasy: 1c, 1d Rok szkolny 2019/2020 Nauczyciel: Aneta Patrzałek Szczegółowe wymagania edukacyjne z chemii na poszczególne stopnie: Wymagania na każdy stopień
Test kompetencji z chemii do liceum. Grupa A.
 Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
SCENARIUSZ LEKCJI prowadzonej pod kątem hospitacji diagnozującej w klasie pierwszej gimnazjum
 Literka.pl Atom i cząsteczka Data dodania: 2010-05-31 11:51:50 Autor: Anna Piwowarczyk Podsumowanie wiadomości o wewnętrznej budowie materii. SCENARIUSZ LEKCJI prowadzonej pod kątem hospitacji diagnozującej
Literka.pl Atom i cząsteczka Data dodania: 2010-05-31 11:51:50 Autor: Anna Piwowarczyk Podsumowanie wiadomości o wewnętrznej budowie materii. SCENARIUSZ LEKCJI prowadzonej pod kątem hospitacji diagnozującej
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe)
 Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu
Konkurs przedmiotowy z chemii dla uczniów dotychczasowych gimnazjów 24 stycznia 2018 r. zawody II stopnia (rejonowe) Kod ucznia Suma punktów Witamy Cię na drugim etapie konkursu chemicznego. Podczas konkursu
Chemia Ogólna wykład 1
 Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
E e l kt k r t o r n o ow o a w a s t s r t u r kt k u t ra r a at a o t m o u
 Elektronowa struktura atomu Anna Pietnoczka BUDOWA ATOMU CZĄSTKA SYMBOL WYSTĘPOWANIE MASA ŁADUNEK ELEKTRYCZNY PROTON p + jądroatomowe około 1 u + 1 NEUTRON n 0 jądroatomowe około 1u Brak ELEKTRON e - powłoki
Elektronowa struktura atomu Anna Pietnoczka BUDOWA ATOMU CZĄSTKA SYMBOL WYSTĘPOWANIE MASA ŁADUNEK ELEKTRYCZNY PROTON p + jądroatomowe około 1 u + 1 NEUTRON n 0 jądroatomowe około 1u Brak ELEKTRON e - powłoki
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450
 Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW. Eliminacje szkolne I stopień
 POUFNE Pieczątka szkoły 9 listopada 2015 r. Imię Czas pracy 60 minut Nazwisko KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje szkolne I stopień Informacje: 1. Przeczytaj uważnie
POUFNE Pieczątka szkoły 9 listopada 2015 r. Imię Czas pracy 60 minut Nazwisko KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2015/2016 Eliminacje szkolne I stopień Informacje: 1. Przeczytaj uważnie
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
