Ćwiczenia 1 Wirtualne Klonowanie. Prowadzący: mgr Anna Pawlik i mgr Maciej Dylewski. Część teoretyczna:
|
|
|
- Amalia Marszałek
- 7 lat temu
- Przeglądów:
Transkrypt
1 Uniwersytet Gdański, Wydział Biologii Biologia i Biologia Medyczna II rok Katedra Biologii Molekularnej Przedmiot: Biologia Molekularna z Biotechnologią =============================================================================================== Cel ćwiczenia: Ćwiczenia 1 Wirtualne Klonowanie Prowadzący: mgr Anna Pawlik i mgr Maciej Dylewski Część teoretyczna: Celem ćwiczenia jest zapoznanie się z planowaniem konstrukcji zrekombinowanego wektora, czyli klonowania genów klonowanie in silico. Do tego celu wykorzystamy program komputerowy Serial Cloner. Ćwiczenia 2-4 będą obejmowały realizację klonowania genu z wykorzystaniem technik inżynierii genetycznej w warunkach laboratoryjnych klonowanie w praktyce, na stole laboratoryjnym. Rysunek 1 Schemat klonowania.
2 Poniżej zostały wymienione etapy klonowania genu wraz z zaznaczeniem, na których ćwiczeniach dany etap będzie wykonywany oraz jaki rodzaj DNA będzie stanowił materiał badawczy podczas ćwiczeń (rys. 1): 1. Wybór i izolacja wektora: wektor puc18. Instrukcja do ćwiczeń: podpunkt I. Realizacja: ćwiczenie 2 2. Przygotowanie wstawki (z wykorzystaniem reakcji PCR)Instrukcja do ćwiczeń: podpunkt II. A. Realizacja: ćwiczenie 3 3. Trawienie restrykcyjne wektora: enzymami BamHI oraz PstI, oraz modyfikacja końców wstawki (enzymem fosforylującym końce DNA). Instrukcja do ćwiczeń: podpunkt II.B/C. Realizacja: ćwiczenie 3 4. Ligacja, czyli reakcja łączenia wektora ze wstawką. Instrukcja do ćwiczeń: podpunkt III. Realizacja: ćwiczenie 4 5. Wprowadzenie otrzymanego konstruktu do komórek gospodarza, czyli transformacja komórek biorcy otrzymanym konstruktem. Instrukcja do ćwiczeń: podpunkt IV. Realizacja: ćwiczenie 4 6. Selekcja transformantów - po ćwiczeniu 4 Do klonowania genów są potrzebne: I. Wektor, zapewniający powielenie obcego DNA w komórkach gospodarza. Stosuje się generalnie dwa rodzaje wektorów: plazmidowe i pochodzenia wirusowego. II. Fragment DNA, który zamierzamy klonować. Najczęściej jest to krótki odcinek DNA powstały po trawieniu odpowiednimi enzymami restrykcyjnymi (posiada lepkie lub tępe końce), bądź produkt PCR stworzony z wykorzystaniem komplementarnych primerów (starterów). III. IV. Ligaza, enzym niezbędny podczas reakcji ligacji, czyli łączenia wektora ze wstawką Gospodarz, zwykle jest to szczep bakteryjny, drożdżowy lub eukariotyczna linia komórkowa o odpowiednio zmodyfikowanym dla celów inżynierii genetycznej i ściśle określonym genotypie niezbędny w procesie transformacji. I. Wektory Plazmidy - koliste zamknięte, autonomicznie replikujące się cząsteczki DNA. Stały się one główną bazą do konstrukcji wektorów plazmidowych. Występują naturalnie w komórkach wielu gatunków bakterii Gramdodatnich i Gram-ujemnych. Przenoszą informację genetyczną, która wielokrotnie pełni ważną funkcje w komórce. Wśród najistotniejszych cech fenotypowych kodowanych przez plazmidowe DNA wymienić można: oporność na antybiotyki, jony metali ciężkich, produkcję antybiotyków, prostych węglowodanów, niektórych toksyn itp. Wektor to autonomicznie replikująca się cząsteczka DNA, która została skonstruowana sztucznie, na bazie naturalnych plazmidów, w celu przenoszenia dodatkowej informacji genetycznej. Ogólnie rzecz biorąc wektory są pochodnymi naturalnie występujących plazmidów. W celu uzyskania dobrego wektora wprowadza się do wektorów plazmidowych pewne modyfikacje: 1. Redukcja masy cząsteczkowej. Im mniejszy wektor tym większa jego pojemność oraz prościej nim manipulować (np. tworzyć mapę restrykcyjną klonowanego DNA) 2. Usunięcie genów warunkujących możliwość transferu zrekombinowanego plazmidu do innych bakterii przekazywanie wektora odbywać się będzie jedynie w pionie (czyli z komórek macierzystych do potomnych). 3. Włączenie w miejscu gdzie ma być wklonowane obce DNA syntetycznego oligonukleotydu z sekwencjami rozpoznawanymi przez wiele enzymów restrykcyjnych miejsce wielokrotnego klonowania (ang. Multiple Cloning Sites MCS). MCS umożliwia bezpośrednie wstawienie fragmentów klonowanego DNA, które
3 powstały przez trawienie jednym z wielu lub (najczęściej) dwoma różnymi enzymami. Oznacza to, że wektor, który zostanie wybrany do klonowania musi w miejscu MCS posiadać miejsca restrykcyjne dla takich samych enzymów, jakimi zostanie potraktowany fragment obcego DNA, który ma być do niego wprowadzony. Dzięki temu łączone za pomocą ligazy końce będą komplementarne. Inne istotne cechy, które powinien posiadać dobry wektor: Obecność jednego lub kilku genów markerowych, służących do wyróżnienia i selekcji transformantów, czyli komórek, które pobrały zrekombinowany wektor (głównie są to geny oporności na antybiotyk, np. ampicylinę, tetracyklinę, chloramfenikol, kanamycynę) Powinien być dobrze scharakteryzowaną pod względem fizycznym i chemicznym cząsteczką, łatwą do oczyszczenia. Posiadać miejsce MCS II. Do konstrukcji wstawki potrzebne są: A)Produkt PCR fragment DNA uzyskany w wyniku reakcji PCR z wykorzystaniem odpowiednich primerów (starterów). Primer jest to krótki, zsyntetyzowany fragment DNA (10-30 par zasad), komplementarny do matrycy DNA, z której chcemy uzyskać produkt PCR Podczas konstrukcji primerów możemy wprowadzić miejsce cięcia dla enzymów restrykcyjnych na końcu 5, aby możliwe było trawienie restrykcyjne, a później klonowanie. Primery powinny spełniać kilka warunków: Długość startera: nt Temperatura topnienia: C Oba startery w parze powinny mieć zbliżoną temperaturę topnienia [T m ] 40< %GC < 60 Sekwencja startera powinna być pozbawiona powtórzeń (ang. runs), np. AAAA Starter nie powinien mieć powtórzeń G/C na końcach 5 i 3, ale dobrze jeśli występuje jeden nt C lub G Przynajmniej jeden starter powinien być specyficzny dla fragmentu (fragmentów) DNA, który może zostać powielony B) Enzymy restrykcyjne - Enzymy restrykcyjne (zwane także restryktazami, endonukleazami restrykcyjnymi) są enzymami izolowanymi z bakterii, zdolnymi do rozpoznawania specyficznych sekwencji w DNA i do
4 przecinania dwuniciowej cząsteczki DNA. W przypadku cięcia enzymami restrykcyjnymi powstają tępe i lepkie końce, pozwalające na wklonowanie genu w odpowiedniej orientacji. C) Podstawowe enzymy modyfikujące DNA przydatne do klonowania: 1) Alkaliczna fosfataza: Katalizuje usuwanie grup 5 fosforanowych z DNA, RNA oraz tri fosforanów. Zastosowanie: - defosforylacja końców DNA przy przygotowywaniu wektorów do klonowania (fragmenty pozbawione grup fosforanowych na końcach nie mogą zamykać się w kółko w reakcji ligacji) - defosforylacja DNA lub RNA przed znakowaniem końców przy użyciu kinazy polinukleotydowej T4 - defosforylacja białek 2) Fragment Klenowa polimerazy DNA I: Fragment Klenowa jest produktem proteolizy polimerazy DNA I z E.coli, który ma aktywność polimeryzacji (3' 5 ) i aktywność egzonukleolityczną 3' 5, ale stracił aktywność egzonukleolityczną 5' 3. Dzięki temu zachował wierność polimeryzacji holoenzymu nie degradując końców 5. Zastosowanie: - fosforylacja - wypełnianie lepkich końców (jednoniciowe odcinki wysunięte w kierunku 5, nić3 cofnięta) - sekwencjonowanie metodą Sangera - synteza drugiej nici cdna III. Ligacja i ligazy Ligazy DNA są klasą enzymów modyfikujących DNA. W organizmie żywym pełnią kluczową rolę - bez nich wszelkie procesy genetyczne nie byłyby możliwe. Ligazy DNA są enzymami ligującymi, co oznacza, że potrafią tworzyć wiązania chemiczne pomiędzy dwoma fragmentami. Funkcją ligaz DNA jest łączenie przerw w DNA, co ma miejsce przy wszystkich procesach angażujących syntezę nowych nici DNA (replikacja, naprawa DNA) czy wycinanie i wstawianie ich fragmentów (rekombinacja genetyczna). Działanie ligaz opiera się na prostej reakcji chemicznej, która, będąc endoenergetyczną, wymaga do prawidłowego przebiegu obecności substratu energetycznego - ATP. Ligacja proces łączenia dwóch fragmentów lub końców nici DNA za pomocą ligazy. Proces ligacji wymaga energii w postaci ATP lub NAD (w zależności od ligazy). Rysunek 2 Reakcja ligacji
5 IV. Gospodarz Transformacja proces pobierania dostępnego DNA (np. zrekombinowany wektor uzyskany podczas klonowania) ze środowiska przez komórki gospodarza Escherichia coli. Zagadnienia do samodzielnego przygotowania: 1. Rodzaje wektorów do klonowania 2. Wektory wahadłowe 3. Wektory wysoko- i niskokopijne oraz ich zastosowanie Literatura 1. J. Kur Podstawy inżynierii genetycznej. Teoria, ćwiczenia, testy. Wydawnictwo PG, B. Zalewska-Piątek, M. Olszewski, R. Piątek, S. Milewski, J. Kur Biologia molekularna. Ćwiczenia laboratoryjne. Wydawnictwo PG, Część praktyczna W części praktycznej wykorzystywać będziemy darmowy program SerialCloner, który posiada m. in. funkcje wirtualnego klonowania fragmentów DNA, projektowania starterów do reakcji PCR, czy sprawdzenia homologii dwóch sekwencji DNA. Wykorzystanie programu Serial Cloner podczas kolejnych etapów klonowania: 1. Wybór i izolacja wektora (wektor puc18) wizualizacja sekwencji, MCS oraz dostępnych genów markerowych 2. Przygotowanie wstawki pochodzącej z plazmidu pcb104 symulacja przebiegu reakcji PCR 3. Trawienie restrykcyjne wektora (enzymami BamHI oraz PstI) oraz fosforylacja końców wstawki (enzymami modyfikującymi DNA) dobór enzymów restrykcyjnych i przedstawienie graficzne powstałych fragmentów 4. Ligacja czyli reakcja łączenia wektora ze wstawką wizualizacja powstałego konstruktu (zrekombinowanego wektora)
6 Wprowadzenie do programu: Widok okna programu. Podstawowe narzędzia, które będziemy wykorzystywać w pracy z tym programem na zajęciach: 1 otwiera nową sekwencję do obróbki 2 otwiera sekwencję DNA zapisaną na dysku, nad którą wcześniej pracowaliśmy 3 zapisuje zmienioną sekwencję DNA 4 pokazuje w sposób graficzny otwartą sekwencji DNA 5 pokazuje szczegóły wczytanej sekwencji z miejscami restrykcyjnymi 6 wskazuje ilość miejsc cięcia dla danego enzymu restrykcyjnego w wybranej sekwencji DNA 7 pozwala przeprowadzić analizę po użyciu enzymów restrykcyjnych na żelu agarozwym 8 zaznacza miejsca z genami, które warunkują specyficzne cechy wektora 9 pozwala odnaleźć odpowiednie miejsca na wskazanej sekwencji, np. miejsca restrykcyjne 10 pozwala na przeprowadzenie wirtualnej ligacji fragmentów DNA 11 pozwala na projektowanie primerów i przeprowadzenie wirtualnej reakcji PCR 12 pozwala na sprawdzenie miejsc homologicznych pomiędzy sekwencjami Wprowadzanie sekwencji do programu: file open wybór pliku (plazmid pcb104) w celu wizualizacji plazmidu wybierz opcję Graphic Map, a następnie wybierz opcję Circularize
7 Po wczytaniu danej sekwencji DNA do programu, możemy określić jej wielkość, wskazać miejsce inicjacji replikacji, czy sprawdzić występujące tu markery selekcyjne, np. geny warunkujące oporności na antybiotyki. Projektowanie primerów/ reakcja PCR: Aby uzyskać produkt po reakcji PCR i kolejno wklonować go do wektora, konieczne jest zaprojektowanie primerów komplementarnych do interesującej nas sekwencji DNA (matrycy DNA), którą chcemy powielić. Podczas konstrukcji wprowadzamy miejsce cięcia dla enzymów restrykcyjnych na końcu 5, aby możliwe było trawienie restrykcyjne, a następnie reakcja ligacji. Wprowadzamy sekwencję, do której chcemy zaprojektować startery, i zaznaczamy fragment sekwencji. Sprawdzamy czy starter ma odpowiednią długość, ilość par GC, temperaturę topnienia.
8 Za pomocą tego programu możemy również przeprowadzić wirtualną reakcję PCR z wykorzystaniem ówcześnie zaprojektowanych pimerów. Wczytujemy sekwencję matrycową (opcja u dołu okna Run a PCR ), czyli tę samą do której projektowaliśmy primery, i otrzymujemy produkt PCR, który później będziemy wykorzystać do reakcji ligacji. Etapy: wybierz opcję PCR wstaw sekwencje rozpoznawane i cięte przez oba enzymy restrykcyjne na końcach 5 projektowanych primerów w miejscu oligo tail not indentical to the target sequence, oraz sekwencje pochodzące z plazmidu pcb104 w miejscu segment identical to the target sequence. Po wyborze sekwencji pochodzącej z plazmidu pcb104 należy zaznaczyć opcję use as PCR forward primer oraz use as PCR reverse primer wstaw matrycę select target DNA i wybierz pcb104 wciśnij Run PCR Wirtualne ligowanie dwóch fragmentów DNA: Program ten pozwala na przeprowadzenie wirtualnej reakcji ligacji dwóch fragmentów DNA: wektora oraz wstawki (fragmentu DNA po reakcji PCR), które zostały potrawione tymi samymi enzymami restrykcyjnymi. Wprowadzamy wcześniej przygotowaną i sprawdzoną sekwencję DNA do programu SerialCloner. Zaznaczamy wybrane przez nas enzymy restrykcyjne i uzyskujemy informację na temat rodzaju cięcia restrykcyjnego: końce tępe, lepkie oraz wielkości otrzymanego fragmentu DNA. Tak uzyskane fragmenty DNA ligujemy, a uzyskany konstrukt zapisujemy poniżej mapa powstałego konstruktu oraz dwóch plazmidów wykorzystanych do jego stworzenia. Etapy ligacji: po pocięciu enzymami restrykcyjnymi plazmidu puc19 oraz wstawki z plazmidu pcb104 wybieramy opcję Construct, a następnie wstawiamy otwartą sekwencję nukleotydową plazmidu puc19 w Select DNA 1 oraz sekwencję nukleotydową wstawki w Select DNA2 reakcję wirtualnej ligacji przeprowadzamy poprzez naciśnięcie opcji LIGATE
9 Plazmind pcb104 zawierający gen, który zostanie wklonowany w MCS plazmidu puc19
10 Plazmid puc19 zawierający fragment genu lacz kodujący N-końcowy fragment β-galaktozydazy
11 Konstruk uzyskany w wyniku molekularnego klonowania
Ćwiczenia 1 Wirtualne Klonowanie Prowadzący: mgr inż. Joanna Tymeck-Mulik i mgr Lidia Gaffke. Część teoretyczna:
 Uniwersytet Gdański, Wydział Biologii Katedra Biologii Molekularnej Przedmiot: Biologia Molekularna z Biotechnologią Biologia II rok ===============================================================================================
Uniwersytet Gdański, Wydział Biologii Katedra Biologii Molekularnej Przedmiot: Biologia Molekularna z Biotechnologią Biologia II rok ===============================================================================================
Biologia Molekularna z Biotechnologią ===============================================================================================
 Uniwersytet Gdański, Wydział Biologii Biologia i Biologia Medyczna II rok Katedra Genetyki Molekularnej Bakterii Katedra Biologii i Genetyki Medycznej Przedmiot: Katedra Biologii Molekularnej Biologia
Uniwersytet Gdański, Wydział Biologii Biologia i Biologia Medyczna II rok Katedra Genetyki Molekularnej Bakterii Katedra Biologii i Genetyki Medycznej Przedmiot: Katedra Biologii Molekularnej Biologia
Klonowanie molekularne Kurs doskonalący. Zakład Geriatrii i Gerontologii CMKP
 Klonowanie molekularne Kurs doskonalący Zakład Geriatrii i Gerontologii CMKP Etapy klonowania molekularnego 1. Wybór wektora i organizmu gospodarza Po co klonuję (do namnożenia DNA [czy ma być metylowane
Klonowanie molekularne Kurs doskonalący Zakład Geriatrii i Gerontologii CMKP Etapy klonowania molekularnego 1. Wybór wektora i organizmu gospodarza Po co klonuję (do namnożenia DNA [czy ma być metylowane
KLONOWANIE DNA REKOMBINACJA DNA WEKTORY
 KLONOWANIE DNA Klonowanie DNA jest techniką powielania fragmentów DNA DNA można powielać w komórkach (replikacja in vivo) W probówce (PCR) Do przeniesienia fragmentu DNA do komórek gospodarza potrzebny
KLONOWANIE DNA Klonowanie DNA jest techniką powielania fragmentów DNA DNA można powielać w komórkach (replikacja in vivo) W probówce (PCR) Do przeniesienia fragmentu DNA do komórek gospodarza potrzebny
Najważniejsze z nich to: enzymy restrykcyjne wektory DNA inne enzymy np. ligazy, fosfatazy, polimerazy, nukleazy
 Aby manipulować genami niezbędne są odpowiednie narzędzia molekularne, które pozwalają uzyskać tzw. zrekombinowane DNA (umożliwiają rekombinację materiału genetycznego in vitro czyli w próbówce) Najważniejsze
Aby manipulować genami niezbędne są odpowiednie narzędzia molekularne, które pozwalają uzyskać tzw. zrekombinowane DNA (umożliwiają rekombinację materiału genetycznego in vitro czyli w próbówce) Najważniejsze
Inżynieria Genetyczna ćw. 3
 Materiały do ćwiczeń z przedmiotu Genetyka z inżynierią genetyczną D - blok Inżynieria Genetyczna ćw. 3 Instytut Genetyki i Biotechnologii, Wydział Biologii, Uniwersytet Warszawski, rok akad. 2018/2019
Materiały do ćwiczeń z przedmiotu Genetyka z inżynierią genetyczną D - blok Inżynieria Genetyczna ćw. 3 Instytut Genetyki i Biotechnologii, Wydział Biologii, Uniwersytet Warszawski, rok akad. 2018/2019
Najważniejsze z nich to: enzymy restrykcyjne wektory DNA inne enzymy np. ligazy, fosfatazy, polimerazy, nukleazy
 Aby manipulować genami niezbędne są odpowiednie narzędzia molekularne, które pozwalają uzyskać tzw. zrekombinowane DNA (umożliwiają rekombinację materiału genetycznego in vitro czyli w próbówce) Najważniejsze
Aby manipulować genami niezbędne są odpowiednie narzędzia molekularne, które pozwalają uzyskać tzw. zrekombinowane DNA (umożliwiają rekombinację materiału genetycznego in vitro czyli w próbówce) Najważniejsze
Hybrydyzacja kwasów nukleinowych
 Hybrydyzacja kwasów nukleinowych Jaka jest lokalizacja tego genu na chromosomie? Jakie jest jego sąsiedztwo? Hybrydyzacja - powstawanie stabilnych struktur dwuniciowych z cząsteczek jednoniciowych o komplementarnych
Hybrydyzacja kwasów nukleinowych Jaka jest lokalizacja tego genu na chromosomie? Jakie jest jego sąsiedztwo? Hybrydyzacja - powstawanie stabilnych struktur dwuniciowych z cząsteczek jednoniciowych o komplementarnych
KLONOWANIE DNA REKOMBINACJA DNA WEKTORY
 KLONOWANIE DNA Klonowanie DNA jest techniką powielania fragmentów DNA DNA można powielać w komórkach (replikacja in vivo) W probówce (PCR) Do przeniesienia fragmentu DNA do komórek gospodarza potrzebny
KLONOWANIE DNA Klonowanie DNA jest techniką powielania fragmentów DNA DNA można powielać w komórkach (replikacja in vivo) W probówce (PCR) Do przeniesienia fragmentu DNA do komórek gospodarza potrzebny
Transformacja pośrednia składa się z trzech etapów:
 Transformacja pośrednia składa się z trzech etapów: 1. Otrzymanie pożądanego odcinka DNA z materiału genetycznego dawcy 2. Wprowadzenie obcego DNA do wektora 3. Wprowadzenie wektora, niosącego w sobie
Transformacja pośrednia składa się z trzech etapów: 1. Otrzymanie pożądanego odcinka DNA z materiału genetycznego dawcy 2. Wprowadzenie obcego DNA do wektora 3. Wprowadzenie wektora, niosącego w sobie
Najważniejsze z nich to: enzymy restrykcyjne wektory DNA inne enzymy np. ligazy, fosfatazy, polimerazy, kinazy, nukleazy
 Aby manipulować genami niezbędne są odpowiednie narzędzia molekularne, które pozwalają uzyskać tzw. zrekombinowane DNA (umożliwiają rekombinację materiału genetycznego in vitro czyli w próbówce) Najważniejsze
Aby manipulować genami niezbędne są odpowiednie narzędzia molekularne, które pozwalają uzyskać tzw. zrekombinowane DNA (umożliwiają rekombinację materiału genetycznego in vitro czyli w próbówce) Najważniejsze
Hybrydyzacja kwasów nukleinowych
 Hybrydyzacja kwasów nukleinowych Jaka jest lokalizacja genu na chromosomie? Jakie jest jego sąsiedztwo? Hybrydyzacja - powstawanie stabilnych struktur dwuniciowych z cząsteczek jednoniciowych o komplementarnych
Hybrydyzacja kwasów nukleinowych Jaka jest lokalizacja genu na chromosomie? Jakie jest jego sąsiedztwo? Hybrydyzacja - powstawanie stabilnych struktur dwuniciowych z cząsteczek jednoniciowych o komplementarnych
Definicje. Białka rekombinowane (ang. recombinant proteins, r-proteins) Ukierunkowana mutageneza (ang. site-directed/site-specific mutagenesis)
 Definicje Białka rekombinowane (ang. recombinant proteins, r-proteins) Białka, które powstały w żywych organizmach (lub liniach komórkowych) w wyniku ekspresji rekombinowanego DNA. Rekombinowany DNA jest
Definicje Białka rekombinowane (ang. recombinant proteins, r-proteins) Białka, które powstały w żywych organizmach (lub liniach komórkowych) w wyniku ekspresji rekombinowanego DNA. Rekombinowany DNA jest
WEKTORY WAHADŁOWE ENZYMY W KLONOWANIU POLIMERAZY
 WEKTORY WAHADŁOWE Replikują się w organizmach prokariotycznych i eukariotycznych (również ssaków) Złożone z fragmentów DNA charakterystycznych dla Procaryota i Eukaryota - pierwsza część zawiera ori i
WEKTORY WAHADŁOWE Replikują się w organizmach prokariotycznych i eukariotycznych (również ssaków) Złożone z fragmentów DNA charakterystycznych dla Procaryota i Eukaryota - pierwsza część zawiera ori i
Ćwiczenie 5 Klonowanie DNA w wektorach plazmidowych
 Ćwiczenie 5 Klonowanie DNA w wektorach plazmidowych Celem ćwiczenia jest sklonowanie fragmentu DNA (powielonego techniką PCR i wyizolowanego z żelu agarozowego na poprzednich zajęciach) do wektora plazmidowego
Ćwiczenie 5 Klonowanie DNA w wektorach plazmidowych Celem ćwiczenia jest sklonowanie fragmentu DNA (powielonego techniką PCR i wyizolowanego z żelu agarozowego na poprzednich zajęciach) do wektora plazmidowego
2. Enzymy pozwalające na manipulację DNA a. Polimerazy DNA b. Nukleazy c. Ligazy
 Metody analizy DNA 1. Budowa DNA. 2. Enzymy pozwalające na manipulację DNA a. Polimerazy DNA b. Nukleazy c. Ligazy 3. Klonowanie in vivo a. w bakteriach, wektory plazmidowe b. w fagach, kosmidy c. w drożdżach,
Metody analizy DNA 1. Budowa DNA. 2. Enzymy pozwalające na manipulację DNA a. Polimerazy DNA b. Nukleazy c. Ligazy 3. Klonowanie in vivo a. w bakteriach, wektory plazmidowe b. w fagach, kosmidy c. w drożdżach,
SYLABUS. Wydział Biologiczno-Rolniczy. Katedra Biochemii i Biologii Komórki
 SYLABUS 1.1. PODSTAWOWE INFORMACJE O PRZEDMIOCIE/MODULE Nazwa przedmiotu/ modułu Biologia molekularna Kod przedmiotu/ modułu* Wydział (nazwa jednostki prowadzącej kierunek) Nazwa jednostki realizującej
SYLABUS 1.1. PODSTAWOWE INFORMACJE O PRZEDMIOCIE/MODULE Nazwa przedmiotu/ modułu Biologia molekularna Kod przedmiotu/ modułu* Wydział (nazwa jednostki prowadzącej kierunek) Nazwa jednostki realizującej
Powodzenie reakcji PCR wymaga właściwego doboru szeregu parametrów:
 Powodzenie reakcji PCR wymaga właściwego doboru szeregu parametrów: dobór warunków samej reakcji PCR (temperatury, czas trwania cykli, ilości cykli itp.) dobór odpowiednich starterów do reakcji amplifikacji
Powodzenie reakcji PCR wymaga właściwego doboru szeregu parametrów: dobór warunków samej reakcji PCR (temperatury, czas trwania cykli, ilości cykli itp.) dobór odpowiednich starterów do reakcji amplifikacji
Ligazy. Zastosowanie ligazy w inżynierii genetycznej:
 Ligazy Katalizują tworzenie wiązań fosfodiestrowych między sąsiednimi grupami 3 OH i 5 PO 4 w kwasach nukleinowych DNA lub RNA. W reakcji tworzą się wysokoenergetyczne pośredniki z udziałem NAD + lub ATP
Ligazy Katalizują tworzenie wiązań fosfodiestrowych między sąsiednimi grupami 3 OH i 5 PO 4 w kwasach nukleinowych DNA lub RNA. W reakcji tworzą się wysokoenergetyczne pośredniki z udziałem NAD + lub ATP
Inżynieria genetyczna
 Inżynieria genetyczna i technologia rekombinowanego DNA Dr n. biol. Urszula Wasik Zakład Biologii Medycznej Inżynieria genetyczna świadoma, celowa, kontrolowana ingerencja w materiał genetyczny organizmów
Inżynieria genetyczna i technologia rekombinowanego DNA Dr n. biol. Urszula Wasik Zakład Biologii Medycznej Inżynieria genetyczna świadoma, celowa, kontrolowana ingerencja w materiał genetyczny organizmów
Jaka jest lokalizacja genu na chromosomie? Jakie jest jego sąsiedztwo?
 Jaka jest lokalizacja genu na chromosomie? Jakie jest jego sąsiedztwo? Hybrydyzacja - powstawanie stabilnych struktur dwuniciowych z cząsteczek jednoniciowych o komplementarnych sekwencjach nukleotydów
Jaka jest lokalizacja genu na chromosomie? Jakie jest jego sąsiedztwo? Hybrydyzacja - powstawanie stabilnych struktur dwuniciowych z cząsteczek jednoniciowych o komplementarnych sekwencjach nukleotydów
POLIMERAZY DNA- PROCARYOTA
 Enzymy DNA-zależne, katalizujące syntezę DNA wykazują aktywność polimerazy zawsze w kierunku 5 3 wykazują aktywność polimerazy zawsze wobec jednoniciowej cząsteczki DNA do utworzenia kompleksu z ssdna
Enzymy DNA-zależne, katalizujące syntezę DNA wykazują aktywność polimerazy zawsze w kierunku 5 3 wykazują aktywność polimerazy zawsze wobec jednoniciowej cząsteczki DNA do utworzenia kompleksu z ssdna
2015-11-18. DNA i RNA ENZYMY MODYFIKUJĄCE KOŃCE CZĄSTECZEK. DNA i RNA. DNA i RNA
 Fosfataza alkaliczna CIP Calf Intestine Phosphatase- pochodzenie: jelito cielęce BAP Bacterial Alcaline Phosphatase- pochodzenie: E. coli SAP Shrimp Alcaline Phosphatase- pochodzenie: krewetki Pandalus
Fosfataza alkaliczna CIP Calf Intestine Phosphatase- pochodzenie: jelito cielęce BAP Bacterial Alcaline Phosphatase- pochodzenie: E. coli SAP Shrimp Alcaline Phosphatase- pochodzenie: krewetki Pandalus
Ćwiczenie 3 PCR i trawienie DNA enzymami restrykcyjnymi
 Uniwersytet Gdański, Wydział Biologii Katedra Genetyki Molekularnej Bakterii Katedra Biologii i Genetyki Medycznej Katedra Biologii Molekularnej Biologia i Biologia Medyczna II rok Przedmiot: Biologia
Uniwersytet Gdański, Wydział Biologii Katedra Genetyki Molekularnej Bakterii Katedra Biologii i Genetyki Medycznej Katedra Biologii Molekularnej Biologia i Biologia Medyczna II rok Przedmiot: Biologia
Mapowanie fizyczne genomów -konstrukcja map wyskalowanych w jednostkach fizycznych -najdokładniejszą mapą fizyczną genomu, o największej
 Mapowanie fizyczne genomów -konstrukcja map wyskalowanych w jednostkach fizycznych -najdokładniejszą mapą fizyczną genomu, o największej rozdzielczości jest sekwencja nukleotydowa -mapowanie fizyczne genomu
Mapowanie fizyczne genomów -konstrukcja map wyskalowanych w jednostkach fizycznych -najdokładniejszą mapą fizyczną genomu, o największej rozdzielczości jest sekwencja nukleotydowa -mapowanie fizyczne genomu
Prokariota i Eukariota
 Prokariota i Eukariota W komórkach organizmów żywych ilość DNA jest zazwyczaj stała i charakterystyczna dla danego gatunku. ILOŚĆ DNA PRZYPADAJĄCA NA APARAT GENETYCZNY WZRASTA WRAZ Z BARDZIEJ FILOGENETYCZNIE
Prokariota i Eukariota W komórkach organizmów żywych ilość DNA jest zazwyczaj stała i charakterystyczna dla danego gatunku. ILOŚĆ DNA PRZYPADAJĄCA NA APARAT GENETYCZNY WZRASTA WRAZ Z BARDZIEJ FILOGENETYCZNIE
Mieszanina trójfosforanów deoksyrybonukleotydów (dntp: datp, dgtp, dctp, dttp) Bufor reakcyjny zapewniający odpowiednie warunki reakcji
 Uniwersytet Gdański, Wydział Biologii Biologia i Biologia medyczna II rok Katedra Biologii Molekularnej Przedmiot: Biologia Molekularna z Biotechnologią =================================================================
Uniwersytet Gdański, Wydział Biologii Biologia i Biologia medyczna II rok Katedra Biologii Molekularnej Przedmiot: Biologia Molekularna z Biotechnologią =================================================================
Nowoczesne systemy ekspresji genów
 Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
Nowoczesne systemy ekspresji genów Ekspresja genów w organizmach żywych GEN - pojęcia podstawowe promotor sekwencja kodująca RNA terminator gen Gen - odcinek DNA zawierający zakodowaną informację wystarczającą
PCR - ang. polymerase chain reaction
 PCR - ang. polymerase chain reaction łańcuchowa (cykliczna) reakcja polimerazy Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
PCR - ang. polymerase chain reaction łańcuchowa (cykliczna) reakcja polimerazy Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
Dominika Stelmach Gr. 10B2
 Dominika Stelmach Gr. 10B2 Czym jest DNA? Wielkocząsteczkowy organiczny związek chemiczny z grupy kwasów nukleinowych Zawiera kwas deoksyrybonukleoinowy U organizmów eukariotycznych zlokalizowany w jądrze
Dominika Stelmach Gr. 10B2 Czym jest DNA? Wielkocząsteczkowy organiczny związek chemiczny z grupy kwasów nukleinowych Zawiera kwas deoksyrybonukleoinowy U organizmów eukariotycznych zlokalizowany w jądrze
Metody odczytu kolejności nukleotydów - sekwencjonowania DNA
 Metody odczytu kolejności nukleotydów - sekwencjonowania DNA 1. Metoda chemicznej degradacji DNA (metoda Maxama i Gilberta 1977) 2. Metoda terminacji syntezy łańcucha DNA - klasyczna metoda Sangera (Sanger
Metody odczytu kolejności nukleotydów - sekwencjonowania DNA 1. Metoda chemicznej degradacji DNA (metoda Maxama i Gilberta 1977) 2. Metoda terminacji syntezy łańcucha DNA - klasyczna metoda Sangera (Sanger
O trawieniu restrykcyjnym
 O trawieniu restrykcyjnym Enzymy II klasy, Mg 2+, dsdna z rozpoznawaną sekwencją, tępe, lepkie (kohezyjne) końce, warunki reakcji bufor o różnym stężeniu NaCl i określonym ph BSA -stabilizator 37 o C /lub
O trawieniu restrykcyjnym Enzymy II klasy, Mg 2+, dsdna z rozpoznawaną sekwencją, tępe, lepkie (kohezyjne) końce, warunki reakcji bufor o różnym stężeniu NaCl i określonym ph BSA -stabilizator 37 o C /lub
Inżynieria Genetyczna ćw. 1
 Materiały do ćwiczeń z przedmiotu Genetyka z inżynierią genetyczną D - blok Inżynieria Genetyczna ćw. 1 Instytut Genetyki i Biotechnologii, Wydział Biologii, Uniwersytet Warszawski, rok akad. 2018/2019
Materiały do ćwiczeń z przedmiotu Genetyka z inżynierią genetyczną D - blok Inżynieria Genetyczna ćw. 1 Instytut Genetyki i Biotechnologii, Wydział Biologii, Uniwersytet Warszawski, rok akad. 2018/2019
SYLABUS. Wydział Biologiczno-Rolniczy. Katedra Biochemii i Biologii Komórki
 SYLABUS 1.1. PODSTAWOWE INFORMACJE O PRZEDMIOCIE/MODULE Nazwa przedmiotu/ modułu Biologia molekularna z elementami inżynierii genetycznej Kod przedmiotu/ modułu* Wydział (nazwa jednostki prowadzącej kierunek)
SYLABUS 1.1. PODSTAWOWE INFORMACJE O PRZEDMIOCIE/MODULE Nazwa przedmiotu/ modułu Biologia molekularna z elementami inżynierii genetycznej Kod przedmiotu/ modułu* Wydział (nazwa jednostki prowadzącej kierunek)
S YL AB US MODUŁ U ( PRZEDMIOTU) I nforma c j e ogólne
 Załącznik Nr 3 do Uchwały Senatu PUM 14/2012 S YL AB US MODUŁ U ( PRZEDMIOTU) I nforma c j e ogólne Kod modułu Rodzaj modułu Wydział PUM Kierunek studiów Specjalność Poziom studiów Nazwa modułu INŻYNIERIA
Załącznik Nr 3 do Uchwały Senatu PUM 14/2012 S YL AB US MODUŁ U ( PRZEDMIOTU) I nforma c j e ogólne Kod modułu Rodzaj modułu Wydział PUM Kierunek studiów Specjalność Poziom studiów Nazwa modułu INŻYNIERIA
Techniki molekularne w mikrobiologii SYLABUS A. Informacje ogólne
 Techniki molekularne w mikrobiologii A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Rodzaj Rok studiów
Techniki molekularne w mikrobiologii A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Rodzaj Rok studiów
Metody inżynierii genetycznej SYLABUS A. Informacje ogólne
 Metody inżynierii genetycznej A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Rodzaj Rok studiów /semestr
Metody inżynierii genetycznej A. Informacje ogólne Elementy sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Rodzaj Rok studiów /semestr
Rok akademicki: 2014/2015 Kod: EIB-2-206-BN-s Punkty ECTS: 3. Kierunek: Inżynieria Biomedyczna Specjalność: Bionanotechnologie
 Nazwa modułu: Genetyka molekularna Rok akademicki: 2014/2015 Kod: EIB-2-206-BN-s Punkty ECTS: 3 Wydział: Elektrotechniki, Automatyki, Informatyki i Inżynierii Biomedycznej Kierunek: Inżynieria Biomedyczna
Nazwa modułu: Genetyka molekularna Rok akademicki: 2014/2015 Kod: EIB-2-206-BN-s Punkty ECTS: 3 Wydział: Elektrotechniki, Automatyki, Informatyki i Inżynierii Biomedycznej Kierunek: Inżynieria Biomedyczna
Inżynieria genetyczna- 6 ECTS. Inżynieria genetyczna. Podstawowe pojęcia Część II Klonowanie ekspresyjne Od genu do białka
 Inżynieria genetyczna- 6 ECTS Część I Badanie ekspresji genów Podstawy klonowania i różnicowania transformantów Kolokwium (14pkt) Część II Klonowanie ekspresyjne Od genu do białka Kolokwium (26pkt) EGZAMIN
Inżynieria genetyczna- 6 ECTS Część I Badanie ekspresji genów Podstawy klonowania i różnicowania transformantów Kolokwium (14pkt) Część II Klonowanie ekspresyjne Od genu do białka Kolokwium (26pkt) EGZAMIN
Biotechnologia i inżynieria genetyczna
 Wersja A Test podsumowujący rozdział II i inżynieria genetyczna..................................... Imię i nazwisko.............................. Data Klasa oniższy test składa się z 16 zadań. rzy każdym
Wersja A Test podsumowujący rozdział II i inżynieria genetyczna..................................... Imię i nazwisko.............................. Data Klasa oniższy test składa się z 16 zadań. rzy każdym
POLIMERAZY DNA- PROCARYOTA
 Enzymy DNA-zależne, katalizujące syntezę DNA wykazują aktywność polimerazy zawsze w kierunku 5 3 wykazują aktywność polimerazy zawsze wobec jednoniciowej cząsteczki DNA do utworzenia kompleksu z ssdna
Enzymy DNA-zależne, katalizujące syntezę DNA wykazują aktywność polimerazy zawsze w kierunku 5 3 wykazują aktywność polimerazy zawsze wobec jednoniciowej cząsteczki DNA do utworzenia kompleksu z ssdna
Konstrukcja wektora plazmidowego DNA do klonowania genów i/lub wektora plazmidowego do sekrecji w bakteriach mlekowych
 Konstrukcja wektora plazmidowego DNA do klonowania genów i/lub wektora plazmidowego do sekrecji w bakteriach mlekowych Łukasz Tranda Promotor: doc. dr hab. Jacek Bardowski, IBB Promotor: dr hab. Edward
Konstrukcja wektora plazmidowego DNA do klonowania genów i/lub wektora plazmidowego do sekrecji w bakteriach mlekowych Łukasz Tranda Promotor: doc. dr hab. Jacek Bardowski, IBB Promotor: dr hab. Edward
PCR - ang. polymerase chain reaction
 PCR - ang. polymerase chain reaction łańcuchowa (cykliczna) reakcja polimerazy Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
PCR - ang. polymerase chain reaction łańcuchowa (cykliczna) reakcja polimerazy Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
Klonowanie i transgeneza. dr n.med. Katarzyna Wicher
 Klonowanie i transgeneza dr n.med. Katarzyna Wicher Klonowanie proces tworzenia idealnej kopii z oryginału oznacza powstawanie lub otrzymywanie genetycznie identycznych: cząsteczek DNA komórek organizmów
Klonowanie i transgeneza dr n.med. Katarzyna Wicher Klonowanie proces tworzenia idealnej kopii z oryginału oznacza powstawanie lub otrzymywanie genetycznie identycznych: cząsteczek DNA komórek organizmów
PCR - ang. polymerase chain reaction
 PCR - ang. polymerase chain reaction łańcuchowa (cykliczna) reakcja polimerazy Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
PCR - ang. polymerase chain reaction łańcuchowa (cykliczna) reakcja polimerazy Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
Ćwiczenie 7 Klonowanie DNA w wektorach plazmidowych
 Ćwiczenie 7 Klonowanie DNA w wektorach plazmidowych Celem ćwiczenia jest sklonowanie fragmentu DNA (powielonego techniką PCR i wyizolowanego z żelu agarozowego na poprzednich zajęciach) do wektora plazmidowego
Ćwiczenie 7 Klonowanie DNA w wektorach plazmidowych Celem ćwiczenia jest sklonowanie fragmentu DNA (powielonego techniką PCR i wyizolowanego z żelu agarozowego na poprzednich zajęciach) do wektora plazmidowego
Replikacja DNA. Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego.
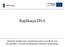 Replikacja DNA Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Replikacja DNA jest bardzo złożonym procesem, w którym biorą udział setki
Replikacja DNA Materiały dydaktyczne współfinansowane ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego. Replikacja DNA jest bardzo złożonym procesem, w którym biorą udział setki
Inżynieria Genetyczna ćw. 2
 Materiały do ćwiczeń z przedmiotu Genetyka z inżynierią genetyczną D - blok Inżynieria Genetyczna ćw. 2 Instytut Genetyki i Biotechnologii, Wydział Biologii, Uniwersytet Warszawski, rok akad. 2018/2019
Materiały do ćwiczeń z przedmiotu Genetyka z inżynierią genetyczną D - blok Inżynieria Genetyczna ćw. 2 Instytut Genetyki i Biotechnologii, Wydział Biologii, Uniwersytet Warszawski, rok akad. 2018/2019
REPLIKACJA, NAPRAWA i REKOMBINACJA DNA
 REPLIKACJA, NAPRAWA i REKOMBINACJA DNA 1) Replikacja DNA 2) Replikacja całych chromosomów 3) Replikacja telomerów 4) Naprawa DNA przy jego syntezie 5) Naprawa DNA poza jego syntezą 6) Naprawa DNA system
REPLIKACJA, NAPRAWA i REKOMBINACJA DNA 1) Replikacja DNA 2) Replikacja całych chromosomów 3) Replikacja telomerów 4) Naprawa DNA przy jego syntezie 5) Naprawa DNA poza jego syntezą 6) Naprawa DNA system
Podstawy inżynierii genetycznej
 Metody bioinformatyki Podstawy inżynierii genetycznej prof. dr hab. Jan Mulawka Czym jest inżynieria genetyczna Zbiór technik rekombinowania i klonowania DNA Wydzielanie i charakteryzowanie pojedyńczych
Metody bioinformatyki Podstawy inżynierii genetycznej prof. dr hab. Jan Mulawka Czym jest inżynieria genetyczna Zbiór technik rekombinowania i klonowania DNA Wydzielanie i charakteryzowanie pojedyńczych
Olimpiada Biologiczna
 Olimpiada Biologiczna Informator narzędzia bioinformatyczne Katarzyna Grudziąż, Takao Ishikawa Warszawa, luty 2019 r. Bioinformatyka to dziedzina nauki łącząca w sobie wiedzę z dziedziny biologii z wykorzystaniem
Olimpiada Biologiczna Informator narzędzia bioinformatyczne Katarzyna Grudziąż, Takao Ishikawa Warszawa, luty 2019 r. Bioinformatyka to dziedzina nauki łącząca w sobie wiedzę z dziedziny biologii z wykorzystaniem
PCR łańcuchowa reakcja polimerazy
 PCR łańcuchowa reakcja polimerazy PCR - ang. polymerase chain reaction Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
PCR łańcuchowa reakcja polimerazy PCR - ang. polymerase chain reaction Technika PCR umożliwia otrzymywanie dużej liczby kopii specyficznych fragmentów DNA (czyli amplifikację zwielokrotnienie fragmentu
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU PCR sposób na DNA.
 SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU PCR sposób na DNA. SPIS TREŚCI: 1. Wprowadzenie. 2. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. 3. Karty pracy. 1. Karta
SCENARIUSZ LEKCJI BIOLOGII Z WYKORZYSTANIEM FILMU PCR sposób na DNA. SPIS TREŚCI: 1. Wprowadzenie. 2. Części lekcji. 1. Część wstępna. 2. Część realizacji. 3. Część podsumowująca. 3. Karty pracy. 1. Karta
Znaczenie genetyki. Opracował A. Podgórski
 Znaczenie genetyki Opracował A. Podgórski InŜynieria genetyczna InŜynieria genetyczna ingerencja w materiał genetyczny organizmów, w celu zmiany ich właściwości dziedzicznych. Istota inŝynierii genetycznej
Znaczenie genetyki Opracował A. Podgórski InŜynieria genetyczna InŜynieria genetyczna ingerencja w materiał genetyczny organizmów, w celu zmiany ich właściwości dziedzicznych. Istota inŝynierii genetycznej
Skąd się wzięła biologia syntetyczna? Co to są standardowe części biologiczne?
 Skąd się wzięła biologia syntetyczna? Mało kto zdaje sobie sprawę z tego, że termin "biologia syntetyczna" został ukuty w 1974 roku przez polskiego genetyka i biochemika Wacława Szybalskiego. Biologia
Skąd się wzięła biologia syntetyczna? Mało kto zdaje sobie sprawę z tego, że termin "biologia syntetyczna" został ukuty w 1974 roku przez polskiego genetyka i biochemika Wacława Szybalskiego. Biologia
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Ekspresja genów jest regulowana
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ Ekspresja genów jest regulowana
Wektory DNA - klonowanie molekularne
 Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Ćwiczenia 2-4 KLONOWANIE DNA
 Ćwiczenia 2-4 KLONOWANIE DNA Klonowanie DNA jest podstawową techniką biologii molekularnej umożliwiającą powielenie określonego fragmentu DNA (najczęściej genu) w komórkach gospodarza np. bakteriach Escherichia
Ćwiczenia 2-4 KLONOWANIE DNA Klonowanie DNA jest podstawową techniką biologii molekularnej umożliwiającą powielenie określonego fragmentu DNA (najczęściej genu) w komórkach gospodarza np. bakteriach Escherichia
Polimeraza Taq (1U/ l) 1-2 U 1 polimeraza Taq jako ostatni składniki mieszaniny końcowa objętość
 Ćwiczenie 6 Technika PCR Celem ćwiczenia jest zastosowanie techniki PCR do amplifikacji fragmentu DNA z bakterii R. leguminosarum bv. trifolii TA1 (RtTA1). Studenci przygotowują reakcję PCR wykorzystując
Ćwiczenie 6 Technika PCR Celem ćwiczenia jest zastosowanie techniki PCR do amplifikacji fragmentu DNA z bakterii R. leguminosarum bv. trifolii TA1 (RtTA1). Studenci przygotowują reakcję PCR wykorzystując
Metody badania polimorfizmu/mutacji DNA. Aleksandra Sałagacka Pracownia Diagnostyki Molekularnej i Farmakogenomiki Uniwersytet Medyczny w Łodzi
 Metody badania polimorfizmu/mutacji DNA Aleksandra Sałagacka Pracownia Diagnostyki Molekularnej i Farmakogenomiki Uniwersytet Medyczny w Łodzi Mutacja Mutacja (łac. mutatio zmiana) - zmiana materialnego
Metody badania polimorfizmu/mutacji DNA Aleksandra Sałagacka Pracownia Diagnostyki Molekularnej i Farmakogenomiki Uniwersytet Medyczny w Łodzi Mutacja Mutacja (łac. mutatio zmiana) - zmiana materialnego
Biologia Molekularna Podstawy
 Biologia Molekularna Podstawy Budowa DNA Budowa DNA Zasady: Purynowe: adenina i guanina Pirymidynowe: cytozyna i tymina 2 -deoksyryboza Grupy fosforanowe Budowa RNA Budowa RNA Zasady: purynowe: adenina
Biologia Molekularna Podstawy Budowa DNA Budowa DNA Zasady: Purynowe: adenina i guanina Pirymidynowe: cytozyna i tymina 2 -deoksyryboza Grupy fosforanowe Budowa RNA Budowa RNA Zasady: purynowe: adenina
MATERIAŁY DO BLOKU INŻYNIERIA GENETYCZNA
 MATERIAŁY DO BLOKU INŻYNIERIA GENETYCZNA 1. AMPLIFIKACJA FRAGMENTU DNA METODĄ PCR Otrzymywanie dużej liczby kopii określonego fragmentu DNA możliwe jest przy zastosowaniu procedur klonowania lub znacznie
MATERIAŁY DO BLOKU INŻYNIERIA GENETYCZNA 1. AMPLIFIKACJA FRAGMENTU DNA METODĄ PCR Otrzymywanie dużej liczby kopii określonego fragmentu DNA możliwe jest przy zastosowaniu procedur klonowania lub znacznie
Biotechnologia jest dyscypliną nauk technicznych, która wykorzystuje procesy biologiczne na skalę przemysłową. Inaczej są to wszelkie działania na
 Biotechnologia jest dyscypliną nauk technicznych, która wykorzystuje procesy biologiczne na skalę przemysłową. Inaczej są to wszelkie działania na żywych organizmach prowadzące do uzyskania konkretnych
Biotechnologia jest dyscypliną nauk technicznych, która wykorzystuje procesy biologiczne na skalę przemysłową. Inaczej są to wszelkie działania na żywych organizmach prowadzące do uzyskania konkretnych
Biologia medyczna, materiały dla studentów
 Zasada reakcji PCR Reakcja PCR (replikacja in vitro) obejmuje denaturację DNA, przyłączanie starterów (annealing) i syntezę nowych nici DNA (elongacja). 1. Denaturacja: rozplecenie nici DNA, temp. 94 o
Zasada reakcji PCR Reakcja PCR (replikacja in vitro) obejmuje denaturację DNA, przyłączanie starterów (annealing) i syntezę nowych nici DNA (elongacja). 1. Denaturacja: rozplecenie nici DNA, temp. 94 o
Mikrosatelitarne sekwencje DNA
 Mikrosatelitarne sekwencje DNA Małgorzata Pałucka Wykorzystanie sekwencji mikrosatelitarnych w jądrowym DNA drzew leśnych do udowodnienia pochodzenia materiału dowodowego w postępowaniu sądowym 27.09.2012
Mikrosatelitarne sekwencje DNA Małgorzata Pałucka Wykorzystanie sekwencji mikrosatelitarnych w jądrowym DNA drzew leśnych do udowodnienia pochodzenia materiału dowodowego w postępowaniu sądowym 27.09.2012
Wektory DNA - klonowanie molekularne
 Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
SCENARIUSZ LEKCJI. TEMAT LEKCJI: Podstawowe techniki inżynierii genetycznej. Streszczenie
 SCENARIUSZ LEKCJI OPRACOWANY W RAMACH PROJEKTU: INFORMATYKA MÓJ SPOSÓB NA POZNANIE I OPISANIE ŚWIATA. PROGRAM NAUCZANIA INFORMATYKI Z ELEMENTAMI PRZEDMIOTÓW MATEMATYCZNO-PRZYRODNICZYCH Autorzy scenariusza:
SCENARIUSZ LEKCJI OPRACOWANY W RAMACH PROJEKTU: INFORMATYKA MÓJ SPOSÓB NA POZNANIE I OPISANIE ŚWIATA. PROGRAM NAUCZANIA INFORMATYKI Z ELEMENTAMI PRZEDMIOTÓW MATEMATYCZNO-PRZYRODNICZYCH Autorzy scenariusza:
Dr. habil. Anna Salek International Bio-Consulting 1 Germany
 1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
1 2 3 Drożdże są najprostszymi Eukariontami 4 Eucaryota Procaryota 5 6 Informacja genetyczna dla każdej komórki drożdży jest identyczna A zatem każda komórka koduje w DNA wszystkie swoje substancje 7 Przy
Wektory DNA - klonowanie molekularne
 Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Metody analizy genomu
 Metody analizy genomu 1. Mapowanie restrykcyjne. 2. Sondy do rozpoznawania DNA 3. FISH 4. Odczytanie sekwencji DNA 5. Interpretacja sekwencji DNA genomu 6. Transkryptom 7. Proteom 1. Mapy restrykcyjne
Metody analizy genomu 1. Mapowanie restrykcyjne. 2. Sondy do rozpoznawania DNA 3. FISH 4. Odczytanie sekwencji DNA 5. Interpretacja sekwencji DNA genomu 6. Transkryptom 7. Proteom 1. Mapy restrykcyjne
Wykład 14 Biosynteza białek
 BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
BIOCHEMIA Kierunek: Technologia Żywności i Żywienie Człowieka semestr III Wykład 14 Biosynteza białek WYDZIAŁ NAUK O ŻYWNOŚCI I RYBACTWA CENTRUM BIOIMMOBILIZACJI I INNOWACYJNYCH MATERIAŁÓW OPAKOWANIOWYCH
Sylabus Biologia molekularna
 Sylabus Biologia molekularna 1. Metryczka Nazwa Wydziału Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Analityka Medyczna, studia jednolite magisterskie, studia stacjonarne
Sylabus Biologia molekularna 1. Metryczka Nazwa Wydziału Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Analityka Medyczna, studia jednolite magisterskie, studia stacjonarne
Wektory DNA - klonowanie molekularne
 Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Wstęp. Jak programować w DNA? Idea oraz przykład. Problem FSAT charakterystyka i rozwiązanie za pomocą DNA. Jak w ogólności rozwiązywać problemy
 Ariel Zakrzewski Wstęp. Jak programować w DNA? Idea oraz przykład. Problem FSAT charakterystyka i rozwiązanie za pomocą DNA. Jak w ogólności rozwiązywać problemy matematyczne z użyciem DNA? Gdzie są problemy?
Ariel Zakrzewski Wstęp. Jak programować w DNA? Idea oraz przykład. Problem FSAT charakterystyka i rozwiązanie za pomocą DNA. Jak w ogólności rozwiązywać problemy matematyczne z użyciem DNA? Gdzie są problemy?
Prof. UG, dr hab. Uniwersytet Gdański, Wydział Chemii, Wita Stwosza 63, Gdańsk tel ,
 Prof. UG, dr hab. Uniwersytet Gdański, Wydział Chemii, Wita Stwosza 63, Gdańsk 80-308 Piotr Mucha tel. 0585235432, e-mail: piotr.mucha@ug.edu.pl Gdańsk, 17.10.2015r. Recenzja pracy doktorskiej mgr Ireneusza
Prof. UG, dr hab. Uniwersytet Gdański, Wydział Chemii, Wita Stwosza 63, Gdańsk 80-308 Piotr Mucha tel. 0585235432, e-mail: piotr.mucha@ug.edu.pl Gdańsk, 17.10.2015r. Recenzja pracy doktorskiej mgr Ireneusza
TECHNIKI ANALIZY RNA TECHNIKI ANALIZY RNA TECHNIKI ANALIZY RNA
 DNA 28SRNA 18/16S RNA 5SRNA mrna Ilościowa analiza mrna aktywność genów w zależności od wybranych czynników: o rodzaju tkanki o rodzaju czynnika zewnętrznego o rodzaju upośledzenia szlaku metabolicznego
DNA 28SRNA 18/16S RNA 5SRNA mrna Ilościowa analiza mrna aktywność genów w zależności od wybranych czynników: o rodzaju tkanki o rodzaju czynnika zewnętrznego o rodzaju upośledzenia szlaku metabolicznego
wykład dla studentów II roku biotechnologii Andrzej Wierzbicki
 Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
Genetyka ogólna wykład dla studentów II roku biotechnologii Andrzej Wierzbicki Uniwersytet Warszawski Wydział Biologii andw@ibb.waw.pl http://arete.ibb.waw.pl/private/genetyka/ 1. Gen to odcinek DNA odpowiedzialny
(12) O PIS PATENTOWY (19) PL (11) (13) B1
 RZECZPOSPOLITA POLSKA (12) O PIS PATENTOWY (19) PL (11) 159844 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 273721 ( 2) Data zgłoszenia: 14.07.1988 (51) IntCl.5: C12N 15/51
RZECZPOSPOLITA POLSKA (12) O PIS PATENTOWY (19) PL (11) 159844 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 273721 ( 2) Data zgłoszenia: 14.07.1988 (51) IntCl.5: C12N 15/51
PODSTAWY BIOTECHNOLOGII Piotr Solarczyk
 PODSTAWY BIOTECHNOLOGII Piotr Solarczyk EFEKT KOŃCOWY Po zakończeniu seminarium powinieneś umieć: wyjaśnić pojęcia plazmid, fag, wektor, wektor ekspresyjny i czółenkowy, klonowanie, transfekcja, transformacja,
PODSTAWY BIOTECHNOLOGII Piotr Solarczyk EFEKT KOŃCOWY Po zakończeniu seminarium powinieneś umieć: wyjaśnić pojęcia plazmid, fag, wektor, wektor ekspresyjny i czółenkowy, klonowanie, transfekcja, transformacja,
Inne podejścia do klonowania
 Inne podejścia do klonowania 12/14-12-2017 Piotr Gawroński piotr_gawronski@sggw.pl 2/68 pt. 12-13 sites.google.com/site/chlorotfs Klasyczne klonowanie Universal TA clonning TdT = terminal deoxynucleotidyl-transferase
Inne podejścia do klonowania 12/14-12-2017 Piotr Gawroński piotr_gawronski@sggw.pl 2/68 pt. 12-13 sites.google.com/site/chlorotfs Klasyczne klonowanie Universal TA clonning TdT = terminal deoxynucleotidyl-transferase
Techniki biologii molekularnej Kod przedmiotu
 Techniki biologii molekularnej - opis przedmiotu Informacje ogólne Nazwa przedmiotu Techniki biologii molekularnej Kod przedmiotu 13.9-WB-BMD-TBM-W-S14_pNadGenI2Q8V Wydział Kierunek Wydział Nauk Biologicznych
Techniki biologii molekularnej - opis przedmiotu Informacje ogólne Nazwa przedmiotu Techniki biologii molekularnej Kod przedmiotu 13.9-WB-BMD-TBM-W-S14_pNadGenI2Q8V Wydział Kierunek Wydział Nauk Biologicznych
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii
 Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
Możliwości współczesnej inżynierii genetycznej w obszarze biotechnologii 1. Technologia rekombinowanego DNA jest podstawą uzyskiwania genetycznie zmodyfikowanych organizmów 2. Medycyna i ochrona zdrowia
WPROWADZENIE DO GENETYKI MOLEKULARNEJ
 WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
WPROWADZENIE DO GENETYKI MOLEKULARNEJ
 WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
WPROWADZENIE DO GENETYKI MOLEKULARNEJ Replikacja organizacja widełek replikacyjnych Transkrypcja i biosynteza białek Operon regulacja ekspresji genów Prowadzący wykład: prof. dr hab. Jarosław Burczyk REPLIKACJA
Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją).
 Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją). Czym jest życie? metabolizm + informacja (replikacja) 2 Cząsteczki organiczne mog y powstać w atmosferze pierwotnej
Historia informacji genetycznej. Jak ewolucja tworzy nową informację (z ma ą dygresją). Czym jest życie? metabolizm + informacja (replikacja) 2 Cząsteczki organiczne mog y powstać w atmosferze pierwotnej
TaqNova-RED. Polimeraza DNA RP20R, RP100R
 TaqNova-RED Polimeraza DNA RP20R, RP100R RP20R, RP100R TaqNova-RED Polimeraza DNA Rekombinowana termostabilna polimeraza DNA Taq zawierająca czerwony barwnik, izolowana z Thermus aquaticus, o przybliżonej
TaqNova-RED Polimeraza DNA RP20R, RP100R RP20R, RP100R TaqNova-RED Polimeraza DNA Rekombinowana termostabilna polimeraza DNA Taq zawierająca czerwony barwnik, izolowana z Thermus aquaticus, o przybliżonej
Ekspresja genów heterogenicznych w drożdżach Pichia pastoris
 Ekspresja genów heterogenicznych w drożdżach Pichia pastoris Ekspresja genów heterogenicznych w drożdżach Pichia pastoris Drożdże Pichia pastoris należą do drożdży metanolotroficznych tj. zdolnych do wykorzystywania
Ekspresja genów heterogenicznych w drożdżach Pichia pastoris Ekspresja genów heterogenicznych w drożdżach Pichia pastoris Drożdże Pichia pastoris należą do drożdży metanolotroficznych tj. zdolnych do wykorzystywania
Badanie funkcji genu
 Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
Badanie funkcji genu Funkcję genu można zbadać różnymi sposobami Przypadkowa analizy funkcji genu MUTACJA FENOTYP GEN Strategia ukierunkowanej analizy funkcji genu GEN 1. wprowadzenie mutacji w genie 2.
Informacje dotyczące pracy kontrolnej
 Informacje dotyczące pracy kontrolnej Słuchacze, którzy z przyczyn usprawiedliwionych nie przystąpili do pracy kontrolnej lub otrzymali z niej ocenę negatywną zobowiązani są do dnia 06 grudnia 2015 r.
Informacje dotyczące pracy kontrolnej Słuchacze, którzy z przyczyn usprawiedliwionych nie przystąpili do pracy kontrolnej lub otrzymali z niej ocenę negatywną zobowiązani są do dnia 06 grudnia 2015 r.
Drożdżowe systemy ekspresyjne
 Drożdże Drożdżowe systemy ekspresyjne Zalety: możliwość uzyskania dużej biomasy modyfikacje postranslacyjne eksprymowanych białek transport eksprymowanych białek do pożywki Duża biomasa W przypadku hodowli
Drożdże Drożdżowe systemy ekspresyjne Zalety: możliwość uzyskania dużej biomasy modyfikacje postranslacyjne eksprymowanych białek transport eksprymowanych białek do pożywki Duża biomasa W przypadku hodowli
Program ćwiczeń z inżynierii genetycznej KP-III rok Biologii
 Program ćwiczeń z inżynierii genetycznej KP-III rok Biologii Ćwiczenie 1 i 2: Metody izolacji, oczyszczania DNA kolokwium wstępne: sprawdzenie podstawowych wiadomości z zakresu genetyki, i biologii molekularnej
Program ćwiczeń z inżynierii genetycznej KP-III rok Biologii Ćwiczenie 1 i 2: Metody izolacji, oczyszczania DNA kolokwium wstępne: sprawdzenie podstawowych wiadomości z zakresu genetyki, i biologii molekularnej
Wprowadzanie zrekombinowanego DNA do komórek bakterii. Sposoby wprowadzania DNA do innych (niż bakterie) typów komórek
 Ligacja DNA - rekombinacja in vitro Wprowadzanie zrekombinowanego DNA do komórek bakterii Sposoby wprowadzania DNA do innych (niż bakterie) typów komórek Jak otrzymać zrekombinowane DNA-schemat klonowania
Ligacja DNA - rekombinacja in vitro Wprowadzanie zrekombinowanego DNA do komórek bakterii Sposoby wprowadzania DNA do innych (niż bakterie) typów komórek Jak otrzymać zrekombinowane DNA-schemat klonowania
Biologia molekularna
 Biologia molekularna 1. Metryczka Nazwa Wydziału Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Analityka Medyczna, studia jednolite magisterskie, studia stacjonarne i niestacjonarne
Biologia molekularna 1. Metryczka Nazwa Wydziału Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Analityka Medyczna, studia jednolite magisterskie, studia stacjonarne i niestacjonarne
Wektory DNA - klonowanie molekularne
 Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Wektory DNA - klonowanie molekularne Fragment DNA (np. pojedynczy gen) można trwale wprowadzić do komórek gospodarza (tzn. zmusić go do powielania w tym gospodarzu) tylko wtedy, gdy zostanie on wbudowany
Wybrane techniki badania białek -proteomika funkcjonalna
 Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Wybrane techniki badania białek -proteomika funkcjonalna Proteomika: umożliwia badanie zestawu wszystkich (lub prawie wszystkich) białek komórkowych Zalety analizy proteomu np. w porównaniu z analizą trankryptomu:
Kwasy Nukleinowe. Rys. 1 Struktura typowego dinukleotydu
 Kwasy Nukleinowe Kwasy nukleinowe są biopolimerami występującymi w komórkach wszystkich organizmów. Wyróżnia się dwa główne typy kwasów nukleinowych: Kwas deoksyrybonukleinowy (DNA) Kwasy rybonukleinowe
Kwasy Nukleinowe Kwasy nukleinowe są biopolimerami występującymi w komórkach wszystkich organizmów. Wyróżnia się dwa główne typy kwasów nukleinowych: Kwas deoksyrybonukleinowy (DNA) Kwasy rybonukleinowe
na zakup usługi badawczej
 Łódź, dn. 08.09.2015r. Zapytanie ofertowe nr 1/OF/2015 na zakup usługi badawczej w ramach projektu,, Bakteriofagowy preparat do leczenia zapalenia wymienia u krów wywołanego bakteriami antybiotykopornymi
Łódź, dn. 08.09.2015r. Zapytanie ofertowe nr 1/OF/2015 na zakup usługi badawczej w ramach projektu,, Bakteriofagowy preparat do leczenia zapalenia wymienia u krów wywołanego bakteriami antybiotykopornymi
Specjalność (studia II stopnia) Oczyszczanie i analiza produktów biotechnologicznych
 Specjalność (studia II stopnia) Oczyszczanie i analiza produktów biotechnologicznych Studia magisterskie przedmioty specjalizacyjne Bioinformatyka w analizie genomu Diagnostyka molekularna Elementy biosyntezy
Specjalność (studia II stopnia) Oczyszczanie i analiza produktów biotechnologicznych Studia magisterskie przedmioty specjalizacyjne Bioinformatyka w analizie genomu Diagnostyka molekularna Elementy biosyntezy
Mikroorganizmy Zmodyfikowane Genetycznie
 Mikroorganizmy Zmodyfikowane Genetycznie DEFINICJA Mikroorganizm (drobnoustrój) to organizm niewidoczny gołym okiem. Pojęcie to nie jest zbyt precyzyjne lecz z pewnością mikroorganizmami są: bakterie,
Mikroorganizmy Zmodyfikowane Genetycznie DEFINICJA Mikroorganizm (drobnoustrój) to organizm niewidoczny gołym okiem. Pojęcie to nie jest zbyt precyzyjne lecz z pewnością mikroorganizmami są: bakterie,
