Punkty decyzyjne w zarządzaniu projektem
|
|
|
- Alojzy Bielecki
- 10 lat temu
- Przeglądów:
Transkrypt
1 Punkty decyzyjne w zarządzaniu projektem Rafał Derlacz Zakład Regulacji Metabolizmu, Wydział Biologii, UW rderlacz@biol.uw.edu.pl rafal.derlacz@adamed.com.pl
2 >100 USD Early Target Preclinical Research Clinical Research Commercialization Discovery Screen Hit-tolead Lead Opt Preclinical Phase 1 Phase 2 Phase 3 Filing Launch/ Post-Launch 5%
3 Trzy podstawowe etapy rozwoju projektu 1. Badania podstawowe i ocena możliwości rozwoju danej cząsteczki kandydata; 2. Badania fazy przedklinicznej i badania poza kliniczne (ang. nonclinical); 3. Badania kliniczne.
4 Przykładowe ramy czasowe rozwoju projektu Główna faza badań klinicznych Wczesna faza badań klinicznych Badania poza-kliniczne Badania podstawowe
5 Przykładowe ramy czasowe rozwoju projektu Faktyczne badania PRZEDkliniczne Główna faza badań klinicznych Badania podstawowe Wczesna faza badań klinicznych Badania poza-kliniczne
6 Logiczny plan rozwoju projektu Badania podstawowe Ocena możliwości rozwoju Wybór cząsteczki-kandydata IND Badania przedkliniczne Badania kliniczne Badania poza-kliniczne NDA
7 Pre IND meeting package content
8 Pre IND meeting package content Tab A Table of Contents Tab B List of Proposed Attendees Tab C Introduction Company s background, location, products Meeting information (product name, indication(s), sponsor, meeting date & time Tab D Mechanism of action Tab E Nonclinical Safety Studies Table of all studies (safety & efficacy) Summary of each safety study Proposed additional studies: proposed 4 week study (NOAEL) Rat: 100, 500, 1000 mg/kg Dog: 100, 500, 1000 mg/kg Tab F Previous Human Experience Similar products (adverse effects) Tab G Clinical Program Introduction (TPP) Rationale for clinical studies First Protocol (Single Dose) Starting dose in grams/mass Planned program Tab H CMC section Short product description & method of manufacture; analytical methods API 30 days stability Formulation 30 days stability Proposals for ongoing and future stability studies Impurity Profile Tab I Questions for FDA
9 Odrobina statystyki Na 5 cząsteczek dla których składa się dokumentację NDA (ang. new drug application), tylko 2 zwrócą koszty swojego rozwoju; Przeprowadzając proste i stosunkowo mało kosztowne doświadczenia z zakresu PK i metabolizmu leków in vitro w początkowych etapach projektu można zwiększyć szanse powodzenia cząsteczki kandydata na lek do ok. 10 % (obecnie jest to ok. 3,5 5%); Postawienie odpowiednich pytań na początku projektu pozwala na zdecydowaną redukcję jego kosztów.
10 Podstawowe pytania, które warto sobie zadać Cząsteczka kandydat: Wskazanie: Terapia/podanie: Droga podania: związek małocząsteczkowy czy białko? schorzenie zagrażające życiu czy nie? ostre czy przewlekłe? dożylne czy inne?
11 Podstawowe pytania, które warto sobie zadać Czy lek osiągnie miejsce swojego działania w organizmie i będzie pozostawał tam wystarczająco długo i w wystarczającym stężeniu, żeby wywołać efekt terapeutyczny?
12 Określenie możliwości rozwoju projektu Farmakologia Chemia analityczna Rozpuszczalność i stabilność Dostępność Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
13 Określenie możliwości rozwoju projektu BADANIA PODSTAWOWE: Farmakologia Chemia analityczna Rozpuszczalność i stabilność Dostępność Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
14 Określenie możliwości rozwoju projektu BADANIA PODSTAWOWE: Farmakologia Chemia analityczna Rozpuszczalność i stabilność Ocena możliwości rozwoju projektu Rozwój i walidacja metod analitycznych; Badania stabilności i rozpuszczalności in vitro oraz we krwi i w surowicy; Określenie zależności między budową cząsteczki a jej aktywnością; Potwierdzenie mechanizmu działania in vitro;
15 Określenie możliwości rozwoju projektu BADANIA PRZEDKLINICZNE: Farmakologia Chemia analityczna Rozpuszczalność i stabilność Dostępność Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
16 Określenie możliwości rozwoju projektu BADANIA PRZEDKLINICZNE: Wybór techniki bioanalitycznej (LC MS MS, HPLC, ELISA, RIA); Rozwój metod bioanalitycznych dla różnych matryc; Wstępna walidacja metod bioanalitycznych. Dostępność Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
17 Określenie możliwości rozwoju projektu BADANIA PRZEDKLINICZNE: Badania in vitro z wykorzystaniem modeli barier biologicznych; Testy wiązania do białek surowicy; Dostępność Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
18 Określenie możliwości rozwoju projektu BADANIA PRZEDKLINICZNE: Wstępne badanie PK aby móc wyznaczyć punkty w TK; Dostępność Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
19 Określenie możliwości rozwoju projektu BADANIA PRZEDKLINICZNE: Wstępne profilowanie metabolitów in vitro aby móc odpowiednio dobrać gatunki zwierząt do badań toksyczności; Dostępność Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
20 Określenie możliwości rozwoju projektu BADANIA PRZEDKLINICZNE: Badanie toksyczności ostrej; Badanie toksyczności przy wielokrotnym podaniu z profilowaniem TK. Dostarczanie Ocena możliwości rozwoju projektu Metabolizm Farmakokinetyka Chemia bioanalityczna Toksykologia
21 BADANIA PODSTAWOWE: Chemia analityczna Stabilność i rozpuszczalność Wstępna farmakologia (in vitro) BADANIA PRZEDKLINICZNE: Chemia bioanalityczna Dostępność Farmakokinetyka Metabolizm Toksykologia Farmakologia in vivo Sposób na podjęcie decyzji
22 Translational medicine Industry perspective: How to effectively deliver the preclinical data now required for regulatory submission Dr Karen Cornelissen, Scientific Director, Covance, UK Regulatory perspective on the pre clinical data required for Phase I approval gaining greater control though translational medicine Walter Janssens PhD, Senior Assessor, Preclinical Department Research & Development, Federal Agency for Medicinal and Health Products, Belgium Comparing and contrasting European and FDA guidelines on risk mitigation in FIM studies Anthea Cromie, Head of Clinical, Pharmacology Europe, MDS Pharma Services, UK Designing efficient Phase I studies Mario Tanguay, B.Pharm, Ph.D, Vice President, Scientific & Regulatory Affairs, Anapharm New thinking in overcoming FIM dosing challenges James Dow PhD, Director of Clinical, Pharmacology & DMPK, (OSI) Prosidion, UK Selecting the correct starting dose for FIM antibody studies Peter Lloyd, Head of PKPD, Novartis Biologics, UK
23 Early Target Preclinical Research Clinical Research Commercialization Discovery Screen Hit-tolead Lead Opt Preclinical Phase 1 Phase 2 Phase 3 Filing Launch/ Post-Launch NO ADVERSE EFFECT LEVEL MINIMAL ANTICIPATED BIOLOGICAL EFFECT LEVEL
24
25 ?
26
27 NOAEL 65% MABEL 5% PK/PD 15%
28 NOAEL HED Human Equivalent Dose /10 Safety Factor MRSD Maximum Recommended Safe Dose
29 NOAEL NOAEL 50 mg/kg (psy) HED 50/1,8 = 2,7 mg/kg Human Equivalent Dose /10 Safety Factor 27 * 60 kg = 1620 mg HED /10 SF = 160 mg MRSD MRSD Maximum Recommended Safe Dose
30
31 MRSD na podstawie NOAEL/10 MRSD na podstawie MABEL (80 times < NOAEL/10)
32
33
34
35
36
Najbardziej obiecujące terapie lekami biopodobnymi - Rak piersi
 Warszawa, 27.02.2018 MEDYCYNA XXI wieku III EDYCJA Leki biopodobne 2018 Najbardziej obiecujące terapie lekami biopodobnymi - Rak piersi Dr n. med. Agnieszka Jagiełło-Gruszfeld 1 Breast Cancer (C50.0-C50.9):
Warszawa, 27.02.2018 MEDYCYNA XXI wieku III EDYCJA Leki biopodobne 2018 Najbardziej obiecujące terapie lekami biopodobnymi - Rak piersi Dr n. med. Agnieszka Jagiełło-Gruszfeld 1 Breast Cancer (C50.0-C50.9):
Interdyscyplinarny charakter badań równoważności biologicznej produktów leczniczych
 Interdyscyplinarny charakter badań równoważności biologicznej produktów leczniczych Piotr Rudzki Zakład Farmakologii, w Warszawie Kongres Świata Przemysłu Farmaceutycznego Łódź, 25 VI 2009 r. Prace badawczo-wdrożeniowe
Interdyscyplinarny charakter badań równoważności biologicznej produktów leczniczych Piotr Rudzki Zakład Farmakologii, w Warszawie Kongres Świata Przemysłu Farmaceutycznego Łódź, 25 VI 2009 r. Prace badawczo-wdrożeniowe
Ekonomia nowoczesnych technologii
 Ekonomia nowoczesnych technologii Rafał Derlacz Zakład Regulacji Metabolizmu, Wydział Biologii, UW rderlacz@biol.uw.edu.pl rafal.derlacz@adamed.com.pl Success is the ability to go from one failure to another
Ekonomia nowoczesnych technologii Rafał Derlacz Zakład Regulacji Metabolizmu, Wydział Biologii, UW rderlacz@biol.uw.edu.pl rafal.derlacz@adamed.com.pl Success is the ability to go from one failure to another
Badania kliniczne w procesie powstawania leku
 Ukończył specjalizację z zakresu chorób wewnętrznych w Klinice Gastroenterologii i Hepatologii Centrum Medycznego Kształcenia Podyplomowego w Warszawie oraz specjalizację z medycyny farmaceutycznej na
Ukończył specjalizację z zakresu chorób wewnętrznych w Klinice Gastroenterologii i Hepatologii Centrum Medycznego Kształcenia Podyplomowego w Warszawie oraz specjalizację z medycyny farmaceutycznej na
Badania Kliniczne w Chorobach Rzadkich. Bożenna Dembowska-Bagińska Instytut Pomnik Centrum Zdrowia Dziecka członek COMP/EMA
 Badania Kliniczne w Chorobach Rzadkich. Bożenna Dembowska-Bagińska Instytut Pomnik Centrum Zdrowia Dziecka członek COMP/EMA Choroba rzadka RARE DISEASE mała liczba pacjentów kosztowny, nie przynoszący
Badania Kliniczne w Chorobach Rzadkich. Bożenna Dembowska-Bagińska Instytut Pomnik Centrum Zdrowia Dziecka członek COMP/EMA Choroba rzadka RARE DISEASE mała liczba pacjentów kosztowny, nie przynoszący
PROGRAM STAŻU. Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o.
 PROGRAM STAŻU Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o. Miejsce odbywania stażu / Legal address Muchoborska 8, 54-424 Wroclaw Stanowisko, obszar działania/
PROGRAM STAŻU Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o. Miejsce odbywania stażu / Legal address Muchoborska 8, 54-424 Wroclaw Stanowisko, obszar działania/
, Warszawa
 Kierunki rozwoju nowych leków w pediatrii z perspektywy Komitetu Pediatrycznego EMA. Wpływ Rozporządzenia Pediatrycznego na pediatryczne badania kliniczne w Europie Marek Migdał, Klinika Anestezjologii
Kierunki rozwoju nowych leków w pediatrii z perspektywy Komitetu Pediatrycznego EMA. Wpływ Rozporządzenia Pediatrycznego na pediatryczne badania kliniczne w Europie Marek Migdał, Klinika Anestezjologii
Sylabus - Biofarmacja
 Sylabus - Biofarmacja 1. Metryczka Nazwa Wydziału: Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Kierunek: farmacja Poziom: jednolite studia magisterskie Profil: praktyczny
Sylabus - Biofarmacja 1. Metryczka Nazwa Wydziału: Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Kierunek: farmacja Poziom: jednolite studia magisterskie Profil: praktyczny
PROJECT. Syllabus for course Principles of Marketing. on the study program: Management
 Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Principles of Marketing on the study program: Management I. General information
Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Principles of Marketing on the study program: Management I. General information
Yousuke Tamura Programmer Clinical Science Dep., R&D AstraZeneca K.K. 2005/11/30 1
 - Word SAS - Yousuke Tamura Programmer Clinical Science Dep., R&D AstraZeneca K.K. 2005/11/30 1 Contents Background Previous method Change/Shift/Transition Current method Benefit of current method Application
- Word SAS - Yousuke Tamura Programmer Clinical Science Dep., R&D AstraZeneca K.K. 2005/11/30 1 Contents Background Previous method Change/Shift/Transition Current method Benefit of current method Application
Finansowanie badań klinicznych niekomercyjnych
 Finansowanie badań klinicznych niekomercyjnych www.kpk.gov.pl W niniejszej prezentacji wykorzystano materiały udostępnione m.in. przez KE i/lub Ministerstwa oraz Agendy RP Badania kliniczne w programach
Finansowanie badań klinicznych niekomercyjnych www.kpk.gov.pl W niniejszej prezentacji wykorzystano materiały udostępnione m.in. przez KE i/lub Ministerstwa oraz Agendy RP Badania kliniczne w programach
Instrukcja do ćwiczeń laboratoryjnych
 UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 4 i 5 OCENA EKOTOKSYCZNOŚCI TEORIA Chemia zanieczyszczeń środowiska
UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 4 i 5 OCENA EKOTOKSYCZNOŚCI TEORIA Chemia zanieczyszczeń środowiska
Kardiologia małych zwierząt
 Międzynarodowa Konferencja VetCo Kardiologia małych zwierząt 5-6 września 2015 Warszawa Materiały konferencyjne Wydawca biuletynu: VetCo Veterinary Consulting & Control Al. 3 Maja 7/2, 00-401 Warszawa
Międzynarodowa Konferencja VetCo Kardiologia małych zwierząt 5-6 września 2015 Warszawa Materiały konferencyjne Wydawca biuletynu: VetCo Veterinary Consulting & Control Al. 3 Maja 7/2, 00-401 Warszawa
PROJECT. Syllabus for course Negotiations. on the study program: Management
 Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Negotiations on the study program: Management I. General information 1. Name
Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Negotiations on the study program: Management I. General information 1. Name
PROJECT. Syllabus for course Global Marketing. on the study program: Management
 Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Global Marketing on the study program: Management I. General information 1. Name
Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Global Marketing on the study program: Management I. General information 1. Name
Sylabus - Biofarmacja
 Sylabus - Biofarmacja 1. Metryczka Nazwa Wydziału Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Rok akademicki 2016/2017 Kierunek: farmacja Poziom: jednolite studia magisterskie
Sylabus - Biofarmacja 1. Metryczka Nazwa Wydziału Program kształcenia Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Rok akademicki 2016/2017 Kierunek: farmacja Poziom: jednolite studia magisterskie
Sylabus z modułu. [39B] Toksykologia. Zapoznanie z regulacjami prawnymi z zakresu bezpieczeństwa wyrobów kosmetycznych.
![Sylabus z modułu. [39B] Toksykologia. Zapoznanie z regulacjami prawnymi z zakresu bezpieczeństwa wyrobów kosmetycznych. Sylabus z modułu. [39B] Toksykologia. Zapoznanie z regulacjami prawnymi z zakresu bezpieczeństwa wyrobów kosmetycznych.](/thumbs/98/135233609.jpg) 1. Ogólne informacje o module Sylabus z modułu [39B] Toksykologia Nazwa modułu TOKSYKOLOGIA Kod modułu Nazwa jednostki prowadzącej moduł Nazwa kierunku studiów Forma studiów Profil kształcenia Semestr
1. Ogólne informacje o module Sylabus z modułu [39B] Toksykologia Nazwa modułu TOKSYKOLOGIA Kod modułu Nazwa jednostki prowadzącej moduł Nazwa kierunku studiów Forma studiów Profil kształcenia Semestr
BLIRT S.A., ul. Trzy Lipy 3/1.38, Gdańsk, tel. (58) , fax. (58) ,
 tel. (58) 739 61 50, fax. (58) 739 61 51, info@blirt.eu 04.06.2013 Wyniki finansowe Bilans Rachunek Zysków i Strat (dane nieuadytowane, w tys. PLN) I Q 2011 II Q 2011 III Q 2011 IV Q 2011 I Q 2012 II Q
tel. (58) 739 61 50, fax. (58) 739 61 51, info@blirt.eu 04.06.2013 Wyniki finansowe Bilans Rachunek Zysków i Strat (dane nieuadytowane, w tys. PLN) I Q 2011 II Q 2011 III Q 2011 IV Q 2011 I Q 2012 II Q
10. 11. Histologia. 12. Bioetyka 13. 14. 15. 1,5 45 16. 0,5 4 17. 0,5 2 18. 0,5 3 19. Matematyka ze statystyką Mathematics and Statistics
 PLAN STUDIÓW - I rok - Biotechnologia specjalność biotechnologia medyczna (studia I stopnia) STUDY PLAN I year - Biotechnology program, specialty in Medical Biotechnology (first cycle) Matematyka ze statystyką
PLAN STUDIÓW - I rok - Biotechnologia specjalność biotechnologia medyczna (studia I stopnia) STUDY PLAN I year - Biotechnology program, specialty in Medical Biotechnology (first cycle) Matematyka ze statystyką
1
 Plan prezentacji 1. 2. Procedura PIP Aktualności z Europejskiej Agencji Leków Warszawa, 6-7 marca 2013 3. Wnioski PUMA 4. Nowości z Agencji Prezentujący: Piotr Kozarewicz Administrator Naukowy l Jakość
Plan prezentacji 1. 2. Procedura PIP Aktualności z Europejskiej Agencji Leków Warszawa, 6-7 marca 2013 3. Wnioski PUMA 4. Nowości z Agencji Prezentujący: Piotr Kozarewicz Administrator Naukowy l Jakość
ASPEKTY PRACY DZIAŁU STATISTICAL PROGRAMMING I RELACJE Z DATA MANAGEMENT MARZENA MARCINOWSKA
 ASPEKTY PRACY DZIAŁU STATISTICAL PROGRAMMING I RELACJE Z DATA MANAGEMENT MARZENA MARCINOWSKA Seminarium GCPpl: Metodologia Badań Klinicznych, Warszawa, 15 marca 2016 AGENDA 1. Dział Statistical Programming
ASPEKTY PRACY DZIAŁU STATISTICAL PROGRAMMING I RELACJE Z DATA MANAGEMENT MARZENA MARCINOWSKA Seminarium GCPpl: Metodologia Badań Klinicznych, Warszawa, 15 marca 2016 AGENDA 1. Dział Statistical Programming
Zastosowanie programu komputerowego TopFit do wyznaczania parametrów farmakokinetycznych dla modelu dwukompartmentowego.
 Ćwiczenie 5. Zastosowanie programu komputerowego TopFit do wyznaczania parametrów farmakokinetycznych dla modelu dwukompartmentowego. Farmakokinetyka stosowana w praktyce klinicznej Celem ćwiczenia jest
Ćwiczenie 5. Zastosowanie programu komputerowego TopFit do wyznaczania parametrów farmakokinetycznych dla modelu dwukompartmentowego. Farmakokinetyka stosowana w praktyce klinicznej Celem ćwiczenia jest
Zmiany w prawie europejskim dotyczące monitorowania bezpieczeństwa farmakoterapii
 Zmiany w prawie europejskim dotyczące monitorowania bezpieczeństwa farmakoterapii Monika Trojan Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Stan obecny Rejestracja
Zmiany w prawie europejskim dotyczące monitorowania bezpieczeństwa farmakoterapii Monika Trojan Urząd Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Stan obecny Rejestracja
PROGRAM STAŻU. IBM Global Services Delivery Centre Sp z o.o. Nazwa podmiotu oferującego staż / Company name. Muchoborska 8, 54-424 Wroclaw
 PROGRAM STAŻU Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o. Miejsce odbywania stażu / Legal address Muchoborska 8, 54-424 Wroclaw Stanowisko, obszar działania/
PROGRAM STAŻU Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o. Miejsce odbywania stażu / Legal address Muchoborska 8, 54-424 Wroclaw Stanowisko, obszar działania/
PROJECT. Syllabus for course Techniques of negotiations and mediations in administration. on the study program: Administration
 Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Techniques of negotiations and mediations in administration on the study program:
Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Techniques of negotiations and mediations in administration on the study program:
Leki chemiczne a leki biologiczne
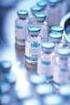 Leki chemiczne a leki biologiczne LEKI CHEMICZNE A LEKI BIOLOGICZNE Produkt syntezy chemicznej Produkt roślinny Produkt immunologiczny BIOLOGICZNE Produkt homeopatyczny Produkt z krwi/osocza - BIOLOGICZNE
Leki chemiczne a leki biologiczne LEKI CHEMICZNE A LEKI BIOLOGICZNE Produkt syntezy chemicznej Produkt roślinny Produkt immunologiczny BIOLOGICZNE Produkt homeopatyczny Produkt z krwi/osocza - BIOLOGICZNE
ĆWICZENIE 3. Farmakokinetyka nieliniowa i jej konsekwencje terapeutyczne na podstawie zmian stężenia fenytoiny w osoczu krwi
 ĆWICZENIE 3 Farmakokinetyka nieliniowa i jej konsekwencje terapeutyczne na podstawie zmian stężenia fenytoiny w osoczu krwi Celem ćwiczenia jest wyznaczenie podstawowych parametrów charakteryzujących kinetykę
ĆWICZENIE 3 Farmakokinetyka nieliniowa i jej konsekwencje terapeutyczne na podstawie zmian stężenia fenytoiny w osoczu krwi Celem ćwiczenia jest wyznaczenie podstawowych parametrów charakteryzujących kinetykę
ĆWICZENIE 2. Farmakokinetyka wlewu dożylnego
 ĆWICZENIE 2 Farmakokinetyka wlewu dożylnego Celem ćwiczenia jest wyznaczenie parametrów farmakokinetycznych leku podanego drogą wlewu dożylnego w modelu 1-kompartmentowym z wykorzystaniem programu TopFit
ĆWICZENIE 2 Farmakokinetyka wlewu dożylnego Celem ćwiczenia jest wyznaczenie parametrów farmakokinetycznych leku podanego drogą wlewu dożylnego w modelu 1-kompartmentowym z wykorzystaniem programu TopFit
ZAPROSZENIE DO SKŁADANIA OFERT CENOWYCH NR 30/ ARG. Osoba do kontaktu: Joanna Lipner
 Warszawa, dnia 27/05/2017 ZAPROSZENIE DO SKŁADANIA OFERT CENOWYCH NR 30/2017 - ARG I. ZAMAWIAJĄCY: OncoArendi Therapeutics SA ul. Żwirki i Wigury 101 02-089 Warszawa NIP: 728 27 89 248 Osoba do kontaktu:
Warszawa, dnia 27/05/2017 ZAPROSZENIE DO SKŁADANIA OFERT CENOWYCH NR 30/2017 - ARG I. ZAMAWIAJĄCY: OncoArendi Therapeutics SA ul. Żwirki i Wigury 101 02-089 Warszawa NIP: 728 27 89 248 Osoba do kontaktu:
LEKI CHEMICZNE A LEKI BIOLOGICZNE
 LEKI CHEMICZNE A LEKI BIOLOGICZNE PRODUKT LECZNICZY - DEFINICJA Art. 2 pkt.32 Ustawy - Prawo farmaceutyczne Substancja lub mieszanina substancji, przedstawiana jako posiadająca właściwości: zapobiegania
LEKI CHEMICZNE A LEKI BIOLOGICZNE PRODUKT LECZNICZY - DEFINICJA Art. 2 pkt.32 Ustawy - Prawo farmaceutyczne Substancja lub mieszanina substancji, przedstawiana jako posiadająca właściwości: zapobiegania
Potrzeby instytutów badawczych w zakresie wsparcia procesu rozwoju nowych leków, terapii, urządzeń medycznych... OŚRODEK TRANSFERU TECHNOLOGII
 Potrzeby instytutów badawczych w zakresie wsparcia procesu rozwoju nowych leków, terapii, urządzeń medycznych... DR ADAM SOBCZAK OŚRODEK TRANSFERU TECHNOLOGII BIO&TECHNOLOGY INNOVATIONS PLATFORM POLCRO
Potrzeby instytutów badawczych w zakresie wsparcia procesu rozwoju nowych leków, terapii, urządzeń medycznych... DR ADAM SOBCZAK OŚRODEK TRANSFERU TECHNOLOGII BIO&TECHNOLOGY INNOVATIONS PLATFORM POLCRO
Prowadzenie badań klinicznych praktyczne aspekty według metodologii Good Clinical Practice (GCP)
 URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH, WYROBÓW MEDYCZNYCH I PRODUKTÓW BIOBÓJCZYCH Prowadzenie badań klinicznych praktyczne aspekty według metodologii Good Clinical Practice (GCP) Michał Gryz Departament
URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH, WYROBÓW MEDYCZNYCH I PRODUKTÓW BIOBÓJCZYCH Prowadzenie badań klinicznych praktyczne aspekty według metodologii Good Clinical Practice (GCP) Michał Gryz Departament
PROGRAM STAŻU. Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o.
 PROGRAM STAŻU Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o. Miejsce odbywania stażu / Legal address Muchoborska 8, 54-424 Wroclaw Stanowisko, obszar działania/
PROGRAM STAŻU Nazwa podmiotu oferującego staż / Company name IBM Global Services Delivery Centre Sp z o.o. Miejsce odbywania stażu / Legal address Muchoborska 8, 54-424 Wroclaw Stanowisko, obszar działania/
Podstawy projektowania leków wykład 1
 Podstawy projektowania leków wykład 1 Łukasz Berlicki Sprawy techniczne E-mail: lukasz.berlicki@pwr.edu.pl Konsultacje: p.322a/a2, wtorek, piątek, godz. 10-12 Egzamin, 27 stycznia, godz. 15.15 Poprawa
Podstawy projektowania leków wykład 1 Łukasz Berlicki Sprawy techniczne E-mail: lukasz.berlicki@pwr.edu.pl Konsultacje: p.322a/a2, wtorek, piątek, godz. 10-12 Egzamin, 27 stycznia, godz. 15.15 Poprawa
Metodologia prowadzenia badań klinicznych - wprowadzenie
 Metodologia badań klinicznych 15 Marca 2016 Metodologia prowadzenia badań klinicznych - wprowadzenie na podstawie definicji ICH GCP E9 oraz zaleceń WHO mgr inż. Katarzyna Draga Definicja badania klinicznego
Metodologia badań klinicznych 15 Marca 2016 Metodologia prowadzenia badań klinicznych - wprowadzenie na podstawie definicji ICH GCP E9 oraz zaleceń WHO mgr inż. Katarzyna Draga Definicja badania klinicznego
Prezentacja dla inwestorów
 Prezentacja dla inwestorów 4.10.2019 Sytuacja Spółki na półmetku 2019 r Zyskowna działalność Brak Valzka Ograniczony profit sharing Brak milestonów Wyższe koszty w obszarze infrastruktury i innowacji Koszty
Prezentacja dla inwestorów 4.10.2019 Sytuacja Spółki na półmetku 2019 r Zyskowna działalność Brak Valzka Ograniczony profit sharing Brak milestonów Wyższe koszty w obszarze infrastruktury i innowacji Koszty
Stowarzyszenie GCPpl w Polskiej Sieci Badań w Pediatrii
 Stowarzyszenie na Rzecz Dobrej Praktyki Badań Klinicznych w Polsce (Association for Good Clinical Practice in Poland) Stowarzyszenie w Polskiej Sieci Badań w Pediatrii Antoni Jędrzejowski, MD, PhD, PMP
Stowarzyszenie na Rzecz Dobrej Praktyki Badań Klinicznych w Polsce (Association for Good Clinical Practice in Poland) Stowarzyszenie w Polskiej Sieci Badań w Pediatrii Antoni Jędrzejowski, MD, PhD, PMP
Rozwój kliniczny leków. Studium porzypadków poszukiwania oszczędności i zarządzania ryzykiem Perspektywa średniej wielkości firmy biofarmaceutycznej
 Rozwój kliniczny leków. Studium porzypadków poszukiwania oszczędności i zarządzania ryzykiem Perspektywa średniej wielkości firmy biofarmaceutycznej dr n.med. Maciej Wieczorek Prezes Zarządu Celon Pharma
Rozwój kliniczny leków. Studium porzypadków poszukiwania oszczędności i zarządzania ryzykiem Perspektywa średniej wielkości firmy biofarmaceutycznej dr n.med. Maciej Wieczorek Prezes Zarządu Celon Pharma
Tabletten Liebigstraße Flörsheim/Main Niemcy. Vertisan 16 mg Таблетка. Vertisan 8 mg Tableta 8 mg tabletki podanie doustne
 ANEKS I WYKAZ NAZW, POSTAĆ(CI) FARMACEUTYCZNA(YCH), MOC(Y) PRODUKTÓW LECZNICZYCH, DROGA(DRÓG) PODANIA, WNIOSKODAWCA(Y), PODMIOT(Y) ODPOWIEDZIALNY(E) POSIADAJĄCY(E) POZWOLENIE NA DOPUSZCZENIE DO OBROTU
ANEKS I WYKAZ NAZW, POSTAĆ(CI) FARMACEUTYCZNA(YCH), MOC(Y) PRODUKTÓW LECZNICZYCH, DROGA(DRÓG) PODANIA, WNIOSKODAWCA(Y), PODMIOT(Y) ODPOWIEDZIALNY(E) POSIADAJĄCY(E) POZWOLENIE NA DOPUSZCZENIE DO OBROTU
Rola badań klinicznych faz wczesnych w procesie rejestracji produktów leczniczych
 Rola badań klinicznych faz wczesnych w procesie rejestracji produktów leczniczych Dr Katarzyna Jarus-Dziedzic Prezes i Dyrektor Medyczny i Naukowy BioVirtus Research Site Sp. z o. o. Od cząsteczki do leku
Rola badań klinicznych faz wczesnych w procesie rejestracji produktów leczniczych Dr Katarzyna Jarus-Dziedzic Prezes i Dyrektor Medyczny i Naukowy BioVirtus Research Site Sp. z o. o. Od cząsteczki do leku
PROJECT. Syllabus for course Principles of Marketing. on the study program: Administration
 Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Principles of Marketing on the study program: Administration I. General information
Poznań, 2012, September 20th Doctor Anna Scheibe adiunct in the Department of Economic Sciences PROJECT Syllabus for course Principles of Marketing on the study program: Administration I. General information
Farmakologia nauka o interakcjach pomiędzy substancjami chemicznymi a żywymi organizmami.
 Farmakologia nauka o interakcjach pomiędzy substancjami chemicznymi a żywymi organizmami. Każda substancja chemiczna oddziałująca na organizmy żywe może być zdefiniowana jako środek farmakologiczny (ang.
Farmakologia nauka o interakcjach pomiędzy substancjami chemicznymi a żywymi organizmami. Każda substancja chemiczna oddziałująca na organizmy żywe może być zdefiniowana jako środek farmakologiczny (ang.
Potrafi objaśnić wymogi i metody kontroli jakości leków. Zna założenia i zasady programu kwalifikacji dostawców
 WIEDZA K_W01 K_W02 K_W03 K_W04 K_W05 K_W06 K_W07 K_W08 K_W09 K_W10 K_W11 K_W12 K_W13 K_W14 K_W15 K_W16 K_W17 Charakteryzuje współczesne metody projektowania i otrzymywania leków w oparciu o naturalne źródła
WIEDZA K_W01 K_W02 K_W03 K_W04 K_W05 K_W06 K_W07 K_W08 K_W09 K_W10 K_W11 K_W12 K_W13 K_W14 K_W15 K_W16 K_W17 Charakteryzuje współczesne metody projektowania i otrzymywania leków w oparciu o naturalne źródła
KARTA KURSU (realizowanego w module specjalności) Biologia z chemią
 KARTA KURSU (realizowanego w module specjalności) Biologia z chemią.. (nazwa specjalności) Nazwa Nazwa w j. ang. Chemia leków Medicinal Chemistry Kod Punktacja ECTS* 1 Koordynator Dr Iwona Stawoska Zespół
KARTA KURSU (realizowanego w module specjalności) Biologia z chemią.. (nazwa specjalności) Nazwa Nazwa w j. ang. Chemia leków Medicinal Chemistry Kod Punktacja ECTS* 1 Koordynator Dr Iwona Stawoska Zespół
Magdalena Szymaniak EMA, Biologics Working Party
 Magdalena Szymaniak EMA, Biologics Working Party Punkty prezentacji Biologiczne produkty lecznicze, w tym referencyjne i biopodobne Sposoby rejestracji leków biologicznych Wymagania rejestracyjne dla leków
Magdalena Szymaniak EMA, Biologics Working Party Punkty prezentacji Biologiczne produkty lecznicze, w tym referencyjne i biopodobne Sposoby rejestracji leków biologicznych Wymagania rejestracyjne dla leków
Faculty: Management and Finance. Management
 Faculty: Management and Finance The name of field of study: Management Type of subject: basic Supervisor: prof. nadzw. dr hab. Anna Antczak-Barzan Studies level (BSc or MA): bachelor studies Type of studies:
Faculty: Management and Finance The name of field of study: Management Type of subject: basic Supervisor: prof. nadzw. dr hab. Anna Antczak-Barzan Studies level (BSc or MA): bachelor studies Type of studies:
KOŁO NAUKOWE IMMUNOLOGII. Mikrochimeryzm badania w hodowlach leukocytów in vitro
 KOŁO NAUKOWE IMMUNOLOGII Mikrochimeryzm badania w hodowlach leukocytów in vitro Koło Naukowe Immunolgii kolo_immunologii@biol.uw.edu.pl kolo_immunologii.kn@uw.edu.pl CEL I PRZEDMIOT PROJEKTU Celem doświadczenia
KOŁO NAUKOWE IMMUNOLOGII Mikrochimeryzm badania w hodowlach leukocytów in vitro Koło Naukowe Immunolgii kolo_immunologii@biol.uw.edu.pl kolo_immunologii.kn@uw.edu.pl CEL I PRZEDMIOT PROJEKTU Celem doświadczenia
CYKL ŻYCIA LEKU OD POMYSŁU DO WDROŻENIA
 CYKL ŻYCIA LEKU OD POMYSŁU DO WDROŻENIA PUNKTY KLUCZOWE PROCESU Wynalezienie substancji Patent Badania Przed- kliniczne Badania Kliniczne Produkcja (skala micro) Ustalenie nazwy handlowej i jej zastrzeżenie
CYKL ŻYCIA LEKU OD POMYSŁU DO WDROŻENIA PUNKTY KLUCZOWE PROCESU Wynalezienie substancji Patent Badania Przed- kliniczne Badania Kliniczne Produkcja (skala micro) Ustalenie nazwy handlowej i jej zastrzeżenie
Opis zakładanych efektów kształcenia na studiach podyplomowych: WIEDZA
 Opis zakładanych efektów kształcenia na studiach podyplomowych: Nazwa studiów: Farmacja przemysłowa Typ studiów: doskonalące Załącznik nr 7 zarządzenie Rektora UJ z 15 lutego 2012 Symbol Efekty kształcenia
Opis zakładanych efektów kształcenia na studiach podyplomowych: Nazwa studiów: Farmacja przemysłowa Typ studiów: doskonalące Załącznik nr 7 zarządzenie Rektora UJ z 15 lutego 2012 Symbol Efekty kształcenia
WULS Plant Health-Warsaw Plant Health Initiative Regpot (EU FP7)
 SZKOŁA GŁÓWNA GOSPODARSTWA WIEJSKIEGO W WARSZAWIE Wydział Ogrodnictwa, Biotechnologii i Architektury Krajobrazu WULS Plant Health-Warsaw Plant Health Initiative Regpot -2011-1 (EU FP7) SZKOŁA GŁÓWNA GOSPODARSTWA
SZKOŁA GŁÓWNA GOSPODARSTWA WIEJSKIEGO W WARSZAWIE Wydział Ogrodnictwa, Biotechnologii i Architektury Krajobrazu WULS Plant Health-Warsaw Plant Health Initiative Regpot -2011-1 (EU FP7) SZKOŁA GŁÓWNA GOSPODARSTWA
ĆWICZENIE 1. Farmakokinetyka podania dożylnego i pozanaczyniowego leku w modelu jednokompartmentowym
 ĆWICZENIE 1 Farmakokinetyka podania dożylnego i pozanaczyniowego leku w modelu jednokompartmentowym Celem ćwiczenia jest wyznaczenie parametrów farmakokinetycznych leków podanych w jednorazowych dawkach:
ĆWICZENIE 1 Farmakokinetyka podania dożylnego i pozanaczyniowego leku w modelu jednokompartmentowym Celem ćwiczenia jest wyznaczenie parametrów farmakokinetycznych leków podanych w jednorazowych dawkach:
Dom Development S.A., Pl. Piłsudskiego 3, 00-078 Warsaw
 Jarosław Szanajca President of the Management Board Age: 45 Higher, Master of Law, Department of Law and Administration, Warsaw University 1996 present Dom Development S.A. in Warsaw, President of the
Jarosław Szanajca President of the Management Board Age: 45 Higher, Master of Law, Department of Law and Administration, Warsaw University 1996 present Dom Development S.A. in Warsaw, President of the
KARTA KURSU. Podstawy toksykologii. Kod Punktacja ECTS* 1
 KARTA KURSU Nazwa Nazwa w j. ang. Podstawy toksykologii Basis of toxicology Kod Punktacja ECTS* 1 Koordynator Dr hab. Grzegorz Formicki Zespół dydaktyczny Prof. dr bab Peter Massanyi Dr hab. Grzegorz Formicki
KARTA KURSU Nazwa Nazwa w j. ang. Podstawy toksykologii Basis of toxicology Kod Punktacja ECTS* 1 Koordynator Dr hab. Grzegorz Formicki Zespół dydaktyczny Prof. dr bab Peter Massanyi Dr hab. Grzegorz Formicki
Clinical Trials. Anna Dziąg, MD, ąg,, Associate Director Site Start Up Quintiles
 Polandchallenges in Clinical Trials Anna Dziąg, MD, ąg,, Associate Director Site Start Up Quintiles Poland- legislation 1996-2003 Ustawa z dnia 5 grudnia 1996 r o zawodach lekarza i lekarza dentysty, z
Polandchallenges in Clinical Trials Anna Dziąg, MD, ąg,, Associate Director Site Start Up Quintiles Poland- legislation 1996-2003 Ustawa z dnia 5 grudnia 1996 r o zawodach lekarza i lekarza dentysty, z
Towards Stability Analysis of Data Transport Mechanisms: a Fluid Model and an Application
 Towards Stability Analysis of Data Transport Mechanisms: a Fluid Model and an Application Gayane Vardoyan *, C. V. Hollot, Don Towsley* * College of Information and Computer Sciences, Department of Electrical
Towards Stability Analysis of Data Transport Mechanisms: a Fluid Model and an Application Gayane Vardoyan *, C. V. Hollot, Don Towsley* * College of Information and Computer Sciences, Department of Electrical
KWESTIONARIUSZ OCENY RYZYKA / INSURANCE QUESTIONNAIRE
 Ubezpieczenie odpowiedzialności cywilnej z tytułu prowadzenia badań klinicznych/ Clinical trials liability insurance KWESTIONARIUSZ OCENY RYZYKA / INSURANCE QUESTIONNAIRE ZEZWOLENIA PUNU NR 1098/02 I NR
Ubezpieczenie odpowiedzialności cywilnej z tytułu prowadzenia badań klinicznych/ Clinical trials liability insurance KWESTIONARIUSZ OCENY RYZYKA / INSURANCE QUESTIONNAIRE ZEZWOLENIA PUNU NR 1098/02 I NR
Space for your logo, a photograph etc. Action 3.3.1 (WBU) www.viaregiaplus.eu
 Space for your logo, a photograph etc. Action 3.3.1 (WBU) THE ANALYSIS CONCERNING THE DESIGNATION OF THE ROUTE THAT INTEGRATES THE SOUTH OF THE LOWER SILESIA PROVINCE TOGETHER WITH NORTH - SOUTHLINKS Analiza
Space for your logo, a photograph etc. Action 3.3.1 (WBU) THE ANALYSIS CONCERNING THE DESIGNATION OF THE ROUTE THAT INTEGRATES THE SOUTH OF THE LOWER SILESIA PROVINCE TOGETHER WITH NORTH - SOUTHLINKS Analiza
The list of 20 abstracts, prepared in March 2005 CIS (994-1013) [Nr 31]
![The list of 20 abstracts, prepared in March 2005 CIS (994-1013) [Nr 31] The list of 20 abstracts, prepared in March 2005 CIS (994-1013) [Nr 31]](/thumbs/33/16311607.jpg) The list of 20 abstracts, prepared in March 2005 CIS (994-1013) [Nr 31] 994. pracy w Polsce do standardów Unii Europejskiej : Część A. Program realizacji badań naukowych i prac rozwojowych 1.01 31.12.2002.
The list of 20 abstracts, prepared in March 2005 CIS (994-1013) [Nr 31] 994. pracy w Polsce do standardów Unii Europejskiej : Część A. Program realizacji badań naukowych i prac rozwojowych 1.01 31.12.2002.
Harmonogram zajęć dla kierunku: Dietetyka, studia stacjonarne, II rok, semestr IV
 Harmonogram zajęć dla kierunku: Dietetyka, studia stacjonarne, II rok, semestr IV Przedmiot: Podstawy farmakologii i farmakoterapii żywieniowej oraz interakcji leków z żywnością Wykłady (5 wykładów, każdy
Harmonogram zajęć dla kierunku: Dietetyka, studia stacjonarne, II rok, semestr IV Przedmiot: Podstawy farmakologii i farmakoterapii żywieniowej oraz interakcji leków z żywnością Wykłady (5 wykładów, każdy
Modelowy plan studiów dla wszystkich polskich specjalności status i nazwa przedmiotu liczba godz. zajęć w tygodniu punkty w c lk Semestr 0
 Modelowy plan studiów legenda: status przedmiotu: K wykład /moduł obowiązkowy dla wszystkich studentów kier. Biotechnologia HES przedmiot humanistyczno-ekonomiczno-społeczny LD obowiazkowe lab. przeddyplomowe
Modelowy plan studiów legenda: status przedmiotu: K wykład /moduł obowiązkowy dla wszystkich studentów kier. Biotechnologia HES przedmiot humanistyczno-ekonomiczno-społeczny LD obowiazkowe lab. przeddyplomowe
Czy można zastosować ultradźwięki do niszczenia tkanki nowotworowej?
 Czy można zastosować ultradźwięki do niszczenia tkanki nowotworowej? Bezpośrednie działanie mało efektywne, efekty uboczne ( T), problemy z selektywnością In vitro działanie na wyizolowane DNA degradacja
Czy można zastosować ultradźwięki do niszczenia tkanki nowotworowej? Bezpośrednie działanie mało efektywne, efekty uboczne ( T), problemy z selektywnością In vitro działanie na wyizolowane DNA degradacja
ANEKS I. Strona 1 z 5
 ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC WETERYNARYJNYCH PRODUKTÓW LECZNICZYCH, GATUNKI ZWIERZĄT, DROGA PODANIA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH
ANEKS I WYKAZ NAZW, POSTAĆ FARMACEUTYCZNA, MOC WETERYNARYJNYCH PRODUKTÓW LECZNICZYCH, GATUNKI ZWIERZĄT, DROGA PODANIA, PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU W PAŃSTWACH
Zasady prowadzenia badań klinicznych
 Ocena skuteczności i bezpieczeństwa leku X u chorych z samoistnym łagodnym Zasady prowadzenia badań klinicznych nadciśnieniem tętniczym. Badanie randomizowane, podwójnie zaślepione, kontrolowane placebo,
Ocena skuteczności i bezpieczeństwa leku X u chorych z samoistnym łagodnym Zasady prowadzenia badań klinicznych nadciśnieniem tętniczym. Badanie randomizowane, podwójnie zaślepione, kontrolowane placebo,
Katedra Technologii Postaci Leku i Biofaramcji. W zakresie wiedzy:
 Sylabus modułów kształcenia Nazwa Wydziału Nazwa jednostki prowadzącej moduł Nazwa modułu kształcenia modułu Język kształcenia Efekty kształcenia dla modułu kształcenia Typ modułu kształcenia (obowiązkowy/fakultatywny)
Sylabus modułów kształcenia Nazwa Wydziału Nazwa jednostki prowadzącej moduł Nazwa modułu kształcenia modułu Język kształcenia Efekty kształcenia dla modułu kształcenia Typ modułu kształcenia (obowiązkowy/fakultatywny)
Wyniki H Wrzesień
 Wyniki H1 2017 Wrzesień 2017 www.selvita.com DISCLAIMER Niniejszy dokument nie stanowi oferty publicznej w rozumieniu ustawy z dnia 29 lipca 2005 r. o ofercie publicznej i warunkach wprowadzania instrumentów
Wyniki H1 2017 Wrzesień 2017 www.selvita.com DISCLAIMER Niniejszy dokument nie stanowi oferty publicznej w rozumieniu ustawy z dnia 29 lipca 2005 r. o ofercie publicznej i warunkach wprowadzania instrumentów
efekty kształcenia grupa zajęć** K7_K03 K7_W05 K7_U02 K7_W05 A Z K7_K02 K7_W05 K7_U02 A Z K7_U03 K7_U04 K7_W01
 WYDZIAŁ: KIERUNEK: poziom kształcenia: profil: forma studiów: PLAN STUDIÓW Wydział Chemiczny Zielone Technologie i Monitoring / Green Technologies and Monitoring II stopnia ogólnoakademicki stacjonarne
WYDZIAŁ: KIERUNEK: poziom kształcenia: profil: forma studiów: PLAN STUDIÓW Wydział Chemiczny Zielone Technologie i Monitoring / Green Technologies and Monitoring II stopnia ogólnoakademicki stacjonarne
Katedra i Zakład Anatomii Prawidłowej A Z. 1. Anatomia człowieka. 2. Biofizyka Katedra i Zakład Biofizyki B Z
 PLAN STUDIÓW rok akadem. 2018/19 Kierunek: farmacja Rok: I Semestr: I II Lp. Przedmiot Jednostka organizująca Kateg. liczba godzin Razem I sem. II sem. Wykłady Ćwiczenia Seminaria Samokształc. I sem. II
PLAN STUDIÓW rok akadem. 2018/19 Kierunek: farmacja Rok: I Semestr: I II Lp. Przedmiot Jednostka organizująca Kateg. liczba godzin Razem I sem. II sem. Wykłady Ćwiczenia Seminaria Samokształc. I sem. II
Podstawy automatyki. Energetics 1 st degree (1st degree / 2nd degree) General (general / practical) Full-time (full-time / part-time)
 MODULE DESCRIPTION Module code Module name Podstawy automatyki Module name in English The Fundamentals of Automatic Control Valid from academic year 2012/2013 MODULE PLACEMENT IN THE SYLLABUS Subject Level
MODULE DESCRIPTION Module code Module name Podstawy automatyki Module name in English The Fundamentals of Automatic Control Valid from academic year 2012/2013 MODULE PLACEMENT IN THE SYLLABUS Subject Level
PLAN STUDIÓW na rok akademicki 2018/2019 uchwalony przez Radę Wydziału w dniu nr Uchwały 31/4/2018
 Rok studiów I 1 obowiązkowe Anatomia 15 45 15 60 zal. 1 60 1 2 obowiązkowe Anatomia 15 15 15 zal. 2 15 2 3 obowiązkowe Biofizyka 14 45 14 59 zal. 1 59 1 4 obowiązkowe Biofizyka 16 16 16 zal. 2 16 2 5 obowiązkowe
Rok studiów I 1 obowiązkowe Anatomia 15 45 15 60 zal. 1 60 1 2 obowiązkowe Anatomia 15 15 15 zal. 2 15 2 3 obowiązkowe Biofizyka 14 45 14 59 zal. 1 59 1 4 obowiązkowe Biofizyka 16 16 16 zal. 2 16 2 5 obowiązkowe
I INTERNATIONAL SCIENTIFIC CONFERENCE
 I INTERNATIONAL SCIENTIFIC CONFERENCE EU SECURITY AND CRISIS MANAGEMENT FLOOD-2010 ATENEUM UNIVERSITY IN GDANSK P FUNDATION PRO POMERANIA NOTICE NO. 1 I International Scientific Conference EU SECURITY
I INTERNATIONAL SCIENTIFIC CONFERENCE EU SECURITY AND CRISIS MANAGEMENT FLOOD-2010 ATENEUM UNIVERSITY IN GDANSK P FUNDATION PRO POMERANIA NOTICE NO. 1 I International Scientific Conference EU SECURITY
Aneks II. Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję ds. Leków
 Aneks II Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję ds. Leków 4 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej produktu Furosemide Vitabalans i nazw produktów
Aneks II Wnioski naukowe i podstawy do odmowy przedstawione przez Europejską Agencję ds. Leków 4 Wnioski naukowe Ogólne podsumowanie oceny naukowej dotyczącej produktu Furosemide Vitabalans i nazw produktów
Informacje ogólne o kierunku studiów
 Informacje ogólne o kierunku studiów kierunku studiów Poziom kształcenia Liczba ów i liczba punktów konieczna do ukończenia studiów na danym poziomie Profil kształcenia Formy studiów Tytuł zawodowy uzyskany
Informacje ogólne o kierunku studiów kierunku studiów Poziom kształcenia Liczba ów i liczba punktów konieczna do ukończenia studiów na danym poziomie Profil kształcenia Formy studiów Tytuł zawodowy uzyskany
4) badanie zanieczyszczeń: mineralnych, biologicznych lub botanicznych innych niż opisanych dla homeopatycznej substancji czynnej; 5) oznaczenie
 Załącznik nr 4 Sposób przedstawiania dokumentacji dotyczącej jakości dołączanej do wniosku o dopuszczenie do obrotu produktów leczniczych homeopatycznych z użyciem formatu CTD Celem tego załącznika jest
Załącznik nr 4 Sposób przedstawiania dokumentacji dotyczącej jakości dołączanej do wniosku o dopuszczenie do obrotu produktów leczniczych homeopatycznych z użyciem formatu CTD Celem tego załącznika jest
WYKLUCZENIE CYFROWE NA RYNKU PRACY. redakcja naukowa Elżbieta Kryńska i Łukasz Arendt
 WYKLUCZENIE CYFROWE NA RYNKU PRACY redakcja naukowa Elżbieta Kryńska i Łukasz Arendt Warszawa 2010 SPIS TREŚCI WYKAZ UŻYWANYCH SKRÓTÓW 9 V WPROWADZENIE - ZARYS PROBLEMATYKI BADAWCZEJ (Elżbieta Kryńska,
WYKLUCZENIE CYFROWE NA RYNKU PRACY redakcja naukowa Elżbieta Kryńska i Łukasz Arendt Warszawa 2010 SPIS TREŚCI WYKAZ UŻYWANYCH SKRÓTÓW 9 V WPROWADZENIE - ZARYS PROBLEMATYKI BADAWCZEJ (Elżbieta Kryńska,
FORMULARZ DLA OGŁOSZENIODAWCÓW
 FORMULARZ DLA OGŁOSZENIODAWCÓW INSTYTUCJA: Uniwersytet Kazimierza Wielkiego, Wydział Administracji i Nauk Społecznych, Katedra Informacji Naukowej i Bibliologii. MIASTO: Bydgoszcz STANOWISKO: adiunkt DYSCYPLINA
FORMULARZ DLA OGŁOSZENIODAWCÓW INSTYTUCJA: Uniwersytet Kazimierza Wielkiego, Wydział Administracji i Nauk Społecznych, Katedra Informacji Naukowej i Bibliologii. MIASTO: Bydgoszcz STANOWISKO: adiunkt DYSCYPLINA
3 GENERAL INFORMATION ABOUT THE CLINICAL TRIAL
 Page 1 of 6 1 TRIAL NAME Brief trial name: A clinical trial to measure tapentadol in the bloodstream of young children after they drink it Full trial name: Open-label evaluation of the population pharmacokinetic
Page 1 of 6 1 TRIAL NAME Brief trial name: A clinical trial to measure tapentadol in the bloodstream of young children after they drink it Full trial name: Open-label evaluation of the population pharmacokinetic
Możliwości dofinansowania z priorytetu Zdrowie, Horyzont 2020 Innovative Medicines Initiative 2 Joint Undertaking
 Jak ugryźć 10 milionów cz. IV - Finansowanie badań naukowych 21.05.2015 Warszawa Możliwości dofinansowania z priorytetu Zdrowie, Horyzont 2020 Innovative Medicines Initiative 2 Joint Undertaking W niniejszej
Jak ugryźć 10 milionów cz. IV - Finansowanie badań naukowych 21.05.2015 Warszawa Możliwości dofinansowania z priorytetu Zdrowie, Horyzont 2020 Innovative Medicines Initiative 2 Joint Undertaking W niniejszej
Alternatywne metody badania kosmetyków
 Alternatywne metody badania kosmetyków Błażej Dolniak, PhD Cell Line Research Wprowadzenie Before humans can be exposed to new chemical substances their tendency to cause skin damage must be determined
Alternatywne metody badania kosmetyków Błażej Dolniak, PhD Cell Line Research Wprowadzenie Before humans can be exposed to new chemical substances their tendency to cause skin damage must be determined
Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych?
 Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych? prof. dr hab. med.. Piotr Fiedor Warszawski Uniwersytet Medyczny
Kiedy lekarz powinien decydować o wyborze terapii oraz klinicznej ocenie korzyści do ryzyka stosowania leków biologicznych lub biopodobnych? prof. dr hab. med.. Piotr Fiedor Warszawski Uniwersytet Medyczny
PLAN STUDIÓW na rok akademicki 2018/2019 uchwalony przez Radę Wydziału w dniu nr Uchwały 31/4/2018
 Rok studiów I 1 obowiązkowe Anatomia 15 15 45 30 75 zal. 3 75 3 2 obowiązkowe Biofizyka 14 16 45 30 75 zal. 3 75 3 3 obowiązkowe Biologia i genetyka 30 6 24 90 60 150 egz. 6 150 6 4 obowiązkowe Botanika
Rok studiów I 1 obowiązkowe Anatomia 15 15 45 30 75 zal. 3 75 3 2 obowiązkowe Biofizyka 14 16 45 30 75 zal. 3 75 3 3 obowiązkowe Biologia i genetyka 30 6 24 90 60 150 egz. 6 150 6 4 obowiązkowe Botanika
CZ.II S/T Scientific and/or technological excellence Naukowa i/lub technologiczna doskonałość formularz B
 Szkolenie SGGW, 03.11.2009 CZ.II S/T Scientific and/or technological excellence Naukowa i/lub technologiczna doskonałość formularz B Joanna Niedziałek Krajowy Punkt Kontaktowy Programów Badawczych UE Instytut
Szkolenie SGGW, 03.11.2009 CZ.II S/T Scientific and/or technological excellence Naukowa i/lub technologiczna doskonałość formularz B Joanna Niedziałek Krajowy Punkt Kontaktowy Programów Badawczych UE Instytut
kierunek: Biologia studia niestacjonarne II stopnia realizacja od roku akad. 2017/2018 Przedmioty podstawowe Przedmioty kierunkowe
 Zatwierdzono na Radzie Wydziału 21.06.2017 Przedmioty podstawowe specjalność: Biologia środowiskowa I rok II rok Wymiar godzin 1 sem 2 sem 3 sem 4 sem ćw. ćw. wyk. w. ćw. w. ćw. w. ćw. w. ćw. aud. lab.
Zatwierdzono na Radzie Wydziału 21.06.2017 Przedmioty podstawowe specjalność: Biologia środowiskowa I rok II rok Wymiar godzin 1 sem 2 sem 3 sem 4 sem ćw. ćw. wyk. w. ćw. w. ćw. w. ćw. w. ćw. aud. lab.
kierunek: Biologia studia stacjonarne II stopnia realizacja od roku akad. 2017/2018 Przedmioty podstawowe Przedmioty kierunkowe
 Zatwierdzono na Radzie Wydziału 21.06.2017 Przedmioty podstawowe specjalność: Biologia środowiskowa I rok II rok Wymiar godzin 1 sem 2 sem 3 sem 4 sem ćw. ćw. wyk. w. ćw. w. ćw. w. ćw. w. ćw. aud. lab.
Zatwierdzono na Radzie Wydziału 21.06.2017 Przedmioty podstawowe specjalność: Biologia środowiskowa I rok II rok Wymiar godzin 1 sem 2 sem 3 sem 4 sem ćw. ćw. wyk. w. ćw. w. ćw. w. ćw. w. ćw. aud. lab.
LEARNING AGREEMENT FOR STUDIES
 LEARNING AGREEMENT FOR STUDIES The Student First and last name(s) Nationality E-mail Academic year 2014/2015 Study period 1 st semester 2 nd semester Study cycle Bachelor Master Doctoral Subject area,
LEARNING AGREEMENT FOR STUDIES The Student First and last name(s) Nationality E-mail Academic year 2014/2015 Study period 1 st semester 2 nd semester Study cycle Bachelor Master Doctoral Subject area,
1. Metryczka. Wydział Farmaceutyczny. Nazwa Wydziału:
 Fakultet przygotowany w ramach projektu WUM AID Akademia Innowacyjnej Dydaktyki Warszawskiego Uniwersytetu Medycznego współfinansowanego ze środków Europejskiego Funduszu Społecznego w ramach POWER 2014-2020
Fakultet przygotowany w ramach projektu WUM AID Akademia Innowacyjnej Dydaktyki Warszawskiego Uniwersytetu Medycznego współfinansowanego ze środków Europejskiego Funduszu Społecznego w ramach POWER 2014-2020
Forma kształcenia: jednolite magisterskie. Katedrai Zakład Anatomii Prawidłowej Katedra i Zakład Biofizyki A Z. 1.
 PLAN STUDIÓW rok akadem. 2017/18 Kierunek: farmacja Rok: I Semestr: I II studiów: stacjonarne Lp. Przedmiot Jednostka organizująca Kategoria liczba godzin Razem I sem. II sem. Wykłady Liczba godzin kształcenia:
PLAN STUDIÓW rok akadem. 2017/18 Kierunek: farmacja Rok: I Semestr: I II studiów: stacjonarne Lp. Przedmiot Jednostka organizująca Kategoria liczba godzin Razem I sem. II sem. Wykłady Liczba godzin kształcenia:
PLANY I PROGRAMY STUDIÓW
 WYDZIAŁ INŻYNIERII PRODUKCJI I LOGISTYKI PLANY I PROGRAMY STUDIÓW STUDY PLANS AND PROGRAMS KIERUNEK STUDIÓW FIELD OF STUDY - INŻYNIERIA BEZPIECZEŃSTWA - SECURITY ENGINEERING Studia niestacjonarne pierwszego
WYDZIAŁ INŻYNIERII PRODUKCJI I LOGISTYKI PLANY I PROGRAMY STUDIÓW STUDY PLANS AND PROGRAMS KIERUNEK STUDIÓW FIELD OF STUDY - INŻYNIERIA BEZPIECZEŃSTWA - SECURITY ENGINEERING Studia niestacjonarne pierwszego
CI WYKSZTAŁCENIA I WYMIANY MI
 Attach photo here Print your first and last name on the reverse side of each photo To be typewritten in English. BIURO UZNAWALNOŚCI WYKSZTAŁCENIA I WYMIANY MIĘDZYNARODOWEJ ul. Smolna 13, 00-375 Warszawa
Attach photo here Print your first and last name on the reverse side of each photo To be typewritten in English. BIURO UZNAWALNOŚCI WYKSZTAŁCENIA I WYMIANY MIĘDZYNARODOWEJ ul. Smolna 13, 00-375 Warszawa
Katedrai Zakład Anatomii Prawidłowej. Anatomia człowieka A Z. Katedra i Zakład Biofizyki B Z. 2.
 PLAN STUDIÓW rok akadem. 2016/17 Kierunek: farmacja Rok: I Semestr: I II studiów: stacjonarne kształcenia: jednolite magisterskie Kateg. liczba godzin Razem I sem. Wykłady Ćwiczenia Seminaria Samokształc.
PLAN STUDIÓW rok akadem. 2016/17 Kierunek: farmacja Rok: I Semestr: I II studiów: stacjonarne kształcenia: jednolite magisterskie Kateg. liczba godzin Razem I sem. Wykłady Ćwiczenia Seminaria Samokształc.
Redakcja naukowa Stanislawa Borkowska i Anna Jawor- Joniewicz. Anna Rogozinska-Pawelczyk Barbara Sajkiewicz Piotr Chmielarz KSZTALTOWANIE
 Redakcja naukowa Stanislawa Borkowska i Anna Jawor- Joniewicz Anna Rogozinska-Pawelczyk Barbara Sajkiewicz Piotr Chmielarz KSZTALTOWANIE ZAANGAZOWANIA PRACOWNIRÖW W RONTERSCIE ZARZADZANIA RÖZNORODNOSCIA
Redakcja naukowa Stanislawa Borkowska i Anna Jawor- Joniewicz Anna Rogozinska-Pawelczyk Barbara Sajkiewicz Piotr Chmielarz KSZTALTOWANIE ZAANGAZOWANIA PRACOWNIRÖW W RONTERSCIE ZARZADZANIA RÖZNORODNOSCIA
Forma kształcenia: jednolite magisterskie. Katedrai Zakład Anatomii Prawidłowej Katedra i Zakład Biofizyki A Z. 1.
 PLAN STUDIÓW rok akadem. 2015/16 Kierunek: farmacja Rok: I Semestr: I II studiów: stacjonarne kształcenia: jednolite magisterskie Lp. Przedmiot Jednostka organizująca Kategoria liczba godzin Razem I sem.
PLAN STUDIÓW rok akadem. 2015/16 Kierunek: farmacja Rok: I Semestr: I II studiów: stacjonarne kształcenia: jednolite magisterskie Lp. Przedmiot Jednostka organizująca Kategoria liczba godzin Razem I sem.
OFERTA: 2. Szkolenia praktyczne z technik biochemicznych i analitycznych
 OFERTA: 1. Szkolenia otwarte, zamknięte i na życzenie 2. Szkolenia praktyczne z technik biochemicznych i analitycznych 3. Konsulting przy wdrażaniu GLP/GMP, ISO 17025, HACCP, ISO 9001, GMP Kosmetyczne,
OFERTA: 1. Szkolenia otwarte, zamknięte i na życzenie 2. Szkolenia praktyczne z technik biochemicznych i analitycznych 3. Konsulting przy wdrażaniu GLP/GMP, ISO 17025, HACCP, ISO 9001, GMP Kosmetyczne,
4. EKSPLOATACJA UKŁADU NAPĘD ZWROTNICOWY ROZJAZD. DEFINICJA SIŁ W UKŁADZIE Siła nastawcza Siła trzymania
 3 SPIS TREŚCI Przedmowa... 11 1. WPROWADZENIE... 13 1.1. Budowa rozjazdów kolejowych... 14 1.2. Napędy zwrotnicowe... 15 1.2.1. Napęd zwrotnicowy EEA-4... 18 1.2.2. Napęd zwrotnicowy EEA-5... 20 1.3. Współpraca
3 SPIS TREŚCI Przedmowa... 11 1. WPROWADZENIE... 13 1.1. Budowa rozjazdów kolejowych... 14 1.2. Napędy zwrotnicowe... 15 1.2.1. Napęd zwrotnicowy EEA-4... 18 1.2.2. Napęd zwrotnicowy EEA-5... 20 1.3. Współpraca
H11 advanced stage HL trial
 H11 advanced stage HL trial Baseline PET/CT + tumortarc and plasmatarc Experimental Arm Standard Arm 1 x ABVD 1 x BEAesc PET/CT + plasmatarc PET+ PET- PET+/- 3 x BEAesc 3 x ABVD 3 x BEAesc CT + plasmatarc
H11 advanced stage HL trial Baseline PET/CT + tumortarc and plasmatarc Experimental Arm Standard Arm 1 x ABVD 1 x BEAesc PET/CT + plasmatarc PET+ PET- PET+/- 3 x BEAesc 3 x ABVD 3 x BEAesc CT + plasmatarc
