AUTOREFERAT. Chiralne połączenia azirydynowe jako wysoce wydajne katalizatory wybranych reakcji syntezy asymetrycznej. Dr Michał Rachwalski
|
|
|
- Łucja Marciniak
- 7 lat temu
- Przeglądów:
Transkrypt
1 Załącznik nr 1 AUTREFERAT Chiralne połączenia azirydynowe jako wysoce wydajne katalizatory wybranych reakcji syntezy asymetrycznej Dr Michał Rachwalski Zakład Katalizy i Syntezy rganicznej, Katedra Chemii rganicznej i Stosowanej, Wydział Chemii, Uniwersytet Łódzki Łódź 2014
2 Spis treści 1. Dane osobowe Imię i nazwisko Posiadane dyplomy i stopnie naukowe Informacje o dotychczasowym zatrudnieniu Liczbowe zestawienie dorobku naukowego mówienie najważniejszych osiągnięć naukowych Spis publikacji stanowiących osiągnięcie naukowe Wstęp dotyczący tematyki badawczej mówienie wyników opisanych w publikacjach stanowiących osiągnięcie naukowe Pozostałe publikacje i osiągnięcia Publikacje dodatkowe Doniesienia konferencyjne agrody, wyróżnienia dbyte staże Udział w projektach naukowych Inna działalność związana z pracą naukowo-dydaktyczną oraz organizacyjną Członkowstwo w organizacjach naukowych
3 1. Dane osobowe 1.1. Imię i nazwisko Michał Rachwalski 1.2. Posiadane dyplomy i stopnie naukowe Pracę magisterską zatytułowaną Próby syntezy związków o potencjalnych właściwościach fluorescencyjnych wykonałem w Katedrze Chemii rganicznej Wyższej Szkoły Pedagogicznej (obecnie Akademii im. Jana Długosza) w Częstochowie pod kierunkiem dr Barbary Bachowskiej. Rozprawę doktorską zatytułowaną Katalizowane enzymami deracemizacje i desymetryzacje jako metody syntezy chiralnych połączeń heteroorganicznych wykonałem w Zakładzie Chemii eteroorganicznej Centrum Badań Molekularnych i Makromolekularnych Polskiej Akademii auk w Łodzi pod kierunkiem prof. dr hab. Piotra Kiełbasińskiego. iniejsza rozprawa ukazała nowe możliwości zastosowania enzymów w syntezie chiralnych nieracemicznych związków heteroorganicznych zawierających centrum stereogeniczne zarówno na atomie siarki lub fosforu, jak i na atomie węgla związanym z podstawnikiem heteroorganicznym. I tak, przykładowo, katalizowany enzymami dynamiczny kinetyczny rozdział racemicznych sulfonów arylowo-β-hydroksyalkilowych prowadził do uzyskania odpowiednich pochodnych acetylowych z wysokimi wydajnościami chemicznymi i o bardzo wysokich nadmiarach enancjomerycznych. Przeprowadzono również skuteczne enzymatyczne desymetryzacje prochiralnego sulfotlenku bis(hydroksymetylofenylowego), sulfotlenku bis(cyjanometylowego) oraz tlenku bis(cyjanometylo)fenylofosfiny. Warto zauważyć, iż metody enzymatyczne do desymetryzacji takich prochiralnych bis-nitryli heteroorganicznych zostały zastosowane po raz pierwszy. Rozprawa doktorska uzyskała wyróżnienie Rady aukowej CBMiM PA w Łodzi. 2
4 1.3. Informacje o dotychczasowym zatrudnieniu 01.XI IX.2008 pracownik inżynieryjno-techniczny, a następnie asystent w Zakładzie Chemii eteroorganicznej CBMiM PA w Łodzi 2.X.2008 obecnie adiunkt w Katedrze Chemii rganicznej i Stosowanej UŁ 1.4. Liczbowe zestawienie dorobku naukowego Prace oryginalne: - łącznie 23 prace (22 prace eksperymentalne w pełnej wersji, wszystkie w czasopismach zagranicznych oraz 1 praca przeglądowa w Chemical Society Reviews) w tym jako pierwszy autor 14 prac, jako autor do korespondencji 12 prac). Sumaryczny IF wszystkich prac: 88,867 (3,86 na jedną pracę) Suma punktów MiSW: 745 (32,39 na jedną pracę) Sumaryczny IF prac stanowiących podstawę habilitacji: 12,69 (2,12 na jedną pracę) Suma punktów MiSW prac stanowiących podstawę habilitacji: 180 (30,0 na jedną pracę) Sumaryczny IF prac przed uzyskaniem stopnia doktora: 15,632 (3,13 na jedną pracę) Suma punktów MiSW prac przed uzyskaniem stopnia doktora: 165 (33 na jedną pracę) Sumaryczny IF prac po uzyskaniu stopnia doktora: (4,07 na jedną pracę) Suma punktów MiSW prac po uzyskaniu stopnia doktora: 580 (32,22 na jedną pracę) 3
5 Całkowita liczba cytowań: 186 (wg Web of Science), 195 (wg Scopus) na dzień 27.I.2014 Indeks irscha: 9 (wg Web of Science), 10 (wg Scopus) na dzień 27.I.2014 Impact factor (IF) publikacji naukowych podano zgodnie z rokiem ich opublikowania. 2. mówienie najważniejszych osiągnięć naukowych 2.1. Spis publikacji stanowiących osiągnięcie naukowe 1. M. Rachwalski *, S. Jarzyński, S. Leśniak ighly efficient aziridine ring-containing chiral ligands as catalysts in asymmetric synthesis Tetrahedron: Asymmetry 2013, 24, oraz Synfacts 2013, 9, 0751 (brak IF) IF = 2,115 (30 pkt. MiSW) Mój wkład polegał na: przeprowadzeniu testowych reakcji asymetrycznych dla wszystkich otrzymanych katalizatorów, wydzieleniu i oczyszczeniu produktów w/w reakcji, analizie PLC, opisaniu i interpretacji wyników oraz napisaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 50%. Warto zauważyć, iż praca ta również ukazała się w Synfacts. 2. M. Rachwalski *, S. Jarzyński, M. Jasiński, S. Leśniak Mandelic acid derived α-aziridinyl alcohols as highly efficient ligands for asymmetric additions of zinc organyls to aldehydes Tetrahedron: Asymmetry 2013, 24, IF = 2,115 (30 pkt. MiSW) Mój wkład polegał częściowo na syntezie, wydzieleniu i oczyszczeniu nowo otrzymanych katalizatorów, przeprowadzeniu testowych reakcji asymetrycznych dla wszystkich otrzymanych katalizatorów, wydzieleniu i oczyszczeniu produktów w/w reakcji, analizie PLC, opisaniu i interpretacji wyników oraz częściowym napisaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 60%. 3. M. Rachwalski *, S. Jarzyński, S. Leśniak ighly efficient conjugate addition of diethylzinc to enones catalyzed by chiral ligands derived from -mandelic acid 4
6 Tetrahedron: Asymmetry 2013, 24, IF = 2,115 (30 pkt. MiSW) Mój wkład polegał częściowo na syntezie, wydzieleniu i oczyszczeniu nowo otrzymanych katalizatorów, przeprowadzeniu testowych reakcji asymetrycznych dla wszystkich otrzymanych katalizatorów, wydzieleniu i oczyszczeniu produktów w/w reakcji, analizie PLC, opisaniu i interpretacji wyników oraz napisaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 60%. 4. S. Leśniak, M. Rachwalski *, S. Jarzyński, E. bijalska Lactic acid derived aziridinyl alcohols as highly effective catalysts for asymmetric additions of organozinc species to aldehydes Tetrahedron: Asymmetry 2013, 24, IF = 2,115 (30 pkt. MiSW) Mój wkład polegał częściowo na syntezie, wydzieleniu i oczyszczeniu nowo otrzymanych katalizatorów, przeprowadzeniu testowych reakcji asymetrycznych dla wszystkich otrzymanych katalizatorów, wydzieleniu i oczyszczeniu produktów w/w reakcji, analizie PLC, opisaniu i interpretacji wyników oraz napisaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 70%. 5. M. Rachwalski * Limonene oxide derived aziridinyl alcohols as highly efficient catalysts for asymmetric additions of organozinc species to aldehydes Tetrahedron: Asymmetry 2013, IF = 2,115 (30 pkt. MiSW) Mój wkład polegał na syntezie, wydzieleniu i oczyszczeniu nowo otrzymanych katalizatorów, przeprowadzeniu testowych reakcji asymetrycznych dla wszystkich otrzymanych katalizatorów, wydzieleniu i oczyszczeniu produktów w/w reakcji, analizie PLC, opisaniu i interpretacji wyników oraz napisaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 100%. 6. S. Leśniak, A. M. Pieczonka, S. Jarzyński, K. Justyna, M. Rachwalski * Synthesis and evaluation of catalytic properties of semicarbazides derived from - triphenylmethyl-aziridine-2-carbohydrazides Tetrahedron: Asymmetry 2013, 24,
7 IF = 2,115 (30 pkt. MiSW) Mój wkład polegał na: przeprowadzeniu testowych reakcji asymetrycznych dla wszystkich otrzymanych katalizatorów, wydzieleniu i oczyszczeniu produktów w/w reakcji, analizie PLC, częściowym napisaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 20%. 6
8 2.2. Wstęp dotyczący tematyki badawczej Asymetryczna synteza organiczna jest ciągle intensywnie rozwijaną dziedziną chemii organicznej. Fakt, który ze stereoizomerów danej substancji optycznie czystej zostanie otrzymany w wyniku syntezy stereokontrolowanej jest szczególnie istotny, gdy w/w produkty reakcji mają znaleźć zastosowanie zwłaszcza w przemyśle farmaceutycznym czy spożywczym. Uzyskanie konkretnego stereoizomeru pożądanego związku jest ściśle zdeterminowane przez dobór odpowiedniego chiralnego katalizatora. Dlatego też, dalsze poszukiwanie efektywnych katalizatorów syntezy stereokontrolowanej pozostaje ciągle bardzo istotnym zagadnieniem w syntetycznej chemii organicznej. Moje zainteresowania badawcze początkowo dotyczyły zastosowania chiralnych, optycznie czystych aminoalkoholi jako efektywnych katalizatorów syntezy stereokontrolowanej. Jednakże, literatura chemiczna dotycząca użycia chiralnych katalizatorów tego typu w syntezie asymetrycznej, jest niezwykle bogata i spektrum nowych, możliwych do wykorzystania w budowaniu struktur katalizatorów chiralnych amin staje się coraz bardziej ograniczone. Elementem oryginalności moich badań jest użycie chiralnego lub achiralnego pierścienia azirydynowego jako funkcji aminowej w syntezie chiralnych aminoalkoholi jako potencjalnych katalizatorów w syntezie asymetrycznej. Cechą szczególną azirydyn jest tworzenie trwałych kompleksów z halogenkami cynku, co stwierdzono wcześniej w naszym ośrodku naukowym wykazując, iż azirydynyloketony tworzą z bromkiem lub chlorkiem cynku wyjątkowo trwałe kompleksy zbudowane z dwóch cząsteczek azirydyny i jednej cząsteczki halogenku cynku. 1 ajistotniejszą cechą tych kompleksów jest ich zdolność do ulegania całkowicie stereoselektywnej redukcji, przy użyciu borowodorku sodu, do odpowiednich azirydynyloalkoholi. 2,3 Z dwóch możliwych diastereoizomerów powstawał wyłącznie jeden. Ten sam stereochemiczny rezultat otrzymano, poddając redukcji wolny azirydynyloketon przy użyciu borowodorku cynku. atomiast stwierdzono, iż redukcja przy nieobecności soli cynku jest reakcją o bardzo niskiej stereoselektywności. Jedną z klasycznych reakcji testujących katalizatory do syntezy asymetrycznej jest reakcja addycji dietylocynku do aldehydów. Kierując się wcześniejszą wiedzą o kompleksotwórczych właściwościach azirydyn postanowiłem wcześniej zbadać 1 R. Faure,. Loiseleur, R. Bartnik, S. Leśniak, A. Laurent, Cryst. Struct. Commun. 1981, 10, R. Bartnik, S. Leśniak, A. Laurent, Tetrahedron Lett. 1981, R. Bartnik, S. Leśniak, A. Laurent, J. Chem. Res. 1982, 287,
9 efektywność takich ligandów, w których funkcję aminową pełniłby pierścień azirydynowy. Przykładowo, ligandy typu aminoalkoholi, zawierające chiralne aminy oraz dodatkowo, chiralne centrum sulfinylowe, wykazywały umiarkowaną aktywność katalityczną w reakcji addycji dietylocynku do benzaldehydu (nadmiary enancjomeryczne rzędu 50%). 4 Zmodyfikowanie tych związków przez wprowadzenie chiralnych azirydyn jako funkcji aminowych skutkowało podniesieniem ich efektywności w tej reakcji do przeciętnie 95% ee. 5 Podobnie, bardzo wysokie nadmiary enancjomeryczne uzyskano stosując te katalizatory w addycji dietylocynku do enonów 6 oraz addycji fenyloetynylocynku do aldehydów. 7 Powyższe obserwacje upoważniły mnie do postawienia hipotezy, że aminoalkohole, w których funkcję aminową pełni pierścień azirydynowy, będą niezwykle skutecznymi katalizatorami/ligandami w stereokontrolowanych reakcjach z udziałem jonów cynkowych. Moja strategia badawcza obejmowała syntezę pochodnych, w których do określonego achiralnego lub chiralnego rdzenia zawierającego grupę hydroksylową został dołączony pierścień chiralnej lub achiralnej azirydyny. ajprostszymi achiralnymi związkami wyjściowymi okazały się aromatyczne kwasy karboksylowe zawierające dodatkowo grupę hydroksylową (1). Transformacji grupy karboksylowej w pierścień azirydynowy dokonano przez przeprowadzenie najpierw grupy kwasowej w odpowiedni chlorek kwasowy, następnie w reakcji z azirydyną otrzymano odpowiednie amidy zawierające pierścień azirydynowy. Redukcja grupy karbonylowej amidu przy użyciu trietoksysilanu 8 prowadziła do azirydynyloalkoholi, w których chiralny pierścień azirydynowy wbudowany jest w achiralny alkohol (1). atomiast chiralne jednostki budulcowe zawierające grupę hydroksylową, były pochodnymi optycznie czynnych hydroksykwasów, takich jak kwas -(+)-migdałowy (2, 3) oraz kwas -(+)-mlekowy (4). Wprowadzenie zarówno chiralnej, jak i achiralnej azirydyny zostało zrealizowane poprzez przeprowadzenie w pierwszym etapie grupy karboksylowej w chlorek kwasowy, następnie reakcje z odpowiednią azirydyną i redukcję odpowiedniego amidu przy użyciu trietoksysilanu do pożądanego azirydynyloalkoholu. 4 M. Rachwalski, M. Kwiatkowska, J. Drabowicz, M. Kłos, W. M. Wieczorek, M. Szyrej, L. Sieroń, P. Kiełbasiński, Tetrahedron: Asymmetry 2008, 19, S. Leśniak, M. Rachwalski, E. Sznajder, P. Kiełbasiński, Tetrahedron: Asymmetry 2009, 20, M. Rachwalski, S. Leśniak, P. Kiełbasiński, Tetrahedron: Asymmetry 2010, 21, M. Rachwalski, S. Leśniak, P. Kiełbasiński, Tetrahedron: Asymmetry 2010, 21, S. Das, D. Addis, S. Zhou, K. Junge. M. Beller, J. Am. Chem. Soc. 2010, 132,
10 Podobny aspekt badawczy obejmuje syntezę azirydynyloalkoholi zbudowanych na układzie monoterpenu, jakim jest limonen (5). ajprostszą drogą syntezy tego typu układów jest reakcja nukleofilowego otwarcia pierścienia oksiranowego łatwo dostępnych optycznie czynnych oksiranów terpenów za pomocą pierścienia azirydynowego jako odczynnika nukleofilowego. statnią grupą chiralnych katalizatorów będących treścią niniejszego dokonania naukowego są związki będące pochodnymi -trifenylometyloazirydyno-2-karbohydrazydów (6). Wszystkie chiralne katalizatory otrzymane w postaci optycznie czystej zostały przebadane w reakcjach asymetrycznej addycji dietylocynku oraz fenyloetynylocynku do aldehydów aromatycznych i alifatycznych prowadząc do uzyskania odpowiednich chiralnych alkoholi z bardzo dobrymi wydajnościami chemicznymi oraz wysokimi wartościami nadmiarów enancjomerycznych. Jak wiadomo z wcześniejszych doniesień, 9 prosty difenylo-(1-fenyloetylo)azirydyn-2-ylo-metanol użyty jako ligand w reakcjach addycji dietylocynku do aldehydów pozwolił na otrzymanie adduktów z doskonałymi nadmiarami enancjomerycznymi, co wskazuje, że czynnikiem determinującym stereochemiczny wynik reakcji addycji jest konfiguracja pierścienia azirydynowego. Wyniki będące przedmiotem niniejszego dokonania naukowego w pełni potwierdzają tę obserwację. Co więcej, zaproponowany zestaw katalizatorów, obok ich znaczenia jako efektywnych ligandów, pozwolił określić, czy poza fragmentem azirydynowym, inne centra stereogeniczne również posiadają wpływ na stereochemię reakcji addycji. Celem podjętych badań było: 1) Zaprojektowanie i zrealizowanie syntez wszystkich chiralnych połączeń zawierających pierścień azirydynowy: a) opracowanie i optymalizacja warunków syntezy w/w potencjalnych katalizatorów chiralnych; b) wydzielenie w stanie czystym, pełna charakterystyka spektralna oraz określenie czystości optycznej chiralnych połączeń azirydynowych; 9 M.-C. Wang, Y.-. Wang, G.-W. Li, P.-P. Sun, J.-X. Tian,.-J. Lu, Tetrahedron: Asymmetry 2011, 22,
11 2) Zrealizowanie testowych prób reakcji asymetrycznych dla wszystkich nowo otrzymanych chiralnych katalizatorów: a) przeprowadzenie reakcji asymetrycznych addycji dietylocynku i fenyloetynylocynku do aldehydów aromatycznych i alifatycznych oraz dietylocynku do enonów; b) wydzielenie wszystkich produktów addycji w stanie czystym, podstawowa charakterystyka spektralna ( 1 MR), określenie czystości optycznej i przypisanie konfiguracji absolutnej tych adduktów; c) wyjaśnienie wpływu elementów strukturalnych chiralnych katalizatorów (w szczególności centrów stereogenicznych) na stereochemię reakcji addycji mówienie wyników opisanych w publikacjach stanowiących osiągnięcie naukowe Publikacja 1 ighly efficient aziridine ring-containing chiral ligands as catalysts in asymmetric synthesis Tetrahedron: Asymmetry 2013, 24, oraz Synfacts 2013, 9, Praca opisuje wysoko wydajną syntezę chiralnych azirydynyloalkoholi zbudowanych na prostych achiralnych szkieletach takich związków jak kwas salicylowy oraz kwas 2- hydroksymetylobenzoesowy i zawierających jednostkę azirydynową jako funkcję aminową, a także użycie w/w związków jako wydajnych katalizatorów w reakcjach asymetrycznej addycji dietylocynku i fenyloetynylocynku do aromatycznych i alifatycznych aldehydów. W pierwszej kolejności, ftalid 1 przekształcono w kwas 2-benzoiloksymetylobenzoesowy 2 działaniem a i chlorku benzoilu. Wydajność tej reakcji była niska (26%), lecz podobna do tej opisanej wcześniej w literaturze. 10 astępnie kwas ten pod działaniem chlorku tionylu w obecności pirydyny został przekształcony w chlorek 2-benzoiloksymetylobenzoilu 3 z %-ową wydajnością (Schemat 1). W kolejnym etapie syntezy, chlorek 2- benzoiloksymetylobenzoilu 3 oraz zsyntetyzowany wcześniej zgodnie literaturą, 11 chlorek - acetylosalicyloilowy 4, poddano reakcjom z enancjomerycznie czystymi azirydynami 5a-c 10 Y.-K. Cheng, P. Duncanson, D. Vaughan Griffiths, Tetrahedron 2008, 64, K. R. A. Abdellatif, M. A. Chowdhury, Y. Dong, D. Das, G. Yu, C. A. Velázquez, M. R. Suresh, E. E. Knaus, Bioorg. Med. Chem. Lett. 2009, 19,
12 (otrzymanymi zgodnie z procedurą opisaną wcześniej 12 ) uzyskując odpowiednie amidy 6a-b i 7a-c z wydajnościami chemicznymi w granicach 89 96% (Schemat 2). Amidy zredukowano do odpowiednich azirydynyloalkoholi 8a-b i 9a-c działając trietoksysilanem w obecności octanu cynku. Reakcje redukcji amidów przebiegały z wydajnościami w granicach 96% (Schemat 3). W celu uzyskania związków 8a-b, po reakcji redukcji, niezbędna była deprotekcja grupy benzoilowej w ostrzejszych warunkach (ab 4, TF/Me). Deprotekcja grupy acetylowej (związki 9a-c) następowała spontanicznie w trakcie obróbki mieszaniny po reakcji redukcji. Cl a/ 2 C 6 5 CCl SCl 2 pirydyna, benzen Schemat 1. Synteza chlorku 2-benzoiloksymetylobenzoilu 3 Cl R 2 R 1, Et 3 R1 R 2 Et 2, rt Cl 3 Me R 2 R 1, Et 3 Et 2, rt R1 R 2 6a-b Me 4 7a-c Azirydyny Me Pr i Pr i 5a) (-)--2-metyloazirydyna 5b) (-)--2-izopropyloazirydyna 5c) (+)--2-izopropyloazirydyna 5a 5b 5c Schemat 2. Synteza amidów 6a-b i 7a-c 12 J. Xu, Tetrahedron: Asymmetry 2002, 13,
13 R1 R 2 R 1 R 2 R1 R 2 1.(Et) 3 Si Zn(Ac) 2, TF 2. a ab 4 Me TF 6a-b 8a`-b` 8a-b R 1 R 2 R 1 R 2 Me 1.(Et)3Si Zn(Ac) 2, TF 2. a 7a-c 9a-c Schemat 3. Redukcja amidów do finalnych azirydynylolalkoholi 8a-b i 9a-c Celem zbadania aktywności katalitycznej związków 8a-b i 9a-c w reakcjach asymetrycznej addycji dietylocynku i fenyloetynylocynku do aldehydów, wybrano addycję w/w związków cynkoorganicznych do benzaldehydu jako reakcje modelowe (Schemat 4). Rezultaty tych transformacji zebrano w Tabeli 1. C Ligand, Et 2 Zn toluen 10a + C Ligand, Et 2 Zn TF 11a Schemat 4. Asymetryczna addycja dietylo- i fenyloetynylocynku do benzaldehydu Jak wynika z Tabeli 1, chiralne produkty 10a i 11a powstały z dobrymi wydajnościami chemicznymi i dużymi nadmiarami enancjomerycznymi. ajlepsze wyniki uzyskano stosując katalizator 8b zbudowany na szkielecie kwasu 2-hydroksymetylobenzoesowego i zawierający układ -2-izopropyloazirydyny jako funkcję aminową. Ponadto, użycie dwóch enancjomerycznych katalizatorów 9b i 9c prowadziło do powstawania przeciwnych enancjomerów produktów 10a i 11a. a podstawie tych wyników można stwierdzić, iż centrum stereogeniczne zlokalizowane na jednostce azirydynowej ma decydujący wpływ na stereochemię obu reakcji addycji, a więc i na konfigurację absolutną produktów tych reakcji. 12
14 Tabela 1 Badanie aktywności katalitycznej ligandów 8a-b i 9a-c Produkt 10a Produkt 11a r Ligand W [%] [α] D a ee Abs. [%] b konf. W [%] [α] D a ee [%] b Abs. konf. c 1 8a b a b c a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 13 Ligand 8b wykazujący najwyższą aktywność katalityczną w reakcjach addycji dietylocynku i fenyloetynylocynku do benzaldehydu użyto jako katalizator w analogicznych reakcjach addycji z wykorzystaniem szerszej gamy aldehydów (Schemat 5). Wyniki zebrano w Tabeli 2. RC Ligand 8b, Et 2 Zn toluen R 10a-e + RC Ligand 8b, Et 2 Zn TF 11a-e R Schemat 5. Asymetryczna addycja dietylo- i fenyloetynylocynku do aldehydów w obecności katalizatora 8b 13 J.-C. Zhong, S.-C. ou, Q.-. Bian, M.-M. Yin, R.-S. a, B. Zheng, Z.-Y. Li, S.-Z. Liu, M. Wang, Chem. Eur. J. 2009, 15,
15 Tabela 2 Addycja dietylo- i fenyloetynylocynku do aldehydów w obecności katalizatora 8b Produkty 10a-e Produkty 11a-e r R W [%] [α] D a ee [%] b Abs. konf. c W [%] [α] D a ee [%] b Abs. konf. c MeC n-pr BrC MeC a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 5,7,14,15 Wyniki zebrane w Tabelach 1 i 2 jednoznacznie wykazują, iż wybrany ligand 8b jest efektywnym katalizatorem obu reakcji addycji dając pożądane produkty chiralne z dobrymi wydajnościami chemicznymi i dużymi nadmiarami enancjomerycznymi. Warto zauważyć, iż każdy z enancjomerów produktów addycji może zostać otrzymany poprzez dobór odpowiedniego enancjomeru azirydyny do syntezy enancjomerycznie czystego katalizatora, rozpoczynając syntezę od tego samego achiralnego prekursora. Publikacja 2 Mandelic acid derived α-aziridinyl alcohols as highly efficient ligands for asymmetric additions of zinc organyls to aldehydes Tetrahedron: Asymmetry 2013, 24, Praca opisuje wysoko wydajną syntezę chiralnych azirydynyloalkoholi zbudowanych na chiralnych szkielecie kwasu -(+)-migdałowego i zawierających jednostkę azirydynową jako funkcję aminową, a także zastosowanie tych połączeń jako efektywnych katalizatorów 5 S. Leśniak, M. Rachwalski, E. Sznajder, P. Kiełbasiński, Tetrahedron: Asymmetry 2009, 20, M. Rachwalski, S. Leśniak, P. Kiełbasiński, Tetrahedron: Asymmetry 2010, 21, C.-. Zhang, S.-J. Yan, S.-Q. Pan, R. uang, J. Lin, Bull. Korean. Chem. Soc. 2010, 31, Y.-J. Chen, R.-X. Lin, C. Chen, Tetrahedron: Asymmetry 2004, 15,
16 w reakcjach asymetrycznej addycji dietylocynku i fenyloetynylocynku do aromatycznych i alifatycznych aldehydów. Trójetapowa synteza tego typu połączeń obejmuje zabezpieczenie wolnej grupy hydroksylowej kwasu -(+)-migdałowego 12 za pomocą chlorku acetylu oraz przekształcenie w chlorek kwasowy z użyciem chlorku oksalilu, dając w efekcie chlorek kwasu --acetylomigdałowego 13 z ilościową wydajnością. Chlorek ten następnie poddano działaniu serii azirydyn 5a-d w obecności trietyloaminy w temperaturze pokojowej uzyskując serię amidów typu 14 z doskonałymi wydajnościami ponad 97%. statecznie, amidy 14a-d zredukowano do odpowiednich azirydynyloalkoholi 15a-d za pomocą trietoksysilanu w obecności octanu cynku, we wrzącym tetrahydrofuranie (Schemat 6). Wydajności chemiczne reakcji redukcji były w granicach 81 85%. Ac 1. AcCl, rt, 2h 2. (CCl) 2 /DCM, DMF, rt, 2h Cl 100% R 2 R 1, Et 3 Et2, rt Ac R 2 R a-d Ac R 2 R 1 1.(Et) 3 Si Zn(Ac) 2, TF 2. a R 2 R 1 14a-d 15a-d Me Pr i 5a 5b 5c Pr i Azirydyny 5d Me Me 5a) (-)--2-metyloazirydyna 5b) (-)-(S )-2-izopropyloazirydyna 5c) (+)--2-izopropyloazirydyna 5d) 2,2-dimetyloazirydyna Schemat 6. Trójetapowa synteza azirydynyloalkoholi 15a-d Warto również dodać, iż widma 1 MR pochodnych 15a-c zawierających niesymetrycznie podstawione jednostki azirydynowe, zawierały tylko jeden zestaw sygnałów, natomiast w widmie protonowym pochodnej 15d (zawierającą achiralną 2,2-dimetyloazirydynę) wykryto dwa zestawy sygnałów przypisane odpowiednim inwertomerom związku 15d. 15
17 Aktywność katalityczna azirydynyloalkoholi 15d została sprawdzona w reakcjach addycji dietylocynku i fenyloetynylocynku do benzaldehydu jako modelowego substratu (Schemat 4). Wyniki zebrano w Tabeli 3. Tabela 3 Addycja dietylo- i fenyloetynylocynku do aldehydów w obecności katalizatorów 15a-d r Ligand 15a 15b 15c 15d W [%] a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 13 Produkt 10a [α] D a ee Abs. [%] b konf W [%] Produkt 11a [α] D a ee Abs. [%] b konf. c Jak wynika z Tabeli 3, wszystkie testowane azirydynyloalkohole 15a-d zbudowane na chiralnym szkielecie kwasu -(+)-migdałowego wykazują aktywność katalityczną w powyższych reakcjach asymetrycznych addycji dając pożądane chiralne alkohole 10a i 11a z wysokimi wartościami wydajności chemicznych i doskonałymi nadmiarami enancjomerycznymi (>92%). W przypadku pochodnej 15d zawierającej jednostkę achiralnej 2,2-dimetyloazirydyny zaobserwowano znaczny spadek tych wartości (odpowiednio 62% i 59% wydajności chemicznej oraz 42% i 40% nadmiaru enancjomerycznego). Sugeruje to, iż obecność centrum stereogenicznego w jednostce azirydynowej ma decydujący wpływ na stereochemię reakcji katalitycznej. Potwierdzają to również eksperymenty, w których użyto dwa diastereomeryczne ligandy 15b-c, w wyniku których uzyskano oba enancjomery adduktów. 13 J.-C. Zhong, S.-C. ou, Q.-. Bian, M.-M. Yin, R.-S. a, B. Zheng, Z.-Y. Li, S.-Z. Liu, M. Wang, Chem. Eur. J. 2009, 15,
18 Katalizator 15b wykazujący największą efektywność w obu reakcjach testowych zastosowano następnie w analogicznych reakcjach testujących z użyciem serii aldehydów (Schemat 7, Tabela 4). RC Ligand 15b, Et 2 Zn toluen R 10a-e Ligand 15b, Et 2 Zn + RC TF R 11a-e Schemat 7. Asymetryczna addycja dietylo- i fenyloetynylocynku do aldehydów w obecności katalizatora 15b Tabela 4 Addycja dietylo- i fenyloetynylocynku do aldehydów w obecności katalizatora 15b r R 2-MeC 6 4 n-pr 4-BrC MeC 6 4 W [%] a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 5,7,14,15 Produkty 10a-e [α] D a ee Abs. [%] b konf. c W [%] Produkty 11a-e [α] D a ee Abs. [%] b konf. c Dane w Tabeli 4 jednoznacznie wskazują, iż wybrany ligand 15b jest wysoce aktywnym katalizatorem asymetrycznych reakcji addycji dietylocynku i fenyloetynylocynku do aldehydów prowadząc do otrzymania odpowiednich chiralnych alkoholi z wysokimi wartościami wydajności chemicznych oraz doskonałymi nadmiarami enancjomerycznymi. 5 S. Leśniak, M. Rachwalski, E. Sznajder, P. Kiełbasiński, Tetrahedron: Asymmetry 2009, 20, M. Rachwalski, S. Leśniak, P. Kiełbasiński, Tetrahedron: Asymmetry 2010, 21, C.-. Zhang, S.-J. Yan, S.-Q. Pan, R. uang, J. Lin, Bull. Korean. Chem. Soc. 2010, 31, Y.-J. Chen, R.-X. Lin, C. Chen, Tetrahedron: Asymmetry 2004, 15,
19 Publikacja 3 ighly efficient conjugate addition of diethylzinc to enones catalyzed by chiral ligands derived from -mandelic acid Tetrahedron: Asymmetry 2013, 24, Praca opisuje zastosowanie zsyntetyzowanych wcześniej azirydynyloalkoholi 15a-d (2) jako chiralnych katalizatorów w reakcji asymetrycznej addycji Michaela dietylocynku do α,β-nienasyconych związków karbonylowych (enonów). Przeprowadzono zatem reakcje addycji dietylocynku do chalkonu 16 i 2-cykloheksen-1-onu 18 w obecności katalizatorów 15a-d oraz katalizatora metalicznego, jakim był acetyloacetonian niklu i(acac) 2 (Schemat 8). Celem udowodnienia ważności zastosowania katalizatora metalicznego 16,17,18 przeprowadzono również eksperyment bez użycia i(acac) 2. Wszystkie rezultaty zebrano w Tabeli 5. Et Ligand 15, i(acac) 2 + Et 2 Zn Toluen Ligand 15, i(acac) 2 + Et 2 Zn Toluen Et Schemat 8. Asymetryczna addycja Michaela dietylocynku do enonów w obecności ligandów 15a-d Jak wynika z Tabeli 5, najskuteczniejszym katalizatorem okazał się azirydynyloalkohol 15b zawierający resztę -2-izopropyloazirydyny. Tworzenie się enancjomerycznie wzbogaconych produktów 17 i 19 w obecności katalizatora 15d (z resztą achiralnej 2,2- dimetyloazirydyny), sugeruje, iż centrum stereogeniczne umiejscowione w jednostce azirydynowej ma decydujący wpływ na przebieg stereochemiczny reakcji addycji. Użycie dwóch diastereomerycznych ligandów 15b i 15c prowadziło do tworzenia chiralnych produktów 17 i 19 z przeciwnymi konfiguracjami absolutnymi. Ponadto, w przypadku reakcji 16 L. A. Arnold, R. Imbos, A. Mandoli, A.. M. de Vries, R. aasz, B. L. Feringa, Tetrahedron 2000, 56, A.. M. de Vries, R. Imbos, B. L. Feringa, Tetrahedron: Asymmetry 1997, 9, J. Kang, J.. Lee, D. S. Lim, Tetrahedron: Asymmetry 2003, 14,
20 addycji przeprowadzonej bez użycia katalizatora metalicznego, produkty 17 i 19 powstały ze znacznie niższymi wartościami wydajności chemicznych oraz niskimi nadmiarami enancjomerycznymi, co sugeruje, iż obecność metalicznego katalizatora w środowisku reakcji addycji jest niezbędna. Tabela 5 Asymetryczna addycja Michaela dietylocynku do enonów katalizowana ligandami 15a-d r Ligand Produkt 17 Produkt 19 W [%] [α] D a ee [%] b Abs. konf. c W [%] [α] D a ee [%] b Abs. konf. c 1 15a b b d c d 42 a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury d Bez użycia i(acac) 2 Publikacja 4 Lactic acid derived aziridinyl alcohols as highly effective catalysts for asymmetric additions of organozinc species to aldehydes Tetrahedron: Asymmetry 2013, 24, Praca opisuje wydajną syntezę azirydynyloalkoholi skonstruowanych na chiralnym szkielecie handlowo dostępnego kwasu -(+)-mlekowego oraz zastosowanie ich jako chiralnych katalizatorów w asymetrycznych reakcjach addycji dietylocynku i fenyloetynylocynku do aldehydów. W pierwszym etapie syntezy, kwas -(+)-mlekowy 20 poddano działaniu chlorku acetylu oraz chlorku tionylu celem otrzymania chlorku -2-acetoksypropionylu 21. Synteza 19 A. ajra,. Yoshikai, E. akamura, rg. Lett. 2006, 8,
21 przebiegła z wydajnością 70%. 20 Chlorek ten następnie potraktowano szeregiem azirydyn 5ad w obecności trietyloaminy w temperaturze pokojowej, uzyskując odpowiednie amidy 22a-d z wysokimi wydajnościami chemicznymi w granicach 96 97%. Amidy te następnie poddano redukcji w warunkach opisanych poprzednio (1, 2), otrzymując pożądane azirydynyloalkohole 23a-d z wydajnościami w granicach 77 80% (Schemat 9). Me 1. AcCl, rt, 24 h 2. SCl 2, rt, 24h Me 70% Ac Cl R 2 R 1, Et 3 Et2, rt Me Ac R 2 R a-d Me Ac R 2 R 1 1.(Et) 3 Si Zn(Ac) 2, TF 2. a Me R 2 R 1 22a-d 23a-d Me Pr i 5a 5b 5c Pr i Azirydyny 5d Me Me 5a) (-)--2-metyloazirydyna 5b) (-)--2-izopropyloazirydyna 5c) (+)--2-izopropyloazirydyna 5d) 2,2-dimetyloazirydyna Schemat 9. Synteza chiralnych katalizatorów 23a-d Związki 23a-d sprawdzono w modelowych reakcjach addycji dietylocynku i fenyloetynylocynku do benzaldehydu (Schemat 4). Wyniki zgromadzone w Tabeli 6 wykazują, iż wszystkie azirydynyloalkohole 23a-d wykazują aktywność katalityczną w modelowych reakcjach addycji związków cynkoorganicznych do benzaldehydu dając pożądane chiralne alkohole 10a i 11a z wysokimi wartościami wydajności chemicznych (>85%) i dużymi nadmiarami enancjomerycznymi (>85%). Podobnie, jak w przypadku katalizatorów zbudowanych na chiralnym szkielecie kwasu -(+)-migdałowego (2), zastosowanie związku 23d zawierającego resztę achiralnej 2,2-dimetyloazirydyny prowadziło do uzyskania produktów z niższą wydajnością chemiczną i przeciętnym nadmiarem 20 D. Buisson, R. Azerad, Tetrahedron: Asymmetry 1999, 10,
22 enancjomerycznym. Co więcej, użycie dwóch diastereomerycznych katalizatorów 23b i 23c dało produkty o porównywalnych wartościach skręcalności optycznej, ale o przeciwnych znakach (a zatem, przeciwnych konfiguracjach absolutnych). Powyższe rezultaty sugerują, iż stereochemia procesu addycji zależy w głównej mierze od obecności centrum stereogenicznego w jednostce azirydynowej. Tabela 6 Badanie azirydynyloalkoholi 23a-d w asymetrycznej addycji dietylocynku i fenyloetynylocynku do benzaldehydu r 1 Ligand 23a Produkt 10a a ee Abs. W [%] [α] D [%] b konf Produkt 11a a ee Abs. W [%] [α] D [%] b konf. c b c d 49 a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury Katalizator 23b wykazujący najwyższą efektywność w obu reakcjach modelowych, został sprawdzony w analogicznych reakcjach z użyciem innych aldehydów (Schemat 10). RC Ligand 23b, Et 2 Zn toluen R 10a-e Ligand 23b, Et 2 Zn + RC TF R 11a-e Schemat 10. Addycje związków cynkoorganicznych do aldehydów w obecności katalizatora 23b 15 Y.-J. Chen, R.-X. Lin, C. Chen, Tetrahedron: Asymmetry 2004, 15,
23 Wyniki przedstawione w Tabeli 7 potwierdzają wybór związku 23b jako najskuteczniejszego katalizatora dla opisanych wcześniej reakcji addycji. Aktywność katalityczna wykazywana przez wszystkie azirydynyloalkohole 23a-d zbudowane na chiralnej platformie kwasu -(+)- mlekowego jest podobna do tej, opisanej wcześniej dla pochodnych kwasu -(+)- migdałowego (2). Tabela 7 Addycje związków cynkoorganicznych do aldehydów w obecności katalizatora 23b r R 2-MeC 6 4 n-pr 4-BrC MeC 6 4 W [%] a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 5,7,15 Publikacja 5 Produkty 10a-e [α] D a ee Abs. [%] b konf. c W [%] Produkty 11a-e [α] D a ee Abs. [%] b konf. c Limonene oxide derived aziridinyl alcohols as highly efficient catalysts for asymmetric additions of organozinc species to aldehydes Tetrahedron: Asymmetry 2013, Praca opisuje wydajną, jednoetapową syntezę azirydynyloalkoholi zbudowanych na szkielecie związku terpenowego. Jak wiadomo z literatury, 21,22 diastereomer cis -(+)- tlenku limonenu można wyizolować z dostępnej handlowo mieszaniny (1:1) 5 S. Leśniak, M. Rachwalski, E. Sznajder, P. Kiełbasiński, Tetrahedron: Asymmetry 2009, 20, M. Rachwalski, S. Leśniak, P. Kiełbasiński, Tetrahedron: Asymmetry 2010, 21, Y.-J. Chen, R.-X. Lin, C. Chen, Tetrahedron: Asymmetry 2004, 15, C. C. Watts, P. Thoniyot, L. C. irayama, T. Romano, B. Singaram, Tetrahedron: Asymmetry 2005, 16, D. Steiner, L. Ivison, C. T. Goralski, R. B. Appell, J. R. Gojkovic, B. Singaram, Tetrahedron: Asymmetry 2002, 13,
24 diastereomerycznych tlenków limonenu 24. Selektywne otwarcie pierścienia epoksydowego za pomocą enancjomerycznie czystych azirydyn w obecności trietyloaminy pozwoliło otrzymać β-azirydynyloalkohole 25a-c oraz 25e wyłącznie z epoksydu trans (Schemat 11). Wykorzystując tę reakcję, dokonano syntezy czterech stereoizomerów β-aminoalkoholi 25a-c oraz 25e o konfiguracji absolutnej (1S,2S,4R) z (+)-tlenku limonenu, co jest w zgodzie z doniesieniem literaturowym. 23 Chiralne katalizatory uzyskano z wydajnościami 82 85%. Me + Me R 2 R 1, Et 3 Me R 2 R 1 + cis-24 2, reflux tr ans-24 cis-24 (1S,2S,4R)-25a-c oraz e Azirydyny Me Pr i Pr i 5a) (-)-(S )-2-metyloazirydyna 5b) (-)--2-izopropyloazirydyna 5c) (+)--2-izopropyloazirydyna 5e) (-)--2-fenyloazirydyna 5a 5b 5c 5e Schemat 11. Synteza azirydynyloalkoholi z (+)-tlenku limonenu 24 Podobnie jak w poprzednich pracach (1, 2 i 4), nowe związki 25a-c oraz 25e przetestowano w modelowych reakcjach addycji dietylocynku i fenyloetynylocynku do benzaldehydu (Schemat 4). Wyniki tych reakcji (zebrane w Tabeli 8) wskazały, iż wszystkie azirydynyloalkohole 25 są bardzo wydajnymi katalizatorami w/w reakcji testowych, prowadząc do odpowiednich chiralnych alkoholi 10a i 11a z wysokimi wartościami wydajności chemicznych i dużymi nadmiarami enancjomerycznymi. Rezultaty sugerują również, że wpływ centrum stereogenicznego umiejscowionego w jednostce azirydynowej na stereochemię reakcji addycji nie jest decydujący w tym przypadku. Wyniki reakcji addycji katalizowanych diastereomerycznymi ligandami 25b i 25c, gdzie chiralne produkty wykazywały porównywalne skręcalności optyczne i identyczne konfiguracje absolutne, są potwierdzeniem tego spostrzeżenia. 23 D. Steiner, S. G. Sethofer, C. T. Goralski, B. Singaram, Tetrahedron: Asymmetry 2002, 13,
25 Tabela 8 Addycja dietylo- i fenyloetynylocynku do benzaldehydu katalizowana ligandami 25 r Ligand 25a 25b 25c 25e Produkt 10a ee Abs. a W [%] [α] D [%] b konf a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury Produkt 11a W [%] [α] D a ee [%] b Abs. konf. c Zakres badania aktywności katalitycznej azirydynyloalkoholu 25b został poszerzony o reakcje addycji związków cynkoorganicznych z innymi aldehydami (Schemat 12). RC Ligand 25b, Et 2 Zn toluen R 10a-e Ligand 25b, Et 2 Zn + RC TF R 11a-e Schemat 12. Addycja związków cynkoorganicznych do aldehydów katalizowana ligandem 25b Jak pokazują dane zebrane w Tabeli 9, wszystkie w/w reakcje addycji przebiegły niezwykle wydajnie, prowadząc do chiralnych alkoholi 10a-e i 11a-e z bardzo wysokimi wartościami wydajności chemicznych i doskonałymi nadmiarami enancjomerycznymi. 13 J.-C. Zhong, S.-C. ou, Q.-. Bian, M.-M. Yin, R.-S. a, B. Zheng, Z.-Y. Li, S.-Z. Liu, M. Wang, Chem. Eur. J. 2009, 15,
26 Tabela 9 Addycja związków cynkoorganicznych do aldehydów w obecności katalizatora 25b r R 2-MeC 6 4 n-pr 4-BrC MeC 6 4 W [%] a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 5,7,14,15 Produkty 10a-e [α] D a ee Abs. [%] b konf. c W [%] Produkty 11a-e [α] D a ee Abs. [%] b konf. c Analiza konfiguracji absolutnych adduktów sugeruje, iż atak reagentów cynkoorganicznych katalizowany przez ligand 25b zawsze następuje od tej samej strony, co jest zgodne z zaproponowanymi modelami stanów przejściowych dla reakcji addycji dietylocynku i alkinylocynku katalizowanych przez pochodne (+)-tlenku limonenu. 21,23 Użycie chiralnych aminoalkoholi o absolutnej konfiguracji (1S,2S,4R) (z (+)-tlenku limonenu) prowadziło do powstawania adduktów o konfiguracji dla dietylocynku oraz adduktów o konfiguracji dla fenyloetynylocynku. 5 S. Leśniak, M. Rachwalski, E. Sznajder, P. Kiełbasiński, Tetrahedron: Asymmetry 2009, 20, M. Rachwalski, S. Leśniak, P. Kiełbasiński, Tetrahedron: Asymmetry 2010, 21, C.-. Zhang, S.-J. Yan, S.-Q. Pan, R. uang, J. Lin, Bull. Korean. Chem. Soc. 2010, 31, Y.-J. Chen, R.-X. Lin, C. Chen, Tetrahedron: Asymmetry 2004, 15, C. C. Watts, P. Thoniyot, L. C. irayama, T. Romano, B. Singaram, Tetrahedron: Asymmetry 2005, 16, D. Steiner, S. G. Sethofer, C. T. Goralski, B. Singaram, Tetrahedron: Asymmetry 2002, 13,
27 Publikacja 6 Synthesis and evaluation of catalytic properties of semicarbazides derived from - triphenylmethyl-aziridine-2-carbohydrazides Tetrahedron: Asymmetry 2013, 24, Praca opisuje wydajną syntezę semikarbazydów z -trifenylometyloazirydyno-2- karbohydrazydu i wykorzystanie ich jako katalizatorów w asymetrycznej addycji związków cynkoorganicznych do aldehydów. gólną metodą syntezy estrów typu 26 jest cyklizacja dostępnych handlowo pochodnych L- seryny. 24 Tak uzyskany --trifenylometyloazirydynian metylu 26 przekształcono działaniem wodzianu hydrazyny w hydrazyd --trifenylometyloazirydyny 27 z wydajnością %. Reakcje hydrazydu 27 z izocyjanianami alkilowymi w chlorku metylenu w temperaturze pokojowej dały w efekcie semikarbazydy 28 z bardzo wysokimi wydajnościami chemicznymi (97 98%) (Schemat 13). C Me * 2 2 RC R Schemat 13. Synteza semikarbazydów 28 28a, R = butyl 28b, R = tert-butyl 28c, R = cykloheksyl Wartym podkreślenia jest fakt, iż w przypadku reakcji związku 27 z izocyjanianem fenylu w analogicznych warunkach stosowanych w syntezie pochodnych 28, jako jedyny produkt powstał 1,2,4-triazolo-3-on 29a. Postanowiono zatem otrzymać 1,2,4-triazolo-3-on z semikarbazydu 28 w warunkach zasadowych. I tak, ogrzewanie związku 28a w 5% wodnym roztworze a prowadziło do oczekiwanego produktu cyklicznego 29b z wydajnością 20% (Schemat 14). 24. Liu, V. R. Pattabiraman, J. C. Vederas, rg. Lett. 2007, 9,
28 Bu 5% a R C 2 28a a, R = fenyl 29b, R = butyl Schemat 14. Synteza 1,2,4-triazolo-3-onów 29 Aktywność katalityczna nowo otrzymanych semikarbazydów 28a-c została sprawdzona w modelowych reakcjach addycji dietylocynku i fenyloetynylocynku do benzaldehydu (Schemat 4). Pochodne cykliczne 29a-b okazały się praktycznie nierozpuszczalne w większości dostępnych rozpuszczalników organicznych, skutkiem czego ich zastosowanie w syntezie asymetrycznej okazało się niemożliwe. Tabela 10 Addycja związków cynkoorganicznych do benzaldehydu katalizowana semikarbazydami 28 r 1 Ligand 28a Produkt 10a Produkt 11a a ee Abs. W [%] [α] D [%] b konf. c a ee Abs. W [%] [α] D [%] b konf. c b c a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 25 Jak wynika z Tabeli 10, wszystkie semikarbazydy 28 okazały się skutecznymi katalizatorami modelowych reakcji addycji. Użycie katalizatora 28a zawierającego resztę n-butylową prowadziło do otrzymania chiralnych alkoholi 10a i 11a z nieco niższymi wartościami wydajności chemicznych i nadmiarów enancjomerycznych. Może to sugerować, iż rozmiar podstawnika ma wpływ na stereochemię procesów addycji. 25 M. Rachwalski, S. Jarzyński, S. Leśniak, Tetrahedron: Asymmetry 2013, 24,
29 Inne aldehydy zostały użyte jako substraty w analogicznych reakcjach addycji celem rozszerzenia badań aktywności katalitycznej semikarbazydu 28c (Schemat 15). RC Ligand 28c, Et 2 Zn toluen R 10a-e Ligand 28c, Et 2 Zn + RC TF R 11a-e Schemat 15. Addycje związków cynkoorganicznych do aldehydów w obecności 28c Tabela 11 Addycje związków cynkoorganicznych do aldehydów katalizowane ligandem 28c r 1 R W [%] 97 Produkty 10a-e a ee Abs. [α] D [%] b konf. c W [%] 95 Produkty 11a-e a ee Abs. [α] D [%] b konf. c MeC n-pr BrC MeC a W chloroformie (c 1). b kreślony za pomocą chiralnej PLC. c Dane wzięte z literatury. 5,7,14,15 Jak wynika z Tabeli 11, chiralne alkohole 10a-e i 11a-e powstały z bardzo wysokimi wartościami wydajności chemicznych i dużymi nadmiarami enancjomerycznymi. ieco niższe wartości uzyskano w przypadku, gdy aldehyd masłowy został użyty jako substrat. 5 S. Leśniak, M. Rachwalski, E. Sznajder, P. Kiełbasiński, Tetrahedron: Asymmetry 2009, 20, M. Rachwalski, S. Leśniak, P. Kiełbasiński, Tetrahedron: Asymmetry 2010, 21, C.-. Zhang, S.-J. Yan, S.-Q. Pan, R. uang, J. Lin, Bull. Korean. Chem. Soc. 2010, 31, Y.-J. Chen, R.-X. Lin, C. Chen, Tetrahedron: Asymmetry 2004, 15,
30 Konkluzje i perspektywy na przyszłość: Postawiona na początku badań hipoteza zakładająca, iż aminoalkohole, w których funkcję aminową pełni pierścień azirydynowy, będą skutecznymi katalizatorami w stereokontrolowanych reakcjach z udziałem jonów cynkowych, została w pełni potwierdzona. Wszystkie nowo otrzymane chiralne połączenia azirydynowe zbudowane zarówno na achiralnych, jak i chiralnych platformach, wykazały bardzo wysoką aktywność katalityczną w testowych reakcjach asymetrycznych prowadząc do uzyskania chiralnych produktów z wysokimi wartościami wydajności chemicznych oraz dużymi nadmiarami enancjomerycznymi. Wyniki będące treścią publikacji wskazanych jako osiągnięcie naukowe pozwalają na planowanie z dużym optymizmem metod syntezy kolejnych chiralnych połączeń azirydynowych będących potencjalnymi skutecznymi katalizatorami w syntezie asymetrycznej. pracowanie i realizacja metodologii syntezy chiralnych azirydynyloalkoholi zbudowanych na szkieletach związków bicyklicznych oraz poszerzenie spektrum testowych reakcji asymetrycznych stanowią cele na najbliższą przyszłość. 3. Pozostałe publikacje i osiągnięcia naukowe 3.1. Publikacje dodatkowe Publikacje oryginalne przed uzyskaniem stopnia naukowego doktora: 1) P. Kiełbasiński, M. Rachwalski, M. Mikołajczyk, M. A.. Moelands, B. Zwanenburg, F. P. J. T. Rutjes Lipase-promoted dynamic kinetic resolution of racemic β-hydroxyalkyl sulfones Tetrahedron: Asymmetry 2005, 16, , IF = 2,429 (30 pkt. MiSW) Mój wkład polegał na syntezie wyjściowych racemicznych sulfonów, przeprowadzeniu chemoenzymatycznych procesów DKR, izolacji produktów, rejestracji i interpretacji widm MR oraz oszacowaniu wartości nadmiarów enancjomerycznych. Mój udział oceniam na 50%. 2) P. Kiełbasiński, M. Rachwalski, M. Mikołajczyk, M. Szyrej, M. W. Wieczorek, R. Wijtmans, F. P. J. T. Rutjes Enzyme-promoted desymmetrisation of prochiral bis(cyanomethyl) sulfoxide Adv. Synth. Catal. 2007, 349, , IF = 4,977 (45 pkt. MiSW) 29
31 Mój wkład polegał na syntezie prochiralnego sulfotlenku bis-cyjanometylowego, przeprowadzeniu enzymatycznych reakcji desymetryzacji, izolacji produktów, rejestracji i interpretacji widm MR, określaniu nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 60%. 3) P. Kiełbasiński, M. Rachwalski, M. Kwiatkowska, M. Mikołajczyk, W. M. Wieczorek, M. Szyrej, L. Sieroń, F. P. J. T. Rutjes Enzyme-promoted desymmetrisation of prochiral bis(cyanomethyl)phenylphosphine oxide Tetrahedron: Asymmetry 2007, 18, , IF = 2,634 (30 pkt. MiSW) Mój wkład polegał na syntezie wyjściowego prochiralnego tlenku fosfiny, przeprowadzeniu enzymatycznych desymetryzacji, izolacji produktów, rejestracji i interpretacji widm MR, określaniu nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 60%. 4) P. Kiełbasiński, M. Rachwalski, M. Mikołajczyk, F. P. J. T. Rutjes itrilase-catalysed hydrolysis of cyanomethyl p-tolyl sulfoxide: stereochemistry and mechanism Tetrahedron: Asymmetry 2008, 19, , IF = 2,796 (30 pkt. MiSW) Mój wkład polegał na syntezie wyjściowego racemicznego sulfotlenku, przeprowadzeniu enzymatycznych desymetryzacji, izolacji produktów, rejestracji i interpretacji widm MR, określaniu nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 60%. 5) M. Rachwalski, M. Kwiatkowska, J. Drabowicz, M. Kłos, W. M. Wieczorek, M. Szyrej, L. Sieroń, P. Kiełbasiński Enzyme-promoted desymmetrization of bis(2-hydroxymethylphenyl)sulfoxide as a route to tridentate chiral catalysts Tetrahedron: Asymmetry 2008, 19, , IF = 2,796 (30 pkt. MiSW) Mój wkład polegał na syntezie wyjściowego prochiralnego sulfotlenku, przeprowadzeniu enzymatycznych desymetryzacji, izolacji produktów, rejestracji i interpretacji widm MR oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 50%. Publikacje oryginalne po uzyskaniu stopnia naukowego doktora (prace nie są częścią dorobku zawartego w punkcie 2.1): 1) M. Rachwalski, S. Leśniak, E. Sznajder, P. Kiełbasiński ighly enantioselective enry reaction catalyzed by chiral tridentate heteroorganic ligands Tetrahedron: Asymmetry 2009, 20, , IF = 2,625 (30 pkt. MiSW) 30
32 Mój wkład polegał na przeprowadzeniu reakcji enry`ego dla różnych aldehydów, izolacji produktów, interpretacji widm MR, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 60%. 2) A. Chrostowska, A. Dargelos, A. Graciaa, S. Khayar, S. Leśniak, R. B. azarski, T.-X. Mai guyen, M. Maciejczyk, M. Rachwalski Flash vacuum thermolysis generation and UV-photoelectron spectroscopy study of the -substituted iminoacetonitriles Tetrahedron 2009, 65, , IF = 3,219 (30 pkt. MiSW) Mój wkład polegał na syntezie związku wyjściowego. Mój udział oceniam na 10%. 3) S. Leśniak, M. Rachwalski, E. Sznajder, P. Kiełbasiński ew highly efficient aziridine-functionalized tridentate sulfinyl catalysts for enantioselective diethylzinc addition to carbonyl compounds Tetrahedron: Asymmetry 2009, 20, , IF = 2,625 (30 pkt. MiSW) Mój wkład polegał na przeprowadzeniu reakcji addycji dietylocynku do różnych aldehydów, izolacji produktów, interpretacji widm MR, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 60%. 4) M. Rachwalski, S. Leśniak, P. Kiełbasiński ighly enantioselective conjugate addition of diethylzinc to enones using aziridine-functionalized tridentate sulfinyl ligands Tetrahedron: Asymmetry 2010, 21, , IF = 2,484 (30 pkt. MiSW) Mój wkład polegał na syntezie ligandów, przeprowadzeniu reakcji addycji dietylocynku do enonów, izolacji produktów, interpretacji widm MR, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 70%. 5) M. Rachwalski*, S. Leśniak, P. Kiełbasiński ighly enantioselective addition of phenylethynylzinc to aldehydes using aziridine-functionalized tridentate sulfinyl ligands Tetrahedron: Asymmetry 2010, 21, , IF = 2,484 (30 pkt. MiSW) Mój wkład polegał na syntezie ligandów, przeprowadzeniu reakcji addycji fenyloetynylocynku do różnych aldehydów, izolacji produktów, interpretacji widm MR, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 70%. 6) M. Rachwalski*, S. Leśniak, P. Kiełbasiński ighly enantioselective Aza-enry reaction promoted by amine-functionalized tridentate sulfinyl ligands Tetrahedron: Asymmetry 2011, 22, , IF = 2,652 (30 pkt. MiSW) 31
33 Mój wkład polegał na syntezie ligandów, przeprowadzeniu reakcji Aza-enry`ego, izolacji produktów, interpretacji widm MR, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 70%. 7) S. Kaczmarczyk, M. Kwiatkowska, L. Madalińska, A. Barbachowska, M. Rachwalski, J. Błaszczyk, L. Sieroń, P. Kiełbasiński Enzymatic synthesis of enantiopure precursors of chiral bidentate and tridentate phosphorus catalysts Adv. Synth. Catal. 2011, 353, , IF = 6,048 (45 pkt. MiSW) Mój wkład polegał na wstępnych próbach syntezy połączeń fosforoorganicznych. Mój udział oceniam na 15%. 8) M. Rachwalski*, S. Leśniak, P. Kiełbasiński ighly enantioselective asymmetric direct aldol reaction catalyzed by aminefunctionalized tridentate sulfinyl ligands Tetrahedron: Asymmetry 2011, 22, , IF = 2,652 (30 pkt. MiSW) Mój wkład polegał na syntezie ligandów, przeprowadzeniu reakcji kondensacji aldolowej, izolacji produktów, interpretacji widm MR, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 70%. 9) M. Rachwalski*, T. Leenders, S. Kaczmarczyk, P. Kiełbasiński, S. Leśniak, F. P. J. T. Rutjes Efficient catalysts for asymmetric Mannich reactions rg. Biomol. Chem. 2013, 11, , IF = 3,568 (35 pkt. MiSW) Mój wkład polegał na częściowym przeprowadzeniu reakcji Mannicha, izolacji produktów, interpretacji widm MR, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu i wysłaniu go do redakcji. Mój udział oceniam na 50%. 10) P. Kiełbasiński, M. Rachwalski, S. Kaczmarczyk, S. Leśniak Polydentate chiral heteroorganic ligands/catalysts impact of particular functional groups on their activity in selected reactions of asymmetric synthesis Tetrahedron: Asymmetry 2013, 24, , IF = 2,115 (30 pkt. MiSW) Mój wkład polegał na częściowej syntezie ligandów, przeprowadzeniu reakcji enry`ego, izolacji produktów, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 60%. 11) M. Rachwalski*, S. Kaczmarczyk, S. Leśniak, P. Kiełbasiński ighly efficient asymmetric Simmons-Smith cyclopropanation promoted by chiral heteroorganic aziridinyl ligands 32
34 ChemCatChem 2014, 6, DI: /cctc , IF = 5,181 (30 pkt. MiSW) Mój wkład polegał na częściowej syntezie ligandów, przeprowadzeniu reakcji Simmonsa-Smitha, izolacji produktów, określaniu wartości nadmiarów enancjomerycznych oraz częściowym redagowaniu manuskryptu. Mój udział oceniam na 60%. Publikacje przeglądowe po uzyskaniu stopnia naukowego doktora (prace nie są częścią dorobku zawartego w punkcie 2.1): 1) M. Rachwalski*,. Vermue, F. P. J. T. Rutjes Recent advances in enzymatic and chemical deracemisation of racemic compounds Chem. Soc. Rev. 2013, 42, , IF = 24,892 (50 pkt. MiSW) Mój wkład polegał na częściowemu zebraniu materiałów i częściowej redakcji manuskryptu. Mój udział oceniam na 40% Doniesienia konferencyjne Komunikaty ustne przed uzyskaniem stopnia naukowego doktora: 1) P. Kiełbasiński, M. Rachwalski, M. Mikołajczyk Katalizowane enzymami deracemizacje i desymetryzacje jako metody syntezy chiralnych połączeń heteroorganicznych Postępy w syntezie związków nieracemicznych, III Seminarium Sekcji Chemii rganicznej PTChem, Karpacz, października 2006, Abstrakt K 17. 2) M. Rachwalski, P. Kiełbasiński Enzyme-promoted desymmetrisation in the synthesis of chiral non-racemic organophosphorus compounds 5 th European Workshop on osphorus Chemistry, Regensburg (iemcy), marca 2008, Abstrakt 6-2 Komunikaty posterowe przed uzyskaniem stopnia naukowego doktora: 1) P. Kiełbasiński, M. Rachwalski, M. Mikołajczyk Lipase-catalysed kinetic resolution of hydroxyalkyl sulfones 7 th International Conference on eteroatom Chemistry (ICAC-7), Shanghai (Chiny), września ) P. Kiełbasiński, M. Rachwalski, M. Mikołajczyk, R. Wijtmans, F. P. J. T. Rutjes 33
35 Enzyme-promoted hydrolysis of prochiral bis(cyanomethyl) sulfoxide 22 nd International Symposium on the rganic Chemistry of Sulfur, Saitama (Japonia), września 2006, Abstrakt P 60 3) M. Rachwalski, P. Kiełbasiński, W. M. Wieczorek, M. Szyrej, L. Sieroń Crystal and molecular structure of 2-acetoxymethylphenyl-2`-hydroxymethylphenyl sulfoxide XII th International Seminar on ysics and Chemistry of Solids, Ustroń Śląski, czerwca 2007, Abstrakt P2_18 4) P. Kiełbasiński, M. Rachwalski, M. Mikołajczyk Enzymatic desymmetrisation of bis(2-hydroxymethylphenyl) sulfoxide and phosphine oxides 8 th International Symposium on Biocatalysis and Biotransformations (Biotrans 2007), viedo (iszpania), 8 13 lipca 2007, Abstrakt P 162 5) M. Rachwalski, P. Kiełbasiński, M. Mikołajczyk Enzyme-promoted kinetic resolution of racemic cyanomethyl p-tolyl sulfoxide 5 th International Congress of Young Chemists, Jurata, października 2007, Abstrakt P 26 6) P. Kiełbasiński, M. Rachwalski, M. Kwiatkowska, M. Mikołajczyk Katalizowana enzymami desymetryzacja jako źródło potencjalnych trójzębnych ligandów w katalizie organicznej VIII gólnopolskie Sympozjum Chemii rganicznej (SC-VIII), Łódź, kwietnia 2008, Abstrakt P 105 7) P. Kiełbasiński, M. Rachwalski, M. Kwiatkowska ew achievements in enzyme-promoted syntheses of chiral, non-racemic heteroorganic compounds V th International Congress on Biocatalysis (BICAT 2008), amburg (iemcy), 31 sierpnia 4 września 2008, Abstrakt L 59a Komunikaty ustne po uzyskaniu stopnia naukowego doktora: 1) M. Rachwalski Biotransformations as synthetic methods Wykład seminaryjny w grupie prof. P. Schreinera, Uniwersytet Justusa-Liebiga w Giessen (iemcy), 12 grudnia
36 2) M. Rachwalski Chiral tridentate ligands as catalysts in asymmetric synthesis III rd International Mini-Symposium Advances in rganocatalysis and Related Problems, Łódź, 25 maja 2010, Abstrakt L 6. 3) M. Rachwalski Chiralne ligandy trójzębne jako katalizatory w syntezie asymetrycznej Postępy w syntezie związków nieracemicznych V Seminarium Sekcji Chemii rganicznej PTChem, Kudowa Zdrój, października 2010, Abstrakt K 18. 4) M. Rachwalski Enzymy w chemii Akademia Ciekawej Chemii 2010/2011, Uniwersytet Łódzki, 16 lutego ) M. Rachwalski Chiral ligands as catalysts in asymmetric synthesis Wykład seminaryjny w grupie prof. P. Schreinera, Uniwersytet Justusa-Liebiga w Giessen (iemcy), 16 czerwca ) M. Rachwalski, S. Leśniak owe chiralne ligandy jako katalizatory w syntezie asymetrycznej 54 Zjazd PTChem, Lublin, września 2011, Abstrakt S04 K9. 7) S. Jarzyński, M. Rachwalski, S. Leśniak ptycznie czyste azirydynyloalkohole jako katalizatory w syntezie asymetrycznej 30 Wiosenny zjazd Sekcji Studenckiej PTChem, Augustów, kwietnia 2013, Abstrakt 17 8) S. Jarzyński, M. Rachwalski, S. Leśniak Asymetryczna addycja dietylocynku i fenyloetynylocynku do aldehydów katalizowana chiralnymi ligandami I Łódzkie Sympozjum Doktorantów Chemii, Łódź, kwietnia 2013, Abstrakt (Prezentacja nr 10) 9) S. Jarzyński, M. Rachwalski, S. Leśniak owe chiralne azirydynoalkohole jako efektywne katalizatory w asymetrycznej addycji związków cynkoorganicznych do aldehydów 16 gólnopolska Sesja Wykładowa Koła aukowego Studentów Wydziału Chemii Politechniki Łódzkiej, Konopnica, maja, Abstrakt str ) M. Rachwalski, P. Kiełbasiński, S. Leśniak, F. P. J. T. Rutjes 35
37 Asymetryczna reakcja Mannicha katalizowana chiralnymi ligandami i ultradźwiękami 56 Zjazd aukowy PTChem i Stowarzyszenia Inżynierów i Techników Przymysłu Chemicznego, Siedlce, września, Abstrakt S01K14 Komunikaty posterowe po uzyskaniu stopnia naukowego doktora: 1) M. Rachwalski, S. Leśniak, P. Kiełbasiński Trójzębne ligandy jako enancjoselektywne katalizatory w syntezie asymetrycznej 52 Zjazd PTChem, Łódź, września 2009, Abstrakt A 048 2) M. Rachwalski, S. Leśniak, P. Kiełbasiński Asymetryczna addycja dietylocynku dietylocynku do związków karbonylowych katalizowana trójzębnymi chiralnymi ligandami XII gólnopolskie Sympozjum Sekcji Chemii eteroorganicznej PTChem Postępy w chemii związków heteroorganicznych, Łódź, 27 listopada 2009, Abstrakt P 40 3) M. Rachwalski, S. Leśniak, P. Kiełbasiński Asymetryczna addycja fenyloetynylocynku do aldehydów, katalizowana trójzębnymi chiralnymi ligandami XIII gólnopolskie Sympozjum Chemii eteroorganicznej PTChem Postępy w chemii związków heteroorganicznych, Łódź, 19 listopada 2010, Abstrakt P 21 4) M. Rachwalski, S. Leśniak, M. Jasiński, G. Mlostoń owe chiralne ligandy funkcjonalizowane azirydynami jako potencjalne katalizatory w syntezie asymetrycznej IX gólnopolskie Sympozjum Chemii rganicznej, Warszawa, 6 9 kwietnia 2011, Abstrakt P 42 5) M. Rachwalski, S. Leśniak, P. Kiełbasiński Tridentne heteroorganiczne ligandy jako wydajne katalizatory w syntezie asymetrycznej XIV gólnopolskie Sympozjum Sekcji Chemii eteroorganicznej PTChem Postępy w chemii związków heteroorganicznych, Łódź, 18 listopada 2011, Abstrakt P 13 6) M. Rachwalski, T. Leenders, P. Kiełbasiński, F. P. J. T. Rutjes ew catalysts for asymmetric Mannich re action 36
38 W CW Study group meeting rganic Chemistry & Synthesis, Lunteren (olandia), października 2012, Abstrakt 134 7) S. Jarzyński, S. Leśniak, M. Rachwalski Synteza i badanie aktywności katalitycznej nowych chiralnych ligandów azirydynowych III Sesja Magistrantów i Doktorantów Łódzkiego Środowiska Chemików, Łódź, 12 czerwca 2012, Abstrakt 113 8) S. Kaczmarczyk, M. Rachwalski, S. Leśniak, P. Kiełbasiński 25 th International Symposium on the rganic Chemistry of Sulfur, Częstochowa, czerwca 2012, Abstrakt PC 20 9) S. Jarzyński, S. Leśniak, M. Rachwalski Synthesis and studies on the catalytic activity of ew chiral aziridinyl ligands XV gólnopolskie Sympozjum Sekcji Chemii eteroorganicznej PTChem Postępy w chemii związków heteroorganicznych, Łódź, 16 listopada 2012, Abstrakt P 72 10) M. Rachwalski, S. Kaczmarczyk, T. Leenders, P. Kiełbasiński, S. Leśniak, F. P. J. T. Rutjes ew tridentate sulfinyl ligands for asymmetric Mannich reactions XV gólnopolskie Sympozjum Sekcji Chemii eteroorganicznej PTChem Postępy w chemii związków heteroorganicznych, Łódź, 16 listopada 2012, Abstrakt P 81 11) S. Jarzyński, S. Leśniak, M. Rachwalski Synthesis and studies on the catalytic activity of new aziridinyl ligands 15 th JCF-Früjahrssymposium, Berlin, 6 9 marca 2013, Abstrakt ) A. M. Pieczonka, M. Rachwalski, S. Jarzyński, K. Justyna, S. Leśniak Synteza i badanie właściwości katalitycznych nowych semikarbazydów pochodnych hydrazydu kwasu -trifenylometylo-azirydyno-2-karboksylowego 56 Zjazd aukowy PTChem i Stowarzyszenia Inżynierów i Techników Przemysłu Chemicznego, Siedlce, września 2013, Abstrakt S01P68 13) S. Jarzyński, M. Rachwalski, S. Leśniak owe chiralne azirydynoalkohole jako efektywne katalizatory w syntezie asymetrycznej 37
39 56 Zjazd aukowy PTChem i Stowarzyszenia Inżynierów i Techników Przemysłu Chemicznego, Siedlce, września 2013, Abstrakt S01P117 14) M. Rachwalski Limonene oxide derived aziridinyl alcohols as highly efficient catalysts for asymmetric additions of organozinc species to aldehydes XVI International Symposium Advances in the chemistry of heteroorganic compounds, Łódź, 15 listopada 2013, Abstrakt P ) S. Jarzyński, S. Leśniak, M. Rachwalski Mandelic acid derived α-aziridinyl alcohols as effective ligands for asymmetric synthesis XVI International Symposium Advances in the chemistry of heteroorganic compounds, Łódź, 15 listopada 2013, Abstrakt P ) A. M. Pieczonka, M. Rachwalski, S. Leśniak ew aziridinesemicarbazides as highly efficient ligands in asymmetric synthesis XVI International Symposium Advances in the chemistry of heteroorganic compounds, Łódź, 15 listopada 2013, Abstrakt P agrody, wyróżnienia Wyróżnienie Rady aukowej Centrum Badań Molekularnych i Makromolekularnych Polskiej Akademii auk w Łodzi za rozprawę doktorską Katalizowane enzymami deracemizacje i desymetryzacje jako metody syntezy chiralnych połączeń heteroorganicznych agroda aukowa Fundacji Uniwersytetu Łódzkiego dla Młodego aukowca 3.4. dbyte staże a) staże długoterminowe: olandia, Uniwersytet Radboud w ijmegen (grupa prof. F. Rutjesa), staż podoktorski, 1.I XI.2012 (1 rok) 38
40 b) staże krótkoterminowe: olandia, Uniwersytet Radboud w ijmegen (grupa prof. F. Rutjesa), wizyta naukowa, listopad 2005 (1 tydzień) olandia, Uniwersytet Radboud w ijmegen (grupa prof. F. Rutjesa), pobyt naukowy, październik 2007 (2 tygodnie) olandia, Uniwersytet Radboud w ijmegen (grupa prof. F. Rutjesa), pobyt naukowy, luty 2008 (1 miesiąc) iemcy, Uniwersytet Justusa Liebiga w Giessen (grupa prof. P. R. Schreinera), wizyta naukowa, grudzień 2008 (1 tydzień) iemcy, Uniwersytet Justusa Liebiga w Giessen, (grupa prof. P. R. Schreinera), wizyta naukowa, lipiec 2010 (1 tydzień) iemcy, Uniwersytet Justusa Liebiga w Giessen, (grupa prof. P. R. Schreinera), wizyta naukowa, czerwiec 2011 (1 tydzień) 3.5. Udział w projektach naukowych Grant MiI r 3 T09A Biokatalityczne syntezy nowych preparatywnie użytecznych, chiralnych związków heteroorganicznych ( ) wykonawca ( PL) Zadanie badawcze - owe podejścia do katalizowanych enzymami syntez chiralnych nieracemicznych związków heteroorganicznych ( ) w ramach grantu zamawianego MniSzW r PBZ-KB-126/T09/03 wykonawca ( PL) Grant C (SATA) nr 2012/05/D/ST5/00505 Synteza nowych, optycznie czynnych azirydynyloalkoholi i ich zastosowanie w syntezie asymetrycznej ( ) kierownik ( PL) Inna działalność związana z pracą naukowo-dydaktyczną oraz organizacyjną Prowadzone zajęcia dydaktyczne: Chemia organiczna laboratorium, II rok ochrony środowiska Chemia organiczna laboratorium, III rok chemii Chemia organiczna II laboratorium, IV rok chemii zaocznej 39
41 Chemia organiczna II konwersatorium, III rok chemii Chemia organiczna laboratorium, II rok chemii Chemia organiczna laboratorium, I rok biotechnologii Chemia organiczna laboratorium, I rok biologii Chemia organiczna konwersatorium, II rok chemii Spektroskopia laboratorium, I rok chemii, studia II stopnia Język angielski w chemii konwersatorium, I rok chemii, studia II stopnia Biomateriały Chemia Związków aturalnych laboratorium, III rok chemii Biochemia konwersatorium, III rok chemii Wymiar godzinowy zajęć: w roku akademickim 2008/ godzin w roku akademickim 2009/ godzin w roku akademickim 2010/ godzin w roku akademickim 2011/ godzin Liczba ukończonych prac magisterskich, których byłem opiekunem: 5 Liczba ukończonych prac dyplomowych, którymi kierowałem: 4 Promotor pomocniczy w przewodzie doktorskim: 1 Recenzje: - dla Current rganic Chemistry; - prac dyplomowych na Wydziale Chemii UŁ 3.7. Członkowstwo w organizacjach naukowych członek Polskiego Towarzystwa Chemicznego. 40
Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku
 Streszczenie pracy doktorskiej Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku mgr Agata Dudek Promotor: prof. dr hab. Jacek Młynarski Praca została wykonana w Zespole Stereokotrolowanej
Streszczenie pracy doktorskiej Enancjoselektywne reakcje addycje do imin katalizowane kompleksami cynku mgr Agata Dudek Promotor: prof. dr hab. Jacek Młynarski Praca została wykonana w Zespole Stereokotrolowanej
Tematy prac magisterskich w Katedrze Chemii Organicznej i Stosowanej Rok akademicki 2009/2010. Studia Stacjonarne
 Prof. dr hab. Grzegorz Mlostoń Wydział Chemii UŁ Katedra Chemii Organicznej i Stosowanej e-mail: gmloston@uni.lodz.pl Wrzesień 2009 Tematy prac magisterskich w Katedrze Chemii Organicznej i Stosowanej
Prof. dr hab. Grzegorz Mlostoń Wydział Chemii UŁ Katedra Chemii Organicznej i Stosowanej e-mail: gmloston@uni.lodz.pl Wrzesień 2009 Tematy prac magisterskich w Katedrze Chemii Organicznej i Stosowanej
Prof. dr hab. K. Michał Pietrusiewicz Zakład Chemii Organicznej Wydział Chemii, UMCS Lublin, 19 września 2014 RECENZJA
 Prof. dr hab. K. Michał Pietrusiewicz Zakład Chemii Organicznej Wydział Chemii, UMCS Lublin, 19 września 2014 RECENZJA pracy doktorskiej mgr Sylwii Kaczmarczyk p.t. Chiralne hydroksylowe pochodne sulfotlenków
Prof. dr hab. K. Michał Pietrusiewicz Zakład Chemii Organicznej Wydział Chemii, UMCS Lublin, 19 września 2014 RECENZJA pracy doktorskiej mgr Sylwii Kaczmarczyk p.t. Chiralne hydroksylowe pochodne sulfotlenków
b. Rozdział mieszaniny racemicznej na CHIRALNEJ kolumnie (Y. Okamoto, T. Ikai, Chem. Soc. Rev., 2008, 37, )
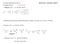 Jak otrzymać związki optycznie czynne??? ławomir Jarosz stereochemia- wykład VII Ze związków chiralnych 1. ozdział racematu a. Klasyczny : A (rac) 50% A() 50%A() b. ozdział mieszaniny racemicznej na CIAEJ
Jak otrzymać związki optycznie czynne??? ławomir Jarosz stereochemia- wykład VII Ze związków chiralnych 1. ozdział racematu a. Klasyczny : A (rac) 50% A() 50%A() b. ozdział mieszaniny racemicznej na CIAEJ
ENZYMY W CHEMII. Michał Rachwalski. Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii Organicznej i Stosowanej
 ENZYMY W CHEMII Michał Rachwalski Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii rganicznej i Stosowanej Czym są enzymy? Enzymy są białkami zawierającymi od 60 do 1000 reszt aminokwasów; Enzymy są
ENZYMY W CHEMII Michał Rachwalski Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii rganicznej i Stosowanej Czym są enzymy? Enzymy są białkami zawierającymi od 60 do 1000 reszt aminokwasów; Enzymy są
Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej
 Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej Zespół VI Opiekun: dr hab. Jacek Młynarski, prof. nadzw. Oskar Popik Wstęp Początki organokatalizy Pierwszy przykład organokatalitycznej
Aminy pierwszorzędowe - niedoceniane katalizatory w syntezie asymetrycznej Zespół VI Opiekun: dr hab. Jacek Młynarski, prof. nadzw. Oskar Popik Wstęp Początki organokatalizy Pierwszy przykład organokatalitycznej
We wstępie autorka pracy zaprezentowała cel pracy opracowanie syntezy trzech optycznie czynnych kwasów aminofosfonowych, zawierających w swojej
 dr hab. Jacek Ścianowski, prof. UMK Toruń, 29 października 2016r. Katedra Chemii Organicznej, Wydział Chemii, Uniwersytet Mikołaja Kopernika w Toruniu 87-100 Toruń, ul. Gagarina 7 Recenzja rozprawy doktorskiej
dr hab. Jacek Ścianowski, prof. UMK Toruń, 29 października 2016r. Katedra Chemii Organicznej, Wydział Chemii, Uniwersytet Mikołaja Kopernika w Toruniu 87-100 Toruń, ul. Gagarina 7 Recenzja rozprawy doktorskiej
Otrzymywanie -aminokwasów
 trzymywanie -aminokwasów Przykłady -aminokwasów o znaczeniu praktycznym Cl Cl 2 C 2 Melaphalan (lek przeciwnowotworowy) 2 C 2 Levodopa (stosowana w chorobie Parkinsona) 1 1 2 2 3 C środowisko wodne reakcja
trzymywanie -aminokwasów Przykłady -aminokwasów o znaczeniu praktycznym Cl Cl 2 C 2 Melaphalan (lek przeciwnowotworowy) 2 C 2 Levodopa (stosowana w chorobie Parkinsona) 1 1 2 2 3 C środowisko wodne reakcja
STEREOCHEMIA ORGANICZNA
 STEECEMIA GANICZNA Sławomir Jarosz Wykład 6 Typowe energie (ev) i współczynniki orbitalne X LUM 1.5 1.0 C 0 Z +3.0 M -10.5-9.1 C -10.9 Z -9.0 X Typowe energie (ev) i współczynniki orbitalne X LUM 1.0 +0.5
STEECEMIA GANICZNA Sławomir Jarosz Wykład 6 Typowe energie (ev) i współczynniki orbitalne X LUM 1.5 1.0 C 0 Z +3.0 M -10.5-9.1 C -10.9 Z -9.0 X Typowe energie (ev) i współczynniki orbitalne X LUM 1.0 +0.5
STEREOCHEMIA ORGANICZNA Wykład 6
 STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne 1.5 1.0 0 +3.0 1.0 +0.5-0.5 +2.5-10.5-9.1-10.9-9.0-9.1-8.2-9.5-8.5 Me x (-8.5 ev) (+2.5 ev) x+n y (~0 ev) y+m (-10.9 ev) Me x x+n
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Nazwa przedmiotu (w języku. Chemia organiczna II polskim oraz angielskim)
 Nazwa pola Komentarz Nazwa (w języku Chemia organiczna II polskim oraz angielskim) Organic Chemistry II Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
Nazwa pola Komentarz Nazwa (w języku Chemia organiczna II polskim oraz angielskim) Organic Chemistry II Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
ENZYMY W CHEMII. Michał Rachwalski. Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii Organicznej i Stosowanej
 ENZYMY W CHEMII Michał Rachwalski Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii rganicznej i Stosowanej - pojęcie enzymu; Plan wykładu - enzymy izolowane a całe komórki - enzymy jako katalizatory
ENZYMY W CHEMII Michał Rachwalski Uniwersytet Łódzki, Wydział Chemii, Katedra Chemii rganicznej i Stosowanej - pojęcie enzymu; Plan wykładu - enzymy izolowane a całe komórki - enzymy jako katalizatory
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
STEREOCHEMIA ORGANICZNA
 STERECEMIA RGANICZNA Sławomir Jarosz Wykład 6 Jak otrzymać związki optycznie czynne??? 1. Ze związków chiralnych a. Klasyczny : A (rac) b. Rozdział mieszaniny racemicznej na CIRALNEJ kolumnie (Y. kamoto,
STERECEMIA RGANICZNA Sławomir Jarosz Wykład 6 Jak otrzymać związki optycznie czynne??? 1. Ze związków chiralnych a. Klasyczny : A (rac) b. Rozdział mieszaniny racemicznej na CIRALNEJ kolumnie (Y. kamoto,
RECENZJA PRACY DOKTORSKIEJ
 Prof. dr hab. Piotr Kiełbasiński Kierownik Zakładu Chemii Heteroorganicznej Centrum Badań Molekularnych i Makromolekularnych Polskiej Akademii Nauk ul. Sienkiewicza 112, 90-363 Łódź Tel: (42) 680 32 21
Prof. dr hab. Piotr Kiełbasiński Kierownik Zakładu Chemii Heteroorganicznej Centrum Badań Molekularnych i Makromolekularnych Polskiej Akademii Nauk ul. Sienkiewicza 112, 90-363 Łódź Tel: (42) 680 32 21
prof. dr hab. Zbigniew Czarnocki Warszawa, 3 lipca 2015 Uniwersytet Warszawski Wydział Chemii
 prof. dr hab. Zbigniew Czarnocki Warszawa, 3 lipca 2015 Uniwersytet Warszawski Wydział Chemii Recenzja pracy doktorskiej Pana mgr Michała Smolenia, zatytułowanej Modyfikacja N-heterocyklicznych karbenów
prof. dr hab. Zbigniew Czarnocki Warszawa, 3 lipca 2015 Uniwersytet Warszawski Wydział Chemii Recenzja pracy doktorskiej Pana mgr Michała Smolenia, zatytułowanej Modyfikacja N-heterocyklicznych karbenów
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
CENTRUM BADAŃ MOLEKULARNYCH I MAKROMOLEKULARNYCH POLSKA AKADEMIA NAUK Zakład Chemii Heteroorganicznej Łódź, Sienkiewicza 112
 CENTRUM BADAŃ MOLEKULARNYCH I MAKROMOLEKULARNYCH POLSKA AKADEMIA NAUK Zakład Chemii Heteroorganicznej 90-363 Łódź, Sienkiewicza 112 Tel.: (+48-42) 680-32-34 Fax: (+48-42) 684-71-26 E-mail: draj@bilbo.cbmm.lodz.pl
CENTRUM BADAŃ MOLEKULARNYCH I MAKROMOLEKULARNYCH POLSKA AKADEMIA NAUK Zakład Chemii Heteroorganicznej 90-363 Łódź, Sienkiewicza 112 Tel.: (+48-42) 680-32-34 Fax: (+48-42) 684-71-26 E-mail: draj@bilbo.cbmm.lodz.pl
Mg I. I Mg. Nie można ich jednak otrzymać ze związków, które posiadają grupy chlorowcowe w tak zwanym ustawieniu wicynalnym.
 nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
nformacje do zadań kwalifikacyjnych na "Analizę retrosyntetyczną" Urszula Chrośniak, Marcin Goławski Właściwe zadania znajdują się na stronach 9.-10. Strony 1.-8. zawieraja niezbędne informacje wstępne.
Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady
 Synteza i wykorzystanie -aminoketonów (zasad Mannicha) Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady i-pr Falicain środek zneczulający 2 Tramadol środek przeciwbólowy snervan choroba
Synteza i wykorzystanie -aminoketonów (zasad Mannicha) Zasady Mannicha i ich pochodne stosowane w lecznictwie - przykłady i-pr Falicain środek zneczulający 2 Tramadol środek przeciwbólowy snervan choroba
Prof. dr hab. Inż. Jacek Skarżewski
 Prof. dr hab. Inż. Jacek Skarżewski Zakład Chemii Organicznej, Wydział Chemiczny Politechnika Wrocławska, Wyb. Wyspiańskiego 27 50-370 Wrocław Tel.: (071) 320 2464, fax.: (071) 328 4064 E-mail: jacek.skarzewski@pwr.wroc.pl
Prof. dr hab. Inż. Jacek Skarżewski Zakład Chemii Organicznej, Wydział Chemiczny Politechnika Wrocławska, Wyb. Wyspiańskiego 27 50-370 Wrocław Tel.: (071) 320 2464, fax.: (071) 328 4064 E-mail: jacek.skarzewski@pwr.wroc.pl
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Rys. 1. Podstawowy koncept nukleozydów acyklicznych. a-podstawienie nukleofilowe grupy nukleofugowej w czynniku alkilującycm
 Nukleozydy acykliczne Jak już wspomniano nukleozydy acykliczne formalnie są N-alkilowymi pochodnymi nukleozasad. Fragment acykliczny najczęściej zawiera atom tlenu naśladujący tlen pierścieniowy jak również
Nukleozydy acykliczne Jak już wspomniano nukleozydy acykliczne formalnie są N-alkilowymi pochodnymi nukleozasad. Fragment acykliczny najczęściej zawiera atom tlenu naśladujący tlen pierścieniowy jak również
CHIRALNOŚĆ WŁAŚCIWOŚĆ MATERII EGZOTYCZNA CZY WSZECHOBECNA?
 IRALNŚĆ WŁAŚIWŚĆ MATERII EGZTYZNA ZY WSZEBENA? Stanisław Krompiec Uniwersytet Śląski, Katowice, 2017 r. hiralność definicja biekty achiralne i chiralne biekt achiralny biekty achiralne - przykłady hiralność
IRALNŚĆ WŁAŚIWŚĆ MATERII EGZTYZNA ZY WSZEBENA? Stanisław Krompiec Uniwersytet Śląski, Katowice, 2017 r. hiralność definicja biekty achiralne i chiralne biekt achiralny biekty achiralne - przykłady hiralność
ZWIĄZKI FOSFOROORGANICZNE
 ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
ZWIĄZKI FSFGANICZNE Związki fosforoorganiczne związki zawierające wiązanie węgiel-fosfor (C-) Wiązanie fosfor-wodór (-H; 77 kcal/mol) jest słabsze niż wiązanie azot-wodór (N-H; 93.4 kcal/mol). Wiązanie
PL B1. Kwasy α-hydroksymetylofosfonowe pochodne 2-azanorbornanu i sposób ich wytwarzania. POLITECHNIKA WROCŁAWSKA, Wrocław, PL
 PL 223370 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 223370 (13) B1 (21) Numer zgłoszenia: 407598 (51) Int.Cl. C07D 471/08 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data zgłoszenia:
PL 223370 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 223370 (13) B1 (21) Numer zgłoszenia: 407598 (51) Int.Cl. C07D 471/08 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data zgłoszenia:
Br Br. Br Br OH 2 OH NH NH 2 2. Zakład Chemii Organicznej: kopiowanie zabronione
 Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Reakcje związków karbonylowych zudziałem atomu węgla alfa (C- )
 34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
34-37. eakcje związków karbonylowych zudziałem atomu węgla alfa (C- ) stabilizacja rezonansem (przez delokalizację elektronów), może uczestniczyć w delokalizacji elektronów C- -, podatny na oderwanie ze
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Substytucje Nukleofilowe w Pochodnych Karbonylowych
 J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
J 1 Substytucje kleofilowe w Pochodnych Karbonylowych Y Y Y Slides 1 to 21 J 2 Addycje vs Podstawienia Ładunek δ zlokalizowany na atomie węgla w grupy karbonylowej powoduje, Ŝe e atak nukleofila moŝe doprowadzić
LNA i metody jego syntezy
 LNA i metody jego syntezy LNA (Locked Nucleic Acids) nazwa ta obejmuje jeden z typów modyfikowanych kwasów nukleinowych, w których pentofuranozowy fragment cukrowy ma utrwaloną konformację pierścienia
LNA i metody jego syntezy LNA (Locked Nucleic Acids) nazwa ta obejmuje jeden z typów modyfikowanych kwasów nukleinowych, w których pentofuranozowy fragment cukrowy ma utrwaloną konformację pierścienia
Układy pięcioczłonowe z jednym heteroatomem
 WYKŁAD 7 Układy pięcioczłonowe z jednym heteroatomem Furan 1-Pirol Tiofen Benzofuran 1-Indol Benzo[b]tiofen Tetrahydrofuran Pirolidyna Tiolan 1 1. Muskaryna (I, muscarine) Alkaloid pochodzenia naturalnego
WYKŁAD 7 Układy pięcioczłonowe z jednym heteroatomem Furan 1-Pirol Tiofen Benzofuran 1-Indol Benzo[b]tiofen Tetrahydrofuran Pirolidyna Tiolan 1 1. Muskaryna (I, muscarine) Alkaloid pochodzenia naturalnego
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
EGZAMIN WSTĘPNY NA STUDIUM DOKTORANCKIE W CBMIM PAN W ŁODZI. Zestaw pytań z chemii organicznej
 EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
EGZMIN WSTĘPNY N STUDIUM DKTRNKIE W BMIM PN W ŁDZI Zestaw pytań z chemii organicznej 1. Proszę narysować orbitalny obraz cząsteczki allenu 2 == 2. Jaka jest hybrydyzacja środkowego atomu węgla: sp 2 czy
I KSZTAŁCENIA PRAKTYCZNEGO. Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty
 ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
ŁÓDZKIE CENTRUM DOSKONALENIA NAUCZYCIELI I KSZTAŁCENIA PRAKTYCZNEGO XV Konkurs Chemii Organicznej rok szkolny 2011/12 Imię i nazwisko Szkoła Klasa Nauczyciel Uzyskane punkty Zadanie 1 (9 pkt) Ciekłą mieszaninę,
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Heteroatomowe analogi cyklopropenonu
 RACE AUKWE Akademii im. Jana Długosza w Częstochowie eria: CEMIA I CRA ŚRDWIKA 2008, XII, 83-89 Adrian Zając a,b Józef Drabowicz a,b a Instytut Chemii i chrony Środowiska, Akademia im. Jana Długosza, 42
RACE AUKWE Akademii im. Jana Długosza w Częstochowie eria: CEMIA I CRA ŚRDWIKA 2008, XII, 83-89 Adrian Zając a,b Józef Drabowicz a,b a Instytut Chemii i chrony Środowiska, Akademia im. Jana Długosza, 42
14. Reakcje kwasów karboksylowych i ich pochodnych
 14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
14. Reakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór R N R R grupa karbonylowa atom (, N lub Cl) o
Zadanie: 2 (4 pkt) Napisz, uzgodnij i opisz równania reakcji, które zaszły w probówkach:
 Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
Zadanie: 1 (1 pkt) Aby otrzymać ester o wzorze CH 3 CH 2 COOCH 3 należy jako substratów użyć: a) Kwasu etanowego i metanolu b) Kwasu etanowego i etanolu c) Kwasu metanowego i etanolu d) Kwasu propanowego
CHIRALNE KWASY FOSFOROWE WŁAŚCIWOŚCI I ZASTOSOWANIE. Anna Kozioł Zespół II
 CHIRALNE KWASY FSFRWE WŁAŚCIWŚCI I ZASTSWANIE Anna Kozioł Zespół II STATNIE ZASTSWANIA KWASÓW W FSFRWYCH PARTYCH NA BINLU KWASY BRØNSTEDA JAK KATALIZATRY Model aktywacji kwasami Brønsteda Rozwój enancjoselektywnych,
CHIRALNE KWASY FSFRWE WŁAŚCIWŚCI I ZASTSWANIE Anna Kozioł Zespół II STATNIE ZASTSWANIA KWASÓW W FSFRWYCH PARTYCH NA BINLU KWASY BRØNSTEDA JAK KATALIZATRY Model aktywacji kwasami Brønsteda Rozwój enancjoselektywnych,
Węglowodory poziom rozszerzony
 Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Wydział Chemii. Prof. dr hab. Grzegorz Schroeder Poznań, dnia 17 grudnia 2016 r.
 Wydział Chemii Prof. dr hab. Grzegorz Schroeder Poznań, dnia 17 grudnia 2016 r. RECENZJA osiągnięcia naukowego pt. Aminokwasy jako platformy molekularne w projektowaniu receptorów par jonowych oraz całokształtu
Wydział Chemii Prof. dr hab. Grzegorz Schroeder Poznań, dnia 17 grudnia 2016 r. RECENZJA osiągnięcia naukowego pt. Aminokwasy jako platformy molekularne w projektowaniu receptorów par jonowych oraz całokształtu
Stereochemia Ułożenie atomów w przestrzeni
 Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Slajd 1 Stereochemia Ułożenie atomów w przestrzeni Slajd 2 Izomery Izomery to różne związki posiadające ten sam wzór sumaryczny izomery izomery konstytucyjne stereoizomery izomery cis-trans izomery zawierające
Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
 Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
Zadanie 1. (2 pkt) Poniżej przedstawiono schemat syntezy pewnego związku. Zidentyfikuj związki A i B. w tym celu podaj ich wzory półstrukturalne Podaj nazwy grup związków organicznych, do których one należą.
RJC # Alk l a k ny n Ster St eoi er zom eoi er zom y er Slides 1 to 30
 Alkany Stereoizomery Slides 1 to 30 Centrum asymetryczne (stereogeniczne) Atom węgla o hybrydyzacji sp 3 połączony z czterema róŝnymi podstawnikami tworzy centrum asymetryczne (stereogeniczne). Chiralność
Alkany Stereoizomery Slides 1 to 30 Centrum asymetryczne (stereogeniczne) Atom węgla o hybrydyzacji sp 3 połączony z czterema róŝnymi podstawnikami tworzy centrum asymetryczne (stereogeniczne). Chiralność
Różnorodny świat izomerów powtórzenie wiadomości przed maturą
 Różnorodny świat izomerów powtórzenie wiadomości przed maturą Maria Kluz Klasa III, profil biologiczno-chemiczny i matematyczno-chemiczny 1 godzina lekcyjna, praca w grupie 16-osobowej. Cele edukacyjne:
Różnorodny świat izomerów powtórzenie wiadomości przed maturą Maria Kluz Klasa III, profil biologiczno-chemiczny i matematyczno-chemiczny 1 godzina lekcyjna, praca w grupie 16-osobowej. Cele edukacyjne:
RECENZJA pracy doktorskiej mgr Piotra Pomarańskiego Zastosowanie kompleksów palladu do syntezy pochodnych aromatycznych o chiralności osiowej
 Strona1 Dr hab. Beata Jasiewicz, prof. UAM Poznań, dnia 15 lipca 2019 r. Uniwersytet im. Adama Mickiewicza Ul. Uniwersytetu Poznańskiego 8 61-614 Poznań beatakoz@amu.edu.pl RECENZJA pracy doktorskiej mgr
Strona1 Dr hab. Beata Jasiewicz, prof. UAM Poznań, dnia 15 lipca 2019 r. Uniwersytet im. Adama Mickiewicza Ul. Uniwersytetu Poznańskiego 8 61-614 Poznań beatakoz@amu.edu.pl RECENZJA pracy doktorskiej mgr
Materiały dodatkowe związki karbonylowe
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe związki karbonylowe 1. Polaryzacja wiązania C= Charakterystyczną cechą związków posiadających grupę karbonylową
Skala ocen: ndst 0 20, dst , dst , db , db , bdb Informacja:
 Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
59 Olimpiada Chemiczna I etap PRÓBA. 10 października 2012, 10:00 15:00. redagowanie treści: Kuba Skrzeczkowski
 59 Olimpiada Chemiczna I etap PRÓBA 10 października 2012, 10:00 15:00 redagowanie treści: Kuba Skrzeczkowski ZADANIE 1. Dwa problemy z kinetyki chemicznej A. W podwyższonej temperaturze izomery geometryczne
59 Olimpiada Chemiczna I etap PRÓBA 10 października 2012, 10:00 15:00 redagowanie treści: Kuba Skrzeczkowski ZADANIE 1. Dwa problemy z kinetyki chemicznej A. W podwyższonej temperaturze izomery geometryczne
Nazwa przedmiotu (w języku. CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot
 Nazwa pola Komentarz Nazwa (w języku CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
Nazwa pola Komentarz Nazwa (w języku CHEMIA ORGANICZNA I polskim oraz angielskim) ORGANIC CHEMISTRY I Jednostka oferująca przedmiot CBMiM PAN Liczba punktów ECTS 5 Sposób zaliczenia Egzamin Język wykładowy
Wydział Chemii. Strona1
 Strona1 Dr hab. Beata Jasiewicz, prof. UAM Poznań, dnia 15 kwietnia 2019 r. Uniwersytet im. Adama Mickiewicza Ul. Umultowska 89b 61-614 Poznań beatakoz@amu.edu.pl RECENZJA pracy doktorskiej mgr Moniki
Strona1 Dr hab. Beata Jasiewicz, prof. UAM Poznań, dnia 15 kwietnia 2019 r. Uniwersytet im. Adama Mickiewicza Ul. Umultowska 89b 61-614 Poznań beatakoz@amu.edu.pl RECENZJA pracy doktorskiej mgr Moniki
Rys. 1. C-nukleozydy występujące w trna
 C-Nukleozydy Z próbek transferowego kwasu rybonukleinowego (trna) w roku 1957 wydzielono związek, zawierający w swej strukturze pierścień uracylowy i cukrowy, połączone odmiennie niż w klasycznych nukleozydach.
C-Nukleozydy Z próbek transferowego kwasu rybonukleinowego (trna) w roku 1957 wydzielono związek, zawierający w swej strukturze pierścień uracylowy i cukrowy, połączone odmiennie niż w klasycznych nukleozydach.
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
CHEMIA ORGANICZNA II nazwa SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów Kod Język
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne
 CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
CHEMIA ORGANICZNA II nazwa przedmiotu SYLABUS A. Informacje ogólne Elementy składowe sylabusu Nazwa jednostki prowadzącej kierunek Nazwa kierunku studiów Poziom kształcenia Profil studiów Forma studiów
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
Metody fosforylacji. Schemat 1. Powstawanie trifosforanu nukleozydu
 Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Metody fosforylacji Fosforylacja jest procesem przenoszenia reszty fosforanowej do nukleofilowego atomu dowolnego związku chemicznego. Najczęściej fosforylację przeprowadza się na atomie tlenu grupy hydroksylowej
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Reakcje alkoholi, eterów, epoksydów, amin i tioli
 22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
22-24. Reakcje alkoholi, eterów, epoksydów, amin i tioli gr. odchodząca wymaga aktywacji gr. najłatwiej odchodząca gr. najtrudniej odchodząca najmocniejszy kwas X = Cl, Br, I najsłabszy kwas Chemia rganiczna,
Otrzymywanie i zastosowanie chiralnych monotosylowanych 1,2-dwuamin w syntezie asymetrycznej
 Dr Piotr Roszkowski Uniwersytet Warszawski Wydział Chemii Zakład Chemii rganicznej i Technologii Chemicznej Pracownia Chemii Związków aturalnych ul. Pasteura 1 02-093 Warszawa trzymywanie i zastosowanie
Dr Piotr Roszkowski Uniwersytet Warszawski Wydział Chemii Zakład Chemii rganicznej i Technologii Chemicznej Pracownia Chemii Związków aturalnych ul. Pasteura 1 02-093 Warszawa trzymywanie i zastosowanie
Chemia organiczna. Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok)
 Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Chemia organiczna Zagadnienia i przykładowe pytania do kolokwiów dla Biotechnologii (I rok) Zakład Chemii Organicznej Wydział Chemii Uniwersytet Wrocławski 2005 Lista zagadnień: Kolokwium I...3 Kolokwium
Organokataliza mechanizmy, katalizatory, reakcje. Maria Rogozińska Zespół VI
 rganokataliza mechanizmy, katalizatory, reakcje Maria ogozińska Zespół VI rganokataliza Katalizowanie reakcji chemicznych małymi cząsteczkami organicznymi, zbudowanymi z węgla, wodoru, fosforu, azotu,
rganokataliza mechanizmy, katalizatory, reakcje Maria ogozińska Zespół VI rganokataliza Katalizowanie reakcji chemicznych małymi cząsteczkami organicznymi, zbudowanymi z węgla, wodoru, fosforu, azotu,
Rzeszów, 27 listopada, 2012 r.
 Rzeszów, 27 listopada, 2012 r. OPINIA o całokształcie dorobku naukowego dr inż. Marii MADEJ- LACHOWSKIEJ ze szczególnym uwzględnieniem rozprawy habilitacyjnej pt. Reforming metanolu parą wodną termodynamika,
Rzeszów, 27 listopada, 2012 r. OPINIA o całokształcie dorobku naukowego dr inż. Marii MADEJ- LACHOWSKIEJ ze szczególnym uwzględnieniem rozprawy habilitacyjnej pt. Reforming metanolu parą wodną termodynamika,
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA
 Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
RECENZJA PRACY DOKTORSKIEJ
 Prof. dr hab. Piotr Kiełbasiński Koordynator Działu Chemii Organicznej Centrum Badań Molekularnych i Makromolekularnych Polskiej Akademii Nauk ul. Sienkiewicza 112, 90-363 Łódź Tel.: (42); 680 32 13; Fax.:
Prof. dr hab. Piotr Kiełbasiński Koordynator Działu Chemii Organicznej Centrum Badań Molekularnych i Makromolekularnych Polskiej Akademii Nauk ul. Sienkiewicza 112, 90-363 Łódź Tel.: (42); 680 32 13; Fax.:
1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne
 B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
B T E C N L CEMA G RGANCZNA A Synteza 1. Katalityczna redukcja węglowodorów zawierających wiązania wielokrotne C C / Pt C C C C W reakcji tej łańcuch węglowy pozostaje zachowany (nie ulega zmianie jego
Węglowodory poziom podstawowy
 Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
CF 3. Praca ma charakter eksperymentalny, powstałe produkty będą analizowane głównie metodami NMR (1D, 2D).
 Tematy prac magisterskich 2017/2018 Prof. dr hab. Henryk Koroniak Zakład Syntezy i Struktury Związków rganicznych Zespół Dydaktyczny Chemii rganicznej i Bioorganicznej 1. Synteza fosfonianowych pochodnych
Tematy prac magisterskich 2017/2018 Prof. dr hab. Henryk Koroniak Zakład Syntezy i Struktury Związków rganicznych Zespół Dydaktyczny Chemii rganicznej i Bioorganicznej 1. Synteza fosfonianowych pochodnych
II Podkarpacki Konkurs Chemiczny 2009/10. ETAP II r. Godz Zadanie 1 (10 pkt.)
 II Podkarpacki Konkurs Chemiczny 2009/10 ETAP II 19.12.2009 r. Godz. 10.00-12.00 KPKCh Zadanie 1 (10 pkt.) 1. Gęstość 22% roztworu kwasu chlorowodorowego o stężeniu 6,69 mol/dm 3 wynosi: a) 1,19 g/cm 3
II Podkarpacki Konkurs Chemiczny 2009/10 ETAP II 19.12.2009 r. Godz. 10.00-12.00 KPKCh Zadanie 1 (10 pkt.) 1. Gęstość 22% roztworu kwasu chlorowodorowego o stężeniu 6,69 mol/dm 3 wynosi: a) 1,19 g/cm 3
SYNTEZA 2,4,6-TRIARYLOPIRYDYNY (wprowadzenie teoretyczne)
 SYTEZA 2,4,6-TRIARYLPIRYDYY (wprowadzenie teoretyczne) ZADAIA 2A-B 2,4,6-Trifenylopirydyna została otrzymana po raz pierwszy już ponad sto lat temu. Wykorzystana wówczas metoda polegała na reakcji soli
SYTEZA 2,4,6-TRIARYLPIRYDYY (wprowadzenie teoretyczne) ZADAIA 2A-B 2,4,6-Trifenylopirydyna została otrzymana po raz pierwszy już ponad sto lat temu. Wykorzystana wówczas metoda polegała na reakcji soli
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Kierunek i poziom studiów: Biotechnologia, pierwszy. Nazwa wariantu modułu (opcjonalnie): nie dotyczy
 Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
Kierunek i poziom studiów: Biotechnologia, pierwszy Sylabus modułu: Chemia organiczna (1BT_13) Nazwa wariantu modułu (opcjonalnie): nie dotyczy 1. Informacje ogólne koordynator modułu/wariantu Dr Halina
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE
 PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
LCH 1 Zajęcia nr 60 Diagnoza końcowa. Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach:
 LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
LCH 1 Zajęcia nr 60 Diagnoza końcowa Zadanie 1 (3 pkt) Zaprojektuj jedno doświadczenie pozwalające na odróżnienie dwóch węglowodorów o wzorach: H 3 C CH 2 CH 2 CH 2 CH 2 a) b) W tym celu: a) wybierz odpowiedni
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Alkeny - reaktywność
 11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
11-13. Alkeny - reaktywność 1 6.1. Addycja elektrofilowa - wprowadzenie nukleofil elektrofil elektrofil nukleofil wolno szybko nowe wiązanie utworzone przez elektrony z wiązania nowe wiązanie utworzone
Jak analizować widmo IR?
 Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
Jak analizować widmo IR? Literatura: W. Zieliński, A. Rajca, Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych. WNT. R. M. Silverstein, F. X. Webster, D. J. Kiemle, Spektroskopowe
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
wykład monograficzny O niektórych sposobach udoskonalania procesów katalizowanych metalami i ich związkami
 wykład monograficzny niektórych sposobach udoskonalania procesów katalizowanych metalami i ich związkami rocesy katalizowane kompleksami metali Wybrane przykłady ydroodsiarczanie ropy naftowej e, Mo ydroformylacja
wykład monograficzny niektórych sposobach udoskonalania procesów katalizowanych metalami i ich związkami rocesy katalizowane kompleksami metali Wybrane przykłady ydroodsiarczanie ropy naftowej e, Mo ydroformylacja
Reakcje kwasów karboksylowych i ich pochodnych
 27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
27-29. eakcje kwasów karboksylowych i ich pochodnych nazwa ogólna kwas karboksylowy bezwodnik kwasowy chlorek kwasowy ester amid 1 amid 2 amid 3 nitryl wzór N grupa karbonylowa atom (, N lub Cl) o większej
Właściwości chemiczne nukleozydów pirymidynowych i purynowych
 Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
Właściwości chemiczne nukleozydów pirymidynowych i purynowych Właściwości nukleozydów są ściśle powiązane z elementami strukturalnymi ich budowy. Zasada azotowa obecna w nukleozydach może być poddawana
KWASY KARBOKSYLOWE I ICH POCHODNE. R-COOH lub R C gdzie R = H, CH 3 -, C 6 H 5 -, itp.
 KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
KWASY KARBKSYLWE I IH PHDNE I. Wprowadzenie teoretyczne Kwasy karboksylowe Kwasami organicznymi nazywamy związki, w których grupa funkcyjna H zwana grupą karboksylową jest związana z rodnikiem węglowodorowym
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
O MATURZE Z CHEMII ANALIZA TRUDNYCH DLA ZDAJĄCYCH PROBLEMÓW
 O MATURZE Z CHEMII ANALIZA TRUDNYCH DLA ZDAJĄCYCH PROBLEMÓW Jolanta Baldy Wrocław, 2 grudnia 2016 r. Matura 2016 z chemii w liczbach Średni wynik procentowy Województwo dolnośląskie 36% (1981) Województwo
O MATURZE Z CHEMII ANALIZA TRUDNYCH DLA ZDAJĄCYCH PROBLEMÓW Jolanta Baldy Wrocław, 2 grudnia 2016 r. Matura 2016 z chemii w liczbach Średni wynik procentowy Województwo dolnośląskie 36% (1981) Województwo
Opinia o pracy doktorskiej pani mgr Beaty Łukasik pt. Synteza nowych chiralnych bloków budulcowych i ich zastosowanie w syntezie cyklopentanoidów
 Prof. dr hab. Inż. Jacek Skarżewski Zakład Chemii Organicznej, Wydział Chemiczny Politechnika Wrocławska, Wyb. Wyspiańskiego 27 50-370 Wrocław Tel.: (071) 320 2464, fax.: (071) 328 4064 E-mail: jacek.skarzewski@pwr.wroc.pl
Prof. dr hab. Inż. Jacek Skarżewski Zakład Chemii Organicznej, Wydział Chemiczny Politechnika Wrocławska, Wyb. Wyspiańskiego 27 50-370 Wrocław Tel.: (071) 320 2464, fax.: (071) 328 4064 E-mail: jacek.skarzewski@pwr.wroc.pl
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego O O
 Zastosowanie spektrometrii mas do określania struktury związków organicznych (opracowała Anna Kolasa) Uwaga: Informacje na temat nowych technik jonizacji, budowy analizatorów, nowych metod detekcji jonów
Zastosowanie spektrometrii mas do określania struktury związków organicznych (opracowała Anna Kolasa) Uwaga: Informacje na temat nowych technik jonizacji, budowy analizatorów, nowych metod detekcji jonów
ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY
 ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Poprawne rozwiązania zadań, uwzględniające
ODPOWIEDZI I SCHEMAT PUNKTOWANIA POZIOM ROZSZERZONY Zdający otrzymuje punkty tylko za poprawne rozwiązania, precyzyjnie odpowiadające poleceniom zawartym w zadaniach. Poprawne rozwiązania zadań, uwzględniające
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
MIKROANALIZY WĘGLOWODORY. W1 Utlenianie węglowodorów nadmanganianem potasu w środowisku kwaśnym (w temp. pokojowej) RÓWNANIA REAKCJI: OBSERWACJE:
 MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
MIKROANALIZY imię i nazwisko Rubryki odpowiednio opisane (lekko przyciemnione) należy wypełniać przed rozpoczęciem zajęć. Opisując obserwacje reakcji należy wyraźnie napisać co się zmienia lub nie. Jeśli
Laboratorium. Podstawowe procesy jednostkowe w technologii chemicznej
 Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
ZAAWANSOWANE METODY USTALANIA BUDOWY ZWIĄZKÓW ORGANICZNYCH
 ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
ZAAWANSWANE METDY USTALANIA BUDWY ZWIĄZKÓW RGANICZNYC Witold Danikiewicz Instytut Chemii rganicznej PAN ul. Kasprzaka /52, 0-22 Warszawa Interpretacja widm NMR, IR i MS prostych cząsteczek Czyli jak powiązać
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII
 ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
dr hab. Witold Gładkowski Wrocław, Katedra Chemii Uniwersytet Przyrodniczy we Wrocławiu
 dr hab. Witold Gładkowski Wrocław, 25.08.2017 Katedra Chemii Uniwersytet Przyrodniczy we Wrocławiu Recenzja pracy doktorskiej Pana mgr Adama Dropa pt. Stereoselektywne reakcje jonów enolanowych pochodnych
dr hab. Witold Gładkowski Wrocław, 25.08.2017 Katedra Chemii Uniwersytet Przyrodniczy we Wrocławiu Recenzja pracy doktorskiej Pana mgr Adama Dropa pt. Stereoselektywne reakcje jonów enolanowych pochodnych
STEREOCHEMIA ORGANICZNA Wykład 6
 STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne Reakcja Dielsa Aldera - Regioselektywność w reakcjach DA LUM M 1.5-10.5 M 1.0-9.1 LUM 0-10.9 +3.0-9.0 Me M (-8.5 ev) LUM (+2.5 ev)
STEREEMIA RGAIA Wykład 6 Typowe energie (ev) i współczynniki orbitalne Reakcja Dielsa Aldera - Regioselektywność w reakcjach DA LUM M 1.5-10.5 M 1.0-9.1 LUM 0-10.9 +3.0-9.0 Me M (-8.5 ev) LUM (+2.5 ev)
