Rekomendacje Recommendations
|
|
|
- Mariusz Witek
- 9 lat temu
- Przeglądów:
Transkrypt
1 diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab 2014; 50(1): Rekomendacje Recommendations Postępowanie przedanalityczne w laboratoryjnej diagnostyce zaburzeń hemostazy Zalecenia Sekcji Laboratoryjnej Diagnostyki Zaburzeń Hemostazy Polskiego Towarzystwa Diagnostyki Laboratoryjnej Preanalytical procedure in laboratory diagnostics of coagulation disorders Recommendations of the Haemostatic Disorders Working Group, Polish Society of Laboratory Diagnostics Anna Raszeja-Specht 1 Jacek Golański 2 1 Zakład Medycyny Laboratoryjnej, Katedra Biochemii Klinicznej, Gdański Uniwersytet Medyczny; 2 Zakład Zaburzeń Krzepnięcia Krwi, Katedra Nauk Biomedycznych, Uniwersytet Medyczny w Łodzi Opracowanie materiału przed wykonaniem badania z zakresu laboratoryjnej diagnostyki hemostazy w istotny sposób wpływa na końcowy wynik oznaczenia [1-4]. Szacuje się, że błędy związane z niewłaściwym postępowaniem przedanalitycznym, wykluczające materiał z dalszych badań i obniżające wiarygodność uzyskiwanych wyników, wynoszą w przypadku hemostazy 5-10% i mogą pojawiać się na kilku etapach postępowania z materiałem (tab. I). Z analizy piśmiennictwa wynika, że obecnie przy pobieraniu krwi do badań hemostazy nie podlega dyskusji zastosowanie cytrynianu sodu o stężeniu 3,2% [1], ale nie ma jasnych danych na temat przewagi buforowanego cytrynianu nad niebuforowanym [5]. Niestety, w dalszym ciągu nie ma pełnej zgodności w sprawie sposobu pobierania krwi do badań [6-10] i czasu jego przechowywania przed wykonaniem oznaczeń [1, 11-14]. Szczególnie wiele kontrowersji wywołały zalecenia opublikowane przez Clinical Laboratory and Standards Institute (CLSI), z których wynika, że krew do badania czasu protrombinowego można przechowywać przez 24 godziny [1]. Zalecenie to jest powielane przez wydawnictwa książkowe [2, 3], warto jest jednak zwrócić uwagę na zastrzeżenie, iż konieczne jest ustalenie własnych standardów przechowywania materiału [15]. W przywoływanej w dokumencie CLSI publikacji Van Geest-Daalderop i wsp. sugerowany, maksymalny czas przechowywania materiału przed oznaczeniem wynosi 6 godzin. Dyskusja o czasie przechowywania materiału [11-14, 16] będzie prawdopodobnie trwała do czasu Tabela I. Przedanalityczne problemy w badaniach układu hemostazy [18,19] Procedura przedanalityczna Przygotowanie pacjenta Pobranie próbki Postępowanie z próbką Transport próbki Przechowywanie próbki Przygotowanie próbki Problemy związane z procedurą Aktywność fizyczna, dieta, używki, leki itp. Identyfikacja pacjenta/ próbki Niewłaściwa procedura pobrania (wybór miejsca pobrania, staza) Niewłaściwy sprzęt (igły, motylki, zestawy infuzyjne) Niewłaściwe probówki/ antykoagulant Niewłaściwa objętość (proporcje krew/ antykoagulant) Hemoliza Mieszanie próbki (wykrzepianie) Temperatura, czas, warunki Temperatura, czas, mrożenie Wirowanie: temperatura, czas, prędkość, postępowanie z osoczem 65
2 opublikowania nowych zaleceń CLSI. Na spotkaniach Sekcji Laboratoryjnej Diagnostyki Hemostazy Polskiego Towarzystwa Diagnostyki Laboratoryjnej podjęto decyzję o przygotowaniu polskich zaleceń w sprawie postępowania przedanalitycznego w diagnostyce hemostazy, ze szczególnym uwzględnieniem czasu przechowywania materiału. Zalecenia przeznaczone są dla laboratoriów wykonujących podstawową diagnostykę hemostazy, jednakże z uwagi na konieczność opracowywania materiału dla specjalistycznych pracowni dołączone zostały wskazówki dotyczące przygotowania próbek i ich transportu w celu wykonania diagnostyki: trombofilii, małopłytkowości wywołanej heparyną (HIT Heparin Induced Thrombocytopenia), zespołu antyfosfolipidowego (APS - antiphospholipid syndrome), funkcji płytek krwi. Podstawą prawną zaleceń jest Rozporządzenie Ministra Zdrowia z dnia 21 stycznia 2009 r. zmieniające rozporządzenie w sprawie standardów jakości dla medycznych laboratoriów diagnostycznych i mikrobiologicznych [17]. Przygotowane zalecenia mają na celu uszczegółowienie wytycznych zawartych w wyżej wymienionym rozporządzeniu i z założenia są bardziej rygorystyczne niż te zawarte w dokumencie CLSI. Omówienie kolejnych etapów postępowania przedanalitycznego podzielone jest na zalecenia ogólne i szczegółowe, dedykowane konkretnym oznaczeniom. ZALECENIA DOTYCZĄCE POSTĘPOWANIA PRZEDA- NALITYCZNEGO Podstawowe problemy związane z procedurą przedanalityczną zestawiono w tabeli I. PRZYGOTOWANIE PACJENTA 1. Zalecenia ogólne Wysiłek Na 24 godziny przed pobraniem krwi do badań należy unikać intensywnego fizycznego wysiłku. Przed pobraniem krwi zalecany jest relaksujący, minutowy odpoczynek. Dieta W dniu poprzedzającym badanie zalecana jest lekkostrawna, niskotłuszczowa dieta oraz powstrzymanie się od używek, należy uwzględnić pokarmy i suplementy diety bogate w witaminę K i potencjalnie przeciwzakrzepowe. Zdecydowanie niewskazane jest picie kawy naturalnej i palenie nikotyny w dniu pobrania. Zaleca się w dniu pobrania krwi wypicie ok. 0,5 litra wody. Zmienność dobowa Wskazane jest pobieranie krwi w godzinach porannych (do godz. 10). 2. Zalecenia szczegółowe W celu diagnostyki trombofilii krew należy pobrać przed rozpoczęciem leczenia przeciwzakrzepowego lub po upływie odpowiednio długiego czasu po jego zakończeniu (1-2 tygodnie). U osób leczonych heparyną występuje obniżenie aktywności antytrombiny (AT), a u osób leczonych pochodnymi kumaryny występuje obniżenie stężenia czynników z grupy protrombiny oraz białek C i S. W czasie incydentu zakrzepowo-zatorowego oraz bezpośrednio po nim może dojść do obniżenia poziomu AT i aktywności białka S, dlatego badania można wykonywać po 6 tygodniach od wystąpieniu incydentu zakrzepowego. Niewskazane jest wykonywanie badań w czasie infekcji. W tabeli II zaznaczono kierunki zmian podstawowych i dodatkowych badań układu krzepnięcia. Tabela II. Kierunki zmian najważniejszych parametrów układu hemostazy w różnych stanach klinicznych i w trakcie terapii przeciwzakrzepowej [19]. PLT PT APTT Fibrynogen Dimer D Białko C Białko S AT Ciąża N N N lub Okres noworodkowy N N bd bd bd Stan zapalny N N N lub bd bd N lub Zabieg operacyjny lub uraz N N N lub bd bd bd Nowotwory N N N N N N N N Choroby wątroby N N N N N N N Aktywna zakrzepica* N N N Heparyna N N ** bd bd bd bd Antagoniści witaminy K N N N N N * Diagnostyka laboratoryjna trombofilii możliwa jest do wykonania po 6. tygodniach od wystąpienia incydentu zakrzepowego. ** Niskocząsteczkowa heparyna może nie wpływać na wydłużenie APTT bd brak danych 66
3 W przypadku oznaczeń czynnika von Willebranda, czynnika VIII i badań funkcji płytek u kobiet zaleca się pobieranie krwi w okresie miesiączki lub we wczesnej fazie folikularnej [20]. POBIERANIE MATERIAŁU DO BADAŃ Sposób pobrania materiału Zaleca się pobieranie krwi w pozycji siedzącej. W celu unikania problemów z hemolizą wywołaną przez alkohol, skórę po dezynfekcji należy dokładnie osuszyć. Do pobierania krwi należy używać igły o możliwie dużej średnicy (nie więcej niż 19G), dostosowując jej rozmiar do objętości pobieranej krwi. Dla dorosłych minimalna średnica igły wynosi 21G, dla dzieci minimum to rozmiar 23G [1]. Krew należy pobierać z dużych naczyń żylnych, przede wszystkim z żyły łokciowej przy zastosowaniu minimalnego ucisku stazy, bezpośrednio do probówek z antykoagulantem [8]. W wyjątkowych przypadkach możliwe jest wykorzystywanie do badań koagulologicznych krwi tętniczej, jednak w tym przypadku konieczna jest walidacja metody. W przypadku badań PT probówka koagulologiczna może być pobierana w pierwszej kolejności (nie ma potrzeby odrzucania pierwszej porcji krwi) [21]. Jeżeli krew musi być pobrana ze stałego dojścia (brak możliwości uzyskania krwi w zalecany sposób), konieczne jest odciągnięcie ok. 5 ml krwi [7]. W pozostałych przypadkach krew do badań koagulologicznych powinna być pobierana jako druga probówka, chociaż z powodu braku badań porównawczych nie jest to wymaganie obligatoryjne. Po pobraniu, krew należy niezwłocznie wymieszać. Wystarczające jest 5-6 krotne, łagodne odwrócenie probówki o 180. Probówek nie wolno wytrząsać [22, 23]. Pojemnik na próbkę materiał, antykoagulant Zgodnie z aktualnymi przepisami obowiązują zamknięte systemy to pobierania krwi. Probówki stosowane do badań koagulologicznych są wykonane z tworzywa sztucznego (polipropylen), nie aktywującego układu hemostazy. Zaleca się stosowanie probówek specjalnie przeznaczonych do badań koagulologicznych (producent powinien dostarczyć stosowną informację). Należy stosować wodny roztwór cytrynianu sodu o stężeniu od 105 do 109 mmol/l (3,13% do 3,2%). Dopuszcza się stosowanie zarówno buforowanego jak i niebuforowanego roztworu cytrynianu. Krew do antykagulantu pobiera się w stosunku 9:1. Stosowany może być również 3,2% buforowany cytrynian w mieszaninie z teofiliną, adenozyną i dipirydamolem (CTAD), co stabilizuje płytki i blokuje reakcję uwalniania płytkowego. Dopuszcza się probówki zawierające 129 mm cytrynian sodowy (3,8%) w badaniach funkcji płytek krwi w analizatorze PFA-100/200. Dla osób z hematokrytem >55% należy przygotowywać indywidualne probówki, stosując odpowiedni wzór do obliczania właściwej objętości cytrynianu (C) [18, 22, 23]: C = objętość krwi x (1,85 x 10 3 ) x (100 Ht) przy czym: C objętość cytrynianu, Ht - hematokryt Makroskopowa ocena jakości dostarczonego materiału Ze względu na zasadniczy wpływ pobrania krwi na wyniki badań koagulologicznych, wskazana jest ocena jakości próbki. Przed odwirowaniem krwi należy sprawdzić, czy w probówce znajduje się właściwa objętość krwi (niedopełnienie lub przepełnienie) oraz powoli obracając probówkę wykluczyć obecność skrzepu na ścianie probówki. W przypadku probówek próżniowych, próbka powinna zostać odrzucona, jeżeli zawiera <90% oczekiwanej objętości [24]. Typowy obraz koagulogramu wykonany w częściowo wykrzepionej krwi to: małopłytkowość, skrócone czasy - protrombinowy i APTT oraz podwyższone stężenie dimeru D (wartości mogą wielokrotnie przekraczać zakres referencyjny). Ocenie powinno być także poddane osocze. Próbki z hemolizą oraz niejednorodne (obecność strątów, lipemia) nie nadają się do badań. W niedalekiej przyszłości, dzięki zastosowaniu analizatorów automatycznie oceniających obecność hemolizy czy lipemii, ocena makroskopowa osocza nie będzie już konieczna [4]. OPRACOWANIE MATERIAŁU Badania przeprowadzane są w osoczu po odwirowaniu krwi w określonych warunkach. Wirowanie Czas wirowania zalecany 15 min (niektórzy autorzy dopuszczają czas 5-10 min dla podstawowych testów hemostazy) [24]. Siła odśrodkowa [g] 1500 (wyższa - może aktywować płytki oraz powodować hemolizę) Temperatura wirowania - pokojowa. Wskazane jest wirowanie jednokrotne w w/w warunkach, a w sytuacjach szczególnych (np. diagnostyka zespołu antyfosfolipidowego) - dwukrotne. W tym przypadku drugie wirowanie powinno odbywać się przez 10 min, przy sile odśrodkowej >2500 g. Obecnie nie zaleca się stosowania osocza filtrowanego [24]. Proponowane są różne parametry wirowania, ale większość autorów jest zgodna, że końcowym efektem wirowania jest uzyskanie osocza, w którym nie może być więcej płytek niż 10 x 10 9 /l. Warto o tym pamiętać decydując się na stosowanie hamowania w wirówce, ponieważ hamowanie wiąże się ze zwiększeniem liczby płytek w osoczu [25]. W związku z powyższym zaleca się sprawdzanie parametrów wirowania przed dopuszczeniem wirówki do pracy w laboratorium. Z doświadczenia autorów wynika, że wystarczy oznaczyć liczbę płytek krwi po odwirowaniu krwi w trzech próbkach pochodzących od pacjentów typowych dla danego laboratorium i trzech - od zdrowych dawców. Podobną procedurę należy wykonać dla próbek przeznaczonych do diagnostyki zespołu antyfosfolipidowego. W tym przypadku liczba płytek nie powinna przekraczać wartości tła w analizatorze (1-2 x 10 9 /l), a za wartość dopuszczającą do analizy uznaje się liczbę płytek <7 x 10 9 /l [26]. 67
4 PRZECHOWYWANIE MATERIAŁU 1. Zalecenia ogólne Krew należy przechowywać w temp. pokojowej, zawsze w zamkniętych probówkach (bez odwirowania lub po odwirowaniu). Stabilność oznaczanego parametru określana jest dla materiału pozostającego w spoczynku. Przewożenie nieodwirowanej krwi powinno się odbywać zgodnie z obowiązującymi normami prawnymi w specjalnie do tego przeznaczonych izotermicznych pojemnikach, w statywach, w pozycji pionowej. Zgodnie z najnowszymi doniesieniami w piśmiennictwie, dotyczącymi próbek pochodzących od osób zdrowych, przechowywanie krwi do 24 godzin w temperaturze pokojowej lub 4 C nie wpływa na wyniki oznaczeń PT, TT, DD i fibrynogenu [14], natomiast krew na oznaczenia APTT nie może być przechowywana dłużej niż 8 godzin [13]. Dlatego bezpieczniej będzie uznać, że krew po odwirowaniu powinna być przechowywana w temperaturze pokojowej w szczelnie zamkniętych probówkach nie dłużej niż 6 godzin dla krwi pobranej od pacjentów pozostających na leczeniu antagonistami witaminy K [15] oraz nie dłużej niż 4 godziny dla krwi pobranej od pacjentów leczonych niefrakcjonowaną heparyną. Informacja ta jest kluczowa dla postępowania przedanalitycznego, gdyż w tym przypadku krew musi być odwirowana w ciągu godziny od pobrania [22, 23]. W czasie przechowywania krwi z płytek krwi uwalnia się czynnik antyheparynowy (PF4), który wiążąc heparynę uniemożliwia rzetelną ocenę jej działania za pomocą APTT w próbkach krwi, które nie zostały odwirowane w ciągu godziny. Nie ma konieczności zlewania i oddzielnego przechowywania osocza. Przechowywanie zamrożonych próbek osocza jest dopuszczalne, ale nie zalecane. Dopuszczalny czas przechowywania zamrożonego materiału jest uzależniony od temperatury (tab. III). 2. Zalecenia szczegółowe W przypadku przechowywania materiału do oznaczeń stężenia dimeru D zastosowanie ma podstawowe zalecenie, czyli 4 godziny przechowywania w temperaturze pokojowej z możliwością wydłużenia tego czasu do 24 godzin w warunkach chłodniczych [27]. Ponieważ aktywność (stężenie) przeciwciał oznacza się zarówno w surowicy jak i osoczu, to dla uproszczenia laboratoryjnej procedury można przyjąć, że wszystkie oznaczenia wykonywane są w osoczu i związku z tym ustalić jednolity czas przechowywania materiału do badań koagulologicznych (tab. III). Najnowsze badania wykazały, że w diagnostyce HIT wyniki badań uzyskanych z osocza nie różniły się od wykonanych z surowicy [28]. Badania czynności płytek krwi są wykonywane sporadycznie, ale warto wiedzieć, że przechowywana może być pełna krew pobrana na cytrynian, nie dłużej niż 4 godziny i jedynie w temperaturze pokojowej (tab. III) [4]. Do badań genetycznych krew pełna pobierana jest wg zaleceń pracowni specjalistycznej. Standardowo wykorzystywane są probówki do badań morfologicznych z wersenianem potasu. Pełną krew można przechowywać wiele dni (np. tydzień) w temperaturze pokojowej lub dłużej (brak szczegółowych danych) w warunkach chłodniczych. Na ogół pełna krew jest zamrażana, a jej przydatność do oznaczeń diagnostycznych została potwierdzona przy przechowywaniu do ponad dwóch lat (-70 C) [1]. TRANSPORT 1. Zalecenia ogólne Transport materiału powinien się dostosowany do omówionych powyżej warunków przechowywania. Przewożenie nieodwirowanej krwi powinno się odbywać zgodnie z obowiązującymi normami prawnymi w specjalnie do tego przeznaczonych izotermicznych pojemnikach, w statywach w pozycji pionowej. Próbki mrożonego osocza należy przewozić w pojemnikach z suchym lodem. Zgodnie z obowiązującymi przepisami przewożenie materiału do badań laboratoryjnych możliwe jest przez firmy posiadające stosowny certyfikat. Konieczne jest udokumentowane potwierdzenie czasu trwania transportu i temperatury w pojemniku do przewożenia próbek (dotyczy zarówno krwi jak i mrożonego osocza). Rozmrażanie należy przeprowadzać szybko (5-10 min) w 37 C. Po rozmrożeniu należy próbkę delikatnie wymieszać i sprawdzić występowanie precypitatów. W przypadkach wątpliwych można oznaczyć fibrynogen, którego stężenie nie powinno różnić się o więcej niż 20 % od wyniku uzyskanego Tabela III. Przechowywanie materiału do badań koagulologicznych podsumowanie Badanie pełna krew [godziny] *nie mniej niż ** osocze super-ubogopłytkowe (podwójne wirowanie) bd brak wiarygodnych danych materiał po odwirowaniu [godziny] osocze (-20 C)* [tygodnie] osocze (-70 C)* [miesiące] PT 6 6 bd bd APTT 1 4 bd bd HIT lub APS** (osocze) Inne (osocze) dimer D 4 (25 C), 12 (4 C) 4 (25 C), 24 (4 C)
5 przed zamrożeniem. Oznaczenie należy wykonać w ciągu 2 godzin. Próbki niejednorodne nie nadają się do badań. 2. Zalecenia szczegółowe Najwięcej problemów przysparza wysyłanie materiału w celu wykonania badań czynności płytek krwi. Należy zapewnić stałą temperaturę zbliżoną do pokojowej (pojemniki izotermiczne). Badania tego typu są wykonywane rzadko, stąd rzeczywistym problemem jest transport zamrożonych próbek osocza, do którego konieczny jest suchy lód. Transportem zmrożonego materiału powinny się zajmować uprawnione do tego firmy. W przypadku transportu krwi, nie ma aż takich rygorów, należy unikać wstrząsania próbką, gdyż prowadzi to do aktywacji płytek krwi. Nie ma problemu z przesyłaniem materiału do badań genetycznych, a pozostałe oznaczenia mają ujednolicone wymagania, zgodne z czasem przechowywania materiału (tab. III). OPIS SKIEROWANIA Zalecenia zamieszczone w Zarządzeniu Ministra Zdrowia [17] są w zupełności wystarczające. Warto jednak przypomnieć, że bez wpisanej godziny pobrania (z dokładnością do 5 minut) oraz bez podania danych klinicznych mających wpływ na postępowanie przedanalityczne, materiał nie może być przyjęty do laboratorium. Powszechnie wiadomo, że wymagany w Zarządzeniu Ministra Zdrowia opis kliniczny jest powszechnie ignorowany przez jednostki zlecające wykonanie badania. Skierowanie na badania koagulologiczne musi zawierać następujące informacje kliniczne o pacjencie: rodzaj zaburzeń hemostazy (podejrzenie), zastosowane leki wpływające na wyniki oznaczeń, sposób pobrania krwi (bezpośrednie wkłucie, pobranie ze stałego dojścia) Bez wyżej wymienionych danych nie jest możliwe zapewnienie jakości fazy przedanalitycznej. PODSUMOWANIE Zalecenia uzgodnione w czasie prac Sekcji Laboratoryjnej Diagnostyki Hemostazy Polskiego Towarzystwa Diagnostyki Laboratoryjnej opierają się zasadniczo na rozporządzeniu Ministra z dnia 21 stycznia 2009 r. zmieniające rozporządzenie w sprawie standardów jakości dla medycznych laboratoriów diagnostycznych i mikrobiologicznych [17], na dokumencie H21-A5 Clinical and Laboratory Standards Institute [1] oraz na wytycznych Brytyjskiego Komitetu ds. Standaryzacji w Hematologii (BCSH; British Committee for Standards in Haematology) [23]. Przedstawiony w pracy opis postępowania przedanalitycznego jest koniecznym kompromisem pomiędzy informacjami dostępnymi w polskim i anglojęzycznym piśmiennictwie [2, 3, 13-15, 23, 29, 30] a także z wytycznymi CLSI [1, 31] i BCSH [23]. Najtrudniej jest wskazać czas przechowywania materiału do oznaczania czasu protrombinowego. Uznano, że w polskich warunkach bardziej właściwe będzie przyjęcie 6 godzin jako maksymalnego czasu przechowywania materiału [15]. Kompromis jest konieczny ponieważ, z jednej strony wytyczne CLSI i cześć autorów [1, 13, 14] dopuszczają 24 godzinne przechowywanie materiału, a z drugiej, praktyczne przewodniki dla pracowników laboratoriów, zalecają przechowywanie materiału nie dłużej niż 4 godziny [13, 14, 18, 23]. Skąd tak wielkie rozbieżności w zaleceniach? W materiale uzyskanym od zdrowych osób lub pacjentów nie leczonych przeciwzakrzepowo stabilność parametrów jest znacznie wyższa niż w grupie przyjmującej leki przeciwkrzepliwe. Dodatkowo należy pamiętać, że standardowo dopuszczalna jest zmiana wartości PT w czasie przechowywania, sięgająca do 10%. Sugerowane w niniejszej publikacji 6 godzin przechowywania materiału przeznaczonego do oznaczeń PT jest uzasadnione wynikami wcześniejszych badań [15] oraz ułatwi transport krwi z punktów pobrań do centralnego laboratorium. Z kolei, zaproponowany 4 godzinny czas przechowywania materiału w odniesieniu pozostałych badań (w tym oznaczenia liczby i oceny czynności płytek krwi) jest zgodny z dokumentem CLSI [1] i wytycznymi BCSH [23]. Kolejnym odstępstwem od danych dostępnych w piśmiennictwie jest długi czas przechowywania krwi, dotyczący oznaczenia stężenia dimeru D (12 godzin w temp. 4 C), a także surowicy do oznaczeń przeciwciał (8 godzin). W przypadku dimeru D wytyczne CLSI zezwalają na przechowywanie materiału nawet powyżej 24 godzin [31]. Uwzględniając jednak specyfikę oznaczeń tego parametru (np. postępująca w czasie proteoliza) oraz na podstawie dostępnych publikacji [27] uznano za zasadne przyjęcie dopuszczalnego czasu przechowywania: dla temp. pokojowej - 4 godziny, a dla temperatury 2-5 C - 12 godzin. W celu łatwego zapamiętania powyższych zaleceń, można zaproponować wprowadzenie schematu 4 (większość oznaczeń) 6 (PT) 12 (DD; 2-5 C) jako prostej formuły opracowywania materiału do badań koagulologicznych. Druga cześć formuły dotyczy przechowywania materiału w stanie zamrożenia. Mrożenie osocza związane jest z ryzykiem wydłużenia czasów przy oznaczaniu PT i APTT [32]. Dlatego zaleca się wykonywanie oznaczeń ze świeżego materiału, a w sytuacji braku możliwości wykonania oznaczeń w czasie opisanym w pierwszej formule, dopuszcza się w wyjątkowych przypadkach mrożenie materiału według schematu: 2 tygodnie (-20 C) 12 miesięcy (<-70 C). Cześć autorów dopuszcza przechowywanie materiału w głębokim zamrożeniu nawet przez 3 lata [33], ale w codziennej praktyce laboratoryjnej powinno wystarczyć 12 miesięcy. Przyjęcie wysokich wymagań daje większą szansę zapewnienia jakości, a ich liberalizacja będzie możliwa po wprowadzeniu pełnej kontroli i nadzoru specjalistycznego nad laboratoryjną diagnostyką hemostazy. Otwarta pozostaje kwestia trybu i zmiany wytycznych na mniej rygorystyczne. 69
6 Uważamy, że po ukazaniu się nowego dokumentu CLSI oraz zebraniu opinii diagnostów laboratoryjnych i klinicystów zostanie opracowana kolejna wersja wytycznych. Piśmiennictwo 1. Adcock DM. Collection, Transport, and Processing of Blood Specimens for Testing Plasma-Based Coagulation Assays and Molecular Hemostasis Assays; Approved Guideline - Fifth Edition. CLSI document H21-A5. Clinical and Laboratory Standards Institute 2008; 28(5). 2. Adcock DM. Sample integrity and preanalytical variables, Quality in laboratory hemostasis and thrombosis. Edited by Kitchen S, Olson JD, Preston FE. Oxford, Wiley-Blackwell, Bennett ST. Collection of coagulation specimens, Laboratory hemostasis. A practical guide for pathologists. Edited by Bennett ST, Lehman CM, Rodgers GM. New York, Springer Science+Business Media, LLC, Lippi G, Becan-McBride K, Behulova D, et al. Preanalytical quality improvement: in quality we trust. Clin Chem Lab Med 2013; 51(1): Lippi G, Salvagno GL, Montagnana M, et al. Influence of two different buffered sodium citrate concentrations on coagulation testing. Blood Coagul Fibrinolysis 2005; 16(5): Bowen RA, Hortin GL, Csako G, et al. Impact of blood collection devices on clinical chemistry assays. Clin Biochem 2010; 43(1-2): Favaloro EJ, Lippi G, Raijmakers MT, et al. Discard tubes are sometimes necessary when drawing samples for hemostasis Am J Clin Pathol. 2010; 134(5): Lima-Oliveira G, Salvagno GL, Lippi G, et al. Elimination of the venous stasis error for routine coagulation testing by transillumination Clin Chim Acta. 2011; 412(15-16): Lippi G, Salvagno GL, Montagnana M, et al. Short-term venous stasis influences routine coagulation testing. Blood Coagul Fibrinolysis 2005; 16(6): Lippi G, Salvagno GL, Montagnana M, et al. Influence of the needle bore size on platelet count and routine coagulation testing. Blood Coagul Fibrinolysis 2006; 17(7): Salvagno GL, Lippi G, Montagnana M, et al. Influence of temperature and time before centrifugation of specimens for routine coagulation testing. Int J Lab Hematol 2009; 31(4): Zurcher M, Sulzer I, Barizzi G, et al. Stability of coagulation assays performed in plasma from citrated whole blood transported at ambient temperature. Thromb Haemost 2008; 99(2): Zhao Y, Lv G. Influence of temperature and storage duration on measurement of activated partial thromboplastin time, D-dimers, fibrinogen, prothrombin time and thrombin time, in citrateanticoagulated whole blood specimens. Int J Lab Hematol 2013; 35(5): Feng L, Zhao Y, Zhao H, et al. Effects of storage time and temperature on coagulation tests and factors in fresh plasma. Sci Rep 2014; 4:3868. doi: /srep Van Geest-Daalderop JH, Mulder AB, Boonman-de Winter LJ, et al. Preanalytical variables and off-site blood collection: influences on the results of the prothrombin time/international normalized ratio test and implications for monitoring of oral anticoagulant therapy. Clin Chem 2005; 51(3): Christensen TD, Jensen C, Larsen TB, et al. International Normalized Ratio (INR), coagulation factor activities and calibrated automated thrombin generation - influence of 24 h storage at ambient temperature. Int J Lab Hematol 2010; 32(2): Rozporządzenie Ministra Zdrowia z dnia 21 stycznia 2009 r. zmieniające rozporządzenie w sprawie standardów jakości dla medycznych laboratoriów diagnostycznych i mikrobiologicznych. Dz.U nr 22 poz Lippi G, Salvagno GL, Montagnana M, et al. Quality standards for sample collection in coagulation testing. Semin Thromb Hemost 2012; 38(6): Tripodi A. D-dimer testing in laboratory practice. Clin Chem 2011; 57(9): Knol HM, Kemperman RF, Kluin-Nelemans HC, et al. Haemostatic variables during normal menstrual cycle. A systematic review. Thromb Haemost 2012; 107(1): Smock KJ, Crist RA, Hansen SJ, et al. Discard tubes are not necessary when drawing samples for specialized coagulation testing. Blood Coagul Fibrinolysis 2010; 21(3): Adcock Funk DM, Lippi G, Favaloro EJ. Quality standards for sample processing, transportation, and storage in hemostasis testing. Semin Thromb Hemost 2012; 38(6): Mackie I, Cooper P, Lawrie A, et al. Guidelines on the laboratory aspects of assays used in haemostasis and thrombosis. Int J Lab Hematol 2012; 35(1): Preston FE, Lippi G, Favaloro EJ, et al. Quality issues in laboratory haemostasis. Haemophilia 2010; 16 Suppl 5: Daves M, Giacomuzzi K, Tagnin E, et al. Influence of centrifuge brake on residual platelet count and routine coagulation tests in citrated plasma. Blood Coagul Fibrinolysis 2014; 25: DOI: /MBC Ortel TL. Laboratory diagnosis of the lupus anticoagulant. Curr Rheumatol Rep 2012; 14(1): Bohm-Weigert M, Wissel T, Muth H, et al. Long- and short-term in vitro D-dimer stability measured with INNOVANCE D-Dimer. Thromb Haemost 2010; 103(2): Kolde HJ, Habrecht U, von HJ, et al. Multicentric validation of a rapid assay for heparin-induced thrombocytopenia with different specimen types. Blood Coagul Fibrinolysis 2014; 25(1): Raszeja-Specht A. Zapewnienie jakości w laboratorium koagulologicznym, w: Diagnostyka laboratoryjna w hemostazie. Jastrzebska M. (red.), Oinpharma, Warszawa 2009; Raszeja-Specht A. Metody badań układu hemostazy, w: Diagnostyka laboratoryjna w hemostazie. Jastrzebska M. (red.), Oinpharma,Warszawa 2009: Olson JD. Quantitative D-dimer for the Exclusion of Venous Thromboembolic Disease; Proposed Guideline, CLSI document H59-A. Clinical and Laboratory Standards Institute 2011; 31(6). 32. Alesci S, Borggrefe M, Dempfle CE. Effect of freezing method and storage at -20 degrees C and -70 degrees C on prothrombin time, aptt and plasma fibrinogen levels. Thromb Res 2009; 124(1): Van Den Besselaar AM, Witteveen E, van der Meer FJ. Longterm stability of frozen pooled plasmas stored at -70 degrees C, -40 degrees C, and -20 degrees C for prothrombin time and International Normalized Ratio (INR) assessment. Thromb Res 2013; 131(4):
KOAGULOLOGIA. Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice.
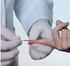 KOAGULOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
KOAGULOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
ZAKŁAD DIAGNOSTYKI LABORATORYJNEJ I IMMUNOLOGII KLINICZNEJ WIEKU ROZOJOWEGO AM W WARSZAWIE.
 ZAKŁAD DIAGNOSTYKI LABORATORYJNEJ I IMMUNOLOGII KLINICZNEJ WIEKU ROZOJOWEGO AKADEMII MEDYCZNEJ W WARSZAWIE. ZAKŁAD DIAGNOSTYKI LABORATOTORYJNEJ WYDZIAŁU NAUKI O ZDROWIU AKADEMII MEDYCZNEJ W WARSZAWIE Przykładowe
ZAKŁAD DIAGNOSTYKI LABORATORYJNEJ I IMMUNOLOGII KLINICZNEJ WIEKU ROZOJOWEGO AKADEMII MEDYCZNEJ W WARSZAWIE. ZAKŁAD DIAGNOSTYKI LABORATOTORYJNEJ WYDZIAŁU NAUKI O ZDROWIU AKADEMII MEDYCZNEJ W WARSZAWIE Przykładowe
Diagnostyka różnicowa przedłużonego APTT
 Maria Podolak-Dawidziak Diagnostyka różnicowa przedłużonego APTT Katedra i Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku AM, Wrocław Czas częściowej tromboplastyny po aktywacji APTT czas
Maria Podolak-Dawidziak Diagnostyka różnicowa przedłużonego APTT Katedra i Klinika Hematologii, Nowotworów Krwi i Transplantacji Szpiku AM, Wrocław Czas częściowej tromboplastyny po aktywacji APTT czas
Tab.1. Charakterystyka materiału do badań w Pracowni Hemostazy LDH
 LABORATORIUM DIAGNOSTYKI HEMATOLOGICZNEJ Pracownia Hemostazy ul. Szamarzewskiego 82/84, 60-569 Poznań tel. 61 854 9576, 61854 9599 Kierownik: dr hab. n. med. Maria Kozłowska-Skrzypczak prof. UM Tab.1.
LABORATORIUM DIAGNOSTYKI HEMATOLOGICZNEJ Pracownia Hemostazy ul. Szamarzewskiego 82/84, 60-569 Poznań tel. 61 854 9576, 61854 9599 Kierownik: dr hab. n. med. Maria Kozłowska-Skrzypczak prof. UM Tab.1.
Stan badań laboratoryjnych układu hemostazy wśród laboratoriów uczestniczących w programie zewnętrznej oceny jakości PPZOJMED
 diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2009 Volume 45 Number 3 203-208 Kontrola jakości Quality control Stan badań laboratoryjnych układu hemostazy wśród laboratoriów uczestniczących
diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2009 Volume 45 Number 3 203-208 Kontrola jakości Quality control Stan badań laboratoryjnych układu hemostazy wśród laboratoriów uczestniczących
Żylna choroba zakrzepowo-zatorowa w świetle nowych badań
 Krystyna Zawilska Żylna choroba zakrzepowo-zatorowa w świetle nowych badań U jakich pacjentów warto diagnozować wrodzoną trombofilię? Trombofilią nazywamy wrodzone lub nabyte zaburzenia mechanizmu hemostazy
Krystyna Zawilska Żylna choroba zakrzepowo-zatorowa w świetle nowych badań U jakich pacjentów warto diagnozować wrodzoną trombofilię? Trombofilią nazywamy wrodzone lub nabyte zaburzenia mechanizmu hemostazy
Faza przedanalityczna w hematologii (cz. II)
 Faza przedanalityczna w hematologii (cz. II) Prawidłowe pobranie próbki krwi odgrywa ważną rolę w procesie przedanalitycznym. W części pierwszej opracowania Faza przedanalityczna w hamatologii znajdują
Faza przedanalityczna w hematologii (cz. II) Prawidłowe pobranie próbki krwi odgrywa ważną rolę w procesie przedanalitycznym. W części pierwszej opracowania Faza przedanalityczna w hamatologii znajdują
PRACOWNIA HEMOSTAZY COZL
 dr n.med. Jarosław Kuna MLD COZL 2017 PRACOWNIA HEMOSTAZY COZL czas PT,APTT,TT Fibrynogen (met. Claussa) czas korekcji APTT D-Dimer PRACOWNIA HEMOSTAZY COZL wykrywanie zaburzeń czynnościowych płytek krwi
dr n.med. Jarosław Kuna MLD COZL 2017 PRACOWNIA HEMOSTAZY COZL czas PT,APTT,TT Fibrynogen (met. Claussa) czas korekcji APTT D-Dimer PRACOWNIA HEMOSTAZY COZL wykrywanie zaburzeń czynnościowych płytek krwi
TROMBOELASTOMETRIA W OIT
 TROMBOELASTOMETRIA W OIT Dr n. med. Dominika Jakubczyk Katedra i Klinika Anestezjologii Intensywnej Terapii Tromboelastografia/tromboelastometria 1948 - Helmut Hartert, twórca techniki tromboelastografii
TROMBOELASTOMETRIA W OIT Dr n. med. Dominika Jakubczyk Katedra i Klinika Anestezjologii Intensywnej Terapii Tromboelastografia/tromboelastometria 1948 - Helmut Hartert, twórca techniki tromboelastografii
u Czynniki ryzyka wystąpienia zakrzepicy? - przykłady cech osobniczych i stanów klinicznych - przykłady interwencji diagnostycznych i leczniczych
 1 TROMBOFILIA 2 Trombofilia = nadkrzepliwość u Genetycznie uwarunkowana lub nabyta skłonność do występowania zakrzepicy żylnej, rzadko tętniczej, spowodowana nieprawidłowościami hematologicznymi 3 4 5
1 TROMBOFILIA 2 Trombofilia = nadkrzepliwość u Genetycznie uwarunkowana lub nabyta skłonność do występowania zakrzepicy żylnej, rzadko tętniczej, spowodowana nieprawidłowościami hematologicznymi 3 4 5
Postępowanie z chorym przed i po implantacji leczonym doustnymi lekami p-zakrzepowymi
 Postępowanie z chorym przed i po implantacji leczonym doustnymi lekami p-zakrzepowymi Dr hab.n.med.barbara Małecka Krakowski Szpital Specjalistyczny im.jana Pawła II 1 1. Leczenie przeciwzakrzepowe wiąże
Postępowanie z chorym przed i po implantacji leczonym doustnymi lekami p-zakrzepowymi Dr hab.n.med.barbara Małecka Krakowski Szpital Specjalistyczny im.jana Pawła II 1 1. Leczenie przeciwzakrzepowe wiąże
Nowe doustne antykoagulanty. okiem diagnosty laboratoryjnego.
 Nowe doustne antykoagulanty okiem diagnosty laboratoryjnego. Paweł Kozłowski Laboratorium Centralne Samodzielny Publiczny Centralny Szpital Kliniczny Zakład Diagnostyki Laboratoryjnej Warszawski Uniwersytet
Nowe doustne antykoagulanty okiem diagnosty laboratoryjnego. Paweł Kozłowski Laboratorium Centralne Samodzielny Publiczny Centralny Szpital Kliniczny Zakład Diagnostyki Laboratoryjnej Warszawski Uniwersytet
Stany nadkrzepliwości (trombofilie)
 Stany nadkrzepliwości (trombofilie) DEFINICJA I ETIOPATOGENEZA Genetycznie uwarunkowana lub nabyta skłonność do zakrzepicy żylnej lub (rzadko) tętniczej, związana z nieprawidłowościami hematologicznymi.
Stany nadkrzepliwości (trombofilie) DEFINICJA I ETIOPATOGENEZA Genetycznie uwarunkowana lub nabyta skłonność do zakrzepicy żylnej lub (rzadko) tętniczej, związana z nieprawidłowościami hematologicznymi.
INSTYTUT HEMATOLOGII I TRANSFUZJOLOGII
 ZAKŁAD HEMOSTAZY I CHORÓB METABOLICZNYCH PRACOWNIA PORFIRII 00-957 Warszawa, ul. Chocimska 5 tel. 22 34 96 617/635 INSTRUKCJA POBIERANIA I TRANSPORTU MATERIAŁU DO BADAŃ LABORATORYJNYCH W KIERUNKU PORFIRII
ZAKŁAD HEMOSTAZY I CHORÓB METABOLICZNYCH PRACOWNIA PORFIRII 00-957 Warszawa, ul. Chocimska 5 tel. 22 34 96 617/635 INSTRUKCJA POBIERANIA I TRANSPORTU MATERIAŁU DO BADAŃ LABORATORYJNYCH W KIERUNKU PORFIRII
Tytuł: Błędy przedlaboratoryjne
 Data obowiązywania: Wydanie: 1 Strona 1 z 5 Karta zmian Nr zmiany Punktu Podpunktu rozdziału Zmiany Akapitu lub fragmentu tekstu ze strony nr Opis zmiany Data zmiany Podpis autora zmiany ZATWIERDZIŁ Dyrektor
Data obowiązywania: Wydanie: 1 Strona 1 z 5 Karta zmian Nr zmiany Punktu Podpunktu rozdziału Zmiany Akapitu lub fragmentu tekstu ze strony nr Opis zmiany Data zmiany Podpis autora zmiany ZATWIERDZIŁ Dyrektor
Ryzyko błędów w fazie przed-analitycznej
 Ryzyko błędów w fazie przed-analitycznej Jan Kanty Kulpa Zakład Analityki i Biochemii Klinicznej Centrum Onkologii Instytut im. M. Skłodowskiej_ Curie Oddział w Krakowie Rozwój: biologii molekularnej biochemii
Ryzyko błędów w fazie przed-analitycznej Jan Kanty Kulpa Zakład Analityki i Biochemii Klinicznej Centrum Onkologii Instytut im. M. Skłodowskiej_ Curie Oddział w Krakowie Rozwój: biologii molekularnej biochemii
Doustne środki antykoncepcyjne a ryzyko wystąpienia zakrzepicy. Dr hab. Jacek Golański Zakład Zaburzeń Krzepnięcia Krwi Uniwersytet Medyczny w Łodzi
 Doustne środki antykoncepcyjne a ryzyko wystąpienia zakrzepicy Dr hab. Jacek Golański Zakład Zaburzeń Krzepnięcia Krwi Uniwersytet Medyczny w Łodzi Żylna choroba zakrzepowozatorowa (ŻChZZ) stanowi ważny
Doustne środki antykoncepcyjne a ryzyko wystąpienia zakrzepicy Dr hab. Jacek Golański Zakład Zaburzeń Krzepnięcia Krwi Uniwersytet Medyczny w Łodzi Żylna choroba zakrzepowozatorowa (ŻChZZ) stanowi ważny
KREW II ZABURZENIA HEMOSTAZY
 KREW II ZABURZENIA HEMOSTAZY HEMOSTAZA DEFINICJA Całość procesów związanych z utrzymaniem krwi w stanie płynnym w obrębie łożyska naczyniowego 1 HEMOSTAZA ZAŁOŻENIA Mechanizmy hemostazy są aktywowane Jedynie
KREW II ZABURZENIA HEMOSTAZY HEMOSTAZA DEFINICJA Całość procesów związanych z utrzymaniem krwi w stanie płynnym w obrębie łożyska naczyniowego 1 HEMOSTAZA ZAŁOŻENIA Mechanizmy hemostazy są aktywowane Jedynie
Czy istnieją nowe i stare glukometry? Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet Jagielloński Collegium Medicum Kraków
 Czy istnieją nowe i stare glukometry? Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet Jagielloński Collegium Medicum Kraków Glukometry nowe stare lepsze gorsze Glukometry mają ok. 45 lat Nowe glukometry
Czy istnieją nowe i stare glukometry? Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet Jagielloński Collegium Medicum Kraków Glukometry nowe stare lepsze gorsze Glukometry mają ok. 45 lat Nowe glukometry
Akademia wiedzy Synevo
 Akademia wiedzy Synevo 1 Ciąża w chorobach układowych tkanki łącznej dr n. med. Magdalena Szmyrka mgr Lucyna Korman Wrocław, 7 czerwca 2018 r. Autoprzeciwciała istotne w ciąży mgr Lucyna Korman Katedra
Akademia wiedzy Synevo 1 Ciąża w chorobach układowych tkanki łącznej dr n. med. Magdalena Szmyrka mgr Lucyna Korman Wrocław, 7 czerwca 2018 r. Autoprzeciwciała istotne w ciąży mgr Lucyna Korman Katedra
Zaburzenia krzepnięcia diagnostyka w systemie przyłóżkowym
 Zaburzenia krzepnięcia diagnostyka w systemie przyłóżkowym Barbara Adamik Katedra i Klinika Anestezjologii i Intensywnej Terapii Uniwersytet Medyczny we Wrocławiu Zaburzenia krzepnięcia - diagnostyka w
Zaburzenia krzepnięcia diagnostyka w systemie przyłóżkowym Barbara Adamik Katedra i Klinika Anestezjologii i Intensywnej Terapii Uniwersytet Medyczny we Wrocławiu Zaburzenia krzepnięcia - diagnostyka w
1.2. Zlecenie może być wystawione w formie elektronicznej z zachowaniem wymagań, o których mowa w poz. 1.1.
 Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
Załączniki do rozporządzenia Ministra Zdrowia z dnia 2005 r. (poz. ) Załącznik Nr 1 Podstawowe standardy jakości w czynnościach laboratoryjnej diagnostyki medycznej, ocenie ich jakości i wartości diagnostycznej
Błędy przedanalityczne
 Błędy przedanalityczne Każdy z etapów badania począwszy od momentu zlecenia testu przez lekarza, poprzez pobranie krwi, analizę próbki, aż po interpretację wyniku na poziomie decyzyjnym, wiąże się z możliwością
Błędy przedanalityczne Każdy z etapów badania począwszy od momentu zlecenia testu przez lekarza, poprzez pobranie krwi, analizę próbki, aż po interpretację wyniku na poziomie decyzyjnym, wiąże się z możliwością
octaplex Zastosuj to, co niezbędne d szybkie i skuteczne działanie o dużym stopniu tolerancji
 octaplex Zastosuj to, co niezbędne d szybkie i skuteczne działanie o dużym stopniu tolerancji PCC w terapii i profilaktyce niedoborów kompleksu protrombiny octaplex F II (protrombina) FVII FIX FX Białko
octaplex Zastosuj to, co niezbędne d szybkie i skuteczne działanie o dużym stopniu tolerancji PCC w terapii i profilaktyce niedoborów kompleksu protrombiny octaplex F II (protrombina) FVII FIX FX Białko
Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu
 Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu PROGRAM WHO ELIMINACJI ODRY/RÓŻYCZKI Program eliminacji odry i różyczki został uchwalony przez Światowe Zgromadzenie Zdrowia 28 maja 2003 roku. Realizacja
Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu PROGRAM WHO ELIMINACJI ODRY/RÓŻYCZKI Program eliminacji odry i różyczki został uchwalony przez Światowe Zgromadzenie Zdrowia 28 maja 2003 roku. Realizacja
Zaburzenia układu hemostazy i ich znaczenie w chirurgii. Propedeutyka chirurgii Seminarium dla studentów III roku kierunku lekarskiego
 Zaburzenia układu hemostazy i ich znaczenie w chirurgii Propedeutyka chirurgii Seminarium dla studentów III roku kierunku lekarskiego dr n. med. Paweł Świercz Katedra i Klinika Chirurgii Ogólnej, Naczyniowej
Zaburzenia układu hemostazy i ich znaczenie w chirurgii Propedeutyka chirurgii Seminarium dla studentów III roku kierunku lekarskiego dr n. med. Paweł Świercz Katedra i Klinika Chirurgii Ogólnej, Naczyniowej
HEMATOLOGIA. Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice.
 HEMATOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi. Zdezynfekować
HEMATOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi. Zdezynfekować
BIOCHEMIA. Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice.
 BIOCHEMIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi. Zdezynfekować
BIOCHEMIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi. Zdezynfekować
PDF created with pdffactory Pro trial version www.pdffactory.com
 Procedura nr 195.101 Wersja nr 5 Strona 2/6 1. CEL PROCEDURY Procedura ma za zadanie ujednolicenie sposobu pobierania, przysyłania i przyjmowania próbek krwi wymagających opracowania w Pracowni Serologicznej
Procedura nr 195.101 Wersja nr 5 Strona 2/6 1. CEL PROCEDURY Procedura ma za zadanie ujednolicenie sposobu pobierania, przysyłania i przyjmowania próbek krwi wymagających opracowania w Pracowni Serologicznej
PATOFIZJOLOGIA ZABURZEŃ HEMOSTAZY. Jakub Klimkiewicz
 PATOFIZJOLOGIA ZABURZEŃ HEMOSTAZY Jakub Klimkiewicz HEMOSTAZA CAŁOŚĆ PROCESÓW ZWIĄZANYCH Z UTRZYMANIEM KRWI W STANIE PŁYNNYM W NACZYNIACH KRWIONOŚNYCH ORAZ HAMOWANIEM KRWAWIENIA W MIEJSCU USZKODZENIA ŚCIANY
PATOFIZJOLOGIA ZABURZEŃ HEMOSTAZY Jakub Klimkiewicz HEMOSTAZA CAŁOŚĆ PROCESÓW ZWIĄZANYCH Z UTRZYMANIEM KRWI W STANIE PŁYNNYM W NACZYNIACH KRWIONOŚNYCH ORAZ HAMOWANIEM KRWAWIENIA W MIEJSCU USZKODZENIA ŚCIANY
WYCIECZKA DO LABORATORIUM
 WYCIECZKA DO LABORATORIUM W ramach projektu e-szkoła udaliśmy się do laboratorium w Krotoszynie na ul. Bolewskiego Mieliśmy okazję przeprowadzić wywiad z kierowniczką laboratorium Panią Hanną Czubak Oprowadzała
WYCIECZKA DO LABORATORIUM W ramach projektu e-szkoła udaliśmy się do laboratorium w Krotoszynie na ul. Bolewskiego Mieliśmy okazję przeprowadzić wywiad z kierowniczką laboratorium Panią Hanną Czubak Oprowadzała
Czas w medycynie laboratoryjnej. Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet Jagielloński Collegium Medicum Kraków
 Czas w medycynie laboratoryjnej Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet Jagielloński Collegium Medicum Kraków Czas w medycynie laboratoryjnej w procesie diagnostycznym pojedynczego pacjenta...
Czas w medycynie laboratoryjnej Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet Jagielloński Collegium Medicum Kraków Czas w medycynie laboratoryjnej w procesie diagnostycznym pojedynczego pacjenta...
Wpływ płynoterapii na krzepnięcie/fibrynolizę
 Wpływ płynoterapii na krzepnięcie/fibrynolizę Piotr Czempik, Katedra i Oddział Anestezjologii i Intensywnej Terapii SUM Uniwersyteckie Centrum Kliniczne w Katowicach Śląska Izba Lekarska, 20.02.2017. 1
Wpływ płynoterapii na krzepnięcie/fibrynolizę Piotr Czempik, Katedra i Oddział Anestezjologii i Intensywnej Terapii SUM Uniwersyteckie Centrum Kliniczne w Katowicach Śląska Izba Lekarska, 20.02.2017. 1
Doustne antykoagulanty o działaniu bezpośrednim nowe wyzwanie dla diagnostyki laboratoryjnej
 diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab 2015; 51(3): 221-228 Praca poglądowa Review Article Doustne antykoagulanty o działaniu bezpośrednim nowe wyzwanie dla diagnostyki laboratoryjnej
diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab 2015; 51(3): 221-228 Praca poglądowa Review Article Doustne antykoagulanty o działaniu bezpośrednim nowe wyzwanie dla diagnostyki laboratoryjnej
DIETA W PRZEWLEKŁEJ CHOROBIE NEREK
 KURS 15.04.2016 Szczecinek DIETA W PRZEWLEKŁEJ CHOROBIE NEREK dr hab. n. med. Sylwia Małgorzewicz, prof.nadzw. Katedra Żywienia Klinicznego Klinika Nefrologii, Transplantologii i Chorób Wewnętrznych Gdański
KURS 15.04.2016 Szczecinek DIETA W PRZEWLEKŁEJ CHOROBIE NEREK dr hab. n. med. Sylwia Małgorzewicz, prof.nadzw. Katedra Żywienia Klinicznego Klinika Nefrologii, Transplantologii i Chorób Wewnętrznych Gdański
Rekomendacje dla medycznych laboratoriów w zakresie diagnostyki toksykologicznej
 Rekomendacje dla medycznych laboratoriów w zakresie diagnostyki toksykologicznej Ewa Gomółka 1, 2 1 Pracownia Informacji Toksykologicznej i Analiz Laboratoryjnych, Katedra Toksykologii i Chorób Środowiskowych,
Rekomendacje dla medycznych laboratoriów w zakresie diagnostyki toksykologicznej Ewa Gomółka 1, 2 1 Pracownia Informacji Toksykologicznej i Analiz Laboratoryjnych, Katedra Toksykologii i Chorób Środowiskowych,
Wskazania do diagnostyki w kierunku trombofilii
 Wskazania do diagnostyki w kierunku trombofilii dr n. med. Agnieszka Padjas II Katedra Chorób Wewnętrznych, Klinika Alergii i Immunologii Uniwersytet Jagielloński, Collegium Medicum Co to jest trombofilia?
Wskazania do diagnostyki w kierunku trombofilii dr n. med. Agnieszka Padjas II Katedra Chorób Wewnętrznych, Klinika Alergii i Immunologii Uniwersytet Jagielloński, Collegium Medicum Co to jest trombofilia?
Tytuł: Kontrola glukometrów
 Data obowiązywania: Wydanie: 1 Strona 1 z 6 Karta zmian 1. CEL: Nr Punktu Podpunktu rozdziału Zmiany Akapitu lub fragmentu tekstu ze strony nr Opis Data Podpis autora ZATWIERDZIŁ Dyrektor Szpitala Dr n.
Data obowiązywania: Wydanie: 1 Strona 1 z 6 Karta zmian 1. CEL: Nr Punktu Podpunktu rozdziału Zmiany Akapitu lub fragmentu tekstu ze strony nr Opis Data Podpis autora ZATWIERDZIŁ Dyrektor Szpitala Dr n.
Układ krzepnięcia a znieczulenia przewodowe
 Układ krzepnięcia a znieczulenia przewodowe We wszystkich obecnie dyscyplinach zabiegowych obowiązuje standard profilaktyki przeciwzakrzepowej z zastosowaniem heparyn (zwłaszcza drobnocząsteczkowych).
Układ krzepnięcia a znieczulenia przewodowe We wszystkich obecnie dyscyplinach zabiegowych obowiązuje standard profilaktyki przeciwzakrzepowej z zastosowaniem heparyn (zwłaszcza drobnocząsteczkowych).
Poniżej prezentuję treść własnego wystąpienia w ramach spotkania okrągłego stołu. Główne punkty wystąpienia:
 Kwalifikacja do leczenia osteoporozy i kosztoefektywność leczenia osteoporozy w Polsce, polska wersja FRAX konferencja okrągłego stołu podczas IV Środkowo Europejskiego Kongresu Osteoporozy i Osteoartrozy
Kwalifikacja do leczenia osteoporozy i kosztoefektywność leczenia osteoporozy w Polsce, polska wersja FRAX konferencja okrągłego stołu podczas IV Środkowo Europejskiego Kongresu Osteoporozy i Osteoartrozy
Formularz asortymentowo-cenowy
 Załącznik nr 2 do SIWZ... (pieczątka firmowa Wykonawcy) Formularz asortymentowo-cenowy Dotyczy postępowania pn. dostawa materiałów laboratoryjnych jednorazowego użytku, elementów zamkniętego systemu pobierania
Załącznik nr 2 do SIWZ... (pieczątka firmowa Wykonawcy) Formularz asortymentowo-cenowy Dotyczy postępowania pn. dostawa materiałów laboratoryjnych jednorazowego użytku, elementów zamkniętego systemu pobierania
Diagnostyka przedłużonego czasu częściowej tromboplastyny po aktywacji (aptt)
 PRACA POGLĄDOWA Hematologia 2010, tom 1, nr 1, 81 86 Copyright 2010 Via Medica ISSN 2081 0768 Diagnostyka przedłużonego czasu częściowej tromboplastyny po aktywacji (aptt) Diagnosis of the prolonged activated
PRACA POGLĄDOWA Hematologia 2010, tom 1, nr 1, 81 86 Copyright 2010 Via Medica ISSN 2081 0768 Diagnostyka przedłużonego czasu częściowej tromboplastyny po aktywacji (aptt) Diagnosis of the prolonged activated
MIEJSCE I ROLA POCT W OIT. Andrzej Kübler Katedra i I Klinika Anestezjologii i Intensywnej Terapii Uniwersytetu Medycznego we Wrocławiu
 MIEJSCE I ROLA POCT W OIT Andrzej Kübler Katedra i I Klinika Anestezjologii i Intensywnej Terapii Uniwersytetu Medycznego we Wrocławiu CO OZNACZA POCT POCT (Point-of-care testing) - oznacza wykonywanie
MIEJSCE I ROLA POCT W OIT Andrzej Kübler Katedra i I Klinika Anestezjologii i Intensywnej Terapii Uniwersytetu Medycznego we Wrocławiu CO OZNACZA POCT POCT (Point-of-care testing) - oznacza wykonywanie
ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE
 NARODOWY INSTYTUT ZDROWIA PUBLICZNEGO - PAŃSTWOWY ZAKŁAD HIGIENY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE ZAKŁAD WIRUSOLOGII NIZP-PZH UL. CHOCIMSKA 24 00-791 WARSZAWA
NARODOWY INSTYTUT ZDROWIA PUBLICZNEGO - PAŃSTWOWY ZAKŁAD HIGIENY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE ZAKŁAD WIRUSOLOGII NIZP-PZH UL. CHOCIMSKA 24 00-791 WARSZAWA
Próżniowy system pobierania krwi Do użytku w diagnostyce in vitro
 Próżniowy system pobierania krwi Do użytku w diagnostyce in vitro Przeznaczenie Probówki do pobierania krwi, uchwyty oraz igły VACUETTE stosuje się wspólnie jako system do pobierania krwi żylnej. Probówki
Próżniowy system pobierania krwi Do użytku w diagnostyce in vitro Przeznaczenie Probówki do pobierania krwi, uchwyty oraz igły VACUETTE stosuje się wspólnie jako system do pobierania krwi żylnej. Probówki
Zakład Diagnostyki Laboratoryjnej, Koagulologii i Mikrobiologii. Transport materiału biologicznego do laboratorium
 Opracował Sprawdził Zatwierdził Lidia Aftyka Małgorzata Szyszkowska Pełnomocnik ds. SZJ Jarosław Bakiera Dyrektor Szpitala Gabriel Maj podpis podpis podpis podpis ORYGINAŁ * Obowiązuje od : 01.02.2014r
Opracował Sprawdził Zatwierdził Lidia Aftyka Małgorzata Szyszkowska Pełnomocnik ds. SZJ Jarosław Bakiera Dyrektor Szpitala Gabriel Maj podpis podpis podpis podpis ORYGINAŁ * Obowiązuje od : 01.02.2014r
IMMUNOCHEMIA. Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice.
 IMMUNOCHEMIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
IMMUNOCHEMIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
ABX Pentra Phosphorus CP
 2013/06/18 A93A01300APL A11A01665 29.5 ml Pentra C400 Odczynnik diagnostyczny do oznaczania ilościowego in vitro stężenia fosforu w surowicy i osoczu krwi oraz moczu metodą kolorymetryczną. QUAL-QA-TEMP-0846
2013/06/18 A93A01300APL A11A01665 29.5 ml Pentra C400 Odczynnik diagnostyczny do oznaczania ilościowego in vitro stężenia fosforu w surowicy i osoczu krwi oraz moczu metodą kolorymetryczną. QUAL-QA-TEMP-0846
P O W I A D O M I E N I E nr 2 o zmianach SIWZ
 Wielospecjalistyczny Szpital Miejski im. dr E. Warmińskiego SPZOZ Szpitalna 19 85-826 Bydgoszcz Znak sprawy: ZP-270-3-2018 Bydgoszcz dnia: 2018-01-22 P O W I A D O M I E N I E nr 2 o zmianach SIWZ Dotyczy:
Wielospecjalistyczny Szpital Miejski im. dr E. Warmińskiego SPZOZ Szpitalna 19 85-826 Bydgoszcz Znak sprawy: ZP-270-3-2018 Bydgoszcz dnia: 2018-01-22 P O W I A D O M I E N I E nr 2 o zmianach SIWZ Dotyczy:
CMC/2015/03/WJ/03. Dzienniczek pomiarów ciśnienia tętniczego i częstości akcji serca
 CMC/2015/03/WJ/03 Dzienniczek pomiarów ciśnienia tętniczego i częstości akcji serca Dane pacjenta Imię:... Nazwisko:... PESEL:... Rozpoznane choroby: Nadciśnienie tętnicze Choroba wieńcowa Przebyty zawał
CMC/2015/03/WJ/03 Dzienniczek pomiarów ciśnienia tętniczego i częstości akcji serca Dane pacjenta Imię:... Nazwisko:... PESEL:... Rozpoznane choroby: Nadciśnienie tętnicze Choroba wieńcowa Przebyty zawał
ZAKRES AKREDYTACJI LABORATORIUM MEDYCZNEGO Nr AM 007
 ZAKRES AKREDYTACJI LABORATORIUM MEDYCZNEGO Nr AM 007 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa, ul. Szczotkarska 42 Wydanie nr 6 Data wydania: 6 maja 2016 r. Nazwa i adres INVICTA Sp. z
ZAKRES AKREDYTACJI LABORATORIUM MEDYCZNEGO Nr AM 007 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa, ul. Szczotkarska 42 Wydanie nr 6 Data wydania: 6 maja 2016 r. Nazwa i adres INVICTA Sp. z
Zespół antyfosfolipidowy obraz kliniczny i pułapki diagnostyczne
 Drn.med.MagdalenaCelińska Löwenhoff KlinikaAlergiiiImmunologii IIKatedraChoróbWewnętrznychUniwersytetuJagiellońskiego,CollegiumMedicum KierownikKatedry:Prof.drhab.JacekMusiał Zespółantyfosfolipidowy obrazklinicznyipułapkidiagnostyczne
Drn.med.MagdalenaCelińska Löwenhoff KlinikaAlergiiiImmunologii IIKatedraChoróbWewnętrznychUniwersytetuJagiellońskiego,CollegiumMedicum KierownikKatedry:Prof.drhab.JacekMusiał Zespółantyfosfolipidowy obrazklinicznyipułapkidiagnostyczne
Stabilność stężenia sodu, potasu i chlorków w surowicy przechowywanej w probówkach z aktywatorem krzepnięcia i separatorem żelowym
 diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab. 2018; 54(1): 23-28 ISSN 0867-4043 Praca oryginalna Original Article Stabilność stężenia sodu, potasu i chlorków w surowicy przechowywanej
diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab. 2018; 54(1): 23-28 ISSN 0867-4043 Praca oryginalna Original Article Stabilność stężenia sodu, potasu i chlorków w surowicy przechowywanej
ZAPROSZENIE NA BADANIA PROFILAKTYCZNE WYKONYWANE W RAMACH PODSTAWOWEJ OPIEKI ZDROWOTNEJ ( )
 ZAPROSZENIE NA BADANIA PROFILAKTYCZNE WYKONYWANE W RAMACH PODSTAWOWEJ OPIEKI ZDROWOTNEJ (2015-08-03) PROFILAKTYKA CHORÓB UKŁADU KRĄŻENIA ADRESACI - Osoby zadeklarowane do lekarza POZ, w wieku 35, 40, 45,
ZAPROSZENIE NA BADANIA PROFILAKTYCZNE WYKONYWANE W RAMACH PODSTAWOWEJ OPIEKI ZDROWOTNEJ (2015-08-03) PROFILAKTYKA CHORÓB UKŁADU KRĄŻENIA ADRESACI - Osoby zadeklarowane do lekarza POZ, w wieku 35, 40, 45,
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010
 Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
Standardy leczenia wirusowych zapaleń wątroby typu C Rekomendacje Polskiej Grupy Ekspertów HCV - maj 2010 1. Leczeniem powinni być objęci chorzy z ostrym, przewlekłym zapaleniem wątroby oraz wyrównaną
załącznik Nr 2 do siwz
 załącznik Nr 2 do siwz Wykonawca:...... Samodzielny Publiczny Zespół... Zakładów Opieki Zdrowotnej w Kozienicach fax./tel:... Al. Wł. Sikorskiego 10 26-00 Kozienice tel.:/fax: (4) 32 7 73/ (4) 614 1 3
załącznik Nr 2 do siwz Wykonawca:...... Samodzielny Publiczny Zespół... Zakładów Opieki Zdrowotnej w Kozienicach fax./tel:... Al. Wł. Sikorskiego 10 26-00 Kozienice tel.:/fax: (4) 32 7 73/ (4) 614 1 3
Największe wyzwania w diagnostyce zaburzeń lipidowych. Cholesterol LDL oznaczany bezpośrednio, czy wyliczany ze wzoru Friedewalna, na czczo czy nie?
 Największe wyzwania w diagnostyce zaburzeń lipidowych. Cholesterol LDL oznaczany bezpośrednio, czy wyliczany ze wzoru Friedewalna, na czczo czy nie? Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet
Największe wyzwania w diagnostyce zaburzeń lipidowych. Cholesterol LDL oznaczany bezpośrednio, czy wyliczany ze wzoru Friedewalna, na czczo czy nie? Bogdan Solnica Katedra Biochemii Klinicznej Uniwersytet
Dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę odczynników do koaguologii wraz z dzierżawą analizatorów.
 Toruń, dnia 21.07.2015 r. SSM.DZP.200.57.2015 Dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę do koaguologii wraz z dzierżawą analizatorów. W związku ze skierowanymi
Toruń, dnia 21.07.2015 r. SSM.DZP.200.57.2015 Dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę do koaguologii wraz z dzierżawą analizatorów. W związku ze skierowanymi
Zajęcia w grupach studenckich/dziekańskich (co najmniej 12 osobowych) 15 Zajęcia w grupach łączonych (co najmniej 24 osobowych) 15
 Kierunek Dietetyka (2-ST) Semestr 2 (I rok) Nazwa przedmiotu Diagnostyka Laboratoryjna Jednostka prowadząca zajęcia Zakład Zaburzeń Krzepnięcia Krwi Katedry Diagnostyki Laboratoryjnej Adres jednostki Szpital
Kierunek Dietetyka (2-ST) Semestr 2 (I rok) Nazwa przedmiotu Diagnostyka Laboratoryjna Jednostka prowadząca zajęcia Zakład Zaburzeń Krzepnięcia Krwi Katedry Diagnostyki Laboratoryjnej Adres jednostki Szpital
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH
 Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
Agencja Oceny Technologii Medycznych
 Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 379/2013 z dnia 30 grudnia 2013 r. w sprawie zasadności dalszego finansowania produktów leczniczych zawierających
Agencja Oceny Technologii Medycznych Rada Przejrzystości Opinia Rady Przejrzystości nr 379/2013 z dnia 30 grudnia 2013 r. w sprawie zasadności dalszego finansowania produktów leczniczych zawierających
dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę odczynników do koagulologii wraz z dzierżawa analizatorów.
 Toruń, dn. 25.10.2013r. L.dz. SSM.DZP.200.170.2013 dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę odczynników do koagulologii wraz z dzierżawa analizatorów.
Toruń, dn. 25.10.2013r. L.dz. SSM.DZP.200.170.2013 dotyczy: postępowania o zamówienie publiczne w trybie przetargu nieograniczonego na dostawę odczynników do koagulologii wraz z dzierżawa analizatorów.
Uniwersytet Medyczny w Łodzi Wydział Nauk o Zdrowiu Sylabus 2011/2012
 Uniwersytet Medyczny w Łodzi Wydział Nauk o Zdrowiu Sylabus 2011/2012 1. Nazwa jednostki realizującej przedmiot (adres, telefon, e-mail): Zakład Zaburzeń Krzepnięcia Krwi Katedra Diagnostyki Laboratoryjnej
Uniwersytet Medyczny w Łodzi Wydział Nauk o Zdrowiu Sylabus 2011/2012 1. Nazwa jednostki realizującej przedmiot (adres, telefon, e-mail): Zakład Zaburzeń Krzepnięcia Krwi Katedra Diagnostyki Laboratoryjnej
ELIMINACJA ODRY/RÓŻYCZKI
 PAŃSTWOWY ZAKŁAD HIGIENY INSTYTUT NAUKOWO-BADAWCZY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE - ZASADY - INSTRUKCJE ZAKŁAD WIRUSOLOGII UL. CHOCIMSKA 24 00-791 WARSZAWA PROGRAM ELIMINACJI
PAŃSTWOWY ZAKŁAD HIGIENY INSTYTUT NAUKOWO-BADAWCZY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE - ZASADY - INSTRUKCJE ZAKŁAD WIRUSOLOGII UL. CHOCIMSKA 24 00-791 WARSZAWA PROGRAM ELIMINACJI
PRZYGOTOWANIE PACJENTA DO BADAŃ LABORATORYJNYCH. Na podstawie: Próbki: od pacjenta do laboratorium
 SP ZOZ w Hrubieszowie Przygotowała i opracowała mgr Marta Telicka PRZEWODNIK PRZYGOTOWANIE PACJENTA DO BADAŃ LABORATORYJNYCH Na podstawie: Próbki: od pacjenta do laboratorium Wpływ zmienności przedanalitycznej
SP ZOZ w Hrubieszowie Przygotowała i opracowała mgr Marta Telicka PRZEWODNIK PRZYGOTOWANIE PACJENTA DO BADAŃ LABORATORYJNYCH Na podstawie: Próbki: od pacjenta do laboratorium Wpływ zmienności przedanalitycznej
ZAKRES AKREDYTACJI LABORATORIUM MEDYCZNEGO Nr AM 007
 ZAKRES AKREDYTACJI LABORATORIUM MEDYCZNEGO Nr AM 007 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa, ul. Szczotkarska 42 Wydanie nr 8 Data wydania: 1 marca 2018 r. Nazwa i adres MEDYCZNE LABORATORIA
ZAKRES AKREDYTACJI LABORATORIUM MEDYCZNEGO Nr AM 007 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa, ul. Szczotkarska 42 Wydanie nr 8 Data wydania: 1 marca 2018 r. Nazwa i adres MEDYCZNE LABORATORIA
1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań
 Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Laboratorium Zakładu Badania Wirusów Grypy, Krajowy Ośrodek ds. Grypy (obowiązuje
Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Laboratorium Zakładu Badania Wirusów Grypy, Krajowy Ośrodek ds. Grypy (obowiązuje
Grant NCN 2011/03/B/ST7/03649. Reguły systemu wsparcia decyzji: wskazania/przeciwskazania trombolizy
 Grant NCN 2011/03/B/ST7/03649 Reguły systemu wsparcia decyzji: wskazania/przeciwskazania trombolizy Kryterium Dane (jakie) Dane (źródło) Reguła Moduł wiek wiek pacjent/osoba > 18 lat (włączająca) kliniczne
Grant NCN 2011/03/B/ST7/03649 Reguły systemu wsparcia decyzji: wskazania/przeciwskazania trombolizy Kryterium Dane (jakie) Dane (źródło) Reguła Moduł wiek wiek pacjent/osoba > 18 lat (włączająca) kliniczne
Najbardziej Wiarygodny, Nieinwazyjny Test Prenatalny wykonywany w Polsce Test NIFTY : tylko mała próbka krwi ciężarnej
 Najbardziej Wiarygodny, Nieinwazyjny Test Prenatalny wykonywany w Polsce Test NIFTY : To nieinwazyjny, genetyczny test prenatalny nowej generacji, który określa ryzyko trisomii chromosomów 21, 18 i 13
Najbardziej Wiarygodny, Nieinwazyjny Test Prenatalny wykonywany w Polsce Test NIFTY : To nieinwazyjny, genetyczny test prenatalny nowej generacji, który określa ryzyko trisomii chromosomów 21, 18 i 13
Próżniowy system pobierania krwi Do użytku w diagnostyce in vitro
 Przeznaczenie Próżniowy system pobierania krwi Do użytku w diagnostyce in vitro Probówki do pobierania krwi, uchwyty oraz igły VACUETTE stosuje się wspólnie jako system do pobierania krwi żylnej. Probówki
Przeznaczenie Próżniowy system pobierania krwi Do użytku w diagnostyce in vitro Probówki do pobierania krwi, uchwyty oraz igły VACUETTE stosuje się wspólnie jako system do pobierania krwi żylnej. Probówki
LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2
 załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
załącznik nr 11 do zarządzenia Nr 36/2008/DGL Prezesa NFZ z dnia 19 czerwca 2008 r. Nazwa programu LECZENIE NADPŁYTKOWOŚCI SAMOISTNEJ ICD - 10 D75.2 - nadpłytkowość samoistna Dziedzina medycyny: hematologia.
Maciej Korpysz. Zakład Diagnostyki Biochemicznej UM Lublin Dział Diagnostyki Laboratoryjnej Samodzielny Publiczny Szpital Kliniczny Nr 1 w Lublinie
 Nowe możliwości oceny białka monoklonalnego za pomocą oznaczeń par ciężki-lekki łańcuch immunoglobulin (test Hevylite) u chorych z dyskrazjami plazmocytowymi. Maciej Korpysz Zakład Diagnostyki Biochemicznej
Nowe możliwości oceny białka monoklonalnego za pomocą oznaczeń par ciężki-lekki łańcuch immunoglobulin (test Hevylite) u chorych z dyskrazjami plazmocytowymi. Maciej Korpysz Zakład Diagnostyki Biochemicznej
Faza przedanalityczna w hematologii (cz. I)
 Faza przedanalityczna w hematologii (cz. I) Optymalną jakość wyników można osiągnąć jedynie, jeśli cały proces diagnostyczny przebiega prawidłowo. Proces ten można podzielić na fazy: przedanalityczną,
Faza przedanalityczna w hematologii (cz. I) Optymalną jakość wyników można osiągnąć jedynie, jeśli cały proces diagnostyczny przebiega prawidłowo. Proces ten można podzielić na fazy: przedanalityczną,
Laboratoryjna Diagnostyka Hematologiczna
 Krajowa Izba Diagnostów Laboratoryjnych, Szpital Kliniczny Przemienienia Pańskiego Uniwersytetu Medycznego im. Karola Marcinkowskiego w Poznaniu oraz BONO SERVIAMUS Stowarzyszenie na Rzecz Rozwoju Szpitala
Krajowa Izba Diagnostów Laboratoryjnych, Szpital Kliniczny Przemienienia Pańskiego Uniwersytetu Medycznego im. Karola Marcinkowskiego w Poznaniu oraz BONO SERVIAMUS Stowarzyszenie na Rzecz Rozwoju Szpitala
1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań
 Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Pracowni Diagnostycznej Laboratorium Zakładu Badania Wirusów Grypy (obowiązuje
Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Pracowni Diagnostycznej Laboratorium Zakładu Badania Wirusów Grypy (obowiązuje
FORMULARZ CENOWY - ZMODYFIKOWANY. Podatek VAT Wartość netto % kwota RAZEM: Ilość ozn. w opakowaniu. Ilość pełnych opakowań
 FORMULARZ CENOWY - ZMODYFIKOWANY Załącznik Nr 2 do SIWZ I. Analizatory: OFERTA NA DZIERśAWĘ ANALIZATORA PODSTAWOWEGO PRZY ZAŁOśENIU, śe POSIADANY PRZEZ ZAMAWIAJĄCEGO ANALIZATOR ACL ELITE PRO BĘDZIE PEŁNIŁ
FORMULARZ CENOWY - ZMODYFIKOWANY Załącznik Nr 2 do SIWZ I. Analizatory: OFERTA NA DZIERśAWĘ ANALIZATORA PODSTAWOWEGO PRZY ZAŁOśENIU, śe POSIADANY PRZEZ ZAMAWIAJĄCEGO ANALIZATOR ACL ELITE PRO BĘDZIE PEŁNIŁ
ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01
![ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01 ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01](/thumbs/25/4516998.jpg) ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Do monitorowania wydajności testu Access HIV combo. - [PL] - 2015/01 Spis treści Access HIV combo QC4 & QC5 1 Przeznaczenie... 3 2 Podsumowanie i objaśnienie
ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Do monitorowania wydajności testu Access HIV combo. - [PL] - 2015/01 Spis treści Access HIV combo QC4 & QC5 1 Przeznaczenie... 3 2 Podsumowanie i objaśnienie
IV Kadencja XIII Posiedzenie KRDL
 IV Kadencja XIII Posiedzenie KRDL Uchwała Nr 111/IV/2017 Krajowej Rady Diagnostów Laboratoryjnych z dnia 8 grudnia 2017 roku w przedmiocie zmiany uchwały Nr 18/IV/2015 Krajowej Rady Diagnostów Laboratoryjnych
IV Kadencja XIII Posiedzenie KRDL Uchwała Nr 111/IV/2017 Krajowej Rady Diagnostów Laboratoryjnych z dnia 8 grudnia 2017 roku w przedmiocie zmiany uchwały Nr 18/IV/2015 Krajowej Rady Diagnostów Laboratoryjnych
Jak przygotować się do badania laboratoryjnego? Badanie krwi
 Badanie krwi Zalecana pora pobierania krwi do badań laboratoryjnych to 7 00 9 00 rano. Pacjent powinien być na czczo, czyli dwanaście godzin przed planowanym pobraniem krwi nie należy jeść, pić, z wyjątkiem
Badanie krwi Zalecana pora pobierania krwi do badań laboratoryjnych to 7 00 9 00 rano. Pacjent powinien być na czczo, czyli dwanaście godzin przed planowanym pobraniem krwi nie należy jeść, pić, z wyjątkiem
Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu.
 WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
ZESTAWIENIE PARAMETRÓW TECHNICZNYCH I WYMOGÓW GRANICZNYCH PAKIET Nr 1 Materiały kontrolne do programu sprawdzianów chemicznych
 PAKIET Nr 1 Materiały kontrolne do programu sprawdzianów chemicznych 1. Oba materiały kontrolne wyprodukowane wyłącznie na bazie surowicy ludzkiej (udokumentować w ulotce). Dwa materiały o różnych poziomach
PAKIET Nr 1 Materiały kontrolne do programu sprawdzianów chemicznych 1. Oba materiały kontrolne wyprodukowane wyłącznie na bazie surowicy ludzkiej (udokumentować w ulotce). Dwa materiały o różnych poziomach
Sylabus. Analityka Medyczna
 Nazwa modułu/przedmiotu Sylabus Opis przedmiotu kształcenia PRAKTYCZNA NAUKA ZAWODU Practical training in laboratory diagnostic Grupa szczegółowych efektów kształcenia Kod grupy Nazwa grupy Wydział Kierunek
Nazwa modułu/przedmiotu Sylabus Opis przedmiotu kształcenia PRAKTYCZNA NAUKA ZAWODU Practical training in laboratory diagnostic Grupa szczegółowych efektów kształcenia Kod grupy Nazwa grupy Wydział Kierunek
Pytania i Odpowiedzi do Przetargu na Odczynniki Laboratoryjne
 Pytania i Odpowiedzi do Przetargu na Odczynniki Laboratoryjne Czy Zamawiający w Pakiecie nr 1, poz. 29 wymaga testu o czułości: 0,1 ng/ml ( w tabeli podano wartość 01 ng/ml brak przecinka)? Odp. Tak wymaga
Pytania i Odpowiedzi do Przetargu na Odczynniki Laboratoryjne Czy Zamawiający w Pakiecie nr 1, poz. 29 wymaga testu o czułości: 0,1 ng/ml ( w tabeli podano wartość 01 ng/ml brak przecinka)? Odp. Tak wymaga
Sepsa, wstrząs septyczny, definicja, rozpoznanie
 Sepsa, wstrząs septyczny, definicja, rozpoznanie dr hab. n.med. Barbara Adamik Katedra i Klinika Anestezjologii i Intensywnej Terapii Uniwersytet Medyczny we Wrocławiu Sepsa, wstrząs septyczny, definicja,
Sepsa, wstrząs septyczny, definicja, rozpoznanie dr hab. n.med. Barbara Adamik Katedra i Klinika Anestezjologii i Intensywnej Terapii Uniwersytet Medyczny we Wrocławiu Sepsa, wstrząs septyczny, definicja,
Karmienie cieląt - jak kontrolować jakość podawanej siary?
 https://www. Karmienie cieląt - jak kontrolować jakość podawanej siary? Autor: dr hab. Robert Kupczyński Data: 24 września 2017 W ostatnim artykule na temat odpajania cieląt zwracaliśmy uwagę na rolę siary
https://www. Karmienie cieląt - jak kontrolować jakość podawanej siary? Autor: dr hab. Robert Kupczyński Data: 24 września 2017 W ostatnim artykule na temat odpajania cieląt zwracaliśmy uwagę na rolę siary
Wpływ czynników przedanalitycznych na wynik badania morfologii krwi
 diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab 2015; 51(4): 271-276 Praca oryginalna Original Article Wpływ czynników przedanalitycznych na wynik badania morfologii krwi The influence
diagnostyka laboratoryjna Journal of Laboratory Diagnostics Diagn Lab 2015; 51(4): 271-276 Praca oryginalna Original Article Wpływ czynników przedanalitycznych na wynik badania morfologii krwi The influence
Krwotok urazowy u chorego leczonego nowoczesnymi doustnymi antykoagulantami
 Krwotok urazowy u chorego leczonego nowoczesnymi doustnymi antykoagulantami dr hab. n. med. Tomasz Łazowski I Klinika Anestezjologii i Intensywnej Terapii Warszawski Uniwersytet Medyczny 2017 Dabigatran
Krwotok urazowy u chorego leczonego nowoczesnymi doustnymi antykoagulantami dr hab. n. med. Tomasz Łazowski I Klinika Anestezjologii i Intensywnej Terapii Warszawski Uniwersytet Medyczny 2017 Dabigatran
10) istotne kliniczne dane pacjenta, w szczególności: rozpoznanie, występujące czynniki ryzyka zakażenia, w tym wcześniejsza antybiotykoterapia,
 Załącznik nr 2 Standardy jakości w zakresie mikrobiologicznych badań laboratoryjnych, w tym badań technikami biologii molekularnej, oceny ich jakości i wartości diagnostycznej oraz laboratoryjnej interpretacji
Załącznik nr 2 Standardy jakości w zakresie mikrobiologicznych badań laboratoryjnych, w tym badań technikami biologii molekularnej, oceny ich jakości i wartości diagnostycznej oraz laboratoryjnej interpretacji
ABX Pentra Glucose HK CP
 2012/04/30 A93A01229DPL A11A01667 56 ml 14 ml Pentra C200 Zastosowanie: Odczynnik diagnostyczny do oznaczania ilościowego in vitro stężenia glukozy w surowicy, osoczu i moczu przy użyciu heksokinazy metodą
2012/04/30 A93A01229DPL A11A01667 56 ml 14 ml Pentra C200 Zastosowanie: Odczynnik diagnostyczny do oznaczania ilościowego in vitro stężenia glukozy w surowicy, osoczu i moczu przy użyciu heksokinazy metodą
Możliwość automatyzacji oznaczania szybkości opadania krwinek czerwonych w laboratorium rutynowym
 diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2013 Volume 49 Number 2 113-117 Praca oryginalna Original Article Możliwość automatyzacji oznaczania szybkości opadania krwinek czerwonych w
diagnostyka laboratoryjna Journal of Laboratory Diagnostics 2013 Volume 49 Number 2 113-117 Praca oryginalna Original Article Możliwość automatyzacji oznaczania szybkości opadania krwinek czerwonych w
PCR bez izolacji testujemy Direct PCR Kits od ThermoFisher Scientific
 PCR bez izolacji testujemy Direct PCR Kits od ThermoFisher Scientific Specjalnie dla Was przetestowaliśmy w naszym laboratorium odczynniki firmy Thermo Scientific umożliwiające przeprowadzanie reakcji
PCR bez izolacji testujemy Direct PCR Kits od ThermoFisher Scientific Specjalnie dla Was przetestowaliśmy w naszym laboratorium odczynniki firmy Thermo Scientific umożliwiające przeprowadzanie reakcji
CIBA-GEIGY Sintrom 4
 CIBA-GEIGY Sintrom 4 Sintrom 4 Substancja czynna: 3-[a-(4-nitrofenylo-)-0- -acetyloetylo]-4-hydroksykumaryna /=acenocoumarol/. Tabletki 4 mg. Sintrom działa szybko i jest wydalany w krótkim okresie czasu.
CIBA-GEIGY Sintrom 4 Sintrom 4 Substancja czynna: 3-[a-(4-nitrofenylo-)-0- -acetyloetylo]-4-hydroksykumaryna /=acenocoumarol/. Tabletki 4 mg. Sintrom działa szybko i jest wydalany w krótkim okresie czasu.
ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67)
 Załącznik B.15. ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii pierwotnej i wtórnej
Załącznik B.15. ZAPOBIEGANIE KRWAWIENIOM U DZIECI Z HEMOFILIĄ A I B (ICD-10 D 66, D 67) ZAKRES ŚWIADCZENIA GWARANTOWANEGO ŚWIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii pierwotnej i wtórnej
Iga Niczyporuk II rok licencjat
 Iga Niczyporuk II rok licencjat jeden z płynów ustrojowych w organizmie człowieka, którego objętość wynosi ok. 5 5,5 litrów. Krew spełnia czynności transportowe, dostarcza do tkanek tlen i substancje odżywcze,
Iga Niczyporuk II rok licencjat jeden z płynów ustrojowych w organizmie człowieka, którego objętość wynosi ok. 5 5,5 litrów. Krew spełnia czynności transportowe, dostarcza do tkanek tlen i substancje odżywcze,
LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0)
 Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
Załącznik B.22. LECZENIE CHOROBY POMPEGO (ICD-10 E 74.0) WIADCZENIOBIORCY Kwalifikacji świadczeniobiorców do terapii dokonuje Zespół Koordynacyjny ds. Chorób Ultrarzadkich powoływany przez Prezesa Narodowego
Bartosz Horosz. Klinika Anestezjologii i Intensywnej Terapii Centrum Medycznego Kształcenia Podyplomowego Warszawa. Sopot, 17 kwietnia 2015r.
 Bartosz Horosz Klinika Anestezjologii i Intensywnej Terapii Centrum Medycznego Kształcenia Podyplomowego Warszawa Sopot, 17 kwietnia 2015r. Zjawisko Śródoperacyjną hipotermię definiuje się jako obniżenie
Bartosz Horosz Klinika Anestezjologii i Intensywnej Terapii Centrum Medycznego Kształcenia Podyplomowego Warszawa Sopot, 17 kwietnia 2015r. Zjawisko Śródoperacyjną hipotermię definiuje się jako obniżenie
Miejsce POCT w szpitalnym systemie diagnostyki laboratoryjnej
 Miejsce POCT w szpitalnym systemie diagnostyki laboratoryjnej Konferencja Naukowo-Szkoleniowa, Jachranka 20-21 listopada 2014 Arkadiusz Wnuk Zakład Diagnostyki Centrum Urazowe Medycyny Ratunkowej i Katastrof
Miejsce POCT w szpitalnym systemie diagnostyki laboratoryjnej Konferencja Naukowo-Szkoleniowa, Jachranka 20-21 listopada 2014 Arkadiusz Wnuk Zakład Diagnostyki Centrum Urazowe Medycyny Ratunkowej i Katastrof
LANGUAGE: NO_DOC_EXT: SOFTWARE VERSION: 9.5.4
 LANGUAGE: PL CATEGORY: ORIG FORM: F14 VERSION: R2.0.9.S02 SENDER: ENOTICES CUSTOMER: AgnieszkaWronka NO_DOC_EXT: 2017-105046 SOFTWARE VERSION: 9.5.4 ORGANISATION: ENOTICES COUNTRY: EU PHONE: / E-mail:
LANGUAGE: PL CATEGORY: ORIG FORM: F14 VERSION: R2.0.9.S02 SENDER: ENOTICES CUSTOMER: AgnieszkaWronka NO_DOC_EXT: 2017-105046 SOFTWARE VERSION: 9.5.4 ORGANISATION: ENOTICES COUNTRY: EU PHONE: / E-mail:
INTERPRETACJA WYNIKÓW BADAŃ MOLEKULARNYCH W CHOROBIE HUNTINGTONA
 XX Międzynarodowa konferencja Polskie Stowarzyszenie Choroby Huntingtona Warszawa, 17-18- 19 kwietnia 2015 r. Metody badań i leczenie choroby Huntingtona - aktualności INTERPRETACJA WYNIKÓW BADAŃ MOLEKULARNYCH
XX Międzynarodowa konferencja Polskie Stowarzyszenie Choroby Huntingtona Warszawa, 17-18- 19 kwietnia 2015 r. Metody badań i leczenie choroby Huntingtona - aktualności INTERPRETACJA WYNIKÓW BADAŃ MOLEKULARNYCH
