Cząsteczki. Opis termodynamiczny Opis kwantowy. Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? typy wiąza.
|
|
|
- Bartosz Józef Kwiatkowski
- 5 lat temu
- Przeglądów:
Transkrypt
1 Cząsteczki 1.Dlczego tomy łącz czą się w cząsteczki?.jk tomy łącz czą się w cząsteczki? 3.Co to jest wiąznie chemiczne? Co to jest rząd d wiązni? Dlczego tomy łącz czą się? Opis termodynmiczny Opis kwntowy
2 Cząsteczki homojądrowe Jk tomy łącz czą się? Jk utworzyć oritl molekulrny? ψ = c ψ c ψ Liniow komincj oritli tomowych (LCAO) Weźmy tomy wodory i utwórzmy molekułę H
3 Jk tomy łącz czą się? Jką postć m opertor energii? Hˆ = Tˆ e, Tˆ e, Vˆ ˆ ˆ e Ve V Vˆ e, e, energi kinetyczn elektronów energi potencjln elektronów w polu jąder energi potencjln jąder i energi potencjln Elektronów z tomów i Jk tomy łącz czą się? Jką postć m funkcj flow molekuły y H? ψ = c ψ ( ) c ψ ( ) MO Przepis n oritl molekulrny (MO): liniow komincj oritli tomowych Cł sztuk przy poszukiwniu funkcji flowej Ψ MO sprowdz się ztem do poszukni wrtości współczynnik czynników c i c
4 Jk tomy łącz czą się? Jką postć m funkcj flow molekuły y H? ψ ψ MO,1 MO, = ψ ( ) ψ ( ) = ψ ( ) ψ ( ) c c = c = c = 1 = 1 Liniow komincj poleg n tym, że e z oritli tomowych powstją zwsze oritle molekulrne, itd Jk tomy łącz czą się? Jką postć m gęstog stość prwdopodoieństw MO molekuły y H? Ψ MO ψ MO,1 = N ψ MO,1 = N = N ( ψ ( ) ψ ( )) ( ψ ( ) ψ ( ) ψ ( ) ψ ( )) = N ( ψ ( ) ψ ( )) ( ψ ( ) ψ ( ) ψ ( ) ψ ( )) = = N współczynnik normujący funkcję
5 Co to jest wiąznie? wzmocnienie 0 ψ = ψ ( ) ψ (1 ) ψ =ψ = e MO, 1 s r oritl wiążą ążący Co to jest wiąznie? osłienie - wygszenie ψ MO, 1 = ψ ( ) ψ ( ) - -
6 Co to jest wiąznie? wzmocnienie osłienie ψ gęstość prwdopodoieństw gęstość prwdopodoieństw MO,1 r r Co to jest wiąznie? energi oritl ntywiążący oritl wiążący
7 Co to jest wiąznie? poziomy energii elektronów E Energy digrm H A H H H B MO Electron proility distri A B () MO 1 () rozkłd gęstości prwdopodoieństw Co to jest wiąznie? ψ ψ MO,1 MO, = σ oritl wiążą ążący = σ * oritl ntywiążą ążący Reguły zpełnini oritli molekulrnych: minimum energii zkz Puliego reguł Hund
8 Co to jest rząd d wiązni? R= n e n oritlu wiążącym - n e n oritlu ntywiążącym R = * n e n e Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * 1 0 R = = 1 H H σ [ H ] = ( σ ) 1
9 Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * R = 0 = 1 H σ H [ H ] = ( σ ) Któr cząsteczk jest rdziej trwł? Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be 1 0 R = = 1 R = 0 = 1 Któr cząsteczk jest rdziej trwł?
10 Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * R = 1 = 1 He He σ * [ He ] = ( σ ) ( σ ) 1 Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * R = = 0 He He σ * [ He ] = ( σ ) ( σ ) He nie istnieje
11 Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * s s σ s σ * s R = 3 = 1 * [ Li ] = ( σ ) ( σ )( σ ) 1 s Li Li σ Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * s s σ s σ * s 4 R = = 1 * [ Li ] = ( σ ) ( σ )( σ ) s Li σ Li Któr cząsteczk jest rdziej trwł?
12 Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * s s σ s σ * s R = 4 3 = 1 Be Be σ * * [ Be ] = ( σ ) ( σ ) ( σ )( σ ) 1 s s Jk przewidywć trwłość molekuł? Któr cząsteczk istnieje? H H He He Li Li Be Be σ * s s σ s σ * s 4 4 R = = 0 * * [ Be ] = ( σ ) ( σ ) ( σ )( σ ) s s Be σ Be Be nie istnieje
13 09_190 Jkie typy oritli molekulrnych tworzą się z oritli tomowych typu p? Antionding σ* p () p x p x σ p Bonding π* p Antionding () p y p y Bonding π p Jkie typy oritli molekulrnych tworzą się z oritli tomowych typu π? B B () π π σ
14 Z jkich oritli tworzą się wiązni σ? s s p p s-oritl s-oritl σ-onding MO p-oritl p-oritl σ-onding MO s p s-oritl p-oritl σ-onding MO Z jkich oritli tworzą się wiązni π? p p p d
15 Przykłd B 1 [ ] ( ) ( ) ( ) ( ) ( )( ) 1 B = σ σ σ * * s s p p σ π π p π * p p σ p π p σ * B B s s () σ Przykłd * * d N [ N ] = ( σ ) ( σ ) ( σ ) ( σ ) ( σ ) ( π ) ( π ) s s px p y pz E p σ * p π * p p σ p π p σ * s s σ
16 Przykłd * * * 1 * d O [ N ] = ( σ ) ( σ ) ( σ ) ( σ ) ( σ ) ( π ) ( π ) ( π )( π ) 1 s s px p y pz p y pz E p σ * p π * p p σ p π p σ * s s σ Przykłd * * * * d F [ N ] = ( σ ) ( σ ) ( σ ) ( σ ) ( σ ) ( π ) ( π ) ( π ) ( π ) s s px p y pz p y pz E p σ * p π * p p σ p π p σ * s s σ
17 B C N O F σ p * π p * σ p * π p * E σ p π p σ s * π p σ p σ s * σ s σ s Rząd d wiązni Energi dysocjcji Długość mgnetyczność pr di di pr di 1.7 przykłdy związków 1.6 długość wiązni O - O - O O BO KO O PtF rząd wiązni
18 Cząsteczki heterojądrowe Przykłd HF 09_198 H tom HF molecule σ * F tom 09_199 E p σ H nucleus F nucleus
19 Jkie są ń? Przykłd LiH
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Inżynieria Biomedyczna. Wykład XII
 Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
TEORIA ORBITALI MOLEKULARNYCH (MO) dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Wiązania. w świetle teorii kwantów fenomenologicznie
 Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
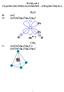 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa. Mechanika kwantowa. dx dy dz. Jak opisać atom wodoru? Jak opisać inne cząsteczki? Równanie Schrödingera. zasada zachowania energii
 Mecnik kwntow Jk opisć tom wodou? Jk opisć inne cąstecki? Mecnik kwntow Równnie Scödinge Ĥ E ψ H ˆψ = Eψ opeto óżnickow Hmilton enegi funkcj flow d d d + + m d d d opeto enegii kinetcn enegi kinetcn elektonu
Mecnik kwntow Jk opisć tom wodou? Jk opisć inne cąstecki? Mecnik kwntow Równnie Scödinge Ĥ E ψ H ˆψ = Eψ opeto óżnickow Hmilton enegi funkcj flow d d d + + m d d d opeto enegii kinetcn enegi kinetcn elektonu
13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe)
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 13 UKŁADY KILKU CZĄSTEK W MECHANICE KWANTOWEJ 13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe) Zajmiemy się kwantowym opisem atomu He
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 13 UKŁADY KILKU CZĄSTEK W MECHANICE KWANTOWEJ 13.1 Układy helopodobne (trójcząstkowe układy dwuelektronowe) Zajmiemy się kwantowym opisem atomu He
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkow Hamiltona energia funkcja falowa h d d d + + m d d dz
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Układ okresowy Przewidywania teorii kwantowej
 Przewiywania teorii kwantowej Chemia kwantowa - oumowanie Czątka w ule Atom wooru Równanie Schroeingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - oumowanie rozwiązanie Czątka w ule Atom wooru Ψn
Przewiywania teorii kwantowej Chemia kwantowa - oumowanie Czątka w ule Atom wooru Równanie Schroeingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - oumowanie rozwiązanie Czątka w ule Atom wooru Ψn
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Prawo Coulomba i pole elektryczne
 Prwo Coulomb i pole elektryczne Mciej J. Mrowiński 4 pździernik 2010 Zdnie PE1 2R R Dwie młe kulki o msie m, posidjące ten sm łdunek, umieszczono w drewninym nczyniu, którego przekrój wygląd tk jk n rysunku
Prwo Coulomb i pole elektryczne Mciej J. Mrowiński 4 pździernik 2010 Zdnie PE1 2R R Dwie młe kulki o msie m, posidjące ten sm łdunek, umieszczono w drewninym nczyniu, którego przekrój wygląd tk jk n rysunku
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej jedną z dwóch metod (teorii): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
cz. 2 dr inż. Zbigniew Szklarski
 Wykłd 11: Elektrosttyk cz. 2 dr inż. Zbigniew Szklrski szkl@gh.edu.pl http://lyer.uci.gh.edu.pl/z.szklrski/ Pole elektryczne przewodnik N powierzchni metlicznej (przewodzącej) cły łdunek gromdzi się n
Wykłd 11: Elektrosttyk cz. 2 dr inż. Zbigniew Szklrski szkl@gh.edu.pl http://lyer.uci.gh.edu.pl/z.szklrski/ Pole elektryczne przewodnik N powierzchni metlicznej (przewodzącej) cły łdunek gromdzi się n
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Oddziaływanie atomu z kwantowym polem E-M: C.D.
 Oddziaływanie atomu z kwantowym polem E-M: C.D. 1 atom jakoźródło 1 fotonu. Emisja spontaniczna wg. złotej reguły Fermiego. Absorpcja i emisja kolektywna ˆ E( x,t)=i λ Powtórzenie d 3 ω k k 2ǫ(2π) 3 e
Oddziaływanie atomu z kwantowym polem E-M: C.D. 1 atom jakoźródło 1 fotonu. Emisja spontaniczna wg. złotej reguły Fermiego. Absorpcja i emisja kolektywna ˆ E( x,t)=i λ Powtórzenie d 3 ω k k 2ǫ(2π) 3 e
Struktura energetyczna ciał stałych-cd. Fizyka II dla Elektroniki, lato
 Struktur energetyczn cił stłych-cd Fizyk II dl Elektroniki, lto 011 1 Fizyk II dl Elektroniki, lto 011 Przybliżenie periodycznego potencjłu sieci krystlicznej model Kronig- Penney potencjł rzeczywisty
Struktur energetyczn cił stłych-cd Fizyk II dl Elektroniki, lto 011 1 Fizyk II dl Elektroniki, lto 011 Przybliżenie periodycznego potencjłu sieci krystlicznej model Kronig- Penney potencjł rzeczywisty
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia. Monika Musia l
 STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Model kroplowy jądra atomowego
 B Model kroplowy jądr tomowego M ( Z, A) = Zm + ( A Z ) m B( Z A) p n, Fenomenologiczny wzór n energię wiązni jądr (Bohr i von Weizsäcker) /3 1/3 1 1/ ( Z, A) c = A A Z A ( A Z ) A + A V S C A V = 15,7
B Model kroplowy jądr tomowego M ( Z, A) = Zm + ( A Z ) m B( Z A) p n, Fenomenologiczny wzór n energię wiązni jądr (Bohr i von Weizsäcker) /3 1/3 1 1/ ( Z, A) c = A A Z A ( A Z ) A + A V S C A V = 15,7
Chemia kwantowa. Pytania egzaminacyjne. 2010/2011: 1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
1 Chemia kwantowa. Pytania egzaminacyjne. 21/211: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny - interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest licza
Praca, potencjał i pojemność
 Prc, potencjł i pojemność Mciej J. Mrowiński 1 listopd 2010 Zdnie PPP1 h Wyzncz wrtość potencjłu elektrycznego w punkcie oddlonym o h od cienkiego, jednorodnie nłdownego łdunkiem Q pierścieni o promieniu.
Prc, potencjł i pojemność Mciej J. Mrowiński 1 listopd 2010 Zdnie PPP1 h Wyzncz wrtość potencjłu elektrycznego w punkcie oddlonym o h od cienkiego, jednorodnie nłdownego łdunkiem Q pierścieni o promieniu.
Symbol termu: edu (sumy ca lkowitego orbitalnego momentu edu i ca lkowitego spinu) Przyk lad: 2 P 3. kwantowa
 Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
26 Okresowy układ pierwiastków
 26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
H H 2.5 < H H CH 3 N O O H C N ŁADUNEK FORMALNY. 2.5 dla atomu węgla C C 2.5 H 2.1. Li 1.0. liczba e - walencyjnych w atomie wolnym C 2.5 H 2.
 .5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
.5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Struktura elektronowa powierzchni. Z. Postawa, "Fizyka powierzchni i nanostruktury" 1. Inne metody wytwarzania cienkich warstw
 truktur elektronow powierzchni truktur elektronow powierzchni metody teoretyczne Prc wyjści truktur elektronow i włsności elektryczne powierzchni posoby bdni psm elektronowych - technik UP Cienkie wrstwy
truktur elektronow powierzchni truktur elektronow powierzchni metody teoretyczne Prc wyjści truktur elektronow i włsności elektryczne powierzchni posoby bdni psm elektronowych - technik UP Cienkie wrstwy
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
3. F jest lewostronnie ciągła
 Def. Zmienną losową nzywmy funkcję X: tką, że x R : { : X( ) < x }. Ozn.: zmist pisd A = { : X( ) < x } piszemy A = { X < x } zdrzenie poleg n tym, że X( )
Def. Zmienną losową nzywmy funkcję X: tką, że x R : { : X( ) < x }. Ozn.: zmist pisd A = { : X( ) < x } piszemy A = { X < x } zdrzenie poleg n tym, że X( )
STEREOCHEMIA ORGANICZNA
 STEREOEMIA ORGANINA Sławomir Jarosz Wykład 5 TOPOWOŚĆ Podział grup wg topowości 1. omotopowe (wymienialne operacją symetrii n ) 2. Enancjotopowe (wymienialne przez płaszczyznę σ) 3. Diastereotopowe (niewymienialne
STEREOEMIA ORGANINA Sławomir Jarosz Wykład 5 TOPOWOŚĆ Podział grup wg topowości 1. omotopowe (wymienialne operacją symetrii n ) 2. Enancjotopowe (wymienialne przez płaszczyznę σ) 3. Diastereotopowe (niewymienialne
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Podstawy mechaniki kwantowej. Jak opisać świat w małej skali?
 Podstawy mechaniki kwantowej Jak opisać świat w małej skali? 1 Promieniowanie elektromagnetyczne gamma X ultrafiolet podczerwień mikrofale radiowe widzialne Wavelength in meters 10-1 10-10 10-8 4 x 10-7
Podstawy mechaniki kwantowej Jak opisać świat w małej skali? 1 Promieniowanie elektromagnetyczne gamma X ultrafiolet podczerwień mikrofale radiowe widzialne Wavelength in meters 10-1 10-10 10-8 4 x 10-7
Metody Lagrange a i Hamiltona w Mechanice
 Metody Lgrnge i Hmilton w Mechnice Mriusz Przybycień Wydził Fizyki i Informtyki Stosownej Akdemi Górniczo-Hutnicz Wykłd 3 M. Przybycień (WFiIS AGH) Metody Lgrnge i Hmilton... Wykłd 3 1 / 15 Przestrzeń
Metody Lgrnge i Hmilton w Mechnice Mriusz Przybycień Wydził Fizyki i Informtyki Stosownej Akdemi Górniczo-Hutnicz Wykłd 3 M. Przybycień (WFiIS AGH) Metody Lgrnge i Hmilton... Wykłd 3 1 / 15 Przestrzeń
λ(pm) p 1 rozpraszanie bez zmiany λ ze wzrostem λ p e 0,07 0,08 λ (nm) tł o
 W 1916r. Einstein rozszerzył swoją koncepcję kwantów światła, przypisując im pęd. Fotonowi o energii ħω odpowiada pęd p ħω/c /λ Efekt Comptona 193r. - rozpraszanie promieni X 1keV- kilka MeV na elektronac
W 1916r. Einstein rozszerzył swoją koncepcję kwantów światła, przypisując im pęd. Fotonowi o energii ħω odpowiada pęd p ħω/c /λ Efekt Comptona 193r. - rozpraszanie promieni X 1keV- kilka MeV na elektronac
Teoria VSEPR. Jak przewidywac strukturę cząsteczki?
 Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
ć Ń
 ć Ń ć ź Ł Ń Ń ź Ł Ń Ń Ń Ń ź ź ć Ń ź Ń Ń ź Ś Ś ź Ś Ś Ń Ń Ń Ę Ś Ę ć ź ź Ę Ś ź Ą ź ź Ś Ś Ę ć Ń Ń Ń Ń Ń ć Ń Ń ć Ł Ł Ń Ę Ę ć Ę Ę Ę ź Ą ć Ł Ę Ę Ś ć ć Ę Ł Ę Ż Ą ź Ł Ą ź Ę ź ć Ę Ł Ę ćł Ł Ł Ą ź Ł Ę ź ć Ę Ę
ć Ń ć ź Ł Ń Ń ź Ł Ń Ń Ń Ń ź ź ć Ń ź Ń Ń ź Ś Ś ź Ś Ś Ń Ń Ń Ę Ś Ę ć ź ź Ę Ś ź Ą ź ź Ś Ś Ę ć Ń Ń Ń Ń Ń ć Ń Ń ć Ł Ł Ń Ę Ę ć Ę Ę Ę ź Ą ć Ł Ę Ę Ś ć ć Ę Ł Ę Ż Ą ź Ł Ą ź Ę ź ć Ę Ł Ę ćł Ł Ł Ą ź Ł Ę ź ć Ę Ę
Podstawy mechaniki kwantowej
 Podstawy mechaniki kwantowej Jak opisać świat w małej skali? Czy świat jest realny? 1 Promieniowanie elektromagnetyczne gamma X ultrafiolet podczerwień mikrofale radiowe widzialne Wavelength in meters
Podstawy mechaniki kwantowej Jak opisać świat w małej skali? Czy świat jest realny? 1 Promieniowanie elektromagnetyczne gamma X ultrafiolet podczerwień mikrofale radiowe widzialne Wavelength in meters
Atom ze spinem i jądrem
 Atom ze spinem i jądrem Powtórzenie E 3s 2s 3p 2p 3d Ruch w polu ekranowym znosi degenracje ze wzgledu na l 1s Li l Powtórzenie 5 2 P 3/2 F=I+J 5P F= I-J 5 2 P 1/2 struktura subtelna struktura nadsubtelna
Atom ze spinem i jądrem Powtórzenie E 3s 2s 3p 2p 3d Ruch w polu ekranowym znosi degenracje ze wzgledu na l 1s Li l Powtórzenie 5 2 P 3/2 F=I+J 5P F= I-J 5 2 P 1/2 struktura subtelna struktura nadsubtelna
Przejścia optyczne w cząsteczkach
 Przejścia optyczne w cząsteczkach Jacek.Szczytko@fuw.edu.pl http://www.fuw.edu.pl/~szczytko/nt http://www.sciencecartoonsplus.com/ Podziękowania za pomoc w przygotowaniu zajęć: Prof. dr hab. Paweł Kowalczyk
Przejścia optyczne w cząsteczkach Jacek.Szczytko@fuw.edu.pl http://www.fuw.edu.pl/~szczytko/nt http://www.sciencecartoonsplus.com/ Podziękowania za pomoc w przygotowaniu zajęć: Prof. dr hab. Paweł Kowalczyk
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Podstawy układów logicznych
 Podstwy ukłdów logicznych Prw logiki /9 Alger Boole Prw logiki WyrŜeni i funkcje logiczne Brmki logiczne Alger Boole /9 Alger Boole' Powszechnie stosowne ukłdy cyfrowe (logiczne) prcują w oprciu o tzw.
Podstwy ukłdów logicznych Prw logiki /9 Alger Boole Prw logiki WyrŜeni i funkcje logiczne Brmki logiczne Alger Boole /9 Alger Boole' Powszechnie stosowne ukłdy cyfrowe (logiczne) prcują w oprciu o tzw.
Podstawy mechaniki kwantowej
 Podstawy mechaniki kwantowej Jak opisać świat w małej skali? Czy świat jest realny? Promieniowanie elektromagnetyczne gamma X ultrafiolet podczerwień mikrofale radiowe widzialne Wavelength in meters 0-0
Podstawy mechaniki kwantowej Jak opisać świat w małej skali? Czy świat jest realny? Promieniowanie elektromagnetyczne gamma X ultrafiolet podczerwień mikrofale radiowe widzialne Wavelength in meters 0-0
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Zad Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji.
 Zad. 1.1. Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji. Zad. 1.1.a. Funkcja: ϕ = sin2x Zad. 1.1.b. Funkcja: ϕ = e x 2 2 Operator: f = d2 dx
Zad. 1.1. Sprawdzić, czy dana funkcja jest funkcją własną danego operatora. Jeśli tak, znaleźć wartość własną funkcji. Zad. 1.1.a. Funkcja: ϕ = sin2x Zad. 1.1.b. Funkcja: ϕ = e x 2 2 Operator: f = d2 dx
Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych
 Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych Justyna Cembrzyńska Zakład Mechaniki Kwantowej Uniwersytet
Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych Justyna Cembrzyńska Zakład Mechaniki Kwantowej Uniwersytet
Struktura elektronowa
 Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Modelowanie i obliczenia techniczne. Metody numeryczne w modelowaniu: Różniczkowanie i całkowanie numeryczne
 Modelownie i obliczeni techniczne Metody numeryczne w modelowniu: Różniczkownie i cłkownie numeryczne Pochodn unkcji Pochodn unkcji w punkcie jest deiniown jko grnic ilorzu różnicowego (jeżeli istnieje):
Modelownie i obliczeni techniczne Metody numeryczne w modelowniu: Różniczkownie i cłkownie numeryczne Pochodn unkcji Pochodn unkcji w punkcie jest deiniown jko grnic ilorzu różnicowego (jeżeli istnieje):
Ato wodoropodobny Eektron poruszjący się w kuobowski pou jądr o łdunku +Ze posid energię potencjną: z -e, V ( r) Ze 4πε r + Ze φ θ r y x
 Ato wodoropodobny z współrzędne w ukłdzie krtezjński r sinθ cosφ x r cosθ φ θ r r sinθ (x,y,z) r sinθ sinφ Biegunowy ukłd współrzędnych y funkcj fow współrzędne w ukłdzie biegunowy ( ) r,θ,φ x r sinθ cosφ
Ato wodoropodobny z współrzędne w ukłdzie krtezjński r sinθ cosφ x r cosθ φ θ r r sinθ (x,y,z) r sinθ sinφ Biegunowy ukłd współrzędnych y funkcj fow współrzędne w ukłdzie biegunowy ( ) r,θ,φ x r sinθ cosφ
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Ł ś Ń Ż Ó Ń Ż Ń Ł Ł
 Ł Ł Ł Ń Ń Ó Ł ś Ń Ż Ó Ń Ż Ń Ł Ł Ł Ó Ś Ś ś ść ś ć ć ć ś ś ś ś ś Ń ś ś ś ś ś ć ć źć ś ć ś ć ś ść ś ś ś Ł ś ś Ł ć Ł ś ć ć ć ś ś ćł ź ść ść ć ść ś ś ć Ż ś ś ś ć ś ć ć źć ź Ń ś ś Ł Ń ć ś ść Ł źć ś ś ć ćń ć
Ł Ł Ł Ń Ń Ó Ł ś Ń Ż Ó Ń Ż Ń Ł Ł Ł Ó Ś Ś ś ść ś ć ć ć ś ś ś ś ś Ń ś ś ś ś ś ć ć źć ś ć ś ć ś ść ś ś ś Ł ś ś Ł ć Ł ś ć ć ć ś ś ćł ź ść ść ć ść ś ś ć Ż ś ś ś ć ś ć ć źć ź Ń ś ś Ł Ń ć ś ść Ł źć ś ś ć ćń ć
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
ż ń ź ń Ł ń Ż ż ż ż ż Ż ń ń ń ń ć
 Ó ź ż ń ć Ą ż ń ź ń Ł ń Ż ż ż ż ż Ż ń ń ń ń ć Ó ń Ź ć Ą ć ń ń ż ń ż Ż ż ń ż ń ń ń ń Ź Ż ń Ż ż ń Ż ć ć ż Ś ń Ż ż ń ż Ę ż ń ń ć Ę ż ć ż ć ż ć ż ż ć Ź ć Ż Ó ż ń ń ź Ł ń ć Ó ż Ż ń ń ż ń ż ć ż ń Ź ń ń ń ń ż
Ó ź ż ń ć Ą ż ń ź ń Ł ń Ż ż ż ż ż Ż ń ń ń ń ć Ó ń Ź ć Ą ć ń ń ż ń ż Ż ż ń ż ń ń ń ń Ź Ż ń Ż ż ń Ż ć ć ż Ś ń Ż ż ń ż Ę ż ń ń ć Ę ż ć ż ć ż ć ż ż ć Ź ć Ż Ó ż ń ń ź Ł ń ć Ó ż Ż ń ń ż ń ż ć ż ń Ź ń ń ń ń ż
Atom wodoru. Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu:
 ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
ATOM WODORU Atom wodoru Model klasyczny: nieruchome jądro +p i poruszający się wokół niego elektron e w odległości r; energia potencjalna elektronu: U = 4πε Opis kwantowy: wykorzystując zasadę odpowiedniości
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Morfologia kryształów
 Morfologi krsztłów Morfologi krsztłu Ścin krsztłu = ogrniczjące powierzchnie Zleżą od ksztłtu komorek elementrnch i od fizcznch wrunków wzrostu krsztłu (T, p, otoczenie, roztwór itd.); Krsztł jest wielościnem
Morfologi krsztłów Morfologi krsztłu Ścin krsztłu = ogrniczjące powierzchnie Zleżą od ksztłtu komorek elementrnch i od fizcznch wrunków wzrostu krsztłu (T, p, otoczenie, roztwór itd.); Krsztł jest wielościnem
Diagnostyka plazmy - spektroskopia molekularna. Ewa Pawelec wykład dla pracowni specjalistycznej
 Diagnostyka plazmy - spektroskopia molekularna Ewa Pawelec wykład dla pracowni specjalistycznej Plazma Różne rodzaje plazmy: http://www.ipp.cas.cz/mi/index.html http://www.pro-fusiononline.com/welding/plasma.htm
Diagnostyka plazmy - spektroskopia molekularna Ewa Pawelec wykład dla pracowni specjalistycznej Plazma Różne rodzaje plazmy: http://www.ipp.cas.cz/mi/index.html http://www.pro-fusiononline.com/welding/plasma.htm
< f g = fg. f = e t f = e t. U nas: e t (α 1)t α 2 dt = 0 + (α 1)Γ(α 1)
 Zdnie X,..., X 5 N(6, 5 ) Y,..., Y 6 N(7, 5 ) X N(6, 5 6 ) Ȳ N(7, 5 6 ) Przy złożeniu niezleżności zmiennych mmy: X Ȳ N(, ) po stndryzcji otrzymmy: Ȳ X N(, ) Pr(Ȳ X < ) = Pr(Ȳ X < ) = φ(, 3) = φ(, 3) =,
Zdnie X,..., X 5 N(6, 5 ) Y,..., Y 6 N(7, 5 ) X N(6, 5 6 ) Ȳ N(7, 5 6 ) Przy złożeniu niezleżności zmiennych mmy: X Ȳ N(, ) po stndryzcji otrzymmy: Ȳ X N(, ) Pr(Ȳ X < ) = Pr(Ȳ X < ) = φ(, 3) = φ(, 3) =,
Stara i nowa teoria kwantowa
 Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
1. Przesłanki doświadczalne mechaniki kwantowej.
 1 Pytania egzaminacyjne: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny- interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest liczba wybijanych elektronów
1 Pytania egzaminacyjne: 1. Przesłanki doświadczalne mechaniki kwantowej. 2. Efekt fotoelektryczny- interpretacja Einsteina. 3. Efekt fotoelektryczny: jak skorelowana jest liczba wybijanych elektronów
Analiza matematyczna v.1.6 egzamin mgr inf niestacj 1. x p. , przy założeniu, że istnieją lim
 Anliz mtemtyczn v..6 egzmin mgr inf niestcj Oznczeni: f, g, h : J R funkcje rzeczywiste określone n J R J przedził, b),, b], [, b), [, b], półprost, b),, b],, ), [, ) lub prost R α, β [min{α, β}, m{α,
Anliz mtemtyczn v..6 egzmin mgr inf niestcj Oznczeni: f, g, h : J R funkcje rzeczywiste określone n J R J przedził, b),, b], [, b), [, b], półprost, b),, b],, ), [, ) lub prost R α, β [min{α, β}, m{α,
Ocena dobra. Uczeń: wymienia wszystkie postulaty teorii Daltona opisuje modele Thomsona, Rutherforda oraz Bohra
 Chemia 1 ZP PLAN WYNIKOWY dla szkół ponadgimnazjalnych (fragmenty zapisane kursywą dotyczą celów i treści spoza podstawy programowej) Temat Ocena dopuszczająca. Uczeń: Ocena dostateczna. Uczeń: Dział 1.
Chemia 1 ZP PLAN WYNIKOWY dla szkół ponadgimnazjalnych (fragmenty zapisane kursywą dotyczą celów i treści spoza podstawy programowej) Temat Ocena dopuszczająca. Uczeń: Ocena dostateczna. Uczeń: Dział 1.
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
OGÓLNE PODSTAWY SPEKTROSKOPII
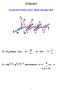 WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
WYKŁAD 8 OGÓLNE PODSTAWY SPEKTROSKOPII E E0 sn( ωt kx) ; k π ; ω πν ; λ T ν E (m c 4 p c ) / E +, dla fotonu m 0 p c p hk Rozkład energ w stane równowag: ROZKŁAD BOLTZMANA!!!!! P(E) e E / kt N E N E/
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki
 OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Równania optyki półklasycznej Posłużymy się teraz równaniem (2.4), i Ψ t = ĤΨ ażeby wyprowadzić
OPTYKA KWANTOWA Wykład dla 5. roku Fizyki c Adam Bechler 2006 Instytut Fizyki Uniwersytetu Szczecińskiego Równania optyki półklasycznej Posłużymy się teraz równaniem (2.4), i Ψ t = ĤΨ ażeby wyprowadzić
Hierarchia baz gaussowskich (5)
 Hierarchia baz gaussowskich (5) Bazy split-valence czyli VDZ, VTZ, etc. (np. bazy Pople a 6-31G, 6-311G, etc) Bazy split-valence spolaryzowane VDZP, VTZP, etc. Bazy bazy Dunninga (konsystentne korelacyjnie)
Hierarchia baz gaussowskich (5) Bazy split-valence czyli VDZ, VTZ, etc. (np. bazy Pople a 6-31G, 6-311G, etc) Bazy split-valence spolaryzowane VDZP, VTZP, etc. Bazy bazy Dunninga (konsystentne korelacyjnie)
SZTUCZNA INTELIGENCJA
 SZTUCZNA INTELIGENCJA WYKŁAD 9. ZBIORY ROZMYTE Częstochow 204 Dr hb. inż. Grzegorz Dudek Wydził Elektryczny Politechnik Częstochowsk ZBIORY ROZMYTE Klsyczne pojęcie zbioru związne jest z logiką dwuwrtościową
SZTUCZNA INTELIGENCJA WYKŁAD 9. ZBIORY ROZMYTE Częstochow 204 Dr hb. inż. Grzegorz Dudek Wydził Elektryczny Politechnik Częstochowsk ZBIORY ROZMYTE Klsyczne pojęcie zbioru związne jest z logiką dwuwrtościową
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab.
 WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
WYKŁAD 2 Podstawy spektroskopii wibracyjnej, model oscylatora harmonicznego i anharmonicznego. Częstość oscylacji a struktura molekuły Prof. dr hab. Halina Abramczyk POLITECHNIKA ŁÓDZKA Wydział Chemiczny
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 2 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 2 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Widmo sodu, serie. p główna s- ostra d rozmyta f -podstawowa
 Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
Zadania. I. Podzielność liczb całkowitych
 Zdni I. Podzielność liczb cłkowitych. Pewn liczb sześciocyfrow kończy się cyfrą 5. Jeśli tę cyfrę przestwimy n miejsce pierwsze ze strony lewej to otrzymmy nową liczbę cztery rzy większą od poprzedniej.
Zdni I. Podzielność liczb cłkowitych. Pewn liczb sześciocyfrow kończy się cyfrą 5. Jeśli tę cyfrę przestwimy n miejsce pierwsze ze strony lewej to otrzymmy nową liczbę cztery rzy większą od poprzedniej.
Podstawy chemii. dr hab. Wacław Makowski. Wykład 1: Wprowadzenie
 Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
zaprezentowana w 1940 roku (Sidgwick i Powell). O budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu
 Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
Mechanika kwantowa. Erwin Schrödinger ( ) Werner Heisenberg
 Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
Mechanika kwantowa Erwin Schrödinger (1887-1961) Werner Heisenberg 1901-1976 Falowe równanie ruchu (uproszczenie: przypadek jednowymiarowy) Dla fotonów Dla cząstek Równanie Schrödingera y x = 1 c y t y(
 Ć Ś Ę Ś ź ź ć ź ń ć ź Ł ź ć ń ć ć ć ź Ś ź ć ć ć ń Ę ń ć ń ĆŚ ź Ę ń ń Ę ń ń ń ź ć ćś Ś ć ń ń Ś ć ćł ć ń Ł ń ć ć ć ć Ę ź ć ź ź Ł ć ź Ę ź ć ć ź ń ć ń Ę ć ć ć ć ć Ę ć ć ć ć ć ć ć ć ć ć ń ń ź ź ń ń Ę ń ń Ś
Ć Ś Ę Ś ź ź ć ź ń ć ź Ł ź ć ń ć ć ć ź Ś ź ć ć ć ń Ę ń ć ń ĆŚ ź Ę ń ń Ę ń ń ń ź ć ćś Ś ć ń ń Ś ć ćł ć ń Ł ń ć ć ć ć Ę ź ć ź ź Ł ć ź Ę ź ć ć ź ń ć ń Ę ć ć ć ć ć Ę ć ć ć ć ć ć ć ć ć ć ń ń ź ź ń ń Ę ń ń Ś
WYMAGANIA EDUKACYJNE Z MATEMATYKI W KLASIE IIc ZAKRES PODSTAWOWY I ROZSZERZONY
 WYMAGANIA EDUKACYJNE Z MATEMATYKI W KLASIE IIc ZAKRES PODSTAWOWY I ROZSZERZONY. JĘZYK MATEMATYKI oblicz wrtość bezwzględną liczby rzeczywistej stosuje interpretcję geometryczną wrtości bezwzględnej liczby
WYMAGANIA EDUKACYJNE Z MATEMATYKI W KLASIE IIc ZAKRES PODSTAWOWY I ROZSZERZONY. JĘZYK MATEMATYKI oblicz wrtość bezwzględną liczby rzeczywistej stosuje interpretcję geometryczną wrtości bezwzględnej liczby
Rachunek prawdopodobieństwa i statystyka matematyczna.
 Rchunek rwdoodobieństw i sttystyk mtemtyczn. Zd 8. {(, : i } Zleżność tą możn rzedstwić w ostci nstęującej interretcji grficznej: Arkdiusz Kwosk Rfł Kukliński Informtyk sem.4 gr. Srwdźmy, czy odne zmienne
Rchunek rwdoodobieństw i sttystyk mtemtyczn. Zd 8. {(, : i } Zleżność tą możn rzedstwić w ostci nstęującej interretcji grficznej: Arkdiusz Kwosk Rfł Kukliński Informtyk sem.4 gr. Srwdźmy, czy odne zmienne
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków).
 Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
2. Obliczyć natężenie pola grawitacyjnego w punkcie A, jeżeli jest ono wytwarzane przez bryłę o masie M, która powstała przez wydrążenie kuli o
 Grwitcj. Obliczyć, jką siłą jest przyciągn s, jeżeli znn jest s plnety orz gęstość i proień drugiej plnety tkże odległości, jk n rysunku. (,, / F ) 5 F G.5.5 7 Sił t jest położon do poziou pod kąte β tki,
Grwitcj. Obliczyć, jką siłą jest przyciągn s, jeżeli znn jest s plnety orz gęstość i proień drugiej plnety tkże odległości, jk n rysunku. (,, / F ) 5 F G.5.5 7 Sił t jest położon do poziou pod kąte β tki,



