Orbitale typu σ i typu π
|
|
|
- Marta Marszałek
- 9 lat temu
- Przeglądów:
Transkrypt
1 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ - orbitale o symetrii osiowej kombinacje orbitali s σ s σ s * kombinacje orbitali p (p z ) σ p σ p *
2 π - orbitale (anty)symetryczne względem płaszczyzny kombinacje orbitali p (p x, p y ) π p π p * kombinacje orbitali d (w kompleksach metali przejściowych) jakie typy orbitali mogą powstać?
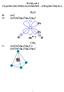
3 Orbitale molekuły C σ* pz π* py π* px σ pz Energie orbitali i obsadzenia elektronami molekuły C (CNDO) π py π px σ* s X Z σ s Y 3
4 Molekuły dwuatomowe homojądrowe orbitale atomu A σ* pz orbitale atomu B π* px π* py p A x,y,z π px π py p B x,y,z σ pz s A σ* s σ s s B s A s B W rzeczywistości oddziaływanie elektronów prowadzi do tego, że σ pz może mieć energię wyższą niż π px i π py (patrz powyżej na schemacie obsadzeń orbitali C oraz poniżej w cząsteczce O ). 4
5 Molekuły dwuatomowe pierwiastków pierwszego i drugiego okresu H + : (σs) E dysocjacji =,79 ev R 0 =,06 Å H : (σs) E dysocjacji =4,75 ev R 0 = 0,73 Å He + : (σs) (σ*s) molekuła trwała He : (σs) (σ*s) molekuła nietrwała Li : (σs) (σ*s) (σs) trwała Be : (σs) (σ*s) (σs) (σ*s) nietrwała (jak hel) B :...(σs) (σ*s) (πp x ) (πp y ) reguła Hunda: paramagnetyzm (C ) N :...(σs) (σ*s) (πp) 4 (σp) wiązanie potrójne O :...(σs) (σ*s) (σp) (πp) 4 (π*p x ) (π*p y ) reguła Hunda: paramagnetyzm 5
6 Hybrydyzacja orbitali atomowych Konfiguracje elektronów w atomach w stanie podstawowym objaśniają tylko część wiązań chemicznych. Np. jak wskazuje doświadczenie, węgiel jest prawie zawsze czterowartościowy chociaż atom węgla ma tylko dwa niesparowane elektrony: (s) (s) (p x ) (p y ) które tworząc parę obsadzającą orbital wiążący mogą z innym atomem utworzyć dwa wiązania. Dla objaśnienia czterowartościowości węgla należy uznać, że jeden elektron s zmienia stan na p: (s) (s) (p x ) (p y ) (p z ) i w rezultacie atom węgla dysponuje czterema elektronami zdolnymi do utworzenia wiązań z elektronami dostarczanymi przez inny atom (inne atomy). Proces ten wymaga energii 4.7 ev, ale jest energetycznie korzystny w całkowitym bilansie energii tworzenia molekuły jeżeli zysk energii po utworzeniu dwu dodatkowych wiązań przewyższa wymagany wkład 4.7 ev. Gdyby atom węgla miał tworzyć wiązania jako rezultat nakrywania orbitali s i p z orbitalami innych atomów (np. s wodoru), to utworzyłby trzy wiązania w prostopadłych kierunkach Ox, Oy, Oz orbitalami p i jedno o nieokreślonym kierunku orbitalem s. Jednak, jeżeli wszystkie cztery wiązane atomy są równoprawne, to należy przyjąć, że węgiel tworzy wiązania nie poprzez czyste orbitale s i p, ale poprzez ich pewne równoprawne kombinacje hybrydy orbitali s i p. 6
7 Obliczenia energii molekuł pokazują, że atom węgla może utworzyć optymalne wiązania z czterema innymi atomami (np. wodoru: CH 4 ) poprzez hybrydowe orbitale o postaci: ψ = ( ϕs + ϕ px + ϕ py ϕ pz ) ψ = ( ϕs + ϕ px ϕ py + ϕ pz ) hybrydy ψ 3 = ( ϕs ϕ px + ϕ py + ϕ pz ) sp 3 ψ 4 = ( ϕs ϕ px ϕ py ϕ pz ) 7
8 Orbitale zhybrydyzowane sp 3 atomu węgla w CH 4 Czarna kropka oznacza położenie jądra atomu węgla. 8
9 metan CH 4 Y hybryda 09.5 Z X s H Podobnie objaśnia się tworzenie wiązań w trzech kierunkach w płaszczyźnie, tworzących kąty po 0. ψ = ϕ + ϕ 3 ( ) s px 6 ψ = ϕ ϕ ϕ 3 + s px py 6 ψ = ϕ ϕ ϕ 3 3 s px py hybrydy sp 0 9
10 Orbital p z pozostaje przy tym niezhybrydyzowany. Jest on prostopadły do płaszczyzny trzech hybryd sp. Z Hybrydy sp tworzą z orbitalami innych atomów wiązania typu σ o symetrii osiowej. Orbital p z jest osiowo symetryczny wokół osi Z i może utworzyć wiązanie typu π w kierunku jednej z hybryd. Przykład: etylen - C H 4 H C C H σ π W etylenie atomy węgla tworzą ze sobą wiązanie podwójne: jedno typu σ i jedno typu π, a z atomami wodoru wiązania σ. Hybrydyzacja sp 0
11 ψ = ϕ + ϕ ψ = ϕs ϕ ( s px ) ( ) px hybrydy sp przekrój orbitali hybrydowych sp atomu węgla Hybrydy sp występują w wiązaniu potrójnym (acetylen C H ). Niezhybrydyzowane orbitale p prostopadłe do osi wyznaczonej przez hybrydy sp tworzą dwa wiązania π. s H s H σ sp Pojedyncze wiązanie σ sp jest uzupełnione dwoma wiązaniami typu π o płaszczyznach symetrii pionowej i poziomej. Zarówno hybrydy jak i niezhybrydyzowane orbitale p mogą tworzyć kombinacje wiążące oraz antywiążące.
12 Orbitale kowalencyjne powstają w rezultacie uwspólnienia jednakowych liczb elektronów od obu atomów tworzących wiązanie. Oprócz orbitali walencyjnych tworzących wiązania z wymianą elektronów, w cząsteczkach istnieją też orbitale obsadzone przez wolne pary elektronowe nie zaangażowane w wiązania kowalencyjne. Wolne pary elektronowe odgrywają ważną rolę w wiązaniach koordynacyjnych i w oddziaływaniach międzycząsteczkowych Struktura powłoki elektronowej przykłady C O C, O hybrydyzacja sp grupa karbonylowa w ketonie H N H H Jaka powinna być struktura NH 4 +? Jaka jest struktura elektronowa salmiaku (NH 4 Cl)? amoniak
13 Przykład: cząsteczka wody H O Atom tlenu ma sześć elektronów walencyjnych. Dwa z nich wraz z dwoma elektronami atomów wodoru obsadzają dwa wiązania O-H typu σ. Pozostałe cztery elektrony atomu tlenu obsadzają parami dwa niewiążące orbitale. σ n σ n Orbitale niewiążące n odgrywają dużą rolę w oddziaływaniach międzycząsteczkowych (wiązania wodorowe) Przykłady: węglowodory nasycone, nienasycone, alkohole, ketony, kwasy, aminy, Przykład: struktura cząsteczki benzenu C 6 H 6 3
14 Struktury diamentu, grafitu i grafenu Kryształ diamentu hybrydyzacja atomów węgla: sp 3 Kryształ grafitu hybrydyzacja atomów węgla: sp 4
15 Podział ładunku elektronów walencyjnych i polaryzacja wiązania Równoprawność atomów w wiązaniach homojądrowych zapewnia równy podział ładunku wiązanie kowalencyjne niespolaryzowane. Wpływ podstawników przy obu atomach może prowadzić do niewielkiej asymetrii wiązanie kowalencyjne spolaryzowane. W wiązaniach atomów różnych pierwiastków o rozkładzie ładunku decyduje elektroujemność pierwiastków. Linus Pauling (93): E Pauling = E A-B (E A-A + E B-B )/ (różnica energii wiązania hetero- i średniej energii wiązań homojądrowych) H:., C:.55, N: 3.04, O: 3.44, F: 4 (maksymalna) Li: 0.98, Na: 0.93, K: 0.8, Rb: 0.8, Cs: 0.79, Fr: 0.7 (minimalna) Atom tego samego pierwiastka może mieć ładunek dodatni lub ujemny w zależności od elektroujemności wiązanych atomów. Różnica elektroujemności (wartości umowne): kowalencyjne niespolaryzowane gdy E < 0.4 kowalencyjne spolaryzowane gdy 0.4 < E <.7 powyżej.7 - wiązanie jonowe Inna skala (zbliżona do skali Paulinga): Allreda-Rochowa - oparta na pojęciu promienia walencyjnego. Skala Mullikena - zmienne wartości elektroujemności zależne od związku chemicznego. Przypadki skrajne: NaCl, KCl, HF, CaCl itp. odpowiadają utworzeniu wiązań silnie spolaryzowanych wiązań jonowych. Polaryzacja wiązań przyczynia się do momentu dipolowego molekuły (lub określonej grupy atomów). Wiązanie metaliczne. 5
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych
 1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Inżynieria Biomedyczna. Wykład XII
 Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
RJC. Wiązania Chemiczne & Slides 1 to 39
 Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Wykład V Wiązanie kowalencyjne. Półprzewodniki
 Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Wiązania jonowe występują w układach złożonych z atomów skrajnie różniących się elektroujemnością.
 105 Elektronowa teoria wiązania chemicznego Cząsteczki powstają w wyniku połączenia się dwóch lub więcej atomów. Już w początkowym okresie rozwoju chemii podejmowano wysiłki zmierzające do wyjaśnienia
105 Elektronowa teoria wiązania chemicznego Cząsteczki powstają w wyniku połączenia się dwóch lub więcej atomów. Już w początkowym okresie rozwoju chemii podejmowano wysiłki zmierzające do wyjaśnienia
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej jedną z dwóch metod (teorii): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
TEORIA ORBITALI MOLEKULARNYCH (MO) dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
Wiązania chemiczne. Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych. 5 typów wiązań
 Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
S. Baran - Podstawy fizyki materii skondensowanej Wiązania chemiczne w ciałach stałych. Wiązania chemiczne w ciałach stałych
 Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Konfiguracja elektronowa atomu
 Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru
 1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Ligand to cząsteczka albo jon, który związany jest z jonem albo atomem centralnym.
 138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
H H 2.5 < H H CH 3 N O O H C N ŁADUNEK FORMALNY. 2.5 dla atomu węgla C C 2.5 H 2.1. Li 1.0. liczba e - walencyjnych w atomie wolnym C 2.5 H 2.
 .5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
.5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Zadanie 2. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach
 Zadanie 1. (2 pkt) Na podstawie budowy powłok elektronowych chloru, azotu i fosforu oraz położenia pierwiastka w układzie okresowym wyjaśnij, dlaczego istnieje PCl 5 a występowanie NCl 5 jest teoretycznie
Zadanie 1. (2 pkt) Na podstawie budowy powłok elektronowych chloru, azotu i fosforu oraz położenia pierwiastka w układzie okresowym wyjaśnij, dlaczego istnieje PCl 5 a występowanie NCl 5 jest teoretycznie
CZ STECZKA. Do opisu wi za chemicznych stosuje si najcz ciej jedn z dwóch metod (teorii): metoda wi za walencyjnych (VB)
 CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
CHEMIA WARTA POZNANIA
 Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Zadanie 1. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach: KBr i HBr.
 Zadanie 1. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach: KBr i HBr. Typ wiązania w KBr... Typ wiązania w HBr... Zadanie 2. (2 pkt) Oceń poprawność poniższych
Zadanie 1. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach: KBr i HBr. Typ wiązania w KBr... Typ wiązania w HBr... Zadanie 2. (2 pkt) Oceń poprawność poniższych
Anna Grych Test z budowy atomu i wiązań chemicznych
 Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne
 Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
Atomy wieloelektronowe i cząsteczki
 Atomy wieloelektronowe i cząsteczki 1 Atomy wieloelektronowe Wodór ma liczbę atomową Z=1 i jest prostym atomem. Zawiera tylko jeden elektron i jeden proton stąd potencjał opisuje oddziaływanie kulombowskie
Atomy wieloelektronowe i cząsteczki 1 Atomy wieloelektronowe Wodór ma liczbę atomową Z=1 i jest prostym atomem. Zawiera tylko jeden elektron i jeden proton stąd potencjał opisuje oddziaływanie kulombowskie
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
pobrano z
 ODPOWIEDZI Zadanie 1. (2 pkt) 1. promienia atomowego, promienia jonowego 2. najwyższego stopnia utlenienia Zadanie 2. (1 pkt) 1. Pierwiastek I jest aktywnym metalem. Tworzy wodorek, w którym wodór przyjmuje
ODPOWIEDZI Zadanie 1. (2 pkt) 1. promienia atomowego, promienia jonowego 2. najwyższego stopnia utlenienia Zadanie 2. (1 pkt) 1. Pierwiastek I jest aktywnym metalem. Tworzy wodorek, w którym wodór przyjmuje
Wykład 16: Atomy wieloelektronowe
 Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
UKŁAD OKRESOWY PIERWIASTKÓW
 UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj.
 Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Wewnętrzna budowa materii - zadania
 Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Jeśli teraz nasz związek, chlorek glinu, ulegnie dysocjacji elektrolitycznej, rozpadnie się na jony według równania:
 Wiązania chemiczne powstają między atomami wówczas, gdy dwa atomy zbliżą się do siebie na tak bliska odległość, że orbital jednego z nich znajdzie się w obrębie orbitala drugiego atomu. Jeśli na każdym
Wiązania chemiczne powstają między atomami wówczas, gdy dwa atomy zbliżą się do siebie na tak bliska odległość, że orbital jednego z nich znajdzie się w obrębie orbitala drugiego atomu. Jeśli na każdym
Wiązania. w świetle teorii kwantów fenomenologicznie
 Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Chemia Grudzień Styczeń
 Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
2. WIĄZANIA CHEMICZNE, BUDOWA CZĄSTECZEK. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu)
 2. WIĄZANIA CHEMICZNE, BUDOWA CZĄSTECZEK Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Wiązania chemiczne Podstawowe stany skupienia materii (w
2. WIĄZANIA CHEMICZNE, BUDOWA CZĄSTECZEK Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Wiązania chemiczne Podstawowe stany skupienia materii (w
Zaliczenie przedmiotu: 17.12.2010 21.01.2011. - ocena pozytywna z ćwiczeń jest warunkiem koniecznym przystąpienia do egzaminu
 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. R. M.Silverstein,. X. Webster,
1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. R. M.Silverstein,. X. Webster,
Zadanie do rozwiązania 1. Dla podanych nuklidów o ogólnym symbolu: E;
 Cz. IV Budowa atomu - konfiguracja elektronowa, przemiany jądrowe, promień jonowy, promień atomowy, jonizacja, hybrydyzacja, moment dipolowy A. Budowa atomu Nuklidy atomy o identycznej budowie jadra atomowego
Cz. IV Budowa atomu - konfiguracja elektronowa, przemiany jądrowe, promień jonowy, promień atomowy, jonizacja, hybrydyzacja, moment dipolowy A. Budowa atomu Nuklidy atomy o identycznej budowie jadra atomowego
Wiązania kowalencyjne
 Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
11) Stan energetyczny elektronu w atomie kwantowanym jest zespołem : a dwóch liczb kwantowych b + czterech liczb kwantowych c nie jest kwantowany
 PYTANIA EGZAMINACYJNE Z CHEMII OGÓLNEJ I Podstawowe pojęcia chemiczne 1) Pierwiastkiem nazywamy : a zbiór atomów o tej samej liczbie masowej b + zbiór atomów o tej samej liczbie atomowej c zbiór atomów
PYTANIA EGZAMINACYJNE Z CHEMII OGÓLNEJ I Podstawowe pojęcia chemiczne 1) Pierwiastkiem nazywamy : a zbiór atomów o tej samej liczbie masowej b + zbiór atomów o tej samej liczbie atomowej c zbiór atomów
E e l kt k r t o r n o ow o a w a s t s r t u r kt k u t ra r a at a o t m o u
 Elektronowa struktura atomu Anna Pietnoczka BUDOWA ATOMU CZĄSTKA SYMBOL WYSTĘPOWANIE MASA ŁADUNEK ELEKTRYCZNY PROTON p + jądroatomowe około 1 u + 1 NEUTRON n 0 jądroatomowe około 1u Brak ELEKTRON e - powłoki
Elektronowa struktura atomu Anna Pietnoczka BUDOWA ATOMU CZĄSTKA SYMBOL WYSTĘPOWANIE MASA ŁADUNEK ELEKTRYCZNY PROTON p + jądroatomowe około 1 u + 1 NEUTRON n 0 jądroatomowe około 1u Brak ELEKTRON e - powłoki
Projekt Era inżyniera pewna lokata na przyszłość jest współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego
 TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Chemia Nieorganiczna I (3.3.PBN.CHE108), konwersatorium Chemia, I stopień, II r., semestr 4. Lista 1.
 Lista 1. 1. Omów dualny charakter elektronów. Podaj i omów fakty za i przeciw falowej naturze.. Co to jest radialna funkcji rozkładu? Podaj wykres tej funkcji dla orbitali 1s, s, 3s, p, 3p i 3d w atomie
Lista 1. 1. Omów dualny charakter elektronów. Podaj i omów fakty za i przeciw falowej naturze.. Co to jest radialna funkcji rozkładu? Podaj wykres tej funkcji dla orbitali 1s, s, 3s, p, 3p i 3d w atomie
Struktura elektronowa
 Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową
 Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową Kryształy Atomy w krysztale ułożone są w pewien powtarzający się regularny wzór zwany siecią krystaliczną. Struktura kryształu NaCl Polikryształy
Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową Kryształy Atomy w krysztale ułożone są w pewien powtarzający się regularny wzór zwany siecią krystaliczną. Struktura kryształu NaCl Polikryształy
CZĄSTECZKI BUDOWA I ODDZIAŁYWANIA
 CZĄSTECZKI BUDOWA I ODDZIAŁYWANIA 2.1. Długość cząsteczki wody jest w przybliżeniu równa 3 10 10 m. Łańcuch utworzony z cząsteczek wody zawartych w jednej szklance (ok. 180 g) miałby orientacyjnie długość
CZĄSTECZKI BUDOWA I ODDZIAŁYWANIA 2.1. Długość cząsteczki wody jest w przybliżeniu równa 3 10 10 m. Łańcuch utworzony z cząsteczek wody zawartych w jednej szklance (ok. 180 g) miałby orientacyjnie długość
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
2
 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 ZADANIA I PROBLEMY 1). Chlor naturalny jest mieszaniną dwóch izotopów o liczbach masowych 35 i 37, a eksperymentalnie wyznaczona masa atomowa chloru wynosi
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 ZADANIA I PROBLEMY 1). Chlor naturalny jest mieszaniną dwóch izotopów o liczbach masowych 35 i 37, a eksperymentalnie wyznaczona masa atomowa chloru wynosi
Podstawy chemii. dr hab. Wacław Makowski. Wykład 1: Wprowadzenie
 Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Propozycje metod godzin. (fragmenty zapisane kursywą dotyczą. podręcznik teoria budowy atomu. łączenie nazwisk uczonych z ich teoriami
 Chemia 1 ZP Roczny plan dydaktyczny dla szkół ponadgimnazjalnych Temat Liczba Treści podstawy Cele ogólne Kształcone Propozycje metod Propozycje środków godzin programowej (fragmenty zapisane kursywą dotyczą
Chemia 1 ZP Roczny plan dydaktyczny dla szkół ponadgimnazjalnych Temat Liczba Treści podstawy Cele ogólne Kształcone Propozycje metod Propozycje środków godzin programowej (fragmenty zapisane kursywą dotyczą
Modelowanie zjawisk fizycznych (struktury molekularnej, procesów chemicznych i układów biologicznych)
 Modelowanie zjawisk fizycznych (struktury molekularnej, procesów chemicznych i układów biologicznych) Dr inż. Marta Łabuda Politechnika Gdańska Katedra Fizyki Teoretycznej i Informatyki Kwantowej p. 409
Modelowanie zjawisk fizycznych (struktury molekularnej, procesów chemicznych i układów biologicznych) Dr inż. Marta Łabuda Politechnika Gdańska Katedra Fizyki Teoretycznej i Informatyki Kwantowej p. 409
Wewnętrzna budowa materii
 Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Ocena dobra. Uczeń: wymienia wszystkie postulaty teorii Daltona opisuje modele Thomsona, Rutherforda oraz Bohra
 Chemia 1 ZP PLAN WYNIKOWY dla szkół ponadgimnazjalnych (fragmenty zapisane kursywą dotyczą celów i treści spoza podstawy programowej) Temat Ocena dopuszczająca. Uczeń: Ocena dostateczna. Uczeń: Dział 1.
Chemia 1 ZP PLAN WYNIKOWY dla szkół ponadgimnazjalnych (fragmenty zapisane kursywą dotyczą celów i treści spoza podstawy programowej) Temat Ocena dopuszczająca. Uczeń: Ocena dostateczna. Uczeń: Dział 1.
Zadanie 1. (1 pkt). Informacja do zada 2. i 3. Zadanie 2. (1 pkt) { Zadania 2., 3. i 4 s dla poziomu rozszerzonego} zania zania Zadanie 3.
 2. ELEKTRONY W ATOMACH I CZĄSTECZKACH. A1 - POZIOM PODSTAWOWY. Zadanie 1. (1 pkt). Konfigurację elektronową 1s 2 2s 2 2p 6 3s 2 3p 6 mają atomy i jony: A. Mg 2+, Cl -, K +, B. Ar, S 2-, K +, C. Ar, Na
2. ELEKTRONY W ATOMACH I CZĄSTECZKACH. A1 - POZIOM PODSTAWOWY. Zadanie 1. (1 pkt). Konfigurację elektronową 1s 2 2s 2 2p 6 3s 2 3p 6 mają atomy i jony: A. Mg 2+, Cl -, K +, B. Ar, S 2-, K +, C. Ar, Na
Okresowość właściwości chemicznych pierwiastków. Układ okresowy pierwiastków. 1. Konfiguracje elektronowe pierwiastków
 Układ okresowy pierwiastków Okresowość właściwości chemicznych pierwiastków 1. Konfiguracje elektronowe pierwiastków. Konfiguracje a układ okresowy 3. Budowa układu okresowego 4. Historyczny rozwój układu
Układ okresowy pierwiastków Okresowość właściwości chemicznych pierwiastków 1. Konfiguracje elektronowe pierwiastków. Konfiguracje a układ okresowy 3. Budowa układu okresowego 4. Historyczny rozwój układu
26 Okresowy układ pierwiastków
 26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
Dlaczego sacharoza (cukier trzcinowy) topi się w temperaturze 185 C, podczas
 1 Wiązania chemiczne i zjawisko izomerii Dlaczego sacharoza (cukier trzcinowy) topi się w temperaturze 185 C, podczas gdy chlorek sodowy (sól kuchenna) topi się w znacznie wyższej temperaturze, bo w 801
1 Wiązania chemiczne i zjawisko izomerii Dlaczego sacharoza (cukier trzcinowy) topi się w temperaturze 185 C, podczas gdy chlorek sodowy (sól kuchenna) topi się w znacznie wyższej temperaturze, bo w 801
b) Pierwiastek E tworzy tlenek o wzorze EO 2 i wodorek typu EH 4, a elektrony w jego atomie rozmieszczone są na dwóch powłokach elektronowych
 1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Teoria VSEPR. Jak przewidywac strukturę cząsteczki?
 Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Materiały dodatkowe do zajęć z chemii dla studentów
 Materiały dodatkowe do zajęć z chemii dla studentów Opracowała dr Anna Wisła-Świder UKŁAD OKRESOWY PIERWIASTKÓW Układ okresowy pierwiastków to tablica składająca się z poziomych okresów i pionowych grup.
Materiały dodatkowe do zajęć z chemii dla studentów Opracowała dr Anna Wisła-Świder UKŁAD OKRESOWY PIERWIASTKÓW Układ okresowy pierwiastków to tablica składająca się z poziomych okresów i pionowych grup.
Elektroujemność w konwencji Sandersona. mgr Magdalena Chrzan
 Elektroujemność w konwencji Sandersona mgr Magdalena Chrzan Elektroujemność Siła atomu w cząsteczce do przyciągania elektronów do siebie. Pauling 1932, 1960 Zdolność atomu do przyciągania gęstości elektronowej
Elektroujemność w konwencji Sandersona mgr Magdalena Chrzan Elektroujemność Siła atomu w cząsteczce do przyciągania elektronów do siebie. Pauling 1932, 1960 Zdolność atomu do przyciągania gęstości elektronowej
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Temat 1: Budowa atomu zadania
 Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
CHEMIA OGÓLNA (wykład)
 AKADEMIA GÓRNICZO HUTNICZA WYDZIAŁ ENERGETYKI I PALIW I r. EiP (Technologia Chemiczna) CHEMIA OGÓLNA (wykład) Prof. dr hab. Leszek CZEPIRSKI Kontakt: A4 IV p., p. 424 Tel. 12 617 46 36 email: czepir@agh.edu.pl
AKADEMIA GÓRNICZO HUTNICZA WYDZIAŁ ENERGETYKI I PALIW I r. EiP (Technologia Chemiczna) CHEMIA OGÓLNA (wykład) Prof. dr hab. Leszek CZEPIRSKI Kontakt: A4 IV p., p. 424 Tel. 12 617 46 36 email: czepir@agh.edu.pl
