Inżynieria Biomedyczna. Wykład XII
|
|
|
- Teodor Mucha
- 8 lat temu
- Przeglądów:
Transkrypt
1 Inżynieria Biomedyczna Wykład XII
2 Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja 2
3 DEFINICJE CZĄSTECZKA- układ co najmniej dwóch atomów połączonych wiązaniem (wiązaniami) chemicznymi WIĄZANIE CHEMICZNE- oddziaływanie pomiędzy atomami prowadzące do powstawania sił o charakterze przyciągającym, które są wynikiem zmian struktury elektronowej układu atomów tworzących cząsteczkę 3
4 DEFINICJE REAKCJE CHEMICZNE- procesy, w wyniku których dochodzi do zrywania i/lub tworzenia wiązań chemicznych WIĄZANIE CHEMICZNE powstaje, jeżeli energia utworzonej cząsteczki jest mniejsza od sumy energii oddzielnych atomów 4
5 Dlaczego tworzą się wiązania chemiczne? Cząsteczka składa się przynajmniej z 2 atomów Co oznacza, że mamy co najmniej 2 jadra atomowe oraz 2 elektrony Oddziaływanie pomiędzy atomami: JĄDRO-JĄDRO JĄDRO-ELEKTRON ELEKTRO-ELEKTRON ODPYCHANIE PRZYCIĄGANIE ODPYCHANIE Energia całego układu ulega obniżeniu (zmniejsza się odpychanie) jeżeli elektrony będą się znajdować pomiędzy jądrami STANY ENERGETYCZNE elektronów w cząsteczce, odpowiadają niższym energiom niż w izolowanych atomach 5
6 Energia wiązania a odległość pomiędzy atomami ENERGIA POTENCJALNA Długość wiązania Odległość między atomami 6
7 WIĄZANIE CHEMICZNE-koncepcja Lewisa WIĄZANIE JONOWE: ELEKTROSTATYCZNE PRZYCIĄGANIE KATIONÓW i ANIONÓW ne - A B A n+ B n- 7
8 Wiązanie jonowe cd Symbol Lewisa składa się z symbolu pierwiastka oraz kropek (elektrony walencyjne) Pojedyncza kropka - samotny elektron Para kropek-dwa sparowane elektrony w orbitalu W wyniku przeniesienia elektronu powstałe jony uzyskują szczególnie trwałą konfiguracji gazu szlachetnego REGUŁA OKTETU 8
9 Teoria Lewisa wiązania kowalencyjnego Każdy atom cząsteczki przyłącza elektrony, aż osiągnie konfigurację oktetu, odpowiadającą najbliższemu w układzie okresowym atomowi helowca (wyjątek wodór)
10 Przykłady: Pary wiążące Wolna para elektronowa 12
11 Struktury jonowo-kowalencyjne 13
12 Struktury rezonansowe Elektrony w strukturach rezonansowych są ZDELOKALIZOWANE Dodatkowa gęstość elektronowa, związana z drugą parą elektronów w wiązaniu podwójnym, obejmuje kilka atomów 14
13 Współczesne teorie wiązań chemicznych Metoda wiązań walencyjnych: Valency Bond -VB Metoda orbitali molekularnych: Molecular Orbitals- MO Założenia dla obu metod są podobne, różnica występuje w sposobie dokonywania obliczeń: Zachowanie elektronu ( z osobna ) w cząsteczce opisuje spinorbital molekularny (przybliżenie jednoelektronowe) Funkcja falowa całego układu jest iloczynem tych funkcji Tak jak w przypadku atomów, dwa SPINORBITALE składają się na jeden ORBITAL MOLEKULARNY odpowiadający dwóm elektronom, różniących się spinem, o bardzo podobnym zachowaniu 15
14 Metoda orbitali molekularnych - MO W tworzeniu orbitalu molekularnego praktyczny udział biorą tylko orbitale atomowe należące do elektronów walencyjnych wchodzących w wiązanie atomów. W TEORII ORBITALI MOLEKULARNYCH przyjmujemy, że prawdziwy orbital molekularny Y M można przybliżyć: LINIOWĄ KOMBINACJĄ ATOMOWYCH ORBITALI ELEKTRONÓW WALENCYJNYCH f 1, f 2, f 3,... f n atomów tworzących cząsteczkę: Y m = c 1 f 1 + c 2 f 2 + c 3 f c n f n LCAO-Linear Combination of Atomic Orbitals 16
15 Kiedy stosowanie metody LCAO ma sens? Muszą być spełnione trzy warunki: 1. E A E B, energie obu orbitali atomowych są zbliżone (ale nie muszą być identyczne) 2. Symetria obu orbitali atomowych względem osi wiązania jest identyczna 3. Zachodzi efektywne nakładanie się orbitali (czyli obszarów o niezerowym prawdopodobieństwie napotkania elektronu). 17
16 Jak wyrazić w teorii LCAO przybliżoną postać orbitalu molekularnego cząsteczki NO? konfiguracje elektronowe atomów: N: 1s 2 2s 2 p 3 O: 1s 2 2s 2 p 4 Y NO =c 1 (2s) N + c 2 (2p x ) N + c 3 (2p y ) N + c 4 (2p z ) N + + c 5 (2s) O + c 6 (2p x ) O + c 7 (2p y ) O + c 8 (2p z ) O Orbitale atomowe f i są funkcjami, których postać jest znana, aby znaleźć postać orbitalu molekularnego Y MO należy wyznaczyć wartości współczynników c i Liczba wynikowych kombinacji (orbitali molekularnych) jest zawsze równa liczbie "wyjściowych" orbitali atomowych (takie są reguły tworzenia kombinacji) 18 Każdemu zestawowi współczynników odpowiada wartość energii
17 Zaczynamy od cząsteczki wodoru H 2 dwa zbliżające się atomy H H H oś wiązania Struktura elektronowa atomów H: 1s 1 Przybliżone wyrażenie orbitalu molekularnego Y H2 dla cząsteczki H 2 : Y H2 = c 1 (1s) H-1 + c 2 (1s) H-2 Pamiętamy: liczba współczynników c i = liczba zestawów współczynników c i Czyli otrzymujemy 2 rozwiązania: Y I H2 = c I 1(1s) H-1 + c I 2(1s) H-2 19 Y II H2 = c II 1(1s) H-1 + c II 2(1s) H-2
18 Cząsteczką wodoru H 2 (cd) E Każdemu z tych rozwiązań odpowiada inna wartość energii dla elektronów w cząsteczce wodoru Diagram orbitali dla H 2 : E II II Ψ * σ 1s 1s DE 2 1s DE 1 E I I Ψ σ 1s 20 DE 2 > DE 1 Konfiguracja H 2 : σ1s 2
19 Orbitale wiążące i antywiążące ENERGIA Z dwóch orbitali atomowych powstają dwa orbitale molekularne Y MO i Y * MO o różnej energii orbitale atomowe orbitale molekularne antywiążący Y * MO wiążący Y MO 21
20 Orbitale molekularne typu Dla orbitalu molekularnego typu maksymalne prawdopodobieństwo znalezienia elektronów występuje w obszarze zawierającym oś wiązania Orbitale atomowe Orbitale molekularne 1s antywiążący Oś wiązania 1s 1s 1s wiążący 22
21 Czy istnieje cząsteczka He 2? Struktura elektronowa atomów He: 1s 2 Przybliżone wyrażenie orbitalu molekularnego Y H2 dla cząsteczki H 2 : Y He2 = c 1 (1s) He-1 + c 2 (1s) He-2 E E II II Ψ He2 * σ 1s 1s 2 1s 2 E I I Ψ He2 σ 1s Konfiguracja He 2 : σ 1s2 σ* 1s 2 - nie istnieje 23
22 a cząsteczka He + 2? He: 1s 2 * σ 1s He +: 1s σ 1s Konfiguracja He + 2: σ1s 2 σ*1s 1 - istnieje 24
23 Cząsteczka tlenu O 2 Konfiguracja elektronowa O: 1s 2 2s 2 p 4 przybliżona postać orbitalu molekularnego: Y O2 = c 1 (2s) O-1 + c 2 (2p x ) O-1 + c 3 (2p y ) O-1 + c 4 (2p z ) O c 5 (2s) O-2 + c 6 (2p x ) O-2 + c 7 (2p y ) O-2 +c 8 (2p z ) O-2 tak więc otrzymamy 8 zestawów współczynników c i, 8 orbitali molekularnych Oddziaływanie orbitali 2s i 2p x zachodzi w obszarze osi wiązania w przeciwieństwie do oddziaływania orbitali 2p y, 2p z, 25
24 Orbitale typu Jeżeli oddziaływanie orbitali atomowych zachodzi w obszarze poza osią wiązania to powstają orbitale molekularne typu Dla orbitalu molekularnego maksymalne prawdopodobieństwo napotkania elektronów znajduje się poza obszarem zawierającym oś wiązania Oś wiązania Orbitale atomowe Orbitale molekularne 2p antywiążący 2p wiążący 26 2p z 2p z
25 Klasyfikacja ortbitali molekularnych cd * 2p 2p * 2p 2p * 2p 2p 27
26 Wracamy do cząsteczki O 2 O 2 σ 2s2 σ * 2s 2 σ 2p2 π 2p2 π 2p2 π * 2p 1 π * 2p 1 O: 1s 2 2s 2 p 4 O: 1s 2 2s 2 p 4 σ * 2px π * 2py π * 2pz x y z z y x π 2py π 2pz σ 2px σ * 2s 2s 2s 28 σ 2s
27 Rząd wiązania R.W. R.W.=½(liczba elektronów na orbitalach molekularnych wiążących liczba elektronów na orbitalach molekularnych antywiążących) Przykłady dla H 2 R.W.= ½(2-0)=1 wiązanie pojedyncze dla He 2 R.W.= ½(2-2)=0 brak wiązania dla He + 2 R.W.= ½(2-1)= ½ wiązanie 1-elektronowe dla O 2 R.W.= ½(8-4)=2 wiązanie podwójne dla N 2 R.W.= ½(8-2)=3 wiązanie potrójne Rząd wiązania R.W. może przyjmować wartości niecałkowite, zawarte pomiędzy 0 i 1, 1 i 2 oraz 2 i 3. Im wyższy rząd wiązania pomiędzy dwoma atomami, tym długość wiązania krótsza a wiązanie jest silniejsze. Długość wiązania = odległość pomiędzy jadrami atomowymi 29 Jeżeli R.W. > 0 to znaczy, że energia elektronów w cząsteczce jest niższa niż energia elektronów w atomach, z których cząsteczka powstała.
28 Wracamy do cząsteczki O 2 O 2 σ 2s2 σ * 2s 2 σ 2p2 π 2p2 π 2p2 π * 2p 1 π * 2p 1 O: 1s 2 2s 2 p 4 O: 1s 2 2s 2 p 4 σ * 2px π * 2py π * 2pz x y z z y x π 2py π 2pz σ 2px σ * 2s 2s 2s 30 σ 2s
29 Dwuatomowe homojądrowe cząsteczki II-go okresu Cząsteczki O 2 i F 2 Cząsteczki od B 2 do N 2 * 2p * 2p 2p * 2p 2p 2p * 2p 2p 2p 2p 2p 2p 2s * 2s 2s 2s * 2s 2s 2s 2s 31
30 B 2 C 2 N 2 O 2 F 2 * (2p) * (2p) * (2p) (2p) (2p) * (2p) (2p) * (2s) (2p) (2s) * (2s) 32 (2s)
31 Para i diamagnetyki 33
32 Dwuatomowe cząsteczki heterojądrowe Postać diagramu orbitali dwuatomowych cząsteczek heterojądrowych zależy od faktu posiadania przez atomy tworzące te cząsteczki orbitali tego samego typu. CZĄSTECZKA CO: C: He2s 2 2p 2 O: He2s 2 2p 4 CZĄSTECZKA HF: H: 1s 1 F: He2s 2 2p 5 Diagram orbitalowy podobny do opisanego dla cząsteczek homojądrowych Diagram orbitalowy różny od opisanego dla cząsteczek homojądrowych 34
33 Dwuatomowe cząsteczki heterojądrowe (CO)... kolejność energii orbitali we wszystkich atomach wieloelektronowych jest taka sama, ale taki sam orbital (n,l) w różnych atomach ma różne energie... C * σ 2px C: [He] 2s 2 p 2 O: [He] 2s 2 p 4 O 2p * π 2py * π 2pz 2p π 2py π 2pz 2s * 2s σ 2px 35 2s 2s
34 Cząsteczka HF E F * σ1s 2px HF F: [He]2s 2 2p 5 H: 1s H 1s 2py F 2pz F 3.8 ev 2p σ1s 2px orbitale niewiążące 2s 2s F 36
35 Przesunięcie ładunku wiązania udział orbitalu atomowego 2p x fluoru w orbitalu molekularnym jest większy niż udział orbitalu 1s wodoru prawdopodobieństwo znalezienia elektronów w pobliżu jądra F jest większe niż w pobliżu jądra H ładunek (ujemny) wiązania jest przesunięty w stronę fluoru ORBITAL MOLEKULARNY NIE JEST SYMETRYCZNY! A +δ B -δ 37 δ - wielkość przemieszczonego ładunku (0,e); δ = 0 ładunek jest symetryczny - wiązanie ma charakter kowalencyjny; δ = e przeniesienie ładunku (elektronu) od A do B, wiązanie jonowe
36 Moment dipolowy δ δ - l WIĄZANIE JONOWE μ = δ l moment dipolowy jest tym większy, im większy jest przemieszczony ładunek oraz im większa jest odległość przesunięcia 38 jeśli δ = e, to μ jest maksymalne dla stałej wartości l, WIĄZANIE KOWALENCYJNE δ = 0 μ = 0 Dla częściowego przesunięcia ładunku μ 100 e l procentowy udział charakteru jonowego w wiązaniu... takie wiązanie nazywa się wiązaniem atomowym (kowalencyjnym) spolaryzowanym...
37 Elektroujemność Elektroujemność jest to miara tendencji do przyciągania elektronów w wiązaniu (Mullikan 1935) E ~ I + P e I - pierwsza energia jonizacji P e - powinowactwo elektronowe Względna skala elektroujemności pozwala określić, który z atomów tworzących wiązanie będzie silniej przyciągać wspólne elektrony Wszystkie skale opierają się na własnościach pierwiastków, a przede wszystkim własnościach tworzonych przez nie wiązań: Najbardziej znane skale: - Mullikana - Paulinga - Alfreda - Rochowa - Görlicha... 39
38 Skala elektroujemności Paulinga 40
39 Charakter wiązania Różnica elektroujemności pierwiastków tworzących wiązanie określa jego charakter Wiązanie jonowe Udział wiązania jonowego w % Wiązanie kowalencyjne Różnica elektroujemności 41
40 Charakter wiązania F 2 3,0-3,0 = 0 wiązanie kowalencyjne CsF 4,0-0,7 = 3,3 wiązanie jonowe HCl 3,2-2,2 = 1,0 wiązanie atomowe spolaryzowane H 2 O 3,5-2,2 = 1,3 wiązanie atomowe spolaryzowane 42
41 Kierunkowość wiązań Struktura cząsteczek: Cząsteczki dwuatomowe struktura liniowa Cząsteczki trójatomowe struktura liniowa lub kątowa Cząsteczki o więcej niż trzech atomach - struktura może być trójwymiarowa Wiązania chemiczne tworzą się w tych kierunkach przestrzeni, w których prawdopodobieństwo napotkania elektronów jest duże Struktura geometryczna cząsteczki jest więc wynikiem rozkładu prawdopodobieństwa napotkania elektronów w przestrzeni wokół jąder atomów, które tworzą cząsteczkę
42 Kierunkowość wiązań cd Cząsteczka BeH 2 ma strukturę liniową H Be H Stan podstawowy H: 1s 1 Be: He2s 2 p 0 Jeżeli energie dwóch bliskich poziomów, np. 2s i 2p są podobne, to elektrony mogą być "promowane" (czyli wzbudzone) w dość niskiej temperaturze Stan wzbudzony Be: He2s 1 p 1 2s 2p
43 Cząsteczka BeH 2 cd Atomy wodoru wnoszą do kombinacji liniowej Y BeH2 takie same orbitale typu 1s, natomiast beryl orbital 2s i 2p Powinny więc powstać 2 różne orbitale wiążące typu ( s i s-p ) oraz 2 antywiążące Z danych eksperymentalnych wynika że długość wiązań w cząsteczce BeH 2 JEST TAKA SAMA Co oznacza ze oba wiązania są równocenne (charakteryzują się taka samą energią) Hybrydyzacja czyli mieszanie orbitali atomowych
44 Hybrydyzacja Hybrydyzacja - przekształcenie orbitali, polegające na zmieszaniu" dwóch lub więcej orbitali atomowych, na skutek czego powstają nowe orbitale, posiadające inny kształt i energię. Hybrydyzacja jest operacją matematyczną ułatwiającą skonstruowanie orbitali wchodzących w skład kombinacji liniowych (orbitali molekularnych)
45 Reguły hybrydyzacji tworzymy kombinację liniową orbitali ("atomu centralnego") o takiej samej lub zbliżonej energii; liczba hybrydów jest równa liczbie wziętych do kombinacji O.A., których jednakowy udział w kombinacji bierzemy pod uwagę; efektem kombinacji są hybrydy o jednakowych funkcjach radialnych, a funkcje kątowe różnią się tylko kierunkiem (mają jednakowy kształt); przy udziale orbitali zhybrydyzowanych tworzą się wyłącznie orbitale cząsteczkowe (wiązania) typu σ; jedno wiązanie chemiczne tworzy się przy udziale kilku orbitali jednego z atomów... wiązania mają charakter skierowany w pewnym określonym kierunku w przestrzeni
46 Kierunkowość wiązań cd Cząsteczka BeH 2 ma strukturę liniową H Be H Stan podstawowy H: 1s 1 Be: He2s 2 p 0 Jeżeli energie dwóch bliskich poziomów, np. 2s i 2p są podobne, to elektrony mogą być "promowane" (czyli wzbudzone) w dość niskiej temperaturze Stan wzbudzony Be: He2s 1 p 1 2s 2p
47 Cząsteczka BeH 2 -hybrydyzacja sp Powstają dwie jednakowe hybrydy, leżące na osi x skierowane względem siebie pod kątem 180º - można je wykorzystać w kombinacji liniowej do utworzenia wiązań z innymi atomami... promowany Be H H 1 2 H H
48 hybrydyzacja sp - liniowa (dygonalna) Udział biorą orbitale: 1 orbital typu s i 1 orbiral typu p Wynikiem hybrydyzacji są 2 orbitale zhybrydyzowane o symetrii Hybrydyzacja liniowa występuję w cząsteczkach BeCl 2, BeH 2, CO 2
49 Hybrydyzacja sp 2 (dla BF 3 ) B: 1s 2 2s 2 p 1, F: 1s 2 2s 2 p 5, Trzy hybrydy utworzone przez orbitale 2s, 2px i 2py atomu boru tworzą wiązania z trzema orbitalami 2px fluoru. Elektrony orbitali 2s oraz 2py i 2pz atomów fluoru, prostopadłych do płaszczyzny xy lub osi wiązania nie biorą udziału w wiązaniu B-F. F F F o 120 o 120 o Cząsteczka BF 3 jest trójkątna i płaska
50 Hybrydyzacja sp 3 (dla CH 4 ) C: 1s 2 2s 2 2p 2 H: 1s 1 H H H H Powstają cztery jednakowe hybrydy, skierowane ku narożom czworościanu foremnego (tetraedru) - można je wykorzystać w kombinacji liniowej do utworzenia wiązań z innymi atomami...
51 Hybrydyzacja sp 3 Przyjmując hybrydyzację sp 3 można również wyjaśnić kształt cząsteczek amoniaku NH 3. Hybrydyzacji ulegają orbitale atomów N. NH 3 N:1s 2 2s 2 p 3 H:1s 1 wolne elektrony H H H 1 2 3
52 Hybrydyzacja sp 3 Przyjmując hybrydyzację sp 3 można również wyjaśnić kształt cząsteczek amoniaku NH 3. Hybrydyzacji ulegają orbitale atomów N. NH 3 N:1s 2 2s 2 p 3 H:1s 1 wolne elektrony H H H 1 2 3
53 Hybrydyzacja sp 3 W przypadku cząsteczki H 2 O hybrydyzacji ulegają orbitale atomów O. H 2 O O:1s 2 2s 2 p 4, H:1s 1 wolne elektrony H H 1 2
54
55 Hybrydyzacja cd Hybrydyzacja dsp 3 - bipiramida trygonalna Przykładem zastosowania hybrydyzacji dsp3 (sp3d) jest wytłumaczenie kształtu cząsteczki PCl 5. Orbitale zhybrydyzowane tworzą pięć orbitali typu σ z orbitalami 2px atomów chloru. Elektrony orbitali 2s, 2py i 2pz atomów chloru nie biorą udziału we wiązaniu (tworzeniu orbitali cząsteczkowych. Hybrydyzacja d 2 sp 3 - oktaedryczna Przykładem zastosowania hybrydyzacji d 2 sp 3 (sp 3 d 2 ) jest wytłumaczenie kształtu cząsteczki SF6, powstaje sześć orbitali zhybrydyzowanych, z których tworzy się sześć orbitali molekularnych
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych
 1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas II LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
zaprezentowana w 1940 roku (Sidgwick i Powell). O budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu
 Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
Teoria VSEPR (Valence Shell Electron Pair Repulsion) zaprezentowana w 1940 roku (Sidgwick i Powell). budowie przestrzennej cząsteczki decyduje łączna liczba elektronów walencyjnych wokół atomu centralnego
TEORIA ORBITALI MOLEKULARNYCH (MO) dr Henryk Myszka - Uniwersytet Gdański - Wydział Chemii
 TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
TERIA RBITALI MLEKULARNYCH (M) Metoda (teoria) orbitali molekularnych (M) podstawy metody M - F. Hund, R.S. Mulliken Teoria M zakłada, że zachowanie się elektronu w cząsteczce opisuje orbital molekularny
RJC. Wiązania Chemiczne & Slides 1 to 39
 Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Ligand to cząsteczka albo jon, który związany jest z jonem albo atomem centralnym.
 138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
H H 2.5 < H H CH 3 N O O H C N ŁADUNEK FORMALNY. 2.5 dla atomu węgla C C 2.5 H 2.1. Li 1.0. liczba e - walencyjnych w atomie wolnym C 2.5 H 2.
 .5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
.5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania
 Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Cz. I Materiał powtórzeniowy do sprawdzianu dla klas I LO - Wiązania chemiczne + przykładowe zadania i proponowane rozwiązania I. Elektroujemność pierwiastków i elektronowa teoria wiązań Lewisa-Kossela
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru
 1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
1. Określ liczbę wiązań σ i π w cząsteczkach: wody, amoniaku i chloru 2. Na podstawie struktury cząsteczek wyjaśnij dlaczego N 2 jest bierny a Cl 2 aktywny chemicznie? 3. Które substancje posiadają budowę
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Wiązania jonowe występują w układach złożonych z atomów skrajnie różniących się elektroujemnością.
 105 Elektronowa teoria wiązania chemicznego Cząsteczki powstają w wyniku połączenia się dwóch lub więcej atomów. Już w początkowym okresie rozwoju chemii podejmowano wysiłki zmierzające do wyjaśnienia
105 Elektronowa teoria wiązania chemicznego Cząsteczki powstają w wyniku połączenia się dwóch lub więcej atomów. Już w początkowym okresie rozwoju chemii podejmowano wysiłki zmierzające do wyjaśnienia
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.2. BUDOWA CZĄSTECZEK Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja Kopernika
Wykład V Wiązanie kowalencyjne. Półprzewodniki
 Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
Wykład V Wiązanie kowalencyjne. Półprzewodniki Wiązanie kowalencyjne molekuła H 2 Tworzenie wiązania kowalencyjnego w molekule H 2 : elektron w jednym atomie przyciągany jest przez jądro drugiego. Wiązanie
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
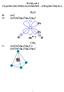 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej jedną z dwóch metod (teorii): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CHEMIA WARTA POZNANIA
 Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Wiązania kowalencyjne
 Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
STEREOCHEMIA ORGANICZNA
 STEREOEMIA ORGANINA Sławomir Jarosz Wykład 5 TOPOWOŚĆ Podział grup wg topowości 1. omotopowe (wymienialne operacją symetrii n ) 2. Enancjotopowe (wymienialne przez płaszczyznę σ) 3. Diastereotopowe (niewymienialne
STEREOEMIA ORGANINA Sławomir Jarosz Wykład 5 TOPOWOŚĆ Podział grup wg topowości 1. omotopowe (wymienialne operacją symetrii n ) 2. Enancjotopowe (wymienialne przez płaszczyznę σ) 3. Diastereotopowe (niewymienialne
Zaliczenie przedmiotu: 17.12.2010 21.01.2011. - ocena pozytywna z ćwiczeń jest warunkiem koniecznym przystąpienia do egzaminu
 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. R. M.Silverstein,. X. Webster,
1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 4. R. M.Silverstein,. X. Webster,
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Zadanie 2. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach
 Zadanie 1. (2 pkt) Na podstawie budowy powłok elektronowych chloru, azotu i fosforu oraz położenia pierwiastka w układzie okresowym wyjaśnij, dlaczego istnieje PCl 5 a występowanie NCl 5 jest teoretycznie
Zadanie 1. (2 pkt) Na podstawie budowy powłok elektronowych chloru, azotu i fosforu oraz położenia pierwiastka w układzie okresowym wyjaśnij, dlaczego istnieje PCl 5 a występowanie NCl 5 jest teoretycznie
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Podstawy chemii. dr hab. Wacław Makowski. Wykład 1: Wprowadzenie
 Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
Podstawy chemii dr hab. Wacław Makowski Wykład 1: Wprowadzenie Wspomnienia ze szkoły Elementarz (powtórka z gimnazjum) Układ okresowy Dalsze wtajemniczenia (liceum) Program zajęć Podręczniki Wydział Chemii
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
2. WIĄZANIA CHEMICZNE, BUDOWA CZĄSTECZEK. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu)
 2. WIĄZANIA CHEMICZNE, BUDOWA CZĄSTECZEK Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Wiązania chemiczne Podstawowe stany skupienia materii (w
2. WIĄZANIA CHEMICZNE, BUDOWA CZĄSTECZEK Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Wiązania chemiczne Podstawowe stany skupienia materii (w
Zadanie 1. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach: KBr i HBr.
 Zadanie 1. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach: KBr i HBr. Typ wiązania w KBr... Typ wiązania w HBr... Zadanie 2. (2 pkt) Oceń poprawność poniższych
Zadanie 1. (2 pkt) Określ, na podstawie różnicy elektroujemności pierwiastków, typ wiązania w związkach: KBr i HBr. Typ wiązania w KBr... Typ wiązania w HBr... Zadanie 2. (2 pkt) Oceń poprawność poniższych
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
1 3 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy Poziom przedmiotu Symbole efektów kształcenia Symbole efektów dla obszaru kształcenia Symbole efektów kierunkowych
2
 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 ZADANIA I PROBLEMY 1). Chlor naturalny jest mieszaniną dwóch izotopów o liczbach masowych 35 i 37, a eksperymentalnie wyznaczona masa atomowa chloru wynosi
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 ZADANIA I PROBLEMY 1). Chlor naturalny jest mieszaniną dwóch izotopów o liczbach masowych 35 i 37, a eksperymentalnie wyznaczona masa atomowa chloru wynosi
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 10 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Paweł Kowalczyk, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2015/16
Anna Grych Test z budowy atomu i wiązań chemicznych
 Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
CZ STECZKA. Do opisu wi za chemicznych stosuje si najcz ciej jedn z dwóch metod (teorii): metoda wi za walencyjnych (VB)
 CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Temat 1: Budowa atomu zadania
 Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
S. Baran - Podstawy fizyki materii skondensowanej Wiązania chemiczne w ciałach stałych. Wiązania chemiczne w ciałach stałych
 Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
26 Okresowy układ pierwiastków
 26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
Teoria VSEPR. Jak przewidywac strukturę cząsteczki?
 Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
Teoria VSEPR Jak przewidywac strukturę cząsteczki? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie. Rozkład elektronów walencyjnych w cząsteczce (struktura Lewisa) stuktura
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
Budowa atomu. Wiązania chemiczne
 strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
strona /6 Budowa atomu. Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu; jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
Wewnętrzna budowa materii - zadania
 Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
b) Pierwiastek E tworzy tlenek o wzorze EO 2 i wodorek typu EH 4, a elektrony w jego atomie rozmieszczone są na dwóch powłokach elektronowych
 1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
Modelowanie zjawisk fizycznych (struktury molekularnej, procesów chemicznych i układów biologicznych)
 Modelowanie zjawisk fizycznych (struktury molekularnej, procesów chemicznych i układów biologicznych) Dr inż. Marta Łabuda Politechnika Gdańska Katedra Fizyki Teoretycznej i Informatyki Kwantowej p. 409
Modelowanie zjawisk fizycznych (struktury molekularnej, procesów chemicznych i układów biologicznych) Dr inż. Marta Łabuda Politechnika Gdańska Katedra Fizyki Teoretycznej i Informatyki Kwantowej p. 409
Wykład 16: Atomy wieloelektronowe
 Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Zadanie do rozwiązania 1. Dla podanych nuklidów o ogólnym symbolu: E;
 Cz. IV Budowa atomu - konfiguracja elektronowa, przemiany jądrowe, promień jonowy, promień atomowy, jonizacja, hybrydyzacja, moment dipolowy A. Budowa atomu Nuklidy atomy o identycznej budowie jadra atomowego
Cz. IV Budowa atomu - konfiguracja elektronowa, przemiany jądrowe, promień jonowy, promień atomowy, jonizacja, hybrydyzacja, moment dipolowy A. Budowa atomu Nuklidy atomy o identycznej budowie jadra atomowego
Wiązania. w świetle teorii kwantów fenomenologicznie
 Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Projekt Era inżyniera pewna lokata na przyszłość jest współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego
 TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
TEMAT I WYBRANE WŁAŚCIWOŚCI ZWIĄZKÓW NIEORGANICZNYCH. STOPNIE UTLENIENIA. WIĄZANIA CHEMICZNE. WZORY SUMARYCZNE I STRUKTURALNE. TYPY REAKCJI CHEMICZNYCH. ILOŚCIOWA INTERPRETACJA WZORÓW I RÓWNAŃ CHEMICZNYCH
Atomy wieloelektronowe i cząsteczki
 Atomy wieloelektronowe i cząsteczki 1 Atomy wieloelektronowe Wodór ma liczbę atomową Z=1 i jest prostym atomem. Zawiera tylko jeden elektron i jeden proton stąd potencjał opisuje oddziaływanie kulombowskie
Atomy wieloelektronowe i cząsteczki 1 Atomy wieloelektronowe Wodór ma liczbę atomową Z=1 i jest prostym atomem. Zawiera tylko jeden elektron i jeden proton stąd potencjał opisuje oddziaływanie kulombowskie
Wykład z Chemii Ogólnej
 Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Wykład z Chemii Ogólnej Część 2 Budowa materii: od atomów do układów molekularnych 2.3. WIĄZANIA CHEMICZNE i ODDZIAŁYWANIA Katedra i Zakład Chemii Fizycznej Collegium Medicum w Bydgoszczy Uniwersytet Mikołaja
Chemia Nieorganiczna I (3.3.PBN.CHE108), konwersatorium Chemia, I stopień, II r., semestr 4. Lista 1.
 Lista 1. 1. Omów dualny charakter elektronów. Podaj i omów fakty za i przeciw falowej naturze.. Co to jest radialna funkcji rozkładu? Podaj wykres tej funkcji dla orbitali 1s, s, 3s, p, 3p i 3d w atomie
Lista 1. 1. Omów dualny charakter elektronów. Podaj i omów fakty za i przeciw falowej naturze.. Co to jest radialna funkcji rozkładu? Podaj wykres tej funkcji dla orbitali 1s, s, 3s, p, 3p i 3d w atomie
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wrocław dn. 23 listopada 2005 roku
 Piotr Chojnacki IV rok, informatyka chemiczna Liceum Ogólnokształcące Nr I we Wrocławiu Wrocław dn. 23 listopada 2005 roku Temat lekcji: Elektroujemność. + kartkówka z układu okresowego Cel ogólny lekcji:
Piotr Chojnacki IV rok, informatyka chemiczna Liceum Ogólnokształcące Nr I we Wrocławiu Wrocław dn. 23 listopada 2005 roku Temat lekcji: Elektroujemność. + kartkówka z układu okresowego Cel ogólny lekcji:
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków).
 Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne
 Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
Anna Grych Test sprawdzający z chemii do klasy I LO i technikum z działu Budowa atomu i wiązania chemiczne Informacja do zadań -7 75 Dany jest pierwiastek 33 As. Zadanie. ( pkt) Uzupełnij poniższą tabelkę.
Na rysunku przedstawiono fragment układu okresowego pierwiastków.
 Na rysunku przedstawiono fragment układu okresowego pierwiastków. Zadanie 1 (0 1) W poniższych zdaniach podano informacje o pierwiastkach i ich tlenkach. Które to tlenki? Wybierz je spośród podanych A
Na rysunku przedstawiono fragment układu okresowego pierwiastków. Zadanie 1 (0 1) W poniższych zdaniach podano informacje o pierwiastkach i ich tlenkach. Które to tlenki? Wybierz je spośród podanych A
CHEMIA OGÓLNA (wykład)
 AKADEMIA GÓRNICZO HUTNICZA WYDZIAŁ ENERGETYKI I PALIW I r. EiP (Technologia Chemiczna) CHEMIA OGÓLNA (wykład) Prof. dr hab. Leszek CZEPIRSKI Kontakt: A4 IV p., p. 424 Tel. 12 617 46 36 email: czepir@agh.edu.pl
AKADEMIA GÓRNICZO HUTNICZA WYDZIAŁ ENERGETYKI I PALIW I r. EiP (Technologia Chemiczna) CHEMIA OGÓLNA (wykład) Prof. dr hab. Leszek CZEPIRSKI Kontakt: A4 IV p., p. 424 Tel. 12 617 46 36 email: czepir@agh.edu.pl
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia. Monika Musia l
 STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
STRUKTURA ELEKTRONOWA CZA STECZEK: METODA ORBITALI MOLEKULARNYCH (MO) Ćwiczenia Monika Musia l Uk lad zamkniȩtopow lokowy: N elektronów; N 2 elektronowa: Ψ = 1 N! orbitali. Funkcja falowa N- φ 1 (1)α(1)
KSZTAŁTY CZĄSTECZEK I JONÓW. METODA VSEPR
 KSZTAŁTY CZĄSTECZEK I JNÓW METDA VSEPR Teoria VSEPR (ang Valence Shell Electron Pair Repulsion odpychanie się elektronów powłoki walencyjnej) jest uproszczonym sposobem przewidywania kształtu kowalencyjnych
KSZTAŁTY CZĄSTECZEK I JNÓW METDA VSEPR Teoria VSEPR (ang Valence Shell Electron Pair Repulsion odpychanie się elektronów powłoki walencyjnej) jest uproszczonym sposobem przewidywania kształtu kowalencyjnych
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 2
 PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE 1 Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Chemia Grudzień Styczeń
 Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
III Podkarpacki Konkurs Chemiczny 2010/2011. ETAP I r. Godz Zadanie 1
 III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
III Podkarpacki Konkurs Chemiczny 2010/2011 KOPKCh ETAP I 22.10.2010 r. Godz. 10.00-12.00 Zadanie 1 1. Jon Al 3+ zbudowany jest z 14 neutronów oraz z: a) 16 protonów i 13 elektronów b) 10 protonów i 13
Jeśli teraz nasz związek, chlorek glinu, ulegnie dysocjacji elektrolitycznej, rozpadnie się na jony według równania:
 Wiązania chemiczne powstają między atomami wówczas, gdy dwa atomy zbliżą się do siebie na tak bliska odległość, że orbital jednego z nich znajdzie się w obrębie orbitala drugiego atomu. Jeśli na każdym
Wiązania chemiczne powstają między atomami wówczas, gdy dwa atomy zbliżą się do siebie na tak bliska odległość, że orbital jednego z nich znajdzie się w obrębie orbitala drugiego atomu. Jeśli na każdym
Zaliczenie przedmiotu: ocena pozytywna z ćwiczeń jest warunkiem koniecznym przystąpienia do egzaminu
 Zaliczenie przedmiotu: 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 KLKWIUM
Zaliczenie przedmiotu: 1. J. D. aserio, M.. Roberts EMIA RGANIZNA, PWN Warszawa, 1969 2. R. T.Morrison, R. N. Boyd EMIA RGANIZNA, PWN Warszawa, 1997 3. J. McMurry EMIA RGANIZNA, PWN Warszawa, 2002 KLKWIUM
Struktura elektronowa
 Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
