Fizyka, technologia oraz modelowanie wzrostu kryształów
|
|
|
- Lidia Witkowska
- 9 lat temu
- Przeglądów:
Transkrypt
1 Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-42 Warszawa, ul Sokołowska 29/37 tel: stach@unipress.waw.pl, mike@unipress.waw.pl Zbigniew Żytkiewicz Instytut Fizyki PAN Warszawa, Al. Lotników 32/46 zytkie@ifpan.edu.pl Wykład 2 godz./tydzień wtorek Interdyscyplinarne Centrum Modelowania UW Budynek Wydziału Geologii UW sala
2 Wykład 4. Równowagowe własności powierzchni krystalicznych Fazy skondensowane (stała, ciekła) ujemna entalpia układu Energia oddziaływania np. potencjał Lennarda-Jonesa (gazy szlachetne) E ( r) = ε r σ 2 r σ 6 V/ε r/σ Do entalpii układu (jego energii wiązania) daje wkład wiele warstw atomowych.
3 Własności energetyczne warstw powierzchniowych Gęstość oraz energia oddziaływania zmienia się w sposób ciągły Energia Gęstość Grubość warstwy powierzchniowej może być bardzo różna, jednak w wielu przypadkach, np. kryształy półprzewodników lub kryształy jonowe, może to być wiele warstw atomowych. Stosuje się wiele różnych przybliżeń do opisu własności powierzchni, jednak najprostszym jest opis Gibbsa
4 Model powierzchni Gibbsa Model Gibbsa jednorodne własności faz objętościowych i dodatkowa gęstość (masy, energii, itp.) przypisywana powierzchni gdy zachodzi taka potrzeba Energia Można wybrać położenie powierzchni tak, aby znikała powierzchniowa gęstość masy lub powierzchniowa gęstość energii. Gęstość W przypadku układy zawierającego kilka składników można wybrać położenie tak aby znikała powierzchniowa gęstość jednego ze składników.
5 Opis standardowy znika powierzchniowa gęstość masy Energia swobodna kryształu F jest sumą wkładu objętościowego i powierzchniowego: F = V s f s r (T, p, r) dv + V l f l r (T, p, r) dv + S γ( θ, ϕ,t,p) ds µ l,s - potencjał chemiczny (s,l) f l,s - gęstość energii swobodnej na jednostkę objętości faz (s,l) γ - gęstość energii powierzchniowej Energia swobodna w modelu Gibbsa jest więc równa: F = f s (T, p)v s + f l (T, p)v l + γ( θ, ϕ,t, p)a
6 Napięcie powierzchniowe - i powierzchniowa gęstość energii Powierzchniowa gęstość energii γ ( θ,t,p) ds = γ( θ,t, p)a Praca potrzebna na zwiększenie obwodu = zmiana energii powierzchni F = Napięcie powierzchniowe siła działające na jednostkę długości obwodu powierzchni σ r A W = r r dlσ* δx r σδa = r σ F pow = γδa σ r = γ
7 Zwilżanie powierzchni Rozważmy 3 układy: faza stała(), faza gazowa(3) oraz inna faza (ciekła lub stała - 2) Własności energetyczne powierzchni są określone przez ich energie powierzchniowe (napięcia powierzchniowe):γ 2, γ 3, γ 23. (A) (B) Całkowite zwilżanie powierzchni (A) zachodzi gdy γ 3 > γ2 + γ 23
8 Częściowe zwilżanie powierzchni kąt zwilżania Częściowe zwilżanie powierzchni (A) zachodzi gdy γ γ 3 < γ2 + γ 23 3 > γ2 γ 23 Kąt zwilżania powierzchni definiujemy jako γ 3 = γ 2 + γ 23 cos ( θ) γ 2 θ γ 3 γ 23
9 Brak zwilżania Kąt zwilżania powierzchni γ 3 = γ 2 + γ 23 cos ( θ) γ 2 θ γ 3 γ 23 Brak zwilżania powierzchni (A) zachodzi gdy γ 2 > γ3 + γ 23
10 Warunki stabilności (V,T) Układy zamknięty warunek na stabilności - fluktuacje izotermicznoizochoryczne δf 0 δf = p δv p2δv + γδa + µ δn + µ 2δN 2 0 N = N + N2 = V = V + V2 = const const Równania równowagi δn δv = δ N 2 = V 2 T = const δt = 0 p δa = p2 + γ µ ( p,t) = µ 2( p,t) δv Stan równowagi zależy od kształtu powierzchni
11 Powierzchnia płaska U,V,N U 2,V 2,N 2 p,t,ρ p 2,T 2,ρ 2 Równania równowagi p δa = p2 + γ µ ( p,t) = µ 2( p,t) δv Dla powierzchni płaskiej wielkość powierzchni nie zależy od objętości faz: δa δv Warunki równowagi nie zależą od ich rozmiaru są to wartości umieszczane na diagramach fazowych = 0 p = p 2 T = = T2 Tp
12 Powierzchnia zakrzywiona przypadek izotropowy Równania równowagi p δa = p2 + γ µ ( p,t) = µ 2( p,t) δv U,V,N p,t,ρ U 2,V 2,N 2 Fazy izotropowe - kula: p 2,T 2,ρ 2 V = 4πR 3 3 A = 4πR 2 δa δv = 2 R = κ + κ 2 κ, κ 2 - krzywizny powierzchni Warunki równowagi zależą od rozmiaru faz p p2 2γ + R = T = T2 T p
13 Powierzchnia zakrzywiona efekt Gibbsa-Thompsona Równania równowagi p = p2 + 2γ R U,V,N p,t,ρ Przesunięcie ciśnienia zmiana warunku równowagi chemicznej U 2,V 2,N 2 p 2,T 2,ρ 2 µ ( + dp,t + dt) = µ ( p,t dt) p 2 + Efekt Gibbsa - Thompsona zmiana temperatury równowagi powierzchni zakrzywionej
14 Powierzchnia płaska Efekt Gibbsa-Thompsona Powierzchnia zakrzywiona µ (,T) = ( p,t) p µ 2 µ ( + dp,t + dt) = µ ( p,t dt) p 2 + Po rozwinięciu otrzymujemy: vdp s dt = s2dt dt = vdp s s 2 = (V / T dp ( S S )/ N S S L N)dp 2 = Vdp 2 = p Efekt Gibbsa - Thompsona zmiana temperatury równowagi powierzchni zakrzywionej T = T p - 2 d R o d o = T p γ = ( S - S ) L l s γ - długość kapilarna L ciepło przemiany na jednostkę objętości
15 Powierzchnia zakrzywiona przypadek anizotropowy Równania równowagi p = p 2 + γ Dla powierzchni są zdefiniowane dwa promienie krzywizny R oraz R 2 które dają rozmiar obszaru fazy 2. Zmiana ta powoduje zmianę potencjału chemicznego µ ( θ, ϕ) + R R ( + dp,t + dt) = µ ( p,t dt) p R 2 R Efekt Gibbsa - Thompsona zmiana temperatury równowagi powierzchni zakrzywionej: T = Tm - do( θ, ϕ) + do( θ, ϕ) R R 2 γ = T m ( θ, ϕ) ( S - S ) l s = γ ( θ, ϕ) L
16 Przypadek anizotropowy - równowagowy kształt powierzchni kryształów W przypadku kryształów energią powierzchniowa zależy od orientacji, tzn. zachodzi γ = γ(θ,ϕ) Wykres tej zależności jest to tzw. γ - plot - wyznaczenie na jego podstawie równowagowego kształtu kryształu nosi nazwę konstrukcji (twierdzenia) Wulfa. Równowagowy kształt kryształu jest wyznaczony przez minimalną obwiednię utworzoną przez płaszczyzny prostopadłe do linii wychodzących ze środka wykresu i przechodzące przez punkty przecięcia linii i tego wykresu Stąd wyznaczenie równowagowego kształtu sprowadza się do wyznaczenia zależności γ(θ,ϕ).
17 dθ Konstrukcja Wulfa E θ E 2 Dana jest zależność energii powierzchniowej od kątów γ(θ,ϕ) Obliczamy wielkość energii powierzchniowej dla kąta dθ Dla przypadku Dla przypadku E2 = E2dl E dl cosθ E dl cosθ E = Edl = = W przypadku gdy E 2 > (E /cosθ) to realizowany będzie przypadek, w przypadku odwrotnym przypadek 2. Jest to konstrukcja Wulfa
18 Kryształ Kossela najprostszy model kryształu Siec kwadratowa (2d) lub regularna( 3d) Oddziaływanie najbliższych sąsiadów Energia oddziaływania nie zależy od kierunku (φ - energia wiązania dwu atomów) Z liczba sąsiadów (d=2 Z=4, d=3 Z=6) φ φ Modyfikacje Oddziaływanie anizotropowe Oddziaływanie drugich sąsiadów φ X φ nn φ Y φ nnn
19 Powierzchnie w krysztale Kossela Powierzchnia układ atomów które nie maja wysycanych wiązań (mają złamane wiązania - broken bonds ) φ Energia kryształu (bez uwzględnienia powierzchni): E S ZNsφ = = Nbond Sφ 2 Energia kryształu (z powierzchnią): Energia powierzchni: E E = N S+ A S bond A φ E NsZφ = + Nbond 2 S+ A A Jest to uproszczony lecz zupełny opis powierzchni dla fazy stałej i fazy gazowej φ
20 Powierzchnie kryształ-ciecz w modelu Kossela Energia wiązania atomów w krysztale - φ ss Energia wiązania atomów w cieczy - φ ll E S E l N Zφ 2 s ss = = Nbond SS N Zφ 2 l ll = = Nbond ll φ φ ll ss Energia wiązania atomu w cieczy i w krysztale - φ sl φ ll φ sl Energia układu z powierzchnią: E S+ A+ L N = bond ls φ ls + N bond ss φ ss N bond ll φ ll φ ss Każde wiązanie łączy dwa atomy, stąd energia powierzchni jest równa: E A = Nbond A φ sl φ ll + φ 2 Jest to zupełny opis powierzchni dla fazy ciekłej i fazy stałej ss
21 Przykład (2d) - powierzchnie (0) oraz powierzchnie nachylone (vicinal surfaces) Powierzchnia (0) Powierzchnia nachylona (vicinal) α ( α) tg = n γ n = tg ( α) ( α) = φ( + n) cos( α) = cos( α) + sin( α) n szerokość stopnia (w stałych sieciowych) [ ] φ φ γ - plot wykres ma wcięcie (cusp) dla płaszczyzn o niskich wskaźnikach Millera (T = 0)
22 2-d kryształ Kossela - zależność kształtu od temperatury kt/ϕ = 0 kt/ϕ = 0.3 kt/ϕ = 0. kt/ϕ = 0.6
23 Powierzchnie 2-d oraz 3-d Stopień jest obiektem -d
24 Struktura powierzchni 3-d F S K Powierzchnie o niskich wskaźnikach Millera nazywamy powierzchniami płaskimi (F flat) Warstwy atomowe zakończone są brzegiem. Brzeg warstwy nazywamy stopniami (S step lub L ledge) Koniec rzędu atomów w stopniu nazywamy kinkiem (K kink) Model nosi nazwę modelu TLK terrace ledge - kink
25 Rodzaje powierzchni 3-d Powierzchnia S(stepped) Powierzchnia F(flat) Powierzchnia K(kinked)
26 3-d Kossel klasyfikacja Rotmana i Wortisa Diagram fazowy Ciemne kropki - punkty osobliwe przejścia od powierzchni gładkiej do powierzchni zakrzywionej
27 Mikroskopowa struktura powierzchni powierzchnie gładkie i szorstkie Szorstkość powierzchni definiujemy jako: R N - N N o o N - ilość złamanych wiązań N o - minimalna ilość złamanych wiązań gladka szorstka Parametr szorstkości zdefiniowany w ten sposób nie jest tożsamy z szorstkością mierzona np. przy pomocy mikroskopu sił atomowych (AFM)
28 Przejście fazowe powierzchnia gładka powierzchnia szorstka: wyniki analityczne Model pojedynczej warstwy: Teoria pola średniego (przybliżenie Bragga Williamsa) Energia swobodna układu jest równa: [ ( - x) ln ( - x) + Z φ x ( - x) ] F = kt x ln x Zφ/kT=3 x N N at o Zφ/kT=2 F/kT Zφ/kT= Przejście fazowe dla Zφ=2kT x
29 Przejście fazowe powierzchnia gładka powierzchnia szorstka: wyniki symulacji komputerowych Różnica energii układu ze stopniami oraz bez stopni: Model ze stopniami Pseudoperiodyczne warunki brzegowe Przybliżenie SOS Leamy & Gilmer α kt φ = kt ε Przejście fazowe dla kt = 0.6φ
30 Równowagowa struktura stopni Stopień obiekt -d Nie występuje przejście fazowe dla struktury stopnia Stopień - obiekt szorstki obecność dużej gęstości kinków Stopień obiekt na którym odbywa się wymiana atomów
31 Powierzchnie kryształów rzeczywistych bez atomów obcych Na powierzchni kryształów rzeczywistych może zajść efekt Jahna-Tellera: spontaniczne złamanie symetrii dla obniżenia energii układu Wyróżniamy dwa rodzaje efektów: relaksację i rekonstrukcje powierzchni Relaksacja powierzchni: zmiana położeń atomów zachowująca symetrię translacyjną sieci (równoległą do powierzchni) Rekonstrukcja powierzchni: zmiana położeń atomów w sieci naruszająca symetrie sieci Bravais
32 Relaksacja powierzchni Występuje w przypadku metali wiązania prawie izotropowe Zachowanie elektrostatycznej struktury powierzchni Powierzchnia prosta Powierzchnia zrelaksowana
33 Powierzchnie ulegające rekonstrukcji przykłady 2x rekonstrukcja brakującego rzędu 2x rekonstrukcja parowania Symetria sieci notacja Wooda
34 Powierzchnia o wskaźnikach krystalograficznych (hkl) Notacja (symbol) Wooda a, a 2 - wektory translacji prymitywnych powierzchni Symbol chemiczny, np. C S(hkl) κ a r r b, a r r b Rϕ o Obrót o kąt ϕº (Dla ϕ=0 symbol jest pomijany) c centrowana p prosta (domyślna w przypadku braku symbolu) b, b 2 - wektory translacji prymitywnych sieci objętościowej Notacja Wooda jest niekiedy niejednoznaczna (dla sieci regularnej)
35 Symbol Wooda - przykłady ( x) ( 2 x) ( 2x2) ( 2x2) ( 2x 2)
36 Powierzchnie półprzewodników rekonstrukcja Silne, kierunkowe wiązania Tendencja do wysycenia przez tworzenie wiązań równoległych do powierzchni: łańcuchów, dimerów itp. Struktura powierzchni może ulec zmianie na skutek przyłączenia obcych atomów wysycających złamane wiązania Rekonstrukcja może sięgać kilku warstw atomowych Ładunki związane ze stanami powierzchniowymi tworzą pola które mogą sięgać głęboko do wnętrza półprzewodnika
37 Powierzchnie półprzewodników - dimery Dimery symetryczne - schemat powstawania Dimery asymetryczne schemat powstawania
38 Skanningowy mikroskop tunelowy (Scanning Tunneling Microscope STM) Nobel Laureates: Heinrich Rohrer and Gerd Binnig
39 Działanie skanningowego mikroskopu tunelowego Oddziaływanie końcówki mikroskopu z powierzchnią Zależność prądu tunelowania od odległości d. K oraz k są stałymi STM osiąga rozdzielczość atomową!
40 Mikroskop sił atomowych (AFM Atomic Force Microscope) Atomic Force Microscope - NovaScan ESPM II OSPM II
41 Działanie mikroskopu sił atomowych Oddziaływanie końcówki mikroskopu z powierzchnią Detekcja ruchu końcówki mikroskopu odbity promień lasera Rozdzielczość atomowa powierzchni miki w roztworze wodnym. Odległość pomiędzy sąsiadującymi wypukłościami wynosi 5.4 Å.
42 Powierzchnie półprzewodników adatomy Si () 7x7 DAS (dimer adatom stacking fault) Adatomy na powierzchni Si () - model STM obraz Adatomy kółka szare
43 Si() rekonstrukcja (7x7) - obrazy STM 3-d model Model - R.M. Tromp (IBM) Obraz STM
44 Adsorpcja Fizysorpcja przyłączanie atomów do powierzchni kryształu/cieczy bez tworzenia wiązań chemicznych. Siły wiążące siły Lennarda Jonesa. Na ogół nie prowadzi do lokalizacji atomu na powierzchni Chemisorpcja przyłączenie atomu do powierzchni kryształu/cieczy powodujące powstanie wiązania chemicznego. Na ogół prowadzi do lokalizacji atomów w węzłach sieci krystalograficznej. Często prowadzi do zmian wiązania w przyłączanych cząsteczkach chemicznych.
45 Fizysorpcja izoterma Langmuira Zakładamy ze istnieje pewna liczba węzłów na których mogą być zaadsorbowane cząstki Pokryciem Γ nazywamy stosunek liczby obsadzonych wezłów do liczby wszystkich węzłów Pokrycie zależy min. od energii wiązania na powierzchni Dla danego układu (tzn. dla określonej energii wiązania) pokrycie jest funkcja ciśnienia gazu nad powierzchnia i temperatury: Γ = Γ o P + P P 2 ( T) Γ E kt o = Γ( P ) 5 2 b P ( T) = P Γ = = CT exp 2 2 E b energia wiązania do powierzchni
46 Przykład - adsorpcja CO/Pd()
47 Chemisorpcja Adsorpcja molekularna Adsorpcja dysocjatywna E dis Energy 0 E dis Energy 0 5 E bar 5 E bar distance distance
48 Oddziaływanie N 2 z Ga(l) N 2 Energia bariery na rozpad Excess energy [ev] ev 4.8 ev 3.2 ev N2 molecule horizontally and cluster of 9 atoms In Ga Al Ga Energia dysocjacji swobodnej cząsteczki N ev/cząsteczkę Distance from surface(a) S. Krukowski and Z. Romanowski Obliczenia kwantowe, Dmol, QM DFT
49 Dysocjacja N 2 na powierzchni Ga 3,5 3,0.0A N - N spacing [A] 2,5 2,0,5.6A 2.6A,0 0,8,2,6 2,0 2,4 2,8 3,2 3,6 4,0 d [A] S. Krukowski and Z. Romanowski Dmol, QM DFT
50 Podsumowanie Powierzchnie, zwłaszcza powierzchnie półprzewodników tworzą struktury o własnościach różnych od własności układów objętościowych Równowagowe struktury powierzchni mogą wykazywać przemiany będące przemianami fazowymi związanymi ze zmianą symetrii (rekonstrukcja). Innego typu zmiany prowadzą do relaksacji powierzchni lub do zmiany jej gładkości. Wizualizacja struktury powierzchni wymaga zastosowanie zaawansowanych technik mikroskopowych, np. AFM lub TEM Adsorpcja gazów na powierzchni może zmieniać ich własności, w tym ich strukturę w sposób zasadniczy Adsorpcja cząsteczek może prowadzić do zmiany ich konformacji chemicznej (chemisorpcja) lub tylko lokalizacji (fizysorpcja) Otrzymanie właściwego obrazu powierzchni, w tym jej struktury oraz procesów powierzchniowych wymaga przeprowadzenia obliczeń kwantowomechanicznych, najczęściej za pomocą metody DFT
Fizyka, technologia oraz modelowanie wzrostu kryształów
 Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-42 Warszawa, ul Sokołowska 29/37 tel: 88 80 244 e-mail: stach@unipress.waw.pl,
Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-42 Warszawa, ul Sokołowska 29/37 tel: 88 80 244 e-mail: stach@unipress.waw.pl,
Fizyka, technologia oraz modelowanie wzrostu kryształów
 Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Fizyka, technologia oraz modelowanie wzrostu kryształów Stanisław Krukowski i Michał Leszczyński Instytut Wysokich Ciśnień PAN 0-4 Warszawa, ul Sokołowska 9/37 tel: 88 80 44 e-mail: stach@unipress.waw.pl,
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 2 v.16 Sieci płaskie i struktura powierzchni 1 Typy sieci dwuwymiarowych (płaskich) Przecinając monokryształ wzdłuż jednej z płaszczyzn
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 2 v.16 Sieci płaskie i struktura powierzchni 1 Typy sieci dwuwymiarowych (płaskich) Przecinając monokryształ wzdłuż jednej z płaszczyzn
Krystalizacja. Zarodkowanie
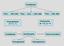 Krystalizacja Ciecz ciało stałe Para ciecz ciało stałe Para ciało stałe Przechłodzenie T = T L - T c Przesycenie p = p g - p z > 0 Krystalizacja Zarodkowanie Rozrost zarodków Homogeniczne Heterogeniczne
Krystalizacja Ciecz ciało stałe Para ciecz ciało stałe Para ciało stałe Przechłodzenie T = T L - T c Przesycenie p = p g - p z > 0 Krystalizacja Zarodkowanie Rozrost zarodków Homogeniczne Heterogeniczne
Zadania treningowe na kolokwium
 Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Elementy teorii powierzchni metali
 Prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład dla studentów fizyki Rok akademicki 2017/18 (30 godz.) Wykład 1 Plan wykładu Struktura periodyczna kryształów, sieć odwrotna Struktura
Prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład dla studentów fizyki Rok akademicki 2017/18 (30 godz.) Wykład 1 Plan wykładu Struktura periodyczna kryształów, sieć odwrotna Struktura
BUDOWA KRYSTALICZNA CIAŁ STAŁYCH. Stopień uporządkowania struktury wewnętrznej ciał stałych decyduje o ich podziale
 BUDOWA KRYSTALICZNA CIAŁ STAŁYCH Stopień uporządkowania struktury wewnętrznej ciał stałych decyduje o ich podziale na: kryształy ciała o okresowym regularnym uporządkowaniu atomów, cząsteczek w całej swojej
BUDOWA KRYSTALICZNA CIAŁ STAŁYCH Stopień uporządkowania struktury wewnętrznej ciał stałych decyduje o ich podziale na: kryształy ciała o okresowym regularnym uporządkowaniu atomów, cząsteczek w całej swojej
Fizyka Ciała Stałego
 Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
Wykład 5. Komórka elementarna. Sieci Bravais go
 Wykład 5 Komórka elementarna Sieci Bravais go Doskonały kryształ składa się z atomów jonów, cząsteczek) uporządkowanych w sieci krystalicznej opisanej przez trzy podstawowe wektory translacji a, b, c,
Wykład 5 Komórka elementarna Sieci Bravais go Doskonały kryształ składa się z atomów jonów, cząsteczek) uporządkowanych w sieci krystalicznej opisanej przez trzy podstawowe wektory translacji a, b, c,
Fizyka statystyczna Fenomenologia przejść fazowych. P. F. Góra
 Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
Statyka Cieczy i Gazów. Temat : Podstawy teorii kinetyczno-molekularnej budowy ciał
 Statyka Cieczy i Gazów Temat : Podstawy teorii kinetyczno-molekularnej budowy ciał 1. Podstawowe założenia teorii kinetyczno-molekularnej budowy ciał: Ciała zbudowane są z cząsteczek. Pomiędzy cząsteczkami
Statyka Cieczy i Gazów Temat : Podstawy teorii kinetyczno-molekularnej budowy ciał 1. Podstawowe założenia teorii kinetyczno-molekularnej budowy ciał: Ciała zbudowane są z cząsteczek. Pomiędzy cząsteczkami
Wiązania chemiczne. Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych. 5 typów wiązań
 Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
Zjawiska powierzchniowe
 Zjawiska powierzchniowe Adsorpcja Model Langmuira Model BET 1 Zjawiska powierzchniowe Adsorpcja Proces gromadzenia się substancji z wnętrza fazy na granicy międzyfazowej; Wynika z tego, że w obszarze powierzchniowym
Zjawiska powierzchniowe Adsorpcja Model Langmuira Model BET 1 Zjawiska powierzchniowe Adsorpcja Proces gromadzenia się substancji z wnętrza fazy na granicy międzyfazowej; Wynika z tego, że w obszarze powierzchniowym
Termodynamika fazy powierzchniowej Zjawisko sorpcji Adsorpcja fizyczna: izoterma Langmuira oraz BET Zjawiska przylegania
 ermodynamika zjawisk powierzchniowych 3.6.1. ermodynamika fazy powierzchniowej 3.6.2. Zjawisko sorpcji 3.6.3. Adsorpcja fizyczna: izoterma Langmuira oraz BE 3.6.4. Zjawiska przylegania ZJAWISKA PWIERZCHNIWE
ermodynamika zjawisk powierzchniowych 3.6.1. ermodynamika fazy powierzchniowej 3.6.2. Zjawisko sorpcji 3.6.3. Adsorpcja fizyczna: izoterma Langmuira oraz BE 3.6.4. Zjawiska przylegania ZJAWISKA PWIERZCHNIWE
STRUKTURA CIAŁA STAŁEGO
 STRUKTURA CIAŁA STAŁEGO Podział ciał stałych Ciała - bezpostaciowe (amorficzne) Szkła, żywice, tłuszcze, niektóre proszki. Nie wykazują żadnych regularnych płaszczyzn ograniczających, nie można w nich
STRUKTURA CIAŁA STAŁEGO Podział ciał stałych Ciała - bezpostaciowe (amorficzne) Szkła, żywice, tłuszcze, niektóre proszki. Nie wykazują żadnych regularnych płaszczyzn ograniczających, nie można w nich
Powierzchnie cienkie warstwy nanostruktury. Józef Korecki, C1, II p., pok. 207
 Powierzchnie cienkie warstwy nanostruktury Józef Korecki, C1, II p., pok. 207 korecki@uci.agh.edu.pl http://korek.uci.agh.edu.pl/priv/jk.htm Obiekty niskowymiarowe Powierzchnia Cienkie warstwy Wielowarstwy
Powierzchnie cienkie warstwy nanostruktury Józef Korecki, C1, II p., pok. 207 korecki@uci.agh.edu.pl http://korek.uci.agh.edu.pl/priv/jk.htm Obiekty niskowymiarowe Powierzchnia Cienkie warstwy Wielowarstwy
Szkła specjalne Przejście szkliste i jego termodynamika Wykład 5. Ryszard J. Barczyński, 2017 Materiały edukacyjne do użytku wewnętrznego
 Szkła specjalne Przejście szkliste i jego termodynamika Wykład 5 Ryszard J. Barczyński, 2017 Materiały edukacyjne do użytku wewnętrznego Czy przejście szkliste jest termodynamicznym przejściem fazowym?
Szkła specjalne Przejście szkliste i jego termodynamika Wykład 5 Ryszard J. Barczyński, 2017 Materiały edukacyjne do użytku wewnętrznego Czy przejście szkliste jest termodynamicznym przejściem fazowym?
Wstęp. Krystalografia geometryczna
 Wstęp Przedmiot badań krystalografii. Wprowadzenie do opisu struktury kryształów. Definicja sieci Bravais go i bazy atomowej, komórki prymitywnej i elementarnej. Podstawowe typy komórek elementarnych.
Wstęp Przedmiot badań krystalografii. Wprowadzenie do opisu struktury kryształów. Definicja sieci Bravais go i bazy atomowej, komórki prymitywnej i elementarnej. Podstawowe typy komórek elementarnych.
Nauka o Materiałach Wykład II Monokryształy Jerzy Lis
 Wykład II Monokryształy Jerzy Lis Treść wykładu: 1. Wstęp stan krystaliczny 2. Budowa kryształów - krystalografia 3. Budowa kryształów rzeczywistych defekty WPROWADZENIE Stan krystaliczny jest podstawową
Wykład II Monokryształy Jerzy Lis Treść wykładu: 1. Wstęp stan krystaliczny 2. Budowa kryształów - krystalografia 3. Budowa kryształów rzeczywistych defekty WPROWADZENIE Stan krystaliczny jest podstawową
STRUKTURA KRYSTALICZNA
 PODSTAWY KRYSTALOGRAFII Struktura krystaliczna Wektory translacji sieci Komórka elementarna Komórka elementarna Wignera-Seitza Jednostkowy element struktury Sieci Bravais go 2D Sieci przestrzenne Bravais
PODSTAWY KRYSTALOGRAFII Struktura krystaliczna Wektory translacji sieci Komórka elementarna Komórka elementarna Wignera-Seitza Jednostkowy element struktury Sieci Bravais go 2D Sieci przestrzenne Bravais
SPM Scanning Probe Microscopy Mikroskopia skanującej sondy STM Scanning Tunneling Microscopy Skaningowa mikroskopia tunelowa AFM Atomic Force
 SPM Scanning Probe Microscopy Mikroskopia skanującej sondy STM Scanning Tunneling Microscopy Skaningowa mikroskopia tunelowa AFM Atomic Force Microscopy Mikroskopia siły atomowej MFM Magnetic Force Microscopy
SPM Scanning Probe Microscopy Mikroskopia skanującej sondy STM Scanning Tunneling Microscopy Skaningowa mikroskopia tunelowa AFM Atomic Force Microscopy Mikroskopia siły atomowej MFM Magnetic Force Microscopy
Podstawy fizyki wykład 2
 D. Halliday, R. Resnick, J.Walker: Podstawy Fizyki, tom 5, PWN, Warszawa 2003. H. D. Young, R. A. Freedman, Sear s & Zemansky s University Physics with Modern Physics, Addison-Wesley Publishing Company,
D. Halliday, R. Resnick, J.Walker: Podstawy Fizyki, tom 5, PWN, Warszawa 2003. H. D. Young, R. A. Freedman, Sear s & Zemansky s University Physics with Modern Physics, Addison-Wesley Publishing Company,
Pasmowa teoria przewodnictwa. Anna Pietnoczka
 Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
Pasmowa teoria przewodnictwa elektrycznego Anna Pietnoczka Wpływ rodzaju wiązań na przewodność próbki: Wiązanie jonowe - izolatory Wiązanie metaliczne - przewodniki Wiązanie kowalencyjne - półprzewodniki
STRUKTURA IDEALNYCH KRYSZTAŁÓW
 BUDOWA WEWNĘTRZNA MATERIAŁÓW METALICZNYCH Zakres tematyczny y 1 STRUKTURA IDEALNYCH KRYSZTAŁÓW 2 1 Sieć przestrzenna kryształu TRANSLACJA WĘZŁA TRANSLACJA PROSTEJ SIECIOWEJ TRANSLACJA PŁASZCZYZNY SIECIOWEJ
BUDOWA WEWNĘTRZNA MATERIAŁÓW METALICZNYCH Zakres tematyczny y 1 STRUKTURA IDEALNYCH KRYSZTAŁÓW 2 1 Sieć przestrzenna kryształu TRANSLACJA WĘZŁA TRANSLACJA PROSTEJ SIECIOWEJ TRANSLACJA PŁASZCZYZNY SIECIOWEJ
Warunki izochoryczno-izotermiczne
 WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych.
 Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
Wykład 3. Entropia i potencjały termodynamiczne
 Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Wykład 3 Entropia i potencjały termodynamiczne dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki statystycznej
Termodynamiczny opis przejść fazowych pierwszego rodzaju
 Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład 4. Przypomnienie z poprzedniego wykładu
 Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Sieć przestrzenna. c r. b r. a r. komórka elementarna. r r
 Sieć przestrzenna c r b r r r u a r vb uvw = + + w c v a r komórka elementarna V = r r a ( b c) v Układy krystalograficzne (7) i Sieci Bravais (14) Triclinic (P) a b c, α β γ 90 ο Monoclinic (P) a b c,
Sieć przestrzenna c r b r r r u a r vb uvw = + + w c v a r komórka elementarna V = r r a ( b c) v Układy krystalograficzne (7) i Sieci Bravais (14) Triclinic (P) a b c, α β γ 90 ο Monoclinic (P) a b c,
Właściwości kryształów
 Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Rozwiązanie: Zadanie 2
 Podstawowe pojęcia. Definicja kryształu. Sieć przestrzenna i sieć krystaliczna. Osie krystalograficzne i jednostki osiowe. Ściana jednostkowa i stosunek osiowy. Położenie węzłów, prostych i płaszczyzn
Podstawowe pojęcia. Definicja kryształu. Sieć przestrzenna i sieć krystaliczna. Osie krystalograficzne i jednostki osiowe. Ściana jednostkowa i stosunek osiowy. Położenie węzłów, prostych i płaszczyzn
Aby opisać strukturę krystaliczną, konieczne jest określenie jej części składowych: sieci przestrzennej oraz bazy atomowej.
 2. Podstawy krystalografii Podczas naszych zajęć skupimy się przede wszystkim na strukturach krystalicznych. Kryształem nazywamy (def. strukturalna) substancję stałą zbudowaną z atomów, jonów lub cząsteczek
2. Podstawy krystalografii Podczas naszych zajęć skupimy się przede wszystkim na strukturach krystalicznych. Kryształem nazywamy (def. strukturalna) substancję stałą zbudowaną z atomów, jonów lub cząsteczek
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY
 WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }
![Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] } Zespół kanoniczny N,V, T. acc o n =min {1, exp [ U n U o ] }](/thumbs/64/51033976.jpg) Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
Zespół kanoniczny Zespół kanoniczny N,V, T acc o n =min {1, exp [ U n U o ] } Zespół izobaryczno-izotermiczny Zespół izobaryczno-izotermiczny N P T acc o n =min {1, exp [ U n U o ] } acc o n =min {1, exp[
TERMODYNAMIKA I TERMOCHEMIA
 TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
Podstawowe pojęcia 1
 Tomasz Lubera Podstawowe pojęcia 1 Układ część przestrzeni wyodrębniona myślowo lub fizycznie z otoczenia Układ izolowany niewymieniający masy i energii z otoczeniem Układ zamknięty wymieniający tylko
Tomasz Lubera Podstawowe pojęcia 1 Układ część przestrzeni wyodrębniona myślowo lub fizycznie z otoczenia Układ izolowany niewymieniający masy i energii z otoczeniem Układ zamknięty wymieniający tylko
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
STRUKTURA MATERIAŁÓW
 STRUKTURA MATERIAŁÓW ELEMENTY STRUKTURY MATERIAŁÓW 1. Wiązania miedzy atomami 2. Układ atomów w przestrzeni 3. Mikrostruktura 4. Makrostruktura 1. WIĄZANIA MIĘDZY ATOMAMI Siły oddziaływania między atomami
STRUKTURA MATERIAŁÓW ELEMENTY STRUKTURY MATERIAŁÓW 1. Wiązania miedzy atomami 2. Układ atomów w przestrzeni 3. Mikrostruktura 4. Makrostruktura 1. WIĄZANIA MIĘDZY ATOMAMI Siły oddziaływania między atomami
Wykład 1. Anna Ptaszek. 5 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 1. Anna Ptaszek 1 / 36
 Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
FIZYKA POWIERZCHNI I NANOSTRUKTURY. Wykład odbędzie się w II semstrze 2005/2006
 FIZYKA POWIERZCHNI I NANOSTRUKTURY dr hab. Zbigniew Postawa Zakład Fizyki Doświadczalnej pok. 016 Tel. 5626 e-mail: zp@castor.if.uj.edu.pl H H C H H C H H Wykład odbędzie się w II semstrze 2005/2006 Bez
FIZYKA POWIERZCHNI I NANOSTRUKTURY dr hab. Zbigniew Postawa Zakład Fizyki Doświadczalnej pok. 016 Tel. 5626 e-mail: zp@castor.if.uj.edu.pl H H C H H C H H Wykład odbędzie się w II semstrze 2005/2006 Bez
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
STRUKTURA PASM ENERGETYCZNYCH
 PODSTAWY TEORII PASMOWEJ Struktura pasm energetycznych Teoria wa Struktura wa stałych Półprzewodniki i ich rodzaje Półprzewodniki domieszkowane Rozkład Fermiego - Diraca Złącze p-n (dioda) Politechnika
PODSTAWY TEORII PASMOWEJ Struktura pasm energetycznych Teoria wa Struktura wa stałych Półprzewodniki i ich rodzaje Półprzewodniki domieszkowane Rozkład Fermiego - Diraca Złącze p-n (dioda) Politechnika
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
3. Przejścia fazowe pomiędzy trzema stanami skupienia materii:
 Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
Termodynamika materiałów
 Termodynamika materiałów Plan wykładu 1. Funkcje termodynamiczne, pojemność cieplna. 2. Warunki równowagi termodynamicznej w układach jedno- i wieloskładnikowych, pojęcie potencjału chemicznego. 3. Modele
Termodynamika materiałów Plan wykładu 1. Funkcje termodynamiczne, pojemność cieplna. 2. Warunki równowagi termodynamicznej w układach jedno- i wieloskładnikowych, pojęcie potencjału chemicznego. 3. Modele
1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej?
 Tematy opisowe 1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej? 2. Omów pomiar potencjału na granicy faz elektroda/roztwór elektrolitu. Podaj przykład, omów skale potencjału i elektrody
Tematy opisowe 1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej? 2. Omów pomiar potencjału na granicy faz elektroda/roztwór elektrolitu. Podaj przykład, omów skale potencjału i elektrody
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Repeta z wykładu nr 3. Detekcja światła. Struktura krystaliczna. Plan na dzisiaj
 Repeta z wykładu nr 3 Detekcja światła Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 Konsultacje:
Repeta z wykładu nr 3 Detekcja światła Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 Konsultacje:
TEORIA PASMOWA CIAŁ STAŁYCH
 TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
TEORIA PASMOWA CIAŁ STAŁYCH Skolektywizowane elektrony w metalu Weźmy pod uwagę pewną ilość atomów jakiegoś metalu, np. sodu. Pojedynczy atom sodu zawiera 11 elektronów o konfiguracji 1s 2 2s 2 2p 6 3s
Czym się różni ciecz od ciała stałego?
 Szkła Czym się różni ciecz od ciała stałego? gęstość Czy szkło to ciecz czy ciało stałe? Szkło powstaje w procesie chłodzenia cieczy. Czy szkło to ciecz przechłodzona? kryształ szkło ciecz przechłodzona
Szkła Czym się różni ciecz od ciała stałego? gęstość Czy szkło to ciecz czy ciało stałe? Szkło powstaje w procesie chłodzenia cieczy. Czy szkło to ciecz przechłodzona? kryształ szkło ciecz przechłodzona
MATERIA. = m i liczby całkowite. ciała stałe. - kryształy - ciała bezpostaciowe (amorficzne) - ciecze KRYSZTAŁY. Periodyczność
 MATERIA ciała stałe - kryształy - ciała bezpostaciowe (amorficzne) - ciecze - gazy KRYSZTAŁY Periodyczność Kryształ (idealny) struktura zbudowana z powtarzających się w przestrzeni periodycznie identycznych
MATERIA ciała stałe - kryształy - ciała bezpostaciowe (amorficzne) - ciecze - gazy KRYSZTAŁY Periodyczność Kryształ (idealny) struktura zbudowana z powtarzających się w przestrzeni periodycznie identycznych
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wstęp do Optyki i Fizyki Materii Skondensowanej. Mateusz Goryca
 Wstęp do Optyki i Fizyki Materii Skondensowanej Mateusz Goryca mgoryca@fuw.edu.pl Uniwersytet Warszawski 2015 Materia skondensowana OC 6 H 13 H 13 C 6 O OC 6 H 13 H 17 C 8 O H 17 C 8 O N N Cu O O H 21
Wstęp do Optyki i Fizyki Materii Skondensowanej Mateusz Goryca mgoryca@fuw.edu.pl Uniwersytet Warszawski 2015 Materia skondensowana OC 6 H 13 H 13 C 6 O OC 6 H 13 H 17 C 8 O H 17 C 8 O N N Cu O O H 21
Wykład 21: Studnie i bariery cz.2.
 Wykład 21: Studnie i bariery cz.2. Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.321 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ 1 Przykłady tunelowania: rozpad alfa, synteza
Wykład 21: Studnie i bariery cz.2. Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.321 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ 1 Przykłady tunelowania: rozpad alfa, synteza
WYKONUJEMY POMIARY. Ocenę DOSTATECZNĄ otrzymuje uczeń, który :
 WYKONUJEMY POMIARY Ocenę DOPUSZCZAJĄCĄ otrzymuje uczeń, który : wie, w jakich jednostkach mierzy się masę, długość, czas, temperaturę wie, do pomiaru jakich wielkości służy barometr, menzurka i siłomierz
WYKONUJEMY POMIARY Ocenę DOPUSZCZAJĄCĄ otrzymuje uczeń, który : wie, w jakich jednostkach mierzy się masę, długość, czas, temperaturę wie, do pomiaru jakich wielkości służy barometr, menzurka i siłomierz
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny
 Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
Termodynamika Część 6 Związki i tożsamości termodynamiczne Potencjały termodynamiczne Warunki równowagi termodynamicznej Potencjał chemiczny Janusz Brzychczyk, Instytut Fizyki UJ Związek pomiędzy równaniem
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ
 CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
S. Baran - Podstawy fizyki materii skondensowanej Wiązania chemiczne w ciałach stałych. Wiązania chemiczne w ciałach stałych
 Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Wiązania chemiczne w ciałach stałych Wiązania chemiczne w ciałach stałych typ kowalencyjne jonowe metaliczne Van der Waalsa wodorowe siła* silne silne silne pochodzenie uwspólnienie e- (pary e-) przez
Wykład Praca (1.1) c Całka liniowa definiuje pracę wykonaną w kierunku działania siły. Reinhard Kulessa 1
 1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
Elektrostatyka ŁADUNEK. Ładunek elektryczny. Dr PPotera wyklady fizyka dosw st podypl. n p. Cząstka α
 Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
Wykład VI. Teoria pasmowa ciał stałych
 Wykład VI Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Wykład VI Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Zasady termodynamiki
 Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
Zasady termodynamiki Energia wewnętrzna (U) Opis mikroskopowy: Jest to suma średnich energii kinetycznych oraz energii oddziaływań międzycząsteczkowych i wewnątrzcząsteczkowych. Opis makroskopowy: Jest
chemia wykład 3 Przemiany fazowe
 Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Wykład III. Teoria pasmowa ciał stałych
 Wykład III Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Wykład III Teoria pasmowa ciał stałych Energia elektronu (ev) Powstawanie pasm w krysztale sodu pasmo walencyjne (zapełnione częściowo) Konfiguracja w izolowanym atomie Na: 1s 2 2s 2 2p 6 3s 1 Ne Położenie
Wykład 14 Przejścia fazowe
 Wykład 14 Przejścia fazowe Z izoterm gazu Van der Waalsa (rys.14.1) wynika, że dla T < T k izotermy zawierają obszary w których gaz Van der Waalsa zachowuje się niefizycznie. W tych niefizycznych obszarach
Wykład 14 Przejścia fazowe Z izoterm gazu Van der Waalsa (rys.14.1) wynika, że dla T < T k izotermy zawierają obszary w których gaz Van der Waalsa zachowuje się niefizycznie. W tych niefizycznych obszarach
Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne
 Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne W3. Zjawiska transportu Zjawiska transportu zachodzą gdy układ dąży do stanu równowagi. W zjawiskach
Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne W3. Zjawiska transportu Zjawiska transportu zachodzą gdy układ dąży do stanu równowagi. W zjawiskach
Wykład 1 i 2. Termodynamika klasyczna, gaz doskonały
 Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Wykład 1 i 2 Termodynamika klasyczna, gaz doskonały dr hab. Agata Fronczak, prof. PW Wydział Fizyki, Politechnika Warszawska 1 stycznia 2017 dr hab. A. Fronczak (Wydział Fizyki PW) Wykład: Elementy fizyki
Ogólny schemat postępowania
 Ogólny schemat postępowania 1. Należy zdecydować, który rozkład prawdopodobieństwa chcemy badać. Rozkład oznaczamy przez P; zależy od zespołu statystycznego. 2. Narzucamy warunek równowagi szczegółowej,
Ogólny schemat postępowania 1. Należy zdecydować, który rozkład prawdopodobieństwa chcemy badać. Rozkład oznaczamy przez P; zależy od zespołu statystycznego. 2. Narzucamy warunek równowagi szczegółowej,
Diagramy fazowe graficzna reprezentacja warunków równowagi
 Diagramy fazowe graficzna reprezentacja warunków równowagi Faza jednorodna część układu, oddzielona od innych części granicami faz, na których zachodzi skokowa zmiana pewnych własności fizycznych. B 0
Diagramy fazowe graficzna reprezentacja warunków równowagi Faza jednorodna część układu, oddzielona od innych części granicami faz, na których zachodzi skokowa zmiana pewnych własności fizycznych. B 0
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Elementy wiedzy o powierzchni ciała stałego
 Elementy wiedzy o powierzchni ciała stałego Struktura powierzchni Procesy zachodzące na powierzchni Bolesław AUGUSTYNIAK Powierzchnia jak ją zdefiniować? Obszar kryształu, dla którego nie da się zastosować
Elementy wiedzy o powierzchni ciała stałego Struktura powierzchni Procesy zachodzące na powierzchni Bolesław AUGUSTYNIAK Powierzchnia jak ją zdefiniować? Obszar kryształu, dla którego nie da się zastosować
Termodynamika i właściwości fizyczne stopów - zastosowanie w przemyśle
 Termodynamika i właściwości fizyczne stopów - zastosowanie w przemyśle Marcela Trybuła Władysław Gąsior Alain Pasturel Noel Jakse Plan: 1. Materiał badawczy 2. Eksperyment Metodologia 3. Teoria Metodologia
Termodynamika i właściwości fizyczne stopów - zastosowanie w przemyśle Marcela Trybuła Władysław Gąsior Alain Pasturel Noel Jakse Plan: 1. Materiał badawczy 2. Eksperyment Metodologia 3. Teoria Metodologia
Prowadzący. http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5)
 Tomasz Lubera dr Tomasz Lubera mail: luberski@interia.pl Prowadzący http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5) Konsultacje: we wtorki
Tomasz Lubera dr Tomasz Lubera mail: luberski@interia.pl Prowadzący http://luberski.w.interia.pl telefon PK: 126282746 Pokój 210A (Katedra Biotechnologii i Chemii Fizycznej C-5) Konsultacje: we wtorki
Laboratorium techniki laserowej. Ćwiczenie 5. Modulator PLZT
 Laboratorium techniki laserowej Katedra Optoelektroniki i Systemów Elektronicznych, WETI, Politechnika Gdaoska Gdańsk 006 1.Wstęp Rozwój techniki optoelektronicznej spowodował poszukiwania nowych materiałów
Laboratorium techniki laserowej Katedra Optoelektroniki i Systemów Elektronicznych, WETI, Politechnika Gdaoska Gdańsk 006 1.Wstęp Rozwój techniki optoelektronicznej spowodował poszukiwania nowych materiałów
Układ termodynamiczny Parametry układu termodynamicznego Proces termodynamiczny Układ izolowany Układ zamknięty Stan równowagi termodynamicznej
 termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
powierzchnia rozdziału - dwie fazy ciekłe - jedna faza gazowa - dwa składniki
 Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
E dec. Obwód zastępczy. Napięcie rozkładowe
 Obwód zastępczy Obwód zastępczy schematyczny obwód elektryczny, ilustrujący zachowanie się badanego obiektu w polu elektrycznym. Elementy obwodu zastępczego (oporniki, kondensatory, indukcyjności,...)
Obwód zastępczy Obwód zastępczy schematyczny obwód elektryczny, ilustrujący zachowanie się badanego obiektu w polu elektrycznym. Elementy obwodu zastępczego (oporniki, kondensatory, indukcyjności,...)
Symulacja Monte Carlo izotermy adsorpcji w układzie. ciało stałe-gaz
 Ćwiczenie nr 2 Symulacja Monte Carlo izotermy adsorpcji w układzie ciało stałe-gaz I. Cel ćwiczenia Celem ćwiczenia jest określenie wpływu parametrów takich jak temperatura, energia oddziaływania cząsteczka-powierzchnia
Ćwiczenie nr 2 Symulacja Monte Carlo izotermy adsorpcji w układzie ciało stałe-gaz I. Cel ćwiczenia Celem ćwiczenia jest określenie wpływu parametrów takich jak temperatura, energia oddziaływania cząsteczka-powierzchnia
Termodynamika Część 3
 Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
Termodynamika Część 3 Formy różniczkowe w termodynamice Praca i ciepło Pierwsza zasada termodynamiki Pojemność cieplna i ciepło właściwe Ciepło właściwe gazów doskonałych Ciepło właściwe ciała stałego
WYKŁAD 2 TERMODYNAMIKA. Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami
 WYKŁAD 2 TERMODYNAMIKA Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami Zasada zerowa Kiedy obiekt gorący znajduje się w kontakcie cieplnym z obiektem zimnym następuje
WYKŁAD 2 TERMODYNAMIKA Termodynamika opiera się na czterech obserwacjach fenomenologicznych zwanych zasadami Zasada zerowa Kiedy obiekt gorący znajduje się w kontakcie cieplnym z obiektem zimnym następuje
Technologie wytwarzania metali. Odlewanie Metalurgia proszków Otrzymywanie monokryształów Otrzymywanie materiałów superczystych Techniki próżniowe
 Technologie wytwarzania metali Odlewanie Metalurgia proszków Otrzymywanie monokryształów Otrzymywanie materiałów superczystych Techniki próżniowe KRYSTALIZACJA METALI I STOPÓW Krzepnięcie - przemiana fazy
Technologie wytwarzania metali Odlewanie Metalurgia proszków Otrzymywanie monokryształów Otrzymywanie materiałów superczystych Techniki próżniowe KRYSTALIZACJA METALI I STOPÓW Krzepnięcie - przemiana fazy
Technologie wytwarzania metali. Odlewanie Metalurgia proszków Otrzymywanie monokryształów Otrzymywanie materiałów superczystych Techniki próżniowe
 Technologie wytwarzania metali Odlewanie Metalurgia proszków Otrzymywanie monokryształów Otrzymywanie materiałów superczystych Techniki próżniowe KRYSTALIZACJA METALI I STOPÓW Krzepnięcie - przemiana fazy
Technologie wytwarzania metali Odlewanie Metalurgia proszków Otrzymywanie monokryształów Otrzymywanie materiałów superczystych Techniki próżniowe KRYSTALIZACJA METALI I STOPÓW Krzepnięcie - przemiana fazy
Program MC. Obliczyć radialną funkcję korelacji. Zrobić jej wykres. Odczytać z wykresu wartość radialnej funkcji korelacji w punkcie r=
 Program MC Napisać program symulujący twarde kule w zespole kanonicznym. Dla N > 100 twardych kul. Gęstość liczbowa 0.1 < N/V < 0.4. Zrobić obliczenia dla 2,3 różnych wartości gęstości. Obliczyć radialną
Program MC Napisać program symulujący twarde kule w zespole kanonicznym. Dla N > 100 twardych kul. Gęstość liczbowa 0.1 < N/V < 0.4. Zrobić obliczenia dla 2,3 różnych wartości gęstości. Obliczyć radialną
Wytwarzanie niskowymiarowych struktur półprzewodnikowych
 Większość struktur niskowymiarowych wytwarzanych jest za pomocą technik epitaksjalnych. Najczęściej wykorzystywane metody wzrostu: - epitaksja z wiązki molekularnej (MBE Molecular Beam Epitaxy) - epitaksja
Większość struktur niskowymiarowych wytwarzanych jest za pomocą technik epitaksjalnych. Najczęściej wykorzystywane metody wzrostu: - epitaksja z wiązki molekularnej (MBE Molecular Beam Epitaxy) - epitaksja
Studnia skończona. Heterostruktury półprzewodnikowe studnie kwantowe (cd) Heterostruktury mogą mieć różne masy efektywne w różnych obszarach:
 Heterostruktury półprzewodnikowe studnie kwantowe (cd) Studnia skończona Heterostruktury mogą mieć różne masy efektywne w różnych obszarach: V z Okazuje się, że zamiana nie jest dobrym rozwiązaniem problemu
Heterostruktury półprzewodnikowe studnie kwantowe (cd) Studnia skończona Heterostruktury mogą mieć różne masy efektywne w różnych obszarach: V z Okazuje się, że zamiana nie jest dobrym rozwiązaniem problemu
Fizyka powierzchni. Dr Piotr Sitarek. Katedra Fizyki Doświadczalnej, Wydział Podstawowych Problemów Techniki, Politechnika Wrocławska
 Fizyka powierzchni 1 Dr Piotr Sitarek Katedra Fizyki Doświadczalnej, Wydział Podstawowych Problemów Techniki, Politechnika Wrocławska Lista zagadnień Fizyka powierzchni i międzypowierzchni, struktura powierzchni
Fizyka powierzchni 1 Dr Piotr Sitarek Katedra Fizyki Doświadczalnej, Wydział Podstawowych Problemów Techniki, Politechnika Wrocławska Lista zagadnień Fizyka powierzchni i międzypowierzchni, struktura powierzchni
ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa
 Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Wprowadzenie do WK1 Stan naprężenia
 Wytrzymałość materiałów i konstrukcji 1 Wykład 1 Wprowadzenie do WK1 Stan naprężenia Płaski stan naprężenia Dr inż. Piotr Marek Wytrzymałość Konstrukcji (Wytrzymałość materiałów, Mechanika konstrukcji)
Wytrzymałość materiałów i konstrukcji 1 Wykład 1 Wprowadzenie do WK1 Stan naprężenia Płaski stan naprężenia Dr inż. Piotr Marek Wytrzymałość Konstrukcji (Wytrzymałość materiałów, Mechanika konstrukcji)
Ciśnienie i temperatura model mikroskopowy
 Ciśnienie i temperatura model mikroskopowy Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy
Ciśnienie i temperatura model mikroskopowy Mikroskopowy model ciśnienia gazu wzór na ciśnienie gazu Mikroskopowa interpretacja temperatury Średnia energia cząsteczki gazu zasada ekwipartycji energii Czy
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego
 Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
S. Baran - Podstawy fizyki materii skondensowanej Fonony. Fonony
 Fonony Drgania płaszczyzn sieciowych podłużne poprzeczne źródło: Ch. Kittel Wstęp do fizyki..., rozdz. 4, rys. 2, 3, str. 118 Drgania płaszczyzn sieciowych Do opisu drgań sieci krystalicznej wystarczą
Fonony Drgania płaszczyzn sieciowych podłużne poprzeczne źródło: Ch. Kittel Wstęp do fizyki..., rozdz. 4, rys. 2, 3, str. 118 Drgania płaszczyzn sieciowych Do opisu drgań sieci krystalicznej wystarczą
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek
 Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 17 KLASYCZNA DYNAMIKA MOLEKULARNA 17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek Rozważamy układ N punktowych cząstek
Janusz Adamowski METODY OBLICZENIOWE FIZYKI 1 Rozdział 17 KLASYCZNA DYNAMIKA MOLEKULARNA 17.1 Podstawy metod symulacji komputerowych dla klasycznych układów wielu cząstek Rozważamy układ N punktowych cząstek
Wzrost fazy krystalicznej
 Wzrost fazy krystalicznej Wydzielenie nowej fazy może różnić się of fazy pierwotnej : składem chemicznym strukturą krystaliczną orientacją krystalograficzną... faza pierwotna nowa faza Analogia elektryczna
Wzrost fazy krystalicznej Wydzielenie nowej fazy może różnić się of fazy pierwotnej : składem chemicznym strukturą krystaliczną orientacją krystalograficzną... faza pierwotna nowa faza Analogia elektryczna
Struktura energetyczna ciał stałych. Fizyka II dla EiT oraz E, lato
 Struktura energetyczna ciał stałych Fizyka II dla EiT oraz E, lato 016 1 Struktura kryształu Doskonały kryształ składa się z uporządkowanych atomów w sieci krystalicznej, opisanej przez trzy podstawowe
Struktura energetyczna ciał stałych Fizyka II dla EiT oraz E, lato 016 1 Struktura kryształu Doskonały kryształ składa się z uporządkowanych atomów w sieci krystalicznej, opisanej przez trzy podstawowe
Termodynamika. Część 4. Procesy izoparametryczne Entropia Druga zasada termodynamiki. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Termodynamika Część 4 Procesy izoparametryczne Entropia Druga zasada termodynamiki Janusz Brzychczyk, Instytut Fizyki UJ Pierwsza zasada termodynamiki procesy kwazistatyczne Zgodnie z pierwszą zasadą termodynamiki,
Ciała stałe. Ciała krystaliczne. Ciała amorficzne. Bardzo często mamy do czynienia z ciałami polikrystalicznymi, rzadko monokryształami.
 Ciała stałe Ciała krystaliczne Ciała amorficzne Bardzo często mamy do czynienia z ciałami polikrystalicznymi, rzadko monokryształami. r T = Kryształy rosną przez regularne powtarzanie się identycznych
Ciała stałe Ciała krystaliczne Ciała amorficzne Bardzo często mamy do czynienia z ciałami polikrystalicznymi, rzadko monokryształami. r T = Kryształy rosną przez regularne powtarzanie się identycznych
