Wykład 14 Przejścia fazowe
|
|
|
- Jacek Leśniak
- 8 lat temu
- Przeglądów:
Transkrypt
1 Wykład 14 Przejścia fazowe Z izoterm gazu Van der Waalsa (rys.14.1) wynika, że dla T < T k izotermy zawierają obszary w których gaz Van der Waalsa zachowuje się niefizycznie. W tych niefizycznych obszarach zwiększenie objętości gazu powoduję zwiększenie jego ciśnienia. Takie gazy w przyrodzie nie istnieją i w rzeczywistym eksperymencie w punkcie C / ciśnienie gazu przestaje rosnąć aż do punktu C (rys.14.1). Z doświadczeń wynika również, że w obszarze od punktu C / do punktu C w naczyniu zawierającym gaz oprócz gazu obserwują się również kropli cieczy. A zatem ten obszar na izotermie Van der Waalsa odpowiada stanowi niejednorodnemu substancji: jednocześnie istnieją tu faza gazowa i faza ciekła. W termodynamice fazą nazywamy jednorodny zespół części posiadających taki sam skład chemiczny i takie same właściwości fizyczne. Rys Izoterma Van der Waalsa 173
2 W punkcie C gaz całkowicie przechodzi w stan ciekły i dalej przy obniżaniu ciśnienia ciecz zachowuję się zgodnie z równaniem Van der Waalsa. Natomiast w punkcie C / znikają kropli cieczy i pozostaje tylko faza gazowa. Przejście fazowe C C / odbywa się w stałej temperaturze (temperatura wrzenia) i pod stałym ciśnieniem. Gaz, który znajduje się w stanie równowagi ze swoją cieczą w obszarze między punktami C i C / nazywamy parą nasyconą. Ciśnienie p p.n. przy którym istnieje równowaga gazu ze swoją cieczą w określonej temperaturze nazywamy ciśnieniem pary nasyconej. Z powyższych rozważań wynika, że dla tego żeby otrzymać równanie poprawnie opisujące gaz rzeczywisty, musimy rozwiązanie Van der Waalsa w obszarze niejednorodnym zastąpić odcinkiem linii poziomej (rys.14.1). Wykażemy, że linię poziomą, którą przyjmuje się za rozwiązanie prawidłowe, musimy narysować tak, aby pola powierzchni S i S / były równe. Rozważmy cykl odwracalny izotermiczny wzdłuż krzywej CADBC / DC. Zgodnie z pierwszą zasadą termodynamiki dla takiego cyklu ds du + T = pdv. (14.1) Rys Izotermy Van der Waalsa 174
3 Ponieważ proces jest izotermiczny i odwracalnie zamknięty pierwsze dwie całki po lewej stronie równania (14.1) są równe zeru, a zatem pdv = 0. (14.2) Równość (14.2) zachodzi tylko wtedy, gdy pola powierzchni S i S / są sobie równe. Zwiększanie temperatury powoduje, że długość linii poziomej C-C / maleje i w temperaturze T k linia ta ściska się do punktu K (rys.14.2). Więc przy temperaturach większych od T k stan substancji staje się jednorodny i substancja może znajdować się tylko w fazie gazowej. Rys Krzywa stanu substancji. 175
4 Przy temperaturach mniejszych od T k substancja może znajdować się w fazie ciekłej, w fazie "przejściowej", gdy istnieje cieć i para nasycona, oraz w fazie gazowej (rys.14.2). Temperatura T k nazywa się temperaturą krytyczną. W punkcie K wszystkie możliwe fazy substancji istnieją jednocześnie. Punkt ten nazywa się punktem krytycznym. Zwykle przy przejściu z jednej fazy do drugiej koniecznie jest doprowadzenie do substancji lub odprowadzenie z substancji ciepła. Ciepło to nazywamy ciepłem przejścia fazowego. Na przykład przy tąpnięciu lodu zachodzi pochłonięcie ciepła. Taka sama ilość ciepła wydziela się przy przejściu wody do fazy stałej (lodu). Przejścia fazowe, przy których musimy doprowadzić (lub odprowadzić) ciepło do układu nazywamy przejściami fazowymi pierwszego rodzaju. W niektórych ciałach stałych przy przejściach fazowych od jednej struktury krystalicznej do drugiej nie zachodzi absorpcja albo emisja ciepła. Takie przejścia fazowe nazywamy przejściami fazowymi drugiego rodzaju. Dla przejść fazowych drugiego rodzaju gęstość substancji nie zmienia się. Natomiast tracą ciągłość krzywa zależności temperaturowej ciepła właściwego i inne charakterystyki substancji. Przykładami przejścia drugiego rodzaju są: przejście żelaza ze stanu magnetycznie uporządkowanego do stanu paramagnetycznego; przejście niektórych ciał w bardzo niskich temperaturach w stan nadprzewodnictwa itd. Przy przejściu od jednej fazy substancji do drugiej w fazie przejściowej różne fazy istnieją jednocześnie. Równowaga różnych faz obserwuje się w skończonym obszarze temperatur. Przy tym dla każdej temperatury T istnieję swoje ciśnienie p. Krzywa p = f(t) określa warunki, w których mogą istnieć różne fazy substancji (rys.14.3). Za pomocą krzywej stanu substancji p = f(t) łatwo przepowiedzieć "los" substancji. Na przykład, jeżeli weźmiemy substancję, której stan określa punkt 1 na rys.14.3 i zaczniemy przy stałym ciśnieniu (izobarycznie) ogrzewać tą substancję, to jak widać z rys.14.3 stan substancji będzie zmieniał się wzdłuż krzywej 1-2: ciało stałe - ciecz - gaz. Jeżeli rozważmy punkt 3, to przy izobarycznym ogrzewaniu stan substancji zmienia się wzdłuż krzywej 3-4: ciało stałe - gaz. A zatem przejście fazowe wzdłuż prostej 3-4 omija stan ciekły. Takie przejście fazowe od stanu stałego w gazowy nazywamy sublimacją. Przejście fazowe ze stanu stałego w stan ciekły nazywamy topnieniem. Ciała krystaliczne i amorficzne Każda substancja ciekła (z wyjątkiem helu) podczas oziębiania traci swoje własności ciekłe i przechodzi w ciało stałe. Jednakże proces przejścia ze stanu ciekłego w stan stały dla 176
5 różnych substancji jest różny. Znane są dwa procesy zestalania się cieczy. Pierwszy proces nosi nazwę krystalizacji i polega na tym, że w cieczy, oziębionej do określonej temperatury, pojawiają się tzw. centra krystalizacji - drobne kryształki, czyli obszary uporządkowanych i trwale związanych ze sobą cząstek. W warunkach umożliwiających swobodny wzrost, przy dalszym oziębianiu cieczy centra krystalizacji rozrastają się w kryształy, tj. w trójwymiarowe okresowe ułożenia atomów, lub grup atomów (rys.14.4). Dla drugiego procesu zestalanie się cieczy zachodzi wskutek stosunkowo szybkiego zwiększenia lepkości cieczy przy obniżaniu temperatury. Znane są dwa rodzaje tego procesu zestalania się. W niektórych substancjach (lak, wosk, smoła i inne) w ogóle nie obserwuje się krystalizacji. Takie substancje nie występują w postaci krystalicznej i noszą nazwę ciał amorficznych. Rys Komórka elementarna. 177
6 Inne substancje, na przykład szkło, są zdolne do krystalizacji. Jednak wskutek szybkiego wzrostu ich lepkości przy obniżaniu temperatury (co powoduje, że ruch cząsteczek konieczny do uformowania się i wzrostu kryształu jest utrudniony) substancja zestala się wcześniej niż nastąpi krystalizacja. Substancje takie nazywamy szkłopodobnymi. Substancje szkłopodobne samorzutnie powoli przekształcają się w postać krystaliczną. Różnica między amorficznymi, szkłopodobnymi i krystalicznymi ciałami nie ogranicza się tylko do osobliwości, które występują podczas zestalania się odpowiednich cieczy Jedną z podstawowych cech ciał krystalicznych jest anizotropia ich własności fizycznych, tj. zależność własności fizycznych ciała od kierunku w tym ciele. Na przykład, jeżeli umieścimy kryształ w polu elektrycznym kondensatora i będziemy mierzyli prąd elektryczny przepływający przez kryształ przy stałej wartości napięcia na kondensatorze, to zauważymy, że przy obrocie kryształu wokół dowolnej osi wartość prądu elektrycznego zmienia się. Mówimy, że kryształ jest anizotropowy ze względu na przewodnictwo elektryczne. Najbardziej widocznym efektem anizotropii kryształów jest ich wzrost: kryształy przy wzroście nie przyjmują postaci kuli, a mają postać symetrycznego wielościanu. Podstawą budowy kryształów jest komórka elementarna kryształu (rys.14.4). Cały kryształ możemy "zbudować" powtarzając wielokrotnie w trzech wymiarach komórkę elementarną. Jedną z podstawowych cech ciał krystalicznych jest ich zdolność przyjmować postać symetrycznego wielościanu. Symetria formy zewnętrznej kryształów jest wyrazem osobliwości ich budowy wewnętrznej i ujawnia się w tym, że wielościan krystaliczny może pokrywać się z sobą za pomocą przekształceń symetrycznych. Do elementów symetrii wielościanów krystalicznych należą: płaszczyzna symetrii, środek symetrii, oś symetrii, oś inwersyjna. Badaniem symetrii budowy kryształów zajmuje się krystalografia. W zależności od istniejących w krysztale elementów symetrii wszystkie kryształy zostały podzielone na siedem układów krystalicznych. Układ krystaliczny Parametry komórki elementarnej Trójskośny a b c α β γ Jednoskośny a b c α = γ = 90 0 β Rombowy a b c α = β = γ = 90 0 Tetragonalny a = b c α = β = γ = 90 0 Regularny a = b = c α = β = γ = 90 0 Heksagonalny a = b c Trygonalny α = β = 90 0 γ =
7 Ciała krystaliczne, w zależności od charakteru wiązań chemicznych dzielimy na: kryształy jonowe; kryształy kowalencyjne (atomowe); kryształy metaliczne; kryształy molekularne. W kryształach jonowych w węzłach sieci krystalicznej znajdują się jony różnych znaków. Wiązanie między jonami naładowanymi dodatnie i ujemnie zachodzi wskutek oddziaływania Coulomba. Takie wiązanie nazywamy wiązaniem jonowym albo heteropolarnym. Przykładem kryształu jonowego jest sól kuchenna (NaCl - chlorek sodu). Energia tego wiązania rzędu 1000 kj/mol. W krysztale kowalentnym, w odróżnieniu od kryształów jonowych, w których każdy jon oddziałuje ze wszystkimi pozostałymi jonami, wiązanie chemiczne występuje tylko między parą neutralnych atomów. Wiązanie to nosi nazwę wiązania kowalencyjnego albo homopolarnego Wiązanie to powstaje wskutek wzajemnego nakrywania się powłok elektronowych atomów. Przykładami kryształów atomowych są grafit, diament, które są po prostu różnymi odmianami C (węgła). Energia wiązania kowalencyjnego też rzędu 1000 kj/mol. (W ostatnich latach intensywnie badają kryształy zbudowany z dużych molekuł C 60 - fullerenów). W kryształach metalicznych w węzłach sieci znajdują się ciężkie jony naładowane dodatnie. Elektrony swobodne, podobne cząstkom gazu chaotyczne poruszając między węzłami sieci tworzą ujemnie naładowany "klej", który kompensuje odpychanie elektrostatyczne między dodatnie naładowanymi jonami nie dając im możliwości rozlecieć się w różne strony. Energia wiązania metalicznego jest rzędu 100 kj/mol. W kryształach molekularnych w węzłach sieci znajdują się molekuły neutralny elektryczne. Jednak w takich molekułach, wskutek niewielkich deformacji molekuły albo asymetrii w budowie molekuły, zachodzi przesuniecie ładunku elektrycznego ujemnego względem ładunku elektrycznego dodatniego. Molekuła taka posiada tak zwany moment dipolowy. Między dipolowymi momentami różnych molekuł działa siła przyciągania, która utrzymuje molekuły w stanie krystalicznym. Siły taki nazywamy siłami Van der Waalsa. Są oni najsłabszymi ze wszystkich sił: Coulomba, kowalencyjnych, metalicznych.. Wskutek małej wartości sił Van der Waalsa kryształy molekularne istnieją w bardzo niskich temperaturach. Przykładami kryształów molekularnych są tlen (O 2 ), azot (N 2 ), wodór (H 2 ). Energia wiązania kryształów molekularnych jest rzędu 10 kj/mol. 179
8 Cieczy Cieczy zajmują położenie środkowe między ciałami stałymi i gazami. Z jednej strony ciecz, podobnie do gazu, zawsze przyjmuje kształt naczynia, w jakim znajduje się. Ciecz, tak samo jak gaz płynie. Z drugiej strony w cieczy, jak w ciele stałym główną role zaczynają odgrywać oddziaływania wzajemne między cząstkami. Ciecze podobnie jak ciała stałe, są mało ściśliwe i mają stosunkowo dużą gęstość. Z nowoczesnych badań mikroskopowej struktury cieczy wynika, że w cieczy każda molekuła ma prawie podobne otoczenie. Mówimy, że w cieczy w rozmieszczeniu cząstek istnieje uporządkowanie bliskiego zasięgu. W gazie takiego uporządkowania nie ma. Jednak, w odróżnieniu od ciał krystalicznych w cieczach nie ma uporządkowania dalekiego zasięgu. Istnienie w cieczy uporządkowania bliskiego zasięgu i brak uporządkowania dalekiego zasięgu możemy wytłumaczyć w następujący sposób. W procesie topnienia ciała stałego objętość cieczy nieznacznie wzrasta. Pozwala to rozpatrywać cieć jako ciało stałe rozerwane w różnych miejscach. Z tego powodu najbliższe otoczenie każdej cząstki w cieczy jest podobne do otoczenia w ciele stałym. Natomiast uporządkowanie dalekiego zasięgu znika. Zwiększenie objętości ciała przy topnieniu a zatem powstawanie dodatkowej wolnej od cząstek przestrzeni tłumaczy też płynność cieczy. Większość cieczy ma izotropowe właściwości fizyczne. Są jednak cieczy zbudowane z długich molekuł organicznych, w których wskutek istnienia uporządkowania w rozmieszczeniu osi długich molekuł, ciecz wykazuje anizotropię właściwości fizycznych. Takie cieczy znajdują się jeszcze bliżej do kryształów i noszą nazwę kryształów ciekłych. Napięcie powierzchniowe i zwilżanie Ciecz jak ciało stałe jest ograniczona powierzchnią. W warstwie cieczy, która znajduje się około powierzchni cieczy oddziaływanie molekuł cieczy różni się od oddziaływań molekuł znajdujących się wgłębi cieczy. Na molekuły, które znajdują się wgłębi cieczy działają siły ze strony wszystkich molekuł otoczenia tak, że wypadkowa siła działająca na molekułę równa zeru. Molekuły w warstwie przypowierzchniowej mają w otoczeniu molekuły cieczy tylko z jednej strony, wskutek czego wypadkowa siła działająca na takie "powierzchniowe" molekuły nie jest równa zeru i jest skierowana wgłęb cieczy. Siła działająca na molekuły w warstwie przypowierzchniowej maleje, gdy przechodzimy wgłęb cieczy. Wskutek istnienia sił powierzchniowych przemieszczenie molekuły z wewnętrznej części cieczy na powierzchnie wymaga wykonania pracy ujemnej, a zatem molekuły w warstwie przypowierzchniowej posiadają dodatkową energią potencjalną, która daje dodatkową energię do całkowitej 180
9 wewnętrznej energii cieczy. Energia potencjalna warstwy powierzchniowej jest wprost proporcjonalna do pola powierzchni otaczającej ciecz, a zatem jeżeli zwiększamy na przykład pole powierzchni cieczy o ds, to zwiększamy energię potencjalna powierzchniową o du. Stosunek du σ = (14.3) ds nazywamy współczynnikiem napięcia powierzchniowego. Współczynnik ten zależy od temperatury: ze wzrostem temperatury on maleje i jest równy zeru w temperaturze krytycznej. Jeżeli powierzchnia cieczy jest ograniczona przez obwód zwilżania (perymetr zwilżania), to wartość σ jest równa sile działającej na jednostkę długości tego obwodu zwilżania. Siła ta leży w płaszczyźnie stycznej do powierzchni cieczy i jest skierowana prostopadle do obwodu zwilżania. Stanowi równowagi układu fizycznego, jak wiemy, odpowiada minimum energii potencjalnej układu. Z tego powodu stanowi równowagi cieczy odpowiada taki stan, dla którego stosunek powierzchni do objętości jest minimalny. Ze wszystkich możliwych kształtów, tylko kula ma najmniejszą powierzchnie względem objętości, a zatem istnienie energii potencjalnej powierzchniowej cieczy powoduje, że kropli cieczy swobodnej przyjmują kształt kuli. W przypadku, gdy ciecz znajduję się w kontakcie z ciałem stałym oraz gazem musimy uwzględnić natężenia powierzchniowe na granice wszystkich kontaktujących ciał. Rozważmy kroplę cieczy na powierzchni poziomej stołu (rys.14.5). Kropla może płynąć po powierzchni stołu. A zatem, żeby mieliśmy stan równowagowy kropli i kropla nie mogła poruszać się, suma rzutów wszystkich sił działających w każdym punkcie cieczy znajdującym się na powierzchni stołu musi być równa zeru. Oznaczmy przez σ s,c natężenie powierzchniowe na granice ciało stałe i ciecz; przez σ s,g natężenie powierzchniowe na granice ciało stałe i gaz, oraz przez σ c,g natężenie powierzchniowe na granice ciecz i gaz. Oznaczmy kąt między stycznymi do powierzchni ciała stałego i powierzchni kropli jako kat ϑ (rys.14.5). Kąt ϑ nazywamy katem zwilżania. W stanie równowagi kropli (rys.14.5a) σ s, g = σ s, c + σ c, g cosϑ. (14.4) 181
10 Rys Zwilżanie powierzchni. Jeżeli σ s,g σ s,c + σ c,g warunek (14.4) może być spełniony tylko wtedy, gdy mamy znak równości. W tym przypadku ϑ = 0 0, a zatem kropla po prostu rozpływa się po powierzchni stołu. Mówimy, że w tym przypadku mamy zwilżanie doskonałe. Jeżeli σ s,c σ s,g + σ c,g warunek (14.4) może być spełniony tylko, gdy mamy znak równości. W tym przypadku ϑ = 180 0, a zatem kropla całkowicie oddziela się od powierzchni stołu stykając z nim w jednym punkcie. Mówimy, że w tym przypadku mamy niezwilżanie doskonałe. Przypadkowi ϑ 90 0, zgodnie z równaniem (14.4) odpowiada warunek σ s,g σ s,c. Jeżeli kąt krajowy ϑ 90 0, mówimy, ciecz zwilża powierzchnię (rys.14.5b). Jeżeli ϑ 90 0, mówimy, że ciecz nie zwilża powierzchnię (rys.14.5c). Zgodnie z równaniem (14.4) temu odpowiada warunek σ s,g σ s,c. 182
11 Zjawiska kapilarne Dążenie powierzchni cieczy do zmniejszenie swojej powierzchni powoduje, że ciśnienie pod powierzchnią wykrzywionej jest inne niż pod powierzchnią płaskiej. Dodatkowe ciśnienie, które powstaje wskutek wykrzywienia powierzchni cieczy musi zależeć od natężenia powierzchniowego oraz od krzywizny powierzchni. Znajdziemy dodatkowe ciśnienie na najprostszym przykładzie powierzchni kulistej o promieniu R. Podzielimy kulę na dwie równe połowy. Wskutek istnienia sił natężenia powierzchniowego dwie połowy kuli będą przyciągały się z siłą F = 2πRσ. Rys Menisk 183
12 Ta siła działa na powierzchnię o polu S = πr 2 a zatem dodatkowe ciśnienie, związane z wykrzywieniem powierzchni wynosi F 2σ p = =. (14.5) S R Ciśnienie dodatkowe, związane z wykrzywieniem powierzchni cieczy nosi nazwę ciśnienia kapilarnego. Właśnie wskutek istnienia tego ciśnienia obserwujemy wielu zjawisk kapilarnych: dostarczenie wody do liści przez kapilary drzew; podnoszenie wód gruntowych na powierzchnie Ziemi, pochłanianie wody przez papier itd. Do zjawisk kapilarnych należy też zjawisko powstawania zakrzywionej powierzchni cieczy w pobliżu ścianek naczynia, którą nazywamy meniskiem. Jeżeli ciecz zwilża ścianki kapilara, menisk jest wklęsły (rys.14.6a). Jeżeli ciecz nie zwilża ścianki kapilara, menisk ma wypukłą formę (rys.14.6b). Jeżeli kapilar zanurzamy w jakiś duże naczynie, to poziom cieczy w kapilarze jest zawsze inny niż w naczynie. Związane to z tym, że dodatkowe ciśnienie powierzchniowe w kapilarze powoduje, że ciśnie na powierzchni cieczy naczynia różni się od ciśnienia na powierzchni cieczy w kapilarze. Różnicę h poziomów cieczy w dużym naczyniu i kapilarze obliczymy z warunku równości ciśnienia kapilarnego (14.5) i ciśnieniem hydrostatycznym 2σ = ρgh R. (14.6) Tu ρ jest gęstością cieczy. Z rys.14.6a widzimy, że R = r/cosϑ, a zatem ze wzoru (14.6) otrzymujemy 2σ h = cos ϑ. (14.7) ρgr Ze wzoru (14.7) wynika, że jeżeli ciecz zwilża ścianki kapilara i ϑ 90 0 (cosϑ 0), ciecz w kapilarze zajmuje wyższy poziom względem poziomu cieczy w naczyniu (h > 0). Jeżeli ciecz nie zwilża ścianki kapilara i ϑ 90 0 (cosϑ 0), ciecz w kapilarze zajmuje niższy poziom względem poziomu cieczy w naczyniu (h < 0). 184
Wykład 1. Symetria Budowy Kryształów
 Wykład Symetria Budowy Kryształów Ciała krystaliczne i amorficzne Każda substancja ciekła (z wyjątkiem helu) podczas oziębiania traci swoje własności ciekłe i przechodzi w ciało stałe. Jednakże proces
Wykład Symetria Budowy Kryształów Ciała krystaliczne i amorficzne Każda substancja ciekła (z wyjątkiem helu) podczas oziębiania traci swoje własności ciekłe i przechodzi w ciało stałe. Jednakże proces
Statyka Cieczy i Gazów. Temat : Podstawy teorii kinetyczno-molekularnej budowy ciał
 Statyka Cieczy i Gazów Temat : Podstawy teorii kinetyczno-molekularnej budowy ciał 1. Podstawowe założenia teorii kinetyczno-molekularnej budowy ciał: Ciała zbudowane są z cząsteczek. Pomiędzy cząsteczkami
Statyka Cieczy i Gazów Temat : Podstawy teorii kinetyczno-molekularnej budowy ciał 1. Podstawowe założenia teorii kinetyczno-molekularnej budowy ciał: Ciała zbudowane są z cząsteczek. Pomiędzy cząsteczkami
Fizyka Ciała Stałego
 Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
Wykład III Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć krystaliczną. Amorficzne, brak uporządkowania,
STRUKTURA CIAŁA STAŁEGO
 STRUKTURA CIAŁA STAŁEGO Podział ciał stałych Ciała - bezpostaciowe (amorficzne) Szkła, żywice, tłuszcze, niektóre proszki. Nie wykazują żadnych regularnych płaszczyzn ograniczających, nie można w nich
STRUKTURA CIAŁA STAŁEGO Podział ciał stałych Ciała - bezpostaciowe (amorficzne) Szkła, żywice, tłuszcze, niektóre proszki. Nie wykazują żadnych regularnych płaszczyzn ograniczających, nie można w nich
Stany skupienia materii
 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -słabo ściśliwe - uporządkowanie bliskiego zasięgu -tworzą powierzchnię
1) Rozmiar atomu to około? Która z odpowiedzi jest nieprawidłowa? a) 0, m b) 10-8 mm c) m d) km e) m f)
 1) Rozmiar atomu to około? Która z odpowiedzi jest nieprawidłowa? a) 0,0000000001 m b) 10-8 mm c) 10-10 m d) 10-12 km e) 10-15 m f) 2) Z jakich cząstek składają się dodatnio naładowane jądra atomów? (e
1) Rozmiar atomu to około? Która z odpowiedzi jest nieprawidłowa? a) 0,0000000001 m b) 10-8 mm c) 10-10 m d) 10-12 km e) 10-15 m f) 2) Z jakich cząstek składają się dodatnio naładowane jądra atomów? (e
BUDOWA KRYSTALICZNA CIAŁ STAŁYCH. Stopień uporządkowania struktury wewnętrznej ciał stałych decyduje o ich podziale
 BUDOWA KRYSTALICZNA CIAŁ STAŁYCH Stopień uporządkowania struktury wewnętrznej ciał stałych decyduje o ich podziale na: kryształy ciała o okresowym regularnym uporządkowaniu atomów, cząsteczek w całej swojej
BUDOWA KRYSTALICZNA CIAŁ STAŁYCH Stopień uporządkowania struktury wewnętrznej ciał stałych decyduje o ich podziale na: kryształy ciała o okresowym regularnym uporządkowaniu atomów, cząsteczek w całej swojej
Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową
 Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową Kryształy Atomy w krysztale ułożone są w pewien powtarzający się regularny wzór zwany siecią krystaliczną. Struktura kryształu NaCl Polikryształy
Podział ciał stałych ze względu na strukturę atomowo-cząsteczkową Kryształy Atomy w krysztale ułożone są w pewien powtarzający się regularny wzór zwany siecią krystaliczną. Struktura kryształu NaCl Polikryształy
Termodynamiczny opis przejść fazowych pierwszego rodzaju
 Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Wykład II Przejścia fazowe 1 Termodynamiczny opis przejść fazowych pierwszego rodzaju Woda występuje w trzech stanach skupienia jako ciecz, jako gaz, czyli para wodna, oraz jako ciało stałe, a więc lód.
Ładunki elektryczne i siły ich wzajemnego oddziaływania. Pole elektryczne. Copyright by pleciuga@ o2.pl
 Ładunki elektryczne i siły ich wzajemnego oddziaływania Pole elektryczne Copyright by pleciuga@ o2.pl Ładunek punktowy Ładunek punktowy (q) jest to wyidealizowany model, który zastępuje rzeczywiste naelektryzowane
Ładunki elektryczne i siły ich wzajemnego oddziaływania Pole elektryczne Copyright by pleciuga@ o2.pl Ładunek punktowy Ładunek punktowy (q) jest to wyidealizowany model, który zastępuje rzeczywiste naelektryzowane
Właściwości kryształów
 Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Wykład 4. Przypomnienie z poprzedniego wykładu
 Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
Wykład 4 Przejścia fazowe materii Diagram fazowy Ciepło Procesy termodynamiczne Proces kwazistatyczny Procesy odwracalne i nieodwracalne Pokazy doświadczalne W. Dominik Wydział Fizyki UW Termodynamika
STRUKTURA KRYSTALICZNA
 PODSTAWY KRYSTALOGRAFII Struktura krystaliczna Wektory translacji sieci Komórka elementarna Komórka elementarna Wignera-Seitza Jednostkowy element struktury Sieci Bravais go 2D Sieci przestrzenne Bravais
PODSTAWY KRYSTALOGRAFII Struktura krystaliczna Wektory translacji sieci Komórka elementarna Komórka elementarna Wignera-Seitza Jednostkowy element struktury Sieci Bravais go 2D Sieci przestrzenne Bravais
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Podstawy fizyki wykład 8
 Podstawy fizyki wykład 8 Dr Piotr Sitarek Instytut Fizyki, Politechnika Wrocławska Ładunek elektryczny Grecy ok. 600 r p.n.e. odkryli, że bursztyn potarty o wełnę przyciąga inne (drobne) przedmioty. słowo
Podstawy fizyki wykład 8 Dr Piotr Sitarek Instytut Fizyki, Politechnika Wrocławska Ładunek elektryczny Grecy ok. 600 r p.n.e. odkryli, że bursztyn potarty o wełnę przyciąga inne (drobne) przedmioty. słowo
Krystalizacja. Zarodkowanie
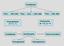 Krystalizacja Ciecz ciało stałe Para ciecz ciało stałe Para ciało stałe Przechłodzenie T = T L - T c Przesycenie p = p g - p z > 0 Krystalizacja Zarodkowanie Rozrost zarodków Homogeniczne Heterogeniczne
Krystalizacja Ciecz ciało stałe Para ciecz ciało stałe Para ciało stałe Przechłodzenie T = T L - T c Przesycenie p = p g - p z > 0 Krystalizacja Zarodkowanie Rozrost zarodków Homogeniczne Heterogeniczne
Klasyfikacja przemian fazowych
 Klasyfikacja przemian fazowych Faza- jednorodna pod względem własności część układu, oddzielona od pozostałej częsci układu powierzchnią graniczną, po której przekroczeniu własności zmieniaja się w sposób
Klasyfikacja przemian fazowych Faza- jednorodna pod względem własności część układu, oddzielona od pozostałej częsci układu powierzchnią graniczną, po której przekroczeniu własności zmieniaja się w sposób
Wykład 1. Anna Ptaszek. 5 października Katedra Inżynierii i Aparatury Przemysłu Spożywczego. Chemia fizyczna - wykład 1. Anna Ptaszek 1 / 36
 Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 1 Katedra Inżynierii i Aparatury Przemysłu Spożywczego 5 października 2015 1 / 36 Podstawowe pojęcia Układ termodynamiczny To zbiór niezależnych elementów, które oddziałują ze sobą tworząc integralną
Wykład 6. Klasyfikacja przemian fazowych
 Wykład 6 Klasyfikacja przemian fazowych JS Klasyfikacja Ehrenfesta Ehrenfest klasyfikuje przemiany fazowe w oparciu o potencjał chemiczny. nieciągłość Przemiany fazowe pierwszego rodzaju pochodne potencjału
Wykład 6 Klasyfikacja przemian fazowych JS Klasyfikacja Ehrenfesta Ehrenfest klasyfikuje przemiany fazowe w oparciu o potencjał chemiczny. nieciągłość Przemiany fazowe pierwszego rodzaju pochodne potencjału
Elementy teorii powierzchni metali
 prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
prof. dr hab. Adam Kiejna Elementy teorii powierzchni metali Wykład 4 v.16 Wiązanie metaliczne Wiązanie metaliczne Zajmujemy się tylko metalami dlatego w zasadzie interesuje nas tylko wiązanie metaliczne.
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY
 WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
WŁASNOŚCI CIAŁ STAŁYCH I CIECZY Polimery Sieć krystaliczna Napięcie powierzchniowe Dyfuzja 2 BUDOWA CIAŁ STAŁYCH Ciała krystaliczne (kryształy): monokryształy, polikryształy Ciała amorficzne (bezpostaciowe)
WIĄZANIA. Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE
 WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
WIĄZANIA Co sprawia, że ciała stałe istnieją i są stabilne? PRZYCIĄGANIE ODPYCHANIE Przyciąganie Wynika z elektrostatycznego oddziaływania między elektronami a dodatnimi jądrami atomowymi. Może to być
Utrwalenie wiadomości. Fizyka, klasa 1 Gimnazjum im. Jana Pawła II w Sułowie
 Utrwalenie wiadomości Fizyka, klasa 1 Gimnazjum im. Jana Pawła II w Sułowie Za tydzień sprawdzian Ciało fizyczne a substancja Ciało Substancja gwóźdź żelazo szklanka szkło krzesło drewno Obok podanych
Utrwalenie wiadomości Fizyka, klasa 1 Gimnazjum im. Jana Pawła II w Sułowie Za tydzień sprawdzian Ciało fizyczne a substancja Ciało Substancja gwóźdź żelazo szklanka szkło krzesło drewno Obok podanych
Wstęp. Krystalografia geometryczna
 Wstęp Przedmiot badań krystalografii. Wprowadzenie do opisu struktury kryształów. Definicja sieci Bravais go i bazy atomowej, komórki prymitywnej i elementarnej. Podstawowe typy komórek elementarnych.
Wstęp Przedmiot badań krystalografii. Wprowadzenie do opisu struktury kryształów. Definicja sieci Bravais go i bazy atomowej, komórki prymitywnej i elementarnej. Podstawowe typy komórek elementarnych.
Termodynamika Część 7 Trzecia zasada termodynamiki Metody otrzymywania niskich temperatur Zjawisko Joule'a Thomsona Chłodzenie magnetyczne
 Termodynamika Część 7 Trzecia zasada termodynamiki Metody otrzymywania niskich temperatur Zjawisko Joule'a Thomsona Chłodzenie magnetyczne Janusz Brzychczyk, Instytut Fizyki UJ Postulat Nernsta (1906):
Termodynamika Część 7 Trzecia zasada termodynamiki Metody otrzymywania niskich temperatur Zjawisko Joule'a Thomsona Chłodzenie magnetyczne Janusz Brzychczyk, Instytut Fizyki UJ Postulat Nernsta (1906):
3. Przejścia fazowe pomiędzy trzema stanami skupienia materii:
 Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
Temat: Zmiany stanu skupienia. 1. Energia sieci krystalicznej- wielkość dzięki której można oszacować siły przyciągania w krysztale 2. Energia wiązania sieci krystalicznej- ilość energii potrzebnej do
Fizyka statystyczna Fenomenologia przejść fazowych. P. F. Góra
 Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych.
 Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
Tematy opisowe 1. Kryształy jonowe omówić oddziaływania w kryształach jonowych oraz typy struktur jonowych. 2. Dlaczego do kadłubów statków, doków, falochronów i filarów mostów przymocowuje się płyty z
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12
 Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Podstawowe pojęcia Masa atomowa (cząsteczkowa) - to stosunek masy atomu danego pierwiastka chemicznego (cząsteczki związku chemicznego) do masy 1/12 atomu węgla 12 C. Mol - jest taką ilością danej substancji,
Nauka o Materiałach Wykład II Monokryształy Jerzy Lis
 Wykład II Monokryształy Jerzy Lis Treść wykładu: 1. Wstęp stan krystaliczny 2. Budowa kryształów - krystalografia 3. Budowa kryształów rzeczywistych defekty WPROWADZENIE Stan krystaliczny jest podstawową
Wykład II Monokryształy Jerzy Lis Treść wykładu: 1. Wstęp stan krystaliczny 2. Budowa kryształów - krystalografia 3. Budowa kryształów rzeczywistych defekty WPROWADZENIE Stan krystaliczny jest podstawową
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ
 CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
CIEPLNE I MECHANICZNE WŁASNOŚCI CIAŁ Ciepło i temperatura Pojemność cieplna i ciepło właściwe Ciepło przemiany Przejścia między stanami Rozszerzalność cieplna Sprężystość ciał Prawo Hooke a Mechaniczne
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wykład 18 Dielektryk w polu elektrycznym
 Wykład 8 Dielektryk w polu elektrycznym Polaryzacja dielektryka Dielektryk (izolator), w odróżnieniu od przewodnika, nie posiada ładunków swobodnych zdolnych do przemieszczenia się na duże odległości.
Wykład 8 Dielektryk w polu elektrycznym Polaryzacja dielektryka Dielektryk (izolator), w odróżnieniu od przewodnika, nie posiada ładunków swobodnych zdolnych do przemieszczenia się na duże odległości.
Zadania treningowe na kolokwium
 Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Zadania treningowe na kolokwium 3.12.2010 1. Stan układu binarnego zawierającego n 1 moli substancji typu 1 i n 2 moli substancji typu 2 parametryzujemy za pomocą stężenia substancji 1: x n 1. Stabilność
Wykład 3. Diagramy fazowe P-v-T dla substancji czystych w trzech stanach. skupienia. skupienia
 Wykład 3 Substancje proste i czyste Przemiany w systemie dwufazowym woda para wodna Diagram T-v dla przejścia fazowego woda para wodna Diagramy T-v i P-v dla wody Punkt krytyczny Temperatura nasycenia
Wykład 3 Substancje proste i czyste Przemiany w systemie dwufazowym woda para wodna Diagram T-v dla przejścia fazowego woda para wodna Diagramy T-v i P-v dla wody Punkt krytyczny Temperatura nasycenia
Stany skupienia materii
 Stany skupienia materii Ciała stałe Ciecze Płyny Gazy Plazma 1 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -
Stany skupienia materii Ciała stałe Ciecze Płyny Gazy Plazma 1 Stany skupienia materii Ciała stałe - ustalony kształt i objętość - uporządkowanie dalekiego zasięgu - oddziaływania harmoniczne Ciecze -
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej jedną z dwóch metod (teorii): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA. Do opisu wiązań chemicznych stosuje się najczęściej metodę (teorię): metoda wiązań walencyjnych (VB)
 CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
CZĄSTECZKA Stanislao Cannizzaro (1826-1910) cząstki - elementy mikroświata, termin obejmujący zarówno cząstki elementarne, jak i atomy, jony proste i złożone, cząsteczki, rodniki, cząstki koloidowe; cząsteczka
Fizyka Ciała Stałego. Struktura krystaliczna. Struktura amorficzna
 Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wykład II Struktura krystaliczna Fizyka Ciała Stałego Ciała stałe można podzielić na: Amorficzne, brak uporządkowania, np. szkła; Krystaliczne, o uporządkowanym ułożeniu atomów lub molekuł tworzącym sieć
Wiązania chemiczne. Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych. 5 typów wiązań
 Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
Wiązania chemiczne Związek klasyfikacji ciał krystalicznych z charakterem wiązań atomowych 5 typów wiązań wodorowe A - H - A, jonowe ( np. KCl ) molekularne (pomiędzy atomami gazów szlachetnych i małymi
KRYTERIA OCEN Z FIZYKI DLA KLASY II GIMNAZJUM. ENERGIA I. NIEDOSTATECZNY - Uczeń nie opanował wiedzy i umiejętności niezbędnych w dalszej nauce.
 KRYTERIA OCEN Z FIZYKI DLA KLASY II GIMNAZJUM ENERGIA - Uczeń nie opanował wiedzy i umiejętności niezbędnych w dalszej nauce. - Wie, kiedy jest wykonywana praca mechaniczna. - Wie, że każde urządzenie
KRYTERIA OCEN Z FIZYKI DLA KLASY II GIMNAZJUM ENERGIA - Uczeń nie opanował wiedzy i umiejętności niezbędnych w dalszej nauce. - Wie, kiedy jest wykonywana praca mechaniczna. - Wie, że każde urządzenie
ROZDZIAŁ I. Symetria budowy kryształów
 ROZDZIAŁ I Symetria budowy kryształów I Ciała krystaliczne i amorficzne Każda substancja ciekła z wyjątkiem helu) podczas oziębiania traci swoje własności ciekłe i przechodzi w ciało stałe Jednakże proces
ROZDZIAŁ I Symetria budowy kryształów I Ciała krystaliczne i amorficzne Każda substancja ciekła z wyjątkiem helu) podczas oziębiania traci swoje własności ciekłe i przechodzi w ciało stałe Jednakże proces
Czym jest prąd elektryczny
 Prąd elektryczny Ruch elektronów w przewodniku Wektor gęstości prądu Przewodność elektryczna Prawo Ohma Klasyczny model przewodnictwa w metalach Zależność przewodności/oporności od temperatury dla metali,
Prąd elektryczny Ruch elektronów w przewodniku Wektor gęstości prądu Przewodność elektryczna Prawo Ohma Klasyczny model przewodnictwa w metalach Zależność przewodności/oporności od temperatury dla metali,
MATERIA. = m i liczby całkowite. ciała stałe. - kryształy - ciała bezpostaciowe (amorficzne) - ciecze KRYSZTAŁY. Periodyczność
 MATERIA ciała stałe - kryształy - ciała bezpostaciowe (amorficzne) - ciecze - gazy KRYSZTAŁY Periodyczność Kryształ (idealny) struktura zbudowana z powtarzających się w przestrzeni periodycznie identycznych
MATERIA ciała stałe - kryształy - ciała bezpostaciowe (amorficzne) - ciecze - gazy KRYSZTAŁY Periodyczność Kryształ (idealny) struktura zbudowana z powtarzających się w przestrzeni periodycznie identycznych
INŻYNIERIA BIOMEDYCZNA
 INŻYNIERIA BIOMEDYCZNA 21.01.2018 1 Stan materii a stan skupienia Stan materii podział z punktu widzenia mikroskopowego (struktury jakie tworzą atomy, cząsteczki, jony) Stan skupienia - forma występowania
INŻYNIERIA BIOMEDYCZNA 21.01.2018 1 Stan materii a stan skupienia Stan materii podział z punktu widzenia mikroskopowego (struktury jakie tworzą atomy, cząsteczki, jony) Stan skupienia - forma występowania
Warunki izochoryczno-izotermiczne
 WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
WYKŁAD 5 Pojęcie potencjału chemicznego. Układy jednoskładnikowe W zależności od warunków termodynamicznych potencjał chemiczny substancji czystej definiujemy następująco: Warunki izobaryczno-izotermiczne
Wymiana ciepła. Ładunek jest skwantowany. q=n. e gdzie n = ±1, ±2, ±3 [1C = 6, e] e=1, C
![Wymiana ciepła. Ładunek jest skwantowany. q=n. e gdzie n = ±1, ±2, ±3 [1C = 6, e] e=1, C Wymiana ciepła. Ładunek jest skwantowany. q=n. e gdzie n = ±1, ±2, ±3 [1C = 6, e] e=1, C](/thumbs/63/50333873.jpg) Wymiana ciepła Ładunek jest skwantowany ładunek elementarny ładunek pojedynczego elektronu (e). Każdy ładunek q (dodatni lub ujemny) jest całkowitą wielokrotnością jego bezwzględnej wartości. q=n. e gdzie
Wymiana ciepła Ładunek jest skwantowany ładunek elementarny ładunek pojedynczego elektronu (e). Każdy ładunek q (dodatni lub ujemny) jest całkowitą wielokrotnością jego bezwzględnej wartości. q=n. e gdzie
Wykład 17 Izolatory i przewodniki
 Wykład 7 Izolatory i przewodniki Wszystkie ciała możemy podzielić na przewodniki i izolatory albo dielektryki. Przewodnikami są wszystkie metale, roztwory kwasów i zasad, roztopione soli, nagrzane gazy
Wykład 7 Izolatory i przewodniki Wszystkie ciała możemy podzielić na przewodniki i izolatory albo dielektryki. Przewodnikami są wszystkie metale, roztwory kwasów i zasad, roztopione soli, nagrzane gazy
Termodynamika Część 2
 Termodynamika Część 2 Równanie stanu Równanie stanu gazu doskonałego Równania stanu gazów rzeczywistych rozwinięcie wirialne równanie van der Waalsa hipoteza odpowiedniości stanów inne równania stanu Równanie
Termodynamika Część 2 Równanie stanu Równanie stanu gazu doskonałego Równania stanu gazów rzeczywistych rozwinięcie wirialne równanie van der Waalsa hipoteza odpowiedniości stanów inne równania stanu Równanie
INŻYNIERIA BIOMEDYCZNA
 INŻYNIERIA BIOMEDYCZNA 19.01.2019 1 Stan materii a stan skupienia Stan materii podział z punktu widzenia mikroskopowego (struktury jakie tworzą atomy, cząsteczki, jony) Stan skupienia - forma występowania
INŻYNIERIA BIOMEDYCZNA 19.01.2019 1 Stan materii a stan skupienia Stan materii podział z punktu widzenia mikroskopowego (struktury jakie tworzą atomy, cząsteczki, jony) Stan skupienia - forma występowania
DEFEKTY SIECI KRYSTALICZNEJ W kryształach rzeczywistych występuje cały szereg wad (defektów), które w istotny sposób wpływają na własności kryształu:
 FIZYKA CIAŁA STAŁEGO Stany skupienia materii, typy i zasięg uporządkowań Kryształ idealny i właściwości kryształów Kryształy rzeczywiste i defekty sieci krystalicznej Ciała amorficzne, rozdaje i cechy
FIZYKA CIAŁA STAŁEGO Stany skupienia materii, typy i zasięg uporządkowań Kryształ idealny i właściwości kryształów Kryształy rzeczywiste i defekty sieci krystalicznej Ciała amorficzne, rozdaje i cechy
Elektrostatyka ŁADUNEK. Ładunek elektryczny. Dr PPotera wyklady fizyka dosw st podypl. n p. Cząstka α
 Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
Równanie gazu doskonałego
 Równanie gazu doskonałego Gaz doskonały to abstrakcyjny model gazu, który zakłada, że gaz jest zbiorem sprężyście zderzających się kulek. Wiele gazów w warunkach normalnych zachowuje się jak gaz doskonały.
Równanie gazu doskonałego Gaz doskonały to abstrakcyjny model gazu, który zakłada, że gaz jest zbiorem sprężyście zderzających się kulek. Wiele gazów w warunkach normalnych zachowuje się jak gaz doskonały.
Aby opisać strukturę krystaliczną, konieczne jest określenie jej części składowych: sieci przestrzennej oraz bazy atomowej.
 2. Podstawy krystalografii Podczas naszych zajęć skupimy się przede wszystkim na strukturach krystalicznych. Kryształem nazywamy (def. strukturalna) substancję stałą zbudowaną z atomów, jonów lub cząsteczek
2. Podstawy krystalografii Podczas naszych zajęć skupimy się przede wszystkim na strukturach krystalicznych. Kryształem nazywamy (def. strukturalna) substancję stałą zbudowaną z atomów, jonów lub cząsteczek
Laboratorium inżynierii materiałowej LIM
 Laboratorium inżynierii materiałowej LIM wybrane zagadnienia fizyki ciała stałego czyli skrót skróconego skrótu dr hab. inż.. Ryszard Pawlak, P prof. PŁP Fizyka Ciała Stałego I. Wstęp Związki Fizyki Ciała
Laboratorium inżynierii materiałowej LIM wybrane zagadnienia fizyki ciała stałego czyli skrót skróconego skrótu dr hab. inż.. Ryszard Pawlak, P prof. PŁP Fizyka Ciała Stałego I. Wstęp Związki Fizyki Ciała
Woda. Najpospolitsza czy najbardziej niezwykła substancja Świata?
 Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
Powtórzenie wiadomości z klasy I. Cząsteczkowa budowa materii. Ciśnienie, prawo Pascala - obliczenia.
 Powtórzenie wiadomości z klasy I Cząsteczkowa budowa materii. Ciśnienie, prawo Pascala - obliczenia. Atomy i cząsteczki 1. Materia składa się z cząsteczek zbudowanych z atomów. 2. Atomy są bardzo małe,
Powtórzenie wiadomości z klasy I Cząsteczkowa budowa materii. Ciśnienie, prawo Pascala - obliczenia. Atomy i cząsteczki 1. Materia składa się z cząsteczek zbudowanych z atomów. 2. Atomy są bardzo małe,
Układ termodynamiczny Parametry układu termodynamicznego Proces termodynamiczny Układ izolowany Układ zamknięty Stan równowagi termodynamicznej
 termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
termodynamika - podstawowe pojęcia Układ termodynamiczny - wyodrębniona część otaczającego nas świata. Parametry układu termodynamicznego - wielkości fizyczne, za pomocą których opisujemy stan układu termodynamicznego,
prof. dr hab. Małgorzata Jóźwiak
 Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Czy równowaga w przyrodzie i w chemii jest korzystna? prof. dr hab. Małgorzata Jóźwiak 1 Pojęcie równowagi łańcuch pokarmowy równowagi fazowe równowaga ciało stałe - ciecz równowaga ciecz - gaz równowaga
Dielektryki polaryzację dielektryka Dipole trwałe Dipole indukowane Polaryzacja kryształów jonowych
 Dielektryki Dielektryk- ciało gazowe, ciekłe lub stałe niebędące przewodnikiem prądu elektrycznego (ładunki elektryczne wchodzące w skład każdego ciała są w dielektryku związane ze sobą) Jeżeli do dielektryka
Dielektryki Dielektryk- ciało gazowe, ciekłe lub stałe niebędące przewodnikiem prądu elektrycznego (ładunki elektryczne wchodzące w skład każdego ciała są w dielektryku związane ze sobą) Jeżeli do dielektryka
powierzchnia rozdziału - dwie fazy ciekłe - jedna faza gazowa - dwa składniki
 Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
Przejścia fazowe. powierzchnia rozdziału - skokowa zmiana niektórych parametrów na granicy faz. kropeki wody w atmosferze - dwie fazy ciekłe - jedna faza gazowa - dwa składniki Przykłady przejść fazowych:
Ciekłe kryształy. - definicja - klasyfikacja - własności - zastosowania
 Ciekłe kryształy - definicja - klasyfikacja - własności - zastosowania Nota biograficzna: Odkrywcą był austriacki botanik F. Reinitzer (1888), który został zaskoczony nienormalnym, dwustopniowym sposobem
Ciekłe kryształy - definicja - klasyfikacja - własności - zastosowania Nota biograficzna: Odkrywcą był austriacki botanik F. Reinitzer (1888), który został zaskoczony nienormalnym, dwustopniowym sposobem
Budowa ciał stałych. sieć krystaliczna układy krystalograficzne sieć realna defekty wiązania w ciałach stałych
 Budowa ciał stałych sieć krystaliczna układy krystalograficzne sieć realna defekty wiązania w ciałach stałych Ciała stałe to substancje o regularnej, przestrzennej budowie krystalicznej, czyli regularnym
Budowa ciał stałych sieć krystaliczna układy krystalograficzne sieć realna defekty wiązania w ciałach stałych Ciała stałe to substancje o regularnej, przestrzennej budowie krystalicznej, czyli regularnym
[ ] ρ m. Wykłady z Hydrauliki - dr inż. Paweł Zawadzki, KIWIS WYKŁAD WPROWADZENIE 1.1. Definicje wstępne
![[ ] ρ m. Wykłady z Hydrauliki - dr inż. Paweł Zawadzki, KIWIS WYKŁAD WPROWADZENIE 1.1. Definicje wstępne [ ] ρ m. Wykłady z Hydrauliki - dr inż. Paweł Zawadzki, KIWIS WYKŁAD WPROWADZENIE 1.1. Definicje wstępne](/thumbs/93/111388021.jpg) WYKŁAD 1 1. WPROWADZENIE 1.1. Definicje wstępne Płyn - ciało o module sprężystości postaciowej równym zero; do płynów zaliczamy ciecze i gazy (brak sztywności) Ciecz - płyn o małym współczynniku ściśliwości,
WYKŁAD 1 1. WPROWADZENIE 1.1. Definicje wstępne Płyn - ciało o module sprężystości postaciowej równym zero; do płynów zaliczamy ciecze i gazy (brak sztywności) Ciecz - płyn o małym współczynniku ściśliwości,
Nadprzewodniki. W takich materiałach kiedy nastąpi przepływ prądu może on płynąć nawet bez przyłożonego napięcia przez długi czas! )Ba 2. Tl 0.2.
 Nadprzewodniki Pewna klasa materiałów wykazuje prawie zerową oporność (R=0) poniżej pewnej temperatury zwanej temperaturą krytyczną T c Większość przewodników wykazuje nadprzewodnictwo dopiero w temperaturze
Nadprzewodniki Pewna klasa materiałów wykazuje prawie zerową oporność (R=0) poniżej pewnej temperatury zwanej temperaturą krytyczną T c Większość przewodników wykazuje nadprzewodnictwo dopiero w temperaturze
Projekt Inżynier mechanik zawód z przyszłością współfinansowany ze środków Unii Europejskiej w ramach Europejskiego Funduszu Społecznego
 Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Zajęcia wyrównawcze z fizyki -Zestaw 4 -eoria ermodynamika Równanie stanu gazu doskonałego Izoprzemiany gazowe Energia wewnętrzna gazu doskonałego Praca i ciepło w przemianach gazowych Silniki cieplne
Wykład 5. Komórka elementarna. Sieci Bravais go
 Wykład 5 Komórka elementarna Sieci Bravais go Doskonały kryształ składa się z atomów jonów, cząsteczek) uporządkowanych w sieci krystalicznej opisanej przez trzy podstawowe wektory translacji a, b, c,
Wykład 5 Komórka elementarna Sieci Bravais go Doskonały kryształ składa się z atomów jonów, cząsteczek) uporządkowanych w sieci krystalicznej opisanej przez trzy podstawowe wektory translacji a, b, c,
FIZYKA Podręcznik: Fizyka i astronomia dla każdego pod red. Barbary Sagnowskiej, wyd. ZamKor.
 DKOS-5002-2\04 Anna Basza-Szuland FIZYKA Podręcznik: Fizyka i astronomia dla każdego pod red. Barbary Sagnowskiej, wyd. ZamKor. WYMAGANIA NA OCENĘ DOPUSZCZAJĄCĄ DLA REALIZOWANYCH TREŚCI PROGRAMOWYCH Kinematyka
DKOS-5002-2\04 Anna Basza-Szuland FIZYKA Podręcznik: Fizyka i astronomia dla każdego pod red. Barbary Sagnowskiej, wyd. ZamKor. WYMAGANIA NA OCENĘ DOPUSZCZAJĄCĄ DLA REALIZOWANYCH TREŚCI PROGRAMOWYCH Kinematyka
Atomy wieloelektronowe i cząsteczki
 Atomy wieloelektronowe i cząsteczki 1 Atomy wieloelektronowe Wodór ma liczbę atomową Z=1 i jest prostym atomem. Zawiera tylko jeden elektron i jeden proton stąd potencjał opisuje oddziaływanie kulombowskie
Atomy wieloelektronowe i cząsteczki 1 Atomy wieloelektronowe Wodór ma liczbę atomową Z=1 i jest prostym atomem. Zawiera tylko jeden elektron i jeden proton stąd potencjał opisuje oddziaływanie kulombowskie
Ciała stałe. Ciała krystaliczne. Ciała amorficzne. Bardzo często mamy do czynienia z ciałami polikrystalicznymi, rzadko monokryształami.
 Ciała stałe Ciała krystaliczne Ciała amorficzne Bardzo często mamy do czynienia z ciałami polikrystalicznymi, rzadko monokryształami. r T = Kryształy rosną przez regularne powtarzanie się identycznych
Ciała stałe Ciała krystaliczne Ciała amorficzne Bardzo często mamy do czynienia z ciałami polikrystalicznymi, rzadko monokryształami. r T = Kryształy rosną przez regularne powtarzanie się identycznych
Zjawiska powierzchniowe
 Zjawiska powierzchniowe Adsorpcja Model Langmuira Model BET 1 Zjawiska powierzchniowe Adsorpcja Proces gromadzenia się substancji z wnętrza fazy na granicy międzyfazowej; Wynika z tego, że w obszarze powierzchniowym
Zjawiska powierzchniowe Adsorpcja Model Langmuira Model BET 1 Zjawiska powierzchniowe Adsorpcja Proces gromadzenia się substancji z wnętrza fazy na granicy międzyfazowej; Wynika z tego, że w obszarze powierzchniowym
Ciśnienie definiujemy jako stosunek siły parcia działającej na jednostkę powierzchni do wielkości tej powierzchni.
 Ciśnienie i gęstość płynów Autorzy: Zbigniew Kąkol, Bartek Wiendlocha Powszechnie przyjęty jest podział materii na ciała stałe i płyny. Pod pojęciem substancji, która może płynąć rozumiemy zarówno ciecze
Ciśnienie i gęstość płynów Autorzy: Zbigniew Kąkol, Bartek Wiendlocha Powszechnie przyjęty jest podział materii na ciała stałe i płyny. Pod pojęciem substancji, która może płynąć rozumiemy zarówno ciecze
Równowagi fazowe. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Równowagi fazowe Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny Równowaga termodynamiczna Przemianom fazowym towarzyszą procesy, podczas których nie zmienia się skład chemiczny układu, polegają
Różne dziwne przewodniki
 Różne dziwne przewodniki czyli trzy po trzy o mechanizmach przewodzenia prądu elektrycznego Przewodniki elektronowe Metale Metale (zwane również przewodnikami) charakteryzują się tym, że elektrony ich
Różne dziwne przewodniki czyli trzy po trzy o mechanizmach przewodzenia prądu elektrycznego Przewodniki elektronowe Metale Metale (zwane również przewodnikami) charakteryzują się tym, że elektrony ich
Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne
 Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne W3. Zjawiska transportu Zjawiska transportu zachodzą gdy układ dąży do stanu równowagi. W zjawiskach
Wykład 3 Zjawiska transportu Dyfuzja w gazie, przewodnictwo cieplne, lepkość gazu, przewodnictwo elektryczne W3. Zjawiska transportu Zjawiska transportu zachodzą gdy układ dąży do stanu równowagi. W zjawiskach
Termodynamika. Część 12. Procesy transportu. Janusz Brzychczyk, Instytut Fizyki UJ
 Termodynamika Część 12 Procesy transportu Janusz Brzychczyk, Instytut Fizyki UJ Zjawiska transportu Zjawiska transportu są typowymi procesami nieodwracalnymi zachodzącymi w przyrodzie. Zjawiska te polegają
Termodynamika Część 12 Procesy transportu Janusz Brzychczyk, Instytut Fizyki UJ Zjawiska transportu Zjawiska transportu są typowymi procesami nieodwracalnymi zachodzącymi w przyrodzie. Zjawiska te polegają
Własności magnetyczne materii
 Własności magnetyczne materii Dipole magnetyczne Najprostszą strukturą magnetyczną są magnetyczne dipole. Fe 3 O 4 Kompas, Chiny 220 p.n.e Kołowy obwód z prądem dipol magnetyczny! Wartość B w środku kołowego
Własności magnetyczne materii Dipole magnetyczne Najprostszą strukturą magnetyczną są magnetyczne dipole. Fe 3 O 4 Kompas, Chiny 220 p.n.e Kołowy obwód z prądem dipol magnetyczny! Wartość B w środku kołowego
Czym się różni ciecz od ciała stałego?
 Szkła Czym się różni ciecz od ciała stałego? gęstość Czy szkło to ciecz czy ciało stałe? Szkło powstaje w procesie chłodzenia cieczy. Czy szkło to ciecz przechłodzona? kryształ szkło ciecz przechłodzona
Szkła Czym się różni ciecz od ciała stałego? gęstość Czy szkło to ciecz czy ciało stałe? Szkło powstaje w procesie chłodzenia cieczy. Czy szkło to ciecz przechłodzona? kryształ szkło ciecz przechłodzona
CZ STECZKA. Do opisu wi za chemicznych stosuje si najcz ciej jedn z dwóch metod (teorii): metoda wi za walencyjnych (VB)
 CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
CZ STECZKA Stanislao Cannizzaro (1826-1910) cz stki - elementy mikro wiata, termin obejmuj cy zarówno cz stki elementarne, jak i atomy, jony proste i zło one, cz steczki, rodniki, cz stki koloidowe; cz
J. Szantyr - Wykład 3 Równowaga płynu
 J. Szantyr - Wykład 3 Równowaga płynu Siły wewnętrzne wzajemne oddziaływania elementów mas wydzielonego obszaru płynu, siły o charakterze powierzchniowym, znoszące się parami. Siły zewnętrzne wynik oddziaływania
J. Szantyr - Wykład 3 Równowaga płynu Siły wewnętrzne wzajemne oddziaływania elementów mas wydzielonego obszaru płynu, siły o charakterze powierzchniowym, znoszące się parami. Siły zewnętrzne wynik oddziaływania
BUDOWA ATOMU KRYSTYNA SITKO
 BUDOWA ATOMU KRYSTYNA SITKO Ziarnista budowa materii Otaczająca nas materia to świat różnorodnych substancji np. woda, powietrze, drewno, metale. Sprawiają one wrażenie, że mają budowę ciągłą, to znaczy
BUDOWA ATOMU KRYSTYNA SITKO Ziarnista budowa materii Otaczająca nas materia to świat różnorodnych substancji np. woda, powietrze, drewno, metale. Sprawiają one wrażenie, że mają budowę ciągłą, to znaczy
SPIS TREŚCI ««*» ( # * *»»
 ««*» ( # * *»» CZĘŚĆ I. POJĘCIA PODSTAWOWE 1. Co to jest fizyka? 11 2. Wielkości fizyczne 11 3. Prawa fizyki 17 4. Teorie fizyki 19 5. Układ jednostek SI 20 6. Stałe fizyczne 20 CZĘŚĆ II. MECHANIKA 7.
««*» ( # * *»» CZĘŚĆ I. POJĘCIA PODSTAWOWE 1. Co to jest fizyka? 11 2. Wielkości fizyczne 11 3. Prawa fizyki 17 4. Teorie fizyki 19 5. Układ jednostek SI 20 6. Stałe fizyczne 20 CZĘŚĆ II. MECHANIKA 7.
INŻYNIERIA BIOMEDYCZNA
 INŻYNIERIA BIOMEDYCZNA 2017-02-04 1 Stan materii a stan skupienia Stan materii podział z punktu widzenia mikroskopowego (struktury jakie tworzą atomy, cząsteczki, jony) Stan skupienia - forma występowania
INŻYNIERIA BIOMEDYCZNA 2017-02-04 1 Stan materii a stan skupienia Stan materii podział z punktu widzenia mikroskopowego (struktury jakie tworzą atomy, cząsteczki, jony) Stan skupienia - forma występowania
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
Wstęp do Optyki i Fizyki Materii Skondensowanej. Mateusz Goryca
 Wstęp do Optyki i Fizyki Materii Skondensowanej Mateusz Goryca mgoryca@fuw.edu.pl Uniwersytet Warszawski 2015 Materia skondensowana OC 6 H 13 H 13 C 6 O OC 6 H 13 H 17 C 8 O H 17 C 8 O N N Cu O O H 21
Wstęp do Optyki i Fizyki Materii Skondensowanej Mateusz Goryca mgoryca@fuw.edu.pl Uniwersytet Warszawski 2015 Materia skondensowana OC 6 H 13 H 13 C 6 O OC 6 H 13 H 17 C 8 O H 17 C 8 O N N Cu O O H 21
Q t lub precyzyjniej w postaci różniczkowej. dq dt Jednostką natężenia prądu jest amper oznaczany przez A.
 Prąd elektryczny Dotychczas zajmowaliśmy się zjawiskami związanymi z ładunkami spoczywającymi. Obecnie zajmiemy się zjawiskami zachodzącymi podczas uporządkowanego ruchu ładunków, który często nazywamy
Prąd elektryczny Dotychczas zajmowaliśmy się zjawiskami związanymi z ładunkami spoczywającymi. Obecnie zajmiemy się zjawiskami zachodzącymi podczas uporządkowanego ruchu ładunków, który często nazywamy
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Dr inż. Zbigniew Szklarski
 Wykład : Ciało stałe Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.31 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Struktura kryształu Ciała stałe o budowie bezpostaciowej
Wykład : Ciało stałe Dr inż. Zbigniew Szklarski Katedra Elektroniki, paw. C-1, pok.31 szkla@agh.edu.pl http://layer.uci.agh.edu.pl/z.szklarski/ Struktura kryształu Ciała stałe o budowie bezpostaciowej
Wykład Praca (1.1) c Całka liniowa definiuje pracę wykonaną w kierunku działania siły. Reinhard Kulessa 1
 1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
1.6 Praca Wykład 2 Praca zdefiniowana jest jako ilość energii dostarczanej przez siłę działającą na pewnej drodze i matematycznie jest zapisana jako: W = c r F r ds (1.1) ds F θ c Całka liniowa definiuje
Szkła specjalne Przejście szkliste i jego termodynamika Wykład 5. Ryszard J. Barczyński, 2017 Materiały edukacyjne do użytku wewnętrznego
 Szkła specjalne Przejście szkliste i jego termodynamika Wykład 5 Ryszard J. Barczyński, 2017 Materiały edukacyjne do użytku wewnętrznego Czy przejście szkliste jest termodynamicznym przejściem fazowym?
Szkła specjalne Przejście szkliste i jego termodynamika Wykład 5 Ryszard J. Barczyński, 2017 Materiały edukacyjne do użytku wewnętrznego Czy przejście szkliste jest termodynamicznym przejściem fazowym?
Przykładowe zadania/problemy egzaminacyjne. Wszystkie bezwymiarowe wartości liczbowe występujące w treści zadań podane są w jednostkach SI.
 Przykładowe zadania/problemy egzaminacyjne. Wszystkie bezwymiarowe wartości liczbowe występujące w treści zadań podane są w jednostkach SI. 1. Ładunki q 1 =3,2 10 17 i q 2 =1,6 10 18 znajdują się w próżni
Przykładowe zadania/problemy egzaminacyjne. Wszystkie bezwymiarowe wartości liczbowe występujące w treści zadań podane są w jednostkach SI. 1. Ładunki q 1 =3,2 10 17 i q 2 =1,6 10 18 znajdują się w próżni
Rozwiązanie: Zadanie 2
 Podstawowe pojęcia. Definicja kryształu. Sieć przestrzenna i sieć krystaliczna. Osie krystalograficzne i jednostki osiowe. Ściana jednostkowa i stosunek osiowy. Położenie węzłów, prostych i płaszczyzn
Podstawowe pojęcia. Definicja kryształu. Sieć przestrzenna i sieć krystaliczna. Osie krystalograficzne i jednostki osiowe. Ściana jednostkowa i stosunek osiowy. Położenie węzłów, prostych i płaszczyzn
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wykład 8 ELEKTROMAGNETYZM
 Wykład 8 ELEKTROMAGNETYZM Równania Maxwella dive = ρ εε 0 prawo Gaussa dla pola elektrycznego divb = 0 rote = db dt prawo Gaussa dla pola magnetycznego prawo indukcji Faradaya rotb = μμ 0 j + εε 0 μμ 0
Wykład 8 ELEKTROMAGNETYZM Równania Maxwella dive = ρ εε 0 prawo Gaussa dla pola elektrycznego divb = 0 rote = db dt prawo Gaussa dla pola magnetycznego prawo indukcji Faradaya rotb = μμ 0 j + εε 0 μμ 0
Odp.: F e /F g = 1 2,
 Segment B.IX Pole elektrostatyczne Przygotował: mgr Adam Urbanowicz Zad. 1 W atomie wodoru odległość między elektronem i protonem wynosi około r = 5,3 10 11 m. Obliczyć siłę przyciągania elektrostatycznego
Segment B.IX Pole elektrostatyczne Przygotował: mgr Adam Urbanowicz Zad. 1 W atomie wodoru odległość między elektronem i protonem wynosi około r = 5,3 10 11 m. Obliczyć siłę przyciągania elektrostatycznego
chemia wykład 3 Przemiany fazowe
 Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Przemiany fazowe Przemiany fazowe substancji czystych Wrzenie, krzepnięcie, przemiana grafitu w diament stanowią przykłady przemian fazowych, które zachodzą bez zmiany składu chemicznego. Diagramy fazowe
Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca. Uczeń:
 Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
Chemia - klasa I (część 2) Wymagania edukacyjne Temat Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra Ocena celująca Dział 1. Chemia nieorganiczna Lekcja organizacyjna. Zapoznanie
