/11 1. PRZEZNACZENIE
|
|
|
- Paulina Borowska
- 6 lat temu
- Przeglądów:
Transkrypt
1 PLATELIA LYME IgG 1 płytka TEST IMMUNOENZYMATYCZNY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO BORRELIA BURGDORFERI SENSU LATO W LUDZKIEJ SUROWICY, OSOCZU LUB PŁYNIE MÓZGOWO- RDZENIOWYM /11 1. PRZEZNACZENIE Platelia TM Lyme IgG jest pośrednim testem immunoenzymatycznym do jakościowego wykrywania przeciwciał klasy IgG przeciwko Borrelia burgdorferi sensu lato w ludzkiej surowicy, osoczu lub płynie mózgowo-rdzeniowym (PMR). 2. ZNACZENIE KLINICZNE Borelioza z Lyme (lub choroba z Lyme) jest to choroba niezakaźna, wywoływana przez Borrelia burgdorferi bakterię z rodziny krętków, przenoszoną przez kleszcze z rodzaju Ixodes (2). Gospodarzami tej bakterii są różne zwierzęta, a przeniesienie choroby na człowieka zachodzi poprzez ukąszenie przez zainfekowanego kleszcza. Ryzyko przeniesienia zakażenia jest tym większe im dłuższy jest czas pobierania pokarmu przez kleszcza (tj. czas ukąszenia). Częstość występowania choroby z Lyme jest wysoka w krajach o klimacie umiarkowanym i chłodnym na półkuli północnej, od Chin do Ameryki Północnej oraz od Skandynawii po Afrykę Północną. Szacuje się, że każdego roku w Stanach Zjednoczonych zgłaszanych jest około przypadków (3), a w Europie przypuszczalnie ponad , przy czym stwierdzonym dodatnim gradiencie częstości w kierunku z zachodu na wschód(4). Wyraźnie wykazano, że Borrelia burgdorferi opisana w 1984 roku jako unikalny gatunek bakterii, w rzeczywistości sklada się z kilku gatunków, spośród których pięć jest chorobotwórczych dla człowieka: Borrelia burgdorferi sensu stricto (ss), Borrelia garinii, Borrelia afzelii, Borrelia spielmanii i Borrelia bavariensis (7,8). Dwa pozostałe gatunki są potencjalnie patogenne: Borrelia valaisiana i Borrelia lusitaniae. Te siedem gatunków krąży w Europie, a tylko B. burgdorferi sensu stricto występuje w Stanach Zjednoczonych. Objawy kliniczne choroby z Lyme są zróżnicowane i czasami trudne do rozpoznania (6). W klinicznym przebiegu choroby wyróżnić można trzy etapy. Etap wczesny (Stadium I) może być bezobjawowy i charakteryzuje się występowaniem zespołu objawów grypopodobnych. W 50 do 80% przypadków, kilka dni lub tygodni po ukąszeniu, pojawia się typowo zlokalizowana wysypka skórna, rozchodząca się koliście, określana jako rumień wędrujący (erythema migrans, EM). Jeżeli nie zostanie wdrożone leczenie, rozsiew bakterii drogą krwiopochodną powoduje wystąpienie po kilku tygodniach zapalenia stawów, zaburzeń neurologicznych lub o charakterze zapalenia opon mózgowo-rdzeniowych oraz objawów skórnych lub sercowych (Stadium II). Po kilku miesiącach lub latach, choroba może przejść w stadium przewlekłe związane z występowaniem zanikowego zapalenia skóry obwodowych części kończyn (acrodermatitis chronica atrophicans), zapalenia mózgu, zapalenia mózgu i rdzenia kręgowego oraz przewlekłego zapalenia stawów (Stadium III) (1). Każdy z gatunków Borrelia burgdorferi wykazuje specyficzny tropizm. Rumień wędrujący w stadium I występuje w przypadku wszystkich trzech gatunków. Jednakże powikłania neurologiczne częściej występują w przypadku zakażenia wywołanego przez B. garinii, zapalenie stawów częściej związane jest z zakażeniem wywołanym przez B. burgdorferi ss, podczas gdy zanikowe zapalenie skóry jest swoiste dla B. afzelii. Nie należy stawiać rozpoznania boreliozy bez dokładnej analizy historii choroby pacjenta, kryteriów klinicznych i biologicznych oraz bez oszacowania ryzyka narażenia na ukąszenie przez kleszcze. Ze względu na trudności w wykryciu bezpośrednim, izolacji z hodowli i wdrażaniu metod biologii molekularnej, badania serologiczne stanowią kluczowy element w biologicznej diagnostyce boreliozy (1,5,9). Przeciwciała klasy IgM przeciwko Borrelia burgdorferi pojawiają się około 3 do 6 tygodni po zakażeniu i mogą utrzymywać się przez okres rozwoju choroby, podczas gdy przeciwciała klasy IgG pojawiają się później i osiągają wysoki poziom dopiero po kilku miesiącach lub latach. Nawet, jeżeli badanie serologiczne jest mniej przydatne w stadium wczesnym, jest ono bardzo istotne w stadium drugim i trzecim, zwłaszcza przy braku rumienia wędrującego. Jeżeli wynik badania serologicznego jest ujemny, mimo sugerującego zakażenie obrazu klinicznego, kolejne badanie serologiczne należy wykonać po trzech tygodniach od pierwszego badania. Obecność swoistych przeciwciał klasy IgM nie jest jednoznaczna ze stwierdzeniem niedawnego zakażenia. Podobnie, obecność swoistych przeciwciał klasy IgG nie zawsze świadczy o przebytym zakażeniu. Ponadto, oznaczenie indeksu wewnątrzoponowej syntezy swoistych przeciwciał klasy IgG przeciwko Borrelia burgdorferi sensu lato stanowi element pomocniczy przy podejrzeniu neuroboreliozy (10,11,12). Antygeny i przeciwciała wykorzystane w testach Platelia TM Lyme IgG (nr ref ) oraz Platelia TM Lyme IgM (nr ref ) zostały dobrane tak, aby pozwolić na wykrycie swoistych przeciwciał klasy IgG i klasy IgM, przeciwko zróżnicowanym amerykańskim i europejskim szczepom Borrelia burgdorferi sensu lato (B. burgdorferi ss, B. garinii, B. azfelii). 1
2 3. ZASADA Platelia TM Lyme IgG jest pośrednim testem immunoenzymatycznym testem do jakościowego wykrywania przeciwciał klasy IgG przeciwko Borrelia burgdorferi sensu lato w ludzkiej surowicy, osoczu lub PMR. Mikropłytkę opłaszczono inaktywowanymi antygenami Borrelia burgdorferi. W koniugacie zastosowano przeciwciało monoklonalne, znakowane peroksydazą, swoiste wobec ludzkich łańcuchów gamma (anty-igg). Wykonanie oznaczenia obejmuje następujące etapy: Etap 1 Próbki pacjenta (surowica lub osocze) i kontrole rozcieńczane są w stosunku 1:101. Próbki CSF rozcieńczane są w stosunku 1:2. Rozcieńczone próbki są następnie nanoszone do studzienek mikropłytki. Podczas trwającej jedną godzinę inkubacji w temperaturze 37 C, przeciwciała klasy IgG przeciwko Borrelia burgdorferi, występujące w próbce, wiążą się z antygenem Borrelia, którym opłaszczone są studzienki mikropłytki. Po inkubacji, niezwiązane przeciwciała niespecyficzne i inne białka surowicy usuwane są w trakcie płukania. Etap 2 Do studzienek mikropłytki dodawany jest koniugat (przeciwciało monoklonalne swoiste wobec ludzkich łańcuchów gamma, znakowane peroksydazą). Podczas trwającej jedną godzinę inkubacji w temperaturze 37 C, znakowane przeciwciało monoklonalne wiąże się do przeciwciał klasy IgG surowicy, wychwyconych przez antygen Borrelia. Niezwiązany koniugat usuwany jest przez płukanie po zakończeniu inkubacji. Etap 3 Obecność kompleksów immunologicznych (antygen Borrelia, przeciwciało klasy IgG przeciwko Borrelia burgdorferii, koniugat IgG) wykazywana jest poprzez dodanie do studzienki roztworu wyzwalającego reakcję enzymatyczną. Etap 4 Po inkubacji w temperaturze pokojowej ( C), reakcja enzymatyczna zatrzymywana jest przez dodanie roztworu 1N kwasu siarkowego. Odczyt gęstości optycznej uzyskany za pomocą czytnika ustawionego na 450/620 nm jest proporcjonalny do ilości przeciwciał klasy IgG przeciwko Borrelia burgdorferi, występujących w próbce. 4. INFORMACJA O PRODUKCIE Dostarczona ilość odczynników umożliwia wykonanie 96 oznaczeń w maksymalnie 6 seriach. Wszystkie odczynniki przeznaczone są wyłącznie do diagnostyki in vitro. Etykieta Odczynnik Ilość R1 Mikropłytka Mikropłytka (gotowa do użytku) 1 mikropłytka 12 pasków po 8 odłamywalnych studzienek każdy, opłaszczonych inaktywowanym antygenem Borrelia R2 Stężony roztwór płuczący (20x) Stężony roztwór płuczący (20x) Bufor Tris-NaCl (ph 7.4), 2% Tween 20 1 fiolki 70 ml Środek konserwujący: 0,04 % ProClin 300 R3 Kontrola ujemna Kontrola ujemna Ludzka surowica, ujemna pod względem przeciwciał klasy IgG przeciwko Borrelia burgdorferi oraz ujemna pod względem antygenu HBs, przeciwciał anty-hiv1, anty-hiv2 i anty-hcv Środek konserwujący: 0,15 % ProClin 300 R4 Kontrola wartości odcięcia Kontrola wartości odcięcia Ludzka surowica reaktywna pod względem przeciwciał klasy IgG przeciwko Borrelia burgdorferi oraz ujemna pod względem antygenu HBs, przeciwciał anty-hiv1, anty-anti-hiv2 i anty-hcv Środek konserwujący: 0,15 % ProClin 300 R5 Kontrola dodatnia Kontrola dodatnia Ludzka surowica reaktywna pod względem przeciwciał klasy IgG przeciwko Borrelia burgdorferi oraz ujemna pod względem antygenu HBs, przeciwciał anty-hiv1, anty-anti-hiv2 i anty-hcv Środek konserwujący: 0,15 % ProClin 300 R6 Koniugat (51x) Koniugat (51x) Mysie przeciwciało monoklonalne przeciwko ludzkim łańcuchom gamma, skoniugowane z peroksydazą chrzanową Środek konserwujący: 0,16 % ProClin 300 R7 Rozcieńczalnik Rozcieńczalnik dla próbek i koniugatu (gotowy do użytku) Tris-NaCl (ph 7.7), płodowa surowica cielęca, 0.1% Tween 20 oraz czerwień fenolowa Środek konserwujący: 0,15 % ProClin 300 R9 Chromogen TMB Chromogen (gotowy do użytku) 3,3,5,5 tetrametylobenzydyna (< 0.1%), H 2O 2 (<1%) R10 Roztwór zatrzymujący Roztwór zatrzymujący reakcję (gotowy do użytku) reakcję 1N roztwór kwasu siarkowego Warunki przechowywania oraz datę przydatności do użytku podano na opakowaniu zestawu. 1 fiolka 0.75 ml 1 fiolka 0.75 ml 1 fiolka 0.75 ml 1 fiolka 0.7 ml 2 fiolki 65 ml 1 fiolka 28 ml 1 fiolka 28 ml 2
3 5. ZALECENIA DLA UŻYTKOWNIKA Wiarygodność uzyskiwanych wyników zależy od właściwego stosowania następujących zasad Dobrej Praktyki Laboratoryjnej: Nie używać odczynników po upływie daty ważności. Nie mieszać i nie łączyć w ramach jednego oznaczenia odczynników z różnych serii. UWAGA: W przypadku roztworu płuczącego (R2, oznaczenie na etykiecie: 20x, kolor zielony), chromogenu (R9, oznaczenie na etykiecie: TMB, kolor turkusowy) oraz roztworu zatrzymującego reakcję (R10, oznaczenie na etykiecie: 1N, kolor czerwony), można stosować inne serie niż zawarte w zestawie, pod warunkiem, że odczynniki są ściśle równoważne i w ramach jednego oznaczenia stosowana jest ta sama seria odczynnika. Przed użyciem odczekać 30 minut, aby odczynniki osiągnęły temperaturę pokojową ( C). Starannie rekonstytuować lub rozcieńczać odczynniki, unikając ich zanieczyszczenia. Nie wykonywać oznaczenia w obecności reaktywnych par związków (kwasów, zasad, aldehydów) lub kurzu, które mogą wpływać na aktywność enzymatyczną koniugatu. Stosować naczynia szklane dokładnie umyte i wypłukane wodą dejonizowaną lub najlepiej materiały jednorazowego użytku. Płukanie mikropłytki stanowi ważny etap procedury: należy przestrzegać zalecanej liczby cykli płukania i upewnić się, że studzienki są całkowicie napełniane, a następnie całkowicie opróżniane. Nieprawidłowe płukanie może być przyczyną do błednych wyników. Nie dopuszczać do wyschnięcia mikropłytki między zakończeniem płukania a naniesieniem odczynnika. Nie stosować nigdy tych samych pojemników do pipetowania koniugatu i roztworu wywołującego. Reakcja enzymatyczna jest bardzo wrażliwa na metale lub jony metali. W związku z tym nie należy dopuszczać do kontaktu jakiegokolwiek elementu metalowego z roztworami zawierającymi koniugat lub chromogen. Roztwór chromogenu (R9) powinien być bezbarwny. Pojawienie się niebieskiego zabarwienia oznacza, że odczynnik nie może być stosowany i musi zostać wymieniony. Do każdej próbki stosować nową końcówkę pipety. Sprawdzać pipety i pozostały sprzęt pod względem dokładności i poprawności działania. Higiena i bezpieczeństwo pracy Materiał pochodzenia ludzkiego użyty do przygotowania odczynników został przebadany i uznany za niereaktywny pod względem obecności antygenu powierzchniowego wirusa zapalenia wątroby typu B (HBs Ag), przeciwciał przeciwko wirusowi zapalenia wątroby typu C (anty-hcv) oraz przeciwko ludzkiemu wirusowi niedoboru odporności (anty-hiv1 i anty-hiv2). Ze względu na to, iż żadna metoda nie daje całkowitej pewności co do braku czynników zakaźnych, odczynniki pochodzenia ludzkiego oraz próbki pacjentów należy traktować jako potencjalnie zakaźne. Każdy materiał, który ma bezpośredni kontakt z próbkami i odczynnikami zawierającymi materiały pochodzenia ludzkiego, również roztwory płuczące, należy traktować jak materiał potencjalnie zakaźny. Pracując z próbkami i odczynnikami stosować rękawice jednorazowego użytku. Nie pipetować ustami. Unikać rozlewania próbek lub roztworów zawierających próbki. Rozlany materiał należy spłukać wybielaczem, rozcieńczonym do 10%. W razie rozlania kwasu, należy najpierw zobojętnić go dwuwęglanem sodu, a następnie spłukać środkiem wybielającym rozcieńczonym do 10% i osuszyć bibułą. Materiał stosowany do czyszczenia należy wyrzucać do pojemnika z odpadami zakaźnymi. Próbki pacjenta, odczynniki zawierające materiał pochodzenia ludzkiego, jak również materiały skażone należy wyrzucać po odkażeniu: - przez zanurzenie w środku wybielającym o ostatecznym stężeniu podchlorynu sodu wynoszącym 5%, na 30 minut; - lub przez sterylizację w autoklawie w temperaturze 121 C przez co najmniej 2 godziny. UWAGA: Nie wstawiać do autoklawu roztworów zawierających podchloryn sodu. Unikać kontaktu chromogenu i roztworu zatrzymującego reakcję ze skórą i błoną śluzową (ryzyko zatrucia, podrażnienia lub poparzenia). Z odpadami chemicznymi i biologicznymi należy postępować i usuwać je zgodnie z zasadami Dobrej Praktyki Laboratoryjnej. Wszystkie odczynniki w zestawie przeznaczone są wyłącznie do diagnostyki in vitro. W celu zapoznania się z zaleceniami dotyczącymi zagrożeń i środków ostrożności związanych z niektórymi substancjami chemicznymi zawartymi w niniejszym zestawie należy skorzystać z piktogramów wskazujących rodzaj zagrożenia znajdujących się na etykietach i w informacjach zamieszczonych na końcu instrukcji obsługi. Karta charakterystyki jest dostępna na stronie internetowej 3
4 6. POBIERANIE, PRZYGOTOWANIE I PRZECHOWYWANIE PRÓBEK 1. Zalecane rodzaje próbek to surowica i osocze (pobrane na EDTA, heparynę lub cytrynian) oraz PMR. 2. Podczas pobierania, obróbki i przechowywania próbek krwi należy przestrzegać poniższych zaleceń: Próbki krwi żylnej pobierać zgodnie z rutynową procedurą. W przypadku surowicy, przed wirowaniem odczekać do pełnego wykrzepienia próbek. Probówki powinny być cały czas zamknięte. Po odwirowaniu, oddzielić surowicę lub osocze od skrzepu lub krwinek czerwonych do dokładnie zamkniętej probówki do przechowywania. Próbki można przechowywać w temperaturze +2-8 C, jeżeli badanie zostanie wykonane w ciągu 7 dni. Jeżeli badanie nie zostanie wykonane w ciągu 7 dni lub w przypadku przygotowania do wysyłki, próbki należy zamrozić w temperaturze -20 C lub niższej. Nie używać próbek, które były rozmrażane więcej niż pięć razy. Uprzednio zamrożone próbki należy przed badaniem, po rozmrożeniu, dokładnie wymieszać (Vortex). 3. Próbki surowicy lub osocza zawierające 90 g/l albumin lub 100 mg/l niezwiązanej bilirubiny, próbki lipemiczne zawierające równoważność 36 g/l trójoleiny (trójglicerydy) oraz próbki zhemolizowane, zawierające do 10 g/l hemoglobiny nie wpływają na uzyskane wyniki. 4. Nie ogrzewać próbek. 5. W celu wykazania wewnątrzoponowej syntezy IgG, należy użyć próbek PMR pobranych metodą nakłucia lędźwiowego odcinka kręgosłupa, jednocześnie z pobraniem próbki z surowicy lub osocza. Należy stosować się do rutynowych zaleceń mających zastosowanie w przypadku pobierania próbek PMR. Szczególnie istotnym jest, nieużywanie do oznaczeń próbek zmienionych, o niejednorodnym wyglądzie (w takim wypadku preferowanym materiałem jest supernatant po odwirowaniu) lub próbek silnie zhemolizowanych. PMR należy oznaczać niezwłocznie po pobraniu. Jeśli konieczne jest przechowywanie PMR w celu dalszych badań, można to zrobić w temperaturze 4-8 C (krótki czas) lub -20 C (w dłuższym okresie) (11). UWAGA: Stabilność próbek PMR w temperaturze 4-8 C lub -20 C lub po wielu cyklach zamrażania i rozmrażania lub w obecności czynników interferujących, wymienionych powyżej w punkcie 3 nie była badana. 7. PROCEDURA BADANIA 7.1 MATERIAŁY WYMAGANE, ALE NIE DOSTARCZONE PRZEZ PRODUCENTA Mieszadło Vortex. Czytnik mikropłytek wyposażony w filtry o długości fali 450 nm i 620 nm (*). Inkubator mikropłytek z termostatem ustawionym na temp. 37±1 C (*). Automatyczne, półautomatyczne lub ręczne urządzenie do płukania mikropłytek (*). Jałowa woda destylowana lub dejonizowana. Rękawiczki jednorazowego użytku. Gogle lub okulary ochronne. Bibuła. Automatyczne lub półautomatyczne, nastawne lub stało-objętościowe pipety jedno- lub wielokanałowe, do odmierzania i dozowania objętości od 10 µl do 1000 µl oraz 1 ml, 2 ml i 10 ml. Cylindry miarowe o pojemności 25 ml, 50 ml, 100 ml i 1000 ml. Podchloryn sodu (środek wybielający) i dwuwęglan sodu. Pojemnik na odpady zakaźne. Probówki jednorazowego użytku. (*) Szczegółowe informacje dotyczące zalecanego wyposażenia uzyskać można w naszym dziale technicznym. 7.2 REKONSTUTUCJA ODCZYNNIKÓW R1: Przed otwarciem torebki, odczekać 30 minut, aby ogrzać mikropłytkę do temperatury pokojowej ( C). Wyjąć ramkę, niewykorzystywane paski włożyć natychmiast z powrotem do torebki i sprawdzić czy w torebce znajduje się środek osuszający. Dokładnie zamknąć torebkę i przechowywać ją w temperaturze +2-8 C. R2: Rozcieńczyć roztwór płuczący 1/20 w wodzie destylowanej: na przykład 50 ml R2 i 950 ml wody destylowanej, aby uzyskać gotowy do użytku roztwór płuczący. Jeżeli płukanie wykonywane jest ręcznie, przygotować 350 ml rozcieńczonego roztworu płuczącego na jedną płytkę zawierającą 12 pasków. R3, R4, R5: Rozcieńczyć 1/101 w Rozcieńczalniku (R7) (przykład: 10 µl R3 + 1 ml R7). R6+R7: Koniugat (R6) jest stężony 51x, odczynnik przed użyciem wymieszać. Rozcieńczyć 1/51 w rozcieńczalniku (R7). Na jedną płytkę rozcieńczyć 0.5 ml koniugatu (R6) w 25 ml rozcieńczalnika (R7). Podzielić te objętości przez 5, aby uzyskać objętość potrzebną na dwa paski. 7.3 PRZECHOWYWANIE ORAZ TRWAŁOŚĆ OTWARTYCH I / LUB ZREKONSTYTUOWANYCH ODCZYNNIKÓW Zestaw należy przechowywać w temperaturze +2-8 C. Przed pierwszym otwarciem, każdy składnik zestawu przechowywanego w temperaturze +2-8 C, zachowuje trwałość do daty przydatności do użytku, podanej na etykiecie zewnętrznej zestawu. R1: Po otwarciu, paski pozostają stabilne przez okres jednego miesiąca, o ile przechowywane są w temperaturze +2-8 C, w tej samej dokładnie zamkniętej torebce (sprawdzić czy w torebce jest środek osuszający). R2: Roztwór płuczący po rozcieńczeniu można przechowywać przez 2 tygodnie w temperaturze C. Stężony roztwór płuczący, przechowywany w temp C, jest stabilny do czasu upływu terminu przydatności do użytku podanego na etykiecie, pod warunkiem, że nie dojdzie do zanieczyszczenia. 4
5 R3, R4, R5, R6, R7: Po otwarciu, jeżeli nie dojdzie do zanieczyszczenia, odczynniki przechowywane w temperaturze +2-8 C, są stabilne przez okres do jednego miesiąca. R6 + R7: Po rozcieńczeniu, roboczy roztwór koniugatu jest stabilny przez 8 godzin w temperaturze pokojowej ( C) lub przez 24 godziny w temperaturze +2-8 C. R9: Po otwarciu, jeżeli nie dojdzie do zanieczyszczenia, odczynnik przechowywany w temperaturze +2-8 C jest stabilny przez okres 2 miesięcy. R10: Po otwarciu, jeżeli nie dojdzie do zanieczyszczenia, odczynnik przechowywany w temperaturze +2-8 C jest stabilny do czasu upływu terminu przydatności podanego na etykiecie. 7.4 PROCEDURA DLA PRÓBEK SUROWICY I OSOCZA Ściśle przestrzegać procedury badania oraz zasad Dobrej Praktyki Laboratoryjnej. Przed użyciem odczekać, aby odczynniki osiągnęły temperaturę pokojową ( C). W celu walidacji uzyskanych wyników, w każdej serii badań stosować kontrolę ujemną, kontrolę cut-off oraz kontrolę dodatnią. 1. Dokładnie ustalić rozkład i plan identyfikacji kontroli i próbek pacjentów. 2. Przygotować rozcieńczony roztwór płuczący (R2) [Zobacz Rozdział 7.2]. 3. Wyjąć ramkę i paski (R1) z torebki ochronnej [Zobacz Rozdział 7.2]. 4. Rozcieńczyć kontrole R3, R4, R5 oraz próbki pacjentów (S1, S2...) w rozcieńczalniku (R7), aby uzyskać rozcieńczenie 1/101: 10 µl próbki i 1.0 ml rozcieńczalnika (R7). Wymieszać rozcieńczone próbki na mieszadle Vortex. 5. Ściśle przestrzegać przedstawionej poniżej sekwencji postępowania, nanieść do każdej studzienki po 200 µl rozcieńczonych kontroli i próbek pacjenta: A R3 S5 S13 B R4 S6 C R4 S7 D R5 S8 E S1 S9 F S2 S10 G S3 S11 H S4 S12 6. Zakryć mikropłytkę folią adhezyjną i docisnąć mocno do płytki, aby zapewnić szczelność. Natychmiast inkubować mikropłytkę w łaźni wodnej kontrolowanej termostatem lub w suchym inkubatorze przez 1 godzinę ± 5 minut w temperaturze 37 C ± 1 C. 7. Po zakończeniu pierwszej inkubacji zdjąć folię. Zaaspirować zawartość wszystkich studzienek i usunąć do pojemnika na odpady zakaźne (zawierającego podchloryn sodu). Wypłukać mikropłytkę 4 razy stosując 350 µl roztworu płuczącego (R2). Odwrócić mikropłytkę na bibule i delikatnie postukując usunąć pozostały płyn. 8. Przygotować roztwór roboczy koniugatu (R6 + R7) [Zobacz Rozdział 7.2]. Natychmiast nanieść po 200 µl roztworu roboczego koniugatu (R6 + R7) do wszystkich studzienek. Roztwór należy delikatnie wstrząsnąć przed użyciem. 9. Zakryć mikropłytkę folią adhezyjną i docisnąć mocno do płytki, aby zapewnić szczelność. Natychmiast inkubować mikropłytkę w łaźni wodnej kontrolowanej termostatem lub w suchym inkubatorze, przez 1 godzinę ± 5 minut, w temperaturze 37 C ± 1 C. 10. Po zakończeniu drugiej inkubacji zdjąć folię adhezyjną. Zaaspirować zawartość wszystkich studzienek i usunąć do pojemnika na odpady zakaźne (zawierającego podchloryn sodu). Wypłukać mikropłytkę 4 razy stosując 350 µl roztworu płuczącego (R2). Odwrócić mikropłytkę na bibule i delikatnie postukując usunąć pozostały płyn. 11. Chroniąc przed dostępem światła, szybko nanieść do każdej studzienki po 200 µl roztworu chromogenu (R9). Inkubować reakcję w ciemności, przez 30 ± 5 minut, w temperaturze pokojowej ( C). Nie stosować folii adhezyjnej podczas tej inkubacji. 12. Zatrzymać reakcję enzymatyczną dodając po 100 µl roztworu zatrzymującego reakcję (R10) do każdej studzienki. Nanosić roztwór w tej samej kolejności i z taką samą szybkością jak roztwór wywołujący reakcję. 13. Ostrożnie wytrzeć spód płytki. W ciągu 30 minut po zatrzymaniu reakcji, odczytać gęstość optyczną przy filtrze 450/620 nm, stosując czytnik płytek. Przed odczytem chronić paski przed działaniem światła. 14. Przed podaniem wyników, sprawdzić zgodność między odczytem a planem rozkładu płytki i próbek. 7.4 PROCEDURA DLA PRÓBEK PŁYNU MÓZGOWO-RDZENIOWEGO UWAGA: Oznaczenie wewnątrzoponowej syntezy przeciwciał klasy IgG w diagnostyce boreliozy opiera się na zastosowaniu wzoru Reibera. Dla każdego pacjenta z podejrzeniem neuroboreliozy, pobierane są jednocześnie sparowane próbki surowicy/osocza i PMR. Obie próbki badane są w jednym cyklu. Należy rozcieńczyć próbki CSF w rozcieńczalniku (R7), aby uzyskać rozcieńczenie 1:2: 150 µl próbki CSF i 150 µl rozcieńczalnika (R7). Za wyjątkiem rozcieńczenia próbek CSF, należy ściśle przestrzegać opisanego wyżej protokołu dla próbek surowicy lub osocza. 5
6 8 OBLICZANIE I INTERPRETACJA WYNIKÓW 8.1 Obliczanie wartości odcięcia (CO) Wartość odcięcia (cut-off value, CO) odpowiada średniej wartości gęstości optycznej (OD) duplikatów kontroli cut-off (R4): CO = średnia z OD R4 8.2 Obliczanie indeksu próbki (surowica lub osocze) Wynik próbki podawany jest jako indeks, przy zastosowaniu następującego wzoru: Indeks próbki = OD próbki/co 8.3 Kontrola jakości Na każdej płytce i w każdej serii oznaczeń należy uwzględniać wszystkie kontrole i przeanalizować uzyskane wyniki. W celu walidacji serii oznaczeń, muszą być spełnione następujące kryteria: Wartości gęstości optycznej: - CO > x CO < OD R4 powtórzenie 1 < 1.20 x CO x CO < OD R4 powtórzenie 2 < 1.20 x CO (OD każdego powtórzenia kontroli wartości odcięcia (R4) nie może różnić się o więcej niż 20% od wartości CO). Indeks gęstości optycznej: - Indeks R3 (OD R3 / CO) < Indeks R5 (OD R5 / CO) >2.0 Jeżeli nie są spełnione powyższe kryteria kontroli jakości, oznaczenie należy powtórzyć. 8.4 Interpretacja wyników (surowica lub osocze) Indeks próbki Wynik Interpretacja Indeks < 0,80 Ujemny Próbkę należy traktować jako niereaktywną pod względem przeciwciał klasy IgG przeciwko Borrelia burgdorferi sensu lato. 0,80 Indeks < 1,2 Niejednoznaczny Próbka traktowana jest jako niejednoznaczna pod względem przeciwciał klasy IgG przeciwko Borrelia burgdorferi sensu lato. Wynik należy potwierdzić za pomocą kolejnego badania, wykonanego na nowej próbce krwi, pobranej w odstępie co najmniej 3 tygodni od czasu tego badania. Indeks 1,2 Dodatni Próbkę należy traktować jako reaktywną pod względem przeciwciał klasy IgG przeciwko Borrelia burgdorferi sensu lato. Jeżeli podejrzewa się zakażenie, do potwierdzenia rozpoznania przydatne mogą być uzupełniające badania serologiczne takie jak wykrywanie przeciwciał klasy IgM anty-borrelia. Jeżeli wynik badania serologicznego jest dodatni lub niejednoznaczny, zaleca się przebadanie próbki metodą potwierdzającą np. Western-Blot (9). 8.5 Obliczenia w celu oznaczenia syntezy wewnątrzoponowej Oznaczenie syntezy wewnątrzoponowej wykonywane jest z użyciem indeksu przeciwciał IgG (AI IgG) wyliczanego za pomocą wzoru Reibera (10,11,12). Dla każdej sparowanej próbki surowicy i PMR należy określić wartości OD (OD IgG Serum, OD IgG PMR) i sprawdzić, czy mieszczą się one w zakresie od 0,000 do 3,000. OSTRZEŻENIE: Jeśli OD surowicy (OD IgG surowica) lub OD PMR (OD IgG PMR) są poza zakresem OD wymienionym powyżej, próbkę należy zbadać ponownie, korzystając z większego rozcieńczenia w rozcieńczalniku R7 dostarczonym z zestawem. Po rozcieńczeniu, OD próbki musi zawierać się w zakresie od 0,000 do 3,000. W takim przypadku należy uwzględnić współczynnik rozcieńczenia zastosowany do obliczenia indeksu syntezy wewnątrzoponowej (patrz poniżej). Dla każdej badanej próbki surowicy należy określić następujące dane: Albuminy (g/l) = Albuminy surowica Całkowite IgG (g/l) = Całkowite IgG surowica Dla każdej badanej próbki PMR należy określić następujące dane: Albuminy (mg/l) = Albuminy PMR Całkowite IgG (mg/l) = Całkowite IgG PMR 6
7 Oblicz potrzebne wartości za pomocą wzorów poniżej:: Q Alb = Albuminy PMR / [Albuminy Surowica x 1000] Q lim(igg) = 0,93 x [Q Alb 2 + (6 x 10-6 )] 1/2 1,7 x 10-3 Q IgG = Całkowite IgG PMR / [Całkowite IgG Surowica x 1000] Q Spec(IgG) = OD IgG PMR / [OD IgG Surowica x 50,5] OSTRZEŻENIE: Jeśli np. próbki PMR i surowicy były rozcieńczone odpowiednio 1:5 i 1:10, aby mieściły się w przedziale OD od 0,000 do 3,000 OD, przed podstawieniem danych do wzoru na obliczenie Q Spec(IgG) należy pomnożyć OD CSF (OD IgG PMR) razy 5, a OD surowicy (OD IgG Surowica) razy 10. Indeks przeciwciał IgG (AI IgG) należy określić za pomocą jednego z dwóch wzorów podanych niżej: AI IgG = Q Spec(IgG) / Q IgG [jeśli Q IgG < Q lim(igg)] lub AI IgG = Q Spec(IgG) / Q lim(igg) [jeśli Q IgG > Q lim(igg)] 8.6 Interpretacja indeksu przeciwciał (AI IgG) w celu oznaczenia syntezy wewnątrzoponowej Wzór Reibera na określenie indeksu przeciwciał IgG nie ma zastosowania w następujących sytuacjach: indeks próbki PMR < 0,50 (*) indeks próbki PMR 0,50, przy indeksie surowicy/osocza < 0,50 (*) (*) indeks = OD / średnia R4 Wyniki dla PMR należy interpretować zgodnie z algorytmem poniżej: Oznaczenie indeksu PMR Indeks PMR < 0,50 Indeks PMR 0,50 PMR IgG ujemny Oznaczyć indeks surowicy Indeks surowicy < 0,50 Indeks surowicy 0,50 Indeks PMR< 0,80 Indeks PMR 0,80 Wzór Reibera Nie interpretować wyniku PMR PMR IgG dodatni Interpretacja indeksu przeciwciał IgG Algorytm oznaczania indeksu przeciwciał IgG za pomocą zestawu Platelia Lyme IgG Wewnątrzoponowa synteza IgG jest potwierdzona, kiedy indeks przeciwciał IgG jest wyższy niż 1,3. Brak wewnątrzoponowej syntezy IgG, jeśli indeks przeciwciał IgG jest wyższy niż 0,70, lecz niższy lub równy 1,30. Wynik nie powinien zostać uznany za prawidłowy, jeśli indeks przeciwciał IgG jest niższy lub równy 0,70 (błąd procedury, próbki surowicy i CSF pobrane innego dnia, skażenie CSF, itp.). Interpretacja AI IgG Dodatni AI IgG > 1,30 Ujemny 0,70 < AI IgG 1,30 Wynik nieprawidłowy AI IgG 0,70 7
8 8.7 Rozwiązywanie problemów Wyniki nie spełniające kryteriów walidacji lub niepowtarzalne mogą wynikać z następujących przyczyn: Niewłaściwe płukanie mikropłytki. Zanieczyszczenie próbek ujemnych przez surowicę lub osocze o wyższym mianie przeciwciał. Zanieczyszczenie roztworu wywołującego reakcję przez utleniające czynniki chemiczne (środek wybielający, jony metali...). Zanieczyszczenie roztworu zatrzymującego reakcję. 8.8 Przykład obliczeń (surowica lub osocze) Uwaga: Poniższe dane stanowią przykład i nie powinny być stosowane zamiast wyników uzyskanych przez użytkownika. Kontrole i próbki pacjentów OD (450/620 nm) Współczynnik Wynik R Ujemny R / / R / / R Dodatni Próbka Dodatni Próbka 2, itd Ujemny Wartość odcięcia: - CO = ( )/2 = Wartości gęstości optycznej: - OD CO = (N > 0.200) - OD R4 Powtórzenie 1 = (0.80 x OD CO < OD R4 Powtórzenie 1 < 1.20 x OD CO) - OD R4 Powtórzenie 2 = (0.80 x OD CO < OD R4 Powtórzenie 2 < 1.20 x OD CO) Indeks gęstości optycznej: - Indeks R3 = 0.29 (N < 0.5) - Indeks R5 = 2.88 (N > 2.0) Kontrola jakości: Zaakceptowana 9 CHARAKTERYSTYKA TESTU 9.1 Wartości spodziewane Wartości spodziewane dla oznaczenia poziomu przeciwciał klasy IgG przeciwko Borrelia burgdorferi sensu lato w surowicy ludzkiej wyznaczono wykorzystując panel 295 próbek pochodzących od dawców krwi z terenu Francji Północnej. Uzyskano następujące wyniki: 291 ujemnych, 1 niejednoznaczna, 3 surowice dodatnie. Prewalencja wyznaczona z wykorzystaniem testu Platelia Lyme IgG wynosi 1.02% (3/295). 9.2 Swoistość Swoistość na terenach nie-endemicznych Swoistość oznaczono wykorzystując panel 279 surowic uzyskanych od zdrowych dawców krwi pochodzących z rejonów nieendemicznych na terenie północnej Francji. Próbki zostały wyselekcjonowane na podstawie ujemnego wyniku badania z użyciem komercyjnych testów EIA wykorzystywanych w Europie (oznakowanych znakiem CE) i uznanych za referencyjne Swoistość na terenach endemicznych Swoistość oznaczono także z wykorzystaniem panelu 193 surowic uzyskanych od zdrowych dawców krwi pochodzących z rejonów endemicznych na terenie wschodniej Francji, z których żaden nie spełniał kryteriów kwalifikujących w kierunku choroby z Lyme (brak objawów klinicznych boreliozy, ani też doniesień o ugryzieniu przez kleszcza). Próbki zostały wyselekcjonowane na podstawie ujemnego wyniku badania z użyciem komercyjnych testów EIA wykorzystywanych w Europie (oznakowanych znakiem CE) i uznanych za referencyjne. Uzyskane wyniki przedstawiono w tabeli: Panel surowic Ujemny Niejednoznaczny (1) Dodatni (2) Swoistość Rejon nie-endemiczny (n=279) (278/278) [98,9%-] Rejon endemiczny (n=193) (1) Wyniki niejednoznaczne nie zostały uwzględnione w obliczeniach swoistości. (2) Próbki dodatnie w teście Platelia Lyme IgG były ujemne w teście Western-Blot. IC 95%: 95% przedział ufności. 99,5% (190/191) [97,1%-99,9%] 8
9 9.3 Czułość Czułość testu Platelia Lyme IgG wyznaczono z użyciem panelu 70 próbek pochodzących od pacjentów prezentującyh zróżnicowane objawy boreliozy z różnych etapów zakażenia i podano razem z wynikami czułości dla testu Platelia Lyme IgM (nr kat ). Uzyskane wyniki przedstawiono w poniżej tabeli i porównano z wynikami czułości uzyskanymi dla komercyjnych testów EIA wykorzystywanych w Europie (oznakowanych znakiem CE) i uznanych za referencyjne: Stadium kliniczne Liczba surowic Platelia Lyme (1) Test ref. Europa (1) IgG IgM IgG + IgM IgG + IgM Erythema migrans (Stadium I) 17 66,7% [38,4%-88,2%] 58,8% [32,9%-81,6%] 82,4% [56,6%-96,2%] 93,3% [68,1%-99,8%] Neuroborelioza (Stadium II) 33 96,9% [83,4%-99,9%] 36,7% [19,9%-56,1%] 96,9% [83,4%-99,9%] 97,0% [84,2%-99,9%] Acrodermatitis chronica atrophicans (Stadium III) 5 [54,9%-] 20,0% [0,05%-71,6%] [54,9%-] [54,9%-] Lyme Arthritis (Stadium III) 15 [81,9%-] (1) Wyniki niejednoznaczne nie zostały uwzględnione w obliczeniach czułości. IC 95%: 95% przedział ufności. 0,0% [0,0%-18,1%] [81,9%-] [81,9%-] Czułość testu Platelia Lyme IgG wyznaczono także z użyciem panelu udokumentowanych próbek z kolekcji CDC (Centre for Disease Control) i porównano z wynikami czułości uzyskanymi dla komercyjnych testów EIA wykorzystywanych w Europie (oznakowanych znakiem CE) oraz USA (zatwierdzonych przez FDA) i uznanych za referencyjne. Wyniki przedstawiono w poniższej tabeli: Stadium kliniczne Erythema migrans Liczba surowic 28 Test referencyjny Platelia Lyme (1) Europa (1) USA (1) IgG IgM IgG + IgM IgG + IgM IgG + IgM 38,5% [20,2%-59,5%] 73,7% [48,8%-90,9%] 86,4% [65,1%-97,1%] 70,4% [49,8%-86,3%] 87,0% [66,4%-97,2%] Arthritis / Arthralgia 6 [60,7%- ] 40,0% [5,3%-85,3%] [60,7%- ] [60,7%-] [60,7%-] Stadium nieznane 4 [36,8%- ] [0,05%- ] (1) Wyniki niejednoznaczne nie zostały uwzględnione w obliczeniach czułości. IC 95%: 95% przedział ufności. [47,3%- ] [19,4%-99,9%] [36,8%-] 9
10 9.4 Obliczanie indeksu przeciwciał IgG w celu oznaczenia syntezy wewnątrzoponowej Zewnętrzną ocenę przeprowadzono na 104 parach próbek od pacjentów bez neuroboreliozy (n=19), z podejrzeniem (n=29), prawdopodobną (n=36) lub zdiagnozowaną (n=20) neuroboreliozą. Szczegółowe wyniki dla każdej kategorii przedstawiono poniżej: Status Razem PMR nieinterpretacyjny PMR ujemny PMR dodatni Indeks AI IgG dodatni Indeks AI IgG ujemny Indeks AI IgG prawidłowy Brak LNB Podejrzenie LNB Prawdopodobieństwo LNB Zdiagnozowana LNB Status Razem Dodatni (indeks PMR lub AI IgG) Ujemny (indeks PMR lub AI IgG) Niemożliwy do interpretacji (indeks PMR lub AI IgG) Brak LNB 19 1 (5,3%) 18 (94,7%) 0 (0,0%) Podejrzenie LNB (48,3%) 15 (51,7%) 0 (0,0%) Prawdopodobieństwo LNB (66,7%) 10 (27,8%) 2 (5,5%) Zdiagnozowana LNB (85,0%) 2 (10,0%) 1 (5,0%) 9.5 Dokładność Dokładność wewnątrz-testowa (powtarzalność): W celu oceny powtarzalności, jedną próbkę ujemną i trzy dodatnie przebadano 30 razy w ramach jednej serii. Dla każdej próbki określono współczynnik (OD próbki / CO). Średni współczynnik, odchylenie standardowe (SD) oraz współczynnik zmienności (%CV) dla każdej z czterech próbek podano w poniższej tabeli: Dokładność wewnątrz-testowa (powtarzalność) N=30 Próbka ujemna Próbka dodatnia o Próbka dodatnia o Próbka dodatnia niskim mianie wysokim mianie Indeks (OD próbki / wartość odcięcia) Średnia SD %CV 6.0% 8.6% 8.4% 2.1% Powtarzalność między-testowa (odtwarzalność): W celu oceny odtwarzalności, każdą z czterech próbek (jedna ujemna i trzy dodatnie) badano w duplikatach, w dwóch seriach dziennie, przez 20 dni. Dla każdej próbki określono współczynnik (OD próbki / CO). Średni współczynnik, odchylenie standardowe (SD) oraz współczynnik zmienności (%CV) dla każdej z czterech próbek podano w poniższej tabeli: Powtarzalność między-testowa (odtwarzalność) N=80 Próbka negatywna Próbka pozytywna o Próbka pozytywna o Próbka pozytywna niskim mianie wysokim mianie Indeks (OD próbki / wartość odcięcia) Średnia SD %CV 17.3% 14.8% 8.4% 9.7% 10
11 9.6 Reakcje krzyżowe Z użyciem testu Platelia Lyme IgG przebadano 384 próbki krwi, których charakter stwarza potencjalnie ryzyko wystąpienia reakcji niespecyficznych. Wyniki oznaczeń podano w poniższej tabeli: Panel Liczba próbek Niejednoznaczne (1) Dodatnie % reakcji krzyżowych Kiła % (2) CMV % (2) EBV % Leptospiroza % (2) Malaria % (2) Przeciwciała przeciwjądrowe (ANA) Przeciwciała heterofline (HAMA) ,0% % Czynnik reumatoidalny % (2) HSV % Toksoplazmoza % Różyczka % Odra % Świnka % HIV % VZV % RAZEM % (1) Wyniki niejednoznaczne wykluczono z obliczeń reaktywności krzyżowej. (2) Różnica nieistotna w porównaniu do wartości oczekiwanych w rejonach endemicznych (Test Fisher a, p>0.05). Dwie surowice z panelu CMV oraz malaria uznane za dodatnie w teście Platelia Lyme IgG, zostały uznane za dodatnie także w komercyjnym teście EIA wykorzystywanym w Europie (oznakowanym znakiem CE), ale nie zostały potwierdzone metodą western-blot. Surowice z czynnikiem reumatoidalnym uznane za dodatnie w teście Platelia Lyme IgG, zostały uznane za dodatnie także w komercyjnym teście EIA wykorzystywanym w Europie (oznakowanym znakiem CE), a także metodą western-blot. Surowice z panelu leptospiroz uznane za dodatnie w teście Platelia Lyme IgG, zostały uznane za niejednoznaczne w komercyjnym teście EIA wykorzystywanym w Europie (oznakowanym znakiem CE), ale nie zostały potwierdzone metodą western-blot. Surowice z panelu kiły uznane za dodatnie w teście Platelia Lyme IgG, zostały uznane za ujemne w komercyjnym teście EIA wykorzystywanym w Europie (oznakowanym znakiem CE) i nie zostały potwierdzone metodą western-blot 10 OGRANICZENIA PROCEDURY Rozpoznanie zakażenia wywołanego przez Borrelia burgdorferi można postawić wyłącznie na podstawie kombinacji danych klinicznych i biologicznych. Wynik pojedynczego oznaczenia w kierunku przeciwciał klasy IgG przeciwko Borrelia burgdorferi nie stanowi wystarczającego dowodu do postawienia rozpoznania zakażenia wywołanego przez Borrelia burgdorferi sensu lato. Jeżeli wynik badania serologicznego jest dodatni lub niejednoznaczny, zaleca się przebadanie próbki za pomocą metody potwierdzającej takiej jak Western-Blot (9). Rozpoznanie neuroboreliozy można postawić wyłącznie na podstawie kombinacji danych klinicznych i biologicznych swoistych dla pacjenta. Wyników oznaczenia PMR oraz ich interpretacji uzyskanych za pomocą niniejszego protokołu nie należy analizować pojedynczo i uznawać ich za wystarczający dowód do postawienia diagnozy. Obliczenie indeksu IgG za pomocą wzoru Reibera w niniejszym protokole jest nieprawidłowe, jeśli nie uwzględniono wszystkich danych biologicznych (Albuminy surowica, Albuminy PMR, Całkowite IgG Surowica, Całkowite Ig PMR, OD IgG Surowica i OD IgG PMR). Ważne jest także zastosowanie odpowiednich jednostek, jak opisano we wzorze powyżej. Niniejszy protokół zaadaptowano wyłącznie dla przeciwciał IgG przeciwko Borrelia. Nie oceniano go dla przeciwciał IgM przeciwko Borrelia, ani innych przeciwciał IgG. Niniejszy protokół zaadaptowany jest wyłącznie do badania PMR. Żadne inne płyny biologiczne (maziowe,...) nie były ewaluowane. 11
12 11 KONTROLA JAKOŚCI PRODUCENTA Wszystkie odczynniki są przygotowywane zgodnie z naszym systemem jakości, począwszy od materiału wyjściowego aż do ostatecznego produktu komercyjnego. Każda seria ostatecznego produktu podlega oznaczeniu kontrolnemu i jest dopuszczona do użytku, jeśli spełnia wymagane kryteria. Bio-Rad posiada protokoły produkcji i kontroli jakości każdej serii odczynników. 12 LITERATURA 1. Aguero-Rosenfeld, M. E., Wang, G., Schwartz, I., Wormser, G Diagnosis of Lyme borreliosis. Clin. Microbiol. Rev. 18: Burgdorfer, W., Barbour, A. G., Hayes, S. F., Benach, J. L., Grunwaldt, E., Davis, J.P Lyme disease a tickborne spirochetosis? Science. 216: Center for Disease Control and Prevention Lyme disease United States, Morb. Mortal. Wkly. Rep. 53: Hubalek, Z., Halouzka, J Distribution of Borrelia burgdorferi sensu lato genomic groups in Europe, a review. Eur. J. Epidemiol. 13: Reed, K. D Laboratory testing for Lyme disease: possibilities and practicalities. J. Clin. Microbiol. 40: Stanek, G., Strle, F Lyme borreliosis. Lancet. 362: Wang, G., Van Dam, A. P., Spanjaard, L., Dankert, J Molecular typing of Borrelia burgdorferi sensu lato: taxonomic, epidemiological, and clinical implications. Clin. Microbiol. Rev. 12: Rudenko, N., Golovchenko, M., Grubhoffer, L Updates on Borrelia burgdorferi sensu lato complex with respect to public health. Ticks Tick Borne Dis. 2(3): Wilske, B Diagnosis of Lyme borreliosis in Europe. Vector Borne Zoonotic Dis. 3: Bednarova, J Cerebrospinal-Fluid profile in neuroborreliosis and its diagnosis significance. Folia Microbiol. 51: Deisenhammer F., Bartos A., Egg R., Gilhus N.E., Giovannoni G., Rauer S., Sellebjerg F Guidelines on Routine Cerebrospinal Fluid Analysis. Report from EFNS Task Force. Europ. Journ. of Neurol Reiber H., Lange P Quantification of Virus-Specific Antibodies in Cerebrospinal Fluid and Serum: Sensitive and Specific Detection of Antibody Synthesis in Brain. Clin. Chem. 37:
13 13
14 Bio-Rad 3, boulevard Raymond Poincaré Marnes-la-Coquette France Tel. : +33 (0) /11 Fax : +33 (0)
PLATELIA LYME IgM /11
 PLATELIA LYME IgM 1 płytka 96 72951 Test immunoenzymatyczny do jakościowego wykrywania przeciwciał klasy IgM przeciwko borrelia burgdorferi sensu lato w ludzkiej surowicy lub osoczu 883688 2015/11 1. PRZEZNACZENIE
PLATELIA LYME IgM 1 płytka 96 72951 Test immunoenzymatyczny do jakościowego wykrywania przeciwciał klasy IgM przeciwko borrelia burgdorferi sensu lato w ludzkiej surowicy lub osoczu 883688 2015/11 1. PRZEZNACZENIE
Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu.
 WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
WSTĘP Test Immunoenzymatyczny DRG Kortyzol dostarcza materiałów do oznaczania kortyzolu w surowicy i osoczu. Test jest przeznaczony wyłącznie do stosowania ZASADA OZNACZENIA Ten test immunoenzymatyczny
PLATELIA M. PNEUMONIAE IgG TMB 96 testów 72780
 PLATELIA M. PNEUMONIAE IgG TMB 96 testów 72780 TEST IMMUNOENZYMATYCZNY DO PÓŁILOŚCIOWEGO OZNACZANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO MYCOPLASMA PNEUMONIAE W SUROWICY LUDZKIEJ 1- ZNACZENIE KLINICZNE Mycoplasma
PLATELIA M. PNEUMONIAE IgG TMB 96 testów 72780 TEST IMMUNOENZYMATYCZNY DO PÓŁILOŚCIOWEGO OZNACZANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO MYCOPLASMA PNEUMONIAE W SUROWICY LUDZKIEJ 1- ZNACZENIE KLINICZNE Mycoplasma
PLATELIA TM Mumps IgM
 PLATELIA TM Mumps IgM 48 testów 72689 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI ŚWINKI W LUDZKIEJ SUROWICY Polski 1/9 SPIS TREŚCI 1. ZASTOSOWANIE 2. ZNACZENIE KLINICZNE
PLATELIA TM Mumps IgM 48 testów 72689 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI ŚWINKI W LUDZKIEJ SUROWICY Polski 1/9 SPIS TREŚCI 1. ZASTOSOWANIE 2. ZNACZENIE KLINICZNE
Platelia Rubella IgM 1 płytka
 Platelia Rubella IgM 1 płytka 96 72851 TEST IMMUNOENZYMATYCZNY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI RÓŻYCZKI W LUDZKIEJ SUROWICY LUB OSOCZU 881142 2013/11 1. ZASTOSOWANIE
Platelia Rubella IgM 1 płytka 96 72851 TEST IMMUNOENZYMATYCZNY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI RÓŻYCZKI W LUDZKIEJ SUROWICY LUB OSOCZU 881142 2013/11 1. ZASTOSOWANIE
TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY
 PLATELIA TM VZV IgM 48 testów 72685 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI VARICELLA-ZOSTER W LUDZKIEJ SUROWICY Polski 1/10 1. ZASTOSOWANIE SPIS TREŚCI 2. ZNACZENIE
PLATELIA TM VZV IgM 48 testów 72685 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI VARICELLA-ZOSTER W LUDZKIEJ SUROWICY Polski 1/10 1. ZASTOSOWANIE SPIS TREŚCI 2. ZNACZENIE
TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY
 PLATELIA TM VZV IgG 48 testów 72684 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI VARICELLA-ZOSTER W LUDZKIEJ SUROWICY Polski 1/9 1. ZASTOSOWANIE SPIS TREŚCI 2. ZNACZENIE
PLATELIA TM VZV IgG 48 testów 72684 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI VARICELLA-ZOSTER W LUDZKIEJ SUROWICY Polski 1/9 1. ZASTOSOWANIE SPIS TREŚCI 2. ZNACZENIE
PLATELIA TOXO IgG AVIDITY
 PLATELIA TOXO IgG AVIDITY 48 72842 OZNACZANIE AWIDNOŚCI PRZECIWCIAŁ KLASY IGG PRZECIWKO TOXOPLASMA GONDII W LUDZKIEJ SUROWICY METODĄ IMMUNOENZYMATYCZNĄ 881130 2013/11 1. ZASTOSOWANIE Test Platelia Toxo
PLATELIA TOXO IgG AVIDITY 48 72842 OZNACZANIE AWIDNOŚCI PRZECIWCIAŁ KLASY IGG PRZECIWKO TOXOPLASMA GONDII W LUDZKIEJ SUROWICY METODĄ IMMUNOENZYMATYCZNĄ 881130 2013/11 1. ZASTOSOWANIE Test Platelia Toxo
Mycoplasma pneumoniae IgG ELISA
 Instrukcja Użytkownika Mycoplasma pneumoniae IgG ELISA EIA-3499 96 wells DRG Instruments GmbH, Germany Frauenbergstr. 18, D-35039 Marburg Telefon: +49 (0)64 21-1 700 0, Fax: +49-(0)6 42 1-170 0 50 Internet:
Instrukcja Użytkownika Mycoplasma pneumoniae IgG ELISA EIA-3499 96 wells DRG Instruments GmbH, Germany Frauenbergstr. 18, D-35039 Marburg Telefon: +49 (0)64 21-1 700 0, Fax: +49-(0)6 42 1-170 0 50 Internet:
Zastosowanie. Zestaw DRG Epstein Barr Virus (VCA) zapewnia materiały do pomiaru przeciwciał Epstein Barr (VCA) w klasie IgG w surowicy.
 Zastosowanie Zestaw DRG Epstein Barr Virus (VCA) zapewnia materiały do pomiaru przeciwciał Epstein Barr (VCA) w klasie IgG w surowicy. Zasada Metody Zestaw DRG Epstein Barr Virus (VCA) IgG ELISA Kit jest
Zastosowanie Zestaw DRG Epstein Barr Virus (VCA) zapewnia materiały do pomiaru przeciwciał Epstein Barr (VCA) w klasie IgG w surowicy. Zasada Metody Zestaw DRG Epstein Barr Virus (VCA) IgG ELISA Kit jest
Mycoplasma pneumoniae IgM ELISA
 Instrukcja Użytkownika Mycoplasma pneumoniae IgM ELISA EIA-3500 96 wells DRG Instruments GmbH, Germany Frauenbergstr. 18, D-35039 Marburg Telefon: +49 (0)64 21-1 700 0, Fax: +49-(0)6 42 1-170 0 50 Internet:
Instrukcja Użytkownika Mycoplasma pneumoniae IgM ELISA EIA-3500 96 wells DRG Instruments GmbH, Germany Frauenbergstr. 18, D-35039 Marburg Telefon: +49 (0)64 21-1 700 0, Fax: +49-(0)6 42 1-170 0 50 Internet:
SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA Część I
 Część I 1. API 20 E zastosowanie: identyfikacja Salmonella, Yersinia; opakowanie zawiera 25 pasków 2. Suspension Medium (5ml) zastosowanie: identyfikacja Salmonella; produkt płynny; składowe do zestawu
Część I 1. API 20 E zastosowanie: identyfikacja Salmonella, Yersinia; opakowanie zawiera 25 pasków 2. Suspension Medium (5ml) zastosowanie: identyfikacja Salmonella; produkt płynny; składowe do zestawu
DRG International, Inc., USA Fax: (973)
 1. WSTĘP 1.1. Zastosowanie Zestaw DRG Leptin ELISA jest testem immunoenzymatycznym do pomiaru leptyny w surowicy i osoczu. 2. ZASADA TESTU Zestaw DRG leptin ELISA jest testem immunoenzymatycznym stałej
1. WSTĘP 1.1. Zastosowanie Zestaw DRG Leptin ELISA jest testem immunoenzymatycznym do pomiaru leptyny w surowicy i osoczu. 2. ZASADA TESTU Zestaw DRG leptin ELISA jest testem immunoenzymatycznym stałej
/11 1. ZASTOSOWANIE
 PLATELIA CMV IgG 1 płytka 96 72810 TEST IMMUNOENZYMATYCZNY DO ILOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI CYTOMEGALII W LUDZKIEJ SUROWICY LUB OSOCZU 881140 2013/11 1. ZASTOSOWANIE Platelia
PLATELIA CMV IgG 1 płytka 96 72810 TEST IMMUNOENZYMATYCZNY DO ILOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI CYTOMEGALII W LUDZKIEJ SUROWICY LUB OSOCZU 881140 2013/11 1. ZASTOSOWANIE Platelia
Samodzielny Publiczny Zespół... Zakładów Opieki Zdrowotnej w Kozienicach... ul. Al. Wł. Sikorskiego 10
 Załącznik nr 2 do SIWZ Wykonawca:... Samodzielny Publiczny Zespół... Zakładów Opieki Zdrowotnej w Kozienicach... ul. Al. Wł. Sikorskiego 10 tel.:/fax:... 26-900 Kozienice tel.:/fax: (48) 382 88 00/ (48)
Załącznik nr 2 do SIWZ Wykonawca:... Samodzielny Publiczny Zespół... Zakładów Opieki Zdrowotnej w Kozienicach... ul. Al. Wł. Sikorskiego 10 tel.:/fax:... 26-900 Kozienice tel.:/fax: (48) 382 88 00/ (48)
MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ
 MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ Puławy 2013 Opracowanie: Prof. dr hab. Iwona Markowska-Daniel, mgr inż. Kinga Urbaniak,
MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ Puławy 2013 Opracowanie: Prof. dr hab. Iwona Markowska-Daniel, mgr inż. Kinga Urbaniak,
2. ZNACZENIE KLINICZNE
 PLATELIA CMV IgM 1 płytka 96 72811 TEST IMMUNOENZYMATYCZNY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI CYTOMEGALII W LUDZKIEJ SUROWICY LUB OSOCZU 881139 2013/11 1. ZASTOSOWANIE
PLATELIA CMV IgM 1 płytka 96 72811 TEST IMMUNOENZYMATYCZNY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgM PRZECIWKO WIRUSOWI CYTOMEGALII W LUDZKIEJ SUROWICY LUB OSOCZU 881139 2013/11 1. ZASTOSOWANIE
Test DRG DHEA-S ELISA jest testem immunoenzymatycznym do ilościowego diagnostycznego oznaczania DHEA-S w surowicy i osoczu w warunkach in vitro.
 WSTĘP 1.1 Przeznaczenie Test DRG DHEA-S ELISA jest testem immunoenzymatycznym do ilościowego diagnostycznego oznaczania DHEA-S w surowicy i osoczu w warunkach in vitro. 1.2 Streszczenie i Wyjaśnienia Dehydroepiandrosteron
WSTĘP 1.1 Przeznaczenie Test DRG DHEA-S ELISA jest testem immunoenzymatycznym do ilościowego diagnostycznego oznaczania DHEA-S w surowicy i osoczu w warunkach in vitro. 1.2 Streszczenie i Wyjaśnienia Dehydroepiandrosteron
2. ZNACZENIE KLINICZNE
 PLATELIA Toxo IgG 1 płytka 96 72840 TEST IMMUNOENZYMATYCZNY DO ILOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO TOXOPLASMA GONDII W LUDZKIEJ SUROWICY LUB OSOCZU 881127 2013/11 1. ZASTOSOWANIE Platelia
PLATELIA Toxo IgG 1 płytka 96 72840 TEST IMMUNOENZYMATYCZNY DO ILOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO TOXOPLASMA GONDII W LUDZKIEJ SUROWICY LUB OSOCZU 881127 2013/11 1. ZASTOSOWANIE Platelia
ROTA-ADENO Virus Combo Test Device
 Kod produktu: 8.04.73.0.0020 ROTA-ADENO Virus Combo Test Device Tylko do diagnostyki in vitro Przechowywać w 2-30 C ZASTOSOWANIE Wykrywanie antygenów Rotawirusów i Adenowirusów w próbkach kału. WSTĘP Rotawirusy
Kod produktu: 8.04.73.0.0020 ROTA-ADENO Virus Combo Test Device Tylko do diagnostyki in vitro Przechowywać w 2-30 C ZASTOSOWANIE Wykrywanie antygenów Rotawirusów i Adenowirusów w próbkach kału. WSTĘP Rotawirusy
Zestaw DRG Epstein Barr Virus (VCA) IgM zapewnia materiały do pomiaru przeciwciał Epstein Barr (VCA) w klasie IgM w surowicy.
 Zastosowanie Zestaw DRG Epstein Barr Virus (VCA) IgM zapewnia materiały do pomiaru przeciwciał Epstein Barr (VCA) w klasie IgM w surowicy. Zasada Metody Zestaw DRG Epstein Barr Virus (VCA) IgM ELISA Kit
Zastosowanie Zestaw DRG Epstein Barr Virus (VCA) IgM zapewnia materiały do pomiaru przeciwciał Epstein Barr (VCA) w klasie IgM w surowicy. Zasada Metody Zestaw DRG Epstein Barr Virus (VCA) IgM ELISA Kit
1 płytka - 96 72530 5 płytek - 480 72531
 Syphilis Total Ab 1 płytka - 96 72530 5 płytek - 480 72531 ZESTAWY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ TREPONEMA PALLIDUM W SUROWICY LUB OSOCZU KRWI LUDZKIEJ Z ZASTOSOWANIEM TECHNIKI ENZYMATYCZNEGO
Syphilis Total Ab 1 płytka - 96 72530 5 płytek - 480 72531 ZESTAWY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ TREPONEMA PALLIDUM W SUROWICY LUB OSOCZU KRWI LUDZKIEJ Z ZASTOSOWANIEM TECHNIKI ENZYMATYCZNEGO
FORMULARZ CENOWY CZĘŚĆ I. Jedn. miary
 FORMULARZ CENOWY CZĘŚĆ I 1. API 20 E zastosowanie: identyfikacja Salmonella, Yersinia; opakowanie zawiera 25 pasków; 2. Suspension Medium (5ml) zastosowanie: identyfikacja Salmonella; produkt płynny; składowe
FORMULARZ CENOWY CZĘŚĆ I 1. API 20 E zastosowanie: identyfikacja Salmonella, Yersinia; opakowanie zawiera 25 pasków; 2. Suspension Medium (5ml) zastosowanie: identyfikacja Salmonella; produkt płynny; składowe
Platelia CMV IgG AVIDITY
 Platelia CMV IgG AVIDITY 48 72812 TEST IMMUNOENZYMATYCZNY DO OKREŚLANIA AWIDNOŚCI PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI CYTOMEGALII W LUDZKIEJ SUROWICY 881171-2015/01 SPIS TREŚCI 1. ZASTOSOWANIE 2.
Platelia CMV IgG AVIDITY 48 72812 TEST IMMUNOENZYMATYCZNY DO OKREŚLANIA AWIDNOŚCI PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI CYTOMEGALII W LUDZKIEJ SUROWICY 881171-2015/01 SPIS TREŚCI 1. ZASTOSOWANIE 2.
AE/ZP-27-74/16 Załącznik Nr 6
 AE/ZP-27-74/16 Załącznik Nr 6 Wymagania dla UWAGA! Oferta nie spełniająca poniższych wymagań będzie odrzucona L.p. Wymagane parametry Wymagania wobec przedmiotu zmówienia oferowanego w Pakiecie Nr 1 Wszystkie
AE/ZP-27-74/16 Załącznik Nr 6 Wymagania dla UWAGA! Oferta nie spełniająca poniższych wymagań będzie odrzucona L.p. Wymagane parametry Wymagania wobec przedmiotu zmówienia oferowanego w Pakiecie Nr 1 Wszystkie
Cena jedn. netto. A B C D E F G H 1. Paski do moczu 10-cio parametrowe z użyciem aparatu LABUREADER. Szt. 400 oznaczeń
 Sprawa nr 12/D/2010 PAKIET 1 Paski do badań moczu z użyciem aparatu LABUREADER podatku Wartość netto za ilość określoną w 1. Paski do moczu 10-cio parametrowe z użyciem aparatu LABUREADER Szt. 8 000 2.
Sprawa nr 12/D/2010 PAKIET 1 Paski do badań moczu z użyciem aparatu LABUREADER podatku Wartość netto za ilość określoną w 1. Paski do moczu 10-cio parametrowe z użyciem aparatu LABUREADER Szt. 8 000 2.
FORMULARZ ASORTYMENTOWO CENOWY. VAT kolumnie D A B C D E F G H. Szt oznaczeń. PAKIET 1 Cena netto...zł + VAT:...% tj...zł., Cena brutto... zł.
 Sprawa PN/ 12/D/2012 Załącznik nr 1 do siwz UWAGA WYMOGI DLA WSZYSTKICH PAKIETÓW - DO OFERTY NALEŻY DOŁĄCZYĆ: 1. instrukcje w języku polskim, druk czytelny 2. karty charakterystyki dla odczynników zawierających
Sprawa PN/ 12/D/2012 Załącznik nr 1 do siwz UWAGA WYMOGI DLA WSZYSTKICH PAKIETÓW - DO OFERTY NALEŻY DOŁĄCZYĆ: 1. instrukcje w języku polskim, druk czytelny 2. karty charakterystyki dla odczynników zawierających
Monolisa HBs Ag ULTRA 1 płytka 96 testów 72346 5 płytek 480 testów 72348
 Monolisa HBs Ag ULTRA 1 płytka 96 testów 72346 5 płytek 480 testów 72348 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA ANTYGENU POWIERZCHNIOWEGO WIRUSA ZAPALENIA WĄTROBY TYPU B W SUROWICY LUB OSOCZU Wyrób do diagnostyki
Monolisa HBs Ag ULTRA 1 płytka 96 testów 72346 5 płytek 480 testów 72348 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA ANTYGENU POWIERZCHNIOWEGO WIRUSA ZAPALENIA WĄTROBY TYPU B W SUROWICY LUB OSOCZU Wyrób do diagnostyki
FORMULARZ ASORTYMENTOWO CENOWY. PAKIET I Paski do badań moczu z użyciem aparatu LABUREADER. VAT kolumnie D A B C D E F G H. Szt.
 UWAGA WYMOGI DLA WSZYSTKICH PAKIETÓW - DO OFERTY NALEŻY DOŁĄCZYĆ: 1. instrukcje w języku polskim, druk czytelny 2. karty charakterystyki dla odczynników zawierających substancje niebezpieczne PAKIET I
UWAGA WYMOGI DLA WSZYSTKICH PAKIETÓW - DO OFERTY NALEŻY DOŁĄCZYĆ: 1. instrukcje w języku polskim, druk czytelny 2. karty charakterystyki dla odczynników zawierających substancje niebezpieczne PAKIET I
Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu
 Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu PROGRAM WHO ELIMINACJI ODRY/RÓŻYCZKI Program eliminacji odry i różyczki został uchwalony przez Światowe Zgromadzenie Zdrowia 28 maja 2003 roku. Realizacja
Wojewódzka Stacja Sanitarno-Epidemiologiczna w Poznaniu PROGRAM WHO ELIMINACJI ODRY/RÓŻYCZKI Program eliminacji odry i różyczki został uchwalony przez Światowe Zgromadzenie Zdrowia 28 maja 2003 roku. Realizacja
do zastosowania wraz z mikropłytkami MUG/EC do wykrywania Escherichia coli w kąpieliskach.
 AGZ.272.2.206 Część I- MIKROPŁYTKI MUG/EC Załącznik A do siwz. Mikropłytki MUG/EC do wykrywania bakterii Escherichia coli w kąpieliskach 2. Rozcieńczalnik do prób wody DSM z solą zastosowanie: do wykrywania
AGZ.272.2.206 Część I- MIKROPŁYTKI MUG/EC Załącznik A do siwz. Mikropłytki MUG/EC do wykrywania bakterii Escherichia coli w kąpieliskach 2. Rozcieńczalnik do prób wody DSM z solą zastosowanie: do wykrywania
Techniki immunoenzymatycznego oznaczania poziomu hormonów (EIA)
 Techniki immunoenzymatycznego oznaczania poziomu hormonów (EIA) Wstęp: Test ELISA (ang. Enzyme-Linked Immunosorbent Assay), czyli test immunoenzymatyczny (ang. Enzyme Immunoassay - EIA) jest obecnie szeroko
Techniki immunoenzymatycznego oznaczania poziomu hormonów (EIA) Wstęp: Test ELISA (ang. Enzyme-Linked Immunosorbent Assay), czyli test immunoenzymatyczny (ang. Enzyme Immunoassay - EIA) jest obecnie szeroko
RPR
 RPR 100 72515 500 72516 ZESTAWY DO ILOŚCIOWYCH I PÓŁILOŚCIOWYCH TESTÓW KARTOWYCH JEDNORAZOWEGO UŻYTKU, DO WYKRYWANIA NIEKRĘTKOWYCH PRZECIWCIAŁ KIŁOWYCH W SUROWICY LUDZKIEJ I OSOCZU METODĄ AGLUTYNACJI MIKROSKOPOWEJ
RPR 100 72515 500 72516 ZESTAWY DO ILOŚCIOWYCH I PÓŁILOŚCIOWYCH TESTÓW KARTOWYCH JEDNORAZOWEGO UŻYTKU, DO WYKRYWANIA NIEKRĘTKOWYCH PRZECIWCIAŁ KIŁOWYCH W SUROWICY LUDZKIEJ I OSOCZU METODĄ AGLUTYNACJI MIKROSKOPOWEJ
Instrukcja do testu Anty-Borrelia burgdorferi VIsE ELISA (IgG)
 Instrukcja do testu Anty-Borrelia burgdorferi VIsE ELISA (IgG) NUMER KATALOGOWY PRZECIWCIAŁA PRZECIW KLASA IG SUBSTRAT FORMAT EI 2132-9601-1 G antygen Borrelia VlsE IgG Opłaszczona antygenem płyta mikrotitracyjna
Instrukcja do testu Anty-Borrelia burgdorferi VIsE ELISA (IgG) NUMER KATALOGOWY PRZECIWCIAŁA PRZECIW KLASA IG SUBSTRAT FORMAT EI 2132-9601-1 G antygen Borrelia VlsE IgG Opłaszczona antygenem płyta mikrotitracyjna
Monolisa Anti-HBs PLUS 2 płytek - 192 72566
 Monolisa Anti-HBs PLUS 2 płytek - 192 72566 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA I OZNACZANIA POZIOMU PRZECIWCIAŁ PRZECIWKO ANTYGENOWI POWIERZCHNIOWEMU WIRUSA ZAPALENIA WĄTROBY TYPU B (anty-hbs) W LUDZKIEJ
Monolisa Anti-HBs PLUS 2 płytek - 192 72566 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA I OZNACZANIA POZIOMU PRZECIWCIAŁ PRZECIWKO ANTYGENOWI POWIERZCHNIOWEMU WIRUSA ZAPALENIA WĄTROBY TYPU B (anty-hbs) W LUDZKIEJ
ELIMINACJA ODRY/RÓŻYCZKI
 PAŃSTWOWY ZAKŁAD HIGIENY INSTYTUT NAUKOWO-BADAWCZY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE - ZASADY - INSTRUKCJE ZAKŁAD WIRUSOLOGII UL. CHOCIMSKA 24 00-791 WARSZAWA PROGRAM ELIMINACJI
PAŃSTWOWY ZAKŁAD HIGIENY INSTYTUT NAUKOWO-BADAWCZY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE - ZASADY - INSTRUKCJE ZAKŁAD WIRUSOLOGII UL. CHOCIMSKA 24 00-791 WARSZAWA PROGRAM ELIMINACJI
AmpliTest Babesia spp. (PCR)
 AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
(Akty o charakterze nieustawodawczym) DECYZJE
 19.7.2019 PL L 193/1 II (Akty o charakterze nieustawodawczym) DECYZJE DECYZJA WYKONAWCZA KOMISJI (UE) 2019/1244 z dnia 1 lipca 2019 r. zmieniająca decyzję 2002/364/WE w odniesieniu do wymogów dotyczących
19.7.2019 PL L 193/1 II (Akty o charakterze nieustawodawczym) DECYZJE DECYZJA WYKONAWCZA KOMISJI (UE) 2019/1244 z dnia 1 lipca 2019 r. zmieniająca decyzję 2002/364/WE w odniesieniu do wymogów dotyczących
Genomic Mini AX Plant Spin
 Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
Ilość. zestaw = 60 oznaczeń. zestaw = 60 oznaczeń. zestaw = 60 oznaczeń. zestaw = 60 oznaczeń. zestaw = 60 oznaczeń. zestaw = 30 oznaczeń
 EAZ.272.2.20 KALKULACJA CENY OFERTY Część I - Testy diagnostyczne Załącznik 5 do siwz L.p. Przedmiot zamówienia Szczegółowy opis Jednostka miary Ilość Cena jednostkowa brutto [zł]** Wartość brutto [zł].
EAZ.272.2.20 KALKULACJA CENY OFERTY Część I - Testy diagnostyczne Załącznik 5 do siwz L.p. Przedmiot zamówienia Szczegółowy opis Jednostka miary Ilość Cena jednostkowa brutto [zł]** Wartość brutto [zł].
ELISA PeliClass human IgG subclass kit REF M1551
 Sanquin Reagents Plesmanlaan 5 0 CX Amsterdam The Netherlands Phone: +.0.5.599 Fax: +.0.5.570 Email: reagents@sanquin.nl Website: www.sanquinreagents.com M55/ November 007 ELISA PeliClass human IgG subclass
Sanquin Reagents Plesmanlaan 5 0 CX Amsterdam The Netherlands Phone: +.0.5.599 Fax: +.0.5.570 Email: reagents@sanquin.nl Website: www.sanquinreagents.com M55/ November 007 ELISA PeliClass human IgG subclass
Genomic Midi AX Direct zestaw do izolacji genomowego DNA (procedura bez precypitacji) wersja 1215
 Genomic Midi AX Direct zestaw do izolacji genomowego DNA (procedura bez precypitacji) wersja 1215 20 izolacji Nr kat. 895-20D Pojemność kolumny do oczyszczania DNA wynosi 100 µg 1 Skład zestawu Składnik
Genomic Midi AX Direct zestaw do izolacji genomowego DNA (procedura bez precypitacji) wersja 1215 20 izolacji Nr kat. 895-20D Pojemność kolumny do oczyszczania DNA wynosi 100 µg 1 Skład zestawu Składnik
Zestaw do wykrywania Chlamydia trachomatis w moczu lub w kulturach komórkowych
 Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
KOAGULOLOGIA. Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice.
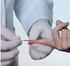 KOAGULOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
KOAGULOLOGIA POBIERANIE KRWI ŻYLNEJ Pobieranie krwi żylnej przy pomocy systemu otwartego: Przed każdym pobieraniem krwi należy umyć ręce i nałożyć rękawice. Wyszukać żyłę odpowiednią do pobrania krwi.
DRG International, Inc., USA Fax: (973)
 Zastosowanie Test DRG -HCG ELISA jest testem immunoenzymatycznym do oznaczania stężenia całkowitej ludzkiej gonadotropiny kosmówkowej (hcg i β-hcg) w surowicy. Streszczenie i wyjaśnienia Ludzka gonadotropina
Zastosowanie Test DRG -HCG ELISA jest testem immunoenzymatycznym do oznaczania stężenia całkowitej ludzkiej gonadotropiny kosmówkowej (hcg i β-hcg) w surowicy. Streszczenie i wyjaśnienia Ludzka gonadotropina
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH
 Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
Wirus zapalenia wątroby typu B
 Wirus zapalenia wątroby typu B Kliniczne następstwa zakażenia odsetek procentowy wyzdrowienie przewlekłe zakażenie Noworodki: 10% 90% Dzieci 1 5 lat: 70% 30% Dzieci starsze oraz 90% 5% - 10% Dorośli Choroby
Wirus zapalenia wątroby typu B Kliniczne następstwa zakażenia odsetek procentowy wyzdrowienie przewlekłe zakażenie Noworodki: 10% 90% Dzieci 1 5 lat: 70% 30% Dzieci starsze oraz 90% 5% - 10% Dorośli Choroby
Testosteron jest odpowiedzialny za rozwój wtórnych męskich cech płciowych i pomiar stężenia tego hormonu jest pomocny w ocenie hypogonadyzmu
 WSTĘP Przeznaczenie Test Testosteron ELISA jest testem immunoenzymatycznym do ilościowego diagnostycznego oznaczania testosteronu w surowicy i osoczu w warunkach in vitro. STRESZCZENIE I WYJAŚNIENIA Testosteron
WSTĘP Przeznaczenie Test Testosteron ELISA jest testem immunoenzymatycznym do ilościowego diagnostycznego oznaczania testosteronu w surowicy i osoczu w warunkach in vitro. STRESZCZENIE I WYJAŚNIENIA Testosteron
Genomic Mini AX Bacteria+ Spin
 Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
AmpliTest Salmonella spp. (Real Time PCR)
 AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
Zestaw do wykrywania Babesia spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych
 Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616
 Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616 10 izolacji Nr kat. 995-10 Pojemność kolumny do oczyszczania DNA wynosi 500 µg 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616 10 izolacji Nr kat. 995-10 Pojemność kolumny do oczyszczania DNA wynosi 500 µg 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
AE/ZP-27-03/16 Załącznik Nr 6
 AE/ZP--0/ Załącznik Nr Wymagania dla przedmiotu zamówienia oferowanego w Pakietach Nr - Lp Parametry wymagane Wymagania dla przedmiotu zamówienia oferowanego w Pakiecie Nr poz..... Surowica antyglobulinowa
AE/ZP--0/ Załącznik Nr Wymagania dla przedmiotu zamówienia oferowanego w Pakietach Nr - Lp Parametry wymagane Wymagania dla przedmiotu zamówienia oferowanego w Pakiecie Nr poz..... Surowica antyglobulinowa
Cena jedn. netto. A B C D E F G H 1. Paski do moczu 10-cio parametrowe z Szt. użyciem aparatu LABUREADER. Szt. 200 oznaczeń
 Sprawa nr 10/D/2009 Formularz asortymentowo cenowy PAKIET 1 Paski do badań moczu podatku Wartość netto za ilość określoną w 1. Paski do moczu 10-cio parametrowe z użyciem aparatu LABUREADER 4 000 2. Gumowe
Sprawa nr 10/D/2009 Formularz asortymentowo cenowy PAKIET 1 Paski do badań moczu podatku Wartość netto za ilość określoną w 1. Paski do moczu 10-cio parametrowe z użyciem aparatu LABUREADER 4 000 2. Gumowe
Genomic Mini AX Milk Spin
 Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Genomic Maxi AX Direct
 Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
Genomic Micro AX Blood Gravity 96-well
 Genomic Micro AX Blood Gravity 96-well Zestaw do izolacji DNA z krwi w formacie płytek na 96 studzienek dedykowany do pracy z pipetą wielokanałową lub automatem typu liquid handler. 960 izolacji Nr kat.
Genomic Micro AX Blood Gravity 96-well Zestaw do izolacji DNA z krwi w formacie płytek na 96 studzienek dedykowany do pracy z pipetą wielokanałową lub automatem typu liquid handler. 960 izolacji Nr kat.
Gel-Out. 50 izolacji, 250 izolacji. Nr kat , Zestaw do izolacji DNA z żelu agarozowego. wersja 0617
 Gel-Out Zestaw do izolacji DNA z żelu agarozowego. wersja 0617 50 izolacji, 250 izolacji Nr kat. 023-50, 023-250 Pojemność kolumny do izolacji DNA - do 20 µg DNA, minimalna pojemność - 2 µg DNA (przy zawartości
Gel-Out Zestaw do izolacji DNA z żelu agarozowego. wersja 0617 50 izolacji, 250 izolacji Nr kat. 023-50, 023-250 Pojemność kolumny do izolacji DNA - do 20 µg DNA, minimalna pojemność - 2 µg DNA (przy zawartości
SPEŁNIENIE DRUGIEGO KRYTERIUM OCENY OFERT
 PN/9OL/09/0 Załącznik nr 8 SPEŁNIENIE DRUGIEGO KRYTERIUM OCENY OFERT PRZEDMIOT ZAMÓWIENIA: dostawy odczynników. Kryterium jakości odczynników (pakiety nr: -, 0-, 7) Nr Nazwa Parametry oceniane Wartość
PN/9OL/09/0 Załącznik nr 8 SPEŁNIENIE DRUGIEGO KRYTERIUM OCENY OFERT PRZEDMIOT ZAMÓWIENIA: dostawy odczynników. Kryterium jakości odczynników (pakiety nr: -, 0-, 7) Nr Nazwa Parametry oceniane Wartość
ZP/220/106/17 Parametry wymagane dla zadania nr 1 załącznik nr 4 do formularza oferty PO MODYFIKACJI
 Zadanie nr 1 odczynniki do badań serologicznych UWAGA: wszystkie metodyki badań opracowane przez producentów powinny być zgodne z obowiązującymi przepisami. Lp. Nazwa PARAMETRY WYMAGANE TAK / NIE Reagujący
Zadanie nr 1 odczynniki do badań serologicznych UWAGA: wszystkie metodyki badań opracowane przez producentów powinny być zgodne z obowiązującymi przepisami. Lp. Nazwa PARAMETRY WYMAGANE TAK / NIE Reagujący
STĘŻENIE CHEMOKINY CXCL13 W PŁYNIE MÓZGOWO-RDZENIOWYM CHORYCH Z NEUROBORELIOZĄ OBSERWACJE WŁASNE
 PRZEGL EPIDEMIOL 2015; 69: 851-855 Problemy zakażeń Lucjan Kępa, Barbara Oczko-Grzesik, Barbara Sobala-Szczygieł, Anna Boroń- Kaczmarska STĘŻENIE CHEMOKINY CXCL13 W PŁYNIE MÓZGOWO-RDZENIOWYM CHORYCH Z
PRZEGL EPIDEMIOL 2015; 69: 851-855 Problemy zakażeń Lucjan Kępa, Barbara Oczko-Grzesik, Barbara Sobala-Szczygieł, Anna Boroń- Kaczmarska STĘŻENIE CHEMOKINY CXCL13 W PŁYNIE MÓZGOWO-RDZENIOWYM CHORYCH Z
AGZ KALKULACJA CENY OFERTY Część I- Wskaźniki biologiczne do kontroli procesu sterylizacji. Załącznik 5 do siwz
 Część I- Wskaźniki biologiczne do kontroli procesu sterylizacji L.p. Przedmiot zamówienia. Sporal A - wskaźnik biologiczny zastosowanie: wskaźnik do kontroli sterylizacji parą wodną w autoklawie wg normy
Część I- Wskaźniki biologiczne do kontroli procesu sterylizacji L.p. Przedmiot zamówienia. Sporal A - wskaźnik biologiczny zastosowanie: wskaźnik do kontroli sterylizacji parą wodną w autoklawie wg normy
Genomic Midi AX. 20 izolacji
 Genomic Midi AX Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura z precypitacją DNA. wersja 0517 20 izolacji Nr kat. 895-20 Pojemność kolumny do oczyszczania
Genomic Midi AX Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura z precypitacją DNA. wersja 0517 20 izolacji Nr kat. 895-20 Pojemność kolumny do oczyszczania
marketinginformacja Diagnostyka weterynaryjna Szybkie testy dla rolnictwa +++ dostępne w SalesPlusie +++
 marketinginformacja Data 24.10.2014 Numer Autor MI_FS_13_2014_Testy weterynaryjne Philipp Peters Diagnostyka weterynaryjna Szybkie testy dla rolnictwa +++ dostępne w SalesPlusie +++ Dzięki szybkim testom
marketinginformacja Data 24.10.2014 Numer Autor MI_FS_13_2014_Testy weterynaryjne Philipp Peters Diagnostyka weterynaryjna Szybkie testy dla rolnictwa +++ dostępne w SalesPlusie +++ Dzięki szybkim testom
Spis treści 1. ZASTOSOWANIE 2. WSKAZANIA 3. STRESZCZENIE I OBJAŚNIENIA 4. ZASADA DZIAŁANIA PROCEDURY 5. ODCZYNNIKI 6 OSTRZEŻENIA DLA UŻYTKOWNIKÓW
 PLATELIA ASPERGILLUS Ag 96 TESTÓW 62794 Test Platelia Aspergillus Ag jest immunoenzymatycznym mikropłytkowym testem typu kanapkowego do wykrywania antygenu galaktomannanowego grzyba Aspergillus w próbkach
PLATELIA ASPERGILLUS Ag 96 TESTÓW 62794 Test Platelia Aspergillus Ag jest immunoenzymatycznym mikropłytkowym testem typu kanapkowego do wykrywania antygenu galaktomannanowego grzyba Aspergillus w próbkach
ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01
![ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01 ACCESS Immunoassay System. HIV combo QC4 & QC5. Do monitorowania wydajności testu Access HIV combo. B71116A - [PL] - 2015/01](/thumbs/25/4516998.jpg) ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Do monitorowania wydajności testu Access HIV combo. - [PL] - 2015/01 Spis treści Access HIV combo QC4 & QC5 1 Przeznaczenie... 3 2 Podsumowanie i objaśnienie
ACCESS Immunoassay System HIV combo QC4 & QC5 B22822 Do monitorowania wydajności testu Access HIV combo. - [PL] - 2015/01 Spis treści Access HIV combo QC4 & QC5 1 Przeznaczenie... 3 2 Podsumowanie i objaśnienie
PASTOREX TOXO WYKRYWANIE PRZECIWCIAŁ TOXOPLASMA GONDII W SUROWICY LUDZKIEJ POPRZEZ AGLUTYNACJĘ CZĄSTEK LATEKSU
 PASTOREX TOXO 72724 100 WYKRYWANIE PRZECIWCIAŁ TOXOPLASMA GONDII W SUROWICY LUDZKIEJ POPRZEZ AGLUTYNACJĘ CZĄSTEK LATEKSU 881157-2014/06 1- ZASTOSOWANIE Toxoplasma gondii jest pierwotniakiem zdolnym do
PASTOREX TOXO 72724 100 WYKRYWANIE PRZECIWCIAŁ TOXOPLASMA GONDII W SUROWICY LUDZKIEJ POPRZEZ AGLUTYNACJĘ CZĄSTEK LATEKSU 881157-2014/06 1- ZASTOSOWANIE Toxoplasma gondii jest pierwotniakiem zdolnym do
QUANTA Lite ENA Do diagnostyki in vitro Złożoność CLIA: Wysoka
 QUANTA Lite ENA 5 708610 Do diagnostyki in vitro Złożoność CLIA: Wysoka Przeznaczenie QUANTA Lite TM ENA 5 jest to immunoenzymatyczny test (ELISA) do półilościowego oznaczania przeciwciał przeciwko Sm,
QUANTA Lite ENA 5 708610 Do diagnostyki in vitro Złożoność CLIA: Wysoka Przeznaczenie QUANTA Lite TM ENA 5 jest to immunoenzymatyczny test (ELISA) do półilościowego oznaczania przeciwciał przeciwko Sm,
Zawiadomienie o zmianie treści specyfikacji istotnych warunków zamówienia
 nr sprawy: WIW.AD.I.271.16.2011 Siedlce, dn. 21 kwietnia 2011 r. Wykonawcy wszyscy Zawiadomienie o zmianie treści specyfikacji istotnych warunków zamówienia Zgodnie z art. 38 ust. 4 ustawy z dnia 29 stycznia
nr sprawy: WIW.AD.I.271.16.2011 Siedlce, dn. 21 kwietnia 2011 r. Wykonawcy wszyscy Zawiadomienie o zmianie treści specyfikacji istotnych warunków zamówienia Zgodnie z art. 38 ust. 4 ustawy z dnia 29 stycznia
QUANTA Lite ACA Screen III Do diagnostyki in vitro Złożoność CLIA: Wysoka
 QUANTA Lite ACA Screen III 708620 Do diagnostyki in vitro Złożoność CLIA: Wysoka Przeznaczenie QUANTA Lite TM ACA Screen III jest to immunoenzymatyczny test (ELISA) do półilościowego oznaczania przeciwciał
QUANTA Lite ACA Screen III 708620 Do diagnostyki in vitro Złożoność CLIA: Wysoka Przeznaczenie QUANTA Lite TM ACA Screen III jest to immunoenzymatyczny test (ELISA) do półilościowego oznaczania przeciwciał
Zestaw do wykrywania Anaplasma phagocytophilum w kleszczach, krwi i hodowlach komórkowych
 Nr kat. PK24N Wersja zestawu: 1.2016 Zestaw do wykrywania phagocytophilum w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Detekcja
Nr kat. PK24N Wersja zestawu: 1.2016 Zestaw do wykrywania phagocytophilum w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Detekcja
ALGALTOXKIT F Procedura testu
 ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE
 NARODOWY INSTYTUT ZDROWIA PUBLICZNEGO - PAŃSTWOWY ZAKŁAD HIGIENY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE ZAKŁAD WIRUSOLOGII NIZP-PZH UL. CHOCIMSKA 24 00-791 WARSZAWA
NARODOWY INSTYTUT ZDROWIA PUBLICZNEGO - PAŃSTWOWY ZAKŁAD HIGIENY ELIMINACJA ODRY/RÓŻYCZKI PROGRAM WHO REALIZACJA W POLSCE ZASADY INSTRUKCJE ZAKŁAD WIRUSOLOGII NIZP-PZH UL. CHOCIMSKA 24 00-791 WARSZAWA
Borrelial lymphocytoma (BL)
 BORELIOZA z Lyme ROZPOZNANIE Podstawą rozpoznania jest stwierdzenie przynajmniej jednego z następujących objawów: Rumień wędrujący (rumień pełzający, erythema migrans EM) Rozpoznanie opiera się na obrazie
BORELIOZA z Lyme ROZPOZNANIE Podstawą rozpoznania jest stwierdzenie przynajmniej jednego z następujących objawów: Rumień wędrujący (rumień pełzający, erythema migrans EM) Rozpoznanie opiera się na obrazie
2- ZNACZENIE KLINICZNE
 PLATELIA TOXO IgA TMB 1 płytka - 96 72737 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgA PRZECIWKO TOXOPLASMA GONDII W W LUDZKIEJ SUROWICY LUB OSOCZU 881129-2014/06 1- ZASTOSOWANIE Test Platelia
PLATELIA TOXO IgA TMB 1 płytka - 96 72737 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA PRZECIWCIAŁ KLASY IgA PRZECIWKO TOXOPLASMA GONDII W W LUDZKIEJ SUROWICY LUB OSOCZU 881129-2014/06 1- ZASTOSOWANIE Test Platelia
E.coli Transformer Kit
 E.coli Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli. Metoda chemiczna. wersja 1117 6 x 40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników
E.coli Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli. Metoda chemiczna. wersja 1117 6 x 40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników
Genscreen HIV-1 Ag Assay 2 płytek
 Genscreen HIV-1 Ag Assay 2 płytek - 192 71120 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA ANTYGENU p24 WIRUSA HIV -1 W LUDZKIEJ SUROWICY, OSOCZU I SUPERNATANCIE HODOWLI KOMÓRKOWYCH 883669-2014/01 SPIS TREŚCI
Genscreen HIV-1 Ag Assay 2 płytek - 192 71120 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA ANTYGENU p24 WIRUSA HIV -1 W LUDZKIEJ SUROWICY, OSOCZU I SUPERNATANCIE HODOWLI KOMÓRKOWYCH 883669-2014/01 SPIS TREŚCI
QUANTA Lite RNP ELISA Do diagnostyki in vitro Złożoność CLIA: Wysoka
 QUANTA Lite RNP ELISA 708565 Do diagnostyki in vitro Złożoność CLIA: Wysoka Przeznaczenie Test QUANTA Lite TM RNP ELISA to test immunoenzymatyczny (ELISA) do półilościowego wykrywania przeciwciał przeciwko
QUANTA Lite RNP ELISA 708565 Do diagnostyki in vitro Złożoność CLIA: Wysoka Przeznaczenie Test QUANTA Lite TM RNP ELISA to test immunoenzymatyczny (ELISA) do półilościowego wykrywania przeciwciał przeciwko
2015/04 1- ZASTOSOWANIE
 Platelia EBV-VCA IgG 1 płytka - 96 72937 TEST IMMUNOENZYMATYCZNY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI EPSTEIN-BARR (PRZECIWKO ANTYGENOWI KAPSYDOWEMU) W SUROWICY LUDZKIEJ
Platelia EBV-VCA IgG 1 płytka - 96 72937 TEST IMMUNOENZYMATYCZNY DO JAKOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO WIRUSOWI EPSTEIN-BARR (PRZECIWKO ANTYGENOWI KAPSYDOWEMU) W SUROWICY LUDZKIEJ
TPHA
 TPHA 200 72503 500 72504 ZESTAWY DO JAKOŚCIOWEGO I PÓŁILOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ PRZECIWKO TREPONEMA PALLIDUM W SUROWICY LUB OSOCZU KRWI LUDZKIEJ ZA POMOCĄ HEMOGLUTYNACJI BIERNEJ 883683-2014/12
TPHA 200 72503 500 72504 ZESTAWY DO JAKOŚCIOWEGO I PÓŁILOŚCIOWEGO WYKRYWANIA PRZECIWCIAŁ PRZECIWKO TREPONEMA PALLIDUM W SUROWICY LUB OSOCZU KRWI LUDZKIEJ ZA POMOCĄ HEMOGLUTYNACJI BIERNEJ 883683-2014/12
Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności
 Załącznik nr 4 Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności 1. Zakres i obszar stosowania Metoda służy do urzędowej kontroli zawartości chlorku winylu uwalnianego
Załącznik nr 4 Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności 1. Zakres i obszar stosowania Metoda służy do urzędowej kontroli zawartości chlorku winylu uwalnianego
Zestaw do oczyszczania DNA po reakcjach enzymatycznych
 Cat. No. EM07.1 Wersja: 1.2017 NOWA WERSJA Zestaw do oczyszczania DNA po reakcjach enzymatycznych EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM07.1 I. PRZEZNACZENIE
Cat. No. EM07.1 Wersja: 1.2017 NOWA WERSJA Zestaw do oczyszczania DNA po reakcjach enzymatycznych EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM07.1 I. PRZEZNACZENIE
Monolisa Anti-HCV PLUS Version 3 1 płytka płytek
 Monolisa Anti-HCV PLUS Version 3 1 płytka - 96 72340 5 płytek - 480 72341 TEST PRZESIEWOWY DO WYKRYWANIA PRZECIWCIAŁ ANTY-HCV (PRZECIWKO WIRUSOWI ZAPALENIA WĄTROBY TYPU C) W OSOCZU LUB SUROWICY LUDZKIEJ
Monolisa Anti-HCV PLUS Version 3 1 płytka - 96 72340 5 płytek - 480 72341 TEST PRZESIEWOWY DO WYKRYWANIA PRZECIWCIAŁ ANTY-HCV (PRZECIWKO WIRUSOWI ZAPALENIA WĄTROBY TYPU C) W OSOCZU LUB SUROWICY LUDZKIEJ
BADANIE PŁYNU MÓZGOWO-RDZENIOWEGO
 BADANIE PŁYNU MÓZGOWO-RDZENIOWEGO 1. Pobranie płynu mózgowo-rdzeniowego (PMR) Podstawowym sposobem uzyskania próbki do badania płynu mózgowo rdzeniowego jest punkcja lędźwiowa. Nakłucie lędźwiowe przeprowadza
BADANIE PŁYNU MÓZGOWO-RDZENIOWEGO 1. Pobranie płynu mózgowo-rdzeniowego (PMR) Podstawowym sposobem uzyskania próbki do badania płynu mózgowo rdzeniowego jest punkcja lędźwiowa. Nakłucie lędźwiowe przeprowadza
TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA I ILOŚCIOWEGO OZNACZANIA PRZECIWCIAŁ KLASY
 PLATELIA TOXO IgG TMB 96 TESTÓW 72741 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA I ILOŚCIOWEGO OZNACZANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO TOXOPLASMA GONDII W LUDZKIEJ SUROWICY LUB OSOCZU Do diagnostyki in vitro
PLATELIA TOXO IgG TMB 96 TESTÓW 72741 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA I ILOŚCIOWEGO OZNACZANIA PRZECIWCIAŁ KLASY IgG PRZECIWKO TOXOPLASMA GONDII W LUDZKIEJ SUROWICY LUB OSOCZU Do diagnostyki in vitro
Zestaw przeznaczony jest do całkowitej izolacji RNA z bakterii, drożdży, hodowli komórkowych, tkanek oraz krwi świeżej (nie mrożonej).
 Total RNA Mini Plus Zestaw do izolacji całkowitego RNA. Procedura izolacji nie wymaga użycia chloroformu wersja 0517 25 izolacji, 100 izolacji Nr kat. 036-25, 036-100 Zestaw przeznaczony jest do całkowitej
Total RNA Mini Plus Zestaw do izolacji całkowitego RNA. Procedura izolacji nie wymaga użycia chloroformu wersja 0517 25 izolacji, 100 izolacji Nr kat. 036-25, 036-100 Zestaw przeznaczony jest do całkowitej
Spis treści. Wstęp faktów o boreliozie, które powinieneś znać Najbardziej charakterystyczne objawów boreliozy... 8
 Spis treści 01 Wstęp........................................................ 3 02 10 faktów o boreliozie, które powinieneś znać.................. 5 03 Najbardziej charakterystyczne objawów boreliozy.............
Spis treści 01 Wstęp........................................................ 3 02 10 faktów o boreliozie, które powinieneś znać.................. 5 03 Najbardziej charakterystyczne objawów boreliozy.............
INSTYTUT HEMATOLOGII I TRANSFUZJOLOGII
 ZAKŁAD HEMOSTAZY I CHORÓB METABOLICZNYCH PRACOWNIA PORFIRII 00-957 Warszawa, ul. Chocimska 5 tel. 22 34 96 617/635 INSTRUKCJA POBIERANIA I TRANSPORTU MATERIAŁU DO BADAŃ LABORATORYJNYCH W KIERUNKU PORFIRII
ZAKŁAD HEMOSTAZY I CHORÓB METABOLICZNYCH PRACOWNIA PORFIRII 00-957 Warszawa, ul. Chocimska 5 tel. 22 34 96 617/635 INSTRUKCJA POBIERANIA I TRANSPORTU MATERIAŁU DO BADAŃ LABORATORYJNYCH W KIERUNKU PORFIRII
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2019 CZĘŚĆ PRAKTYCZNA. Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu
 Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2019 Nazwa kwalifikacji: Wykonywanie badań analitycznych Oznaczenie kwalifikacji: A.60 Numer zadania: 01
Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2019 Nazwa kwalifikacji: Wykonywanie badań analitycznych Oznaczenie kwalifikacji: A.60 Numer zadania: 01
QUANTA Lite Do diagnostyki in vitro Złożoność CLIA: Wysoka. C1q CIC ELISA 704620
 QUANTA Lite Do diagnostyki in vitro Złożoność CLIA: Wysoka C1q CIC ELISA 704620 Przeznaczenie To badanie jest przeznaczone do pomiaru in-vitro krążących kompleksów odpornościowych (CIC), które wiążą C1q
QUANTA Lite Do diagnostyki in vitro Złożoność CLIA: Wysoka C1q CIC ELISA 704620 Przeznaczenie To badanie jest przeznaczone do pomiaru in-vitro krążących kompleksów odpornościowych (CIC), które wiążą C1q
Środki ostrożności uwagi
 QUANTA Lite Do diagnostyki in vitro Złożoność CLIA: Wysoka dsdna SC ELISA 704650 Przeznaczenie Test ten jest przeznaczony do pomiaru in vitro ilości swoistych autoprzeciwciał IgG przeciwko dwuniciowemu
QUANTA Lite Do diagnostyki in vitro Złożoność CLIA: Wysoka dsdna SC ELISA 704650 Przeznaczenie Test ten jest przeznaczony do pomiaru in vitro ilości swoistych autoprzeciwciał IgG przeciwko dwuniciowemu
EGZAMIN POTWIERDZAJĄCY KWALIFIKACJE W ZAWODZIE Rok 2019 CZĘŚĆ PRAKTYCZNA
 Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Wykonywanie badań analitycznych Oznaczenie kwalifikacji: A.60 Numer zadania: 01
Arkusz zawiera informacje prawnie chronione do momentu rozpoczęcia egzaminu Układ graficzny CKE 2018 Nazwa kwalifikacji: Wykonywanie badań analitycznych Oznaczenie kwalifikacji: A.60 Numer zadania: 01
AGZ OPIS PRZEDMIOTU ZAMÓWIENIA Część I- Wskaźniki biologiczne do kontroli procesu sterylizacji. Załącznik 1A do siwz.
 AGZ.272205 Część I- Wskaźniki biologiczne do kontroli procesu sterylizacji Załącznik A do siwz L.p. Przedmiot zamówienia. Sporal A - wskaźnik biologiczny Sporal A - wskaźnik biologiczny Sporal S - wskaźnik
AGZ.272205 Część I- Wskaźniki biologiczne do kontroli procesu sterylizacji Załącznik A do siwz L.p. Przedmiot zamówienia. Sporal A - wskaźnik biologiczny Sporal A - wskaźnik biologiczny Sporal S - wskaźnik
SNAP* BVD. Bovine Virus Diarrhea Antigen Test Kit. Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD)
 SNAP* BVD Bovine Virus Diarrhea Antigen Test Kit Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD) 06-20814-01 Bovine Virus Diarrhea Antigen Test Kit
SNAP* BVD Bovine Virus Diarrhea Antigen Test Kit Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD) 06-20814-01 Bovine Virus Diarrhea Antigen Test Kit
10) istotne kliniczne dane pacjenta, w szczególności: rozpoznanie, występujące czynniki ryzyka zakażenia, w tym wcześniejsza antybiotykoterapia,
 Załącznik nr 2 Standardy jakości w zakresie mikrobiologicznych badań laboratoryjnych, w tym badań technikami biologii molekularnej, oceny ich jakości i wartości diagnostycznej oraz laboratoryjnej interpretacji
Załącznik nr 2 Standardy jakości w zakresie mikrobiologicznych badań laboratoryjnych, w tym badań technikami biologii molekularnej, oceny ich jakości i wartości diagnostycznej oraz laboratoryjnej interpretacji
PLATELIA Aspergillus IgG 1 płytka
 PLATELIA Aspergillus IgG 1 płytka 96 62783 WYKRYWANIE PRZECIWCIAŁ KLASY IgG PRZECIWKO ASPERGILLUS W SUROWICY LUB OSOCZU KRWI LUDZKIEJ METODĄ IMMUNOENZYMATYCZNĄ 881123 2013/11 1- ZASTOSOWANIE Platelia Aspergillus
PLATELIA Aspergillus IgG 1 płytka 96 62783 WYKRYWANIE PRZECIWCIAŁ KLASY IgG PRZECIWKO ASPERGILLUS W SUROWICY LUB OSOCZU KRWI LUDZKIEJ METODĄ IMMUNOENZYMATYCZNĄ 881123 2013/11 1- ZASTOSOWANIE Platelia Aspergillus
PLATELIA CANDIDA Ag 96 TESTÓW 62798 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA ANTYGENU MANNANOWEGO CANDIDA W SUROWICY
 PLATELIA CANDIDA Ag 96 TESTÓW 62798 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA ANTYGENU MANNANOWEGO CANDIDA W SUROWICY 1 1- PRZEZNACZENIE TESTU Platelia Candida Ag jest mikropłytkowym, kanapkowym testem immunoenzymatycznym
PLATELIA CANDIDA Ag 96 TESTÓW 62798 TEST IMMUNOENZYMATYCZNY DO WYKRYWANIA ANTYGENU MANNANOWEGO CANDIDA W SUROWICY 1 1- PRZEZNACZENIE TESTU Platelia Candida Ag jest mikropłytkowym, kanapkowym testem immunoenzymatycznym
NA ZAKAŻENIE HBV i HCV
 NA ZAKAŻENIE HBV i HCV Wojewódzka Stacja Sanitarno-Epidemiologiczna w Gdańsku 18.04.2016r. Aneta Bardoń-Błaszkowska HBV - Hepatitis B Virus Simplified diagram of the structure of hepatitis B virus, Autor
NA ZAKAŻENIE HBV i HCV Wojewódzka Stacja Sanitarno-Epidemiologiczna w Gdańsku 18.04.2016r. Aneta Bardoń-Błaszkowska HBV - Hepatitis B Virus Simplified diagram of the structure of hepatitis B virus, Autor
AmpliTest Chlamydia/Chlamydophila (Real Time PCR)
 AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
Inne choroby zakaźne w środowisku
 Inne choroby zakaźne w środowisku dzieci i młodzieży - zapobieganie Dr n. med. Ewa Duszczyk 05.12.2017 r. O czym będziemy mówić o Wirusowym zapaleniu wątroby typu A Płonicy Chorobie bostońskiej Kleszczowym
Inne choroby zakaźne w środowisku dzieci i młodzieży - zapobieganie Dr n. med. Ewa Duszczyk 05.12.2017 r. O czym będziemy mówić o Wirusowym zapaleniu wątroby typu A Płonicy Chorobie bostońskiej Kleszczowym
