Rozdział 6 Atomy wieloelektronowe
|
|
|
- Arkadiusz Sobczyk
- 8 lat temu
- Przeglądów:
Transkrypt
1 Rozdział 6 Atomy wieloelektronowe 6.1: Atomy a struktura układu okresowego 6.2: Zakaz Pauliego 6.3: Wypełnianie powłok elektronami 6.4: Układ okresowy 6.5: Całkowity moment pędu 6.6: Oddziaływanie spin-orbita 6.7: Reguły Hunda Dimitri Mendelejew Co wyróżniało Mendelejewa było nie tylko geniuszem ale również pasją do pierwiastków, które stały się jego osobistymi przyjaciółmi; wiedział o nich wszystko, znał każdy najmniejszy detal ich budowy. - J. Bronowski Przygotowanie Marek Szopa, na podstawie Rick Trebino, Georgia Tech,
2 6.1: Atomy a struktura układu okresowego Co się dzieje kiedy mamy więcej niż jeden elektron? Hel: jądro o ładunku +2e i dwa elektrony, elektrony odpychania się wzajemnie. Nie można rozwiązać problemu dokładnie z równania Schrödingera z powodu złożoności energii potencjalnej. Jednak da się zrozumieć wyniki eksperymentów bez obliczania funkcji falowych wielu elektronów, stosując jedynie odpowiednie warunki brzegowe i reguły wyboru.
3 Atomy wieloelektronowe Kiedy atom ma więcej niż jeden elektron, energia potencjalna i funkcja falowa są funkcjami położenia każdego elektronu: (,,..., ) V = V r1 r2 r N Ψ = Ψ( r, r,..., r, t) 1 2 Rozwiązanie równania Schrödingera jest w tym przypadku niemożliwe. Ale możemy poszukiwać przybliżonego rozwiązania jako iloczynu jednocząstkowych funkcji falowych: Ψ ( r, r,..., r, t) = Ψ ( r, t) Ψ ( r, t) Ψ ( r, t) 1 2 N N N N Okazuje się, że można przybliżyć każde, korzystając z funkcji falowej atomu wodoru.
4 6.2: Zakaz Pauliego Aby wyjaśnić atomowe dane spektroskopowe, Pauli zaproponował swój słynny zakaz: Żadne dwa elektrony w atomie nie mogą mieć takiego samego zestawu liczb kwantowych (n, l, m l, m s ). Zakaz dotyczy wszystkich cząstek o spinie połówkowym, które nazywamy fermionami. Cząstki w jądrze są również fermionami. Okresowy układ pierwiastków może być zrozumiany przy założeniu Zakazu Pauliego oraz zasady: Elektrony w atomie obsadzają najniższe dostępne poziomy energii.
5 Struktura atomowa Wodór: (n, l, m l, m s ) = (1, 0, 0, ±½) w stanie podstawowym. Jeśli nie ma zewnętrznego pola magnetycznego, stany m s = ½ oraz m s = ½ są zdegenerowane. Hel: (1, 0, 0, ½) dla pierwszego elektronu. (1, 0, 0, ½) dla drugiego elektronu. Elektrony mają przeciwne (m s = +½ i m s = ½) spiny. Główna liczba kwantowa jest również oznaczana literowo. n = Litera = K L M N powłoki n = (np.: powłoka K, L itd.) podpowłoki nl = (np.: 1s, 2p, 3d) Elektrony w atomach wodoru i helu są na powłoce K. H: 1s He: 1s 2
6 Struktura atomowa Ile elektronów może liczyć dana podpowłoka? Dla każdej liczby m l, są dwie wartości m s. Dla każdejl: jest (2l + 1) wartości m l Tak więc mamy 2(2l + 1) elektronów na podpowłoce. Przypomnijmy: l = litera = s p d f g h l = 0, (stan s) może mieć dwa elektrony. l = 1, (stan p) może mieć sześć elektronów itd. Dla niższych wartościl orbity elektronowe są bardziej eliptyczne niż dla wyższych wartości l. Elektrony o wyższej wartościl są bardziej ekranowane od ładunku jądrowego. Elektrony o wyższej wartościl mają wyższą energię od elektronów o niższym l. Podpowłoka 4s jest wypełniana przed 3d.
7 Konfiguracja elektronowa Listę obsadzeń stanów danego atomu nazywamy jego konfiguracją elektronową. n Indeks górny oznacza ilość elektronów obsadzających podpowłokę. Wodór: 1s Hel: 1s 2 Liczba elektronów l Lit: 1s 2 2s Fluor: 1s 2 2s 2 2p 5 itd.
8 6.3: Wypełnianie powłok Reguła Kleczkowskiego regularność ta jest zaburzona w niektórych przypadkach w wyniku tzw. promocji elektronowej (m.in. chrom, molibden, srebro, miedź oraz niektóre lantanowce i aktynowce)
9 Wypełnianie powłok 7s
10 Zamknięta powłoka Grupy: Metale Metale alkaliczne ziem alkalicznych Układ okresowy Halogeny Gazy szlachetne Metale przejściowe Lantanowce Aktynowce
11 Gr. Ia Układ okresowy pierwiastków Gr. VIIIa H 1 1,008 Chemiczny symbol pierwiastka Wodór 1s 1 Gr. IIa Mn 25 Liczba atomowa Gr. IIIa Gr. IVa Gr. Va Gr. VIa Gr. VIIa Li 3 4 6,94 Lit Beryl [He]2s 1 [He]2s 2 Na 11 22,99 Sód [Ne]3s 1 Mg 12 24,31 9,01 54,94 Masa atomowa B 5 10,81 Mangan Nazwa pierwiastka Bor [He]2s 2 p 1 [Ar]3d 5 Konfiguracja elektronowa Al 13 26,98 Magnez [Ne]3s 2 Gr. IIIb Gr. IVb Gr. Vb Gr. VIb Gr. VIIb Gr. VIIIb Gr. Ib Gr. IIb K 19 Ca 20 39,10 40,08 Potas [Ar]4s 1 Rb 37 85,47 Wapń [Ar] Sr 38 87,62 Sc 21 44,96 Skand [Ar]3d 1 Y 39 88,91 Rubid [Kr]5s 1 Stront [Kr]5s 2 Itr [Kr]4d 1 5s 2 Cs ,9 137,3 138,9 Cez Bar Lantan [Xe]6s 1 [Xe]6s 2 [Xe]5d 1 Fr 87 Ra 88 Ac 89 (223) 226,0 (227) Frans [Rn]7s 1 Rad [Rn] Ti 22 47,87 Tytan [Ar]3d 2 Zr 40 91,22 Cyrkon [Kr]4d 2 5s 2 V 23 50,94 Wanad [Ar]3d 3 Cr 24 52,00 Chrom [Ar]3d 5 4s 1 Mn 25 54,94 Mangan [Ar]3d 5 Nb ,91 95,94 Niob Molibden Technet [Kr]4d 4 [Kr]4d 5 [Kr]4d 5 5s 1 5s 1 5s 2 Hf 72 Ta 73 W ,5 180,9 Fe 26 55,85 Żelazo [Ar]3d 6 Co 27 58,93 Kobalt [Ar]3d 7 Ni 28 58,69 Nikiel [Ar]3d 8 Cu 29 63,55 Miedź 4s 1 Zn 30 65,39 Cynk Glin [Ne]3s 2 p 1 Ga 31 69,72 Gal p 1 C 6 12,01 Węgiel [He]2s 2 p 2 Si 14 28,09 N 7 14,01 Azot [He]2s 2 p 3 P 15 30,97 Krzem Fosfor [Ne]3s 2 p 2 [Ne]3s 2 p 3 Ge 32 As 33 72,61 74,92 German p 2 Arsen p 3 O 8 16,00 Tlen [He]2s 2 p 4 S 16 32,07 Siarka [Ne]3s 2 p 4 Se 34 78,96 Selen p 4 F 9 19,00 Fluor [He]2s 2 p 5 Cl 17 35,45 Chlor [Ne]3s 2 p 5 Br 35 79,90 Brom p 5 He 2 4,00 Hel 1s 2 Ne 10 20,18 Neon [He]2s 2 p 6 Ar 18 39,95 Argon [Ne]3s 2 p 6 Kr 36 83,80 Krypton p 6 Ru (98) 101,1 102,9 106,4 107,9 112,4 114,8 118,7 121,8 127,6 126,9 131,3 Ruten Rod Pallad Srebro Kadm Ind Cyna Antymon Tellur Jod Ksenon [Kr]4d 7 [Kr]4d 8 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 5s 1 5s 1 5s 1 5s 2 5s 2 p 1 5s 2 p 2 5s 2 p 3 5s 2 p 4 5s 2 p 5 5s 2 p 6 Os At ,2 190,2 192,2 195,1 197,0 200,6 204,4 207,2 209,0 (209) (210) (222) Re ,8 6s 2 5d 2 6s 2 5d 3 6s 2 5d 4 6s 2 5d 5 6s 2 5d 6 6s 2 5d 7 6s 2 5d 9 6s 1 5d 10 6s 1 5d 10 6s 2 5d 10 6s 2 p 1 5d 10 6s 2 p 2 5d 10 6s 2 p 3 5d 10 6s 2 p 4 5d 10 6s 2 p 5 5d 10 6s 2 p 6 * Hafn Tantal Wolfram Ren Osm Iryd Platyna Złoto Rtęć Tal Ołów Bizmut Polon Astat Radon [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 Rf (258) (262) (266) (264) (267) (268) (271) (272) (277) Masy atomowe podane względem wzorca 12 C = 12. Aktyn * Ruterford Dubn Siborg Borium Hass Maitner W nawiasach masy atomowe najtrwalszego izotopu. [Rn]6d 1 Niektóre pierwiastki, szczególnie te o liczbie atomowej > 95 * [Rn]5f 14 6 d 2 są otrzymywane tylko w sposób sztuczny. Ce ,1 * Lantanowce Cer [Xe]4f 1 * Aktynowce * Pr ,9 Nd ,2 Pm 61 Sm 62 Eu 63 Gd 64 Tb 65 Dy 66 Ho 67 Er 68 Tm 69 Yb 70 Lu 71 (145) 150,4 152,0 157,3 158,9 162,5 164,9 167,3 168,9 144,2 175,0 Prazeodym Neodym Promet Samar Europ Gadolin Terb Dysproz Holm Erb Tul Iterb Lutet [Xe]4f 3 5d 1 6s 2 6s 2 [Xe]4f 4 [Xe]4f 5 [Xe]4f 6 [Xe]4f 7 [Xe]4f 7 [Xe]4f 9 [Xe]4 f 10 [Xe]4f 11 [Xe]4f 12 [Xe]4f 13 [Xe]4f 14 [Xe]4f 14 6s 2 6s 2 6s 2 6s 2 5d 1 6s 2 6s 2 6s 2 6s 2 6s 2 6s 2 6s 2 5d 1 6s 2 Th 90 Pa 91 U 92 Np 93 Pu 94 Am 95 Cm 96 Bk 97 Cf 98 Es 99 Fm 100 Md 101 No 102 Lr ,0 231,0 238,0 (237) (244) (243) (247) (247) (251) (252) (257) (258) (259) (262) Tor [Rn]6d 2 Protaktyn [Rn]5f 2 6d 1 Uran [Rn]5f 3 6d 1 Neptun [Rn]5f 4 6d 1 6.4: Układ okresowy Pluton [Rn]5f 6 Ameryk [Rn]5f 7 Kiur [Rn]5f 7 6d 1 Berkel [Rn]5f 9 Kaliforn [Rn]5f 10 Einstein [Rn]5f 11 Ferm [Rn]5f 12 Mendelew [Rn]5f 13 Nobel [Rn]5f 14 Lorens [Rn]5f 14 6d 1
12 Gr. Ia Układ okresowy pierwiastków Gr. VIIIa H 1 1,008 Chemiczny symbol pierwiastka Wodór 1s 1 Gr. IIa Mn 25 Liczba atomowa Gr. IIIa Gr. IVa Gr. Va Gr. VIa Gr. VIIa Li 3 4 6,94 Lit Beryl [He]2s 1 [He]2s 2 Na 11 22,99 Sód [Ne]3s 1 Mg 12 24,31 9,01 54,94 Masa atomowa B 5 10,81 Mangan Nazwa pierwiastka Bor [He]2s 2 p 1 [Ar]3d 5 Konfiguracja elektronowa Al 13 26,98 Magnez [Ne]3s 2 Gr. IIIb Gr. IVb Gr. Vb Gr. VIb Gr. VIIb Gr. VIIIb Gr. Ib Gr. IIb K 19 Ca 20 39,10 40,08 Potas [Ar]4s 1 Rb 37 85,47 Wapń [Ar] Sr 38 87,62 Sc 21 44,96 Skand [Ar]3d 1 Y 39 88,91 Rubid [Kr]5s 1 Stront [Kr]5s 2 Itr [Kr]4d 1 5s 2 Cs ,9 137,3 138,9 Cez Bar Lantan [Xe]6s 1 [Xe]6s 2 [Xe]5d 1 Fr 87 Ra 88 Ac 89 (223) 226,0 (227) Frans [Rn]7s 1 Rad [Rn] Ti 22 47,87 Tytan [Ar]3d 2 Zr 40 91,22 Cyrkon [Kr]4d 2 5s 2 V 23 50,94 Wanad [Ar]3d 3 Cr 24 52,00 Chrom [Ar]3d 5 4s 1 Mn 25 54,94 Mangan [Ar]3d 5 Nb ,91 95,94 Niob Molibden Technet [Kr]4d 4 [Kr]4d 5 [Kr]4d 5 5s 1 5s 1 5s 2 Hf 72 Ta 73 W ,5 180,9 Fe 26 55,85 Żelazo [Ar]3d 6 Co 27 58,93 Kobalt [Ar]3d 7 Ni 28 58,69 Nikiel [Ar]3d 8 Cu 29 63,55 Miedź 4s 1 Zn 30 65,39 Cynk Glin [Ne]3s 2 p 1 Ga 31 69,72 Gal p 1 C 6 12,01 Węgiel [He]2s 2 p 2 Si 14 28,09 N 7 14,01 Azot [He]2s 2 p 3 P 15 30,97 Krzem Fosfor [Ne]3s 2 p 2 [Ne]3s 2 p 3 Ge 32 As 33 72,61 74,92 German p 2 Arsen p 3 O 8 16,00 Tlen [He]2s 2 p 4 S 16 32,07 Siarka [Ne]3s 2 p 4 Se 34 78,96 Selen p 4 F 9 19,00 Fluor [He]2s 2 p 5 Cl 17 35,45 Chlor [Ne]3s 2 p 5 Br 35 79,90 Brom p 5 He 2 4,00 Hel 1s 2 Ne 10 20,18 Neon [He]2s 2 p 6 Ar 18 39,95 Argon [Ne]3s 2 p 6 Kr 36 83,80 Krypton p 6 Ru (98) 101,1 102,9 106,4 107,9 112,4 114,8 118,7 121,8 127,6 126,9 131,3 Ruten Rod Pallad Srebro Kadm Ind Cyna Antymon Tellur Jod Ksenon [Kr]4d 7 [Kr]4d 8 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 [Kr]4d 10 5s 1 5s 1 5s 1 5s 2 5s 2 p 1 5s 2 p 2 5s 2 p 3 5s 2 p 4 5s 2 p 5 5s 2 p 6 Os At ,2 190,2 192,2 195,1 197,0 200,6 204,4 207,2 209,0 (209) (210) (222) Re ,8 6s 2 5d 2 6s 2 5d 3 6s 2 5d 4 6s 2 5d 5 6s 2 5d 6 6s 2 5d 7 6s 2 5d 9 6s 1 5d 10 6s 1 5d 10 6s 2 5d 10 6s 2 p 1 5d 10 6s 2 p 2 5d 10 6s 2 p 3 5d 10 6s 2 p 4 5d 10 6s 2 p 5 5d 10 6s 2 p 6 * Hafn Tantal Wolfram Ren Osm Iryd Platyna Złoto Rtęć Tal Ołów Bizmut Polon Astat Radon [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 [Xe]4f 14 Rf (258) (262) (266) (264) (267) (268) (271) (272) (277) Masy atomowe podane względem wzorca 12 C = 12. Aktyn * Ruterford Dubn Siborg Borium Hass Maitner W nawiasach masy atomowe najtrwalszego izotopu. [Rn]6d 1 Niektóre pierwiastki, szczególnie te o liczbie atomowej > 95 * [Rn]5f 14 6 d 2 są otrzymywane tylko w sposób sztuczny. Ce ,1 * Lantanowce Cer [Xe]4f 1 * Aktynowce * Pr ,9 Nd ,2 Pm 61 Sm 62 Eu 63 Gd 64 Tb 65 Dy 66 Ho 67 Er 68 Tm 69 Yb 70 Lu 71 (145) 150,4 152,0 157,3 158,9 162,5 164,9 167,3 168,9 144,2 175,0 Prazeodym Neodym Promet Samar Europ Gadolin Terb Dysproz Holm Erb Tul Iterb Lutet [Xe]4f 3 5d 1 6s 2 6s 2 [Xe]4f 4 [Xe]4f 5 [Xe]4f 6 [Xe]4f 7 [Xe]4f 7 [Xe]4f 9 [Xe]4 f 10 [Xe]4f 11 [Xe]4f 12 [Xe]4f 13 [Xe]4f 14 [Xe]4f 14 6s 2 6s 2 6s 2 6s 2 5d 1 6s 2 6s 2 6s 2 6s 2 6s 2 6s 2 6s 2 5d 1 6s 2 Th 90 Pa 91 U 92 Np 93 Pu 94 Am 95 Cm 96 Bk 97 Cf 98 Es 99 Fm 100 Md 101 No 102 Lr ,0 231,0 238,0 (237) (244) (243) (247) (247) (251) (252) (257) (258) (259) (262) Tor [Rn]6d 2 Protaktyn [Rn]5f 2 6d 1 Uran [Rn]5f 3 6d 1 Neptun [Rn]5f 4 6d 1 Promocja elektronowa Pluton [Rn]5f 6 Ameryk [Rn]5f 7 Kiur [Rn]5f 7 6d 1 Berkel [Rn]5f 9 Kaliforn [Rn]5f 10 Einstein [Rn]5f 11 Ferm [Rn]5f 12 Mendelew [Rn]5f 13 Nobel [Rn]5f 14 Lorens [Rn]5f 14 6d 1
13 Grupy i okresy Grupy: Pionowe kolumny. Taka sama liczba elektronów na orbicie l. Tworzą podobne wiązania chemiczne. Okresy: Rzędy poziome. Odpowiadają wypełnianiu podpowłok. Energia jonizacji (ev) Promień atomowy (nm) Liczba atomowa (Z) Liczba atomowa (Z)
14 Układ okresowy Gazy szlachetne (8 grupa): Ostatnia grupa układu okresowego Zamknięta podpowłoka p (za wyjątkiem helu) Zerowy spin wypadkowy i duża energia jonizacji Atomy słabo oddziałują z sobą Metale alkaliczne (1 grupa): Pojedynczy elektron s na zewnątrz zamkniętej powłoki Łatwo je zjonizować, wtedy mają ładunek +1e Najniższa energia jonizacji Największy promień atomowy Stosunkowo dobra przewodność elektryczna Metale ziem alkalicznych (grupa 2a): Dwa elektrony s na zewnątrz zamkniętej powłoki Wysoka przewodność elektryczna
15 Układ okresowy Halogeny (grupa 7a): Potrzeba jednego elektronu aby uzupełnić zewnętrzną podpowłokę p Tworzą silne wiazania jonowe z matalami alkalicznymi Są stabilniejsze jeśli podpowłoka p jest wypełniona Metale przejściowe: Trzy okresy (rzędy) pierwiastków na których są wypełniane powłoki 3d, 4d, i 5d Własności w większym stopniu zależne od elektronów s niż od zapełnianej podpowłoki d Elektrony podpowłoki d mają niesparowany spin W miarę wypełniania podpowłoki d, momenty magnetyczne i tendencja sąsiednich atomów do równoległego ustawiania spinów zmniejsza się
16 Układ okresowy Lantanowce (ziemie rzadkie): Mają całkowicie obsadzoną zewnętrzną podpowłokę 6s 2 Podobnie, jak w przypadku podpowłoki 3d, elektrony na podpowłoce 4f są niesparowane i ustawiają się spinami równolegle do siebie Duży orbitalny moment pędu dodaje się do dużego efektu ferromagnetycznego. Aktynowce: W pełni obsadzona podpowłoka wewnętrzne podpowłoki są kolejno wypełniane Są radioaktywne i trudno zbadać ich własności chemiczne
17 6.5: Całkowity moment pędu Orbitalny moment pędu Spinowy moment pędu Całkowity moment pędu J = L + S L, L z, S, S z, J, i J z są skwantowane.
18 Całkowity moment pędu Niech j i m j będą liczbami kwantowymi całkowitego momentu pędu dla atomu wodoru: J = j( j + 1) ħ J z = m j ħ Ale skwantowane są wszystkie wielkości: L S J = = = l( l + 1) ħ s( s + 1) ħ j( j + 1) ħ Liczba kwantowa całkowitego momentu pędu pojedynczego elektronu może przyjmować jedynie następujące wartości: j =l ± s
19 6.6: Oddziaływanie Spin-Orbita Sprzężenie spinu elektronu i jego orbitalnego momentu pędu nazywa się oddziaływaniem spin-orbita. Energia potencjalna dipola l =. Spinowy moment magnetyczny B wewn. jest polem magnetycznym wynikającym z orbitalnego ruchu elektronu. L V ~ S L = SL cosα sl gdzie α jest kątem pomiędzy
20 Całkowity moment pędu Reguły wyboru dla jednoelektronowego atomu mają postać n = dowolne l = ±1 m j = 0, ±1 j = 0, ±1 Diagram poziomów dla wodoru dla n = 2 i n = 3 ze sprzężeniem spin-orbita Energia Atom Niezaburzony Struktura subtelna
21 6.7: Reguły Hunda 1. Całkowity spinowy moment pędu S powinien być możliwie maksymalny, ale zgodny z zakazem Pauliego. Przykład: tlen o konfiguracji elektronowej 1s 2 2s 2 2p 4 2. O ile zasada 1 nie jest naruszona, L powinien także być zmaksymalizowany. 3. Dla atomów mających podpowłoki zapełnione mniej niż w połowie, J powinien być zminimalizowany, jeśli w ponad połowie J powinien być zmaksymalizowany Dla atomów dwuelektronowych Moment pędu J jest wynikiem sprzężenia LS i sprzężenia JJ J = L 1 + L2 + S1 + S2
22
23
24
Pierwiastek: Na - Sód Stan skupienia: stały Liczba atomowa: 11
 ***Dane Pierwiastków Chemicznych*** - Układ Okresowy Pierwiastków 2.5.1.FREE Pierwiastek: H - Wodór Liczba atomowa: 1 Masa atomowa: 1.00794 Elektroujemność: 2.1 Gęstość: [g/cm sześcienny]: 0.0899 Temperatura
***Dane Pierwiastków Chemicznych*** - Układ Okresowy Pierwiastków 2.5.1.FREE Pierwiastek: H - Wodór Liczba atomowa: 1 Masa atomowa: 1.00794 Elektroujemność: 2.1 Gęstość: [g/cm sześcienny]: 0.0899 Temperatura
Grupa b. Zadania na ocen celujàcà
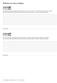 Zadania na ocen celujàcà Grupa a Do reakcji syntezy siarczku glinu przygotowano g glinu i, g siarki. Czy substraty przereagowały w całoêci? JeÊli nie przereagowały, podaj nazw substratu, który nie przereagował
Zadania na ocen celujàcà Grupa a Do reakcji syntezy siarczku glinu przygotowano g glinu i, g siarki. Czy substraty przereagowały w całoêci? JeÊli nie przereagowały, podaj nazw substratu, który nie przereagował
Drogi Uczniu, Przed tobą test złożony z 20 zadań. Czytaj wszystko bardzo uważnie i udziel prawidłowej odpowiedzi w załączonej karcie odpowiedzi.
 B... pieczątka nagłówkowa WKK............... kod pracy ucznia (wpisuje uczeń) KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP WOJEWÓDZKI Drogi Uczniu, Przed tobą test złożony z 20 zadań. Czytaj
B... pieczątka nagłówkowa WKK............... kod pracy ucznia (wpisuje uczeń) KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP WOJEWÓDZKI Drogi Uczniu, Przed tobą test złożony z 20 zadań. Czytaj
a b zasi g kilku centymetrów zasi g kilkudziesi ciu centymetrów zasi g nieograniczony ATOM jàdro atomowe neutrony protony nukleony pow oki elektronowe
 ZAWARTOÂå SK ADNIKA W ROZTWORZE nasyconym i nienasyconym ATOM (najmniejsza czàstka pierwiastka chemicznego) st enie procentowe 2% jàdro atomowe g wody ms = 2 g 00 g roztworu nasyconym protony neutrony
ZAWARTOÂå SK ADNIKA W ROZTWORZE nasyconym i nienasyconym ATOM (najmniejsza czàstka pierwiastka chemicznego) st enie procentowe 2% jàdro atomowe g wody ms = 2 g 00 g roztworu nasyconym protony neutrony
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 ... pieczątka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
... pieczątka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
1/8. KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 6 listopada 2010 roku
 1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 6 listopada 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP II REJONOWY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 6 listopada 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP II REJONOWY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
PIERWIASTKI W UKŁADZIE OKRESOWYM
 PIERWIASTKI W UKŁADZIE OKRESOWYM 1 Układ okresowy Co można odczytać z układu okresowego? - konfigurację elektronową - podział na bloki - podział na grupy i okresy - podział na metale i niemetale - trendy
PIERWIASTKI W UKŁADZIE OKRESOWYM 1 Układ okresowy Co można odczytać z układu okresowego? - konfigurację elektronową - podział na bloki - podział na grupy i okresy - podział na metale i niemetale - trendy
Liczby kwantowe elektronu w atomie wodoru
 Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Badania laboratoryjne składu chemicznego wód podziemnych
 Katowice 27.11.2015r. Odpowiedź na list Towarzystwa na rzecz Ziemi W związku ze zgłaszanymi przez Towarzystwo na rzecz Ziemi (pismo z dnia 05.11.2015r.) pytaniami dotyczącymi pierwiastków występujących
Katowice 27.11.2015r. Odpowiedź na list Towarzystwa na rzecz Ziemi W związku ze zgłaszanymi przez Towarzystwo na rzecz Ziemi (pismo z dnia 05.11.2015r.) pytaniami dotyczącymi pierwiastków występujących
ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050
 ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa ul. Szczotkarska 42 Wydanie nr 7, Data wydania: 14 lipca 2015 r. Nazwa i adres AB 1050 AKADEMIA
ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa ul. Szczotkarska 42 Wydanie nr 7, Data wydania: 14 lipca 2015 r. Nazwa i adres AB 1050 AKADEMIA
Struktura elektronowa
 Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
1/9. zadanie razem Maksymalna liczba punktów
 podpis nauczyciela 1/9 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 08 stycznia 2011 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP III WOJEWÓDZKI KOD UCZNIA:.. zadanie 1 2 4 5 razem Maksymalna
podpis nauczyciela 1/9 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 08 stycznia 2011 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP III WOJEWÓDZKI KOD UCZNIA:.. zadanie 1 2 4 5 razem Maksymalna
1/8. KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 4 października 2010 roku
 1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 4 października 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP I SZKOLNY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 4 października 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP I SZKOLNY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 ... piecztka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uwanie instrukcj i
... piecztka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uwanie instrukcj i
II.3 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy
 II.3 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy 1. Atom helu: struktura poziomów, reguły wyboru, 2. Zakaz Pauliego, 3. Moment pędu w atomach wieloelektronowych: sprzężenie LS i
II.3 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy 1. Atom helu: struktura poziomów, reguły wyboru, 2. Zakaz Pauliego, 3. Moment pędu w atomach wieloelektronowych: sprzężenie LS i
KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 Kod ucznia Kod szkoły... pieczątka WKK Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP WOJEWÓDZKI Drogi Uczniu, witaj na II etapie konkursu chemicznego.
Kod ucznia Kod szkoły... pieczątka WKK Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP WOJEWÓDZKI Drogi Uczniu, witaj na II etapie konkursu chemicznego.
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
III.1 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy
 III.1 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy r. akad. 2004/2005 1. Atom helu: struktura poziomów, reguły wyboru, 2. Zakaz Pauliego, 3. Moment pędu w atomach wieloelektronowych:
III.1 Atom helu i zakaz Pauliego. Atomy wieloelektronowe. Układ okresowy r. akad. 2004/2005 1. Atom helu: struktura poziomów, reguły wyboru, 2. Zakaz Pauliego, 3. Moment pędu w atomach wieloelektronowych:
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Nowa Tablica Układu Okresowego Pierwiastków Chemicznych
 Strona 1 z 5 Nowa Tablica Układu Okresowego Pierwiastków Chemicznych Tablica Klasyczna D. Mendelejew Układ Okresowy a budowa atomu NOWA TABLICA 1-168 zgłoś uwagi str. główna Nowy układ okresowy pierwiastków
Strona 1 z 5 Nowa Tablica Układu Okresowego Pierwiastków Chemicznych Tablica Klasyczna D. Mendelejew Układ Okresowy a budowa atomu NOWA TABLICA 1-168 zgłoś uwagi str. główna Nowy układ okresowy pierwiastków
DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY
 KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY 11 października 2012 Ważne informacje: 1. Masz 60 minut na rozwiązanie wszystkich 20 zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY 11 października 2012 Ważne informacje: 1. Masz 60 minut na rozwiązanie wszystkich 20 zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050
 ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa ul. Szczotkarska 42 Wydanie nr 11 Data wydania: 27 maja 2019 r. Nazwa i adres AB 1050 AKADEMIA
ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa ul. Szczotkarska 42 Wydanie nr 11 Data wydania: 27 maja 2019 r. Nazwa i adres AB 1050 AKADEMIA
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
KONKURS CHEMICZNY DLA UCZNIÓW SZKÓŁ GIMNAZJALNYCH ETAP SZKOLNY
 ... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW SZKÓŁ GIMNAZJALNYCH ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW SZKÓŁ GIMNAZJALNYCH ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Wykład 16: Atomy wieloelektronowe
 Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 16: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Układ okresowy pierwiastków. Myślenie bez intuicji jest puste, intuicja bez myślenia jest ślepa. Albert Einstein
 Układ okresowy pierwiastków Myślenie bez intuicji jest puste, intuicja bez myślenia jest ślepa. Albert Einstein Spis treści Ważne pojęcia Trochę historii O ilu pierwiastkach wiemy Wygląd współczesnego
Układ okresowy pierwiastków Myślenie bez intuicji jest puste, intuicja bez myślenia jest ślepa. Albert Einstein Spis treści Ważne pojęcia Trochę historii O ilu pierwiastkach wiemy Wygląd współczesnego
Chemia Ogólna wykład 1
 Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Poziomy energetyczne powłok i podpowłok elektronowych pierwiastków
 Jeżeli zostało dowiedzione, że własności pierwiastków zależą od wartości liczby atomowej Z, to w kolejnym pytaniu możemy zapytać się w jaki sposób konfiguracja elektronowa pierwiastków decyduje o położeniu
Jeżeli zostało dowiedzione, że własności pierwiastków zależą od wartości liczby atomowej Z, to w kolejnym pytaniu możemy zapytać się w jaki sposób konfiguracja elektronowa pierwiastków decyduje o położeniu
CHEMIA WARTA POZNANIA
 Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Atom wodoru w mechanice kwantowej. Równanie Schrödingera
 Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Fizyka atomowa Atom wodoru w mechanice kwantowej Moment pędu Funkcje falowe atomu wodoru Spin Liczby kwantowe Poprawki do równania Schrödingera: struktura subtelna i nadsubtelna; przesunięcie Lamba Zakaz
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 2015-12-25 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
26 Okresowy układ pierwiastków
 26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
Podstawowe obliczenia w chemii analitycznej
 Podstawowe obliczenia w chemii analitycznej GBC Rodzinnie Zakopane 2012 Jacek Sowiński GBC Polska js@gbcpolska.pl www.gbcpolska.pl Podstawowe parametry obliczane dla wykonywanych analiz Stężenie charakterystyczne
Podstawowe obliczenia w chemii analitycznej GBC Rodzinnie Zakopane 2012 Jacek Sowiński GBC Polska js@gbcpolska.pl www.gbcpolska.pl Podstawowe parametry obliczane dla wykonywanych analiz Stężenie charakterystyczne
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Wykaz ważniejszych symboli agadnienia ogólne Wstęp Zarys historii chemii analitycznej
 Spis rzeczy Z Wykaz ważniejszych symboli............................. 13 1. agadnienia ogólne................................. 15 1.1. Wstęp..................................... 15 1.. Zarys historii chemii
Spis rzeczy Z Wykaz ważniejszych symboli............................. 13 1. agadnienia ogólne................................. 15 1.1. Wstęp..................................... 15 1.. Zarys historii chemii
I. Budowa atomu i model atomu wg. Bohra. 1. Atom - najmniejsza część pierwiastka zachowująca jego właściwości. Jądro atomowe - protony i neutrony
 Materiał powtórzeniowy do sprawdzianów - konfiguracja elektronowa, elektrony walencyjne, współczesny układ pierwiastków chemicznych, przykładowe zadania z rozwiązaniami. I. Budowa atomu i model atomu wg.
Materiał powtórzeniowy do sprawdzianów - konfiguracja elektronowa, elektrony walencyjne, współczesny układ pierwiastków chemicznych, przykładowe zadania z rozwiązaniami. I. Budowa atomu i model atomu wg.
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY
 suma uzyskanych punktów...... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie
suma uzyskanych punktów...... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie
KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY. 09 października 2013
 KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY 09 października 2013 Ważne informacje: 1. Masz 60 minut na rozwiązanie wszystkich zadań. 2. Zapisuj szczegółowe obliczenia i komentarze
KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY 09 października 2013 Ważne informacje: 1. Masz 60 minut na rozwiązanie wszystkich zadań. 2. Zapisuj szczegółowe obliczenia i komentarze
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
INŻYNIERIA BIOMEDYCZNA. Wykład X
 INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
INŻYNIERIA BIOMEDYCZNA Wykład X 16.12.2017 1 Mechanika kwantowa opiera się na dwóch prawach Dualizm korpuskularno-falowy (de Broglie a) λ h p Zasada nieoznaczoności Heisenberga p x h/(4 ) Gęstość prawdopodobieństwa
Anna Grych Test z budowy atomu i wiązań chemicznych
 Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Opracowała: mgr Agata Wiśniewska PRZYKŁADOWE SPRAWDZIANY WIADOMOŚCI l UMIEJĘTNOŚCI Współczesny model budowy atomu (wersja A)
 PRZYKŁADOW SPRAWDZIANY WIADOMOŚCI l UMIJĘTNOŚCI Współczesny model budowy atomu (wersja A) 1. nuklid A. Zbiór atomów o tej samej wartości liczby atomowej. B. Nazwa elektrycznie obojętnej cząstki składowej
PRZYKŁADOW SPRAWDZIANY WIADOMOŚCI l UMIJĘTNOŚCI Współczesny model budowy atomu (wersja A) 1. nuklid A. Zbiór atomów o tej samej wartości liczby atomowej. B. Nazwa elektrycznie obojętnej cząstki składowej
PRÓBNY EGZAMIN MATURALNY Z CHEMII
 (wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO PRÓBNY EGZAMIN MATURALNY Z CHEMII Arkusz I Poziom podstawowy Instrukcja dla zdającego: Czas pracy 120 minut 1. Proszę sprawdzić, czy arkusz zawiera
(wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO PRÓBNY EGZAMIN MATURALNY Z CHEMII Arkusz I Poziom podstawowy Instrukcja dla zdającego: Czas pracy 120 minut 1. Proszę sprawdzić, czy arkusz zawiera
Własności magnetyczne materii
 Własności magnetyczne materii Dipole magnetyczne Najprostszą strukturą magnetyczną są magnetyczne dipole. Fe 3 O 4 Kompas, Chiny 220 p.n.e Kołowy obwód z prądem dipol magnetyczny! Wartość B w środku kołowego
Własności magnetyczne materii Dipole magnetyczne Najprostszą strukturą magnetyczną są magnetyczne dipole. Fe 3 O 4 Kompas, Chiny 220 p.n.e Kołowy obwód z prądem dipol magnetyczny! Wartość B w środku kołowego
CZY POTRZEBNA NAM ENERGETYKA JĄDROWA?
 Kształtowanie kompetencji kluczowych w nauczaniu biologii CZY POTRZEBNA NAM ENERGETYKA JĄDROWA? Danuta Wojcieszyńska, Urszula Guzik Katedra Biochemii Uniwersytet Śląski KAPITAŁ LUDZKI NARODOWA STRATEGIA
Kształtowanie kompetencji kluczowych w nauczaniu biologii CZY POTRZEBNA NAM ENERGETYKA JĄDROWA? Danuta Wojcieszyńska, Urszula Guzik Katedra Biochemii Uniwersytet Śląski KAPITAŁ LUDZKI NARODOWA STRATEGIA
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków).
 Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
Właściwości chemiczne i fizyczne pierwiastków powtarzają się w pewnym cyklu (zebrane w grupy 2, 8, 8, 18, 18, 32 pierwiastków). 1925r. postulat Pauliego: Na jednej orbicie może znajdować się nie więcej
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Temat 1: Budowa atomu zadania
 Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
PRÓBNY EGZAMIN MATURALNY Z CHEMII
 POUFNE do dnia... godz.... KOD ZDAJĄCEGO IMIĘ NAZWISKO WPISUJE PISZĄCY PO OTRZYMANIU PRACY - - WPISAĆ PO ROZKODOWANIU PRACY ARKUSZ II PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 120 minut Informacje 1.
POUFNE do dnia... godz.... KOD ZDAJĄCEGO IMIĘ NAZWISKO WPISUJE PISZĄCY PO OTRZYMANIU PRACY - - WPISAĆ PO ROZKODOWANIU PRACY ARKUSZ II PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 120 minut Informacje 1.
Chemia ogólna nieorganiczna wykład 1 - poziom podstawowy
 W1P UKŁAD OKRESOWY PIERWIASTKÓW 1 2 3 4 1 (IA) 1,01 1 6,94 3 23,00 11 39,10 19 4 12 20 2 (IIA) 9,01 24,31 40,08 3 (IIIB) 4 (IVB) 5 (VB) 6 (VIB) 7 (VIIB) 8 (VIIIB) 9 (VIIIB) 10 (VIIIB) 11 (IB) 12 (IIB)
W1P UKŁAD OKRESOWY PIERWIASTKÓW 1 2 3 4 1 (IA) 1,01 1 6,94 3 23,00 11 39,10 19 4 12 20 2 (IIA) 9,01 24,31 40,08 3 (IIIB) 4 (IVB) 5 (VB) 6 (VIB) 7 (VIIB) 8 (VIIIB) 9 (VIIIB) 10 (VIIIB) 11 (IB) 12 (IIB)
Układ okresowy pierwiastków
 strona 1/8 Układ okresowy pierwiastków Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Teoria atomistyczno-cząsteczkowa, nieciągłość budowy materii. Układ okresowy pierwiastków
strona 1/8 Układ okresowy pierwiastków Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Teoria atomistyczno-cząsteczkowa, nieciągłość budowy materii. Układ okresowy pierwiastków
Wykład 9 Wprowadzenie do krystalochemii
 Wykład 9 Wprowadzenie do krystalochemii 1. Krystalografia a krystalochemia. 2. Prawa krystalochemii 3. Sieć krystaliczna i pozycje atomów 4. Bliskie i dalekie uporządkowanie. 5. Kryształ a cząsteczka.
Wykład 9 Wprowadzenie do krystalochemii 1. Krystalografia a krystalochemia. 2. Prawa krystalochemii 3. Sieć krystaliczna i pozycje atomów 4. Bliskie i dalekie uporządkowanie. 5. Kryształ a cząsteczka.
Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
Wykład 3: Atomy wieloelektronowe
 Wykład 3: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Wykład 3: Atomy wieloelektronowe Funkcje falowe Kolejność zapełniania orbitali Energia elektronów Konfiguracja elektronowa Reguła Hunda i zakaz Pauliego Efektywna liczba atomowa Reguły Slatera Wydział
Widmo sodu, serie. p główna s- ostra d rozmyta f -podstawowa
 Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
Widmo sodu, serie p główna s- ostra d rozmyta f -podstawowa Przejścia dozwolone w Na Reguły wyboru: l =± 1 Diagram Grotriana dla sodu, z lewej strony poziomy energetyczne wodoru; należy zwrócić uwagę,
PRAWO OKRESOWOŚCI. 1.131. Liczba co najmniej częściowo obsadzonych powłok elektronowych decyduje o przynależności pierwiastka
 PRAWO OKRESOWOŚCI 1.125. D. Mendelejew sformułował swoje prawo w następujący sposób: Właściwości fizyczne i chemiczne pierwiastków zmieniają się okresowo w zależności od A) liczby protonów w jądrze atomowym.
PRAWO OKRESOWOŚCI 1.125. D. Mendelejew sformułował swoje prawo w następujący sposób: Właściwości fizyczne i chemiczne pierwiastków zmieniają się okresowo w zależności od A) liczby protonów w jądrze atomowym.
ARKUSZ PRÓBNEJ MATURY Z OPERONEM FIZYKA
 Miejsce na identyfikację szkoły ARKUSZ PRÓBNEJ MATURY Z OPERONEM FIZYKA POZIOM ROZSZERZONY LISTOPAD 2014 Instrukcja dla zdającego Czas pracy: 180 minut 1. Sprawdź, czy arkusz egzaminacyjny zawiera 20 stron
Miejsce na identyfikację szkoły ARKUSZ PRÓBNEJ MATURY Z OPERONEM FIZYKA POZIOM ROZSZERZONY LISTOPAD 2014 Instrukcja dla zdającego Czas pracy: 180 minut 1. Sprawdź, czy arkusz egzaminacyjny zawiera 20 stron
Układ okresowy Przewidywania teorii kwantowej
 Przewiywania teorii kwantowej Chemia kwantowa - oumowanie Czątka w ule Atom wooru Równanie Schroeingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - oumowanie rozwiązanie Czątka w ule Atom wooru Ψn
Przewiywania teorii kwantowej Chemia kwantowa - oumowanie Czątka w ule Atom wooru Równanie Schroeingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - oumowanie rozwiązanie Czątka w ule Atom wooru Ψn
Spis treœci Wstêp Od epoki br¹zu do in ynierii materia³owej Przedmowa Rozdzia³ 1 Budowa atomowa metali Rozdzia³ 2 Krzepniêcie metali
 5 Spis treœci Wstêp Od epoki br¹zu do in ynierii materia³owej Adolf Maciejny... 17 Przedmowa Znaczenie metali w rozwoju cywilizacji... 31 Rozdzia³ 1 Budowa atomowa metali Karol Przyby³owicz... 37 1.1.
5 Spis treœci Wstêp Od epoki br¹zu do in ynierii materia³owej Adolf Maciejny... 17 Przedmowa Znaczenie metali w rozwoju cywilizacji... 31 Rozdzia³ 1 Budowa atomowa metali Karol Przyby³owicz... 37 1.1.
Fizyka 3.3 WYKŁAD II
 Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Fizyka 3.3 WYKŁAD II Promieniowanie elektromagnetyczne Dualizm korpuskularno-falowy światła Fala elektromagnetyczna Strumień fotonów o energii E F : E F = hc λ c = 3 10 8 m/s h = 6. 63 10 34 J s Światło
Źródła światła w AAS. Seminarium Analityczne MS Spektrum Zakopane Jacek Sowiński MS Spektrum
 Źródła światła w AAS Seminarium Analityczne MS Spektrum Zakopane 2013 Jacek Sowiński MS Spektrum js@msspektrum.pl www.msspektrum.pl Lampy HCL Standardowa Super-Lampa 3V 10V specyf. Lampy HCL 1,5 cala
Źródła światła w AAS Seminarium Analityczne MS Spektrum Zakopane 2013 Jacek Sowiński MS Spektrum js@msspektrum.pl www.msspektrum.pl Lampy HCL Standardowa Super-Lampa 3V 10V specyf. Lampy HCL 1,5 cala
Budowa atomu. Izotopy
 Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
b) Pierwiastek E tworzy tlenek o wzorze EO 2 i wodorek typu EH 4, a elektrony w jego atomie rozmieszczone są na dwóch powłokach elektronowych
 1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
KONKURS Z CHEMII DLA UCZNIÓW SZKOŁY PODSTAWOWEJ
 pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS Z CHEMII DLA UCZNIÓW SZKOŁY PODSTAWOWEJ ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie
pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS Z CHEMII DLA UCZNIÓW SZKOŁY PODSTAWOWEJ ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie
Szanowni Państwo, Spis treści
 Szanowni Państwo, z przyjemnością przekazujemy Państwu broszurę, w której przedstawiamy w skrócie najważniejsze informacje dotyczące zmian w szkołach ponadpodstawowych, wynikających z przeprowadzanej reformy
Szanowni Państwo, z przyjemnością przekazujemy Państwu broszurę, w której przedstawiamy w skrócie najważniejsze informacje dotyczące zmian w szkołach ponadpodstawowych, wynikających z przeprowadzanej reformy
Stara i nowa teoria kwantowa
 Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
Stara i nowa teoria kwantowa Braki teorii Bohra: - podane jedynie położenia linii, brak natężeń -nie tłumaczy ilości elektronów na poszczególnych orbitach - model działa gorzej dla atomów z więcej niż
UKŁAD OKRESOWY PIERWIASTKÓW
 UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
Chemia nieorganiczna. Copyright 2000 by Harcourt, Inc. All rights reserved.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]
![3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u] 3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]](/thumbs/58/41892324.jpg) 1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Wewnętrzna budowa materii - zadania
 Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Chemia nieorganiczna. Pierwiastki. niemetale Be. 27 Co. 28 Ni. 26 Fe. 29 Cu. 45 Rh. 44 Ru. 47 Ag. 46 Pd. 78 Pt. 76 Os.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI
 KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI 18 stycznia 2013 Ważne informacje: 1. Masz 120 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI 18 stycznia 2013 Ważne informacje: 1. Masz 120 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
Wzory sumaryczne i strukturalne związków
 Wzory sumaryczne i strukturalne związków H S H 3 PO 4 SO CH 4 H SO 4 OHC H 5 NH Wzory sumaryczne i strukturalne związków H SO 4 CuSO 4 siarczanvi miedziii K SO 4 siarczanvi potasu Fe SO 4 3 siarczanvi
Wzory sumaryczne i strukturalne związków H S H 3 PO 4 SO CH 4 H SO 4 OHC H 5 NH Wzory sumaryczne i strukturalne związków H SO 4 CuSO 4 siarczanvi miedziii K SO 4 siarczanvi potasu Fe SO 4 3 siarczanvi
Konfiguracja elektronowa atomu
 Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
Konfiguracja elektronowa atomu ANALIZA CHEMICZNA BADANIE WŁAŚCIWOŚCI SUBSTANCJI KONTROLA I STEROWANIE PROCESAMI TECHNOLOGICZNYMI Właściwości pierwiastków - Układ okresowy Prawo okresowości Mendelejewa
Piotr Kosztołowicz. Powtórka przed maturą. Chemia. Zadania. Zakres rozszerzony
 Piotr Kosztołowicz Zakres rozszerzony Chemia Powtórka przed maturą Zadania 95 Spis treści Wstęp Rozdział 1. Budowa atomów Rozdział 2. Przemiany jądrowe Rozdział 3. Struktura elektronowa atomu Rozdział
Piotr Kosztołowicz Zakres rozszerzony Chemia Powtórka przed maturą Zadania 95 Spis treści Wstęp Rozdział 1. Budowa atomów Rozdział 2. Przemiany jądrowe Rozdział 3. Struktura elektronowa atomu Rozdział
DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI
 KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI 18 stycznia 2013 Ważne informacje: 1. Masz 120 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI 18 stycznia 2013 Ważne informacje: 1. Masz 120 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI
 KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI 18 stycznia 2013 Ważne informacje: 1. Masz 120 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW III ETAP WOJEWÓDZKI 18 stycznia 2013 Ważne informacje: 1. Masz 120 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
ANALITYKA W KONTROLI JAKOŚCI
 ANALITYKA W KONTROLI JAKOŚCI ANALIZA ŚLADÓW METODA ICP-OES Optyczna spektroskopia emisyjna ze wzbudzeniem w indukcyjnie sprzężonej plazmie WYKŁAD 4 Rodzaje widm i mechanizm ich powstania PODSTAWY SPEKTROSKOPII
ANALITYKA W KONTROLI JAKOŚCI ANALIZA ŚLADÓW METODA ICP-OES Optyczna spektroskopia emisyjna ze wzbudzeniem w indukcyjnie sprzężonej plazmie WYKŁAD 4 Rodzaje widm i mechanizm ich powstania PODSTAWY SPEKTROSKOPII
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu
 Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
Kryształy, półprzewodniki, nanotechnologie. Dr inż. KAROL STRZAŁKOWSKI Instytut Fizyki UMK w Toruniu skaroll@fizyka.umk.pl Plan ogólny Kryształy, półprzewodniki, nanotechnologie, czyli czym będziemy się
CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna. Model atomu Bohra
 CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna Model atomu Bohra SPIS TREŚCI: 1. Modele budowy atomu Thomsona, Rutherforda i Bohra 2. Budowa atomu 3. Liczba atomowa a liczba
CHEMIA LEKCJA 1. Budowa atomu, Izotopy Promieniotwórczość naturalna i sztuczna Model atomu Bohra SPIS TREŚCI: 1. Modele budowy atomu Thomsona, Rutherforda i Bohra 2. Budowa atomu 3. Liczba atomowa a liczba
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Atom wodoru i jony wodoropodobne
 Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Atom wodoru i jony wodoropodobne dr inż. Ireneusz Owczarek CMF PŁ ireneusz.owczarek@p.lodz.pl http://cmf.p.lodz.pl/iowczarek 2012/13 Spis treści Spis treści 1. Model Bohra atomu wodoru 2 1.1. Porządek
Atom wodoropodobny. Biegunowy układ współrzędnych. współrzędne w układzie. kartezjańskim. współrzędne w układzie. (x,y,z) biegunowym.
 Atom wodoropodobny z współrzędne w układzie kartezjańskim r sinθ cosφ x r cosθ φ θ r r sinθ (x,y,z) r sinθ sinφ Biegunowy układ współrzędnych y funkcja faowa współrzędne w układzie biegunowym ( ) r,θ,φ
Atom wodoropodobny z współrzędne w układzie kartezjańskim r sinθ cosφ x r cosθ φ θ r r sinθ (x,y,z) r sinθ sinφ Biegunowy układ współrzędnych y funkcja faowa współrzędne w układzie biegunowym ( ) r,θ,φ
1. JĄDROWA BUDOWA ATOMU. A1 - POZIOM PODSTAWOWY.
 . JĄDROWA BUDOWA ATOMU. A - POIOM PODSTAWOWY. Na początek - przeczytaj uważnie tekst i wykonaj zawarte pod nim polecenia.. Dwie reakcje jądrowe zachodzące w górnych warstwach atmosfery: N + n C + p N +
. JĄDROWA BUDOWA ATOMU. A - POIOM PODSTAWOWY. Na początek - przeczytaj uważnie tekst i wykonaj zawarte pod nim polecenia.. Dwie reakcje jądrowe zachodzące w górnych warstwach atmosfery: N + n C + p N +
Okresowość właściwości chemicznych pierwiastków. Układ okresowy pierwiastków. 1. Konfiguracje elektronowe pierwiastków
 Układ okresowy pierwiastków Okresowość właściwości chemicznych pierwiastków 1. Konfiguracje elektronowe pierwiastków. Konfiguracje a układ okresowy 3. Budowa układu okresowego 4. Historyczny rozwój układu
Układ okresowy pierwiastków Okresowość właściwości chemicznych pierwiastków 1. Konfiguracje elektronowe pierwiastków. Konfiguracje a układ okresowy 3. Budowa układu okresowego 4. Historyczny rozwój układu
Zasady obsadzania poziomów
 Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Zasady obsadzania poziomów Model atomu Bohra Model kwantowy atomu Fala stojąca Liczby kwantowe -główna liczba kwantowa (n = 1,2,3...) kwantuje energię elektronu (numer orbity) -poboczna liczba kwantowa
Lista badań prowadzonych w ramach zakresu elastycznego nr AB 550
 Lista badań prowadzonych w ramach zakresu elastycznego nr AB 550 ZESPÓŁ LABORATORIÓW ENERGOPOMIAR Sp. z o.o. Wydanie nr 2 Imię i nazwisko Podpis Data Weryfikował Damian Adrjan 27.04.2016 Zatwierdził Katarzyna
Lista badań prowadzonych w ramach zakresu elastycznego nr AB 550 ZESPÓŁ LABORATORIÓW ENERGOPOMIAR Sp. z o.o. Wydanie nr 2 Imię i nazwisko Podpis Data Weryfikował Damian Adrjan 27.04.2016 Zatwierdził Katarzyna
Wykład Atom o wielu elektronach Laser Rezonans magnetyczny
 Wykład 21. 12.2016 Atom o wielu elektronach Laser Rezonans magnetyczny Jeszcze o atomach Przypomnienie: liczby kwantowe elektronu w atomie wodoru, zakaz Pauliego, powłoki, podpowłoki, orbitale, Atomy wieloelektronowe
Wykład 21. 12.2016 Atom o wielu elektronach Laser Rezonans magnetyczny Jeszcze o atomach Przypomnienie: liczby kwantowe elektronu w atomie wodoru, zakaz Pauliego, powłoki, podpowłoki, orbitale, Atomy wieloelektronowe
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
