Szanowni Państwo, Spis treści
|
|
|
- Rafał Skrzypczak
- 6 lat temu
- Przeglądów:
Transkrypt
1
2 Szanowni Państwo, z przyjemnością przekazujemy Państwu broszurę, w której przedstawiamy w skrócie najważniejsze informacje dotyczące zmian w szkołach ponadpodstawowych, wynikających z przeprowadzanej reformy oświaty, wchodzącej w życie w tych szkołach we wrześniu 2019 r. Przedstawiamy tu również zapowiedź naszej oferty wydawniczej w związku z początkiem obowiązywania nowej podstawy programowej nauczania chemii w liceach i technikach. Zasadnicza zawartość tej broszury to prezentacja zapowiadanych podręczników do zakresu rozszerzonego. Przedstawia ona podział podręczników na trzy części, zawartość poszczególnych części (w postaci ramowych rozkładów materiału z proponowaną liczbą godzin na jego realizację), zastosowaną strukturę podręczników oraz przykładowe fragmenty, stanowiące zamkniętą zawartość treści lekcji o danym temacie. Po dopuszczeniu przez MEN pierwszej części podręcznika otrzymacie Państwo bezpłatne egzemplarze. Mamy nadzieję, że po zapoznaniu się z podręcznikami i oferowaną do nich obudową dydaktyczną, zdecydujecie się Państwo na skorzystanie z naszej oferty. Zespół Oficyny Edukacyjnej * Krzysztof Pazdro Spis treści Reforma oświaty od roku szkolnego 2019/ Ramowy plan nauczania chemii... 3 Zasadnicze zmiany w nowej podstawie programowej... 3 Nasza oferta dla uczniów i nauczycieli... 5 Ramowy rozkład materiału w częściach Struktura i zawartość podręcznika... 7 Przykładowe fragmenty podręcznika, część Dydaktyczna obudowa podręcznika Zbiór zadań. Zakres rozszerzony
3 Reforma oświaty od roku szkolnego 2019/2020 (zgodnie z ustawą Prawo oświatowe z dn. 14 grudnia 2016 r.) Od roku szkolnego 2019/2020 absolwenci szkół podstawowych będą mogli kontynuować naukę w: 4-letnich liceach ogólnokształcących ( nowa matura w roku 2023), 5-letnich technikach ( nowa matura w roku 2024), 3-letnich szkołach branżowych I stopnia. Uczniowie liceów i techników będą się uczyć zgodnie z nowymi ramowymi planami nauczania i według nowej podstawy programowej. Od początku roku szkolnego 2019/2020, równolegle z absolwentami szkół podstawowych, w tych samych obiektach naukę w pierwszych klasach liceów i techników rozpoczną ostatni absolwenci wygaszanych gimnazjów. Będą oni kończyć realizację obecnie obowiązującej podstawy programowej dla 3-letnich liceów i 4-letnich techników. Zatem w roku szkolnym 2019/2020, w pierwszych klasach wszystkich liceów i techników, nastąpi kumulacja dwóch roczników uczniów. Ostatnie egzaminy maturalne wg obecnej formuły ( stara matura) będą przeprowadzane, odpowiednio, w liceach w roku 2022, w technikach w roku Harmonogram wprowadzania nowego ustroju szkolnego w liceach i technikach Rok szkolny 2018/ / / / / /2024 I kl. II kl. III kl. IV kl. V kl. 8. kl. szk. podst. liceum liceum liceum lic. nowa matura nowa matura I kl. II kl. III kl. IV kl. III kl. gim. liceum liceum lic. stara matura stara matura II kl. III kl. IV kl. I kl. lic. i techn. liceum lic. stara matura stara matura III kl. IV kl. II kl. lic. i techn. lic. stara matura stara matura nowy ustrój szkolny stary ustrój szkolny 2
4 Ramowy plan nauczania chemii w liceach i technikach Zakres rozszerzony Na podstawie rozporządzenia MEN z dn. 28 marca 2017 r. Liczba godzin nauczania w zakresie rozszerzonym: w liceach i w technikach 10 godzin tygodniowo w całym okresie nauczania (łącznie minimum 300 godz.), przy czym dyrektorzy tych szkół, po konsultacjach z radą pedagogiczną, radą rodziców i samorządem uczniowskim podejmują decyzję, czy przedmiot ten będzie nauczany w danej szkole, w przypadku pozytywnej decyzji dyrektorzy ustalają, w których klasach (w liceum: z klas 1 4, w : z klas 1 5) i w jakim wymiarze godzin w danej klasie przedmiot ten będzie realizowany. Zasadnicze zmiany w nowej podstawie programowej kształcenia chemii w liceach i technikach (w porównaniu z podstawą obecnie obowiązującą) Na podstawie rozporządzenia MEN z dn. 30 stycznia 2018 r. Zakres rozszerzony Treści nauczania (wymagania szczegółowe) ujęto w dwudziestu dwóch działach. Obejmują one treści z zakresu: chemii ogólnej, chemii fizycznej, elektrochemii, chemii nieorganicznej i chemii organicznej oraz treści dotyczące ochrony środowiska. We wszystkich działach, tak samo brzmiących jak w zakresie podstawowym, ujęto treści z zakresu podstawowego oraz treści rozszerzające. Treści te obejmują łącznie wszystkie treści nauczania z obecnej podstawy programowej oraz treści dodatkowe, które w większości zebrano w nowych działach, w tym: cały dział IX. Elektrochemia. Ogniwa i elektroliza, cały dział XI. Zastosowania wybranych związków nieorganicznych, cały dział XXI. Chemia wokół nas, cały dział XXII. Elementy ochrony środowiska. 3
5 Pozostałe treści dodatkowe rozmieszczono w innych działach nowej p.p., np.: w dziale II kwantowo-mechaniczny model budowy atomu oraz interpretacja wartości liczb kwantowych, w dziale III tworzenie orbitali zhybrydyzowanych i ich wzajemne ułożenie w przestrzeni oraz przewidywanie budowy przestrzennej drobin metodą VSEPR, w dziale IV określanie rzędu reakcji, energia aktywacji, standardowa entalpia przemiany, prawo Hessa, w dziale VI iloczyn rozpuszczalności, prawo rozcieńczeń Ostwalda, w dziale VIII przewidywanie kierunku przebiegu reakcji redox na podstawie wartości potencjałów standardowych półogniw, w dziale XIII piroliza węgla kamiennego, nazwy i zastosowania produktów pirolizy, procesy krakingu i reformingu w przemyśle. 4
6 Nasza oferta dla uczniów i nauczycieli chemii: Trzyczęściowy podręcznik w zakresie rozszerzonym Na rok szkolny 2019/2020 Na lata szkolne (2024) 5
7 Chemia. Zakres rozszerzony Ramowy rozkład materiału w częściach 1 3 Część 1. Rozdział Liczba godzin 1. Atomy, izotopy i przemiany jądrowe Budowa atomu z elementami mechaniki kwantowej Wiązania chemiczne Budowa cząsteczek i jonów Stechiometria Roztwory Termochemia 9 8. Kinetyka i równowaga chemiczna 14 Razem: 98 Część 2. Rozdział Liczba godzin 1. Chemia roztworów wodnych Elektrochemia Związki nieorganiczne Właściwości pierwiastków grup głównych 16 i ich związków 5. Właściwości pierwiastków grup pobocznych i ich związków 14 Razem: 82 Część 3. Rozdział Liczba godzin 1. Chemia organiczna początek a teraźniejszość 4 2. Związki węgla z wodorem węglowodory Fluorowcopochodne węglowodorów 2 4. Hydroksylowe pochodne węglowodorów 9 5. Związki karbonylowe 7 6. Kwasy karboksylowe i ich pochodne Związki organiczne zawierające azot Cukry i ich pochodzenie Organiczne związki wielkocząsteczkowe Chemia na co dzień Chemia a środowisko naturalne 8 Razem: 120 Łącznie w całym cyklu: 300 godzin 6
8 Struktura i zawartość podręcznika Początek części 1. podręcznika to przypomnienie, w dużym skrócie, wiedzy i umiejętności, które powinien posiadać absolwent szkoły podstawowej. Każdy rozdział w poszczególnych częściach podręcznika dzieli się na paragrafy. Będą one osnową kolejnych lekcji, a ich tytuły mogą być tematami tych lekcji. Tekst główny każdego paragrafu (lekcji), zgodnie z potrzebą, jest uzupełniony i zilustrowany: opisami doświadczeń, tabelami, grafami, przykładami obliczeń, zdjęciami i rysunkami. Każdy paragraf kończy się wykazem Ważnych pojęć w nim przedstawionych (z krótkim opisem lub definicją) oraz kilkoma zadaniami w bloku Rozwiąż zadania. Po każdym rozdziale zamieszczony jest dwustronicowy sprawdzian Sprawdź, co umiesz... Ważne fragmenty tekstu głównego, takie jak istotne informacje i definicje są wyróżnione na zielonym tle, wzory i różne zależności na czerwonym, a prawa chemiczne i zasady na tle żółtym. Odmiany tego samego pierwiastka chemicznego o różnej liczbie neutronów w jądrze są nazywane izotopami. Średnią masę atomową pierwiastka oblicza się ze wzoru: A r = A 1 p 1 + A 2 p A n p n 100% gdzie: A r średnia masa atomowa pierwiastka [u], A 1, A 2, A n masy izotopowe (lub liczby masowe izotopów), p 1, p 2, p n procentowe zawartości izotopów. Przemiany jądrowe podlegają dwóm zasadom. Są to: Zasada zachowania liczby nukleonów, zgodnie z którą: łączna liczba nukleonów w substratach jest równa łącznej liczbie nukleonów w produktach. Zasada zachowania ładunku elektrycznego, zgodnie z którą: sumaryczny ładunek wszystkich jąder i cząstek przed przemianą jest równy sumarycznemu ładunkowi wszystkich produktów przemiany. 7
9 Przykłady obliczeń przedstawiają wzorcowe rozwiązania zadań lub problemów. Przykład 1. Oblicz średnią masę atomową boru, wiedząc, że pierwiastek ten występuje w przyrodzie w postaci mieszaniny dwóch izotopów: bor-10 stanowi 18,83% naturalnego boru, bor-11 stanowi 81,17% naturalnego boru. Wzór na średnią masę atomową, uwzględniający dwa izotopy boru, przyjmuje postać: A r = A 1 p 1 + A 2 p 2 100% Po podstawieniu danych do wzoru otrzymuje się: 10 18,83% ,17% A r = 100% Odpowiedź: Średnia masa atomowa boru wynosi 10,81 u. = 10,81 u Opisy doświadczeń przedstawiają, krok po kroku, kolejność czynności podczas wykonywania danego doświadczenia, i najczęściej są ilustrowane zdjęciem lub rysunkiem. Zamieszczone w opisie Obserwacje i Wnioski są dla uczniów wzorcem ich poprawnego formułowania. Umieszczony przy tytule danego doświadczenia znak oznacza, że może ono być przeprowadzone: U samodzielnie przez uczniów, N tylko przez nauczyciela. Doświadczenie 3.2. Badanie rozpuszczalności azotanu(v) potasu w różnych rozpuszczalnikach Do trzech kolb stożkowych lub probówek wsyp po ok. 2 g azotanu(v) potasu KNO 3 i do każdej wlej po kilka centymetrów sześciennych innej cieczy: KNO a) wody, 3(s) b) benzyny, c) tetrachlorometanu (czterochlorku węgla). Zawartości naczyń dokładnie wymieszaj i obserwuj rezultaty. Obserwacje: Azotan(V) potasu szybko rozpuścił się w wodzie, ale nie rozpuścił się w żadnym z pozostałych rozpuszczalników. Wnioski: woda benzyna tetrachlorometan Sól ta dobrze rozpuszcza się w wodzie, ale nie rozpuszcza się w rozpuszczalnikach organicznych. U 8
10 Zamieszczony przed końcem każdego paragrafu wykaz Ważnych pojęć, jest rodzajem jego podsumowania, systematyzującego i utrwalającego wiedzę uczniów. Ważne pojęcia: Konfiguracja powłokowa rozmieszczenie elektronów w powłokach. Konfigurację tę zapisuje się w postaci kolejnych liter alfabetu oznaczających powłoki (uporządkowane od najbliższej jądra do najdalszej) i prawych górnych indeksów określających liczbę elektronów w danej powłoce, np. 15 P: K2 L 8 M 5 Zadania na końcu każdego paragrafu pozwalają sprawdzić nabytą na lekcji wiedzę i kształtować rachunkowe umiejętności uczniów. Rozwiąż zadania (odpowiedzi nie umieszczaj w podręczniku!) 1. Zapisz konfigurację elektronową powłokową, podpowłokową i orbitalną atomów magnezu i chloru. 2. Zapisz konfigurację elektronową powłokową, podpowłokową i orbitalną atomu galu, a następnie przedstaw za pomocą czterech liczb kwantowych (n, l, m, m s ) stan kwantowy niesparowanego elektronu w atomie tego pierwiastka. Sprawdzian Sprawdź, co umiesz..., zamieszczony po każdym rozdziale, zawiera dziesięć różnorodnych, punktowanych zadań. Są to zadania podobne do zadań zamieszczanych w arkuszach maturalnych. Uczniowie będą więc mogli samodzielnie sprawdzić i ocenić swoją wiedzę oraz umiejętność jej stosowania. Do wszystkich zadań z poszczególnych sprawdzianów podano poprawne odpowiedzi! Sprawdź, co umiesz... (odpowiedzi nie umieszczaj w podręczniku!) Zadanie 1. (0-1p.) Antymon jest pierwiastkiem, który występuje w przyrodzie w postaci mieszaniny dwóch izotopów. Na trzy atomy izotopu o liczbie masowej A 1 = 121 przypadają dwa atomy izotopu o liczbie masowej A 2. Oblicz liczbę masową A 2 drugiego izotopu antymonu, wiedząc, że średnia masa atomowa pierwiastka wynosi 121,76 u. 9
11
12 Spis treści Wstęp Przypomnienie ze szkoły podstawowej Regulamin szkolnej pracowni chemicznej Zasady przeprowadzania doświadczeń chemicznych Podstawowe szkło i sprzęt laboratoryjny Rozdział 1. Atomy, izotopy i przemiany jądrowe 1.1. Składniki atomu 1.2. Izotopowy skład pierwiastka 1.3. Naturalne przemiany jądrowe 1.4. Czas połowicznego zaniku 1.5. Sztuczne przemiany jądrowe 1.6. Właściwości promieniowania jądrowego 1.7. Dozymetria promieniowania 1.8. Energetyka jądrowa Sprawdzian Sprawdź, co umiesz... Rozdział 2. Budowa atomu z elementami mechaniki kwantowej 2.1. Modele budowy atomu 2.2. Kwantowy model budowy atomu 2.3. Konfiguracja elektronowa atomu pierwiastka 2.4. Elektrony w atomie 2.5. Prawo okresowości pierwiastków Sprawdzian Sprawdź, co umiesz... Rozdział 3. Wiązania chemiczne 3.1. Rodzaje wiązań 3.2. Wiązanie jonowe 3.3. Wiązanie kowalencyjne 3.4. Wiązania koordynacyjne 3.5. Energia jonizacji i powinowactwo elektronowe 3.6. Oddziaływania międzycząsteczkowe 3.7. Właściwości substancji jonowych i kowalencyjnych 3.8. Wiązanie metaliczne Sprawdzian Sprawdź, co umiesz... Rozdział 4. Budowa cząsteczek i jonów 4.1. Wiązania σ i wiązania π 4.2. Metoda VSEPR 11
13 4.3. Inne zastosowania metody VSEPR 4.4. Hybrydyzacja orbitali atomowych Sprawdzian Sprawdź, co umiesz... Rozdział 5. Stechiometria 5.1. Skład ilościowy związku chemicznego 5.2. Mol jednostka liczności materii 5.3. Masa molowa 5.4. Objętość molowa gazów 5.5. Stechiometria reakcji chemicznej Sprawdzian Sprawdź, co umiesz... Rozdział 6. Roztwory 6.1. Rodzaje mieszanin 6.2. Koloidy 6.3. Rozpuszczanie substancji 6.4. Metody rozdzielania mieszanin 6.5. Sposoby wyrażania stężeń roztworów 6.6. Rozcieńczanie i zatężanie roztworów 6.7. Rozpuszczanie hydratów Sprawdzian Sprawdź, co umiesz... Rozdział 7. Termochemia 7.1. Efekt energetyczny reakcji chemicznej 7.2. Reakcje endotermiczne i egzotermiczne 7.3. Entalpia tworzenia i entalpia spalania Sprawdzian Sprawdź, co umiesz... Rozdział 8. Kinetyka i równowaga chemiczna 8.1. Szybkość reakcji chemicznej 8.2. Czynniki wpływające na szybkość reakcji 8.3. Kinetyczne teorie przebiegu reakcji 8.4. Kataliza 8.5. Prawo działania mas 8.6. Reguła przekory Sprawdzian Sprawdź, co umiesz... Skorowidz Odpowiedzi do zadań rachunkowych Odpowiedzi do Sprawdź, co umiesz... Tablice uzupełniające Zaznaczone w Spisie treści elementy są przedstawione jako przykładowe fragmenty Podręcznika. Część 1. 12
14 CHEMIA. Podręcznik... Część 1. Zakres rozszerzony 2.5. Prawo okresowości pierwiastków Na Ziemi występują 92 pierwiastki. Są wśród nich takie, które są do siebie bardzo podobne pod względem właściwości, jak i takie, które krańcowo się różnią. Istnieją pierwiastki niezwykle reaktywne, jak i chemicznie bierne. W tym pozornym chaosie istnieje ład, który został odkryty przez rosyjskiego chemika Dymitra Mendelejewa w 1869 r. Prawidłowość ta jest nazywana prawem okresowości i może być przedstawiona graficznie w postaci układu okresowego pierwiastków. Punktem wyjścia w pracach Mendelejewa było uporządkowanie pierwiastków według rosnących mas atomowych. W XIX wieku liczba atomowa nie była jeszcze znana i nie wiedziano również, jak zbudowany jest atom. Istota sukcesu Mendelejewa polegała na tym, że wykrył w tym szeregu okresowe zmiany właściwości pierwiastków. Zostały one zilustrowane strzałkami na poniższym schemacie: Li Be B C N O F Na Mg Al Si P S Cl K Ca Po odkryciu wielu pierwiastków, nieznanych Mendelejewowi, okazało się, że lepszym kryterium tworzenia szeregu jest wzrost liczby atomowej. W myśl prawa okresowości właściwości chemiczne i fizyczne pierwiastków chemicznych są funkcją okresową liczby atomowej. Sens prawa okresowości w wersji współczesnej pokazuje uporządkowany szereg, utworzony z pierwiastków ustawionych według wzrastającej liczby atomowej: Kolory przypisane symbolom pierwiastków mają znaczenie umowne. Każdy z nich określa zespół najważniejszych, charakterystycznych właściwości chemicznych, np. metaliczność, niemetaliczność, reaktywność czy wartościowość. Kolory przypisane symbolom powtarzają się cyklicznie, ale ze zmienną liczbą pierwiastków w cyklu. Wynika to z tego, że w niektórych cyklach pojawiają się pierwiastki o nowych, niewystępujących poprzednio właściwościach. 13
15 2. Budowa atomu z elementami mechaniki kwantowej Rys Krótka wersja tablicy Mendelejewa 20 Os Re W Ir Pt Au Np U Pu Rys Gęstość pierwiastków w funkcji liczby atomowej (gęstości gazów wyznaczone są po ich skropleniu w temperaturze wrzenia) gęstość [g/cm 3 ] B Ne Be C He F H Li N O 1 2 Mg AlSi S P Cl Na 3 Ni Co Cu Fe Cr Zn Mn V Ga As Ge Ti Se Ar Br Kr Sc Ca K 4 Zr Y Rb Ru Rh Pd Tc Mo Ag Nb Sr Cd In Sn Sb Te 5 okresy I Xe Cs La Ba Ta Hf Lu 6 Hg Tl Pb Bi Th Pa Ra Rn Am Cm liczba atomowa Ta W Re Os Rys Temperatura topnienia pierwiastka w funkcji liczby atomowej temperatura topnienia [ C] Nb Mo Ru B Hf 2000 V Tc Rh Cr Zr Th Pt Ti Fe Lu Si Co Sc Y Pd Ni Be Mn Cu U Am Au 1000 Ge Mg Ag La Ca As Sr Sb Te Ba Ce Yb Ac Ra Al Sn Tl Po Np Pu Zn Cd Pb Li Na S Se Bi K 0 F P Rb In I Cs Ga H N O Ne Cl Br Ar Kr Xe Rn He Hg liczba atomowa okresy Ir 14
16 CHEMIA. Podręcznik... Część 1. Zakres rozszerzony 6000 W Ta Re temperatura wrzenia [ C] B C 3000 Be 2000 Li 1000 F N 0 H O He 1 2 Al Si Mg Na P Cl Ne 3 S Ti V Co Sc Fe Ni Ge Cr Cu Ga K Ar Ca Mn 4 Se Zn As Br Nb Mo Tc Zr Kr Sr Rb Ru Rh Y Pd Ag Sn Sb 5 okresy In Te Cd I La Ce Ba Cs Xe 6 Hf Os Ir Pt Hg Au Pb Bi Tl Po At Rn Th Ac U Pu liczba atomowa 7 Rys Temperatura wrzenia pierwiastków w funkcji liczby atomowej Przewidywania dotyczące nieznanych pierwiastków Dzięki odkrytym prawidłowościom Mendelejew mógł ustalić, w których miejscach brak mu pierwiastka o spodziewanych właściwościach. Na przykład gal i german nie były znane w chwili odkrycia prawa okresowości. W szeregu pierwiastków ustawionych według wzrostu masy atomowej ich miejsca zajmowały arsen i selen, które z uwagi na swoje właściwości nie powinny być umieszczone w grupach 13. i 14. Podobnie kolejny brom wykazywał właściwości typowe dla grupy 17. a nie 15. Mendelejew umieścił arsen, selen i brom zgodnie z ich właściwościami, w grupach 15., 16. i 17., zostawiając puste miejsca w grupie 13. pod glinem i w grupie 14. pod krzemem. W wyniku szczegółowej analizy właściwości fizycznych i chemicznych pierwiastków, sąsiadujących z pustymi miejscami w obrębie grupy i w obrębie okresu, określił właściwości chemiczne i fizyczne tych hipotetycznych pierwiastków (tab. 2.1.). Pierwiastki te zostały odkryte w ciągu kolejnych 15 lat, a ich właściwości okazały się zdumiewająco zgodne z przewidywanymi Mendelejewa. Tabela 2.1.Właściwości galu i germanu przewidywane przez Mendelejewa i stwierdzone doświadczalnie po ich odkryciu Masa atomowa [u] Gęstość [g cm 3 ] Gal odkryty w 1875 r. German odkryty w 1886 r. Przewidywania dotyczące nieznanego pierwiastka Właściwości ustalone po odkryciu pierwiastka Przewidywania dotyczące nieznanego pierwiastka Właściwości ustalone po odkryciu pierwiastka 68 69, ,32 6 5,96 5,5 5,47 15
17 2. Budowa atomu z elementami mechaniki kwantowej Temperatura topnienia [ C] Najwyższa wartościowość niska 30 wysoka 958 III III IV IV Wzór tlenku E 2 O 3 Ga 2 O 3 EO 2 GeO 2 Właściwości łatwo się redukuje się biały biały tlenku redukuje wodorem Wzór chlorku ECl 3 GaCl 3 ECl 4 GeCl 4 1 H 1 WODÓR HEL 1 (1868) Li Be Na symbol pierwiastka liczba atomowa B C N O F 2 LIT BERYL (liczba porządkowa) SÓD nazwa BOR WĘGIEL AZOT TLEN FLUOR NEON 2 (1810) rok odkrycia 1808 ST ST-znany w starożytności Na Mg ŚR-odkryty w średniowieczu Al Si P S Cl 3 SÓD MAGNEZ GLIN KRZEM FOSFOR SIARKA CHLOR ARGON ST K 4 POTAS WAPŃ SKAND TYTAN WANAD CHROM MANGAN ŻELAZO KOBALT NIKIEL MIEDŹ CYNK GAL GERMAN ARSEN SELEN BROM KRYPTON ST ST ŚR ŚR Rb 5 RUBID STRONT ITR CYRKON NIOB MOLIBDEN TECHNET RUTEN ROD PALLAD SREBRO KADM IND CYNA ANTYMON TELLUR JOD KSENON ST ST ŚR Cs Ca Sr Ba Y La Ti Zr V Nb Ta Cr Mo W Mn Fe Ru Os Co Rh Ir 6 CEZ BAR LANTAN HAFN TANTAL WOLFRAM REN OSM IRYD PLATYNA ZŁOTO RTĘĆ TAL OŁÓW BIZMUT POLON ASTAT RADON ST ST 1861 ST ŚR FRANS RAD AKTYN RUTHERFORD DUBN SEABORG BOHR HAS MEITNER DARMSTADT ROENTGEN KOPERNIK NIHONIUM FLEROW MOSCOVIUM LIWERMOR TENNESSINE OGANESSON LANTANOWCE Ce Tb Er CER PRAZEODYM NEODYM PROMET SAMAR EUROP GADOLIN TERB DYSPROZ HOLM ERB TUL ITERB LUTET AKTYNOWCE Th U TOR PROTAKTYN URAN NEPTUN PLUTON AMERYK KIUR BERKEL KALIFORN EINSTEIN FERM MENDELEW NOBEL LORENS (1958) 1962 Rys Układ okresowy bez symboli pierwiastków odkrytych po 1869 r. Ni Pd Pt Cu Ag Au Zn Cd Hg In Tl Sn Pb As Sb Bi Se Te Br I 18 Grupy i okresy Tablica Mendelejewa w kolumnach pionowych, zwanych grupami, zawiera pierwiastki o podobnych właściwościach. Każda grupa ma nazwę wywodzącą się z nazwy pierwiastka stojącego najwyżej: litowce berylowce skandowce tytanowce wanadowce chromowce manganowce żelazowce kobaltowce niklowce miedziowce cynkowce borowce węglowce azotowce tlenowce fluorowce helowce 16
18 CHEMIA. Podręcznik... Część 1. Zakres rozszerzony Oprócz nazw całych grup można wprowadzać nazwy ich fragmentów utworzone z nazwy pierwiastka stojącego najwyżej w wybranym fragmencie, np. berylowce Be Mg Ca Sr Ba Ra azotowce wapniowce N P As Sb Bi tlenowce fosforowce O S Se Te Po fluorowce siarkowce F Cl Br I At chlorowce Grupy dzielą się na główne (1., 2., i od 13. do 18.) oraz poboczne (pozostałe). W szeregach poziomych, czyli okresach, znajdują się pierwiastki o właściwościach zmieniających się stopniowo od reaktywnych metali do reaktywnych niemetali. Na końcu każdego okresu znajduje się niemetal niereaktywny helowiec. Dwa szeregi poziome: tzw. lantanowce od 58 Ce do 71 Lu i aktynowce od 90 Th do 103Lr, umieszczono pod tablicą tylko w celu jej skrócenia geometrycznego. Pierwiastki te należą bowiem odpowiednio do 6. i 7. okresu i tworzą czternaście grup (dwupierwiastkowych kolumn pionowych), dla których nie wprowadzono indywidualnej numeracji. Zmiany właściwości fizyko-chemicznych w trzecim okresie układu okresowego Mendelejewa ilustruje zestawienie: reaktywne metale mało reaktywne metale i niemetale reaktywne niemetale niereaktywny helowiec Na Mg Si P S Ar Sód Magnez Glin Krzem Fosfor Siarka Chlor Argon metale niemetale Wśród pierwiastków można wyróżnić dwa ich rodzaje: metale i niemetale. Każda z tych grup ma określony zespół właściwości fizycznych i chemicznych. Podział na metale i niemetale znajduje odzwierciedlenie w tablicy Mendelejewa. W grupach pobocznych znajdują się wyłącznie metale. W grupach głównych granica metale niemetale przesuwa się w prawo ze wzrostem numeru okresu, dzieląc tablicę na dwa trójkąty. Niektóre pierwiastki leżące przy linii rozgraniczającej B, Si, Ge, As, Sb, Te, At są często nazywane półmetalami, ponieważ wykazują częściowo cechy metali, a częściowo cechy niemetali: Li Be B C N O F Ne Na Mg Si P S Ar K Ca Ga Ge As Se Br Kr Rb Sr In Sn Sb Te I Xe Cs Ba Pb Bi Po At Rn 17
19 2. Budowa atomu z elementami mechaniki kwantowej Okresowość konfiguracji elektronowych Przyczyny okresowych zmian właściwości, jak wszystkie przyczyny cech makroskopowych, tkwią w strukturze materii. Współczesny stan wiedzy o budowie atomu pozwala na sformułowanie prawa okresowości w ujęciu mikroskopowym. Konfiguracje elektronowe pierwiastków są funkcją liczby atomowej. Rysunek 2.20 przedstawia zależność między liczbą elektronów walencyjnych pierwiastka, a jego liczbą atomową. Jest to zależność okresowa. Należy pamiętać, że o właściwościach pierwiastków decyduje nie tylko liczba elektronów walencyjnych, lecz również typ konfiguracji walencyjnej i budowa rdzenia. liczba 17 elektronów walencyjnych Lu Lr 16 Yb No 15 Tm Md 14 Er Fm 13 Ho Es 12 Zn Cd Dy Hg Cf Cn 11 Cu Ag Tb Au Bk Rg 10 Ni Pd Gd Pt Cm Ds 9 Co Rh Eu Ir Am Mt 8 Ne Ar Fe Kr Ru Xe Sm Os Rn Pu Hs 7 F Cl Mn Br Tc I Pm Re At Np Bh 6 O S Cr Se No Te Nd W Po U Sg 5 N P V As Nb Sb Pr Ta Bi Pa Db 4 C Si Ti Ge Zr Sn Ce Hf Pb Th Rf 3 B Al Sc Y La Ac He Ga In Tl 2 Be Mg Ca Sr Ba Ra 1 H Li Na K Rb Cs Fr Z Rys Zależność liczby elektronów walencyjnych od liczby atomowej Z W poprzednim paragrafie była już mowa o tym, że blok konfiguracyjny w tablicy Mendelejewa jest to zbiór pierwiastków o określonym typie podpowłokowej konfiguracji walencyjnej. Liczba grup w bloku konfiguracyjnym jest równa pojemności podpowłoki, którą zajmują kolejne, nowo przybywające elektrony w atomach pierwiastków tego bloku. Blok s tworzą pierwiastki o konfiguracji walencyjnej ns 1 lub ns 2, a więc wodór, hel oraz litowce i berylowce. Blok d tworzą pierwiastki o konfiguracji walencyjnej od ns 2 (n 1)d 1 do ns 2 (n 1)d 10, a więc pierwiastki grup pobocznych. Bloki konfiguracyjne 18 Blok p tworzą pierwiastki o konfiguracji walencyjnej od ns 2 np 1 do ns 2 np 6, a więc pierwiastki grup głównych od 13. do 18., ale bez helu. Blok f tworzą pierwiastki o konfiguracji walencyjnej ns (n 1)d (n 2)f. W podpowłoce (n 2)f może być
20 CHEMIA. Podręcznik... Część 1. Zakres rozszerzony H 2 He Li 4 Be 5 B 6 C 7 N 8 O 9 F 10 Ne 3 12 Mg 11 Na 13 Al 14 Si 15 P 16 S 17 Cl 18 Ar K 20 Ca 21 Sc 22 Ti 23 V 24 Cr 25 Mn 26 Fe 27 Co 28 Ni 29 Cu 30 Zn 31 Ga 32 Ge 33 As 34 Se 35 Br 36 Kr 5 37 Rb 38 Sr 39 Y 40 Zr 41 Nb 42 Mo 43 Tc 44 Ru 45 Rh 46 Pd 47 Ag 48 Cd 49 In 50 Sn 51 Sb 52 Te 53 I 54 Xe 6 55 Cs 56 Ba 57 La 72 Hf 73 Ta 74 W 75 Re 76 Os 77 Ir 78 Pt 79 Au 80 Hg 81 Tl 82 Pb 83 Bi 84 Po 85 At 86 Rn 7 87 Fr 88 Ra 89 Ac 104 Rf 105 Db 106 Sg 107 Bh 108 Hs 109 Mt 110 Ds 111 Rg 112 Cn 113 Nh 114 Fl 115 Mc 116 Lv 117 Ts 118 Og blok s blok p blok d blok f 58 Ce 90 Th 59 Pr 91 Pa 60 Nd 61 Pm 62 Sm 63 Eu 64 Gd 65 Tb 66 Dy 67 Ho 68 Er 69 Tm 70 Yb 71 Lu 92 U 93 Np 94 Pu 95 Am 96 Cm 97 Bk 98 Cf 99 Es 100 Fm 101 Md 102 No 103 Lr Rys Układ okresowy pierwiastków z zaznaczonymi blokami konfiguracyjnymi Każda grupa główna (!) układu okresowego ma własną, niepowtarzalną konfigurację walencyjną, a ponadto wszystkie pierwiastki należące do danej grupy mają tyle samo elektronów walencyjnych. Prawidłowości te dla grup głównych ilustruje zestawienie: Grupa Konfiguracja walencyjna Liczba elektronów walencyjnych ns 1 ns 2 ns 2 np 1 ns 2 np 2 ns 2 np 3 ns 2 np 4 ns 2 np 5 ns 2 np Pierwiastki należące do danej grupy różnią się liczbą powłok elektronowych i numerem powłoki walencyjnej. Konfiguracja ns 1 oznacza, że pierwiastek okresu pierwszego (wodór) ma konfigurację walencyjną 1s 1. Pierwiastek tej samej grupy, ale okresu drugiego (lit) ma konfigurację walencyjną 2s 1, a kolejne pierwiastki tej grupy: 3s 1, 4s 1, 5s 1 itd. Pierwiastki grup pobocznych mają następującą konfigurację walencyjną: Grupa Konfiguracja walencyjna Liczba elektronów walencyjnych ns 2 (n 1)d 1 ns 2 (n 1)d 2 ns 2 (n 1)d 3 ns 2 (n 1)d
21 2. Budowa atomu z elementami mechaniki kwantowej O architekturze układu okresowego decyduje kolejność zapełniania elektronami poszczególnych powłok i podpowłok. Prawidłowości w konfiguracjach elektronowych stanu podstawowego prowadzą do następujących wniosków: Okres jest uporządkowanym według wzrastających liczb atomowych szeregiem pierwiastków, których atomy zawierają identyczną liczbę powłok elektronowych. Numer okresu określa liczbę powłok elektronowych. Nowy okres rozpoczyna się dlatego, że po zapełnieniu podpowłoki np energia stanów podstawowych w podpowłoce (n + 1)s jest najniższa wśród energii wszystkich innych stanów podstawowych nieobsadzonych podpowłok. I to ją obsadza nowo pojawiający się elektron. Nowy okres rozpoczyna się wówczas, gdy kolejny, nowo przybywający elektron zajmuje pierwszy stan w nieobsadzonej jeszcze powłoce (za każdym razem jest to stan w podpowłoce s). W skrócie, ale umownie, można powiedzieć, że nowy okres to rozpoczęcie zabudowy nowej powłoki. Grupa jest uporządkowaną według wzrastających liczb atomowych kolumną pierwiastków, których atomy mają charakterystyczną konfigurację walencyjną i tę samą liczbę elektronów walencyjnych. Numer grupy określa liczbę elektronów walencyjnych H He s s 2 Li Be B C N O F Ne s 1 2s 2 2s 2 2p 1 2s 2 2p 2 2s 2 2p 3 2s 2 2p 4 2s 2 2p 5 2s 2 2p 6 Na Mg Al Si P S Cl Ar s 1 3s s 2 3p 1 3s 2 3p 2 3s 2 3p 3 3s 2 3p 4 3s 2 3p 5 3s 2 3p 6 K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr s 1 4s 2 3d 1 4s 2 3d 2 4s 2 3d 3 4s 2 3d 5 4s 1 3d 5 4s 2 3d 6 4s 2 3d 7 4s 2 3d 8 4s 2 3d 10 4s 1 3d 10 4s 2 4s 2 4p 1 4s 2 4p 2 4s 2 4p 3 4s 2 4p 4 4s 2 4p 5 4s 2 4p 6 Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe s 1 5s 2 4d 1 5s 2 4d 2 5s 2 4d 4 5s 1 4d 5 5s 1 4d 6 5s 1 4d 7 5s 1 4d 8 5s 1 4d 10 4d 10 5s 1 4d 10 5 s 2 5s 2 5p 1 5s 2 5p 2 5s 2 5p 3 5s 2 5p 4 5s 2 5p 5 5s 2 5p 6 Cs Ba La Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn s 1 6s 2 5d 1 6s 2 5d 2 6s 2 5d 3 6s 2 5d 4 6s 2 5d 5 6s 2 5d 6 6s 2 5d 7 6s 2 5d 9 6s 1 5d 10 6s 1 5d 10 6 s 2 6s 2 6p 1 6s 2 6p 2 6s 2 6p 3 6s 2 6p 4 6s 2 6p 5 6s 2 6p 6 Fr Ra Ac Rf Db Sg Bh Hs Mt Ds Rg Cn Nh Fl Mc Lv Ts Og s 1 7s 2 6d 1 7s 2 6d 2 7s 2 blok s blok p blok d Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu f 1 5d 1 6s 2 4f 3 5d 0 6s 2 4f 4 5d 0 6s 2 4f 5 5d 0 6s 2 4f 6 5d 0 6s 2 4f 7 5d 0 6s 2 4f 7 5d 1 6s 2 4f 9 5d 0 6s 2 4f 10 5d 0 6s 2 4f 11 5d 0 6s 2 4f 12 5d 0 6s 2 4f 13 5d 0 6s 2 4f 14 5d 0 6s 2 4f 14 5d 1 6s 2 Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr blok f 5f 0 6d 2 7s 2 5f 2 6d 1 7s 2 5f 3 6d 1 7s 2 5f 4 6d 1 7s 2 5f 6 6d 0 7s 2 5f 7 6d 0 7s 2 5f 7 6d 1 7s 2 5f 8 6d 1 7s 2 5f 10 6d 0 7s 2 5f 11 6d 0 7s 2 5f 12 6d 0 7s 2 5f 13 6d 0 7s 2 5f 14 6d 0 7s 2 5f 14 6d 1 7s 2 Rys Układ okresowy pierwiastków z konfiguracją walencyjną 20
22 2. Budowa atomu z elementami mechaniki kwantowej 115 Ważne pojęcia: Prawo okresowości (w ujęciu makroskopowym) mówi o tym, że właściwości pierwiastków zmieniają się okresowo ze wzrostem liczby atomowej. Prawo okresowości (w ujęciu mikroskopowym) mówi o tym, że konfiguracje elektronowe pierwiastków są funkcją okresową liczby atomowej. Tablica Mendelejewa, czyli układ okresowy pierwiastków tablica wszystkich pierwiastków uporządkowanych w kolumny pionowe grupy, i szeregi poziome okresy. Zarówno w grupach jak i w okresach wzrasta liczba atomowa Z pierwiastków i niemal zawsze wzrasta ich masa atomowa. Grupa pionowa kolumna zawierająca pierwiastki o podobnych właściwościach. Jest kolumną pierwiastków, których atomy mają ten sam, niepowtarzalny typ konfiguracji walencyjnej i tę samą liczbę elektronów walencyjnych. Grupy główne: 1., 2. i od 13. do 18. Grupy poboczne: od 3. do 12. Okres jest uporządkowanym według wzrastających liczb atomowych szeregiem pierwiastków o właściwościach zmieniających się stopniowo, których atomy zawierają identyczną liczbę powłok elektronowych. Rozwiąż zadania (odpowiedzi nie umieszczaj w podręczniku!) 1. Przed rokiem 1869 podejmowano różne próby klasyfikacji pierwiastków. Sporządź w zeszycie krótką notatkę na temat triad Döbereinera oraz oktaw Newlandsa na podstawie informacji znalezionych w Internecie lub w innych źródłach wiedzy. 2. Mendelejew nie mógł uszeregować pierwiastków ze wzrostem liczby atomowej, ponieważ w 1869 roku nie posiadano wiedzy na temat budowy atomu. Wykorzystał do tego celu masę atomową. Zauważył jednak, że w kilku przypadkach musiał ułożyć pierwiastek o mniejszej masie za pierwiastkiem o większej masie, aby znalazły się one w odpowiednich grupach układu okresowego. Odszukaj w układzie okresowym dwie pary pierwiastków, które opisują problem, z którym zmierzył się Mendelejew. 3. Na podstawie podanych walencyjnych konfiguracji powłokowych zapisz walencyjne konfiguracje podpowłokowe i ustal nazwy pierwiastków: a) M 6, b) N 3, c) M 2 N 2, d) M 10 N 1. 21
23 116 CHEMIA. Podręcznik... Część 1. Zakres rozszerzony Sprawdź, co umiesz... (odpowiedzi nie umieszczaj w podręczniku!) Zadanie 1. (0-1p.) Zapisz konfigurację graficzną elektronów walencyjnych pierwiastka grupy 17., wiedząc, że jego elektrony rdzenia atomowego o najwyższej energii opisywane są przez główną liczbę kwantową n = 5. Zadanie 2. (0-1p.) Ustal symbole pierwiastków, które spełniają podane warunki: a) są pierwiastkami czwartego okresu, których atomy mają podpowłokę d wypełnioną całkowicie; b) są pierwiastkami czwartego okresu, których atomy zawierają jeden elektron niesparowany. Zadanie 3. (0-1p.) Atomy pierwiastków X i Y mają: cztery powłoki elektronowe; więcej niż trzy elektrony walencyjne, jednak trzy z nich w stanie podstawowym, pozostają niesparowane. Elektrony walencyjne atomu pierwiastka Y znajdują się w jednej powłoce. Elektrony walencyjne atomu pierwiastka X znajdują się w dwóch podpowłokach dwóch różnych powłok, przy czym liczba walencyjnych elektronów sparowanych jest większa od liczby elektronów niesparowanych. Przerysuj i uzupełnij poniższą tabelę. Wpisz symbole chemiczne pierwiastków X i Y, oraz dane dotyczące ich położenia w tablicy Mendelejewa. Pierwiastek Symbol pierwiastka Numer okresu Numer grupy Symbol bloku X Y Zadanie 4. (0-1p.) Z konfiguracji elektronowej atomu pierwiastka E wynika, że w tym atomie: elektrony rozmieszczone są w trzech powłokach elektronowych, liczba elektronów walencyjnych wynosi n 2, gdzie n to maksymalna liczba elektronów, jaka może się zmieścić w podpowłoce p. Zapisz skróconą, podpowłokową konfigurację elektronową pierwiastka E. Zadanie 5. (0-1p.) O elektronie w pewnym atomie wiadomo, że zajmuje poziom energetyczny o głównej liczbie kwantowej n = 2. Ustal, jakie wartości pobocznej liczby kwantowej l oraz magnetycznej liczby kwantowej m opisują stan tego elektronu, jeżeli jego magnetyczna liczba kwantowa przyjmuje największą dopuszczalną wartość dla tej powłoki. Zadanie 6. (0-1p.) Ustal, jaką maksymalną liczbę elektronów może pomieścić podpowłoka f, powłoka M oraz dowolny poziom orbitalny. 22
24 2. Budowa atomu z elementami mechaniki kwantowej 117 Zadanie 7. (0-1p.) W tabeli przedstawiono różne poziomy orbitalne, które oznaczono literami A, B, C i D: A B C D Ocen, czy podane zdania są prawdziwe, czy fałszywe. 1. Poziomy orbitalne oznaczone literami A i B opisywane są przez jednakowe wartości głównej liczby kwantowej n. 2. Poziomy orbitalne oznaczone literami B i C opisywane są przez różne wartości pobocznej liczby kwantowej l. 3. Poziomy orbitalne oznaczone literami C i D opisywane są przez różne wartości magnetycznej liczby kwantowej m. Zadanie 8. (0-1p.) Ustal zestaw czterech liczb kwantowych głównej n, pobocznej l, magnetycznej m i magnetycznej spinowej m s dla elektronu wskazanego w zapisie konfiguracji elektronowej atomu chromu. Załóż, że kolejnym poziomom orbitalnym w zapisie klatkowym odpowiadają wartości magnetycznej liczby kwantowej uporządkowane narastająco: 1s 2s 2p 3s 3p 3d 4s Zadanie 9. (0-1p.) Wyjaśnij, dlaczego wskazany fragment konfiguracji elektronowej atomu węgla jest błędny. 2p Zadanie 10. (0-2p.) Energię poziomu energetycznego w atomie wodoru (wyrażoną w elektronowoltach) można obliczyć ze wzoru: E = 13,60 [ev], n 2 gdzie n to numer powłoki, na której znajduje się elektron (wartość głównej liczby kwantowej). a) Oblicz, ile energii, wyrażonej w elektronowoltach, wyemituje elektron przechodząc z powłoki trzeciej na drugą oraz z powłoki drugiej na pierwszą. b) Ocen, która odległość energetyczna między powłokami jest większa: ta pomiędzy powłoką szóstą a piątą, czy ta pomiędzy powłoką piątą i czwartą. 23
25 Dydaktyczna obudowa podręcznika na naszej stronie internetowej Dla nauczyciela Program nauczania. Szczegółowy rozkład materiału z odniesieniami do treści szczegółowych w podstawie programowej. Plan wynikowy. Wymagania szczegółowe na poszczególne oceny. Sprawdzian na wejściu pomocny w ocenie poziomu wiedzy i umiejętności uczniów rozpoczynających naukę w liceum lub w. Sprawdziany po każdym rozdziale, gotowe do pobrania i wydrukowania. Klasówki samodzielnie komponowane przez nauczyciela za pomocą generatora klasówek. Zadania, ich ilość, typ i rodzaj pod względem treści i stopnia trudności, będzie można pobierać z dostępnej bazy zadań, dostosowując klasówki do swoich potrzeb i możliwości uczniów. Dla ucznia Filmowe wersje większości doświadczeń opisanych w podręczniku. Animacje. 24
26 Zbiór zadań z chemii Zakres rozszerzony Jest to kolejne, jedenaste wydanie powszechnie znanego od wielu lat i cenionego zbioru zadań z chemii w zakresie rozszerzonym, przeznaczonego do liceów i techników. Zbiór ten został po raz kolejny uzupełniony o dodatkowe zadania w kilku obecnych rozdziałach (zwłaszcza w zakresie chemii organicznej), oraz poszerzony o zestaw zadań w rozdziałach nowych, które pojawiły się w podstawie programowej, obowiązującej od roku 2019, takich, jak Chemia wokół nas i Elementy ochrony środowiska. 25
Pierwiastek: Na - Sód Stan skupienia: stały Liczba atomowa: 11
 ***Dane Pierwiastków Chemicznych*** - Układ Okresowy Pierwiastków 2.5.1.FREE Pierwiastek: H - Wodór Liczba atomowa: 1 Masa atomowa: 1.00794 Elektroujemność: 2.1 Gęstość: [g/cm sześcienny]: 0.0899 Temperatura
***Dane Pierwiastków Chemicznych*** - Układ Okresowy Pierwiastków 2.5.1.FREE Pierwiastek: H - Wodór Liczba atomowa: 1 Masa atomowa: 1.00794 Elektroujemność: 2.1 Gęstość: [g/cm sześcienny]: 0.0899 Temperatura
Grupa b. Zadania na ocen celujàcà
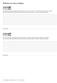 Zadania na ocen celujàcà Grupa a Do reakcji syntezy siarczku glinu przygotowano g glinu i, g siarki. Czy substraty przereagowały w całoêci? JeÊli nie przereagowały, podaj nazw substratu, który nie przereagował
Zadania na ocen celujàcà Grupa a Do reakcji syntezy siarczku glinu przygotowano g glinu i, g siarki. Czy substraty przereagowały w całoêci? JeÊli nie przereagowały, podaj nazw substratu, który nie przereagował
Moduł: Chemia. Fundamenty. Liczba godzin. Nr rozdziału Tytuł. Temat lekcji. Rozdział 1. Przewodnik po chemii (12 godzin)
 Rozkład materiału z chemii w klasie II LO zakres rozszerzony Chemia. Fundamenty. Krzysztof Pazdro, wyd. Oficyna Edukacyjna Krzysztof Pazdro Sp. z o.o.. nr dopuszczenia 565//0 Chemia. i związki nieorganiczne.
Rozkład materiału z chemii w klasie II LO zakres rozszerzony Chemia. Fundamenty. Krzysztof Pazdro, wyd. Oficyna Edukacyjna Krzysztof Pazdro Sp. z o.o.. nr dopuszczenia 565//0 Chemia. i związki nieorganiczne.
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
PIERWIASTKI W UKŁADZIE OKRESOWYM
 PIERWIASTKI W UKŁADZIE OKRESOWYM 1 Układ okresowy Co można odczytać z układu okresowego? - konfigurację elektronową - podział na bloki - podział na grupy i okresy - podział na metale i niemetale - trendy
PIERWIASTKI W UKŁADZIE OKRESOWYM 1 Układ okresowy Co można odczytać z układu okresowego? - konfigurację elektronową - podział na bloki - podział na grupy i okresy - podział na metale i niemetale - trendy
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
b) Pierwiastek E tworzy tlenek o wzorze EO 2 i wodorek typu EH 4, a elektrony w jego atomie rozmieszczone są na dwóch powłokach elektronowych
 1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
1. Ustal jakich trzech różnych pierwiastków dotyczą podane informacje. Zapisz ich symbole a) W przestrzeni wokółjądrowej dwuujemnego jonu tego pierwiastka znajduje się 18 e. b) Pierwiastek E tworzy tlenek
Anna Grych Test z budowy atomu i wiązań chemicznych
 Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
Anna Grych Test z budowy atomu i wiązań chemicznych 1. Uzupełnij tabelkę wpisując odpowiednie dane: Nazwa atomu Liczba nukleonów protonów neutronów elektronów X -... 4 2 Y -... 88 138 Z -... 238 92 W -...
a b zasi g kilku centymetrów zasi g kilkudziesi ciu centymetrów zasi g nieograniczony ATOM jàdro atomowe neutrony protony nukleony pow oki elektronowe
 ZAWARTOÂå SK ADNIKA W ROZTWORZE nasyconym i nienasyconym ATOM (najmniejsza czàstka pierwiastka chemicznego) st enie procentowe 2% jàdro atomowe g wody ms = 2 g 00 g roztworu nasyconym protony neutrony
ZAWARTOÂå SK ADNIKA W ROZTWORZE nasyconym i nienasyconym ATOM (najmniejsza czàstka pierwiastka chemicznego) st enie procentowe 2% jàdro atomowe g wody ms = 2 g 00 g roztworu nasyconym protony neutrony
imię i nazwisko numer w dzienniku klasa
 Test po. części serii Chemia Nowej Ery CHEMIA I grupa imię i nazwisko numer w dzienniku klasa Test składa się z 8 zadań. Czytaj uważnie treść poleceń. W zadaniach. 5., 7.., 3. 7. wybierz poprawną odpowiedź
Test po. części serii Chemia Nowej Ery CHEMIA I grupa imię i nazwisko numer w dzienniku klasa Test składa się z 8 zadań. Czytaj uważnie treść poleceń. W zadaniach. 5., 7.., 3. 7. wybierz poprawną odpowiedź
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj.
 Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Tematy i zakres treści z chemii - zakres rozszerzony, dla klas 2 LO2 i 3 TZA/archt. kraj. Tytuł i numer rozdziału w podręczniku Nr lekcji Temat lekcji Szkło i sprzęt laboratoryjny 1. Pracownia chemiczna.
Nazwy pierwiastków: ...
 Zadanie 1. [ 3 pkt.] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Atom pierwiastka X w reakcjach chemicznych może tworzyć jon zawierający 20
Zadanie 1. [ 3 pkt.] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Atom pierwiastka X w reakcjach chemicznych może tworzyć jon zawierający 20
Temat 1: Budowa atomu zadania
 Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
Budowa atomu Zadanie 1. (0-1) Dany jest atom sodu Temat 1: Budowa atomu zadania 23 11 Na. Uzupełnij poniższą tabelkę. Liczba masowa Liczba powłok elektronowych Ładunek jądra Liczba nukleonów Zadanie 2.
Drogi Uczniu, Przed tobą test złożony z 20 zadań. Czytaj wszystko bardzo uważnie i udziel prawidłowej odpowiedzi w załączonej karcie odpowiedzi.
 B... pieczątka nagłówkowa WKK............... kod pracy ucznia (wpisuje uczeń) KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP WOJEWÓDZKI Drogi Uczniu, Przed tobą test złożony z 20 zadań. Czytaj
B... pieczątka nagłówkowa WKK............... kod pracy ucznia (wpisuje uczeń) KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP WOJEWÓDZKI Drogi Uczniu, Przed tobą test złożony z 20 zadań. Czytaj
Zad: 1 Spośród poniższych jonów wybierz te, które mają identyczną konfigurację elektronową:
 Zad: 1 Spośród poniższych jonów wybierz te, które mają identyczną konfigurację elektronową: Zad: 2 Zapis 1s 2 2s 2 2p 6 3s 2 3p 2 (K 2 L 8 M 4 ) przedstawia konfigurację elektronową atomu A. argonu. B.
Zad: 1 Spośród poniższych jonów wybierz te, które mają identyczną konfigurację elektronową: Zad: 2 Zapis 1s 2 2s 2 2p 6 3s 2 3p 2 (K 2 L 8 M 4 ) przedstawia konfigurację elektronową atomu A. argonu. B.
PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 ... pieczątka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
... pieczątka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Układ okresowy pierwiastków
 strona 1/8 Układ okresowy pierwiastków Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Teoria atomistyczno-cząsteczkowa, nieciągłość budowy materii. Układ okresowy pierwiastków
strona 1/8 Układ okresowy pierwiastków Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Teoria atomistyczno-cząsteczkowa, nieciągłość budowy materii. Układ okresowy pierwiastków
Piotr Kosztołowicz. Powtórka przed maturą. Chemia. Zadania. Zakres rozszerzony
 Piotr Kosztołowicz Zakres rozszerzony Chemia Powtórka przed maturą Zadania 95 Spis treści Wstęp Rozdział 1. Budowa atomów Rozdział 2. Przemiany jądrowe Rozdział 3. Struktura elektronowa atomu Rozdział
Piotr Kosztołowicz Zakres rozszerzony Chemia Powtórka przed maturą Zadania 95 Spis treści Wstęp Rozdział 1. Budowa atomów Rozdział 2. Przemiany jądrowe Rozdział 3. Struktura elektronowa atomu Rozdział
Rozdział 6 Atomy wieloelektronowe
 Rozdział 6 Atomy wieloelektronowe 6.1: Atomy a struktura układu okresowego 6.2: Zakaz Pauliego 6.3: Wypełnianie powłok elektronami 6.4: Układ okresowy 6.5: Całkowity moment pędu 6.6: Oddziaływanie spin-orbita
Rozdział 6 Atomy wieloelektronowe 6.1: Atomy a struktura układu okresowego 6.2: Zakaz Pauliego 6.3: Wypełnianie powłok elektronami 6.4: Układ okresowy 6.5: Całkowity moment pędu 6.6: Oddziaływanie spin-orbita
Opracowała: mgr Agata Wiśniewska PRZYKŁADOWE SPRAWDZIANY WIADOMOŚCI l UMIEJĘTNOŚCI Współczesny model budowy atomu (wersja A)
 PRZYKŁADOW SPRAWDZIANY WIADOMOŚCI l UMIJĘTNOŚCI Współczesny model budowy atomu (wersja A) 1. nuklid A. Zbiór atomów o tej samej wartości liczby atomowej. B. Nazwa elektrycznie obojętnej cząstki składowej
PRZYKŁADOW SPRAWDZIANY WIADOMOŚCI l UMIJĘTNOŚCI Współczesny model budowy atomu (wersja A) 1. nuklid A. Zbiór atomów o tej samej wartości liczby atomowej. B. Nazwa elektrycznie obojętnej cząstki składowej
ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050
 ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa ul. Szczotkarska 42 Wydanie nr 7, Data wydania: 14 lipca 2015 r. Nazwa i adres AB 1050 AKADEMIA
ZAKRES AKREDYTACJI LABORATORIUM BADAWCZEGO Nr AB 1050 wydany przez POLSKIE CENTRUM AKREDYTACJI 01-382 Warszawa ul. Szczotkarska 42 Wydanie nr 7, Data wydania: 14 lipca 2015 r. Nazwa i adres AB 1050 AKADEMIA
1/8. KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 6 listopada 2010 roku
 1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 6 listopada 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP II REJONOWY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 6 listopada 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP II REJONOWY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
Struktura elektronowa
 Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Struktura elektronowa Struktura elektronowa atomów układ okresowy pierwiastków: 1) elektrony w atomie zajmują poziomy energetyczne od dołu, inaczej niż te gołębie (w Australii, ale tam i tak chodzi się
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.)
 Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
Budowa atomu Poziom: rozszerzony Zadanie 1. (2 pkt.) Zadanie 1 2 3 4 5 6 7 8 9 10 Punkty Okres połowiczego rozpadu pewnego radionuklidu wynosi 16 godzin. a) Określ, ile procent atomów tego izotopu rozpadnie
V KONKURS CHEMICZNY 23.X. 2007r. DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚWIĘTOKRZYSKIEGO Etap I ... ... czas trwania: 90 min Nazwa szkoły
 V KONKURS CHEMICZNY 23.X. 2007r. DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚWIĘTOKRZYSKIEGO Etap I...... Imię i nazwisko ucznia ilość pkt.... czas trwania: 90 min Nazwa szkoły... maksymalna ilość punk. 33 Imię
V KONKURS CHEMICZNY 23.X. 2007r. DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚWIĘTOKRZYSKIEGO Etap I...... Imię i nazwisko ucznia ilość pkt.... czas trwania: 90 min Nazwa szkoły... maksymalna ilość punk. 33 Imię
Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Budowa atomu, układ okresowy i promieniotwórczość Monika Gałkiewicz Zad. 1 () Przedstaw pełną konfigurację elektronową atomu pierwiastka
Układ okresowy. Przewidywania teorii kwantowej
 Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
Przewidywania teorii kwantowej 1 Chemia kwantowa - podsumowanie Cząstka w pudle Atom wodoru Równanie Schroedingera H ˆ = ˆ T e Hˆ = Tˆ e + Vˆ e j Chemia kwantowa - podsumowanie rozwiązanie Cząstka w pudle
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Budowa atomu. Izotopy
 Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
1/9. zadanie razem Maksymalna liczba punktów
 podpis nauczyciela 1/9 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 08 stycznia 2011 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP III WOJEWÓDZKI KOD UCZNIA:.. zadanie 1 2 4 5 razem Maksymalna
podpis nauczyciela 1/9 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 08 stycznia 2011 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP III WOJEWÓDZKI KOD UCZNIA:.. zadanie 1 2 4 5 razem Maksymalna
1/8. KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 4 października 2010 roku
 1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 4 października 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP I SZKOLNY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
1/8 KOMISJA WOJEWÓDZKA KONKURSU CHEMICZNEGO Warszawa, dnia 4 października 2010 roku KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ETAP I SZKOLNY KOD UCZNIA:.. zadanie 1 2 3 4 5 6 razem Maksymalna liczba punktów
Wewnętrzna budowa materii - zadania
 Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Poniższe zadania rozwiąż na podstawie układu okresowego. Zadanie 1 Oceń poprawność poniższych zdań, wpisując P, gdy zdanie jest prawdziwe oraz F kiedy ono jest fałszywe. Stwierdzenie Atom potasu posiada
Nazwy pierwiastków: A +Fe 2(SO 4) 3. Wzory związków: A B D. Równania reakcji:
 Zadanie 1. [0-3 pkt] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Suma protonów i elektronów anionu X 2- jest równa 34. II. Stosunek masowy
Zadanie 1. [0-3 pkt] Na podstawie podanych informacji ustal nazwy pierwiastków X, Y, Z i zapisz je we wskazanych miejscach. I. Suma protonów i elektronów anionu X 2- jest równa 34. II. Stosunek masowy
PRAWO OKRESOWOŚCI. 1.131. Liczba co najmniej częściowo obsadzonych powłok elektronowych decyduje o przynależności pierwiastka
 PRAWO OKRESOWOŚCI 1.125. D. Mendelejew sformułował swoje prawo w następujący sposób: Właściwości fizyczne i chemiczne pierwiastków zmieniają się okresowo w zależności od A) liczby protonów w jądrze atomowym.
PRAWO OKRESOWOŚCI 1.125. D. Mendelejew sformułował swoje prawo w następujący sposób: Właściwości fizyczne i chemiczne pierwiastków zmieniają się okresowo w zależności od A) liczby protonów w jądrze atomowym.
I. Substancje i ich przemiany
 NaCoBeZU z chemii dla klasy 1 I. Substancje i ich przemiany 1. Pracownia chemiczna podstawowe szkło i sprzęt laboratoryjny. Przepisy BHP i regulamin pracowni chemicznej zaliczam chemię do nauk przyrodniczych
NaCoBeZU z chemii dla klasy 1 I. Substancje i ich przemiany 1. Pracownia chemiczna podstawowe szkło i sprzęt laboratoryjny. Przepisy BHP i regulamin pracowni chemicznej zaliczam chemię do nauk przyrodniczych
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Badania laboratoryjne składu chemicznego wód podziemnych
 Katowice 27.11.2015r. Odpowiedź na list Towarzystwa na rzecz Ziemi W związku ze zgłaszanymi przez Towarzystwo na rzecz Ziemi (pismo z dnia 05.11.2015r.) pytaniami dotyczącymi pierwiastków występujących
Katowice 27.11.2015r. Odpowiedź na list Towarzystwa na rzecz Ziemi W związku ze zgłaszanymi przez Towarzystwo na rzecz Ziemi (pismo z dnia 05.11.2015r.) pytaniami dotyczącymi pierwiastków występujących
Wewnętrzna budowa materii
 Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
Atom i układ okresowy Wewnętrzna budowa materii Atom jest zbudowany z jądra atomowego oraz krążących wokół niego elektronów. Na jądro atomowe składają się protony oraz neutrony, zwane wspólnie nukleonami.
Scenariusz lekcji otwartej z chemii w klasie II gimnazjum.
 Scenariusz lekcji otwartej z chemii w klasie II gimnazjum. Opracowała: Marzena Bień Termin realizacji: Czas realizacji: 45 minut. Temat: Chemia a budowa atomów. Cel ogólny: Usystematyzowanie wiadomości
Scenariusz lekcji otwartej z chemii w klasie II gimnazjum. Opracowała: Marzena Bień Termin realizacji: Czas realizacji: 45 minut. Temat: Chemia a budowa atomów. Cel ogólny: Usystematyzowanie wiadomości
CHEMIA WARTA POZNANIA
 Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
Materiały do zajęć dokształcających z chemii nieorganicznej i fizycznej Wydział Chemii UAM Poznań 2011 Część I Atom jest najmniejszą częścią pierwiastka chemicznego, która zachowuje jego właściwości chemiczne
KONKURS CHEMICZNY DLA UCZNIÓW SZKÓŁ GIMNAZJALNYCH ETAP SZKOLNY
 ... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW SZKÓŁ GIMNAZJALNYCH ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW SZKÓŁ GIMNAZJALNYCH ETAP SZKOLNY Drogi Uczniu, Witaj w pierwszym etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Wymagania przedmiotowe do podstawy programowej - chemia klasa 7
 Wymagania przedmiotowe do podstawy programowej - chemia klasa 7 I. Substancje i ich właściwości opisuje cechy mieszanin jednorodnych i niejednorodnych, klasyfikuje pierwiastki na metale i niemetale, posługuje
Wymagania przedmiotowe do podstawy programowej - chemia klasa 7 I. Substancje i ich właściwości opisuje cechy mieszanin jednorodnych i niejednorodnych, klasyfikuje pierwiastki na metale i niemetale, posługuje
Chemia nieorganiczna. Copyright 2000 by Harcourt, Inc. All rights reserved.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Pierwiastki 1 1 H 3 Li 11
Realizacja wymagań szczegółowych podstawy programowej z chemii dla klasy siódmej szkoły podstawowej
 Realizacja wymagań szczegółowych podstawy programowej z chemii dla klasy siódmej szkoły podstawowej Nauczyciel: Marta Zielonka Temat w podręczniku Substancje i ich przemiany 1. Zasady bezpiecznej pracy
Realizacja wymagań szczegółowych podstawy programowej z chemii dla klasy siódmej szkoły podstawowej Nauczyciel: Marta Zielonka Temat w podręczniku Substancje i ich przemiany 1. Zasady bezpiecznej pracy
3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]
![3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u] 3. Jaka jest masa atomowa pierwiastka E w następujących związkach? Który to pierwiastek? EO o masie cząsteczkowej 28 [u]](/thumbs/58/41892324.jpg) 1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
1. Masa cząsteczkowa tlenku dwuwartościowego metalu wynosi 56 [u]. Masa atomowa tlenu wynosi 16 [u]. Ustal jaki to metal i podaj jego nazwę. Napisz wzór sumaryczny tego tlenku. 2. Ile razy masa atomowa
Realizacja wymagań szczegółowych podstawy programowej w poszczególnych tematach podręcznika Chemia Nowej Ery dla klasy siódmej szkoły podstawowej
 Realizacja wymagań szczegółowych podstawy programowej w poszczególnych tematach podręcznika Chemia Nowej Ery dla klasy siódmej szkoły podstawowej Temat w podręczniku Substancje i ich przemiany 1. Zasady
Realizacja wymagań szczegółowych podstawy programowej w poszczególnych tematach podręcznika Chemia Nowej Ery dla klasy siódmej szkoły podstawowej Temat w podręczniku Substancje i ich przemiany 1. Zasady
Chemia nieorganiczna. Pierwiastki. niemetale Be. 27 Co. 28 Ni. 26 Fe. 29 Cu. 45 Rh. 44 Ru. 47 Ag. 46 Pd. 78 Pt. 76 Os.
 Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
Chemia nieorganiczna 1. Układ okresowy metale i niemetale 2. Oddziaływania inter- i intramolekularne 3. Ciała stałe rodzaje sieci krystalicznych 4. Przewodnictwo ciał stałych Copyright 2000 by Harcourt,
CHEMIA. Wymagania szczegółowe. Wymagania ogólne
 CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA klasa 1 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 1 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Substancje i ich przemiany WYMAGANIA PODSTAWOWE stosuje zasady bezpieczeństwa
CHEMIA klasa 1 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Substancje i ich przemiany WYMAGANIA PODSTAWOWE stosuje zasady bezpieczeństwa
I Etap szkolny 16 listopada Imię i nazwisko ucznia: Arkusz zawiera 19 zadań. Liczba punktów możliwych do uzyskania: 39 pkt.
 XV Wojewódzki Konkurs z Chemii dla uczniów dotychczasowych gimnazjów oraz klas dotychczasowych gimnazjów prowadzonych w szkołach innego typu województwa świętokrzyskiego I Etap szkolny 16 listopada 2017
XV Wojewódzki Konkurs z Chemii dla uczniów dotychczasowych gimnazjów oraz klas dotychczasowych gimnazjów prowadzonych w szkołach innego typu województwa świętokrzyskiego I Etap szkolny 16 listopada 2017
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 POUFNE Pieczątka szkoły 16 styczeń 2010 r. Kod ucznia Wpisuje uczeń po otrzymaniu zadań Imię Wpisać po rozkodowaniu pracy Czas pracy 90 minut Nazwisko KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY
POUFNE Pieczątka szkoły 16 styczeń 2010 r. Kod ucznia Wpisuje uczeń po otrzymaniu zadań Imię Wpisać po rozkodowaniu pracy Czas pracy 90 minut Nazwisko KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY
Wykład 9 Wprowadzenie do krystalochemii
 Wykład 9 Wprowadzenie do krystalochemii 1. Krystalografia a krystalochemia. 2. Prawa krystalochemii 3. Sieć krystaliczna i pozycje atomów 4. Bliskie i dalekie uporządkowanie. 5. Kryształ a cząsteczka.
Wykład 9 Wprowadzenie do krystalochemii 1. Krystalografia a krystalochemia. 2. Prawa krystalochemii 3. Sieć krystaliczna i pozycje atomów 4. Bliskie i dalekie uporządkowanie. 5. Kryształ a cząsteczka.
DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY
 KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY 11 października 2012 Ważne informacje: 1. Masz 60 minut na rozwiązanie wszystkich 20 zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
KOD UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW I ETAP SZKOLNY 11 października 2012 Ważne informacje: 1. Masz 60 minut na rozwiązanie wszystkich 20 zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną
Na rysunku przedstawiono fragment układu okresowego pierwiastków.
 Na rysunku przedstawiono fragment układu okresowego pierwiastków. Zadanie 1 (0 1) W poniższych zdaniach podano informacje o pierwiastkach i ich tlenkach. Które to tlenki? Wybierz je spośród podanych A
Na rysunku przedstawiono fragment układu okresowego pierwiastków. Zadanie 1 (0 1) W poniższych zdaniach podano informacje o pierwiastkach i ich tlenkach. Które to tlenki? Wybierz je spośród podanych A
CHEMIA I GIMNAZJUM WYMAGANIA PODSTAWOWE
 WYMAGANIA PODSTAWOWE wskazuje w środowisku substancje chemiczne nazywa sprzęt i szkło laboratoryjne opisuje podstawowe właściwości substancji będących głównymi składnikami stosowanych na co dzień produktów
WYMAGANIA PODSTAWOWE wskazuje w środowisku substancje chemiczne nazywa sprzęt i szkło laboratoryjne opisuje podstawowe właściwości substancji będących głównymi składnikami stosowanych na co dzień produktów
Wymagania programowe na poszczególne oceny chemia kl. I
 I. Substancje i ich przemiany Wymagania programowe na poszczególne oceny chemia kl. I Ocena dopuszczająca [1] zalicza chemię do nauk przyrodniczych stosuje zasady bezpieczeństwa obowiązujące w pracowni
I. Substancje i ich przemiany Wymagania programowe na poszczególne oceny chemia kl. I Ocena dopuszczająca [1] zalicza chemię do nauk przyrodniczych stosuje zasady bezpieczeństwa obowiązujące w pracowni
Świat chemii cz. 1, rok szkolny 2016/17 Opis założonych osiągnięć ucznia
 Świat chemii cz. 1, rok szkolny 2016/17 Opis założonych osiągnięć ucznia Osiągnięcia podstawowe Rodzaje i przemiany materii wymienia powtarzające się elementy podręcznika i wskazuje rolę, jaką odgrywają;
Świat chemii cz. 1, rok szkolny 2016/17 Opis założonych osiągnięć ucznia Osiągnięcia podstawowe Rodzaje i przemiany materii wymienia powtarzające się elementy podręcznika i wskazuje rolę, jaką odgrywają;
Szczegółowy opis treści programowych obowiązujących na etapie szkolnym konkursu przedmiotowego z chemii 2018/2019
 Szczegółowy opis treści programowych obowiązujących na etapie szkolnym konkursu przedmiotowego z chemii 2018/2019 I. Eliminacje szkolne (60 minut, liczba punktów: 30). Wymagania szczegółowe. Cele kształcenia
Szczegółowy opis treści programowych obowiązujących na etapie szkolnym konkursu przedmiotowego z chemii 2018/2019 I. Eliminacje szkolne (60 minut, liczba punktów: 30). Wymagania szczegółowe. Cele kształcenia
WOJEWÓDZKI KONKURS PRZEDMIOTOWY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚLĄSKIEGO W ROKU SZKOLNYM 2015/2016 CHEMIA
 WOJEWÓDZKI KONKURS PRZEDMIOTOWY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚLĄSKIEGO W ROKU SZKOLNYM 2015/2016 CHEMIA Informacje dla ucznia 1. Na stronie tytułowej arkusza w wyznaczonym miejscu wpisz swój kod ustalony
WOJEWÓDZKI KONKURS PRZEDMIOTOWY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWA ŚLĄSKIEGO W ROKU SZKOLNYM 2015/2016 CHEMIA Informacje dla ucznia 1. Na stronie tytułowej arkusza w wyznaczonym miejscu wpisz swój kod ustalony
WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII
 KOD UCZNIA... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII Termin: 16.03. 2010 r. godz. 10 00 Czas pracy: 90 minut ETAP III Ilość punktów za rozwiązanie zadań Część I Część II Część III numer zadania numer
KOD UCZNIA... WOJEWÓDZKI KONKURS PRZEDMIOTOWY Z CHEMII Termin: 16.03. 2010 r. godz. 10 00 Czas pracy: 90 minut ETAP III Ilość punktów za rozwiązanie zadań Część I Część II Część III numer zadania numer
BADANIE WYNIKÓW NAUCZANIA Z CHEMII KLASA I GIMNAZJUM. PYTANIA ZAMKNIĘTE.
 BADANIE WYNIKÓW NAUCZANIA Z CHEMII KLASA I GIMNAZJUM. PYTANIA ZAMKNIĘTE. 1. Którą mieszaninę można rozdzielić na składniki poprzez filtrację; A. Wodę z octem. B. Wodę z kredą. C. Piasek z cukrem D. Wodę
BADANIE WYNIKÓW NAUCZANIA Z CHEMII KLASA I GIMNAZJUM. PYTANIA ZAMKNIĘTE. 1. Którą mieszaninę można rozdzielić na składniki poprzez filtrację; A. Wodę z octem. B. Wodę z kredą. C. Piasek z cukrem D. Wodę
Cel główny: Uczeń posiada umiejętność czytania tekstów kultury ze zrozumieniem
 Hospitacja diagnozująca Źródła informacji chemicznej Cel główny: Uczeń posiada umiejętność czytania tekstów kultury ze zrozumieniem Opracowała: mgr Lilla Zmuda Matyja Arkusz Hospitacji Diagnozującej nr
Hospitacja diagnozująca Źródła informacji chemicznej Cel główny: Uczeń posiada umiejętność czytania tekstów kultury ze zrozumieniem Opracowała: mgr Lilla Zmuda Matyja Arkusz Hospitacji Diagnozującej nr
KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 Kod ucznia Kod szkoły... pieczątka WKK Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP WOJEWÓDZKI Drogi Uczniu, witaj na II etapie konkursu chemicznego.
Kod ucznia Kod szkoły... pieczątka WKK Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS PRZEDMIOTOWY CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP WOJEWÓDZKI Drogi Uczniu, witaj na II etapie konkursu chemicznego.
uczeń opanował wszystkie wymagania podstawowe i ponadpodstawowe
 1 Agnieszka Wróbel nauczyciel biologii i chemii Plan pracy dydaktycznej na chemii w klasach pierwszych w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna uczeń nie opanował
1 Agnieszka Wróbel nauczyciel biologii i chemii Plan pracy dydaktycznej na chemii w klasach pierwszych w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna uczeń nie opanował
Wymagania edukacyjne na poszczególne śródroczne oceny klasyfikacyjne z przedmiotu chemia dla klasy 7 w r. szk. 2019/2020
 Wymagania edukacyjne na poszczególne śródroczne oceny klasyfikacyjne z przedmiotu chemia dla klasy 7 w r. szk. 209/2020 Ocenę niedostateczną otrzymuje uczeń, który nie opanował wymagań na ocenę dopuszczającą.
Wymagania edukacyjne na poszczególne śródroczne oceny klasyfikacyjne z przedmiotu chemia dla klasy 7 w r. szk. 209/2020 Ocenę niedostateczną otrzymuje uczeń, który nie opanował wymagań na ocenę dopuszczającą.
Chemia Grudzień Styczeń
 Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
Chemia Grudzień Styczeń Klasa VII IV. Łączenie się atomów. Równania reakcji chemicznych 1. Wiązania kowalencyjne 2. Wiązania jonowe 3. Wpływ rodzaju wiązania na właściwości substancji 4. Elektroujemność
Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami.
![Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami.](/thumbs/100/143872318.jpg) Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. I. Gęstość propanu w warunkach normalnych wynosi II. Jeżeli stężenie procentowe nasyconego roztworu pewnej
Zadanie 1. [ 3 pkt.] Uzupełnij zdania, wpisując brakującą informację z odpowiednimi jednostkami. I. Gęstość propanu w warunkach normalnych wynosi II. Jeżeli stężenie procentowe nasyconego roztworu pewnej
Elektronowa struktura atomu
 Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Elektronowa struktura atomu Model atomu Bohra oparty na teorii klasycznych oddziaływań elektrostatycznych Elektrony mogą przebywać tylko w określonych stanach, zwanych stacjonarnymi, o określonej energii
Inne koncepcje wiązań chemicznych. 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań?
 Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
Inne koncepcje wiązań chemicznych 1. Jak przewidywac strukturę cząsteczki? 2. Co to jest wiązanie? 3. Jakie są rodzaje wiązań? Model VSEPR wiązanie pary elektronowe dzielone między atomy tworzące wiązanie.
DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW II ETAP REJONOWY 16 listopada 2012 Ważne informacje: 1. Masz 90 minut na rozwiązanie wszystkich zadań. 2. W każdym zadaniu zaznacz kółkiem wybraną odpowiedź A, B,
Kryteria oceniania z chemii kl VII
 Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Okresowość właściwości chemicznych pierwiastków. Układ okresowy pierwiastków. 1. Konfiguracje elektronowe pierwiastków
 Układ okresowy pierwiastków Okresowość właściwości chemicznych pierwiastków 1. Konfiguracje elektronowe pierwiastków. Konfiguracje a układ okresowy 3. Budowa układu okresowego 4. Historyczny rozwój układu
Układ okresowy pierwiastków Okresowość właściwości chemicznych pierwiastków 1. Konfiguracje elektronowe pierwiastków. Konfiguracje a układ okresowy 3. Budowa układu okresowego 4. Historyczny rozwój układu
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
pieczątka WKK Kod ucznia - - Dzień Miesiąc Rok DATA URODZENIA UCZNIA KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP REJONOWY Drogi Uczniu, Witaj w drugim etapie konkursu chemicznego. Przeczytaj uważnie instrukcję
Wymagania programowe na poszczególne oceny z chemii w kl.1. I. Substancje i ich przemiany
 Wymagania programowe na poszczególne oceny z chemii w kl.1 I. Substancje i ich przemiany Ocena dopuszczająca [1] Ocena dostateczna [1 + 2] zalicza chemię do nauk przyrodniczych wyjaśnia, dlaczego chemia
Wymagania programowe na poszczególne oceny z chemii w kl.1 I. Substancje i ich przemiany Ocena dopuszczająca [1] Ocena dostateczna [1 + 2] zalicza chemię do nauk przyrodniczych wyjaśnia, dlaczego chemia
Wykaz ważniejszych symboli agadnienia ogólne Wstęp Zarys historii chemii analitycznej
 Spis rzeczy Z Wykaz ważniejszych symboli............................. 13 1. agadnienia ogólne................................. 15 1.1. Wstęp..................................... 15 1.. Zarys historii chemii
Spis rzeczy Z Wykaz ważniejszych symboli............................. 13 1. agadnienia ogólne................................. 15 1.1. Wstęp..................................... 15 1.. Zarys historii chemii
Układ okresowy pierwiastków chemicznych, budowa atomu. Na podstawie fragmentu układu okresowego pierwiastków odpowiedz na pytania:
 Układ okresowy pierwiastków chemicznych, budowa atomu zestaw I Na podstawie fragmentu układu okresowego pierwiastków odpowiedz na pytania: Zad 1 (0-1pkt)Wskaż nazwę pierwiastka, który leży w drugiej grupie
Układ okresowy pierwiastków chemicznych, budowa atomu zestaw I Na podstawie fragmentu układu okresowego pierwiastków odpowiedz na pytania: Zad 1 (0-1pkt)Wskaż nazwę pierwiastka, który leży w drugiej grupie
Budowa atomu Wiązania chemiczne
 strona 1/8 Budowa atomu Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu: jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
strona 1/8 Budowa atomu Wiązania chemiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Budowa atomu: jądro i elektrony, składniki jądra, izotopy. Promieniotwórczość i
MAŁOPOLSKI KONKURS CHEMICZNY
 Kod ucznia MAŁOPOLSKI KONKURS CHEMICZNY dla uczniów dotychczasowych gimnazjów i klas dotychczasowych gimnazjów prowadzonych w szkołach innego typu 8 października 2018 r. Etap I (szkolny) Wypełnia Szkolna
Kod ucznia MAŁOPOLSKI KONKURS CHEMICZNY dla uczniów dotychczasowych gimnazjów i klas dotychczasowych gimnazjów prowadzonych w szkołach innego typu 8 października 2018 r. Etap I (szkolny) Wypełnia Szkolna
Chemia I Semestr I (1 )
 1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
1/ 6 Inżyniera Materiałowa Chemia I Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr inż. Maciej Walewski. 2/ 6 Wykład Program 1. Atomy i cząsteczki: Materia, masa, energia. Cząstki elementarne. Atom,
Wiązania. w świetle teorii kwantów fenomenologicznie
 Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Wiązania w świetle teorii kwantów fenomenologicznie Wiązania Teoria kwantowa: zwiększenie gęstości prawdopodobieństwa znalezienia elektronów w przestrzeni pomiędzy atomami c a a c b b Liniowa kombinacja
Zagadnienia. Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I
 Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Nr zajęć Data Zagadnienia Budowa atomu a. rozmieszczenie elektronów na orbitalach Z = 1-40; I 9.10.2012. b. określenie liczby cząstek elementarnych na podstawie zapisu A z E, również dla jonów; c. określenie
Układ okresowy pierwiastków. Myślenie bez intuicji jest puste, intuicja bez myślenia jest ślepa. Albert Einstein
 Układ okresowy pierwiastków Myślenie bez intuicji jest puste, intuicja bez myślenia jest ślepa. Albert Einstein Spis treści Ważne pojęcia Trochę historii O ilu pierwiastkach wiemy Wygląd współczesnego
Układ okresowy pierwiastków Myślenie bez intuicji jest puste, intuicja bez myślenia jest ślepa. Albert Einstein Spis treści Ważne pojęcia Trochę historii O ilu pierwiastkach wiemy Wygląd współczesnego
Poziomy energetyczne powłok i podpowłok elektronowych pierwiastków
 Jeżeli zostało dowiedzione, że własności pierwiastków zależą od wartości liczby atomowej Z, to w kolejnym pytaniu możemy zapytać się w jaki sposób konfiguracja elektronowa pierwiastków decyduje o położeniu
Jeżeli zostało dowiedzione, że własności pierwiastków zależą od wartości liczby atomowej Z, to w kolejnym pytaniu możemy zapytać się w jaki sposób konfiguracja elektronowa pierwiastków decyduje o położeniu
PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM
 ... piecztka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uwanie instrukcj i
... piecztka nagłówkowa szkoły... kod pracy ucznia PRZEDMIOTOWY KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uwanie instrukcj i
UKŁAD OKRESOWY PIERWIASTKÓW
 UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
UKŁAD OKRESOWY PIERWIASTKÓW Michał Sędziwój (1566-1636) Alchemik Sędziwój - Jan Matejko Pierwiastki chemiczne p.n.e. Sb Sn Zn Pb Hg S Ag C Au Fe Cu (11)* do XVII w. As (1250 r.) P (1669 r.) (2) XVIII
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY
 suma uzyskanych punktów...... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie
suma uzyskanych punktów...... pieczątka nagłówkowa szkoły... kod pracy ucznia KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJUM ETAP SZKOLNY Drogi Uczniu, witaj na I etapie konkursu chemicznego. Przeczytaj uważnie
SCENARIUSZ ZAJĘĆ SZKOLNEGO KOŁA NAUKOWEGO Z PRZEDMIOTU CHEMIA PROWADZONEGO W RAMACH PROJEKTU AKADEMIA UCZNIOWSKA
 SCENARIUSZ ZAJĘĆ SZKOLNEGO KOŁA NAUKOWEGO Z PRZEDMIOTU CHEMIA PROWADZONEGO W RAMACH PROJEKTU AKADEMIA UCZNIOWSKA Temat lekcji Sprawdź swoją wiedzę i umiejętności! Substancje i ich właściwości oraz wewnętrzna
SCENARIUSZ ZAJĘĆ SZKOLNEGO KOŁA NAUKOWEGO Z PRZEDMIOTU CHEMIA PROWADZONEGO W RAMACH PROJEKTU AKADEMIA UCZNIOWSKA Temat lekcji Sprawdź swoją wiedzę i umiejętności! Substancje i ich właściwości oraz wewnętrzna
MARATON WIEDZY CHEMIA CZ. II
 MARATON WIEDZY CHEMIA CZ. II 1. Podaj liczbę elektronów, nukleonów, protonów i neuronów zawartych w następujących atomach: a), b) 2. Podaj liczbę elektronów, nukleonów, protonów i neutronów zawartych w
MARATON WIEDZY CHEMIA CZ. II 1. Podaj liczbę elektronów, nukleonów, protonów i neuronów zawartych w następujących atomach: a), b) 2. Podaj liczbę elektronów, nukleonów, protonów i neutronów zawartych w
XXIII Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych. Etap II. Poznań, Zadanie 1. Zadanie 2. Zadanie 3
 XXIII Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych Etap II Zadanie 1 Poniżej zaprezentowano schemat reakcji, którym ulegają związki manganu. Wszystkie reakcje (poza prażeniem) zachodzą w środowisku
XXIII Konkurs Chemiczny dla Uczniów Szkół Ponadgimnazjalnych Etap II Zadanie 1 Poniżej zaprezentowano schemat reakcji, którym ulegają związki manganu. Wszystkie reakcje (poza prażeniem) zachodzą w środowisku
Chemia nieorganiczna Semestr I (1 )
 1/ 5 Chemia Budowlana Chemia nieorganiczna Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr hab. inż. Jarosław Chojnacki. 2/ 5 Wykład 1. Pochodzenie i rozpowszechnienie pierwiastków we wszechświecie
1/ 5 Chemia Budowlana Chemia nieorganiczna Semestr I (1 ) Osoba odpowiedzialna za przedmiot: dr hab. inż. Jarosław Chojnacki. 2/ 5 Wykład 1. Pochodzenie i rozpowszechnienie pierwiastków we wszechświecie
Szkolny konkurs chemiczny Grupa B. Czas pracy 80 minut
 Szkolny konkurs chemiczny Grupa B Czas pracy 80 minut Piła 1 czerwca 2017 1 Zadanie 1. (0 3) Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie: elektrony rozmieszczone
Szkolny konkurs chemiczny Grupa B Czas pracy 80 minut Piła 1 czerwca 2017 1 Zadanie 1. (0 3) Z konfiguracji elektronowej atomu (w stanie podstawowym) pierwiastka X wynika, że w tym atomie: elektrony rozmieszczone
WYMAGANIA NA POSZCZEGÓLNE STOPNIE SZKOLNE Z CHEMII klasa I
 WYMAGANIA NA POSZCZEGÓLNE STOPNIE SZKOLNE Z CHEMII klasa I Aby uzyskać ocenę wyższą niż dana ocena, uczeń musi opanować wiadomości i umiejętności dotyczące danej oceny oraz ocen od niej niższych. Dział:
WYMAGANIA NA POSZCZEGÓLNE STOPNIE SZKOLNE Z CHEMII klasa I Aby uzyskać ocenę wyższą niż dana ocena, uczeń musi opanować wiadomości i umiejętności dotyczące danej oceny oraz ocen od niej niższych. Dział:
Wymagania programowe na poszczególne oceny
 Przedmiot: chemia Klasa: Ia, Ib Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny I. Substancje i ich przemiany Ocena dopuszczająca [1] zalicza chemię do nauk przyrodniczych stosuje zasady
Przedmiot: chemia Klasa: Ia, Ib Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny I. Substancje i ich przemiany Ocena dopuszczająca [1] zalicza chemię do nauk przyrodniczych stosuje zasady
Lista materiałów dydaktycznych dostępnych w Multitece Chemia Nowej Ery dla klasy 7
 Lista materiałów dydaktycznych dostępnych w Multitece Chemia Nowej Ery dla klasy 7 W tabeli zostały wyróżnione y z doświadczeń zalecanych do realizacji w szkole podstawowej. Temat w podręczniku Tytuł Typ
Lista materiałów dydaktycznych dostępnych w Multitece Chemia Nowej Ery dla klasy 7 W tabeli zostały wyróżnione y z doświadczeń zalecanych do realizacji w szkole podstawowej. Temat w podręczniku Tytuł Typ
Dział 1. Rodzaje i przemiany materii
 Dział 1. Rodzaje i przemiany materii podaje przykłady obecności chemii w swoim życiu; wymienia podstawowe narzędzia pracy chemika; zna i stosuje zasady bezpiecznej pracy w pracowni chemicznej; wie, na
Dział 1. Rodzaje i przemiany materii podaje przykłady obecności chemii w swoim życiu; wymienia podstawowe narzędzia pracy chemika; zna i stosuje zasady bezpiecznej pracy w pracowni chemicznej; wie, na
BUDOWA ATOMU. Pierwiastki chemiczne
 BUDOWA ATOMU Pierwiastki chemiczne p.n.e. Sb Sn n Pb Hg S Ag C Au Fe Cu ()* do XVII w. As (5 r.) P (669 r.) () XVIII w. N Cl Cr Co Y Mn Mo () Ni Pt Te O U H W XIX w. (m.in.) Na Ca Al Si F Cs Ba B Bi I
BUDOWA ATOMU Pierwiastki chemiczne p.n.e. Sb Sn n Pb Hg S Ag C Au Fe Cu ()* do XVII w. As (5 r.) P (669 r.) () XVIII w. N Cl Cr Co Y Mn Mo () Ni Pt Te O U H W XIX w. (m.in.) Na Ca Al Si F Cs Ba B Bi I
SCENARIUSZ LEKCJI CHEMII
 SCENARIUSZ LEKCJI CHEMII Temat: PIERWIASTKI, ICH NAZWY I SYMBOLE Wymagania podstawy programowej uczeń: I.9) posługuje się symbolami pierwiastków ( ): H, C, N, O, Na, Mg, Al, Si, P, S, Cl, K, Ca, Fe, Cu,
SCENARIUSZ LEKCJI CHEMII Temat: PIERWIASTKI, ICH NAZWY I SYMBOLE Wymagania podstawy programowej uczeń: I.9) posługuje się symbolami pierwiastków ( ): H, C, N, O, Na, Mg, Al, Si, P, S, Cl, K, Ca, Fe, Cu,
26 Okresowy układ pierwiastków
 26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
26 Okresowy układ pierwiastków Przyjmując procedurę Hartree ego otrzymujemy poziomy numerowane, jak w atomie wodoru, liczbami kwantowymi (n, l, m) z tym, że degeneracja ze względu na l na ogół już nie
