AN MicroPlate TM. Instrukcja użytkowania. Przeznaczenie: wyłącznie do celów badawczych
|
|
|
- Wiktor Krzemiński
- 6 lat temu
- Przeglądów:
Transkrypt
1 AN MicroPlate TM Instrukcja użytkowania Przeznaczenie: wyłącznie do celów badawczych Dystrybutor: BioMaxima S.A. Centrum Mikrobiologii Emapol ul. Budowlanych Gdańsk Tel.: lub (wewnętrzny 52 lub 51) Fax: office_emapol@biomaxima.com 1
2 PRZEZNACZENIE Mikropłytka AN umożliwia identyfikację szerokiego spektrum bakterii beztlenowych i mikroaerofilnych w oparciu o wyniki 95 różnych testów biochemicznych. Systemy Biolog - Microstation ID System lub OmniLog ID System - służą do odczytu i analizy wyników uzyskany przy użyciu płytek AN. OPIS PRODUKTU Rys. 1 Źródła węgla w poszczególnych studzienkach płytki AN. Charakterystyka bakterii przy użyciu płytek AN obejmuje 95 testów fenotypowych, opartych o metabolizm różnych źródeł węgla. Zdolność drobnoustrojów do metabolizowania poszczególnych źródeł węgla obecnych w studzienkach płytki AN określana jest na podstawie wyniku kolorymetrycznej reakcji redoks (zastosowany barwnik redoks to fiolet tetrazoliowy). Wszystkie niezbędne składniki odżywcze i biochemiczne opłaszczone są bezpośrednio w studzienkach 96-dołkowej płytki. Procedura wykonania oznaczenia jest szybka i prosta. Oznaczany szczep bakterii należy wyhodować na płytce Petriego z odpowiednim podłożem agarowym, po czym przygotować właściwej gęstości zawiesinę drobnoustroju w przeznaczonym do tego celu płynie do inokulacji (IF-AN). Następnie, zawiesina przenoszona jest na mikropłytkę AN (po 100 µl na studzienkę) i całość poddawana jest inkubacji (około godzinnej). Bezpośrednio po inokulacji wszystkie studzienki na płytce są bezbarwne. Jednakże w trakcie inkubacji, niektóre ze studzienek przyjmują barwę fioletową. Jest to spowodowane redukcją obecnego w studzienkach barwnika tetrazoliowego na skutek zachodzenia reakcji metabolicznych (sytuacja taka ma miejsce jeżeli drobnoustrój jest zdolny do metabolizowania zawartego w danej studzience źródła węgla). Studzienka A-1 nie zawierająca żadnego źródła węgla 2
3 stanowi kontrolę negatywną i nie powinna przyjmować zabarwienia fioletowego. Każdy identyfikowany drobnoustrój tworzy niepowtarzalny wzór, na który składają się układ i intensywność poszczególnych wybarwień. Porównanie przez system Biolog tego wzoru ze wzorcami w bazie danych stanowi ostatni etap procesu identyfikacji. ŚRODKI OSTROŻNOŚCI W celu uzyskania precyzyjnych i powtarzalnych wyników powinno się przestrzegać poniższych zaleceń: Przed przystąpieniem do pracy należy dokładnie przeczytać instrukcję użytkowania płytki AN i postępować zgodnie z opisanymi w niej procedurami. Do identyfikacji używamy wyłącznie czystych hodowli (tzw. monokultur). Opisywana technologia nie jest przystosowana do identyfikacji drobnoustrojów z kultur mieszanych. Zastosowane podłoża hodowlane i wielokrotne pasażowanie bakterii może mieć istotny wpływ na ostateczny wynik identyfikacji. Szczepy mogą prezentować odmienne cechy fenotypowe w zależności od tego, jak są one hodowane przed przystąpieniem do wykonania oznaczenia. Realizując poszczególne etapy procedury należy pamiętać o zasadach pracy w warunkach aseptycznych. Zaleca się używanie materiałów jednorazowego użytku np. do przygotowania zawiesiny bakterii, itp. Materiały wielorazowego użytku zawierają niekiedy śladowe ilości detergentów co może mieć negatywny wpływ na ostateczne wyniki identyfikacji. Płytki AN i płyn do inokulacji IF-AN należy przed użyciem ogrzać do temperatury pokojowej. Okresowa kalibracja turbidymetru jest wymagana, podobnie jak każdorazowe sprawdzanie prawidłowości jego wskazań. Co więcej, gęstości przygotowywanych zawiesin bakterii powinny zawsze odpowiadać zakresom wskazanym w odpowiednich procedurach. Płytki AN i płyn do inokulacji IF-AN zawierają substancje wrażliwe na działanie światła i temperatury. Dlatego też, należy je przechowywać w warunkach chłodniczych, w ciemności. Ciemnobrązowe studzienki na płytce AN mogą świadczyć o pogorszenie jej właściwości. Niektóre studzienki mogą mieć zabarwienie żółtawe lub różowe i tym faktem nie należy się przejmować. Opakowanie każdej płytki AN zawiera absorber tlenu. Prawidłowo zapakowana mikropłytka AN wygląda jakby była pakowana próżniowo. Nie należy używać płytki w przypadku stwierdzenia braku szczelności opakowania. Płytki należy przechowywać w temp. 2-8ºC. Nie używać płytek po upływie terminu ważności. Materiały zapewnione: Mikropłytki: Biolog AN MicroPlate (nr kat. 1007) - 10 sztuk w opakowaniu. Przy odbiorze zamówienia należy sprawdzić czy towar nie został uszkodzony podczas transportu. Płytki należy przechowywać w temp. 2-8ºC. Nie należy używać płytek po upływie terminu ważności (data ważności umieszczona jest na opakowaniu każdej płytki). Materiały nie zapewnione: Podłoża hodowlane: BUA (Biolog Universal Anaerobe) Agar, 500 g (nr kat ); BUA Agar + 5% krwi baraniej (BUA + B Agar) (podłoże na płytkach, nr kat ). 3
4 Krążki antybiotykowe: Kanamycyna 1 mg. Płyn do inokulacji: IF-AN w zakręcanej probówce (20 x 113 mm) (nr kat ). Każda probówka zawiera około 14-14,5 ml sterylnego płynu do inokulacji, przygotowanego w warunkach beztlenowych (skład: NaCl 0,40%; Pluronic F-68 0,03%; Gellan Gum 0,02%; NaHCO 3 0,084%; zieleń metylenowa 0,000075%; tioglikolan sodu 0,0015%; ph 7,0-7,2). Inokulatorz TM : Sterylne wymazówki Inokulatorz TM (20x50 - nr kat. 3321; 100x1 nr kat. 3323). Streakerz TM : Sterylne, jednorazowe patyczki do przenoszenia kolonii drobnoustrojów (10x100 - nr kat. 3025; 50x ). Jednorazowe pipety: nr kat Reservoirs: Sterylne, jednorazowe rynienki do przenoszenia zawiesiny drobnoustrojów przy użyciu pipety wielokanałowej (nr kat. 3102). Elektroniczny pipetor wielokanałowy: nr kat Końcówki do elektronicznego pipetora wielokanałowego: Sterylne końcówki w pudełku (nr kat. 3201). Turbidymetr: nr kat Standardy turbidymetryczne: AN (nr kat. 3427). Materiały potrzebne do prowadzenia hodowli drobnoustrojów i inkubacji płytki AN w warunkach beztlenowych. PROCEDURA Przygotowanie wstępne Przed przystąpieniem do wykonania oznaczenia należy doprowadzić mikropłytkę AN i probówki z płynem do inokulacji do temp. pokojowej (około 25ºC) oraz uważnie przeczytać instrukcję użytkowania. Krok 1: Przygotowanie hodowli badanego drobnoustrój na odpowiednim podłożu agarowym Przygotować świeżą hodowlę badanego drobnoustroju (wymagana monokultura) na podłożu rekomendowanym przez firmę Biolog (najlepiej BUA + B Agar) - temp. inkubacji to 26, 30 lub 35-37ºC; warunki beztlenowe. W celu uzyskania możliwie najlepszej izolacji należy dokonywać posiewu metodą redukcyjną. Do badania najlepiej użyć hodowli z drugiego pasażu. Krok 2: Przygotowanie i charakterystyka materiału do badań Wykonać barwienie metodą Grama, co pozwoli zakwalifikować drobnoustrój do jednej z czterech kategorii: Gram-ujemne ziarniaki, Gram-ujemne pałeczki, Gramdodatnie ziarniaki lub Gram-dodatnie pałeczki (taka kategoryzacja ułatwia proces identyfikacji poprzez ukierunkowanie przeszukiwania bazy danych). Drobnoustroje należy hodować w optymalnych dla nich warunkach. Zastosowane podłoże agarowe musi wspomagać wzrost i sprzyjać zachowaniu pełnej aktywności metabolicznej identyfikowanego gatunku. W większości przypadków, drobnoustroje identyfikowane przy użyciu płytki AN powinny być hodowane na podłożu agarowym BUA + B, w warunkach beztlenowych i w temp ºC. Tylko nieliczne gatunki mogą wymagać innej temp. inkubacji: np. 30ºC (Lactobacillus melefermentas, Pectinatus cerevisiiphilus i frisingensis, Tetragenococcus halophilus, Zymomonas 4
5 mobilis, Zymophilus raffinosivorans i paucivorans) lub 26ºC (Lactobacillus collinoides i hilgardii, Leuconostoc gelidum). Dla szybko rosnących Gram-ujemnych pałeczek należy wykonać test wrażliwości na kanamycynę (przy użyciu krążków antybiotykowych o zawartości kanamycyny 1mg). Do badań wykorzystujemy wyłącznie świeże hodowle (aktywność metaboliczna niektórych drobnoustrojów znacznie słabnie w stacjonarnej fazie wzrostu). Zalecany czas inkubacji to dla większości mikroorganizmów godzin. Jeżeli po 48 godzinach inkubacji nie uzyskujemy wystarczającego wzrostu drobnoustroju to należy przedłużyć inkubację o kolejne 24 godziny lub przesiać bakterie na kilka płytek z podłożem agarowym i inkubować godziny. Krok 3: Przygotowanie inokulum Należy sprawdzić czy płyn do inokulacji IF-AN nie zawiera tlenu. Płyn IF-AN powinien być bezbarwny. Jeśli przyjmuje on barwę zielono-niebieską nie należy go używać (jednym ze składników płynu IF-AN jest zieleń metylenowa. Jeżeli płyn nie zawiera tlenu, wówczas zieleń metylenowa pozostaje bezbarwna. Na skutek utlenienia wskaźnika płyn do inokulacji przyjmuje barwę zielono-niebieską). Należy okresowo kalibrować turbidymetr. W tym celu używać odpowiednich standardów turbidymetrycznych (85%T i 65%T) i postępować zgodnie z instrukcjami doręczonymi przez producenta aparatu. Przed każdym oznaczeniem należy wyzerować turbidymetr (ustawić pokrętło turbidymetru na 100%T) przy użyciu probówki zawierającej czysty płyn do inokulacji. Następnie, należy sprawdzić wskazania turbidymetru przy użyciu standardu AN turbidity standard (tę czynność można przeprowadzić jednorazowo, przed serią pomiarów wykonywanych danego dnia). Przed umieszczeniem w turbidymetrze probówkę należy oczyścić papierowym ręcznikiem z wszelkich zabrudzeń. UWAGA: probówki zawierające płyn do inokulacji nie są optycznie jednolite. A zatem, turbidymetr musi być wyzerowany dla każdej probówki z osobna. Podczas przygotowywania homogennej zawiesiny drobnoustroju trzeba pamiętać o zachowaniu warunków beztlenowych. Inokulacja większej ilości płytek AN wymaga przygotowania zawiesin w komorze beztlenowej. Jeżeli jednak planujemy inokulację zaledwie kilku mikropłytek (nie więcej niż 6), wówczas zawiesiny mogą zostać szybko przygotowane w warunkach tlenowych. Jednakże, wszystkie zawiesiny powinny zostać sporządzone w czasie nie przekraczającym 5 minut. Za pomocą sterylnej, bawełnianej wymazówki przenosimy kolonie identyfikowanego drobnoustroju do płynu inokulacyjnego (uważamy, aby nie przenieść podłoża agarowego, na którym hodowano drobnoustrój). Zawiesina musi być homogenna! (nie może zawierać pływających skupisk komórek. Wszelkie grudki i zlepki komórek należy rozetrzeć lub usunąć z płynu do inokulacji przy użyciu wymazówki. Można również nieco odczekać, aż większe fragmenty opadną na dno probówki). Po uzyskaniu homogennej zawiesiny, określamy jej gęstość używając w tym celu turbidymetru. Jeżeli gęstość zawiesiny jest zbyt mała niż podana w instrukcji użytkowania płytki AN należy pobrać więcej materiału, jeśli jest zbyt duża dodajemy odpowiednią ilość płynu do inokulacji. Krok 4: Inokulacja płytki AN Poniższe czynności należy wykonać w warunkach tlenowych, sprawnie i stosunkowo szybko: W przypadku opornych na kanamycynę, Gram-ujemnych, szybko rosnących pałeczek należy otworzyć opakowanie i pozostawić płytkę AN na 20 minut przed inokulacją 5
6 w warunkach tlenowych. Dla wszystkich pozostałych bakterii opakowanie zawierające płytkę AN można otworzyć dopiero wtedy, gdy zawiesina drobnoustroju jest już przygotowana (po otwarciu płytki należy dokonać jej inokulacji w czasie nie przekraczającym 5 minut). Należy odpowiednio oznakować (podpisać) płytkę. Wylać przygotowaną zawiesinę drobnoustroju do sterylnego pojemnika tak, aby można ją było bez problemu pobierać za pomocą pipety wielokanałowej. Nałożyć końcówki na automatyczny pipetor wielokanałowy firmy Biolog lub inny po czym pobrać zawiesinę. Przenieść do studzienek płytki AN po 100 µl zawiesiny (zrobić to w czasie nie dłuższym niż 5 minut). Należy uważać, aby nie przenosić opłaszczenia z jednej studzienki do drugiej oraz nie rozlewać zawiesiny pomiędzy studzienkami. Zaraz po przeniesieniu zawiesiny do studzienek przyjmie ona konsystencję żelową. Przykryć płytkę pokrywką. Pozostawić płytkę na minut w warunkach tlenowych. Krok 5: Inkubacja płytki AN Inkubować płytkę w warunkach beztlenowych (i bez obecności wodoru) przez okres godziny i w temp ºC (lub według potrzeb i wymagań danego drobnoustroju). Zalecane jest używanie jako wskaźnika atmosfery beztlenowej pasków zawierających resazurynę zamiast błękitu metylenowego. Nie inkubować płytek w standardowej komorze beztlenowej (niektóre bakterie beztlenowe wykazują aktywność hydrogenazową i mogą w obecności wodoru redukować barwnik tetrazoliowy zawarty we wszystkich studzienkach płytki AN). WYNIKI Odczyt i interpretacja wyników Mikropłytki AN odczytać przy użyciu oprogramowania MicroLog1, MicroLog2 lub MicroLog3. W tym celu należy postępować zgodnie z instrukcją podaną przez producenta. Do odczytu i interpretacji wyników nie potrzebne są żadne dodatkowe oprogramowania. Intensywne wybarwienie studzienki A-1, która stanowi kontrolę negatywną należy uznać za wynik fałszywie pozytywny. Z taką sytuacją możemy mieć do czynienia identyfikując kilka gatunków bakterii (np. z rodzajów: Actinomyces, Bacteroides oraz Propionibacterium). Zazwyczaj reakcje fałszywie pozytywne prezentują nieznaczny stopień zabarwienia. Nie stanowi to problemu o ile studzienki z reakcjami pozytywnymi przyjmują wyraźny, ciemnofioletowy kolor. Jeżeli jednak identyfikowany drobnoustrój generuje silne tło, co czyni niemożliwym odróżnienie reakcji pozytywnych od negatywnych, wówczas należy powtórzyć oznaczenie inokulując mikropłytkę AN po uprzedniej, 20 minutowej ekspozycji na powietrzu (tzn. w warunkach tlenowych; patrz krok 4) i tabela na str. 7). Większość identyfikowanych bakterii daje wyraźne, ciemnofioletowe reakcje pozytywne. Jednocześnie, w przypadku niektórych drobnoustrojów kolor tych reakcji może być nieco jaśniejszy (np. dla bakterii z rodzaju Clostridium, Eubacterium, Fusobacterium, Prevotella lub Porphyromonas). System poda wynik identyfikacji jeśli współczynnik prawdopodobieństwa SIM po godzinach inkubacji płytki AN osiągnie wartość minimum 0,50. 6
7 Wyjątki Podłoże hodowlane BUA + B Temperatura 35-37ºC 30 lub 26ºC Atmosfera beztlenowa (mikropłytki AN należy inkubować w atmosferze beztlenowej, nie zawierającej również wodoru) Płyn do inokulacji IF-AN Gęstość zawiesiny do inokulacji 65%T Ekspozycja płytek AN na powietrzu (w warunkach tlenowych) - krócej niż 5 minut w warunkach tlenowych tuż przed inokulacją płytki; minut w warunkach tlenowych po inokulacji płytki 20 minut w warunkach tlenowych przed inokulacją płytki w przypadku: a) opornych na kanamycynę, Gramujemnych, szybko rosnących pałeczek; b) szczepów generujących silne tło ( fałszywie pozytywne wybarwienie studzienek) Ilość zawiesiny drobnoustroju w jednej studzience płytki AN 100 ml Czas inkubacji godz. Tabela 1. Podsumowanie kluczowych parametrów wykonania oznaczenia przy użyciu płytki AN ROZWIĄZYWANIE PROBLEMÓW W przypadku jakichkolwiek problemów z wykonaniem oznaczenia należy dokładnie zapoznać się z niniejszą instrukcją postępowania i zweryfikować poprawność wykonania jej poszczególnych etapów. Jeżeli wszystkie studzienki w kolumnach są pozytywne (+) należy upewnić się, że: Inkubujemy płytki AN w warunkach beztlenowych i bez obecności wodoru (wiele bakterii beztlenowych posiada właściwości hydrogenazowe i będzie redukowało barwnik tetrazoliowy tworząc fioletowe zabarwienie studzienek w obecności wodoru). Nie przeniesiono żadnych substancji odżywczych do płynu do inokulacji (np. agaru przy pobieraniu kolonii bakterii). Przygotowana zawiesina bakterii jest homogenna. Gęstość przygotowanej zawiesiny drobnoustroju nie jest zbyt wysoka należy również sprawdzić prawidłowość działania turbidymetru. Studzienka A-1 zawiera odpowiednią ilość zawiesiny bakterii, czyli 100 µl. Płytka AN tuż po zainokulowaniu była poddana minutowej ekspozycji na powietrzu. Wykonano test oporności na kanamycynę dla szybko rosnących, Gram-ujemnych pałeczek. Jeżeli wszystkie studzienki są negatywne (-) należy upewnić się, że: 7
8 Płytka AN była przechowywana do momentu użycia w atmosferze beztlenowej (opakowanie płytki AN do momentu jej użycia pozostało szczelne). Używamy do badania świeżej hodowli bakterii i rekomendowanego podłoża hodowlanego. Temperatura i inne parametry inkubacji są odpowiednio dobrane do potrzeb badanego drobnoustroju. Płyn do inokulacji był właściwie przechowywany i ogrzany do temp. pokojowej przed użyciem. Należy również zwrócić uwagę, czy płyn do inokulacji przed otworzeniem probówki nie zawierał tlenu (nadający się do użycia roztwór IF-AN, zawierający jako indykator zieleń metylenową, powinien być bezbarwny). Używamy materiałów jednorazowego użytku (materiały wielorazowego użytku zawierają niekiedy resztki detergentów, które mogą działać toksycznie na bakterie). Gęstość przygotowanej zawiesiny drobnoustroju nie jest zbyt niska należy również sprawdzić prawidłowość działania turbidymetru. Studzienka A-1 zawiera odpowiednią ilość zawiesiny bakterii, czyli 100 µl. Płytka AN nie była wystawiona na działanie tlenu przez czas dłuższy niż 20 minut podczas całego procesu jej przygotowania do inkubacji. Płytka AN była inkubowana w warunkach beztlenowych. Kryteria skuteczności mikropłytki AN zostały określone poprzez utworzenie bazy danych w oparciu o testy na obszernej kolekcji mikroorganizmów z różnych źródeł. Baza danych została zaprojektowana tak, aby podawać wyniki identyfikacji wszystkich ujętych w niej gatunków zgodnie z obowiązującymi normami klasycznych metod identyfikacji i obecnej nomenklatury systematycznej. Aby uzyskać precyzyjne i powtarzalne wyniki wszystkie procedury oraz zalecenia zawarte w niniejszej instrukcji obsługi muszą być ściśle przestrzegane. OGRANICZENIA TESTU Płytka AN została zaprojektowana do identyfikacji czystych kultur bakterii beztlenowych i mikroaerofilnych, zawartych w aktualnej wersji bazy danych. Inne gatunki nie uzyskają prawidłowego wyniku identyfikacji (uzyskamy komunikat brak identyfikacji ). Nietypowe szczepy mogą również prezentować niski stopień podobieństwa do wzorca w bazie danych i dlatego zostaną one określone jako brak identyfikacji. Opisywany produkt może być wykorzystywany wyłącznie do celów badawczych. KONTROLA JAKOŚCI Wszystkie odczynniki firmy Biolog muszą spełnić wewnętrzne standardy kontroli jakości zanim zostaną dopuszczone do sprzedaży. Jednocześnie, każde laboratorium może samodzielnie dokonać kontroli jakości zakupionych materiałów. W tym celu należy wykonać oznaczenia używając wymienionych poniżej gatunków bakterii, stosując się do wytycznych instrukcji użytkowania płytki AN: Bifidobacterium breve ATCC Clostridium sordellii ATCC 9714 Lactobacillus casei ATCC 393 Micromonas micros ATCC Jeżeli używamy liofilizowanych lub uprzednio zamrożonych kultur bakterii należy je przed badaniem pasażować przynajmniej dwukrotnie. Po inkubacji (około godzinnej) należy odczytać wyniki, które powinny odpowiadać tożsamości szczepu wzorcowego użytego do 8
9 badania. Jeżeli wyniki identyfikacji nie są prawidłowe należy prześledzić procedurę badania, sprawdzić czystość szczepów i powtórzyć badanie. POMOC TECHNICZNA Dystrybutor: BioMaxima S.A. Centrum Mikrobiologii Emapol ul. Budowlanych Gdańsk Tel.: lub (wewnętrzny 52 lub 51) Fax: office_emapol@biomaxima.com REFERENCJE 1. Bochner, BR Sleuthing out Bacterial Identities. Nature 339: Bochner, BR Breathprints at the Microbial Level. ASM News 55: Biolog, Inc., US Patent # 5,627,045. OmniLog, MicroPlate, Streakerz oraz Inoculatorz to znaki towarowe firmy Biolog. 9
GEN III MicroPlate TM
 GEN III MicroPlate TM Instrukcja użytkowania Przeznaczenie: wyłącznie do celów badawczych Dystrybutor: BioMaxima S.A. Centrum Mikrobiologii Emapol ul. Budowlanych 68 80-298 Gdańsk Tel.: + 48 58 556 52
GEN III MicroPlate TM Instrukcja użytkowania Przeznaczenie: wyłącznie do celów badawczych Dystrybutor: BioMaxima S.A. Centrum Mikrobiologii Emapol ul. Budowlanych 68 80-298 Gdańsk Tel.: + 48 58 556 52
Identyfikacja mikroorganizmów systemem firmy Biolog
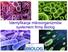 Identyfikacja mikroorganizmów systemem firmy Biolog Główne zalety systemu Ilość mikroorganizmów w bazie danych : Biolog ponad 2500 Vitek 2 ponad 330 Bez barwienia metodą Grama ( Vitek wymaga wstępnego
Identyfikacja mikroorganizmów systemem firmy Biolog Główne zalety systemu Ilość mikroorganizmów w bazie danych : Biolog ponad 2500 Vitek 2 ponad 330 Bez barwienia metodą Grama ( Vitek wymaga wstępnego
XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych. a. Candida albicans preparat z hodowli barwiony metoda Grama
 XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych a. Candida albicans preparat z hodowli barwiony metoda Grama Opis preparatu: b. Saccharomyces cerevisiae preparat z hodowli
XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych a. Candida albicans preparat z hodowli barwiony metoda Grama Opis preparatu: b. Saccharomyces cerevisiae preparat z hodowli
środowiskowych Henryk Różycki
 Fizjologiczny (metaboliczny) fingerprinting wykorzystanie systemu BIOLOG do identyfikacji bakterii oraz do charakterystyki mieszanych zespołów drobnoustrojów środowiskowych Henryk Różycki Zasada fingerprintingu
Fizjologiczny (metaboliczny) fingerprinting wykorzystanie systemu BIOLOG do identyfikacji bakterii oraz do charakterystyki mieszanych zespołów drobnoustrojów środowiskowych Henryk Różycki Zasada fingerprintingu
II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne. Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową
 II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową Zasada metody: Krążki bibułowe nasycone odpowiednimi ilościami antybiotyków
II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową Zasada metody: Krążki bibułowe nasycone odpowiednimi ilościami antybiotyków
XIX. Pałeczki Gram-ujemne część I - ćwiczenia praktyczne
 XIX. Pałeczki Gram-ujemne część I - ćwiczenia praktyczne Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
XIX. Pałeczki Gram-ujemne część I - ćwiczenia praktyczne Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
Hodowlą nazywamy masę drobnoustrojów wyrosłych na podłożu o dowolnej konsystencji.
 Wzrost mikroorganizmów rozumieć można jako: 1. Wzrost masy i rozmiarów pojedynczego osobnika, tj. komórki 2. Wzrost biomasy i liczebności komórek w środowisku, tj. wzrost liczebności populacji Hodowlą
Wzrost mikroorganizmów rozumieć można jako: 1. Wzrost masy i rozmiarów pojedynczego osobnika, tj. komórki 2. Wzrost biomasy i liczebności komórek w środowisku, tj. wzrost liczebności populacji Hodowlą
XIII. Staphylococcus, Micrococcus ćwiczenia praktyczne
 XIII. Staphylococcus, Micrococcus ćwiczenia praktyczne Ćwiczenie 1. Ocena wzrostu szczepów gronkowców na: a. agarze z dodatkiem 5% odwłóknionej krwi baraniej (AK) typ hemolizy morfologia kolonii.. b. podłożu
XIII. Staphylococcus, Micrococcus ćwiczenia praktyczne Ćwiczenie 1. Ocena wzrostu szczepów gronkowców na: a. agarze z dodatkiem 5% odwłóknionej krwi baraniej (AK) typ hemolizy morfologia kolonii.. b. podłożu
Nazwa i typ aparatu:.. Lp. Opis parametru Kryterium Parametr wymagany
 Załącznik nr 3. Aparat do detekcji wzrostu drobnoustrojów z krwi i płynów ustrojowych Parametry graniczne. Nazwa i typ aparatu:.. Lp. Opis parametru Kryterium Parametr wymagany Parametr oferowany 1 Hodowla
Załącznik nr 3. Aparat do detekcji wzrostu drobnoustrojów z krwi i płynów ustrojowych Parametry graniczne. Nazwa i typ aparatu:.. Lp. Opis parametru Kryterium Parametr wymagany Parametr oferowany 1 Hodowla
IV. Streptococcus, Enterococcus ćwiczenia praktyczne
 IV. Streptococcus, Enterococcus ćwiczenia praktyczne Ćwiczenie 1. Ocena wzrostu szczepów paciorkowców na: a. agarze z dodatkiem 5% odwłóknionej krwi baraniej (AK) typ hemolizy morfologia kolonii... gatunek
IV. Streptococcus, Enterococcus ćwiczenia praktyczne Ćwiczenie 1. Ocena wzrostu szczepów paciorkowców na: a. agarze z dodatkiem 5% odwłóknionej krwi baraniej (AK) typ hemolizy morfologia kolonii... gatunek
1. Demonstracja preparatów bakteryjnych barwionych metodą negatywną ukazujących kształty komórek bakteryjnych.
 Ćwiczenie 1. Mikrobiologia ogólna - Budowa komórki bakteryjnej. Metody barwienia preparatów bakteryjnych. Wzrost drobnoustrojów w warunkach laboratoryjnych. Uzyskiwanie czystej hodowli. Identyfikowanie
Ćwiczenie 1. Mikrobiologia ogólna - Budowa komórki bakteryjnej. Metody barwienia preparatów bakteryjnych. Wzrost drobnoustrojów w warunkach laboratoryjnych. Uzyskiwanie czystej hodowli. Identyfikowanie
ODPOWIEDZI NA PYTANIA
 Kraków, 11 września 2015r. wg rozdzielnika NR POSTĘPOWANIA: DZP.272-18/15 Przetarg nieograniczony pn. " Dostawa odczynników" ODPOWIEDZI NA PYTANIA działając na podstawie art. 38 ustawy z dn. 29 stycznia
Kraków, 11 września 2015r. wg rozdzielnika NR POSTĘPOWANIA: DZP.272-18/15 Przetarg nieograniczony pn. " Dostawa odczynników" ODPOWIEDZI NA PYTANIA działając na podstawie art. 38 ustawy z dn. 29 stycznia
E.coli Transformer Kit
 E.coli Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli. Metoda chemiczna. wersja 1117 6 x 40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników
E.coli Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli. Metoda chemiczna. wersja 1117 6 x 40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników
Dostawy
 Strona 1 z 5 Dostawy - 347310-2019 24/07/2019 S141 - - Dostawy - Dodatkowe informacje - Procedura otwarta I. II. VI. VII. Polska-Wałbrzych: Odczynniki laboratoryjne 2019/S 141-347310 Sprostowanie Ogłoszenie
Strona 1 z 5 Dostawy - 347310-2019 24/07/2019 S141 - - Dostawy - Dodatkowe informacje - Procedura otwarta I. II. VI. VII. Polska-Wałbrzych: Odczynniki laboratoryjne 2019/S 141-347310 Sprostowanie Ogłoszenie
Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku chemia kosmetyczna
 1 Zakład Mikrobiologii UJK Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku chemia kosmetyczna 2 Zakład Mikrobiologii UJK Zakres materiału (zagadnienia)
1 Zakład Mikrobiologii UJK Instrukcje do ćwiczeń oraz zakres materiału realizowanego na wykładach z przedmiotu Mikrobiologia na kierunku chemia kosmetyczna 2 Zakład Mikrobiologii UJK Zakres materiału (zagadnienia)
Ćwiczenie 1 Morfologia I fizjologia bakterii
 Ćwiczenie 1 Morfologia I fizjologia bakterii 1. Barwienie złożone - metoda Grama Przygotowanie preparatu: odtłuszczone szkiełko podstawowe, nałożenie bakterii ( z hodowli płynnej 1-2 oczka ezy lub ze stałej
Ćwiczenie 1 Morfologia I fizjologia bakterii 1. Barwienie złożone - metoda Grama Przygotowanie preparatu: odtłuszczone szkiełko podstawowe, nałożenie bakterii ( z hodowli płynnej 1-2 oczka ezy lub ze stałej
ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN
 ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN CZĘŚĆ TEORETYCZNA Mechanizmy promujące wzrost rośli (PGP) Metody badań PGP CZĘŚĆ PRAKTYCZNA 1. Mechanizmy promujące wzrost roślin. Odczyt. a) Wytwarzanie
ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN CZĘŚĆ TEORETYCZNA Mechanizmy promujące wzrost rośli (PGP) Metody badań PGP CZĘŚĆ PRAKTYCZNA 1. Mechanizmy promujące wzrost roślin. Odczyt. a) Wytwarzanie
VII. Pałeczki Gram-dodatnie: Corynebacterium, Listeria, Erysipelothtix, Lactobacillus - ćwiczenia praktyczne
 VII. Pałeczki Gram-dodatnie: Corynebacterium, Listeria, Erysipelothtix, Lactobacillus - ćwiczenia praktyczne Ćwiczenie 1. Wykonanie barwionych preparatów mikroskopowych preparat barwiony metodą Grama z
VII. Pałeczki Gram-dodatnie: Corynebacterium, Listeria, Erysipelothtix, Lactobacillus - ćwiczenia praktyczne Ćwiczenie 1. Wykonanie barwionych preparatów mikroskopowych preparat barwiony metodą Grama z
Ocena skuteczności procesów sterylizacji za pomocą wskaźników biologicznych r.
 Ocena skuteczności procesów sterylizacji za pomocą wskaźników biologicznych 27.04.2015 r. Wstęp Sterylizacja to proces, w wyniku którego zostają zniszczone lub usunięte wszystkie drobnoustroje, zarówno
Ocena skuteczności procesów sterylizacji za pomocą wskaźników biologicznych 27.04.2015 r. Wstęp Sterylizacja to proces, w wyniku którego zostają zniszczone lub usunięte wszystkie drobnoustroje, zarówno
Kontrola pożywek mikrobiologicznych. Sekcja Badań Epidemiologicznych
 Kontrola pożywek mikrobiologicznych Sekcja Badań Epidemiologicznych 27.04.2015 Zgodnie z ISO 17025 oraz ISO 15189 jednym z czynników istotnie wpływających na jakość wyników badań w przypadku badań mikrobiologicznych,
Kontrola pożywek mikrobiologicznych Sekcja Badań Epidemiologicznych 27.04.2015 Zgodnie z ISO 17025 oraz ISO 15189 jednym z czynników istotnie wpływających na jakość wyników badań w przypadku badań mikrobiologicznych,
E.coli Transformer Zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli
 E.coli Transformer Zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli Wersja 0211 6x40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników do przygotowania sześciu
E.coli Transformer Zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli Wersja 0211 6x40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników do przygotowania sześciu
fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 Sierpień 2018
 Sierpień 2018 fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP 957-07-05-191 KRS
Sierpień 2018 fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP 957-07-05-191 KRS
Saccharomyces Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Saccharomyces cerevisiae. Metoda chemiczna.
 Saccharomyces Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Saccharomyces cerevisiae. Metoda chemiczna. wersja 0916 6 x 20 transformacji Nr kat. 4010-120 Zestaw zawiera
Saccharomyces Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Saccharomyces cerevisiae. Metoda chemiczna. wersja 0916 6 x 20 transformacji Nr kat. 4010-120 Zestaw zawiera
Załącznik Nr 7 do SIWZ
 Załącznik Nr 7 do SIWZ Formularz asortymentowo - cenowy Nr 6 Pakiet Nr 6 Testy lateksowe, krążki antybiotykowe, testy MIC, szczepy wzorcowe, podłoża, odczynniki i testy diagnostyczne. Ilość Wartość Wielkość
Załącznik Nr 7 do SIWZ Formularz asortymentowo - cenowy Nr 6 Pakiet Nr 6 Testy lateksowe, krążki antybiotykowe, testy MIC, szczepy wzorcowe, podłoża, odczynniki i testy diagnostyczne. Ilość Wartość Wielkość
II. OZNACZANIE LICZBY BAKTERII Z GRUPY COLI I BAKTERII Z GRUPY COLI TYP FEKALNY METODĄ PŁYTKOWĄ W ŻYWNOŚCI I INNYCH PRODUKTACH wg PN-ISO 4832: 2007
 Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Temat: Żywność jako środowisko życia mikroorganizmów.
Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Temat: Żywność jako środowisko życia mikroorganizmów.
X. Pałeczki Gram-dodatnie. Rodzaje: Corynebacterium, Listeria, Erysipelothtix, Lactobacillus
 X. Pałeczki Gram-dodatnie. Rodzaje: Corynebacterium, Listeria, Erysipelothtix, Lactobacillus Gramujemne pałeczki auksotroficzne. Rodzaj: Haemophilus, Brucella, Legionella Ćwiczenie 1. Wykonanie preparatu
X. Pałeczki Gram-dodatnie. Rodzaje: Corynebacterium, Listeria, Erysipelothtix, Lactobacillus Gramujemne pałeczki auksotroficzne. Rodzaj: Haemophilus, Brucella, Legionella Ćwiczenie 1. Wykonanie preparatu
FORMULARZ ASORTYMENTOWO CENOWY załącznik nr 7
 załącznik nr 7 Pakiet. AUTOMATYCZNY SYSTEM DO IDENTYFIKACJI BAKTERII I GRZYBÓW DROŻDŻOPODOBNYCH ORAZ OZNACZANIA WRAŻLIWOŚCI NA ANTYBIOTYKI: DZIERŻAWA APARATU wraz z wyposażeniem + TESTY DIAGNOSTYCZNE TESTY
załącznik nr 7 Pakiet. AUTOMATYCZNY SYSTEM DO IDENTYFIKACJI BAKTERII I GRZYBÓW DROŻDŻOPODOBNYCH ORAZ OZNACZANIA WRAŻLIWOŚCI NA ANTYBIOTYKI: DZIERŻAWA APARATU wraz z wyposażeniem + TESTY DIAGNOSTYCZNE TESTY
GRUPA I Lp Nazwa Jm Ilość Cena jedn netto 1. Columbia agar z 5 %krwią baranią
 GRUPA I Lp Nazwa Jm Ilość Cena jedn netto 1. Columbia agar z 5 %krwią baranią 2. Agar Colubmia CNA 3. Podłoże chromogenne do posiewu moczu ze wstępną identyfikacją i oceną bakteriurii 4. Podłoże MaConkey
GRUPA I Lp Nazwa Jm Ilość Cena jedn netto 1. Columbia agar z 5 %krwią baranią 2. Agar Colubmia CNA 3. Podłoże chromogenne do posiewu moczu ze wstępną identyfikacją i oceną bakteriurii 4. Podłoże MaConkey
Identyfikacja nigdy nie była tak prosta
 Identyfikacja nigdy nie była tak prosta Od prostego wzoru wzoru do mikrobiologicznego odcisku palca Od prostej technologii do wielopłaszczyznowych systemów identyfikacji bakterii Biolog Unikalna technologia
Identyfikacja nigdy nie była tak prosta Od prostego wzoru wzoru do mikrobiologicznego odcisku palca Od prostej technologii do wielopłaszczyznowych systemów identyfikacji bakterii Biolog Unikalna technologia
RAPORT Z BADAŃ 164/Z/20110825/D/JOGA. Dostarczony materiał: próbki tworzyw sztucznych. Ilość próbek: 1. Rodzaj próbek: tworzywo
 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 164/Z/20110825/D/JOGA NAZWA I ADRES KLIENTA GROUND-Therm spółka z o.o. ul. Stepowa 30 44-105 Gliwice Tytuł zlecenia:
Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 164/Z/20110825/D/JOGA NAZWA I ADRES KLIENTA GROUND-Therm spółka z o.o. ul. Stepowa 30 44-105 Gliwice Tytuł zlecenia:
liczba godzin 2 MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA półpłynne stałe
 MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 6 i 7 6 Fizjologia drobnoustrojów Wymagania metaboliczne bakterii. Rodzaje podłóż mikrobiologicznych.
MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 6 i 7 6 Fizjologia drobnoustrojów Wymagania metaboliczne bakterii. Rodzaje podłóż mikrobiologicznych.
SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20006/11859/09
 SPRAWOZDANIE MOŻE BYĆ POWIELANE TYLKO W CAŁOŚCI. INNA FORMA KOPIOWANIA WYMAGA PISEMNEJ ZGODY LABORATORIUM. SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20006/11859/09 BADANIA WŁASNOŚCI PRZECIWDROBNOUSTROJOWYCH
SPRAWOZDANIE MOŻE BYĆ POWIELANE TYLKO W CAŁOŚCI. INNA FORMA KOPIOWANIA WYMAGA PISEMNEJ ZGODY LABORATORIUM. SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20006/11859/09 BADANIA WŁASNOŚCI PRZECIWDROBNOUSTROJOWYCH
SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20005/11858/09
 SPRAWOZDANIE MOŻE BYĆ POWIELANE TYLKO W CAŁOŚCI. INNA FORMA KOPIOWANIA WYMAGA PISEMNEJ ZGODY LABORATORIUM. SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20005/11858/09 BADANIA WŁASNOŚCI PRZECIWDROBNOUSTROJOWYCH
SPRAWOZDANIE MOŻE BYĆ POWIELANE TYLKO W CAŁOŚCI. INNA FORMA KOPIOWANIA WYMAGA PISEMNEJ ZGODY LABORATORIUM. SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20005/11858/09 BADANIA WŁASNOŚCI PRZECIWDROBNOUSTROJOWYCH
CZĘŚĆ 1 TEST KASETKOWY DO WYKRYWANIA KALPROTEKTYNY I LAKTOFERYNY W KALE. 73/PNP/SW/2018 Załącznik nr 1 do SIWZ formularz asortymentowo cenowy
 formularz asortymentowo cenowy CZĘŚĆ TEST KASETKOWY DO WYKRYWANIA KALPROTEKTYNY I LAKTOFERYNY W KALE Ilość sztuk na 36 za sztukę Immunochromatograficzny, nieinwazyjny szybki test do jakościowego wykrycia
formularz asortymentowo cenowy CZĘŚĆ TEST KASETKOWY DO WYKRYWANIA KALPROTEKTYNY I LAKTOFERYNY W KALE Ilość sztuk na 36 za sztukę Immunochromatograficzny, nieinwazyjny szybki test do jakościowego wykrycia
VIII. Pałeczki Gram-ujemne z rodziny Enterobacteriaceae
 VIII. Pałeczki Gram-ujemne z rodziny Enterobacteriaceae Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
VIII. Pałeczki Gram-ujemne z rodziny Enterobacteriaceae Ćwiczenie 1. Wykonanie preparatu mikroskopowego barwionego metodą Grama Opis preparatu: Ćwiczenie 2. Ocena wzrostu szczepów na podłożach stałych
SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA
 Załącznik nr 2 1 PAKIET NR II SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA Automatyczny analizator mikrobiologiczny do identyfikacji i oznaczania lekowrażliwości drobnoustrojów na antybiotyki z określeniem wartości
Załącznik nr 2 1 PAKIET NR II SZCZEGÓŁOWY OPIS PRZEDMIOTU ZAMÓWIENIA Automatyczny analizator mikrobiologiczny do identyfikacji i oznaczania lekowrażliwości drobnoustrojów na antybiotyki z określeniem wartości
RAPORT Z BADAŃ 01369/2015/D/AGST. Blirt S.A Gdańsk, ul. Trzy Lipy 3/1.38. Dział DNA-Gdańsk. Nr zlecenia
 Strona1/7 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 01369/2015/D/AGST NAZWA I ADRES KLIENTA Zenon Koszorz Ground-Therm Sp z o.o. Ul. Stepowa 30 44-105 Gliwice
Strona1/7 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 01369/2015/D/AGST NAZWA I ADRES KLIENTA Zenon Koszorz Ground-Therm Sp z o.o. Ul. Stepowa 30 44-105 Gliwice
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH
 Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
- podłoża transportowo wzrostowe..
 Ćw. nr 2 Klasyfikacja drobnoustrojów. Zasady pobierania materiałów do badania mikrobiologicznego. 1. Obejrzyj zestawy do pobierania materiałów i wpisz jakie materiały pobieramy na: - wymazówki suche. -
Ćw. nr 2 Klasyfikacja drobnoustrojów. Zasady pobierania materiałów do badania mikrobiologicznego. 1. Obejrzyj zestawy do pobierania materiałów i wpisz jakie materiały pobieramy na: - wymazówki suche. -
Badania mikrobiologiczne wg PN-EN ISO 11737
 Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
Ćwiczenie 4-5 Mikrobiologiczne kryteria oceny sanitarnej wody
 ĆWICZENIA Z GOSPODARKI ENERGETYCZNEJ, WODNEJ I ŚCIEKOWEJ CZĘŚĆ MIKROBIOLOGICZNA Ćwiczenie 4-5 Mikrobiologiczne kryteria oceny sanitarnej wody Część teoretyczna: 1. Kryteria jakości sanitarnej wody przeznaczonej
ĆWICZENIA Z GOSPODARKI ENERGETYCZNEJ, WODNEJ I ŚCIEKOWEJ CZĘŚĆ MIKROBIOLOGICZNA Ćwiczenie 4-5 Mikrobiologiczne kryteria oceny sanitarnej wody Część teoretyczna: 1. Kryteria jakości sanitarnej wody przeznaczonej
1276:1997 13368 (ATCC
 Działanie bakteriobójcze Środka biobójczego Clinell GAMA Healthcare Ltd. zbadane za pomocą Europejskiego Standardowego Testu według normy BS EN 1276:1997 wobec: Klebsiella pneumoniae NCTC 13368 (ATCC 700603).
Działanie bakteriobójcze Środka biobójczego Clinell GAMA Healthcare Ltd. zbadane za pomocą Europejskiego Standardowego Testu według normy BS EN 1276:1997 wobec: Klebsiella pneumoniae NCTC 13368 (ATCC 700603).
Protokoły do zajęć praktycznych z mikrobiologii ogólnej i żywności dla studentów kierunku: Dietetyka
 Protokoły do zajęć praktycznych z mikrobiologii ogólnej i żywności dla studentów kierunku: Dietetyka Protokół I, zajęcia praktyczne 1. Demonstracja wykonania preparatu barwionego metodą Grama (wykonuje
Protokoły do zajęć praktycznych z mikrobiologii ogólnej i żywności dla studentów kierunku: Dietetyka Protokół I, zajęcia praktyczne 1. Demonstracja wykonania preparatu barwionego metodą Grama (wykonuje
Staphylococcus ćwiczenia praktyczne. a. agarze z dodatkiem 5% odwłóknionej krwi baraniej (AK)
 VII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia skóry i tkanek miękkich. Drobnoustroje z rodzajów Staphylococcus, Streptococcus, Enterococcus Staphylococcus ćwiczenia
VII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia skóry i tkanek miękkich. Drobnoustroje z rodzajów Staphylococcus, Streptococcus, Enterococcus Staphylococcus ćwiczenia
Interpretacja wyników analiz ilości i obecności drobnoustrojów zgodnie z zasadami badań mikrobiologicznych żywności i pasz?
 Wydział Biotechnologii i Nauk o Żywności Seminarium STC 2018 Interpretacja wyników analiz ilości i obecności drobnoustrojów zgodnie z zasadami badań mikrobiologicznych żywności i pasz? Dr inż. Agnieszka
Wydział Biotechnologii i Nauk o Żywności Seminarium STC 2018 Interpretacja wyników analiz ilości i obecności drobnoustrojów zgodnie z zasadami badań mikrobiologicznych żywności i pasz? Dr inż. Agnieszka
ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW
 UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW dla studentów I roku II 0 biotechnologii medycznej
UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW dla studentów I roku II 0 biotechnologii medycznej
AmpliTest GMO screening-nos (Real Time PCR)
 AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
Testy aktywności przeciwdrobnoustrojowej na przykładzie metody dyfuzyjnej oraz wyznaczania wartości minimalnego stężenia hamującego wzrost.
 Testy aktywności przeciwdrobnoustrojowej na przykładzie metody dyfuzyjnej oraz wyznaczania wartości minimalnego stężenia hamującego wzrost. Opracowanie: dr inż. Roland Wakieć Wprowadzenie. Najważniejszym
Testy aktywności przeciwdrobnoustrojowej na przykładzie metody dyfuzyjnej oraz wyznaczania wartości minimalnego stężenia hamującego wzrost. Opracowanie: dr inż. Roland Wakieć Wprowadzenie. Najważniejszym
INSTRUKCJA UŻYTKOWANIA
 INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
QMS Quality in Microbiology Scheme Wydanie 14 Data wydania: czerwiec 2018
 Przyjęcie i przechowywanie Po otrzymaniu materiału do badań należy zapisać datę otrzymania, a następnie przechowywać w lodówce w temperaturze 2-8 º C do momentu przeprowadzenia badania. Materiał do badań
Przyjęcie i przechowywanie Po otrzymaniu materiału do badań należy zapisać datę otrzymania, a następnie przechowywać w lodówce w temperaturze 2-8 º C do momentu przeprowadzenia badania. Materiał do badań
INSTRUKCJA UŻYTKOWANIA
 INSTRUKCJA UŻYTKOWANIA EZ-Hydro Shot Microorganisms PRZEZNACZENIE EZ-Hydro Shot są liofilizowanymi, preparatami ilościowymi mikroorganizmów w laboratoriach przemysłowych, służące do kontroli jakości. Te
INSTRUKCJA UŻYTKOWANIA EZ-Hydro Shot Microorganisms PRZEZNACZENIE EZ-Hydro Shot są liofilizowanymi, preparatami ilościowymi mikroorganizmów w laboratoriach przemysłowych, służące do kontroli jakości. Te
Przygotowanie mianowanych zawiesin szczepów wzorcowych znajdujących zastosowanie w badaniach mikrobiologicznych
 Przygotowanie mianowanych zawiesin szczepów wzorcowych znajdujących zastosowanie w badaniach mikrobiologicznych Krystyna Mysłowska, Katarzyna Bucała-Śladowska* Mikrobiologia jest nauką, w której nie mamy
Przygotowanie mianowanych zawiesin szczepów wzorcowych znajdujących zastosowanie w badaniach mikrobiologicznych Krystyna Mysłowska, Katarzyna Bucała-Śladowska* Mikrobiologia jest nauką, w której nie mamy
AmpliTest Salmonella spp. (Real Time PCR)
 AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
Zestaw do wykrywania Chlamydia trachomatis w moczu lub w kulturach komórkowych
 Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
Przedmiot zamówienia -Specyfikacja cenowa
 Przedmiot zamówienia -Specyfikacja cenowa Zał nr 1 do SIWZ Grupa 1: gotowe podłoża, testy i odczynniki Podłoża na płytkach petriego o średnicy 90 mm, podłoża w probówkach,testy i odczynniki mikrobiologiczne
Przedmiot zamówienia -Specyfikacja cenowa Zał nr 1 do SIWZ Grupa 1: gotowe podłoża, testy i odczynniki Podłoża na płytkach petriego o średnicy 90 mm, podłoża w probówkach,testy i odczynniki mikrobiologiczne
7/PNP/SW/2015 Załącznik nr 1 do SIWZ
 Część nr Testy do identyfikacji paciorkowców Testy łączne do automatycznej identyfikacji oraz oznaczania lekowrażliwości paciorkowców, w tym pneumokoków na jednym module testowym. Analiza wykonywana na
Część nr Testy do identyfikacji paciorkowców Testy łączne do automatycznej identyfikacji oraz oznaczania lekowrażliwości paciorkowców, w tym pneumokoków na jednym module testowym. Analiza wykonywana na
SZCZEGÓŁOWY FORMULARZ OFERTY - Pakiet nr 3
 SZCZEGÓŁOWY FORMULARZ OFERTY - Pakiet nr 3 Część I Lp. Przedmiot zamówienia: Ilość zamawiana Wielkość opakowania Ilość opakowania cena brutto za 1 opakowanie Gotowe podłoża na płytkach Petriego Ø 90mm
SZCZEGÓŁOWY FORMULARZ OFERTY - Pakiet nr 3 Część I Lp. Przedmiot zamówienia: Ilość zamawiana Wielkość opakowania Ilość opakowania cena brutto za 1 opakowanie Gotowe podłoża na płytkach Petriego Ø 90mm
Systemy Biolog mające zastosowanie w:
 Systemy Biolog mające zastosowanie w: IDENTYFIKACJI MIKROORGANIZMÓW - wprowadzona przez amerykaoską firmę Biolog, unikalna technologia systemów Biolog umożliwia dokładną identyfikację bakterii i grzybów
Systemy Biolog mające zastosowanie w: IDENTYFIKACJI MIKROORGANIZMÓW - wprowadzona przez amerykaoską firmę Biolog, unikalna technologia systemów Biolog umożliwia dokładną identyfikację bakterii i grzybów
X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria
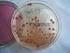 X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria Maczugowce (rodzaj Corynebacterium) Ćwiczenie 1. Wykonanie preparatu
X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria Maczugowce (rodzaj Corynebacterium) Ćwiczenie 1. Wykonanie preparatu
szt op. 12 op. 6
 ZAŁĄCZNIK NR 1A.11 DO SIWZ. Pieczęć nagłówkowa Data... OPIS PRZEDMIOTU ZAMÓWIENIA ARKUSZ KALKULACYJNY OKREŚLAJĄCY CENĘ OFERTY Część nr 11 Odczynniki chemiczne i materiały zużywalne do oznaczania ilości
ZAŁĄCZNIK NR 1A.11 DO SIWZ. Pieczęć nagłówkowa Data... OPIS PRZEDMIOTU ZAMÓWIENIA ARKUSZ KALKULACYJNY OKREŚLAJĄCY CENĘ OFERTY Część nr 11 Odczynniki chemiczne i materiały zużywalne do oznaczania ilości
CZĘŚĆ 1 TEST KASETKOWY DO WYKRYWANIA KALPROTEKTYNY I LAKTOFERYNY W KALE. 53/PNP/SW/2018 Załącznik nr 1 do SIWZ formularz asortymentowo cenowy
 CZĘŚĆ TEST KASETKOWY DO WYKRYWANIA KALPROTEKTYNY I LAKTOFERYNY W KALE sztuk na 6 Nr katal Producent pojedynczego oznaczenia Immunochromatograficzny, nieinwazyjny szybki test do jakościowego wykrycia kalprotektyny
CZĘŚĆ TEST KASETKOWY DO WYKRYWANIA KALPROTEKTYNY I LAKTOFERYNY W KALE sztuk na 6 Nr katal Producent pojedynczego oznaczenia Immunochromatograficzny, nieinwazyjny szybki test do jakościowego wykrycia kalprotektyny
Lista produktów. Testy Ames-, UmuC-, YES/YAS i akcesoria
 Lista produktów Ames MPF, Ames II, UmuC, YES/YAS Strona 1/11 Lista produktów Testy Ames-, UmuC-, YES/YAS i akcesoria Obowiązuje od 01.01.2015. Wersja 260115 1999 TIGRET Sp. z o.o. ul. Warszawska 27 02-495
Lista produktów Ames MPF, Ames II, UmuC, YES/YAS Strona 1/11 Lista produktów Testy Ames-, UmuC-, YES/YAS i akcesoria Obowiązuje od 01.01.2015. Wersja 260115 1999 TIGRET Sp. z o.o. ul. Warszawska 27 02-495
III. Fizjologia bakterii i zasady diagnostyki bakteriologicznej
 III. Fizjologia bakterii i zasady diagnostyki bakteriologicznej Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej
III. Fizjologia bakterii i zasady diagnostyki bakteriologicznej Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej
OSTRACODTOXKIT F Procedura testu
 OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej
 VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej Pałeczki Gram-ujemne niefermentujące Ćwiczenie 1. Wykonanie i ocena preparatu
VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej Pałeczki Gram-ujemne niefermentujące Ćwiczenie 1. Wykonanie i ocena preparatu
ALGALTOXKIT F Procedura testu
 ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
AE/ZP-27-49/14 Załącznik Nr 6
 AE/ZP-27-49/14 Załącznik Nr 6 Wymagania dla przedmiotu zamówienia oferowanego w Pakietach Nr: 1 7 L.p. Wymagane parametry dla: Wpisać oferowane parametry Wymagania wobec przedmiotu zmówienia oferowanego
AE/ZP-27-49/14 Załącznik Nr 6 Wymagania dla przedmiotu zamówienia oferowanego w Pakietach Nr: 1 7 L.p. Wymagane parametry dla: Wpisać oferowane parametry Wymagania wobec przedmiotu zmówienia oferowanego
AmpliTest Chlamydia/Chlamydophila (Real Time PCR)
 AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
Arkusz1. Nazwa artykułu opakowanie ilość opak. 1 Agar Columbia + 5% krew barania 20 płytek* 205
 Nazwa artykułu opakowanie ilość opak. 1 Agar Columbia + 5% krew barania 20 płytek* 205 Agar czekoladowy + suplement antybiotykowy + czynniki wzrostowe dla Haemophilus 2 20 płytek 60 Torebki do hodowli
Nazwa artykułu opakowanie ilość opak. 1 Agar Columbia + 5% krew barania 20 płytek* 205 Agar czekoladowy + suplement antybiotykowy + czynniki wzrostowe dla Haemophilus 2 20 płytek 60 Torebki do hodowli
Ćwiczenie 8, 9, 10 Kontrola mikrobiologiczna środowiska pracy
 MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 8, 9, 10 Kontrola mikrobiologiczna środowiska pracy liczba godzin 8 Badanie mikrobiologicznej czystości
MIKROBIOLOGIA KOSMETOLOGICZNA dla studentów II roku, studiów I st. kierunku KOSMETOLOGIA Ćwiczenie 8, 9, 10 Kontrola mikrobiologiczna środowiska pracy liczba godzin 8 Badanie mikrobiologicznej czystości
ZASADY BADAŃ BAKTERIOLOGICZNYCH
 ZASADY BADAŃ BAKTERIOLOGICZNYCH Joanna Kądzielska Katedra Mikrobiologii Lekarskiej Warszawski Uniwersytet Medyczny METODY HODOWLI BAKTERII METODY MIKROSKOPOWE MORFOLOGIA BAKTERII TOK BADANIA DIAGNOSTYCZNEGO
ZASADY BADAŃ BAKTERIOLOGICZNYCH Joanna Kądzielska Katedra Mikrobiologii Lekarskiej Warszawski Uniwersytet Medyczny METODY HODOWLI BAKTERII METODY MIKROSKOPOWE MORFOLOGIA BAKTERII TOK BADANIA DIAGNOSTYCZNEGO
woda do 1000 ml ph=6,9-7,1. Po sterylizacji dodać nystatynę (końcowe stężenie ok. 50 μg/ml). Agar z wyciągiem glebowym i ekstraktem drożdżowym (YS)
 Ćwiczenie 1, 2, 3, 4 Skrining ze środowiska naturalnego: selekcja promieniowców zdolnych do produkcji antybiotyków. Testowanie zdolności do syntezy antybiotyków przez wyselekcjonowane szczepy promieniowców
Ćwiczenie 1, 2, 3, 4 Skrining ze środowiska naturalnego: selekcja promieniowców zdolnych do produkcji antybiotyków. Testowanie zdolności do syntezy antybiotyków przez wyselekcjonowane szczepy promieniowców
1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań
 Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Pracowni Diagnostycznej Laboratorium Zakładu Badania Wirusów Grypy (obowiązuje
Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Pracowni Diagnostycznej Laboratorium Zakładu Badania Wirusów Grypy (obowiązuje
Do jednego litra medium dodać 10,0 g skrobi ziemniaczanej lub kukurydzianej i mieszać do uzyskania zawiesiny. Sterylizować w autoklawie.
 Ćwiczenie 3. Izolacja laseczek przetrwalnikujących z gleby Cel ćwiczenia: Izolacja i testowanie przydatności biotechnologicznej laseczek z rodzaju Bacillus występujących w glebie. Odczynniki i podłoża:
Ćwiczenie 3. Izolacja laseczek przetrwalnikujących z gleby Cel ćwiczenia: Izolacja i testowanie przydatności biotechnologicznej laseczek z rodzaju Bacillus występujących w glebie. Odczynniki i podłoża:
szt 5400 szt 1500 szt 2500 szt 4000 szt 1500 szt 400 szt 2000 szt 600 szt 500 szt 3000 szt 200
 Dodatek nr. 2 do SIWZ - asortymentowo-cenowy Gotowe podłoża bakteriologiczne na płytkach. Wszystkie podłoża muszą pochodzić od producentów posiadających certyfikat jakości ISO 13485:2003 lub równoważny,
Dodatek nr. 2 do SIWZ - asortymentowo-cenowy Gotowe podłoża bakteriologiczne na płytkach. Wszystkie podłoża muszą pochodzić od producentów posiadających certyfikat jakości ISO 13485:2003 lub równoważny,
Zadanie 1-odczynniki do identyfikacji i oznaczania lekworażliwości oraz odczynniki do posiewów krwi i płynów ustrojowych
 Zadanie 1-odczynniki do identyfikacji i oznaczania lekworażliwości oraz odczynniki do posiewów krwi i płynów ustrojowych Liczba testów w Przewidywana liczba Nr pozycji Asortyment opak opakowań 01 testy
Zadanie 1-odczynniki do identyfikacji i oznaczania lekworażliwości oraz odczynniki do posiewów krwi i płynów ustrojowych Liczba testów w Przewidywana liczba Nr pozycji Asortyment opak opakowań 01 testy
ZAŁĄCZNIK NR 1. Cena jedn. brutto. netto
 PAKIET NR 1 Odczynniki hematologiczne do aparatu ABX MICROS 60 Lp. Nazwa/postać/stężenie Opakowanie Ilość do 1. Roztwór roboczy ( diluent) /8-866/ 1 opakowanie 7 = 20 l. 2. Roztwór roboczy ( diluent) /8-866/
PAKIET NR 1 Odczynniki hematologiczne do aparatu ABX MICROS 60 Lp. Nazwa/postać/stężenie Opakowanie Ilość do 1. Roztwór roboczy ( diluent) /8-866/ 1 opakowanie 7 = 20 l. 2. Roztwór roboczy ( diluent) /8-866/
Załącznik nr 1 do SIWZ Pakiet nr 3 Formularz Szczegółowy Oferty. Oznaczenie postępowania: DA.ZP PAKIET NR 3
 Załącznik nr 1 do SIWZ Pakiet nr 3 Formularz Szczegółowy Oferty Oznaczenie postępowania: DA.ZP.242.68.2017 PAKIET NR 3 Gotowe podłoża na płytkach Petriego wraz z dzierżawą szafy chłodniczej CZĘŚĆ A: GOTOWE
Załącznik nr 1 do SIWZ Pakiet nr 3 Formularz Szczegółowy Oferty Oznaczenie postępowania: DA.ZP.242.68.2017 PAKIET NR 3 Gotowe podłoża na płytkach Petriego wraz z dzierżawą szafy chłodniczej CZĘŚĆ A: GOTOWE
AmpliTest Babesia spp. (PCR)
 AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
PRAKTYCZNY KURS SZKOLENIOWY OCENY MUTAGENNOŚCI WODY WYKONANY TESTEM MIKROPŁYTKOWYM AMES MPF 98/100 AQUA
 1999 PRAKTYCZNY KURS SZKOLENIOWY OCENY MUTAGENNOŚCI WODY WYKONANY TESTEM MIKROPŁYTKOWYM AMES MPF 98/100 AQUA organizowany przez TIGRET Sp. z o.o. pod patronatem naukowym Warszawskiego Uniwersytetu Medycznego,
1999 PRAKTYCZNY KURS SZKOLENIOWY OCENY MUTAGENNOŚCI WODY WYKONANY TESTEM MIKROPŁYTKOWYM AMES MPF 98/100 AQUA organizowany przez TIGRET Sp. z o.o. pod patronatem naukowym Warszawskiego Uniwersytetu Medycznego,
mgr Sławomir Sułowicz Katedra Mikrobiologii UŚ
 mgr Sławomir Sułowicz Katedra Mikrobiologii UŚ 1) Analiza sanitarna wody 2) Analiza mikrobiologiczna gleby 3) Analiza sanitarna powietrza 4) Charakterystyka szczepów bakterii opornych na antybiotyki, wyizolowanych
mgr Sławomir Sułowicz Katedra Mikrobiologii UŚ 1) Analiza sanitarna wody 2) Analiza mikrobiologiczna gleby 3) Analiza sanitarna powietrza 4) Charakterystyka szczepów bakterii opornych na antybiotyki, wyizolowanych
INSTRUKCJA OBSŁUGI. Drobnoustroje Epower PRZEZNACZENIE POSTAĆ I SKŁADNIKI SPECYFIKACJA I DZIAŁANIE
 INSTRUKCJA OBSŁUGI Drobnoustroje Epower PRZEZNACZENIE Drobnoustroje Epower to liofilizowane, ilościowe preparaty drobnoustrojów do stosowania w laboratoriach przemysłowych dla celów kontroli jakości. Certyfikowany
INSTRUKCJA OBSŁUGI Drobnoustroje Epower PRZEZNACZENIE Drobnoustroje Epower to liofilizowane, ilościowe preparaty drobnoustrojów do stosowania w laboratoriach przemysłowych dla celów kontroli jakości. Certyfikowany
INSTRUKCJA OBSŁUGI. Certyfikowany materiał referencyjny Epower PRZEZNACZENIE PODSUMOWANIE I HISTORIA POSTAĆ I SKŁADNIKI
 INSTRUKCJA OBSŁUGI Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny (CRM) Epower to liofilizowane, ilościowe preparaty drobnoustrojów do stosowania w laboratoriach
INSTRUKCJA OBSŁUGI Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny (CRM) Epower to liofilizowane, ilościowe preparaty drobnoustrojów do stosowania w laboratoriach
1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań
 Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Laboratorium Zakładu Badania Wirusów Grypy, Krajowy Ośrodek ds. Grypy (obowiązuje
Zalecenia dotyczące pobierania, przechowywania i transportu materiałów klinicznych przeznaczonych do badań diagnostycznych w Laboratorium Zakładu Badania Wirusów Grypy, Krajowy Ośrodek ds. Grypy (obowiązuje
Temat ćwiczenia: Techniki stosowane w badaniach toksyczności in vitro
 Temat ćwiczenia: Techniki stosowane w badaniach toksyczności in vitro Miarą aktywności cytotoksycznej badanej substancji jest określenie stężenia hamującego, IC 50 (ang. inhibitory concentration), dla
Temat ćwiczenia: Techniki stosowane w badaniach toksyczności in vitro Miarą aktywności cytotoksycznej badanej substancji jest określenie stężenia hamującego, IC 50 (ang. inhibitory concentration), dla
EZ-CFU TM One Step Microorganisms
 EZ-CFU TM One Step Microorganisms OPIS PRODUKTU EZ-CFU TM One Step są liofilizowanymi preparatami szczepów referencyjnych przeznaczonymi do przeprowadzania kontroli w laboratoriach mikrobiologicznych.
EZ-CFU TM One Step Microorganisms OPIS PRODUKTU EZ-CFU TM One Step są liofilizowanymi preparatami szczepów referencyjnych przeznaczonymi do przeprowadzania kontroli w laboratoriach mikrobiologicznych.
Genomic Maxi AX Direct
 Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
Instrukcja do ćwiczeń
 Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Instrukcja do ćwiczeń Temat: Woda jako
Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Instrukcja do ćwiczeń Temat: Woda jako
Laboratorium 7. Testy na genotoksyczność
 Test rewersji mutacji test Amesa Laboratorium 7 Testy na genotoksyczność Test Amesa jest testem bakteryjno-ssaczym. Organizmami testowymi są tutaj bakterie Salmonella typhimurium. W wyniku mutacji, celowo
Test rewersji mutacji test Amesa Laboratorium 7 Testy na genotoksyczność Test Amesa jest testem bakteryjno-ssaczym. Organizmami testowymi są tutaj bakterie Salmonella typhimurium. W wyniku mutacji, celowo
ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO
 ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO CZĘŚĆ TEORETYCZNA Metody badań i cechy w oparciu o które przeprowadzana jest klasyfikacja i identyfikacja mikroorganizmówh Struktura
ĆWICZENIE 3 DGGE- ELEKTROFOREZA W ŻELU Z GRADIENTEM CZYNNIKA DENATURUJĄCEGO CZĘŚĆ TEORETYCZNA Metody badań i cechy w oparciu o które przeprowadzana jest klasyfikacja i identyfikacja mikroorganizmówh Struktura
77/PNP/SW/2015 Dostawa implantów Załącznik nr 1 do SIWZ
 Część nr 1 Podłoża transportowo-wzrostowe do hodowli drobnoustrojów w krwi i płynach ustrojowych Podłoża do kompleksowego wykonywania procedur mikrobiologicznych do posiewów krwi i innych płynów ustrojowych
Część nr 1 Podłoża transportowo-wzrostowe do hodowli drobnoustrojów w krwi i płynach ustrojowych Podłoża do kompleksowego wykonywania procedur mikrobiologicznych do posiewów krwi i innych płynów ustrojowych
ĆWICZENIE NR 3 BADANIE MIKROBIOLOGICZNEGO UTLENIENIA AMONIAKU DO AZOTYNÓW ZA POMOCĄ BAKTERII NITROSOMONAS sp.
 ĆWICZENIE NR 3 BADANIE MIKROBIOLOGICZNEGO UTLENIENIA AMONIAKU DO AZOTYNÓW ZA POMOCĄ BAKTERII NITROSOMONAS sp. Uwaga: Ze względu na laboratoryjny charakter zajęć oraz kontakt z materiałem biologicznym,
ĆWICZENIE NR 3 BADANIE MIKROBIOLOGICZNEGO UTLENIENIA AMONIAKU DO AZOTYNÓW ZA POMOCĄ BAKTERII NITROSOMONAS sp. Uwaga: Ze względu na laboratoryjny charakter zajęć oraz kontakt z materiałem biologicznym,
VII. Fizjologia bakterii - ćwiczenia praktyczne
 VII. Fizjologia bakterii - ćwiczenia praktyczne Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej krwi baraniej
VII. Fizjologia bakterii - ćwiczenia praktyczne Ćwiczenie 1. Rodzaje pożywek i ich zastosowanie a. Podłoże stałe - proste Agar zwykły (AZ) b. Podłoża wzbogacone Agar z dodatkiem 5% odwłóknionej krwi baraniej
Zestaw do wykrywania Babesia spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych
 Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
Stosowanie w skali laboratoryjnej
 Stosowanie w skali laboratoryjnej Spis treści Velcorin Stosowanie w skali laboratoryjnej str. 3 5 Wprowadzenie str. 3 Środki ostrożności str. 3 Metoda pracy (sensorycznie) str. 4 Metoda pracy (mikrobiologicznie)
Stosowanie w skali laboratoryjnej Spis treści Velcorin Stosowanie w skali laboratoryjnej str. 3 5 Wprowadzenie str. 3 Środki ostrożności str. 3 Metoda pracy (sensorycznie) str. 4 Metoda pracy (mikrobiologicznie)
Nowoczesna diagnostyka mikrobiologiczna
 Nowoczesna diagnostyka mikrobiologiczna 1 2 Nowoczesne laboratorium mikrobiologiczne połączenie metod manualnych i automatyzacji Nowoczesne laboratorium mikrobiologiczne To nie tylko sprzęt diagnostyczny,
Nowoczesna diagnostyka mikrobiologiczna 1 2 Nowoczesne laboratorium mikrobiologiczne połączenie metod manualnych i automatyzacji Nowoczesne laboratorium mikrobiologiczne To nie tylko sprzęt diagnostyczny,
Technika hodowli komórek leukemicznych
 Fizjologiczne Techniki Badań Technika hodowli komórek leukemicznych Zasady prowadzenia hodowli komórek leukemicznych, pasażowania, mrożenia, rozmrażania i przechowywania komórek leukemicznych Warunki wstępne:
Fizjologiczne Techniki Badań Technika hodowli komórek leukemicznych Zasady prowadzenia hodowli komórek leukemicznych, pasażowania, mrożenia, rozmrażania i przechowywania komórek leukemicznych Warunki wstępne:
BBL Taxo Discs for Presumptive Identification of Gram-Negative Anaerobic Bacilli
 BBL Taxo Discs for Presumptive Identification of Gram-Negative Anaerobic Bacilli (Krążki do orientacyjnej identyfikacji Gram-ujemnych laseczek beztlenowych) Zobacz objaśnienie symboli na końcu ulotki.
BBL Taxo Discs for Presumptive Identification of Gram-Negative Anaerobic Bacilli (Krążki do orientacyjnej identyfikacji Gram-ujemnych laseczek beztlenowych) Zobacz objaśnienie symboli na końcu ulotki.
Załącznik nr 2 do specyfikacji. ... (Pieczęć Wykonawcy/Wykonawców) FORMULARZ CENOWY. Wykaz odczynników. Wartość netto za okres 48 m-cy (zł)
 ... (Pieczęć Wykonawcy/Wykonawców) FORMULARZ CENOWY Załącznik nr 2 do specyfikacji Wykaz odczynników ZAKUP I DOSTAWA ODCZYNNIKÓW I MATERIAŁÓW ZUŻYWALNYCH DO IDENTYFIKACJI DROBNOUSTROJÓW ORAZ OZNACZANIA
... (Pieczęć Wykonawcy/Wykonawców) FORMULARZ CENOWY Załącznik nr 2 do specyfikacji Wykaz odczynników ZAKUP I DOSTAWA ODCZYNNIKÓW I MATERIAŁÓW ZUŻYWALNYCH DO IDENTYFIKACJI DROBNOUSTROJÓW ORAZ OZNACZANIA
INSTRUKCJA OGÓLNA Zasady prowadzenia Programu Badania Biegłości POLMICRO
 SPIS TREŚCI Strona 1 z 7 1. Cel instrukcji Strona 1 2. Przedmiot i zakres instrukcji Strona 1 3. Terminy i definicje Strona 2 4. Zasady ogólne i odpowiedzialność Strona 2 5. Tryb postępowania Strona 2-7
SPIS TREŚCI Strona 1 z 7 1. Cel instrukcji Strona 1 2. Przedmiot i zakres instrukcji Strona 1 3. Terminy i definicje Strona 2 4. Zasady ogólne i odpowiedzialność Strona 2 5. Tryb postępowania Strona 2-7
