Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy.
|
|
|
- Daria Popławska
- 6 lat temu
- Przeglądów:
Transkrypt
1 Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy. Celem ćwiczenia jest wymodelowanie przebiegu reakcji chemicznej podstawienia nukleofilowego zachodzącego zgodnie z mechanizmem SN2. Wprowadzenie: Badanie mechanizmów reakcji chemicznych stanowi jedną z najbardziej istotnych części badań naukowych. Właściwie każda praca naukowa, której obiektem są nowe związki chemiczne, wymaga podania mechanizmu reakcji. Stanowi to podstawę naszego zrozumienia procesów chemicznych oraz umożliwia nam posługiwanie się tą wiedzą w celu projektowania nowych związków chemicznych (np. leków, katalizatorów). Postęp jaki obserwujemy w ciągu ostatnich lat nie byłby możliwy bez zastosowania narzędzi chemii kwantowej. Zbadanie mechanizmu reakcji na drodze eksperymentu jest jedną z najlepszych dróg do jego poznania. Niestety jest to zwykle bardzo czasochłonne, a otrzymujemy jedynie pewne poszlaki mogące sugerować daną ścieżkę reakcji. Nie możemy fizycznie zaobserwować reagujących obiektów chemicznych (chociaż tutaj w ostatnich 2-3 latach dokonał się olbrzymi postęp np. przy badaniu reakcji na powierzchni lub w fazie stałej). Z drugiej strony zastosowanie obliczeń kwantowo-mechanicznych wymaga od nas pewnej propozycji mechanizmu innymi słowy to my musimy wskazać (na podstawie pewnych przesłanek eksperymentalnych) jak dana reakcja może wyglądać. Uzyskiwane wyniki dają nam obraz czy dana ścieżka jest prawdopodobna, mogą również naprowadzić nas na właściwą ścieżkę reakcji. Szczegóły techniczne: W przypadku poszukiwania stanu przejściowego reakcji, modelowany jest punkt maksimum energetycznego. Jest to w rzeczywistości punkt siodłowy na powierzchni potencjału maksimum energii wzdłuż współrzędnej reakcji (a więc w obszarze centrum reakcji), ale przy optymalizacji innych parametrów geometrycznych molekuły (położenia atomów nie biorących bezpośredniego udziału w reakcji). W programie ORCA czynność tą można zrealizować przy pomocy komendy OptTS. Aby jednak rozpocząć tego typu obliczenia bardzo przydatna jest znajomość przybliżonej geometrii stanu przejściowego. Dlatego w pierwszej kolejności należy wykonać skan energii układu stopniowo zmieniając położenia atomu/grup atomów biorących udział w reakcji z optymalizacją geometrii pozostałych części układu przy każdym kroku takiego skanu jest to tzw. relaxed surface energy scan. Metoda ta polega na wykonaniu automatycznego skanu energii układu przy zmianie danego parametru i optymalizacji wszystkich innych parametrów molekuły. Czynność tą można wykonać otwierając sekcję geom i stosując polecenie Scan.! HF 3-21G Opt Linia komend głównych: Metoda obliczeń HF, baza 3-21G, Opt optymalizacja geometrii. W przypadku optymalizacji geometrii wszystkie parametry i położenia atomów będą optymalizowane przy zachowaniu stałej odległości/kąta/kąta dwuściennego pomiędzy danymi atomami zgodnie z tym jak to zdefiniujemy w sekcji geom. %geom Otwarcie sekcji geometria Scan Otwarcie podsekcji skan B 5 0 = 2.8, 4.8, 21 B skanowana będzie odległość między atomami 5 (Cl) oraz 0 (C) (można wykonać skan kątów międzyatomowych oraz kątów torsyjnych - A kąt, D, kąt dwuścienny), 2.8 to początkowa wartość odległości Cl C, 4.8 końcowa (jednostką
2 end end *xyz 0 1 C Br H H H Cl * jest Å nie a.u.!), zaś 21 to liczba kroków (a zatem zmiana będzie co 0.1 Å proszę pamiętać że należy uwzględnić wartość początkową i końcową). Zakończenie podsekcji skan Zamknięcie sekcji geometria Blok położenia atomów (układ kartezjański) W programie ORCA pierwszy atom ma oznaczenie 0, drugi 1 itp. Wynikiem skanu jest seria plików.xyz zawierających położenia atomów (optymalna geometria) każdego kroku skanu. W pliku wyjściowym (.out) otrzymujemy zestawione wartości skanu odległości B (lub kąty A, D) oraz energii molekuły. Program Orca umożliwia przeprowadzenie skanu jednocześnie dla kilku parametrów w wyniku czego można otrzymać bardzie złożoną powierzchnię energii. Otrzymaną zależność energii można zobrazować w programie Excell. Znalezione maksimum na krzywej energii będzie naszą przybliżoną geometrią do przeprowadzenia obliczeń optymalizacji stanu przejściowego. Dodatkowo należy wykonać obliczenia drań molekuły (opcja NumFreq). Przykładowy plik wejściowy do optymalizacji struktury stanu przejściowego wygląda następująco:! HF 3-21G NumFreq OptTS SlowConv Linia komend głównych: Metoda obliczeń HF, baza 3-21G. NumFreq obliczenia częstości drgań, OptTs poszukiwanie stanu przejściowego (punktu siodłowego), SlowConv polecenie opcjonalne powolne osiąganie zbieżności (małymi krokami). *xyz 0 1 Blok położenia atomów (układ kartezjański) C Br H H H Cl * Ponieważ obliczenia te nie prowadzą do minimum energetycznego (stan przejściowy nie jest układem stabilnym!), w pliku wyjściowym powinna pojawić się jedna ujemna częstość drgań (tzw. imaginary frequency). Jeżeli zobrazujemy to nierzeczywiste drganie to okaże się że biorą w nim udział atomy/grupy atomów których reakcje badamy. Na marginesie chcielibyśmy zwrócić uwagę na dobór metody obliczeniowej i modelu. Poszukiwanie stanu przejściowego oraz jego energia są wrażliwe na dobór metody obliczeniowej oraz bazy. Po drugie, obliczenia prowadzone są najczęściej dla układów izolowanych, podczas gdy większość reakcji chemicznych jest przeprowadzana w roztworze. Zatem dążenie do uzyskania jak najdokładniejszych
3 wyników wymaga zastosowania dokładnych metod obliczeniowych oraz wprowadzenia rozpuszczalnika - w większości przypadków są to modele ciągłe rozpuszczalnika, gdzie oddziaływanie molekuły z rozpuszczalnikiem przybliżane jest poprzez jej oddziaływanie elektrostatyczne z polem ciągłym, które otacza tą molekułę. W programie ORCA można taki model wprowadzić stosując komendę CPCM. Bardziej szczegółowe modele będą wymagały uwzględnienia solwatacji, przeciwjonów (gdy takie występują), możliwości agregacji molekuł itp. Potrzebne jest również uwzględnienie temperatury oraz entropii. Tak uzyskiwane są stosunkowo dokładne wartości entalpii swobodnej reakcji. Jednak koszt czasowy takich obliczeń bywa bardzo wysoki, również nie zawsze prowadzi to do racjonalnych wyników. Stąd zachodzi potrzeba wprowadzania uproszczeń. Mechanizm reakcji SN2: W ćwiczeniu będzie badana reakcja substytucji nukleofilowej zachodząca pomiędzy halogenkiem metanu (CH 3Br lub CH 3Cl) oraz nukleofilem (Cl-, F- lub CN-). Reakcja ma następujący przebieg: S substraty (najlepiej w dużej odległości od siebie ~10A) P produkty (najlepiej w dużej odległości od siebie ~10A) C1 kompleks Nu CH3X C2 kompleks X NuCH3 TS stan przejściowy Należy zwrócić uwagę na powstawanie kompleksów C1 oraz C2 będących efektem oddziaływania cząsteczek chemicznych tuż przed i tuż po reakcji. W rzeczywistości efekty związane z solwatacją mogą mieć znaczny wpływ na energie tego typu kompleksów.
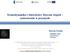
4 Zadania: 1. Wykonaj optymalizację geometrii wszystkich molekuł biorących udział w reakcji. Obliczenia należy wykonać metodą HF stosując bazę orbitali atomowych 3-21G. 2. Wykonaj skan energii odległości d Nu C przy optymalizacji pozostałych parametrów molekuły. Nukleofil oraz atom halogenu powinny znajdować się po przeciwnych stronach molekuły (kąt X C Nu = 180 o ). Metoda HF / 3-21G. Proponowane parametry skanu: Dla reakcji CH 3Br + Cl - odległości Cl- C 3.7 A do 1.7 A, krok 0.1 A; Dla reakcji CH 3Cl+ Br - odległości Cl- C 3.8 A do 1.8 A, krok 0.1 A; 3. Wyniki obliczeń proszę zestawić w tabeli arkusza (E w zależności d Nu C) oraz proszę narysować wykres E = f(d Nu C). 4. Wykonaj analogiczny skan w drugą stronę tzn. dla reakcji X - + NuCH 3. Przedstaw wyniki w arkuszu kalkulacyjnym. 5. Wykonaj optymalizację geometrii stanu przejściowego z opcją Freq. Jakie są odległości Nu C i C X? Sprawdź częstości drgań molekuły. O czym świadczy obecność jednej ujemnej częstości drgania. 6. Wykonaj optymalizację energii kompleksów C1 oraz C2. Metoda HF / 3-21G. 7. Na podstawie uzyskanych wyników przedstaw przebieg reakcji względem współrzędnej reakcji dla reakcji Nu- + CH3X każdej wartości odciętej kroku skanu poczynając od największej odległości Nu- + CH3X aż do TS przypisz wartości całkowite odpowiednio od wartości ujemnej aż do 0, gdzie 0 to TS, zaś dla reakcji NuCH3 + X- każdej wartości odciętej kroku skanu od TS aż do największej odległości X- + NuCH3 przypisać wartości całkowite dodatnie. Wyznacz barierę aktywacji jako E TS-E C1 8. Zadanie opcjonalne: Wyznacz funkcje termodynamiczne (E- energia elektronowa, U energia wewnętrzna, H entalpia, TS czynnik entropowy, G entalpia swobodna) uwzględniając poprawki ZPE oraz poprawki związane z rozkładem statystycznym oscylacyji/rotacji/translacyjni (Temperatura T = 298K) dla układów: S, C1, TS, C2, P. Obliczenia proszę wykonać korzystając z uprzednio zoptymalizowanych geometrii molekuł i bez dalszej optymalizacji (obliczenia single point). Metoda obliczeń HF / 3-21G. 9. Zadanie opcjonalne: Dla układów S, C1, TS, C2, P (geometria uzyskana z poprzednich optymalizacji) proszę wykonać obliczenia single point (bez optymalizacji) metodą HF w bazie G(d), a następnie metodą funkcjonału gęstości (DFT) korzystając z funkcjonału M062X w bazie G(d). Proszę porównać wyniki. Porównaj wyniki z tymi danymi literaturowymi, gdzie autorzy zastosowali jedną z najbardziej dokładnych metod chemii kwantowej metodę sprzężonych klasterów CCDC(T) w bazie 431cGTOs (J. Am. Chem. Soc. 2003, 125, 1014) rysunek poniżej. 10. Zadanie opcjonalne: Wykonaj obliczenia single point metodą HF w bazie G(d) uwzględniając pole rozpuszczalnika (woda) CPCM opcja CPCM(water) w wierszu poleceń. Porównaj uzyskane wyniki. Czy rozpuszczalnik ma istotny wpływ na reakcję?
5 Poziom obliczeń: CCSD(T)/431cGTOs. Izolowany układ reakcyjny.
Ćwiczenie 5. Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W
 Ćwiczenie 5 Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W Co powinieneś umieć przed zajęciami Jak obliczyć energię oscylatora harmonicznego, klasycznego i kwantowego?
Ćwiczenie 5 Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W Co powinieneś umieć przed zajęciami Jak obliczyć energię oscylatora harmonicznego, klasycznego i kwantowego?
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450
 Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Rzędy wiązań chemicznych
 Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Ćwiczenie 3. Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe *
 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * 1 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * I. Narysuj etylen a) Wybierz Default
Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * 1 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * I. Narysuj etylen a) Wybierz Default
EWA PIĘTA. Streszczenie pracy doktorskiej
 EWA PIĘTA Spektroskopowa analiza struktur molekularnych i procesu adsorpcji fosfinowych pochodnych pirydyny, potencjalnych inhibitorów aminopeptydazy N Streszczenie pracy doktorskiej wykonanej na Wydziale
EWA PIĘTA Spektroskopowa analiza struktur molekularnych i procesu adsorpcji fosfinowych pochodnych pirydyny, potencjalnych inhibitorów aminopeptydazy N Streszczenie pracy doktorskiej wykonanej na Wydziale
Dotyczy to zarówno istniejących już związków, jak i związków, których jeszcze dotąd nie otrzymano.
 Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
Chemia teoretyczna to dział chemii zaliczany do chemii fizycznej, zajmujący się zagadnieniami związanymi z wiedzą chemiczną od strony teoretycznej, tj. bez wykonywania eksperymentów na stole laboratoryjnym.
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Ćwiczenie nr 2 Komputerowe modelowanie cząsteczek związków chemicznych przy uŝyciu programu HyperChem Lite
 Ćwiczenie nr 2 Komputerowe modelowanie cząsteczek związków chemicznych przy uŝyciu programu HyperChem Lite Część teoretyczna Cel ćwiczenia 1) Zapoznanie studentów z modelowaniem molekularnym 2) Zapoznanie
Ćwiczenie nr 2 Komputerowe modelowanie cząsteczek związków chemicznych przy uŝyciu programu HyperChem Lite Część teoretyczna Cel ćwiczenia 1) Zapoznanie studentów z modelowaniem molekularnym 2) Zapoznanie
- parametry geometryczne badanego związku: współrzędne i typy atomów, ich masy, ładunki, prędkości początkowe itp. (w NAMD plik.
 Avogadro Tworzenie i manipulacja modelami związków chemicznych. W symulacjach dynamiki molekularnej kluczowych elementem jest przygotowanie układu do symulacji tzn. stworzyć pliki wejściowe zawierające
Avogadro Tworzenie i manipulacja modelami związków chemicznych. W symulacjach dynamiki molekularnej kluczowych elementem jest przygotowanie układu do symulacji tzn. stworzyć pliki wejściowe zawierające
Moduły kształcenia. Efekty kształcenia dla programu kształcenia (kierunku) MK_06 Krystalochemia. MK_01 Chemia fizyczna i jądrowa
 Matryca efektów kształcenia określa relacje między efektami kształcenia zdefiniowanymi dla programu kształcenia (efektami kierunkowymi) i efektami kształcenia zdefiniowanymi dla poszczególnych modułów
Matryca efektów kształcenia określa relacje między efektami kształcenia zdefiniowanymi dla programu kształcenia (efektami kierunkowymi) i efektami kształcenia zdefiniowanymi dla poszczególnych modułów
Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych
 Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych Justyna Cembrzyńska Zakład Mechaniki Kwantowej Uniwersytet
Rozwój i zastosowanie wieloreferencyjnych metod sprzężonych klasterów w opisie stanów podstawowych i wzbudzonych układów atomowych i molekularnych Justyna Cembrzyńska Zakład Mechaniki Kwantowej Uniwersytet
========================= Zapisujemy naszą funkcję kwadratową w postaci kanonicznej: 2
 Leszek Sochański Arkusz przykładowy, poziom podstawowy (A1) Zadanie 1. Wykresem funkcji kwadratowej f jest parabola o wierzchołku 5,7 Wówczas prawdziwa jest równość W. A. f 1 f 9 B. f 1 f 11 C. f 1 f 1
Leszek Sochański Arkusz przykładowy, poziom podstawowy (A1) Zadanie 1. Wykresem funkcji kwadratowej f jest parabola o wierzchołku 5,7 Wówczas prawdziwa jest równość W. A. f 1 f 9 B. f 1 f 11 C. f 1 f 1
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 1, zadanie nr 1 1
 Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Chemia fizyczna/ termodynamika, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący Uwaga! Proszę stosować się do następującego sposobu wprowadzania tekstu w ramkach : pola szare
Politechnika Gdańska Wydział Elektrotechniki i Automatyki Katedra Inżynierii Systemów Sterowania
 Politechnika Gdańska Wydział Elektrotechniki i Automatyki Katedra Inżynierii Systemów Sterowania Metody optymalizacji Metody bezgradientowe optymalizacji bez ograniczeń Materiały pomocnicze do ćwiczeń
Politechnika Gdańska Wydział Elektrotechniki i Automatyki Katedra Inżynierii Systemów Sterowania Metody optymalizacji Metody bezgradientowe optymalizacji bez ograniczeń Materiały pomocnicze do ćwiczeń
Projektowanie Wirtualne bloki tematyczne PW I
 Podstawowe zagadnienia egzaminacyjne Projektowanie Wirtualne - część teoretyczna Projektowanie Wirtualne bloki tematyczne PW I 1. Projektowanie wirtualne specyfika procesu projektowania wirtualnego, podstawowe
Podstawowe zagadnienia egzaminacyjne Projektowanie Wirtualne - część teoretyczna Projektowanie Wirtualne bloki tematyczne PW I 1. Projektowanie wirtualne specyfika procesu projektowania wirtualnego, podstawowe
Teoretyczne badania reakcji odwodornienia borazanu katalizowanych przez kompleksy oparte na palladzie
 Teoretyczne badania reakcji odwodornienia borazanu katalizowanych przez kompleksy oparte na palladzie Monika Parafiniuk Praca wykonywana pod opieką dr Mariusza Mitoraja Cele pracy i plan prezentacji Cel
Teoretyczne badania reakcji odwodornienia borazanu katalizowanych przez kompleksy oparte na palladzie Monika Parafiniuk Praca wykonywana pod opieką dr Mariusza Mitoraja Cele pracy i plan prezentacji Cel
Zadanie 2. (1 pkt) Uzupełnij tabelę, wpisując wzory sumaryczne tlenków w odpowiednie kolumny. CrO CO 2 Fe 2 O 3 BaO SO 3 NO Cu 2 O
 Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
Krystalografia. Analiza wyników rentgenowskiej analizy strukturalnej i sposób ich prezentacji
 Krystalografia Analiza wyników rentgenowskiej analizy strukturalnej i sposób ich prezentacji Opis geometrii Symetria: kryształu: grupa przestrzenna cząsteczki: grupa punktowa Parametry geometryczne współrzędne
Krystalografia Analiza wyników rentgenowskiej analizy strukturalnej i sposób ich prezentacji Opis geometrii Symetria: kryształu: grupa przestrzenna cząsteczki: grupa punktowa Parametry geometryczne współrzędne
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu
 Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
Łukasz Januszkiewicz Technika antenowa
 Instrukcja współfinansowana przez Unię Europejską w ramach Europejskiego Funduszu Społecznego w projekcie Innowacyjna dydaktyka bez ograniczeń zintegrowany rozwój Politechniki Łódzkiej zarządzanie Uczelnią,
Instrukcja współfinansowana przez Unię Europejską w ramach Europejskiego Funduszu Społecznego w projekcie Innowacyjna dydaktyka bez ograniczeń zintegrowany rozwój Politechniki Łódzkiej zarządzanie Uczelnią,
Termodynamika i właściwości fizyczne stopów - zastosowanie w przemyśle
 Termodynamika i właściwości fizyczne stopów - zastosowanie w przemyśle Marcela Trybuła Władysław Gąsior Alain Pasturel Noel Jakse Plan: 1. Materiał badawczy 2. Eksperyment Metodologia 3. Teoria Metodologia
Termodynamika i właściwości fizyczne stopów - zastosowanie w przemyśle Marcela Trybuła Władysław Gąsior Alain Pasturel Noel Jakse Plan: 1. Materiał badawczy 2. Eksperyment Metodologia 3. Teoria Metodologia
INSTRUKCJA DO ĆWICZENIA NR 1
 L01 ---2014/10/17 ---10:52---page1---#1 KATEDRA MECHANIKI STOSOWANEJ Wydział Mechaniczny POLITECHNIKA LUBELSKA INSTRUKCJA DO ĆWICZENIA NR 1 PRZEDMIOT TEMAT Wybrane zagadnienia z optymalizacji elementów
L01 ---2014/10/17 ---10:52---page1---#1 KATEDRA MECHANIKI STOSOWANEJ Wydział Mechaniczny POLITECHNIKA LUBELSKA INSTRUKCJA DO ĆWICZENIA NR 1 PRZEDMIOT TEMAT Wybrane zagadnienia z optymalizacji elementów
Termodynamika techniczna i chemiczna, 2015/16, zadania do kol. 1, zadanie nr 1 1
 Termodynamika techniczna i chemiczna, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący 1. Obliczyć zmianę entalpii dla izobarycznej (p = 1 bar) reakcji chemicznej zapoczątkowanej
Termodynamika techniczna i chemiczna, 2015/16, zadania do kol. 1, zadanie nr 1 1 [Imię, nazwisko, grupa] prowadzący 1. Obliczyć zmianę entalpii dla izobarycznej (p = 1 bar) reakcji chemicznej zapoczątkowanej
10. Eliminacja halogenków alkili
 10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
10. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C-a C-b 2 10.1.1. Regioselektywność
18 i 19. Substytucja nukleofilowa w halogenkach alkili
 8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
8 i 9. Substytucja nukleofilowa w halogenkach alkili Związki pojadające wiązanie C (sp 3 )-atom o większej elektroujemności od at. C elektroujemny atom sp 3 polarne wiązanie 9.. Typowe reakcje halogenków
Korzystanie z podstawowych rozkładów prawdopodobieństwa (tablice i arkusze kalkulacyjne)
 Korzystanie z podstawowych rozkładów prawdopodobieństwa (tablice i arkusze kalkulacyjne) Przygotował: Dr inż. Wojciech Artichowicz Katedra Hydrotechniki PG Zima 2014/15 1 TABLICE ROZKŁADÓW... 3 ROZKŁAD
Korzystanie z podstawowych rozkładów prawdopodobieństwa (tablice i arkusze kalkulacyjne) Przygotował: Dr inż. Wojciech Artichowicz Katedra Hydrotechniki PG Zima 2014/15 1 TABLICE ROZKŁADÓW... 3 ROZKŁAD
Kwantowo-chemiczne badania struktur kompleksów neonikotyny z jonami miedzi (II) oraz cynku (II)
 Wydział Chemii Kwantowo-chemiczne badania struktur kompleksów neonikotyny z jonami miedzi (II) oraz cynku (II) Mgr Wojciech Jankowski Pracownia Chemii Kwantowej Wydział Chemii UAM w.jankowski@amu.edu.pl
Wydział Chemii Kwantowo-chemiczne badania struktur kompleksów neonikotyny z jonami miedzi (II) oraz cynku (II) Mgr Wojciech Jankowski Pracownia Chemii Kwantowej Wydział Chemii UAM w.jankowski@amu.edu.pl
Monitoring procesów z wykorzystaniem systemu ADONIS. Krok po kroku
 z wykorzystaniem systemu ADONIS Krok po kroku BOC Information Technologies Consulting Sp. z o.o. e-mail: boc@boc-pl.com Tel.: (+48 22) 628 00 15, 696 69 26 Fax: (+48 22) 621 66 88 BOC Management Office
z wykorzystaniem systemu ADONIS Krok po kroku BOC Information Technologies Consulting Sp. z o.o. e-mail: boc@boc-pl.com Tel.: (+48 22) 628 00 15, 696 69 26 Fax: (+48 22) 621 66 88 BOC Management Office
Excel - użycie dodatku Solver
 PWSZ w Głogowie Excel - użycie dodatku Solver Dodatek Solver jest narzędziem używanym do numerycznej optymalizacji nieliniowej (szukanie minimum funkcji) oraz rozwiązywania równań nieliniowych. Przed pierwszym
PWSZ w Głogowie Excel - użycie dodatku Solver Dodatek Solver jest narzędziem używanym do numerycznej optymalizacji nieliniowej (szukanie minimum funkcji) oraz rozwiązywania równań nieliniowych. Przed pierwszym
P R Z E T W A R Z A N I E S Y G N A Ł Ó W B I O M E T R Y C Z N Y C H
 W O J S K O W A A K A D E M I A T E C H N I C Z N A W Y D Z I A Ł E L E K T R O N I K I Drukować dwustronnie P R Z E T W A R Z A N I E S Y G N A Ł Ó W B I O M E T R Y C Z N Y C H Grupa... Data wykonania
W O J S K O W A A K A D E M I A T E C H N I C Z N A W Y D Z I A Ł E L E K T R O N I K I Drukować dwustronnie P R Z E T W A R Z A N I E S Y G N A Ł Ó W B I O M E T R Y C Z N Y C H Grupa... Data wykonania
FUNKCJA KWADRATOWA. Zad 1 Przedstaw funkcję kwadratową w postaci ogólnej. Postać ogólna funkcji kwadratowej to: y = ax + bx + c;(
 Zad Przedstaw funkcję kwadratową w postaci ogólnej Przykład y = ( x ) + 5 (postać kanoniczna) FUNKCJA KWADRATOWA Postać ogólna funkcji kwadratowej to: y = ax + bx + c;( a 0) Aby ją uzyskać pozbywamy się
Zad Przedstaw funkcję kwadratową w postaci ogólnej Przykład y = ( x ) + 5 (postać kanoniczna) FUNKCJA KWADRATOWA Postać ogólna funkcji kwadratowej to: y = ax + bx + c;( a 0) Aby ją uzyskać pozbywamy się
Ćwiczenia nr 4. Arkusz kalkulacyjny i programy do obliczeń statystycznych
 Ćwiczenia nr 4 Arkusz kalkulacyjny i programy do obliczeń statystycznych Arkusz kalkulacyjny składa się z komórek powstałych z przecięcia wierszy, oznaczających zwykle przypadki, z kolumnami, oznaczającymi
Ćwiczenia nr 4 Arkusz kalkulacyjny i programy do obliczeń statystycznych Arkusz kalkulacyjny składa się z komórek powstałych z przecięcia wierszy, oznaczających zwykle przypadki, z kolumnami, oznaczającymi
1.3. Optymalizacja geometrii czasteczki
 0 1 Część teoretyczna 13 Optymalizacja geometrii czasteczki Poszukiwanie punktów stacjonarnych (krytycznych) funkcji stanowi niezwykle istotny problem w obliczeniowej chemii kwantowej Sprowadza się on
0 1 Część teoretyczna 13 Optymalizacja geometrii czasteczki Poszukiwanie punktów stacjonarnych (krytycznych) funkcji stanowi niezwykle istotny problem w obliczeniowej chemii kwantowej Sprowadza się on
ARKUSZ PRÓBNEJ MATURY Z OPERONEM CHEMIA
 Miejsce na naklejkę z kodem ARKUSZ PRÓBNEJ MATURY Z OPERONEM CHEMIA POZIOM PODSTAWOWY LISTOPAD ROK 2009 Instrukcja dla zdającego Czas pracy 120 minut 1. Sprawdź, czy arkusz egzaminacyjny zawiera 9 stron
Miejsce na naklejkę z kodem ARKUSZ PRÓBNEJ MATURY Z OPERONEM CHEMIA POZIOM PODSTAWOWY LISTOPAD ROK 2009 Instrukcja dla zdającego Czas pracy 120 minut 1. Sprawdź, czy arkusz egzaminacyjny zawiera 9 stron
Microsoft Access materiały pomocnicze do ćwiczeń cz. 1
 Microsoft Access materiały pomocnicze do ćwiczeń cz. 1 I. Tworzenie bazy danych za pomocą kreatora Celem ćwiczenia jest utworzenie przykładowej bazy danych firmy TEST, zawierającej informacje o pracownikach
Microsoft Access materiały pomocnicze do ćwiczeń cz. 1 I. Tworzenie bazy danych za pomocą kreatora Celem ćwiczenia jest utworzenie przykładowej bazy danych firmy TEST, zawierającej informacje o pracownikach
Wstęp do metod numerycznych Zadania numeryczne 2016/17 1
 Wstęp do metod numerycznych Zadania numeryczne /7 Warunkiem koniecznym (nie wystarczającym) uzyskania zaliczenia jest rozwiązanie co najmniej 3 z poniższych zadań, przy czym zadania oznaczone literą O
Wstęp do metod numerycznych Zadania numeryczne /7 Warunkiem koniecznym (nie wystarczającym) uzyskania zaliczenia jest rozwiązanie co najmniej 3 z poniższych zadań, przy czym zadania oznaczone literą O
Komputerowe wspomaganie projektowania leków
 Komputerowe wspomaganie projektowania leków MECHANIKA MOLEKULARNA I KWANTOWA W MM korzysta się z równań wynikających z praw fizyki klasycznej i stosuje się je do jader atomów z pominięciem elektronów,
Komputerowe wspomaganie projektowania leków MECHANIKA MOLEKULARNA I KWANTOWA W MM korzysta się z równań wynikających z praw fizyki klasycznej i stosuje się je do jader atomów z pominięciem elektronów,
Zastosowanie Informatyki w Chemii Laboratorium. Instrukcje do c wiczen
 Zastosowanie Informatyki w Chemii Laboratorium Instrukcje do c wiczen Plan zajęć 1. Zajęcia organizacyjne. Przypomnienie z Excela. 2. Korelacja, regresja wprowadzenie zadanie część a i b 3. Korelacja,
Zastosowanie Informatyki w Chemii Laboratorium Instrukcje do c wiczen Plan zajęć 1. Zajęcia organizacyjne. Przypomnienie z Excela. 2. Korelacja, regresja wprowadzenie zadanie część a i b 3. Korelacja,
TERMODYNAMIKA I TERMOCHEMIA
 TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
TERMODYNAMIKA I TERMOCHEMIA Termodynamika - opisuje zmiany energii towarzyszące przemianom chemicznym; dział fizyki zajmujący się zjawiskami cieplnymi. Termochemia - dział chemii zajmujący się efektami
Podstawy termodynamiki
 Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
Podstawy termodynamiki Organizm żywy z punktu widzenia termodynamiki Parametry stanu Funkcje stanu: U, H, F, G, S I zasada termodynamiki i prawo Hessa II zasada termodynamiki Kierunek przemian w warunkach
1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej?
 Tematy opisowe 1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej? 2. Omów pomiar potencjału na granicy faz elektroda/roztwór elektrolitu. Podaj przykład, omów skale potencjału i elektrody
Tematy opisowe 1. Od czego i w jaki sposób zależy szybkość reakcji chemicznej? 2. Omów pomiar potencjału na granicy faz elektroda/roztwór elektrolitu. Podaj przykład, omów skale potencjału i elektrody
Obszary sprężyste (bez możliwości uplastycznienia)
 Przewodnik Inżyniera Nr 34 Aktualizacja: 01/2017 Obszary sprężyste (bez możliwości uplastycznienia) Program: MES Plik powiązany: Demo_manual_34.gmk Wprowadzenie Obciążenie gruntu może powodować powstawanie
Przewodnik Inżyniera Nr 34 Aktualizacja: 01/2017 Obszary sprężyste (bez możliwości uplastycznienia) Program: MES Plik powiązany: Demo_manual_34.gmk Wprowadzenie Obciążenie gruntu może powodować powstawanie
Laboratorium przedmiotu Technika Cyfrowa
 Laboratorium przedmiotu Technika Cyfrowa ćw.3 i 4: Asynchroniczne i synchroniczne automaty sekwencyjne 1. Implementacja asynchronicznych i synchronicznych maszyn stanu w języku VERILOG: Maszyny stanu w
Laboratorium przedmiotu Technika Cyfrowa ćw.3 i 4: Asynchroniczne i synchroniczne automaty sekwencyjne 1. Implementacja asynchronicznych i synchronicznych maszyn stanu w języku VERILOG: Maszyny stanu w
Grupa Moniki Musiał. Uniwersytet Śląski Instytut Chemii Zakład Chemii Teoretycznej
 Wieloreferencyjna metoda sprzężonych klasterów w dwuwalencyjnych sektorach przestrzeni Focka oraz metoda równań ruchu w zastosowaniu do opisu stanów wzbudzonych Grupa Moniki Musiał Uniwersytet Śląski Instytut
Wieloreferencyjna metoda sprzężonych klasterów w dwuwalencyjnych sektorach przestrzeni Focka oraz metoda równań ruchu w zastosowaniu do opisu stanów wzbudzonych Grupa Moniki Musiał Uniwersytet Śląski Instytut
Wyznaczanie prędkości dźwięku w powietrzu
 Imię i Nazwisko... Wyznaczanie prędkości dźwięku w powietrzu Opracowanie: Piotr Wróbel 1. Cel ćwiczenia. Celem ćwiczenia jest wyznaczenie prędkości dźwięku w powietrzu, metodą różnicy czasu przelotu. Drgania
Imię i Nazwisko... Wyznaczanie prędkości dźwięku w powietrzu Opracowanie: Piotr Wróbel 1. Cel ćwiczenia. Celem ćwiczenia jest wyznaczenie prędkości dźwięku w powietrzu, metodą różnicy czasu przelotu. Drgania
WZMACNIACZ ODWRACAJĄCY.
 Ćwiczenie 19 Temat: Wzmacniacz odwracający i nieodwracający. Cel ćwiczenia Poznanie zasady działania wzmacniacza odwracającego. Pomiar przebiegów wejściowego wyjściowego oraz wzmocnienia napięciowego wzmacniacza
Ćwiczenie 19 Temat: Wzmacniacz odwracający i nieodwracający. Cel ćwiczenia Poznanie zasady działania wzmacniacza odwracającego. Pomiar przebiegów wejściowego wyjściowego oraz wzmocnienia napięciowego wzmacniacza
Politechnika Warszawska Wydział Mechatroniki Instytut Automatyki i Robotyki
 Politechnika Warszawska Wydział Mechatroniki Instytut Automatyki i Robotyki Ćwiczenie laboratoryjne 2 Temat: Modelowanie powierzchni swobodnych 3D przy użyciu programu Autodesk Inventor Spis treści 1.
Politechnika Warszawska Wydział Mechatroniki Instytut Automatyki i Robotyki Ćwiczenie laboratoryjne 2 Temat: Modelowanie powierzchni swobodnych 3D przy użyciu programu Autodesk Inventor Spis treści 1.
Materiały Reaktorowe. Fizyczne podstawy uszkodzeń radiacyjnych cz. 1.
 Materiały Reaktorowe Fizyczne podstawy uszkodzeń radiacyjnych cz. 1. Uszkodzenie radiacyjne Uszkodzenie radiacyjne przekaz energii od cząstki inicjującej do materiału oraz rozkład jonów w ciele stałym
Materiały Reaktorowe Fizyczne podstawy uszkodzeń radiacyjnych cz. 1. Uszkodzenie radiacyjne Uszkodzenie radiacyjne przekaz energii od cząstki inicjującej do materiału oraz rozkład jonów w ciele stałym
Model wiązania kowalencyjnego cząsteczka H 2
 Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Model wiązania kowalencyjnego cząsteczka H 2 + Współrzędne elektronu i protonów Orbitale wiążący i antywiążący otrzymane jako kombinacje orbitali atomowych Orbital wiążący duża gęstość ładunku między jądrami
Otrzymaliśmy w ten sposób ograniczenie na wartości parametru m.
 Dla jakich wartości parametru m dziedziną funkcji f ( x) = x + mx + m 1 jest zbiór liczb rzeczywistych? We wzorze funkcji f(x) pojawia się funkcja kwadratowa, jednak znajduje się ona pod pierwiastkiem.
Dla jakich wartości parametru m dziedziną funkcji f ( x) = x + mx + m 1 jest zbiór liczb rzeczywistych? We wzorze funkcji f(x) pojawia się funkcja kwadratowa, jednak znajduje się ona pod pierwiastkiem.
Wprowadzenie do rysowania w 3D. Praca w środowisku 3D
 Wprowadzenie do rysowania w 3D 13 Praca w środowisku 3D Pierwszym krokiem niezbędnym do rozpoczęcia pracy w środowisku 3D programu AutoCad 2010 jest wybór odpowiedniego obszaru roboczego. Można tego dokonać
Wprowadzenie do rysowania w 3D 13 Praca w środowisku 3D Pierwszym krokiem niezbędnym do rozpoczęcia pracy w środowisku 3D programu AutoCad 2010 jest wybór odpowiedniego obszaru roboczego. Można tego dokonać
Metoda określania pozycji wodnicy statków na podstawie pomiarów odległości statku od głowic laserowych
 inż. Marek Duczkowski Metoda określania pozycji wodnicy statków na podstawie pomiarów odległości statku od głowic laserowych słowa kluczowe: algorytm gradientowy, optymalizacja, określanie wodnicy W artykule
inż. Marek Duczkowski Metoda określania pozycji wodnicy statków na podstawie pomiarów odległości statku od głowic laserowych słowa kluczowe: algorytm gradientowy, optymalizacja, określanie wodnicy W artykule
Modelowanie bilansu energetycznego pomieszczeń (1)
 Wydział Inżynierii Środowiska Politechnika Wrocławska Modelowanie bilansu energetycznego pomieszczeń (1) 2 / 7 Na czym polega ćwiczenie? Ćwiczenie polega na badaniu modelu nagrzewnicy wodnej i chłodnicy
Wydział Inżynierii Środowiska Politechnika Wrocławska Modelowanie bilansu energetycznego pomieszczeń (1) 2 / 7 Na czym polega ćwiczenie? Ćwiczenie polega na badaniu modelu nagrzewnicy wodnej i chłodnicy
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
10. Alkeny wiadomości wstępne
 0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
Wyłączenie redukcji parametrów wytrzymałościowych ma zastosowanie w następujących sytuacjach:
 Przewodnik Inżyniera Nr 35 Aktualizacja: 01/2017 Obszary bez redukcji Program: MES Plik powiązany: Demo_manual_35.gmk Wprowadzenie Ocena stateczności konstrukcji z wykorzystaniem metody elementów skończonych
Przewodnik Inżyniera Nr 35 Aktualizacja: 01/2017 Obszary bez redukcji Program: MES Plik powiązany: Demo_manual_35.gmk Wprowadzenie Ocena stateczności konstrukcji z wykorzystaniem metody elementów skończonych
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Jak mierzyć i jak liczyć efekty cieplne reakcji?
 Jak mierzyć i jak liczyć efekty cieplne reakcji? Energia Zdolność do wykonywania pracy lub do produkowania ciepła Praca objętościowa praca siła odległość 06_73 P F A W F h N m J P F A Area A ciśnienie
Jak mierzyć i jak liczyć efekty cieplne reakcji? Energia Zdolność do wykonywania pracy lub do produkowania ciepła Praca objętościowa praca siła odległość 06_73 P F A W F h N m J P F A Area A ciśnienie
20 i 21. Eliminacja halogenków alkili
 20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
20 i 21. Eliminacja halogenków alkili 1 10.1. Eliminacja dwucząsteczkowa (E2) 10.1.1. Eliminacja E2 mechanizm reakcji lub B Jednoczesne odejście H + (formalnie) i X, kiedy X = Cl, Br, I C- C- 2 10.1.1.
ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa
 Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Prawo zachowania energii: ZADANIA Z CHEMII Efekty energetyczne reakcji chemicznej - prawo Hessa Ogólny zasób energii jest niezmienny. Jeżeli zwiększa się zasób energii wybranego układu, to wyłącznie kosztem
Rozdział 7 ZARZĄDZANIE PROJEKTAMI
 Wprowadzenie do badań operacyjnych z komputerem Opisy programów, ćwiczenia komputerowe i zadania. T. Trzaskalik (red.) Rozdział 7 ZARZĄDZANIE PROJEKTAMI 7.2. Ćwiczenia komputerowe Ćwiczenie 7.1 Wykorzystując
Wprowadzenie do badań operacyjnych z komputerem Opisy programów, ćwiczenia komputerowe i zadania. T. Trzaskalik (red.) Rozdział 7 ZARZĄDZANIE PROJEKTAMI 7.2. Ćwiczenia komputerowe Ćwiczenie 7.1 Wykorzystując
KADD Minimalizacja funkcji
 Minimalizacja funkcji n-wymiarowych Forma kwadratowa w n wymiarach Procedury minimalizacji Minimalizacja wzdłuż prostej w n-wymiarowej przestrzeni Metody minimalizacji wzdłuż osi współrzędnych wzdłuż kierunków
Minimalizacja funkcji n-wymiarowych Forma kwadratowa w n wymiarach Procedury minimalizacji Minimalizacja wzdłuż prostej w n-wymiarowej przestrzeni Metody minimalizacji wzdłuż osi współrzędnych wzdłuż kierunków
Efekty kształcenia dla kierunku studiów CHEMIA studia pierwszego stopnia profil ogólnoakademicki
 Załącznik nr 1 Efekty kształcenia dla kierunku studiów CHEMIA studia pierwszego stopnia profil ogólnoakademicki Umiejscowienie kierunku w obszarze kształcenia Kierunek studiów chemia należy do obszaru
Załącznik nr 1 Efekty kształcenia dla kierunku studiów CHEMIA studia pierwszego stopnia profil ogólnoakademicki Umiejscowienie kierunku w obszarze kształcenia Kierunek studiów chemia należy do obszaru
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II
 TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
TEST PRZYROSTU KOMPETENCJI Z CHEMII DLA KLAS II Czas trwania testu 120 minut Informacje 1. Proszę sprawdzić czy arkusz zawiera 10 stron. Ewentualny brak należy zgłosić nauczycielowi. 2. Proszę rozwiązać
Ligand to cząsteczka albo jon, który związany jest z jonem albo atomem centralnym.
 138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS
 OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS Zagadnienia teoretyczne. Spektrofotometria jest techniką instrumentalną, w której do celów analitycznych wykorzystuje się przejścia energetyczne zachodzące
OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS Zagadnienia teoretyczne. Spektrofotometria jest techniką instrumentalną, w której do celów analitycznych wykorzystuje się przejścia energetyczne zachodzące
Fizyka statystyczna Fenomenologia przejść fazowych. P. F. Góra
 Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
Fizyka statystyczna Fenomenologia przejść fazowych P. F. Góra http://th-www.if.uj.edu.pl/zfs/gora/ 2015 Przejście fazowe transformacja układu termodynamicznego z jednej fazy (stanu materii) do innej, dokonywane
Symulacja grafenu na powierzchni miedzi. w pakiecie oprogramowania LAMMPS
 Symulacja grafenu na powierzchni miedzi w pakiecie oprogramowania LAMMPS Szymon Romanowski Student 3-go roku Inżynierii Materiałowej Politechniki Warszawskiej szymon1874@gmail.com Praca wykonana we wrześniu
Symulacja grafenu na powierzchni miedzi w pakiecie oprogramowania LAMMPS Szymon Romanowski Student 3-go roku Inżynierii Materiałowej Politechniki Warszawskiej szymon1874@gmail.com Praca wykonana we wrześniu
LABORATORIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE. Ćwiczenie nr 2 Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.
 LABOATOIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwiczenie nr Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.. Wprowadzenie Proces rozpadu drobin związków chemicznych
LABOATOIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwiczenie nr Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.. Wprowadzenie Proces rozpadu drobin związków chemicznych
Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych
 Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych Wstęp Krzywa energii potencjalnej 1 to wykres zależności energii potencjalnej cząsteczek od długości wiązania (czyli od wzajemnej
Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych Wstęp Krzywa energii potencjalnej 1 to wykres zależności energii potencjalnej cząsteczek od długości wiązania (czyli od wzajemnej
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego
 Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
Wykład 5 Widmo rotacyjne dwuatomowego rotatora sztywnego W5. Energia molekuł Przemieszczanie się całych molekuł w przestrzeni - Ruch translacyjny - Odbywa się w fazie gazowej i ciekłej, w fazie stałej
EFEKT SOLNY BRÖNSTEDA
 EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
1. Algorytmy przeszukiwania. Przeszukiwanie wszerz i w głąb.
 1. Algorytmy przeszukiwania. Przeszukiwanie wszerz i w głąb. Algorytmy przeszukiwania w głąb i wszerz są najczęściej stosowanymi algorytmami przeszukiwania. Wykorzystuje się je do zbadania istnienia połączenie
1. Algorytmy przeszukiwania. Przeszukiwanie wszerz i w głąb. Algorytmy przeszukiwania w głąb i wszerz są najczęściej stosowanymi algorytmami przeszukiwania. Wykorzystuje się je do zbadania istnienia połączenie
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
17. Elementy teorii stanu przejściowego
 17. Elementy teorii stanu przejściowego (ang. transition state theory, TST) 30.05.2017 r. 06.06.2017 r. Reakcja chemiczna to ruch jąder na powierzchni energii elektronowej (PES = potential energy surface)
17. Elementy teorii stanu przejściowego (ang. transition state theory, TST) 30.05.2017 r. 06.06.2017 r. Reakcja chemiczna to ruch jąder na powierzchni energii elektronowej (PES = potential energy surface)
Załącznik Nr 5 do Zarz. Nr 33/11/12
 Załącznik Nr 5 do Zarz. Nr 33/11/12 Z1-PU7 WYDANIE N1 Strona 1 z 5 (pieczęć wydziału) KARTA PRZEDMIOTU 1. Nazwa przedmiotu: CHEMIA TEORETYCZNA 2. Kod przedmiotu: - 3. Karta przedmiotu ważna od roku akademickiego:
Załącznik Nr 5 do Zarz. Nr 33/11/12 Z1-PU7 WYDANIE N1 Strona 1 z 5 (pieczęć wydziału) KARTA PRZEDMIOTU 1. Nazwa przedmiotu: CHEMIA TEORETYCZNA 2. Kod przedmiotu: - 3. Karta przedmiotu ważna od roku akademickiego:
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap szkolny rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap szkolny rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
Elektrochemiczna synteza pochodnych cukrowych 5 -steroidów (streszczenie)
 Uniwersytet w Białymstoku Instytut Chemii Elektrochemiczna synteza pochodnych cukrowych 5 -steroidów (streszczenie) Aneta Maria Tomkiel Promotor pracy: prof. dr hab. Jacek W. Morzycki Białystok 2016 Elektrochemiczne
Uniwersytet w Białymstoku Instytut Chemii Elektrochemiczna synteza pochodnych cukrowych 5 -steroidów (streszczenie) Aneta Maria Tomkiel Promotor pracy: prof. dr hab. Jacek W. Morzycki Białystok 2016 Elektrochemiczne
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii
 Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE.
 1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
1 WYKŁAD NR 3 OPIS DRGAŃ NORMALNYCH UJĘCIE KLASYCZNE I KWANTOWE. Współrzędne wewnętrzne 2 F=-fq q ξ i F i =-f ij x j U = 1 2 fq2 U = 1 2 ij f ij ξ i ξ j 3 Najczęściej stosowaną metodą obliczania drgań
Notacja Denavita-Hartenberga
 Notacja DenavitaHartenberga Materiały do ćwiczeń z Podstaw Robotyki Artur Gmerek Umiejętność rozwiązywania prostego zagadnienia kinematycznego jest najbardziej bazową umiejętność zakresu Robotyki. Wyznaczyć
Notacja DenavitaHartenberga Materiały do ćwiczeń z Podstaw Robotyki Artur Gmerek Umiejętność rozwiązywania prostego zagadnienia kinematycznego jest najbardziej bazową umiejętność zakresu Robotyki. Wyznaczyć
Kinetyka reakcji chemicznych. Dr Mariola Samsonowicz
 Kinetyka reakcji chemicznych Dr Mariola Samsonowicz 1 Czym zajmuje się kinetyka chemiczna? Badaniem szybkości reakcji chemicznych poprzez analizę eksperymentalną i teoretyczną. Zdefiniowanie równania kinetycznego
Kinetyka reakcji chemicznych Dr Mariola Samsonowicz 1 Czym zajmuje się kinetyka chemiczna? Badaniem szybkości reakcji chemicznych poprzez analizę eksperymentalną i teoretyczną. Zdefiniowanie równania kinetycznego
Rozwiązywanie równań nieliniowych
 Rozwiązywanie równań nieliniowych Marcin Orchel 1 Wstęp Przykłady wyznaczania miejsc zerowych funkcji f : f(ξ) = 0. Wyszukiwanie miejsc zerowych wielomianu n-tego stopnia. Wymiar tej przestrzeni wektorowej
Rozwiązywanie równań nieliniowych Marcin Orchel 1 Wstęp Przykłady wyznaczania miejsc zerowych funkcji f : f(ξ) = 0. Wyszukiwanie miejsc zerowych wielomianu n-tego stopnia. Wymiar tej przestrzeni wektorowej
Metody numeryczne. materiały do wykładu dla studentów. 7. Całkowanie numeryczne
 Metody numeryczne materiały do wykładu dla studentów 7. Całkowanie numeryczne 7.1. Całkowanie numeryczne 7.2. Metoda trapezów 7.3. Metoda Simpsona 7.4. Metoda 3/8 Newtona 7.5. Ogólna postać wzorów kwadratur
Metody numeryczne materiały do wykładu dla studentów 7. Całkowanie numeryczne 7.1. Całkowanie numeryczne 7.2. Metoda trapezów 7.3. Metoda Simpsona 7.4. Metoda 3/8 Newtona 7.5. Ogólna postać wzorów kwadratur
Wykład 8. Równowaga fazowa Roztwory rzeczywiste
 Wykład 8 Równowaga fazowa Roztwory rzeczywiste Roztwory doskonałe Porównanie roztworów doskonałych i Roztwory Doskonałe rzeczywistych Roztwory Rzeczywiste Spełniają prawo Raoulta Mieszanie w warunkach
Wykład 8 Równowaga fazowa Roztwory rzeczywiste Roztwory doskonałe Porównanie roztworów doskonałych i Roztwory Doskonałe rzeczywistych Roztwory Rzeczywiste Spełniają prawo Raoulta Mieszanie w warunkach
Ćwiczenie nr 2 - Rysowanie precyzyjne
 Ćwiczenie nr 2 - Rysowanie precyzyjne Materiały do kursu Skrypt CAD AutoCAD 2D strony: 37-46. Wprowadzenie Projektowanie wymaga budowania modelu geometrycznego zgodnie z określonymi wymiarami, a to narzuca
Ćwiczenie nr 2 - Rysowanie precyzyjne Materiały do kursu Skrypt CAD AutoCAD 2D strony: 37-46. Wprowadzenie Projektowanie wymaga budowania modelu geometrycznego zgodnie z określonymi wymiarami, a to narzuca
II Podkarpacki Konkurs Chemiczny 2009/10. ETAP II r. Godz Zadanie 1 (10 pkt.)
 II Podkarpacki Konkurs Chemiczny 2009/10 ETAP II 19.12.2009 r. Godz. 10.00-12.00 KPKCh Zadanie 1 (10 pkt.) 1. Gęstość 22% roztworu kwasu chlorowodorowego o stężeniu 6,69 mol/dm 3 wynosi: a) 1,19 g/cm 3
II Podkarpacki Konkurs Chemiczny 2009/10 ETAP II 19.12.2009 r. Godz. 10.00-12.00 KPKCh Zadanie 1 (10 pkt.) 1. Gęstość 22% roztworu kwasu chlorowodorowego o stężeniu 6,69 mol/dm 3 wynosi: a) 1,19 g/cm 3
POLITECHNIKA WARSZAWSKA
 POLITECHNIKA WARSZAWSKA WYDZIAŁ CHEMICZNY Prof. dr hab. inż. Andrzej Sporzyński Noakowskiego 3, 00-664 Warszawa tel.: 22 234 5737 fax: 22 6282741 e-mail: spor@ch.pw.edu.pl Warszawa, 9.04.2016 RECENZJA
POLITECHNIKA WARSZAWSKA WYDZIAŁ CHEMICZNY Prof. dr hab. inż. Andrzej Sporzyński Noakowskiego 3, 00-664 Warszawa tel.: 22 234 5737 fax: 22 6282741 e-mail: spor@ch.pw.edu.pl Warszawa, 9.04.2016 RECENZJA
Właściwości kryształów
 Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Właściwości kryształów Związek pomiędzy właściwościami, strukturą, defektami struktury i wiązaniami chemicznymi Skład i struktura Skład materiału wpływa na wszystko, ale głównie na: właściwości fizyczne
Inteligencja obliczeniowa
 Ćwiczenie nr 3 Zbiory rozmyte logika rozmyta Sterowniki wielowejściowe i wielowyjściowe, relacje rozmyte, sposoby zapisu reguł, aproksymacja funkcji przy użyciu reguł rozmytych, charakterystyki przejściowe
Ćwiczenie nr 3 Zbiory rozmyte logika rozmyta Sterowniki wielowejściowe i wielowyjściowe, relacje rozmyte, sposoby zapisu reguł, aproksymacja funkcji przy użyciu reguł rozmytych, charakterystyki przejściowe
Pytania przykładowe na kolokwium zaliczeniowe z Podstaw Elektrochemii i Korozji
 Pytania przykładowe na kolokwium zaliczeniowe z Podstaw Elektrochemii i Korozji Kolokwium obejmuje zakres materiału z wykładów oraz konwersatorium. Pytania na kolokwium mogą się różnić od pytań przedstawionych
Pytania przykładowe na kolokwium zaliczeniowe z Podstaw Elektrochemii i Korozji Kolokwium obejmuje zakres materiału z wykładów oraz konwersatorium. Pytania na kolokwium mogą się różnić od pytań przedstawionych
Termochemia efekty energetyczne reakcji
 Termochemia efekty energetyczne reakcji 1. Podstawowe pojęcia termodynamiki chemicznej a) Układ i otoczenie Układ, to wyodrębniony obszar materii, oddzielony od otoczenia wyraźnymi granicami (np. reagenty
Termochemia efekty energetyczne reakcji 1. Podstawowe pojęcia termodynamiki chemicznej a) Układ i otoczenie Układ, to wyodrębniony obszar materii, oddzielony od otoczenia wyraźnymi granicami (np. reagenty
DRUGA ZASADA TERMODYNAMIKI
 DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
DRUGA ZASADA TERMODYNAMIKI Procesy odwracalne i nieodwracalne termodynamicznie, samorzutne i niesamorzutne Proces nazywamy termodynamicznie odwracalnym, jeśli bez spowodowania zmian w otoczeniu możliwy
PRZEBIEG LABORATORIUM
 PRZEBIEG LABORATORIUM ZFPB ZADANIE 2 1. Rozpoczęcie pracy a) Otwórz pliki wskazane przez prowadzącego. b) Utwórz folder o nazwie ŚWIADECTWA i zapisz w nim wskazane pliki c) Wykonaj polecenia wskazane w
PRZEBIEG LABORATORIUM ZFPB ZADANIE 2 1. Rozpoczęcie pracy a) Otwórz pliki wskazane przez prowadzącego. b) Utwórz folder o nazwie ŚWIADECTWA i zapisz w nim wskazane pliki c) Wykonaj polecenia wskazane w
