cykloheksen kwas adypinowy cykloheksanol chlorocykloheksanol CHCH 2 CHCHCH 3 CH 3 CHCHCH 3 OH OHOH Cl Cl Cl
|
|
|
- Gabriela Kuczyńska
- 7 lat temu
- Przeglądów:
Transkrypt
1 W Ę G L O W O D O R Y A R O M A T Y C Z N E - ARENY BENZEN Benzen został odkryty przez Faradaya w 1825 r w oleistej pozostałości w londyńskich, ulicznych lampach oświetlanych gazem Michał Faraday ( ); ur W Newington Butts, Surrey, Wielka Brytania, dyrektor laboratoriu w Royal Institution, prof chemii w Royal Institution Cykloheksa-1,3,5-trien, noszący zwyczajową nazwę benzenu, pomimo Ŝe zawiera trzy podwójne wiązania C=C nie wykazuje właściwości chemicznych typowych dla alkenów, ani sprzęŝonych polienów, np heksa-1,3,5-trienu Przede wszystkim nie ulega charakterystycznym dla alkenów reakcjom addycji elektrofilowej cykloheksen KMnO 4 /O + /O /eter COO COO O kwas adypinowy cykloheksanol chlorocykloheksanol Podobnie heksa-1,3,5-trien: C 2 =C-C=C-C=C 2 heksen-1,3,5-trien KMnO 4 /O + /O /eter 2 C 2 O + 2 OCCO C 3 CC 2 CCC 3 C 3 CC 2 CCC 3 O OO aldehydy heksano-2,3,5-triol 2,3,5-trichloroheksan Benzen jest niepodatny na działanie tych reagentów: benzen KMnO 4 /O + /O /eter brak reakcji brak reakcji brak reakcji Geometria wiązań w cząsteczce benzenu jest inna niŝ w alkenach czy polienach sprzęŝonych W benzenie wszystkie wiązania C-C i C=C są jednakowej długości Nie ma róŝnicy pomiędzy 1,2- dimetylobenzem zapisanym wg poniŝej podanych dwóch wzorów To nie są izomery konstytucyjne, tj ten sam związek:
2 C 3 C 3 C 3 C 3 benzen 1,2-dimetylobenzen długość wiązania C-C = C=C = 1,39 Å; kąty w pierścieniu = 120 o Występowanie Węglowodory aromatyczne i inne związki organiczne zawierające układ aromatyczny są rozpowszechnione w przyrodzie, wiele z nich pełni waŝne funkcje biochemiczne: C 2 CCOO N 2 fenyloalanina aminokwas C 2 CCOO N 2 O tyrozyna aminokwas O 3 CN C 3 O O O C 2 NC 3 O 3 C O O O O N C 3 efedryna, adrenalina estradiol morfina, alkaloid neuroprzenośnik Ŝeński hormon narkotyk płciowy alkaloid (lek) Źródła węglowodorów aromatycznych Węglowodory aromatyczne występują w ropie naftowej, w zaleŝności od jej gatunków w mniejszej lub większej ilości Znajdują się w smole pogazowej produkcie wysokotemperaturowej pirolizy węgla kopalnego Wydajność smoły pogazowej wynosi 3-4% wsadu węglowego Obok smoły pogazowej w produktach pirolizy węgla znajduje się gaz (np gaz koksowniczy) i koks Gas koksowniczy po ochłodzeniu ulega częściowo skropleniu i ta ciekła frakcja nazywa się benzolem surowym Znajduje się w niej głównie benzen (>70%) i toluen (~15%) Smołę pogazową bogate źródło arenów poddaje się destylacji na frakcje i zaleŝności od lotności wydziela się: benzen, toluen, ksyleny, etylobenzen, polialkilowane benzeny, kumen, naftalen, inden, antracen i wyŝsze areny oraz pochodne węglowodorów aromatycznych, np fenole, aminy aromatyczne, pirydyna i inne C 3 C 3C3 C 3 C 3 C 2 C 3 C 3 C 3 toluen o-ksylen m-ksylen p-ksylen etylobenzen Areny powstają z węglowodorów alifatycznych (np z frakcji ropy naftowej) w procesie reformingu, polegającym na ogrzewaniu ich w wysokiej temp w obecności katalizatorów Z benzyny lekkiej (frakcji wrzącej w temp o C) powstaje głównie benzen, z frakcji o C w produktach reformingu przewaŝają benzen i toluen, a z destylatu o C otrzymuje się przede wszystkim ksyleny i etylobenzen Proces przekształcania alkanów w areny składa się z
3 etapów cyklizacji i aromatyzacji Najcenniejszym surowcem do otrzymywania arenów są frakcje zawierające duŝo cykloalkanów 500 o C C 3 C 3-2 Pt n-heksan cykloheksan benzen W przemyśle petrochemicznym areny wytwarza się z gazu płynnego, czyli propanu i butanów w procesie dehydrocyklooligomeryzacji, zwanej procesem Cyclar Jest to skomplikowany cykl reakcji od odwodornienia alkanów do alkenów, następnie ich izomeryzację, oligomeryzację, cyklizację i w końcu aromatyzację, czyli dalsze odwodornienie W produktach przewaŝa toluen Aromatyzację cykloalkenów moŝna przeprowadzić za pomocą takich utleniaczy, jak siarka lub selenen, a nawet tlen W reakcjach układów cyklicznych z S lub Se następuje eliminacja odpowiednio 2 S lub 2 Se i utworzenie wiązań podwójnych Im więcej podwójnych wiązań w pierścieniu, tym łatwiej dochodzi do aromatyzacji Stosunkowo łatwo aromatyzacji ulegają produkty addycji Dielsa-Adlera, poniewaŝ one są cykloalkenami Mechanizm reakcji utleniającego odwodornienia: tetralina 250 o C - S S - S S - S S naftalen Do odwodornienia cykloalkanów dochodzi równieŝ w obecności katalizatorów heterogenicznych (np Pt) Jest to odwrócony kierunek uwodornienia Uwodornienie arenów Uwodornienie katalityczne arenów jest moŝliwe, jednak zachodzi znacznie trudniej niŝ alkenów i wydziela się mniej energii niŝ podczas uwodornienia 3 moli alkenu, np cykloheksanu cykloheksen 2 katalizator cykloheksan -28,6 kcal/mol 2 2 katalizator cykloheksa-1,3-dien cykloheksan -55,4 kca/mol benzen 2 2 katalizator cykloheksan -49,8 kcal/mol
4 Ciepło uwodornienia Tabela 1 Substrat Produkt Ciepło uwodornienia o, kcal/mol oczekiwane oznaczone cykloheksen cykloheksan 28,6 28,6 cykloheks-1,3-dien cykloheksan 57,2 55,4 benzen cykloheksan 85,8 49,8 Z porównania obliczonej (oczekiwanej) wartości ciepła uwodornienia (trzykrotnie więcej niŝ wynosi o uwodornienia cykloheksenu), a oznaczonej wartości wynika, Ŝe energia potencjalna benzenu jest o 36 kcal/mol niŝsza niŝ hipotetycznego, niearomatycznego cykloheksa-1,3,5-trienu Benzenu nie moŝna zaliczać do alkenów Tego typu układy nazwano związkami aromatycznymi, w skrócie arenami Charakterystycznymi właściwościami benzenu i wielu innych związków aromatycznych są: cykliczna budowa; planarność i wysoka symetria cząsteczki, np sześciobok foremny o bokach (długościach wiązań) równych 1,39 Å i kątach 120 o ; układ 3 sprzęŝonych podwójnych wiązań; wysoka stabilność układu (niska energia potencjalna); brak aktywności w reakcjach addycji eletrofilowej (typowej dla akenów) podatność na substytucję elektrofilową Te właściwości zostały uznane za cechy związków aromatycznych Wymagania dotyczące struktury elektronowej i geometrii związków aromatycznych zawiera reguła ückela: Do związków aromatycznych zalicza się płaskie układy pierścieniowe, które zawierają elektrony π w liczbie określonej wzorem 4n + 2, gdzie n jest liczba naturalną = 0, 1, 2, 3, 4, Innymi słowy związkami aromatycznymi są te płaskie związki pierścieniowe, w których znajduje się 2, 6, 10, 14, 18 sprzęŝonych elektronów π Erich ückel ( ), ur w Stuttgarcie, doktorat u Debye a w Getyndze, prof fizyki w Stuttgardzie i Marburgu Cząsteczkę benzenu moŝna przedstawić za pomocą dwóch wzorów róŝniących się połoŝeniem elektronów π Przedstawiają one tę samą cząsteczkę, są równocenne i dopiero oba opisują właściwości tej cząsteczki: mezomeryczne wzory cząsteczki benzenu
5 Zjawisko polegające na tym, Ŝe tę samą cząsteczkę moŝna opisać za pomocą dwóch lub więcej wzorów, róŝniących się jedynie połoŝeniem elektronów π lub wolnych elektronów nazywa się mezomerią (rezonansem) i jest charakterystyczne dla związków aromatycznych Zanim zaczęto rysować wzory benzenu w postaci sześcioboku foremnego z trzema podwójnymi wiązaniami rozmieszczonymi symetrycznie były róŝne propozycje Kekulégo, Ladenburga, Dewara i z kółeczkiem w środku obrazującym sprzęŝone elektrony π wzory: Kekulégo Dewara Ladenburga z pierścieniem elektronów π MoŜliwość zapisania cząsteczki za pomocą dwóch lub więcej wzorów mezomerycznych sugeruje niŝszą energię potencjalną danej cząsteczki NiŜszą, niŝ moŝna sądzić obserwując pojedynczy wzór Pojedynczy wzór benzenu sugeruje, Ŝe jest on dienem sprzęŝonym, dwa wzory mezomeryczne świadczą o jego aromatycznym charakterze Czasami cząsteczkę benzenu przedstawia się za pomocą innych pojedynczych wzorów, ale one teŝ nie oddają aromatycznego charakteru związku: Z reguły ückela wynika, Ŝe związek aromatyczny nie musi mieć kształtu sześcioczłonowego pierścienia Istotnie znane są związki aromatyczne zbudowane z pierścieni o innych rozmiarach niŝ homologi benzenu MoŜe to być związek trójczłonowy, np kation cyklopropyliowy: + Sb Sb 6 1,2,3,3-tetrachloropropen jon 1,2,3-trichlorocyklopropyliowy (2 e) Kation cyklopropyliowy jest płaski i spełnia regułę ückela odnośnie liczby elektronów π w pierścieniu MoŜna dla niego rozpisać wzory mezomeryczne: Wzory mezomeryczne kationu cyklopropyliowego Cyklobuta-1,3-dien jest płaski, jednak ma 4 elektrony π, a więc nie spełnia reguły ückela Nie ma właściwości aromatycznych jest bardzo reaktywny, nawet w temperaturze 78 o C,
6 zachowuje się jak sprzęŝony dien, tzn reaguje zgodnie z reakcją Dielsa-Adlera, tworząc tricykliczny oktadien: + cyklobuta-1,3-dien -78 o C reakcja Dielsa-Adlera tricyklo[2,0,2,0]okta-2,6-dien Niektórzy autorzy cyklobuta-1,3-dien nazywają związkiem antyaromatycznym Cyklopenta-1,3-dien jest prawie płaski, ale liczba jego elektronów π nie spełnia reguły ückela ma 4e, zamiast 2 lub 6 Wystarczy jednak cyklopenta-1,3-dien przekształcić w anion, a zyska on cechy aromatyczności, poniewaŝ z anionową parą elektronów osiąga wymaganą liczba 6 elektronów, których orbitale mogą się wzajemnie na siebie nakładać (4π + 2) Z tego powodu allilowe atomy wodoru w cyklopenta-1,3-dienie są wyjątkowo kwaśne, jak na atomy związane z atomem węgla Stosunkowo łatwo moŝna je oderwać Tego typu związki nazywane są C- kwasami C 2 - O : C Cyklopenta-1,3-dien po oderwaniu protonu staje się układem aromatycznym : : Wzory mezomeryczne anionu cyklopentadienowego Benzen, jak juŝ zostało powiedziane spełnia regułę ückela Cyklohepta-1,3,5-trien ma co prawda liczbę elektronów wymaganą przez regułę ückela (6e), ale jego pierścień nie jest płaski Wystarczy jednak przekształcić go w kation, zwany kationem cykloheptatrienylowym lub tropyliowym, Ŝeby cząsteczka stała się płaska, a tym samym układ zyskał właściwości aromatyczne Karbokation ma hybrydyzację sp 2, wobec czego jest płaski Br 2 sp3 - Br + sp 2 Zadanie: Narysuj wzory mezomeryczne kationu cykloheptatrienylowgo Azulen zbudowany z dwóch pierścieni cyklopentadienylowego i cykloheptatrienylowego jest węglowodorem aromatycznym, poniewaŝ w rzeczywistości skondensowane są pierścienie anionu cyklopentadienylowego i kationu cykloheptatrienylowego:
7 - + niebieski moment dipolowy µ = 1,0 D azulen Rozdzielone ładunki wpływają na wzrost wartości momentu dipolowego cząsteczki azulenu Bardziej znany izomer azulenu naftalen jest bezbarwny, a jego moment dipolowy jest równy 0, poniewaŝ oba skondensowane sześcioczłonowe pierścienie w naftalenie, podobnie jak w benzenie są aromatyczne z natury i cząsteczka nie ulega Ŝadnym przemianom, Ŝeby osiągnąć aromatyczność naftalen bezbarwny moment dipolowy µ = 0 Cyklodeka-1,3,5,7,9-pentaen, bardzo zbliŝony budową do naftalenu, szczególnie wtedy, kiedy jest przedstawiony za pomocą wzoru, jak na rysunku nie jest węglowodorem aromatycznym, chociaŝ spełnia regułę ückela (10e) Jednak wbrew pozorom jego cząsteczka nie jest płaska, poniewaŝ atomy wodoru w połoŝeniach 2 i 7 nie mają wystarczająco duŝo miejsca, Ŝeby ułoŝyć się obok siebie; one zajmują połoŝenie nad i pod, przez co odchylają atomy C2 i C7 i zaburzają planarność cząsteczki: cyklodeka-1,3,5,7,9-pentaen Atomy wodoru przy C2 i C7 niszczą planarność cząsteczki cyklodeka-1,3,5,7,9-pentaenu Zadanie: Określ geometrię wiązań podwójnych w cząsteczce cyklodeka-1,3,5,7,9-pentaenu Cząsteczka cyklookta-1,3,5,7-tetraenu, jest płaska (wszystkie atomy C maja hybrydyzację sp 2 ), ale związek staje się aromatycznym dopiero po zyskaniu dwóch elektronów: Na 2e 2 Na + aromatyczny dianion cyklooktatetraenylowy Cyklookta-1,3,5,7-tetraen łatwo reaguje z metalami alkalicznymi, w wyniku czego powstaje dianion cyklooktatetraenylowy, wykazujący właściwości aromatyczne ObniŜenie energii układu
8 poprzez przekształcenie się w związek aromatyczny jest przyczyną duŝej kwasowości dwóch atomów wodoru cyklooktatetraenu przykład C-kwasu Znanych jest wiele węglowodorów aromatycznych, w których strukturach moŝna wyróŝnić skondensowane pierścienie benzenowe: antracen fenantren tetracen pentacen chryzen benzo[a]piren piren koroner Benzo[a]piren naleŝy do najsilniejszych związków rakotwórczych Struktura elektronowa benzenu Wszystkie atomy węgla w cząsteczce benzenu mają hybrydyzację sp 2 Trzy elektrony orbitali sp 2 atomów C benzenu tworzą wiązania σ: jedno z atomem wodoru, dwa z sąsiednimi atomami węgla Sześć orbitali atomowych p, sześciu atomów węgla tworzących cząsteczkę benzenu nakłada się tworząc sześć orbitali cząsteczkowych: trzy wiąŝące i trzy antywiąŝące: energia ψ 6 * ψ* 4, ψ 5 * orbitale antywiąŝące ψ 2, ψ 3 ψ 1 orbitale wiąŝące Rys Sześć orbital atomowych p sześciu atomów węgla w cząsteczce nakłada się i powstaje sześć orbitali cząsteczkowych ψ Z doświadczenia wiadomo, Ŝe orbitale cząsteczkowe benzenu ψ 1, ψ 2 i ψ 3 są równocenne, naleŝy więc przyjąć, Ŝe dochodzi do dalszego ich wzajemnego nałoŝenia i uśrednienia ich energii W takim przypadku mówimy o orbitalach zdegenerowanych (o tej samej energii) Orbital wiąŝący powstały po nałoŝeniu się orbitali ψ 1, ψ 2 i ψ 3 ma kształt dwóch obwarzanek zajmujących pozycje symetryczne do płaszczyzny pierścienia cząsteczki benzenu:
9 Rys Zdelokalizowane orbitale π benzenu, wg J McMurry, Chemia Organiczna, PWN, Warszawa 2000 Struktura elektronowa naftalenu W naftalenie 10 atomowych orbitali p nakłada się tworząc pięć cząsteczkowych orbitali wiąŝących i pięć antywiąŝących Dla zachowania przejrzystości detali waŝnych dla omawianego problemu nie uwzględniono na powyŝszych wzorach 6 atomów wodoru związanych po jednym z kaŝdym atomem węgla Struktura elektronowa anionu cyklopentadienowego W anionie cyklopentadienowym nakładają się na siebie cztery orbitale atomowe p zawierające po 1 elektronie i jeden orbital p anionowego atomu węgla zawierający 2 elektrony: NaleŜy pamiętać jeszcze o atomach wodoru przy kaŝdym z atomów C Nazewnictwo pochodnych benzenu Nazwy pochodnych benzenu tworzy się poprzez dodanie w przedrostku nazwy podstawnika, poprzedzonej lokantem, jeŝeli z pierścieniem związanych jest więcej niŝ jeden podstawnik Wiele popularnych pochodnych benzenu ma nazwy zwyczajowe Często wzajemne połoŝenie dwóch (nie więcej) podstawników w pierścieniu określa się za pomocą pisanych kursywą przerostków orto- (1,2), meta- (1,3) i para 1,4) C 3 C 3C3 C 3 C 3 C 3 C 3 toluen orto-ksylen meta-ksylen para-ksylen (metylobenzen) (1,2-dimetylobenzen) (1,3-dimetylobenzen) (1,4-dimelobenzen) Zamiast pełnych nazw przedrostków stosuje się równieŝ skróty o-, m- i p-: C 3 C 3 C 3 o-chlorotoluen m-chlorotoluen p-chlorotoluen
10 Najczęściej uŝywane nazwy zwyczajowe: O N C C 3C3 2 3 C(C 3 ) 2 3 C C 3 C 3 fenol anilina mezytylen pseudokumen kumen Reszta benzenu po usunięciu atomu wodoru nosi nazwę fenylu Fenyl jako przedrostek słuŝy do tworzenia nazw w sposobie podstawnikowym: O 3 C C 2 -C-C 3 1-fenylo-4-metylocykloheksan 1-fenylopropan-2-ol Właściwości fizyczne: Benzen, toluen i niektóre inne alkilobenzeny są cieczami o aromatycznym zapachu, stąd pochodzi nazwa tej grupy związków Benzen wrze w temperaturze 80 o C, a toluen 111 o C Benzen ze względu na swoją symetryczna budowę, a więc łatwość do tworzenia struktur uporządkowanych ma stosunkowo wysoką tt, wynoszącą 5,5 o C, podczas gdy tt toluenu wynosi 95 o C Naftalen jest ciałem stałym, tt = 80 o C Węglowodory aromatyczne są trudno rozpuszczalne w wodzie Benzen naleŝy do jednych z najbardziej niebezpiecznych popularnych związków organicznych, z uwagi na swoje właściwości toksyczne, kancerogenne i teratogenne Właściwości chemiczne węglowodorów aromatycznych zostaną omówione później
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Węglowodory Aromatyczne
 Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
Węglowodory Aromatyczne Benzen Rezonans & Aromatyczność Nazewnictwo (nomenklatura) Slides 1 to 38 Węglowodory Aromatyczne W pierwotnym znaczeniu słowo aroma nawiązywało do pachnących składników roślin;
WĘGLOWODORY AROMATYCZNE.
 Spis treści 1 WĘGLOWODORY AROMATYCZNE. 2 Budowa i nomenklatura węglowodorów aromatycznych 3 Efekt mezomeryczny 4 Substytucja elektrofilowa w układach aromatycznych 4.1 Profil energetyczny reakcji. 4.2
Spis treści 1 WĘGLOWODORY AROMATYCZNE. 2 Budowa i nomenklatura węglowodorów aromatycznych 3 Efekt mezomeryczny 4 Substytucja elektrofilowa w układach aromatycznych 4.1 Profil energetyczny reakcji. 4.2
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
8. Delokalizacja elektronów i reaktywność dienów sprzężonych
 8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
8. Delokalizacja elektronów i reaktywność dienów sprzężonych 1 8.1. Definicja elektronów zdelokalizowanych Zlokalizowane elektrony rozmieszczone w określonym obszarze cząsteczki, są uwspólnione pomiędzy
Wskaż grupy reakcji, do których można zaliczyć proces opisany w informacji wstępnej. A. I i III B. I i IV C. II i III D. II i IV
 Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
Informacja do zadań 1. i 2. Proces spalania pewnego węglowodoru przebiega według równania: C 4 H 8(g) + 6O 2(g) 4CO 2(g) + 4H 2 O (g) + energia cieplna Zadanie 1. (1 pkt) Procesy chemiczne można zakwalifikować
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego ĆWICZENIE 5. Związki aromatyczne
 ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
PRZYKŁADOWE ZADANIA WĘGLOWODORY
 PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
PRZYKŁADOWE ZADANIA WĘGLOWODORY INFORMACJA DO ZADAŃ 678 680 Poniżej przedstawiono wzory półstrukturalne lub wzory uproszczone różnych węglowodorów. 1. CH 3 2. 3. CH 3 -CH 2 -CH C CH 3 CH 3 -CH-CH 2 -C
Węglowodory poziom podstawowy
 Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
Węglowodory poziom podstawowy Zadanie 1. (2 pkt) Źródło: CKE 2010 (PP), zad. 19. W wyniku całkowitego spalenia 1 mola cząsteczek węglowodoru X powstały 2 mole cząsteczek wody i 3 mole cząsteczek tlenku
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
Wykład 5 XII 2018 Żywienie
 Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Wykład 5 XII 2018 Żywienie Witold Bekas SGGW Chemia organiczna 1828 Wöhler - przypadkowa synteza mocznika izocyjanian amonu NH4NCO związek nieorganiczny mocznik H2NCONH2 związek organiczny obalenie teorii
Kierunki chemicznejprzeróbki frakcji ropy naftowej. Destylacja ropy naftowej. Proces oligomeryzacji. Proces alkilowania. Proces oligomeryzacji
 Destylacja ropy naftowej Kierunki chemicznejprzeróbki frakcji ropy naftowej frakcja proces Gazowe Benzyna lekka Benzyna cięŝka Nafta napędowy mazut lekki średni gudron cięŝki izomeryzacja Reformowanie
Destylacja ropy naftowej Kierunki chemicznejprzeróbki frakcji ropy naftowej frakcja proces Gazowe Benzyna lekka Benzyna cięŝka Nafta napędowy mazut lekki średni gudron cięŝki izomeryzacja Reformowanie
10. Alkeny wiadomości wstępne
 0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
0. Alkeny wiadomości wstępne 5.. Nazewnictwo Nazwa systematyczna eten propen cyklopenten cykloheksen Nazwa zwyczajowa etylen propylen Wiązanie = w łańcuchu głównym, lokant = najniższy z możliwych -propyloheks--en
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, Spis treści
 Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Podstawy chemii organicznej. T. 1 / Aleksander Kołodziejczyk, Krystyna Dzierzbicka. wyd. 3. Gdańsk, 2015 Spis treści Wstęp 9 1. WIĄZANIA CHEMICZNE 11 1.1. Wprowadzenie 11 1.2. Wiązania chemiczne 13 1.3.
Wykład 6. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
RJC. Wiązania Chemiczne & Slides 1 to 39
 Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Wiązania Chemiczne & Struktura Cząsteczki Teoria Orbitali & ybrydyzacja Slides 1 to 39 Układ okresowy pierwiastków Siły występujące w cząsteczce związku organicznego Atomy w cząsteczce związku organicznego
Mechanizm dehydratacji alkoholi
 Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Wykład 5 Mechanizm dehydratacji alkoholi I. Protonowanie II. odszczepienie cząsteczki wody III. odszczepienie protonu Etap 1 Reakcje alkenów Najbardziej reaktywne jest wiązanie podwójne, lub jego sąsiedztwo
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
RJC # Defin i i n c i ja
 Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
Alkany - Izomery Strukturalne & Konformacyjne - Nomenklatura - Projekcje Newmana Slides 1 to 41 Definicja Wzór ogólny dla alkanów C n 2n+2 Przykładowo... metan C 4 etan C 2 6 propan C 3 8 butan C 4 10
Węglowodory poziom rozszerzony
 Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Węglowodory poziom rozszerzony Zadanie 1. (1 pkt) Źródło: KE 2010 (PR), zad. 21. Narysuj wzór strukturalny lub półstrukturalny (grupowy) węglowodoru, w którego cząsteczce występuje osiem wiązań σ i jedno
Zadanie 1. (3 pkt) a) Dokończ poniższe równanie reakcji (stosunek molowy substratów wynosi 1:1).
 Zadanie 1. (3 pkt) a) Dokończ poniższe równanie reakcji (stosunek molowy substratów wynosi 1:1). b) Podaj nazwę systematyczną związku organicznego otrzymanego w tej reakcji. c) Określ, jaką rolę w tej
Zadanie 1. (3 pkt) a) Dokończ poniższe równanie reakcji (stosunek molowy substratów wynosi 1:1). b) Podaj nazwę systematyczną związku organicznego otrzymanego w tej reakcji. c) Określ, jaką rolę w tej
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Węglowodory powtórzenie wiadomości
 Węglowodory powtórzenie wiadomości 1. Cele lekcji a) Wiadomości Uczeń zna: pojęcia: węglowodór nasycony, nienasycony i aromatyczny, izomeria konstytucyjna i geometryczna, sekstet elektronowy, wiązanie
Węglowodory powtórzenie wiadomości 1. Cele lekcji a) Wiadomości Uczeń zna: pojęcia: węglowodór nasycony, nienasycony i aromatyczny, izomeria konstytucyjna i geometryczna, sekstet elektronowy, wiązanie
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka
 Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Slajd 1 Alkeny: Struktura, nazewnictwo, Termodynamika i kinetyka Slajd 2 Alkeny Węglowodory te zawierają wiązanie podwójne C C wiązanie double podwójne bond the grupa functional funkcyjna group centrum
Laboratorium. Podstawowe procesy jednostkowe w technologii chemicznej
 Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Laboratorium Podstawowe procesy jednostkowe w technologii chemicznej Studia niestacjonarne Ćwiczenie Alkilowanie toluenu chlorkiem tert-butylu 1 PROCESY ALKILOWANIA PIERŚCIENIA AROMATYCZNEGO: ALKILOWANIE
Wykład 19 XII 2018 Żywienie
 Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Wykład 19 XII 2018 Żywienie Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas SGGW Witold Bekas
Materiały dodatkowe węglowodory aromatyczne, halogenopochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodory aromatyczne, halogenopochodne Areny 1. Aromatyczność związków niebenzoidowe związki aromatyczne. Benzen
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe węglowodory aromatyczne, halogenopochodne Areny 1. Aromatyczność związków niebenzoidowe związki aromatyczne. Benzen
Związki aromatyczne CH 3 NH 2 OH CN. toluen anilina fenol benzonitryl O CHO CCH 3 COOH CH CH 2. kwas benzoesowy. acetofenon. benzaldehyd.
 Związki aromatyczne Cl NO 2 C 2 C 3 benzen chlorobenzen nitrobenzen etylobenzen C 3 N 2 O CN toluen anilina fenol benzonitryl O CO CC 3 COO C C 2 benzaldehyd acetofenon kwas benzoesowy styren 1 C 3 C 3
Związki aromatyczne Cl NO 2 C 2 C 3 benzen chlorobenzen nitrobenzen etylobenzen C 3 N 2 O CN toluen anilina fenol benzonitryl O CO CC 3 COO C C 2 benzaldehyd acetofenon kwas benzoesowy styren 1 C 3 C 3
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych
 1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Spis treści. Metoda VSEPR. Reguły określania struktury cząsteczek. Ustalanie struktury przestrzennej
 Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
Spis treści 1 Metoda VSEPR 2 Reguły określania struktury cząsteczek 3 Ustalanie struktury przestrzennej 4 Typy geometrii cząsteczek przykłady 41 Przykład 1 określanie struktury BCl 3 42 Przykład 2 określanie
3. Cząsteczki i wiązania
 20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
20161020 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków
Wiązania kowalencyjne
 Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Wiązania kowalencyjne (pierw. o dużej E + pierw. o dużej E), E < 1,8 TERIE WIĄZANIA KWALENCYJNEG Teoria hybrydyzacji orbitali atomowych Teoria orbitali molekularnych Teoria pola ligandów YBRYDYZACJA RBITALI
Zakres materiału do sprawdzianu - alkeny, alkiny i areny + przykładowe zadania
 Zakres materiału do sprawdzianu - alkeny, alkiny i areny + przykładowe zadania I. Węglowodory nienasycone 1. Alkeny - węglowodory nienasycone w cząsteczkach których między atomami węgla występuje jedno
Zakres materiału do sprawdzianu - alkeny, alkiny i areny + przykładowe zadania I. Węglowodory nienasycone 1. Alkeny - węglowodory nienasycone w cząsteczkach których między atomami węgla występuje jedno
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ALDEHYDY, KETONY. I. Wprowadzenie teoretyczne
 ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
ALDEYDY, KETNY I. Wprowadzenie teoretyczne Aldehydy i ketony są produktami utlenienia alkoholi. Aldehydy są produktami utlenienia alkoholi pierwszorzędowych, a ketony produktami utlenienia alkoholi drugorzędowych.
Materiały dodatkowe - węglowodory
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe - węglowodory Alkany 1. Hybrydyzacja atomu węgla Mnogość związków, jakie mogą powstać z udziałem atomów węgla,
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe - węglowodory Alkany 1. Hybrydyzacja atomu węgla Mnogość związków, jakie mogą powstać z udziałem atomów węgla,
PARLAMENT EUROPEJSKI
 PARLAMENT EUROPEJSKI 2004 Dokument z posiedzenia 2009 C6-0267/2006 2003/0256(COD) PL 06/09/2006 Wspólne stanowisko Wspólne stanowisko przyjęte przez Radę w dniu 27 czerwca 2006 r. w celu przyjęcia rozporządzenia
PARLAMENT EUROPEJSKI 2004 Dokument z posiedzenia 2009 C6-0267/2006 2003/0256(COD) PL 06/09/2006 Wspólne stanowisko Wspólne stanowisko przyjęte przez Radę w dniu 27 czerwca 2006 r. w celu przyjęcia rozporządzenia
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Orbitale typu σ i typu π
 Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Orbitale typu σ i typu π Dwa odpowiadające sobie orbitale sąsiednich atomów tworzą kombinacje: wiążącą i antywiążącą. W rezultacie mogą powstać orbitale o rozkładzie przestrzennym dwojakiego typu: σ -
Alkeny. Wzór ogólny alkenów C n H 2n. (Uwaga identyczny wzór ogólny mają cykloakany!!!)
 Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
Alkeny Wzór ogólny alkenów n 2n (Uwaga identyczny wzór ogólny mają cykloakany!!!) Węglowodory nienasycone, zawierające wiązanie podwójne, hybrydyzacja atomow węgla biorących udział w tworzeniu wiązania
EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III
 Miejsce na naklejkę z kodem szkoły iejsce na naklejkę z kodem szkoły dysleksja Liczba pkt: Wynik %: Ocena: MCH-R1A1P-062 EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III ARKUSZ II Arkusz
Miejsce na naklejkę z kodem szkoły iejsce na naklejkę z kodem szkoły dysleksja Liczba pkt: Wynik %: Ocena: MCH-R1A1P-062 EGZAMIN SPRAWDZAJĄCY Z CHEMII - WĘGLOWODORY DLA UCZNIÓW KLASY III ARKUSZ II Arkusz
Aminy. - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin
 Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Aminy - Budowa i klasyfikacja amin - Nazewnictwo i izomeria amin - Otrzymywanie amin - Właściwości amin Budowa i klasyfikacja amin Aminy pochodne amoniaku (NH 3 ), w cząsteczce którego jeden lub kilka
Slajd 1. Reakcje alkinów
 Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Slajd 1 Reakcje alkinów Slajd 2 Alkiny to węglowodory zawierające wiązanie potrójne węgiel-węgiel Wzór ogólny: C n H 2n 2 (łańcuchowy); C n H 2n 4 (cykliczny) 1-heksyn terminalny alkin 3-heksyn wewnętrzny
Materiały i tworzywa pochodzenia naturalnego
 Materiały i tworzywa pochodzenia naturalnego 1. Przyporządkuj opisom odpowiadające im pojęcia. Wpisz litery (A I) w odpowiednie kratki. 3 p. A. hydraty D. wapno palone G. próchnica B. zaprawa wapienna
Materiały i tworzywa pochodzenia naturalnego 1. Przyporządkuj opisom odpowiadające im pojęcia. Wpisz litery (A I) w odpowiednie kratki. 3 p. A. hydraty D. wapno palone G. próchnica B. zaprawa wapienna
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2
![liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2 liczba kwantowa, n kwantowa, l Wanad 3 2 [Ar] 3d 3 4s 2](/thumbs/65/54124071.jpg) Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
Arkusz odpowiedzi Nr Proponowane rozwiązanie zadani a Liczba niesparowanych elektronów w jonie r 3+ jest (mniejsza / większa) od liczby elektronów niesparowanych w jonie Mn +. Pierwiastkiem, którego jony
+ HCl + + CHLOROWCOWANIE
 CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
CHLRWCWANIE Proces chlorowcowania polega na wiązaniu się jednego lub więcej atomów chlorowca ze związkiem organicznym. trzymywanie związków organicznych, zawierających fluor, chlor, brom i jod moŝe być
Test sprawdzający, wielostopniowy z chemii: Węglowodory
 Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
Test sprawdzający, wielostopniowy z chemii: Węglowodory Typ szkoły: Autor testu: technikum mgr Ewa Jagoda Skonstruowany przeze mnie test zawiera pytania zamknięte czterokrotnego wyboru, w których tylko
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
Ligand to cząsteczka albo jon, który związany jest z jonem albo atomem centralnym.
 138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
138 Poznanie struktury cząsteczek jest niezwykle ważnym przedsięwzięciem w chemii, ponieważ pozwala nam zrozumieć zachowanie się materii, ale także daje podstawy do praktycznego wykorzystania zdobytej
Wykład przygotowany w oparciu o podręczniki:
 Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
Slajd 1 Wykład przygotowany w oparciu o podręczniki: Organic Chemistry 4 th Edition Paula Yurkanis Bruice Slajd 2 Struktura elektronowa wiązanie chemiczne Kwasy i zasady Slajd 3 Chemia organiczna Związki
CHEMIA ORGANICZA - węglowodory. Podział węglowodorów
 EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE
 PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
PRZYKŁADOWE ZADANIA ALKOHOLE I FENOLE INFORMACJA DO ZADAŃ 864 865 Poniżej przedstawiono cykl reakcji zachodzących z udziałem związków organicznych. 1 2 cykloheksen cykloheksan chlorocykloheksan Zadanie
ALKENY WĘGLOWODORY NIENASYCONE
 Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
Alkeny ALKENY WĘGLOWODORY NIENASYCONE WĘGLOWODORY ALIFATYCZNE SKŁĄDAJĄ SIĘ Z ATOMÓW WĘGLA I WODORU ZAWIERAJĄ JEDNO LUB KILKA WIĄZAŃ PODWÓJNYCH WĘGIEL WĘGIEL ATOM WĘGLA WIĄZANIA PODWÓJNEGO W HYBRYDYZACJI
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Modele: kulkowy i czaszowy: wzór półstrukturalny: H 2 C=CH 2. Obecność wiązania podwójnego sygnalizuje końcówka nazwy "-en" Wzór strukturalny:
 Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Opracowanie: Marek Walnik, 0 Nazewnictwo alkenów Alkeny, zwane też olefinami, to węglowodory, w których cząsteczkach występują wiązania podwójne =. Węglowodory takie, ook alkinów, z potrójnymi wiązaniami,
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
KONKURS CHEMICZNY ROK PRZED MATURĄ
 Wydział Chemii UMCS Polskie Towarzystwo Chemiczne Doradca metodyczny ds. nauczania chemii KONKURS CHEMICZNY ROK PRZED MATURĄ ROK SZKOLNY 2006/2007 ETAP SZKOLNY Numer kodowy Suma punktów Podpisy Komisji:
Wydział Chemii UMCS Polskie Towarzystwo Chemiczne Doradca metodyczny ds. nauczania chemii KONKURS CHEMICZNY ROK PRZED MATURĄ ROK SZKOLNY 2006/2007 ETAP SZKOLNY Numer kodowy Suma punktów Podpisy Komisji:
XXI Regionalny Konkurs Młody Chemik FINAŁ część I
 Katowice, 16.12.2009 XXI Regionalny Konkurs Młody Chemik FINAŁ część I ZADANIE 1. KRZYśÓWKA ZWIĄZKI WĘGLA I WODORU (9 punktów) RozwiąŜ krzyŝówkę. Litery z wyszczególnionych pól utworzą hasło nazwę węglowodoru:
Katowice, 16.12.2009 XXI Regionalny Konkurs Młody Chemik FINAŁ część I ZADANIE 1. KRZYśÓWKA ZWIĄZKI WĘGLA I WODORU (9 punktów) RozwiąŜ krzyŝówkę. Litery z wyszczególnionych pól utworzą hasło nazwę węglowodoru:
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Slajd 1. Etery i epoksydy. Slajd 2. Wprowadzenie. Wzór R-O-R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: CH 3 O CH 3 O CH 3
 Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Slajd 1 Etery i epoksydy Slajd 2 Wprowadzenie Wzór R--R, gdzie R tos alkil lub aryl Symetryczne lub asymetryczne Przykłady: C 3 C 3 C 3 Slajd 3 Budowa i polarność Wygięta struktura Atom tlenu posiada hybrydyzacjęsp
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem
 Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 2002 BYŁA DZISIAJ CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY ARKUSZ EGZAMINACYJNY I
 MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
MATERIAŁY POMOCNICZE 1 GDYBY MATURA 00 BYŁA DZISIAJ OKRĘ GOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE CHEMIA ZESTAW EGZAMINACYJNY PIERWSZY Informacje ARKUSZ EGZAMINACYJNY I 1. Przy każdym zadaniu podano
KARTA KURSU. Kod Punktacja ECTS* 4
 KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
KARTA KURSU Nazwa Nazwa w j. ang. Chemia organiczna Organic chemistry Kod Punktacja ECTS* 4 Koordynator dr Waldemar Tejchman Zespół dydaktyczny dr Waldemar Tejchman Opis kursu (cele kształcenia) Celem
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Widma UV charakterystyczne cechy ułatwiające określanie struktury pirydyny i pochodnych
 Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
Pirydyna i pochodne 1 Pirydyna Tw 115 o C ; temperatura topnienia -41,6 0 C Miesza się w każdym stosunku z wodą tworząc mieszaninę azeotropowa o Tw 92,6 o C; Energia delokalizacji 133 kj/mol ( benzen 150.5
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
RJC A-B A + B. Slides 1 to 27
 Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Reakcje Rodnikowe rodniki substytucja addycja polimeryzacje A-B A + B Slides 1 to 27 Reakcje Organiczne... powstawanie i rozrywanie wiązań kowalencyjnych. Addycja A + B AB Podstawienie AB + C A + BC Eliminacja
Zarys Chemii Organicznej
 Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
Zarys hemii Organicznej hemię organiczną definiuje się jako chemię związków węgla. Ogólna liczba znanych związków organicznych przekracza obecnie 18 milionów i wielokrotnie przewyższa liczbę znanych związków
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
WĘGLOWODORY AROMATYCZNE
 WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
o skondensowanych pierścieniach.
 Tabela F Wykaz złożonych ropopochodnych znajdujących się w wykazie substancji niebezpiecznych wraz z ich opisem, uporządkowany wg wzrastających mumerów indeksowych nr indeksowy: 649-001-00-3 nr WE: 265-102-1
Tabela F Wykaz złożonych ropopochodnych znajdujących się w wykazie substancji niebezpiecznych wraz z ich opisem, uporządkowany wg wzrastających mumerów indeksowych nr indeksowy: 649-001-00-3 nr WE: 265-102-1
CHARAKTERYSTYKA KARBOKSYLANÓW
 AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
AAKTEYSTYKA KABKSYLANÓW 1. GÓLNA AAKTEYSTYKA KWASÓW KABKSYLWY Spośród związków organicznych, które wykazują znaczną kwasowość najważniejsze są kwasy karboksylowe. Związki te zawierają w cząsteczce grupę
H H 2.5 < H H CH 3 N O O H C N ŁADUNEK FORMALNY. 2.5 dla atomu węgla C C 2.5 H 2.1. Li 1.0. liczba e - walencyjnych w atomie wolnym C 2.5 H 2.
 .5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
.5 dla atomu węgla ŁADUNEK RMALNY pierwiastek o mniejszej elektroujemności od węgla
Treść podstawy programowej
 CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
CHEMIA ZR Ramowy rozkład materiału w kolejnych tomach podręczników I. Atomy, cząsteczki i stechiometria chemiczna Tom I 1. Masa atomowa I.2. 2. Izotopy I.1., I.3. 3. Reakcje jądrowe I.4. 4. Okres półtrwania
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek
 strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
strona 1/11 Zadania powtórkowe do egzaminu maturalnego z chemii Wiązania chemiczne, budowa cząsteczek Monika Gałkiewicz Zad. 1 () Podaj wzory dwóch dowolnych kationów i dwóch dowolnych anionów posiadających
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
PRÓBNY EGZAMIN MATURALNY Z CHEMII
 Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 90 minut Informacje 1.
Miejsce na naklejkę z kodem (Wpisuje zdający przed rozpoczęciem pracy) KOD ZDAJĄCEGO OKRĘGOWA K O M I S J A EGZAMINACYJNA w KRAKOWIE PRÓBNY EGZAMIN MATURALNY Z CHEMII Czas pracy 90 minut Informacje 1.
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 1
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLASY II. Ocena Semestr I Semestr II
 WYMAGANIA PROGRAMOWE Z CHEMII DLA KLASY II Ocena Semestr I Semestr II Wymagania konieczne( ocena dopuszczająca ) - zna treść prawa zachowania masy i prawa stałości składu związku chemicznego - potrafi
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLASY II Ocena Semestr I Semestr II Wymagania konieczne( ocena dopuszczająca ) - zna treść prawa zachowania masy i prawa stałości składu związku chemicznego - potrafi
Woda. Najpospolitsza czy najbardziej niezwykła substancja Świata?
 Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
Woda Najpospolitsza czy najbardziej niezwykła substancja Świata? Cel wykładu Odpowiedź na pytanie zawarte w tytule A także próby odpowiedzi na pytania typu: Dlaczego woda jest mokra a lód śliski? Dlaczego
Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). C. alkiny D. areny
 Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Węglowodory Zadanie 1. Wskaż grupę związków chemicznych, do której należy węglowodór o gęstości 2,5 normalne). (warunki A. alkany B. alkeny C. alkiny D. areny Zadanie 2. Wskaż wzór półstrukturalny węglowodoru
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
STEREOCHEMIA ORGANICZNA
 STEREOEMIA ORGANINA Sławomir Jarosz Wykład 5 TOPOWOŚĆ Podział grup wg topowości 1. omotopowe (wymienialne operacją symetrii n ) 2. Enancjotopowe (wymienialne przez płaszczyznę σ) 3. Diastereotopowe (niewymienialne
STEREOEMIA ORGANINA Sławomir Jarosz Wykład 5 TOPOWOŚĆ Podział grup wg topowości 1. omotopowe (wymienialne operacją symetrii n ) 2. Enancjotopowe (wymienialne przez płaszczyznę σ) 3. Diastereotopowe (niewymienialne
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
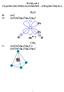 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
Węglowodory. Michał Szewczyk Kl. IV TI
 Węglowodory Michał Szewczyk Kl. IV TI Węglowodory nasycone (Alkany) Węglowodory nasycone (Alkany)- to związki węgla z wodorem, w których pomiędzy atomami węgla występują tylko pojedyncze wiązania. Wzór
Węglowodory Michał Szewczyk Kl. IV TI Węglowodory nasycone (Alkany) Węglowodory nasycone (Alkany)- to związki węgla z wodorem, w których pomiędzy atomami węgla występują tylko pojedyncze wiązania. Wzór
Maksymalna liczba punktów: 40. Czas rozwiązywania zadań: 90 minut.
 Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 20 stycznia 2011 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
Pieczęć KONKURS CHEMICZNY dla uczniów gimnazjów województwa lubuskiego 20 stycznia 2011 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem do rozwiązywania
